 Participez à la création d’un site d'informations accessibles sur les médicaments pensé pour le grand public !
Participez à la création d’un site d'informations accessibles sur les médicaments pensé pour le grand public !Inscrivez-vous ici pour le tester en avant-première, partager vos impressions, et nous aider à l’améliorer !
 Participez à la création d’un site d'informations accessibles sur les médicaments pensé pour le grand public !
Participez à la création d’un site d'informations accessibles sur les médicaments pensé pour le grand public !
Cliquez sur un pictogramme pour aller directement à la rubrique le concernant.
Pour plus d'information sur les pictogrammes, consultez l'aide.
Ce médicament appartient au(x) groupe(s) générique(s) suivants :
 Comprimé (Composition pour un comprimé)
Comprimé (Composition pour un comprimé)
 200 mg
200 mg
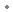 sous forme de : chlorhydrate de tapentadol
sous forme de : chlorhydrate de tapentadol Pas de présentation à afficher
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Insuffisant | Avis du 07/06/2017 | Réévaluation SMR et ASMR | Le service médical rendu par PALEXIA LP est insuffisant pour justifier d’une prise en charge par la solidarité nationale dans le traitement des douleurs chroniques sévères non cancéreuses non neuropathiques de l’adulte, qui ne peuvent être correctement traitées que par des antalgiques opioïdes. |
| Faible | Avis du 25/06/2014 | Inscription (CT) | Le service médical rendu par PALEXIA LP est faible dans le traitement des douleurs chroniques sévères de l’adulte d’origine cancéreuse, qui ne peuvent être correctement traitées que par des antalgiques opioïdes, à l’exception des douleurs d’origine cancéreuse rebelles. |
| Insuffisant | Avis du 25/06/2014 | Inscription (CT) | Le service médical rendu par PALEXIA LP est insuffisant dans le traitement des douleurs chroniques sévères de l’adulte d’origine non cancéreuse, qui ne peuvent être correctement traitées que par des antalgiques opioïdes. |
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 25/06/2014 | Inscription (CT) | PALEXIA LP n’apportent pas d’amélioration du service médical rendu (ASMR V, inexistante) dans le traitement des douleurs chroniques sévères d’origine cancéreuse chez l’adulte, par rapport aux autres opioïdes disponibles. |
|
| Plan du site | Accessibilité | Contact | Téléchargement | Declaration de confidentialité | Service-Public.fr | Legifrance | Gouvernement.fr |