
Cliquez sur un pictogramme pour aller directement à la rubrique le concernant.
Pour plus d'information sur les pictogrammes, consultez l'aide.
Vous trouverez les indications thérapeutiques de ce médicament dans le paragraphe 4.1 du RCP ou dans le paragraphe 1 de la notice. Ces documents sont disponibles en cliquant ici
Ce médicament n'appartient à aucun groupe générique
 Comprimé (Composition pour un comprimé)
Comprimé (Composition pour un comprimé)
 10 mg
10 mg
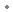 sous forme de : bésilate d'amlodipine
sous forme de : bésilate d'amlodipine  13,87 mg
13,87 mg
 160 mg
160 mg
 12,5 mg
12,5 mg
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 28/03/2012 | Inscription (CT) | Dans la mesure où ces trithérapies fixes concernent des patients hypertendus sévères, la commission considère que le service médical rendu par ces spécialités n'est important que chez les patients stables et dont la pression artérielle est suffisamment contrôlée par l'association libre de chacun des principes actifs (sous forme de trois monothérapies ou d'une bithérapie fixe et d'une monothérapie) aux mêmes doses et pris en charge par un spécialiste de l'hypertension artérielle (cardiologues et néphrologues). Ce service médical rendu sera réévalué dans un délai maximum de 2 ans sur la base des résultats d'un suivi en condition réelle d'utilisation. |
| Insuffisant | Avis du 31/03/2010 | Inscription (CT) | Le service médical rendu par ces spécialités est considéré comme insuffisant pour être pris en charge par la solidarité nationale. |
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 28/03/2012 | Inscription (CT) | EXFORGE HCT, association fixe d'amlodipine, de valsaratan et d'hydrochlorothiazide, n'apporte pas d'amélioration du service médical rendu (ASMR V) par rapport à l'utilisation conjointe de chacun de ses composants pris séparément aux mêmes doses. |
|
| Plan du site | Accessibilité | Contact | Téléchargement | Declaration de confidentialité | Service-Public.fr | Legifrance | Gouvernement.fr |