
Cliquez sur un pictogramme pour aller directement à la rubrique le concernant.
Pour plus d'information sur les pictogrammes, consultez l'aide.

Vous trouverez les indications thérapeutiques de ce médicament dans le paragraphe 4.1 du RCP ou dans le paragraphe 1 de la notice. Ces documents sont disponibles en cliquant ici
Ce médicament appartient au(x) groupe(s) générique(s) suivants :
 Poudre (Composition pour un flacon)
Poudre (Composition pour un flacon)
 1 mg
1 mg
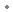 sous forme de : ester boronique de mannitol
sous forme de : ester boronique de mannitol
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Le service médical rendu par VELCADE reste important dans l’indication de l’AMM « en monothérapie ou en association à la dexaméthasone, pour le traitement des patients adultes atteints de myélome multiple en progression, ayant reçu au moins 1 traitement antérieur et ayant déjà bénéficié ou étant inéligibles à une greffe de cellules souches hématopoïétiques ». |
| Insuffisant | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Le service médical rendu par VELCADE en association à la doxorubicine (CAELYX) est insuffisant pour justifier une prise en charge par la solidarité nationale dans l’indication « en association à la doxorubicine liposomale pégylée, pour le traitement des patients adultes atteints de myélome multiple en progression, ayant reçu au moins 1 traitement antérieur et ayant déjà bénéficié ou étant inéligibles à une greffe de cellules souches hématopoïétiques ». |
| Important | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Le service médical rendu par VELCADE reste important dans l’indication de l’AMM « en monothérapie ou en association à la dexaméthasone, pour le traitement des patients adultes atteints de myélome multiple en progression, ayant reçu au moins 1 traitement antérieur et ayant déjà bénéficié ou étant inéligibles à une greffe de cellules souches hématopoïétiques ». |
| Insuffisant | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Le service médical rendu par VELCADE en association à la doxorubicine (CAELYX) est insuffisant pour justifier une prise en charge par la solidarité nationale dans l’indication « en association à la doxorubicine liposomale pégylée, pour le traitement des patients adultes atteints de myélome multiple en progression, ayant reçu au moins 1 traitement antérieur et ayant déjà bénéficié ou étant inéligibles à une greffe de cellules souches hématopoïétiques ». |
| Important | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Le service médical rendu par VELCADE reste important dans l’indication de l’AMM « en monothérapie ou en association à la dexaméthasone, pour le traitement des patients adultes atteints de myélome multiple en progression, ayant reçu au moins 1 traitement antérieur et ayant déjà bénéficié ou étant inéligibles à une greffe de cellules souches hématopoïétiques ». |
| Insuffisant | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Le service médical rendu par VELCADE en association à la doxorubicine (CAELYX) est insuffisant pour justifier une prise en charge par la solidarité nationale dans l’indication « en association à la doxorubicine liposomale pégylée, pour le traitement des patients adultes atteints de myélome multiple en progression, ayant reçu au moins 1 traitement antérieur et ayant déjà bénéficié ou étant inéligibles à une greffe de cellules souches hématopoïétiques ». |
| Important | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Le service médical rendu par VELCADE reste important dans l’indication de l’AMM « en monothérapie ou en association à la dexaméthasone, pour le traitement des patients adultes atteints de myélome multiple en progression, ayant reçu au moins 1 traitement antérieur et ayant déjà bénéficié ou étant inéligibles à une greffe de cellules souches hématopoïétiques ». |
| Insuffisant | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Le service médical rendu par VELCADE en association à la doxorubicine (CAELYX) est insuffisant pour justifier une prise en charge par la solidarité nationale dans l’indication « en association à la doxorubicine liposomale pégylée, pour le traitement des patients adultes atteints de myélome multiple en progression, ayant reçu au moins 1 traitement antérieur et ayant déjà bénéficié ou étant inéligibles à une greffe de cellules souches hématopoïétiques ». |
| Important | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Le service médical rendu par VELCADE reste important dans le myélome multiple non préalablement traité chez les patients : • non éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques, en association au melphalan et à la prednisone . • éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques en traitement d’induction, en association à la dexaméthasone, ou à la dexaméthasone et au thalidomide. |
| Important | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Le service médical rendu par VELCADE reste important dans le myélome multiple non préalablement traité chez les patients : • non éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques, en association au melphalan et à la prednisone . • éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques en traitement d’induction, en association à la dexaméthasone, ou à la dexaméthasone et au thalidomide. |
| Important | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Le service médical rendu par VELCADE reste important dans le myélome multiple non préalablement traité chez les patients : • non éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques, en association au melphalan et à la prednisone . • éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques en traitement d’induction, en association à la dexaméthasone, ou à la dexaméthasone et au thalidomide. |
| Important | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Le service médical rendu par VELCADE reste important dans le myélome multiple non préalablement traité chez les patients : • non éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques, en association au melphalan et à la prednisone . • éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques en traitement d’induction, en association à la dexaméthasone, ou à la dexaméthasone et au thalidomide. |
| Important | Avis du 06/01/2016 | Extension d'indication | Le service médical rendu par VELCADE est important en association au rituximab, au cyclophosphamide, à la doxorubicine et à la prednisone, dans le traitement des patients adultes atteints d'un lymphome à cellules du manteau non traité au préalable, pour lesquels une greffe de cellules souches hématopoïétiques est inadaptée. |
| Important | Avis du 06/01/2016 | Extension d'indication | Le service médical rendu par VELCADE est important en association au rituximab, au cyclophosphamide, à la doxorubicine et à la prednisone, dans le traitement des patients adultes atteints d'un lymphome à cellules du manteau non traité au préalable, pour lesquels une greffe de cellules souches hématopoïétiques est inadaptée. |
| Important | Avis du 06/01/2016 | Extension d'indication | Le service médical rendu par VELCADE est important en association au rituximab, au cyclophosphamide, à la doxorubicine et à la prednisone, dans le traitement des patients adultes atteints d'un lymphome à cellules du manteau non traité au préalable, pour lesquels une greffe de cellules souches hématopoïétiques est inadaptée. |
| Important | Avis du 06/01/2016 | Extension d'indication | Le service médical rendu par VELCADE est important en association au rituximab, au cyclophosphamide, à la doxorubicine et à la prednisone, dans le traitement des patients adultes atteints d'un lymphome à cellules du manteau non traité au préalable, pour lesquels une greffe de cellules souches hématopoïétiques est inadaptée. |
| Important | Avis du 22/01/2014 | Extension d'indication | Le service médical rendu par VELCADE, en association à la dexaméthasone, ou à la dexaméthasone et au thalidomide, est important dans le traitement d’induction des patients adultes atteints de myélome multiple non traité au préalable, éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques. |
| Important | Avis du 22/01/2014 | Extension d'indication | Le service médical rendu par VELCADE, en association à la dexaméthasone, ou à la dexaméthasone et au thalidomide, est important dans le traitement d’induction des patients adultes atteints de myélome multiple non traité au préalable, éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques. |
| Important | Avis du 22/01/2014 | Extension d'indication | Le service médical rendu par VELCADE, en association à la dexaméthasone, ou à la dexaméthasone et au thalidomide, est important dans le traitement d’induction des patients adultes atteints de myélome multiple non traité au préalable, éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques. |
| Important | Avis du 22/01/2014 | Extension d'indication | Le service médical rendu par VELCADE, en association à la dexaméthasone, ou à la dexaméthasone et au thalidomide, est important dans le traitement d’induction des patients adultes atteints de myélome multiple non traité au préalable, éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques. |
| Important | Avis du 10/06/2009 | Extension d'indication | Le service médical rendu par ces spécialités est important dans l’extension d’indication « en association au melphalan et à la prednisone pour le traitement des patients atteints de myélome multiple non traité au préalable, non éligibles à la chimiothérapie intensive accompagnée d’une greffe de moelle osseuse ». |
| Important | Avis du 10/06/2009 | Extension d'indication | Le service médical rendu par ces spécialités est important dans l’extension d’indication « en association au melphalan et à la prednisone pour le traitement des patients atteints de myélome multiple non traité au préalable, non éligibles à la chimiothérapie intensive accompagnée d’une greffe de moelle osseuse ». |
| Important | Avis du 10/06/2009 | Extension d'indication | Le service médical rendu par ces spécialités est important dans l’extension d’indication « en association au melphalan et à la prednisone pour le traitement des patients atteints de myélome multiple non traité au préalable, non éligibles à la chimiothérapie intensive accompagnée d’une greffe de moelle osseuse ». |
| Important | Avis du 10/06/2009 | Extension d'indication | Le service médical rendu par ces spécialités est important dans l’extension d’indication « en association au melphalan et à la prednisone pour le traitement des patients atteints de myélome multiple non traité au préalable, non éligibles à la chimiothérapie intensive accompagnée d’une greffe de moelle osseuse ». |
| Important | Avis du 16/07/2008 | Inscription (CT) | Le service médical rendu par cette spécialité est important dans l’indication de l’A.M.M. |
| Important | Avis du 16/07/2008 | Inscription (CT) | Le service médical rendu par cette spécialité est important dans l’indication de l’A.M.M. |
| Important | Avis du 16/07/2008 | Inscription (CT) | Le service médical rendu par cette spécialité est important dans l’indication de l’A.M.M. |
| Important | Avis du 16/07/2008 | Inscription (CT) | Le service médical rendu par cette spécialité est important dans l’indication de l’A.M.M. |
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence.
Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien "Avis du jj/mm/aaaa" ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Dans le cadre de la prise en charge du myélome multiple en rechute et au regard : • des données déjà évaluées, non comparatives, en monothérapie, chez des patients en 3ème ligne (naïfs de VELCADE) dont le profil ne correspond plus à celui d’aujourd’hui, • du niveau de preuve faible des données portant sur l’association à la dexaméthasone (analyse post-hoc de 127 paires de patients traités par VELCADE seul ou par VELCADE associé à la dexaméthasone), • de l’absence de donnée comparative versus les alternatives recommandées (comprenant REVLIMID associé à la dexaméthasone), la Commission considère que VELCADE, en monothérapie ou en association à la dexaméthasone, n’apporte pas d’amélioration du service médical rendu (ASMR V) dans la stratégie thérapeutique actuelle, comprenant REVLIMID associé à la dexaméthasone, chez les patients ayant reçu au moins 1 traitement antérieur et ayant déjà bénéficié ou étant inéligibles à une greffe de cellules souches hématopoïétiques. |
| V (Inexistant) | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Dans le cadre de la prise en charge du myélome multiple en rechute et au regard : • des données déjà évaluées, non comparatives, en monothérapie, chez des patients en 3ème ligne (naïfs de VELCADE) dont le profil ne correspond plus à celui d’aujourd’hui, • du niveau de preuve faible des données portant sur l’association à la dexaméthasone (analyse post-hoc de 127 paires de patients traités par VELCADE seul ou par VELCADE associé à la dexaméthasone), • de l’absence de donnée comparative versus les alternatives recommandées (comprenant REVLIMID associé à la dexaméthasone), la Commission considère que VELCADE, en monothérapie ou en association à la dexaméthasone, n’apporte pas d’amélioration du service médical rendu (ASMR V) dans la stratégie thérapeutique actuelle, comprenant REVLIMID associé à la dexaméthasone, chez les patients ayant reçu au moins 1 traitement antérieur et ayant déjà bénéficié ou étant inéligibles à une greffe de cellules souches hématopoïétiques. |
| V (Inexistant) | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Dans le cadre de la prise en charge du myélome multiple en rechute et au regard : • des données déjà évaluées, non comparatives, en monothérapie, chez des patients en 3ème ligne (naïfs de VELCADE) dont le profil ne correspond plus à celui d’aujourd’hui, • du niveau de preuve faible des données portant sur l’association à la dexaméthasone (analyse post-hoc de 127 paires de patients traités par VELCADE seul ou par VELCADE associé à la dexaméthasone), • de l’absence de donnée comparative versus les alternatives recommandées (comprenant REVLIMID associé à la dexaméthasone), la Commission considère que VELCADE, en monothérapie ou en association à la dexaméthasone, n’apporte pas d’amélioration du service médical rendu (ASMR V) dans la stratégie thérapeutique actuelle, comprenant REVLIMID associé à la dexaméthasone, chez les patients ayant reçu au moins 1 traitement antérieur et ayant déjà bénéficié ou étant inéligibles à une greffe de cellules souches hématopoïétiques. |
| V (Inexistant) | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Dans le cadre de la prise en charge du myélome multiple en rechute et au regard : • des données déjà évaluées, non comparatives, en monothérapie, chez des patients en 3ème ligne (naïfs de VELCADE) dont le profil ne correspond plus à celui d’aujourd’hui, • du niveau de preuve faible des données portant sur l’association à la dexaméthasone (analyse post-hoc de 127 paires de patients traités par VELCADE seul ou par VELCADE associé à la dexaméthasone), • de l’absence de donnée comparative versus les alternatives recommandées (comprenant REVLIMID associé à la dexaméthasone), la Commission considère que VELCADE, en monothérapie ou en association à la dexaméthasone, n’apporte pas d’amélioration du service médical rendu (ASMR V) dans la stratégie thérapeutique actuelle, comprenant REVLIMID associé à la dexaméthasone, chez les patients ayant reçu au moins 1 traitement antérieur et ayant déjà bénéficié ou étant inéligibles à une greffe de cellules souches hématopoïétiques. |
| III (Modéré) | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Dans le cadre du traitement du myélome multiple non traité au préalable, la Commission considère que VELCADE conserve une amélioration du service médical rendu modérée (ASMR III) chez les patients : • non éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques, en association au melphalan et à la prednisone (schéma MPV) . • éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques en traitement d’induction, en association à la dexaméthasone, ou à la dexaméthasone et au thalidomide (schéma VTD). |
| III (Modéré) | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Dans le cadre du traitement du myélome multiple non traité au préalable, la Commission considère que VELCADE conserve une amélioration du service médical rendu modérée (ASMR III) chez les patients : • non éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques, en association au melphalan et à la prednisone (schéma MPV) . • éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques en traitement d’induction, en association à la dexaméthasone, ou à la dexaméthasone et au thalidomide (schéma VTD). |
| III (Modéré) | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Dans le cadre du traitement du myélome multiple non traité au préalable, la Commission considère que VELCADE conserve une amélioration du service médical rendu modérée (ASMR III) chez les patients : • non éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques, en association au melphalan et à la prednisone (schéma MPV) . • éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques en traitement d’induction, en association à la dexaméthasone, ou à la dexaméthasone et au thalidomide (schéma VTD). |
| III (Modéré) | Avis du 02/03/2016 | Réévaluation SMR et ASMR | Dans le cadre du traitement du myélome multiple non traité au préalable, la Commission considère que VELCADE conserve une amélioration du service médical rendu modérée (ASMR III) chez les patients : • non éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques, en association au melphalan et à la prednisone (schéma MPV) . • éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques en traitement d’induction, en association à la dexaméthasone, ou à la dexaméthasone et au thalidomide (schéma VTD). |
| IV (Mineur) | Avis du 06/01/2016 | Extension d'indication | Considérant l’absence de démonstration à ce jour d’un effet du bortézomib sur la survie globale mais le gain absolu d’environ 10 mois en survie sans progression et le profil de tolérance, moins favorable que son comparateur, la Commission de la transparence considère que VELCADE en association au rituximab, cyclophosphamide, doxorubicine et prednisone (VcR-CAP) apporte une amélioration du service médical rendu mineure (ASMR IV) dans la stratégie de prise en charge des patients atteints d’un lymphome à cellules du manteau inéligibles à une greffe de cellules souches hématopoïétiques. |
| IV (Mineur) | Avis du 06/01/2016 | Extension d'indication | Considérant l’absence de démonstration à ce jour d’un effet du bortézomib sur la survie globale mais le gain absolu d’environ 10 mois en survie sans progression et le profil de tolérance, moins favorable que son comparateur, la Commission de la transparence considère que VELCADE en association au rituximab, cyclophosphamide, doxorubicine et prednisone (VcR-CAP) apporte une amélioration du service médical rendu mineure (ASMR IV) dans la stratégie de prise en charge des patients atteints d’un lymphome à cellules du manteau inéligibles à une greffe de cellules souches hématopoïétiques. |
| IV (Mineur) | Avis du 06/01/2016 | Extension d'indication | Considérant l’absence de démonstration à ce jour d’un effet du bortézomib sur la survie globale mais le gain absolu d’environ 10 mois en survie sans progression et le profil de tolérance, moins favorable que son comparateur, la Commission de la transparence considère que VELCADE en association au rituximab, cyclophosphamide, doxorubicine et prednisone (VcR-CAP) apporte une amélioration du service médical rendu mineure (ASMR IV) dans la stratégie de prise en charge des patients atteints d’un lymphome à cellules du manteau inéligibles à une greffe de cellules souches hématopoïétiques. |
| IV (Mineur) | Avis du 06/01/2016 | Extension d'indication | Considérant l’absence de démonstration à ce jour d’un effet du bortézomib sur la survie globale mais le gain absolu d’environ 10 mois en survie sans progression et le profil de tolérance, moins favorable que son comparateur, la Commission de la transparence considère que VELCADE en association au rituximab, cyclophosphamide, doxorubicine et prednisone (VcR-CAP) apporte une amélioration du service médical rendu mineure (ASMR IV) dans la stratégie de prise en charge des patients atteints d’un lymphome à cellules du manteau inéligibles à une greffe de cellules souches hématopoïétiques. |
| III (Modéré) | Avis du 22/01/2014 | Extension d'indication | VELCADE, en association à la dexaméthasone, ou à la dexaméthasone et au thalidomide, apporte une amélioration du service médical rendu modérée (niveau III) en termes d’efficacité, pour le traitement d’induction des patients adultes atteints de myélome multiple non traité au préalable, éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques. |
| III (Modéré) | Avis du 22/01/2014 | Extension d'indication | VELCADE, en association à la dexaméthasone, ou à la dexaméthasone et au thalidomide, apporte une amélioration du service médical rendu modérée (niveau III) en termes d’efficacité, pour le traitement d’induction des patients adultes atteints de myélome multiple non traité au préalable, éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques. |
| III (Modéré) | Avis du 22/01/2014 | Extension d'indication | VELCADE, en association à la dexaméthasone, ou à la dexaméthasone et au thalidomide, apporte une amélioration du service médical rendu modérée (niveau III) en termes d’efficacité, pour le traitement d’induction des patients adultes atteints de myélome multiple non traité au préalable, éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques. |
| III (Modéré) | Avis du 22/01/2014 | Extension d'indication | VELCADE, en association à la dexaméthasone, ou à la dexaméthasone et au thalidomide, apporte une amélioration du service médical rendu modérée (niveau III) en termes d’efficacité, pour le traitement d’induction des patients adultes atteints de myélome multiple non traité au préalable, éligibles à la chimiothérapie intensive accompagnée d’une greffe de cellules souches hématopoïétiques. |
| III (Modéré) | Avis du 10/06/2009 | Extension d'indication | VELCADE en ajout à l'association melphalan et prednisone apporte une amélioration du service médical rendu modérée (de niveau III) en termes d'efficacité par rapport à l'association melphalan et prednisone seule dans le traitement de première intention des patients atteints de myélome multiple non éligibles à une chimiothérapie intensive accompagnée d'une greffe de moelle osseuse. |
| III (Modéré) | Avis du 10/06/2009 | Extension d'indication | VELCADE en ajout à l'association melphalan et prednisone apporte une amélioration du service médical rendu modérée (de niveau III) en termes d'efficacité par rapport à l'association melphalan et prednisone seule dans le traitement de première intention des patients atteints de myélome multiple non éligibles à une chimiothérapie intensive accompagnée d'une greffe de moelle osseuse. |
| III (Modéré) | Avis du 10/06/2009 | Extension d'indication | VELCADE en ajout à l'association melphalan et prednisone apporte une amélioration du service médical rendu modérée (de niveau III) en termes d'efficacité par rapport à l'association melphalan et prednisone seule dans le traitement de première intention des patients atteints de myélome multiple non éligibles à une chimiothérapie intensive accompagnée d'une greffe de moelle osseuse. |
| III (Modéré) | Avis du 10/06/2009 | Extension d'indication | VELCADE en ajout à l'association melphalan et prednisone apporte une amélioration du service médical rendu modérée (de niveau III) en termes d'efficacité par rapport à l'association melphalan et prednisone seule dans le traitement de première intention des patients atteints de myélome multiple non éligibles à une chimiothérapie intensive accompagnée d'une greffe de moelle osseuse. |
| V (Inexistant) | Avis du 16/07/2008 | Inscription (CT) | Cette spécialité est un complément de gamme qui n’apporte pas d’amélioration du service médical rendu (V). |
| V (Inexistant) | Avis du 16/07/2008 | Inscription (CT) | Cette spécialité est un complément de gamme qui n’apporte pas d’amélioration du service médical rendu (V). |
| V (Inexistant) | Avis du 16/07/2008 | Inscription (CT) | Cette spécialité est un complément de gamme qui n’apporte pas d’amélioration du service médical rendu (V). |
| V (Inexistant) | Avis du 16/07/2008 | Inscription (CT) | Cette spécialité est un complément de gamme qui n’apporte pas d’amélioration du service médical rendu (V). |
|
| Plan du site | Accessibilité | Contact | Téléchargement | Declaration de confidentialité | Service-Public.fr | Legifrance | Gouvernement.fr |