Dernière mise à jour le 02/03/2026
LAMICTAL 100 mg, comprimé dispersible ou à croquer
Indications thérapeutiques
Classe pharmacothérapeutique - code ATC : N03AX09
LAMICTAL traite l'épilepsie en bloquant les signaux du cerveau qui déclenchent les crises d'épilepsie (convulsions).
· Chez les adultes et les enfants âgés de 13 ans et plus, LAMICTAL peut être utilisé seul ou avec d'autres médicaments, pour traiter l'épilepsie. LAMICTAL peut également être utilisé avec d'autres médicaments pour traiter les crises survenant dans une maladie appelée syndrome de Lennox-Gastaut.
· Chez les enfants âgés de 2 à 12 ans, LAMICTAL peut être utilisé avec d'autres médicaments, pour traiter ces maladies. Il peut être utilisé seul pour traiter un type d'épilepsie appelé crises d'absences typiques.
LAMICTAL traite également les troubles bipolaires.
Les personnes ayant des troubles bipolaires (parfois appelés maniaco-dépression) ont des variations d'humeur extrêmes, avec des périodes maniaques (excitation ou euphorie) alternant avec des périodes de dépression (profonde tristesse ou désespoir). Chez les adultes âgés de 18 ans et plus, LAMICTAL peut être utilisé seul ou avec d'autres médicaments, pour prévenir les périodes de dépression qui surviennent dans les troubles bipolaires. On ne sait pas encore comment LAMICTAL agit dans le cerveau pour avoir cet effet.
Présentations
> plaquette(s) PVC PVDC aluminium papier avec fermeture de sécurité enfant de 30 comprimé(s)
Code CIP : 34009 302 250 3 5
Déclaration de commercialisation : 11/07/2023
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 11,87 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 12,89 €
- Taux de remboursement :65 %
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 16/02/2022 | Inscription (CT) | Le service médical rendu par LAMICTAL (lamotrigine) 25 mg, 50 mg, 100 mg, 200mg, comprimé dispersible ou à croquer est important dans les indications de l’AMM. |
| Important | Avis du 26/06/2019 | Renouvellement d'inscription (CT) | Le service médical rendu par LAMICTAL comprimé reste important dans l’ensemble de ses indications. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 16/02/2022 | Inscription (CT) | Ces spécialités sont un complément de gamme qui n’apportent pas d’amélioration du service médical rendu (ASMR V) par rapport à aux présentations déjà inscrites. |
| V (Inexistant) | Avis du 08/09/2010 | Inscription (CT) | Ces spécialités sont des compléments de gamme qui n'apportent pas d'amélioration du service médical rendu (ASMR V). Conditionnement : la présentation en boîte de 28 comprimés n'est pas adaptée aux conditions de prescription. En effet, la Commission rappelle que conformément à ses délibérations en date du 20 juillet 2005, elle recommande pour les traitements d'une durée d'un mois, une harmonisation de la taille des conditionnements à 30 jours de traitement et par conséquent des conditionnements à 90 jours pour les traitements d'une durée de trois mois. Dans un souci de bon usage, la Commission attire l'attention du CEPS sur le fait que les présentations actuellement disponibles répondent aux augmentations posologiques nécessaires à l'instauration du traitement (LAMICSTART) ainsi qu'aux posologies préconisées lors du traitement d'entretien (LAMICTAL en boîte de 30 comprimés). La mise à disposition d'une présentation en boîte de 28 comprimés à l'initiative du laboratoire serait destinée à se substituer aux présentations déjà disponibles sur le marché (à l'exception du dosage à 2 mg qui resterait disponible en boîte de 30). La Commission regrette cette évolution qui va à l'encontre de ses recommandations concernant les conditionnements des médicaments destinés à un traitement d'un mois. Néanmoins, ce conditionnement qui correspond à un multiple de 7 permettrait l'augmentation progressive de la posologie lors de l'instauration du traitement pendant les premières semaines conformément aux schémas posologiques recommandés dans le RCP. Avis favorable à l'inscription sur la liste des spécialités remboursables aux assurés sociaux et sur la liste des médicaments agréés à l'usage des collectivités et divers services publics dans les indications et aux posologies de l'AMM. |
| V (Inexistant) | Avis du 05/05/2010 | Extension d'indication | Ces spécialités n'apportent pas d'amélioration du service médical rendu (ASMR V) dans la prise en charge des absences typiques en monothérapie chez les enfants et adolescents de 2 à 12 ans. |
| V (Inexistant) | Avis du 05/05/2010 | Extension d'indication | Ces spécialités utilisées en seconde intention n'apportent pas d'amélioration du service médical rendu (ASMR V) dans la prévention des épisodes dépressifs chez les adultes ayant un trouble bipolaire de type I et qui ont une prédominance d'épisodes dépressifs. La Commission considère que ces spécialités constituent un moyen thérapeutique supplémentaire. |
ANSM - Mis à jour le : 24/06/2025
LAMICTAL 100 mg, comprimé dispersible ou à croquer
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Lamotrigine ..................................................................................................................... 100,00 mg
Pour un comprimé dispersible ou à croquer.
Pour la liste complète des excipients, voir rubrique 6.1.
Comprimé dispersible ou à croquer.
Comprimés de 8.3 mm super-elliptiques, multi-facettes, blancs à blanchâtres avec une odeur de cassis, marqués « GSCL7 » sur une face et « 100 » sur l’autre. Les comprimés peuvent être légèrement marbrés.
4.1. Indications thérapeutiques
Adultes et adolescents âgés de 13 ans et plus
· Traitement en monothérapie ou en association des épilepsies partielles et généralisées, incluant les crises tonico-cloniques.
· Crises associées au syndrome de Lennox-Gastaut. LAMICTAL est administré en association à un autre traitement mais peut être l'anti-épileptique (AE) de première intention dans le syndrome de Lennox-Gastaut.
Enfants et adolescents de 2 à 12 ans
· Traitement en association des épilepsies partielles et généralisées, incluant les crises tonico-cloniques et les crises associées à un syndrome de Lennox-Gastaut.
· Traitement en monothérapie des absences typiques.
Troubles bipolaires
Adultes âgés de 18 ans et plus
Prévention des épisodes dépressifs chez les patients présentant un trouble bipolaire de type I et qui ont une prédominance d'épisodes dépressifs (voir rubrique 5.1).
LAMICTAL n'est pas indiqué dans le traitement aigu des épisodes maniaques ou dépressifs
4.2. Posologie et mode d'administration
Posologie
Si la posologie calculée de lamotrigine (par exemple pour le traitement d'enfants atteints d'épilepsie ou des patients ayant une insuffisance hépatique) ne correspond pas à un nombre entier de comprimé(s), la dose devant être administrée est égale à l'unité inférieure du nombre de comprimé(s) entier(s).
Réintroduction du traitement
Les prescripteurs doivent évaluer le besoin d'augmenter la dose jusqu’à la posologie d'entretien en cas de réintroduction du traitement chez les patients ayant arrêté de prendre LAMICTAL quelle qu'en soit la raison, étant donné le risque d'éruption cutanée sévère associé à des posologies initiales élevées et excédant le schéma d'escalade de dose recommandée pour la lamotrigine (voir rubrique 4.4). Plus le temps écoulé depuis la dernière prise est grand, plus il faut considérer l'augmentation de la dose jusqu’à la posologie d'entretien. Quand le temps d'arrêt de la prise de lamotrigine excède 5 demi-vies (voir rubrique 5.2), LAMICTAL doit généralement être augmenté jusqu'à la posologie d'entretien selon le schéma approprié.
Il est recommandé de ne pas réintroduire le traitement par LAMICTAL chez les patients ayant arrêté en raison d'une éruption cutanée associée à un traitement antérieur par la lamotrigine tant que le bénéfice potentiel n'excède pas clairement le risque.
Epilepsie
L'augmentation posologique recommandée et les posologies d'entretien pour les adultes et les adolescents à partir de 13 ans (Tableau 1) et pour les enfants et adolescents âgés de 2 à 12 ans (Tableau 2) sont données ci-dessous. En raison du risque d'éruption cutanée, la posologie initiale et les augmentations posologiques suivantes ne doivent pas être dépassées (voir rubrique 4.4).
Lorsque des AEs concomitants sont arrêtés ou d'autres AEs/médicaments sont ajoutés au protocole thérapeutique contenant de la lamotrigine, il faut prendre en considération l'effet que cela peut avoir sur la pharmacocinétique de la lamotrigine (voir rubrique 4.5).
Tableau 1 : Adultes et adolescents à partir de 13 ans - recommandations posologiques dans l'épilepsie
|
Type de traitement |
Semaines 1 + 2 |
Semaines 3 + 4 |
Posologie habituelle d'entretien |
|
Monothérapie : |
25 mg/jour |
50 mg/jour |
100 - 200 mg/jour Pour atteindre le niveau d'entretien, les doses doivent être augmentées par paliers maximum de 50 à 100 mg toutes les 1 à 2 semaines jusqu'à atteindre la réponse optimale 500 mg/jour ont été nécessaires chez certains patients pour atteindre la réponse désirée |
|
Traitement en association AVEC le valproate (inhibiteur de la glucuronisation de la lamotrigine – voir rubrique 4.5) : |
|||
|
Cette posologie doit être utilisée avec le valproate sans tenir compte de tout autre traitement concomitant |
12,5 mg/jour |
25 mg/jour |
100 - 200 mg/jour (en 1 ou 2 prises par jour) Pour atteindre le niveau d'entretien, les doses doivent être augmentées par paliers maximum de 25 à 50 mg toutes les 1 à 2 semaines jusqu'à atteindre la réponse optimale |
|
Traitement en association SANS le valproate et AVEC inducteurs de la glucuronisation de la lamotrigine (voir rubrique 4.5) : |
|||
|
Cette posologie doit être utilisée sans le valproate mais avec : phénytoïne |
50 mg/jour |
100 mg/jour |
200 - 400 mg/jour Pour atteindre le niveau d'entretien, les doses doivent être augmentées par paliers maximum de 100 mg toutes les 1 à 2 semaines jusqu'à atteindre la réponse optimale 700 mg/jour ont été nécessaires chez certains patients pour atteindre la réponse désirée |
|
Traitement en association SANS le valproate et SANS inducteur de la glucuronisation de la lamotrigine (voir rubrique 4.5) : |
|||
|
Cette posologie doit être utilisée avec d'autres médicaments qui n'inhibent ou n'induisent pas significativement la glucuronisation de la lamotrigine |
25 mg/jour |
50 mg/jour |
100 - 200 mg/jour Pour atteindre le niveau d'entretien, les doses doivent être augmentées par paliers maximum de 50 à 100 mg toutes les 1 à 2 semaines jusqu'à atteindre la réponse optimale |
|
Chez les patients prenant des médicaments dont l'interaction pharmacocinétique avec la lamotrigine n'est pas connue actuellement (voir rubrique 4.5), la posologie recommandée de lamotrigine en cas d'association au valproate doit être appliquée. |
|||
Tableau 2 : Enfants et adolescents âgés de 2 à 12 ans - recommandations posologiques dans l'épilepsie (dose quotidienne totale en mg/kg de poids corporel/jour)**
|
Type de traitement |
Semaines 1 + 2 |
Semaines 3 + 4 |
Posologie habituelle d'entretien |
|
Monothérapie des absences typiques : |
0,3 mg/kg/jour |
0,6 mg/kg/jour |
1 - 15 mg/kg/jour Pour atteindre la posologie d'entretien, les doses doivent être augmentées par paliers maximum de 0,6 mg/kg/jour toutes les 1 à 2 semaines jusqu'à atteindre la réponse optimale avec une dose d’entretien maximale de 200 mg/jour |
|
Traitement en association AVEC le valproate (inhibiteur de la glucuronisation de la lamotrigine - voir rubrique 4.5) : |
|||
|
Cette posologie doit être utilisée avec le valproate sans tenir compte de tout autre traitement concomitant |
0,15 mg/kg/jour* |
0,3 mg/kg/jour |
1 - 5 mg/kg/jour Pour atteindre la posologie d'entretien, les doses doivent être augmentées par paliers maximum de 0,3 mg/kg/jour toutes les 1 à 2 semaines jusqu'à atteindre la réponse optimale avec une dose d'entretien maximale de 200 mg/jour |
|
Traitement en association SANS le valproate et AVEC inducteurs de la glucuronisation de la lamotrigine (voir rubrique 4.5) : |
|||
|
Cette posologie doit être utilisée sans le valproate mais avec : phénytoïne |
0,6 mg/kg/ jour |
1,2 mg/kg/jour |
5 - 15 mg/kg/jour Pour atteindre la posologie d'entretien, les doses doivent être augmentées par paliers maximum de 1,2 mg/kg/jour toutes les 1 à 2 semaines jusqu'à atteindre la réponse optimale avec une dose d'entretien maximale de 400 mg/jour |
|
Traitement en association SANS le valproate et SANS inducteur de la glucuronisation de la lamotrigine (voir rubrique 4.5) : |
|||
|
Cette posologie doit être utilisée avec d'autres médicaments qui n'inhibent ou n'induisent pas significativement la glucuronisation de la lamotrigine |
0,3 mg/kg/ jour |
0,6 mg/kg/jour |
1 - 10 mg/kg/jour Pour atteindre la posologie d'entretien, les doses doivent être augmentées par paliers maximum de 0,6 mg/kg/ jour toutes les 1 à 2 semaines jusqu'à atteindre la réponse optimale avec une dose d'entretien maximale de 200 mg/jour |
|
Chez les patients prenant des médicaments dont l'interaction pharmacocinétique avec la lamotrigine n'est pas connue actuellement (voir rubrique 4.5), la posologie recommandée de lamotrigine en cas d'association au valproate doit être appliquée. |
|||
|
*NOTE : - Si la posologie calculée quotidienne chez les patients prenant du valproate est de 1 mg ou plus mais inférieure à 2 mg, alors LAMICTAL 2 mg comprimés dispersibles ou à croquer peut être pris 1 jour sur 2 durant les 2 premières semaines. Si la posologie calculée quotidienne chez les patients prenant du valproate est inférieure à 1 mg, alors LAMICTAL ne doit pas être administré. N’ESSAYEZ PAS d'administrer des quantités partielles de comprimés dispersibles ou à croquer. |
|||
** Si la dose calculée de lamotrigine ne peut être obtenue en utilisant des comprimés entiers, la dose doit être arrondie à l’unité inférieure du nombre de comprimé entier la plus proche.
Afin de s'assurer que la dose thérapeutique est maintenue, le poids de l'enfant doit être contrôlé et la dose doit être revue en cas de modification du poids. Il est probable que les patients âgés de deux à six ans nécessitent une posologie d'entretien se situant vers la limite supérieure de l'intervalle recommandé.
Si le contrôle de l'épilepsie est atteint avec un traitement en association, les AEs associés peuvent être arrêtés et les patients maintenus sous monothérapie par LAMICTAL.
Enfants de moins de 2 ans
Les données concernant la tolérance et l'efficacité de la lamotrigine en association à un autre traitement dans les crises partielles des enfants âgés de 1 mois à 2 ans sont limitées (voir rubrique 4.4). Il n'y a aucune donnée chez les enfants de moins d'un mois. Par conséquent, l'utilisation de LAMICTAL n'est pas recommandée chez les enfants de moins de 2 ans. Néanmoins si cliniquement en fonction du besoin, la décision de traiter a été prise, voir les rubriques 4.4, 5.1 et 5.2.
Troubles bipolaires
Le schéma d'escalade de dose et la posologie d'entretien recommandés chez les adultes de 18 ans et plus sont fournis dans les tableaux ci-dessous. Le schéma de transition implique une augmentation posologique de la lamotrigine jusqu'à une posologie d'entretien à stabilisation sur six semaines (Tableau 3) après lesquelles les autres médicaments psychotropes et/ou AEs peuvent être arrêtés, si cela est indiqué cliniquement (Tableau 4). Les ajustements posologiques suite à l'ajout d'autres médicaments psychotropes et/ou AEs sont également fournis ci-dessous (Tableau 5). En raison du risque de rash, la dose initiale et les augmentations de doses suivantes ne doivent pas être dépassées (voir rubrique 4.4).
Tableau 3 : Adultes de 18 ans et plus - augmentation posologique recommandée jusqu'à la posologie quotidienne totale d'entretien de stabilisation dans le traitement des troubles bipolaires
|
Type de traitement |
Semaines 1 + 2 |
Semaines 3 + 4 |
Semaine 5 |
Posologie cible de stabilisation (Semaine 6)* |
|
Monothérapie avec la lamotrigine OU en association SANS valproate et SANS inducteur de la glucuronisation de la lamotrigine (voir rubrique 4.5) : |
||||
|
Cette posologie doit être utilisée avec d'autres médicaments qui n'inhibent ou n'induisent pas significativement la glucuronisation de la lamotrigine |
25 mg/jour |
50 mg/jour |
100 mg/jour |
200 mg/jour - posologie cible habituelle pour une réponse optimale (en 1 ou 2 prises par jour) Des posologies dans un intervalle allant de 100 à 400 mg/jour ont été utilisées dans les essais cliniques |
|
Traitement en association AVEC le valproate (inhibiteur de la glucuronisation de la lamotrigine - (voir rubrique 4.5) : |
||||
|
Cette posologie doit être utilisée avec le valproate sans tenir compte de tout autre traitement concomitant |
12,5 mg/jour |
25 mg/jour |
50 mg/jour |
100 mg/jour - posologie cible habituelle pour une réponse optimale (une fois par jour ou en 2 prises) Une posologie maximale de 200 mg/jour peut être utilisée selon la réponse clinique |
|
Traitement en association SANS le valproate et AVEC inducteurs de la glucuronisation de la lamotrigine (voir rubrique 4.5) : |
||||
|
Cette posologie doit être utilisée sans le valproate mais avec : phénytoïne |
50 mg/jour |
100 mg/jour |
200 mg/jour |
300 mg/jour à la semaine 6, si nécessaire en augmentant jusqu'à la posologie cible habituelle de 400 mg/jour à la semaine 7, pour atteindre une réponse optimale (en 2 prises par jour) |
|
Chez les patients prenant des médicaments dont l'interaction pharmacocinétique avec la lamotrigine n'est pas connue actuellement (voir rubrique 4.5), la posologie recommandée de lamotrigine en cas d'association au valproate doit être appliquée. |
||||
*La posologie cible de stabilisation variera selon la réponse clinique.
Tableau 4 : Adultes de 18 ans et plus - posologie totale quotidienne d'entretien de stabilisation suite à l'arrêt de médicaments associés dans le traitement des troubles bipolaires
Une fois que la posologie quotidienne d'entretien de stabilisation est atteinte, les autres médicaments peuvent être arrêtés comme indiqué ci-dessous.
|
Type de traitement |
Dose actuelle de stabilisation de la lamotrigine (avant l'arrêt) |
Semaine 1 (démarrage avec arrêt) |
Semaine 2 |
Semaine 3 et suivantes * |
|
Arrêt du valproate (inhibiteur de la glucuronisation de la lamotrigine - voir rubrique 4.5), selon la posologie initiale de lamotrigine : |
||||
|
Lorsque le valproate est arrêté, doubler la posologie de stabilisation, sans dépasser une augmentation de 100 mg/semaine |
100 mg/jour |
200 mg/jour |
Maintenir cette posologie |
|
|
200 mg/jour |
300 mg/jour |
400 mg/jour |
Maintenir cette posologie |
|
|
Arrêt des inducteurs de la glucuronisation de la lamotrigine (voir rubrique 4.5), selon la posologie initiale de lamotrigine : |
||||
|
Cette posologie doit être utilisée à l'arrêt des médicaments suivants : phénytoïne |
400 mg/jour |
400 mg/jour |
300 mg/jour |
200 mg/jour |
|
300 mg/jour |
300 mg/jour |
225 mg/jour |
150 mg/jour |
|
|
200 mg/jour |
200 mg/jour |
150 mg/jour |
100 mg/jour |
|
|
Arrêt des médicaments qui N'inhibent ou N'induisent PAS significativement la glucuronisation de la lamotrigine (voir rubrique 4.5) : |
||||
|
Cette posologie doit être utilisée lorsque d'autres médicaments qui n'inhibent ou n'induisent pas significativement la glucuronisation sont arrêtés |
Maintenir la posologie cible atteinte durant l'escalade de dose (200 mg/jour; en 2 prises) |
|||
|
Chez les patients prenant des médicaments dont l'interaction pharmacocinétique avec la lamotrigine n'est pas connue actuellement (voir rubrique 4.5), il est recommandé de continuer avec la posologie et de l’adapter en fonction de la réponse clinique. |
||||
*Les posologies peuvent être augmentées jusqu'à 400 mg/jour si besoin.
Tableau 5 : Adultes de 18 ans et plus - ajustement de posologie quotidienne de la lamotrigine suite à l'ajout de médicaments associés dans le traitement des troubles bipolaires
Il n'y a aucune expérience clinique dans l'ajustement de posologie quotidienne de la lamotrigine suite à l'ajout d'autres médicaments dans le traitement des troubles bipolaires.
Cependant, sur la base des études d'interactions avec d'autres médicaments, les recommandations suivantes peuvent être faites :
|
Type de traitement |
Dose actuelle de stabilisation de la lamotrigine (avant l'ajout) |
Semaine 1 |
Semaine 2 |
Semaine 3 et suivantes |
|
Ajout du valproate (inhibiteur de la glucuronisation de la lamotrigine - voir rubrique 4.5), selon la posologie initiale de lamotrigine : |
||||
|
Cette posologie doit être utilisée avec le valproate sans tenir compte de tout autre traitement concomitant |
200 mg/jour |
100 mg/jour |
Maintenir cette posologie |
|
|
300 mg/jour |
150 mg/jour |
Maintenir cette posologie |
||
|
400 mg/jour |
200 mg/jour |
Maintenir cette posologie |
||
|
Ajout d'inducteurs de la glucuronisation de la lamotrigine chez les patients NE prenant PAS de valproate (voir rubrique 4.5), selon la posologie initiale de lamotrigine : |
||||
|
Cette posologie doit être utilisée sans le valproate mais avec : phénytoïne |
200 mg/jour |
200 mg/jour |
300 mg/jour |
400 mg/jour |
|
150 mg/jour |
150 mg/jour |
225 mg/jour |
300 mg/jour |
|
|
100 mg/jour |
100 mg/jour |
150 mg/jour |
200 mg/jour |
|
|
Ajout des médicaments qui N'inhibent ou N'induisent PAS significativement la glucuronisation de la lamotrigine (voir rubrique 4.5) : |
||||
|
Cette posologie doit être utilisée lorsque d'autres médicaments qui n'inhibent ou n'induisent pas significativement la glucuronisation sont ajoutés |
Maintenir la posologie cible atteinte durant l'escalade de dose (200 mg/jour ; intervalle posologique 100 à 400 mg/jour) |
|||
|
Chez les patients prenant des médicaments dont l'interaction pharmacocinétique avec la lamotrigine n'est pas connue actuellement (voir rubrique 4.5), la posologie de lamotrigine recommandée en cas d'association au valproate doit être appliquée. |
||||
Arrêt du traitement par LAMICTAL chez les patients atteints de troubles bipolaires
Dans les essais cliniques, il n'y a eu aucune augmentation de l'incidence, de la sévérité ou du type d'effets indésirables suite à un arrêt brutal de la lamotrigine par comparaison avec le placebo. Par conséquent, les patients peuvent arrêter de prendre LAMICTAL sans étape préalable de réduction de la posologie.
Enfants et adolescents de moins de 18 ans
L'utilisation de LAMICTAL n'est pas recommandée chez les enfants de moins de 18 ans suite aux résultats d’une étude comportant une phase en ouvert puis une phase randomisée en double aveugle versus placebo qui n’a démontré aucune efficacité significative et a montré une augmentation des cas de tendances suicidaires (voir rubriques 4.4 et 5.1).
Recommandations posologiques générales pour LAMICTAL chez les populations spéciales de patients
Femmes sous contraception hormonale
L'utilisation de l'association éthinylestradiol/lévonorgestrel (30 µg/150 µg) multiplie environ par 2 la clairance de la lamotrigine, entraînant une diminution des taux de lamotrigine. Après titration, une augmentation de la posologie d'entretien de la lamotrigine (jusqu'à 2 fois la dose initiale) peut être nécessaire pour atteindre la réponse thérapeutique maximale. Durant la semaine sans prise de pilule, un doublement des taux de lamotrigine a été observé. Des effets indésirables dose-dépendants ne peuvent être exclus. Il faut prendre en considération l'utilisation d'une contraception sans semaine sans prise de pilule, comme traitement de première intention (par exemple, contraceptifs hormonaux continus ou méthodes non-hormonales ; voir rubriques 4.4 et 4.5).
Instauration d'une contraception hormonale chez les patientes prenant déjà une posologie d'entretien de la lamotrigine et NE prenant PAS d'inducteurs de la glucuronisation de la lamotrigine
La posologie d'entretien de la lamotrigine devra dans la plupart des cas être doublée (voir rubriques 4.4 et 4.5). Il est recommandé qu'à partir de l'instauration d'une contraception hormonale, la posologie de lamotrigine soit augmentée par paliers de 50 à 100 mg/jour toutes les semaines, selon la réponse clinique individuelle. Les posologies ne doivent pas dépasser ce seuil, à moins qu'en fonction de la réponse clinique des doses supérieures soient nécessaires. La mesure des concentrations sériques de lamotrigine avant et après l'instauration du contraceptif hormonal peut être envisagée pour confirmer que la concentration basale en lamotrigine a été maintenue. Si nécessaire, la posologie doit être adaptée. Chez les femmes prenant un contraceptif hormonal incluant une semaine de traitement inactif (« semaine sans prise de pilule »), un suivi du taux de lamotrigine sérique doit être effectué durant la 3ème semaine de traitement actif, c'est-à-dire du jour 15 à 21 du cycle de la pilule. C'est pourquoi il est préférable d'utiliser une contraception exempte de semaine sans prise de pilule, comme traitement de première intention (par exemple, des contraceptifs hormonaux continus ou des méthodes non-hormonales ; voir rubriques 4.4 et 4.5)
Arrêt d'une contraception hormonale chez les patientes prenant déjà une posologie d'entretien de la lamotrigine et NE prenant PAS d'inducteurs de la glucuronisation de la lamotrigine
La posologie d'entretien de la lamotrigine devra dans la plupart des cas être diminuée de 50 % (voir rubriques 4.4 et 4.5). Il est recommandé de diminuer progressivement la dose quotidienne de lamotrigine par paliers de 50 à 100 mg chaque semaine (à un taux n'excédant pas 25 % de la dose quotidienne totale par semaine) durant une période de 3 semaines, à moins que la réponse clinique indique le contraire. La mesure des concentrations sériques de lamotrigine avant et après l'arrêt du contraceptif hormonal peut être envisagée, pour confirmer que la concentration basale en lamotrigine a été maintenue. Chez les femmes souhaitant arrêter la prise d'un contraceptif hormonal incluant une semaine de traitement inactif (« semaine sans prise de pilule »), un suivi du taux de lamotrigine sérique doit être effectué durant la 3ème semaine active de traitement, c'est-à-dire du jour 15 à 21 du cycle de la pilule. Des échantillons destinés à l'évaluation des taux de lamotrigine après l'arrêt permanent de la pilule contraceptive ne doivent pas être collectés durant la 1ère semaine suivant l'arrêt de la pilule.
Instauration de la lamotrigine chez les patientes prenant déjà une contraception hormonale
Les augmentations posologiques doivent suivre les recommandations posologiques normales décrites dans les tableaux.
Instauration et arrêt d'une contraception hormonale chez les patientes prenant déjà une posologie d'entretien de la lamotrigine et PRENANT des inducteurs de la glucuronisation de la lamotrigine
Un ajustement à la posologie recommandée d'entretien de lamotrigine peut ne pas être nécessaire.
Utilisation avec d'autres médicaments contenant des œstrogènes
D'autres traitements contenant des œstrogènes, tels que les thérapies hormonales substitutives (THS), peuvent interférer avec la lamotrigine. Par conséquent, une surveillance clinique étroite de l'efficacité de la lamotrigine, incluant des mesures des concentrations de lamotrigine, peut être effectuée afin d'informer d’un éventuel ajustement de la dose jugé approprié (voir rubrique 4.4).
Utilisation avec l’association atazanavir/ritonavir
Aucun ajustement du schéma recommandé d’augmentation de dose de la lamotrigine ne devrait être nécessaire lorsque la lamotrigine est ajoutée à un traitement en cours par l’association atazanavir/ritonavir.
Chez les patients recevant déjà une posologie d’entretien de lamotrigine et ne prenant pas d’inducteurs de la glucuronisation de la lamotrigine, il pourra être nécessaire d’augmenter la posologie de lamotrigine si un traitement par l’association atazanavir/ritonavir est ajouté ou diminuer la posologie de lamotrigine si atazanavir/ritonavir est arrêté. La surveillance des concentrations plasmatiques de lamotrigine devra être effectuée avant et pendant les 2 semaines suivant l’instauration ou l'arrêt d’un traitement par l’association atazanavir/ritonavir, afin de voir si un ajustement posologique de la lamotrigine est nécessaire (voir rubrique 4.5).
Utilisation avec l’association lopinavir/ritonavir
Aucun ajustement du schéma recommandé d’augmentation de dose de la lamotrigine ne devrait être nécessaire lorsque la lamotrigine est ajoutée à un traitement en cours par l’association lopinavir/ritonavir.
Chez les patients recevant déjà une posologie d’entretien de lamotrigine et ne prenant pas d’inducteurs de la glucuronisation de la lamotrigine, il pourra être nécessaire d’augmenter la posologie de lamotrigine si un traitement par l’association lopinavir/ritonavir est ajouté ou diminuer la posologie de lamotrigine si lopinavir/ritonavir est arrêté. La surveillance des concentrations plasmatiques de lamotrigine devra être effectuée avant et pendant les 2 semaines suivant l’instauration ou l'arrêt d’un traitement par l’association lopinavir/ritonavir, afin de voir si un ajustement posologique de la lamotrigine est nécessaire (voir rubrique 4.5).
Sujets âgés (plus de 65 ans)
Aucune adaptation posologique à partir du schéma recommandé n'est requise. La pharmacocinétique de la lamotrigine dans cette population ne diffère pas significativement de la population adulte non-âgée (voir rubrique 5.2).
Insuffisant rénal
Des précautions doivent être prises lorsque LAMICTAL est administré à des patients insuffisants rénaux. Pour les patients en stade terminal d'insuffisance rénale, les posologies initiales de lamotrigine doivent se baser sur celles des traitements concomitants de ces patients ; des posologies d'entretien plus faibles peuvent être efficaces pour les patients ayant une insuffisance rénale fonctionnelle significative (voir rubriques 4.4 et 5.2).
Insuffisant hépatique
Les posologies initiales, d'augmentation et d'entretien doivent généralement être réduites d'approximativement 50 % chez les patients ayant une insuffisance hépatique modérée (Child-Pugh de grade B) et de 75 % chez les insuffisants hépatiques sévères (Child-Pugh de grade C). Les augmentations posologiques et les posologies d'entretien doivent être ajustées en fonction de la réponse clinique (voir rubrique 5.2).
Mode d’administration
Utilisation par voie orale.
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
4.4. Mises en garde spéciales et précautions d'emploi
Des effets indésirables cutanés ont été signalés, ils sont généralement survenus dans les 8 premières semaines après l'instauration du traitement par la lamotrigine.
Si la majorité des éruptions sont bénignes et transitoires, des éruptions cutanées graves nécessitant une hospitalisation et un arrêt de la lamotrigine ont également été rapportées. Cela inclut des éruptions pouvant mettre en jeu le pronostic vital, comme le syndrome de Stevens-Johnson (SSJ), le syndrome de Lyell (nécrolyse épidermique toxique (NET)) et le syndrome d’hypersensibilité médicamenteuse avec éosinophilie et symptômes systémiques (syndrome DRESS) ; aussi appelé syndrome d’hypersensibilité médicamenteuse (voir rubrique 4.8).
Chez les adultes recrutés dans les essais utilisant les recommandations posologiques actuelles de la lamotrigine, l'incidence des éruptions cutanées graves est d’environ 1 pour 500 patients épileptiques. Environ la moitié de ces cas a été rapportée comme étant des syndromes de Stevens-Johnson (1 pour 1000). Dans les essais cliniques chez les patients atteints de troubles bipolaires, l'incidence des éruptions cutanées graves est d'environ 1 pour 1000.
Ce risque d'éruptions cutanées graves est plus élevé chez l'enfant que chez l'adulte. Les données disponibles issues de nombreux essais cliniques suggèrent que l'incidence des éruptions ayant conduit à une hospitalisation chez des enfants soit de l'ordre de 1 pour 300 à 1 pour 100.
Chez les enfants, l'aspect initial d'une éruption cutanée peut faire penser à une infection, les médecins doivent envisager l'éventualité d'une réaction au traitement par la lamotrigine chez les enfants développant des symptômes d'éruptions cutanées et de fièvre durant les huit premières semaines de traitement.
De plus, le risque global d'éruptions semble être fortement lié à :
· des posologies initiales de lamotrigine élevées et dépassant le schéma d'escalade de dose recommandée du traitement par la lamotrigine (voir rubrique 4.2)
· l'utilisation concomitante de valproate (voir rubrique 4.2).
Des précautions sont également exigées lors du traitement de patients ayant des antécédents d'allergie ou d'éruptions avec d'autres AEs étant donné que la fréquence d'éruptions cutanées non sévères après un traitement par la lamotrigine a été environ trois fois plus élevée chez ces patients que chez ceux n'ayant pas de tels antécédents.
Il a été observé que la présence de l'allèle HLA-B*1502 chez les sujets d'origine asiatique (principalement les Chinois Han et les Thaïlandais) est associée au risque de développer un SSJ/NET lors d'un traitement par la lamotrigine. Si l'on sait que ces patients sont positifs pour l'allèle HLA-B*1502, l'utilisation de la lamotrigine doit être envisagée avec précaution.
Tous les patients (adultes et enfants) qui développent une éruption doivent être rapidement évalués et LAMICTAL doit être arrêté immédiatement à moins que l'éruption ne soit clairement pas liée à la lamotrigine. Il est recommandé de ne pas réintroduire LAMICTAL chez les patients l'ayant interrompu en raison d'une éruption associée à un traitement antérieur par la lamotrigine, à moins que le bénéfice potentiel ne dépasse clairement le risque. Si le patient a développé un SSJ, une NET ou un DRESS sous lamotrigine, le traitement avec de la lamotrigine ne devra jamais être repris chez ce patient.
L'éruption cutanée a également été rapportée dans le cadre d'un DRESS ; aussi connu sous le nom de syndrome d'hypersensibilité. Cette maladie est associée à un tableau variable de symptômes systémiques incluant fièvre, adénopathies, œdèmes de la face, anomalies hématologiques, hépatiques, rénales et méningite aseptique (voir rubrique 4.8). Le syndrome d'expression clinique variable peut, rarement, conduire à une coagulation intra-vasculaire disséminée (CIVD) et à une défaillance multiviscérale. Il est important de noter que des réactions précoces d'hypersensibilité (par exemple fièvre, adénopathies) peuvent être observées alors qu'une éruption cutanée n'est pas évidente. Si ces signes et symptômes surviennent le patient doit alors être immédiatement examiné et LAMICTAL interrompu si une autre étiologie ne peut être établie.
La méningite aseptique était réversible à l’arrêt du traitement dans la majorité des cas, mais était récurrente dans un certain nombre de cas lors d’une ré-exposition à la lamotrigine. La ré-exposition entrainait la réapparition rapide des symptômes qui étaient fréquemment plus sévères. La lamotrigine ne doit pas être réintroduite chez des patients l’ayant interrompue en raison d’une méningite aseptique due au traitement par la lamotrigine.
Des réactions de photosensibilité associées à l’utilisation de lamotrigine ont également été signalées (voir rubrique 4.8). Dans plusieurs cas, la réaction s’est produite avec une dose élevée (400 mg ou plus), en cas d’augmentation de la dose ou d’une augmentation rapide du titrage. Si l’on soupçonne une photosensibilité associée à la lamotrigine chez un patient présentant des signes de photosensibilité (tels qu’un coup de soleil exagéré), il convient d’envisager l’arrêt du traitement. Si la poursuite du traitement par lamotrigine est jugée cliniquement justifiée, il convient de conseiller au patient d’éviter de s’exposer au soleil et à la lumière UV artificielle et de prendre des mesures de protection (par ex. utilisation de vêtements de protection et d’écrans solaires).
Lymphohistiocytose hémophagocytaire (LHH)
Des cas de LHH ont été rapportés chez des patients traités par lamotrigine (voir rubrique 4.8). La LHH est caractérisée par des signes et des symptômes tels que de la fièvre, une éruption cutanée, des symptômes neurologiques, une hépatosplénomégalie, une lymphadénopathie, une cytopénie, une élévation du taux sérique de ferritine, une hypertriglycéridémie ainsi que des anomalies de la fonction hépatique et de la coagulation. Les symptômes surviennent généralement dans les 4 semaines suivant le début du traitement. La LHH peut menacer le pronostic vital.
Les patients doivent être informés des symptômes associés à la LHH et doivent consulter immédiatement un médecin s’ils présentent ces symptômes lors d’un traitement par lamotrigine.
Les signes et symptômes apparaissant chez les patients doivent être immédiatement évalués et le diagnostic d’une LHH doit être envisagé. Le traitement par lamotrigine doit être immédiatement interrompu à moins qu’une étiologie différente puisse être établie.
Aggravation clinique et risque suicidaire
Des idées et comportements suicidaires ont été rapportés chez des patients traités par des AEs dans plusieurs indications. Une méta-analyse d'essais randomisés, contrôlés versus placebo portant sur des AEs a également montré une légère augmentation du risque d'idées et de comportements suicidaires. Les causes de ce risque ne sont pas connues et les données disponibles n'excluent pas la possibilité d'une augmentation de ce risque pour la lamotrigine.
Par conséquent, les patients doivent être étroitement surveillés pour tout signe d'idées et de comportements suicidaires et un traitement approprié doit être envisagé. Il doit être recommandé aux patients (et à leur personnel soignant) de demander un avis médical en cas de survenue de signes d'idées et de comportements suicidaires.
Les patients atteints de troubles bipolaires peuvent avoir une aggravation de leurs symptômes dépressifs et/ou l'émergence d'idées ou comportements suicidaires qu'ils prennent ou non des médicaments pour les troubles bipolaires, y compris LAMICTAL. De ce fait, les patients sous LAMICTAL pour des troubles bipolaires doivent être étroitement surveillés pour toute aggravation clinique (incluant le développement de nouveaux symptômes) et pour des idées et comportements suicidaires, particulièrement à l'instauration du traitement, ou lors de modifications posologiques.
Certains patients, tels que ceux ayant des antécédents d'idées ou de comportements suicidaires, les jeunes adultes, et ceux exprimant un degré significatif d'idées suicidaires avant le début du traitement, peuvent être plus à risque de pensées suicidaires ou de tentatives de suicide et doivent faire l'objet d'une surveillance attentive pendant le traitement.
Il faut envisager un changement du schéma posologique voire un éventuel arrêt du médicament, chez les patients ayant une aggravation clinique (incluant le développement de nouveaux symptômes) et/ou l'émergence d'idées/comportements suicidaires, particulièrement si ces symptômes sont sévères, surviennent brutalement ou ne faisaient pas partie des symptômes présentés par le patient.
Effets des médicaments contenant des œstrogènes, y compris les contraceptifs hormonaux, sur l'efficacité de la lamotrigine
L'utilisation de l'association éthinylestradiol/lévonorgestrel (30 µg/150 µg) multiplie environ par 2 la clairance de la lamotrigine, entraînant une diminution des taux de lamotrigine (voir rubrique 4.5). Une diminution des taux de lamotrigine a été associée à une perte de contrôle des crises. Après titration, une augmentation de la posologie d'entretien de la lamotrigine (jusqu'à 2 fois la dose initiale) sera nécessaire dans la plupart des cas pour atteindre la réponse thérapeutique maximale. Lors de l'arrêt d'un contraceptif hormonal, la clairance de la lamotrigine peut être réduite de moitié. Des augmentations de taux de la lamotrigine peuvent être associées à des effets indésirables dose dépendants. Les patients doivent être suivis en conséquence.
Chez les femmes ne prenant pas encore d'inducteurs de la glucuronisation de la lamotrigine et prenant un contraceptif hormonal qui inclut une semaine de traitement inactif (par exemple « une semaine sans prise de pilule ») des augmentations progressives et transitoires des taux de lamotrigine surviendront durant la semaine de traitement inactif (voir rubrique 4.2). Ce type de variations des taux de lamotrigine peut être associé à des effets indésirables. Dans ce cas, il faut envisager, en première intention, l'utilisation d'une contraception n'incluant pas une semaine sans prise de pilule (par exemple, contraceptif hormonal continu ou méthodes non hormonales).
Les interactions entre la lamotrigine et d'autres contraceptifs oraux ou d’autres traitements contenant des œstrogènes (tels que les THS) n'ont pas été étudiées, bien qu'ils puissent affecter de la même façon les paramètres pharmacocinétiques de la lamotrigine.
Effets de la lamotrigine sur l'efficacité des contraceptifs hormonaux
Une étude d'interaction chez 16 volontaires sains a montré une faible augmentation de la clairance du lévonorgestrel et des changements des taux de FSH et LH sériques (voir rubrique 4.5) lorsque la lamotrigine était administrée de façon concomitante à un contraceptif hormonal (association éthinylestradiol/lévonorgestrel). L'impact de ces changements sur l'activité ovulatoire ovarienne est inconnu. Cependant on ne peut exclure la possibilité que ces changements conduisent à une diminution de l'efficacité du contraceptif chez certaines patientes prenant des spécialités à base d'hormones avec un traitement par lamotrigine. Aussi, les patientes doivent être informées de la nécessité de rapporter rapidement tout changement de leur cycle menstruel tel qu'un saignement imprévu.
Dihydrofolate réductase
La lamotrigine est un faible inhibiteur de la dihydrofolate réductase et pourrait donc interférer avec le métabolisme des folates lors d'un traitement à long terme (voir rubrique 4.6). Toutefois, dans le cadre d'une utilisation prolongée, la lamotrigine n'a pas induit de changements significatifs de la concentration en hémoglobine, du volume globulaire moyen, ou des concentrations en folates du sérum ou des hématies pendant un an, ni de changements significatifs de la concentration en folates des hématies pendant 5 ans.
Insuffisance rénale
Chez les insuffisants rénaux en stade terminal, des études en administration unique n'ont pas révélé de modifications significatives des concentrations plasmatiques en lamotrigine. Cependant une accumulation du métabolite glucuronoconjugué est à prévoir et des précautions d'emploi doivent donc être prises pour le traitement de ces patients.
Patients prenant d'autres spécialités contenant de la lamotrigine
LAMICTAL ne doit pas être administré aux patients déjà traités par toute autre préparation contenant de la lamotrigine sans consultation médicale.
ECG typique du syndrome de Brugada et autres anomalies du rythme cardiaque et de la conduction
Des anomalies arythmogènes du segment ST-T et un tracé d’ECG typique du syndrome de Brugada ont été rapportés chez des patients traités par lamotrigine. Sur la base de résultats in vitro, la lamotrigine pourrait potentiellement ralentir la conduction ventriculaire (élargissement du QRS) et induire une proarythmie à des concentrations thérapeutiques pertinentes chez les patients atteints de maladie cardiaque. La lamotrigine se comporte comme un agent antiarythmique faible de classe IB avec des risques potentiels associés d'événements cardiaques graves ou mortels. L'utilisation concomitante d'autres bloqueurs des canaux sodiques peut encore augmenter les risques (voir rubrique 5.3). Aux doses thérapeutiques allant jusqu'à 400 mg/jour, la lamotrigine n'a pas ralenti la conduction ventriculaire (élargissement du QRS) ni provoqué d'allongement de l'intervalle QT dans une étude approfondie sur l'intervalle QT menée chez des individus sains. L'utilisation de la lamotrigine doit être soigneusement évaluée chez les patients présentant une maladie cardiaque structurelle ou fonctionnelle cliniquement importante telle que le syndrome de Brugada ou d'autres canalopathies cardiaques, une insuffisance cardiaque, une cardiopathie ischémique, un bloc cardiaque ou des arythmies ventriculaires. Si la lamotrigine est cliniquement justifiée chez ces patients, la consultation d'un cardiologue doit être envisagée avant d'initier la lamotrigine.
Excipients
LAMICTAL contient moins de 1 mmol (23 mg) de sodium par comprimé, c’est-à-dire qu’il est essentiellement ’’sans sodium’’.
Développement chez les enfants
Il n'existe aucune donnée sur l'effet de la lamotrigine sur la croissance, la maturation sexuelle et les développements cognitifs, émotionnels et comportementaux des enfants.
Précautions relatives à l'épilepsie
Comme avec d'autres AEs, l'arrêt brutal de LAMICTAL peut provoquer des crises par un effet rebond. La posologie de LAMICTAL doit être progressivement réduite sur une période de deux semaines, sauf s'il s'agit de problèmes de tolérance (par exemple éruption cutanée) nécessitant un arrêt brutal du traitement.
D'après des données issues de la littérature, des crises convulsives sévères incluant l'état de mal peuvent conduire à une rhabdomyolyse, une défaillance multiviscérale et une coagulation intra-vasculaire disséminée pouvant parfois conduire au décès. Des cas similaires sont survenus en association avec l'utilisation de lamotrigine.
Une aggravation clinique significative de la fréquence des crises peut être observée au lieu d'une amélioration de celle-ci. Chez les patients présentant plusieurs types de crises, le bénéfice observé sur le contrôle d'un type de crise doit être pondéré face à une aggravation d'un autre type de crise.
Les crises myocloniques peuvent être aggravées par la lamotrigine.
Les données suggèrent que les réponses au traitement lors d'une association à des inducteurs enzymatiques sont moindres comparées à une association à des médicaments anti-épileptiques non inducteurs enzymatiques. La cause en est mal connue.
Chez les enfants prenant de la lamotrigine pour le traitement d'absences typiques, l'efficacité peut ne pas se maintenir chez tous les patients.
Précautions relatives aux troubles bipolaires
Enfants et adolescents de moins de 18 ans
Le traitement par anti-dépresseur est associé à une augmentation des idées et comportements suicidaires chez les enfants et les adolescents atteints de troubles dépressifs majeurs et d'autres troubles psychiatriques.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Les études d'interaction n'ont été réalisées que chez l'adulte.
Les Uridines 5’-diphospho (UDP)- glucuronyltransférases (UGT) ont été identifiées comme les enzymes responsables du métabolisme de la lamotrigine. Les médicaments qui induisent ou inhibent la glucuronisation peuvent, par conséquent, affecter la clairance apparente de la lamotrigine. Des inducteurs puissants ou modérés des enzymes du cytochrome P450 3A4 (CYP3A4), qui sont également connus pour induire les UGT, peuvent également renforcer le métabolisme de la lamotrigine. Il n’existe aucune preuve que la lamotrigine provoque une induction ou une inhibition cliniquement significative des enzymes du cytochrome P450. La lamotrigine peut induire son propre métabolisme mais l’effet est modeste et il est peu probable qu’il y ait des conséquences cliniquement significatives.
Les médicaments dont il a été démontré qu'ils ont un impact cliniquement pertinent sur la concentration de la lamotrigine sont décrits dans le tableau 6. Les recommandations posologiques spécifiques à ces médicaments sont fournies à la section 4.2. De plus, ce tableau liste les médicaments qui ont montré avoir peu ou pas d’effets sur la concentration de lamotrigine. L’administration simultanée de ces médicaments ne devrait généralement pas avoir d’incidence clinique. Cependant, une attention particulière doit être prise pour les patients dont l'épilepsie est particulièrement sensible aux fluctuations des concentrations de lamotrigine.
Tableau 6 : Effets des médicaments sur la concentration de la lamotrigine
|
Médicaments qui augmentent la concentration de la lamotrigine |
Médicaments qui diminuent la concentration de la lamotrigine |
Médicaments qui ont peu ou pas d’effet sur la concentration de la lamotrigine |
|
Valproate |
Atazanavir/ritonavir* |
Aripiprazole |
|
Carbamazépine |
Buproprion |
|
|
Association éthinylestradiol/lévonorgestrel* |
Felbamate |
|
|
Lopinavir/ritonavir |
Gabapentine |
|
|
Phénobarbital |
Lacosamide |
|
|
|
Phénytoïne |
Lévétiracétam |
|
|
Primidone |
Lithium |
|
Rifampicine |
Olanzapine |
|
|
Oxcarbazépine |
||
|
|
|
Paracétamol |
|
|
|
Pérempanel |
|
|
|
Prégabaline |
|
|
|
Topiramate |
|
|
|
Zonisamide |
*Pour le schéma posologique, voir rubrique 4.2 et pour les femmes prenant des contraceptifs hormonaux, voir également rubrique 4.4
Interactions impliquant les anti-épileptiques
Le valproate, qui inhibe la glucuronisation de la lamotrigine, réduit le métabolisme de la lamotrigine et augmente la demi-vie de la lamotrigine d'approximativement 2 fois. Chez les patients recevant un traitement concomitant avec le valproate, le schéma posologique approprié doit être appliqué (voir rubrique 4.2).
Certains AEs (tels que la phénytoïne, la carbamazépine, le phénobarbital et la primidone) qui induisent les enzymes du cytochrome P450 induisent également les UGT et donc renforcent le métabolisme de la lamotrigine. Chez les patients recevant un traitement concomitant avec la phénytoïne, la carbamazépine, le phénobarbital ou la primidone, le schéma posologique approprié doit être appliqué (voir rubrique 4.2).
Des évènements affectant le système nerveux central ont été rapportés incluant sensations vertigineuses, ataxie, diplopie, vision floue et nausée suite à l'introduction de la lamotrigine chez des patients prenant de la carbamazépine.
Ces évènements se résolvent habituellement quand la dose de carbamazépine est réduite. Un effet similaire a été observé pendant une étude sur la lamotrigine et l'oxcarbazépine chez des volontaires sains adultes, mais la réduction de doses n'a pas été testée.
Des cas de diminution des taux de lamotrigine ont été rapportés dans la littérature lorsque la lamotrigine était donnée en association avec de l'oxcarbazépine. Cependant, dans une étude prospective chez des volontaires sains adultes prenant des doses de 200 mg de lamotrigine et de 1200 mg d'oxcarbazépine, l'oxcarbazépine n'a pas modifié le métabolisme de la lamotrigine et la lamotrigine n'a pas modifié le métabolisme de l'oxcarbazépine. Par conséquent, chez les patients recevant un traitement concomitant contenant de l'oxcarbazépine, il faut utiliser le schéma posologique de la lamotrigine en association sans le valproate et sans inducteur de la glucuronisation de la lamotrigine (voir rubrique 4.2).
Dans une étude chez des volontaires sains, la coadministration de felbamate (1200 mg 2 fois par jour) avec de la lamotrigine (100 mg 2 fois par jour pendant 10 jours) n'a pas semblé avoir d'effets cliniquement significatifs sur la pharmacocinétique de la lamotrigine.
Sur la base d'analyse rétrospective des taux plasmatiques de patients ayant reçu de la lamotrigine à la fois avec et sans gabapentine, la gabapentine n'a pas semblé modifier la clairance apparente de la lamotrigine.
Les interactions potentielles entre le lévétiracétam et la lamotrigine ont été évaluées par l'examen des concentrations sériques des deux agents durant des essais cliniques contre placebo. Ces données indiquent que la lamotrigine n'influence pas la pharmacocinétique du lévétiracétam et que le lévétiracétam n'influence pas la pharmacocinétique de la lamotrigine.
Les concentrations plasmatiques de la lamotrigine à l’état d’équilibre n’ont pas été affectées par l'administration concomitante de prégabaline (200 mg, 3 fois par jour). Il n'y a aucune interaction pharmacocinétique entre la lamotrigine et la prégabaline.
Le topiramate n'a conduit à aucune modification des concentrations plasmatiques de lamotrigine. L'administration de la lamotrigine a conduit à une augmentation de 15 % des concentrations en topiramate.
Dans un essai chez des patients épileptiques, la coadministration de zonisamide (200 à 400 mg/jour) et de lamotrigine (150 à 500 mg/jour) pendant 35 jours n'a eu aucun effet significatif sur la pharmacocinétique de la lamotrigine.
Dans un essai clinique contrôlé contre placebo chez des patients souffrant de crises partielles, les concentrations plasmatiques de lamotrigine n’ont pas été affectées après administration concomitante de lacosamide (200, 400, ou 600 mg/jour).
L’analyse groupée de données de 3 essais contrôlés contre placebo ayant évalué le traitement en association avec pérampanel chez des patients souffrant de crises partielles et de crises généralisées tonico-cloniques, la dose la plus élevée de pérampanel qui a été évaluée (12 mg/jour) a augmenté la clairance de la lamotrigine de moins de 10%.
Bien que des modifications des concentrations plasmatiques d'autres AEs aient été rapportées, des études contrôlées n'ont révélé aucune preuve que la lamotrigine affecte les concentrations plasmatiques des AEs concomitants. Des preuves issues d'études in vitro indiquent que la lamotrigine ne déplace pas les autres AEs de leurs sites de liaison aux protéines.
Interactions impliquant d'autres agents psycho-actifs
La pharmacocinétique du lithium après la prise de 2 g de gluconate de lithium anhydre deux fois par jour pendant six jours chez 20 sujets sains n'a pas été modifiée par la co-administration de 100 mg/jour de lamotrigine.
Des doses orales multiples de bupropion n'ont eu aucun effet statistiquement significatif sur la pharmacocinétique d'une dose unique de lamotrigine chez 12 sujets et ont donné qu'une légère augmentation de l'ASC du glucuronoconjugué de la lamotrigine.
Dans une étude chez des volontaires adultes sains, 15 mg d'olanzapine a réduit l'ASC et la Cmax de la lamotrigine de valeurs moyennes respectives de 24 % et 20 %. La lamotrigine à 200 mg n'a pas affecté la pharmacocinétique de l'olanzapine.
Des doses orales multiples de lamotrigine de 400 mg par jour n'ont eu aucun effet cliniquement significatif sur la pharmacocinétique d'une dose unique de 2 mg de rispéridone chez 14 adultes volontaires sains.
Suite à la co-administration de 2 mg de rispéridone avec de la lamotrigine, 12 des 14 volontaires ont rapporté une somnolence contre 1 sur 20 quand la rispéridone a été donnée seule et aucun quand la lamotrigine a été administrée seule.
Dans une étude de 18 patients adultes atteints de trouble bipolaire de type I, recevant un traitement d’entretien de lamotrigine (100 – 400 mg / jour), des doses d'aripiprazole ont été augmentées de 10 mg/jour pour atteindre 30 mg/jour sur une période de 7 jours. Cette posologie a été poursuivie pendant les 7 jours suivants à raison d’une prise quotidienne. Une réduction moyenne d'environ 10 % de la Cmax et de l'ASC de la lamotrigine a été observée.
Des expériences in vitro ont indiqué que la formation du métabolite primaire de la lamotrigine, le 2-N-glucuronide, a été inhibée de façon minimale par la co-incubation avec de l'amitriptyline, du bupropion, du clonazépam, de l'halopéridol ou du lorazépam. Ces expériences ont également suggéré qu'il est peu probable que le métabolisme de la lamotrigine ait été inhibé par la clozapine, la fluoxétine, la phénelzine, la rispéridone, la sertraline ou la trazodone. De plus, une étude du métabolisme du bufuralol utilisant des préparations de microsomes hépatiques humains a suggéré que la lamotrigine ne réduirait pas la clairance des médicaments majoritairement métabolisés par le cytochrome CYP2D6.
Interactions impliquant les contraceptifs hormonaux
Effet des contraceptifs hormonaux sur la pharmacocinétique de la lamotrigine
Dans une étude chez 16 femmes volontaires, l'administration de 30 µg d'éthinylestradiol et 150 µg de lévonorgestrel associés dans une pilule contraceptive orale a provoqué approximativement un doublement de la clairance orale de la lamotrigine, conduisant à des réductions moyennes de l'ASC et de la Cmax respectivement de 52 % et 39 %. Les concentrations sériques de la lamotrigine ont augmenté au cours de la semaine de traitement inactif (incluant « la semaine sans prise de pilule »), avec des concentrations avant la prise à la fin de la semaine de traitement inactif, en moyenne, environ 2 fois plus élevées que pendant le traitement associé (voir rubrique 4.4). Aucun ajustement selon les lignes directrices sur l'escalade de dose recommandée de la lamotrigine ne devrait être nécessaire pour la seule raison de l'utilisation de contraceptifs hormonaux, mais la dose d'entretien de la lamotrigine devra être augmentée ou diminuée dans la plupart des cas lors de l'instauration ou de l'arrêt de contraceptifs hormonaux (voir rubrique 4.2).
Effet de la lamotrigine sur la pharmacocinétique des contraceptifs hormonaux
Dans une étude chez 16 femmes volontaires, une dose de maintien de 300 mg de lamotrigine n'a eu aucun effet sur la pharmacocinétique de la composante éthinylestradiol dans l'association d'une pilule contraceptive orale. Il a été observé une légère augmentation de la clairance orale de la composante lévonorgestrel, conduisant à des réductions moyennes de l'ASC et de la Cmax respectivement de 19 % et 12 %. Les mesures des taux sériques de FSH, LH et d'œstradiol pendant l'étude ont indiqué quelques pertes de suppression de l'activité hormonale ovarienne chez quelques femmes, bien que la mesure de la progestérone sérique ait indiqué qu'il n'y a eu aucune preuve hormonale de l'ovulation chez aucun des 16 sujets. L'impact de la légère augmentation de la clairance du lévonorgestrel, et des modifications des taux sériques de FSH et de LH, sur l'activité ovulatoire ovarienne est inconnu (voir rubrique 4.4). Les effets des doses de lamotrigine autres que 300 mg/jour n'ont pas été étudiés et il n'y a pas eu d'études avec d'autres spécialités à base d'hormones féminines.
Interactions impliquant d'autres médicaments
Dans une étude chez 10 hommes volontaires, la rifampicine a augmenté la clairance de la lamotrigine et diminué la demi-vie de la lamotrigine par induction des enzymes hépatiques responsables de la glucuronisation. Chez les patients recevant un traitement concomitant avec la rifampicine, le schéma posologique approprié doit être appliqué (voir rubrique 4.2).
Dans une étude chez des volontaires sains, l'association lopinavir/ritonavir a diminué environ de moitié les concentrations plasmatiques de la lamotrigine, probablement par induction de la glucuronisation. Chez les patients recevant un traitement concomitant avec l'association lopinavir/ritonavir, le schéma posologique approprié doit être appliqué (voir rubrique 4.2).
Dans une étude chez des volontaires sains adultes, l’association atazanavir/ritonavir (300 mg/100 mg) administrée pendant 9 jours, a réduit l’ASC et la Cmax plasmatiques de la lamotrigine (dose unique de 100 mg) en moyenne de 32% et 6%, respectivement. Chez les patients recevant un traitement concomitant avec l'association atazanavir/ritonavir, le schéma posologique approprié doit être appliqué (voir rubrique 4.2).
Dans une étude chez des volontaires sains adultes, 1 g de paracétamol (quatre fois par jour) a réduit l’ASC et la Cmin plasmatiques de la lamotrigine en moyenne de 20 et 25%, respectivement.
Des données in vitro montrent que la lamotrigine, mais pas le métabolite 2-N-glucuronide, est un inhibiteur du transporteur des cations organiques 2 (TCO2) à des concentrations potentiellement cliniquement significatives. Ces données démontrent que la lamotrigine est un inhibiteur du TCO2 avec une valeur de CI50 de 53,8 µM. La co-administration de la lamotrigine avec des médicaments excrétés par les reins qui sont des substrats du TCO2 (par exemple, la metformine, la gabapentine et la varénicline) peut entraîner une augmentation des taux plasmatiques de ces médicaments.
La signification clinique n'a pas été clairement définie, toutefois une attention particulière devra être portée aux patients recevant de telles associations.
4.6. Fertilité, grossesse et allaitement
Risque lié aux antiépileptiques en général
Un avis spécialisé doit être donné aux femmes épileptiques en âge de procréer. Le traitement antiépileptique doit être réévalué lorsqu'une femme envisage une grossesse. Chez les femmes traitées pour une épilepsie, un arrêt brutal du traitement antiépileptique doit être évité car cela peut entraîner la réapparition de crises dont les conséquences pour la mère et le fœtus peuvent être graves. La monothérapie doit être préférée chaque fois que cela est possible car une polythérapie antiépileptique peut être associée à un risque plus élevé de malformations congénitales qu’une monothérapie. Le risque de malformations congénitales lié à la polythérapie varie en fonction des antiépileptiques co-administrés.
Risque lié à la lamotrigine
Grossesse
L’analyse d’un nombre élevé de données chez les femmes exposées à la lamotrigine en monothérapie pendant le premier trimestre de grossesse (plus de 8700) n’a pas mis en évidence d’augmentation substantielle du risque de malformations congénitales majeures y compris les fentes labio-palatines. Les études chez l'animal ont montré une toxicité sur le développement (voir rubrique 5.3).
Si un traitement par LAMICTAL est considéré comme nécessaire durant la grossesse, la dose thérapeutique la plus faible est recommandée.
La lamotrigine a un léger effet inhibiteur sur l'acide dihydrofolique réductase et pourrait par conséquent théoriquement conduire à un risque accru de préjudices embryofœtaux par diminution des taux d'acide folique. La prise d'acide folique doit être envisagée lorsqu'une grossesse est prévue et durant le début de la grossesse.
Les changements physiologiques durant la grossesse peuvent modifier les concentrations de lamotrigine et/ou son effet thérapeutique. Des cas de diminution des taux plasmatiques de lamotrigine durant la grossesse ont été rapportés avec un risque potentiel de perte de contrôle des crises. Après la naissance, les taux de lamotrigine peuvent augmenter rapidement avec un risque d'effets indésirables dose-dépendants. Par conséquent, les concentrations sériques de lamotrigine doivent être surveillées avant, pendant et après la grossesse, tout comme rapidement après la naissance. Si nécessaire, la dose doit être adaptée pour maintenir la concentration sérique de la lamotrigine au même niveau qu’avant la grossesse ou adaptée à la réponse clinique. De plus, les effets indésirables dose-dépendants doivent être surveillés après la naissance.
Il a été rapporté que la lamotrigine passe dans le lait maternel à des concentrations fortement variables entraînant chez les nourrissons des taux en lamotrigine totaux allant jusqu’à environ 50 % de ceux de la mère. Par conséquent, chez les nourrissons allaités, les concentrations sériques de lamotrigine peuvent atteindre des taux auxquels des effets pharmacologiques peuvent survenir.
Les bénéfices potentiels de l'allaitement doivent être évalués face au risque potentiel de survenue d'effets indésirables chez le nourrisson. Si une femme décide d'allaiter son enfant pendant qu'elle est traitée par lamotrigine, il faudra surveiller les effets indésirables chez le nourrisson, tels que la somnolence, une éruption cutanée ou une prise de poids insuffisante.
Fertilité
Des études effectuées chez l'animal n'ont révélé aucune altération de la fertilité par la lamotrigine (voir rubrique 5.3).
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Les effets sur l'aptitude à conduire des véhicules et à utiliser des machines n'ont pas été étudiés. Deux études chez des volontaires ont montré que l'effet de la lamotrigine sur la coordination motrice visuelle fine, les mouvements oculaires, le balancement du corps et les effets sédatifs subjectifs ne sont pas différents par rapport au placebo. Dans les essais cliniques avec la lamotrigine les évènements indésirables à caractère neurologique tels que des sensations vertigineuses et une diplopie ont été rapportés. Par conséquent, les patients doivent voir dans quelle mesure le traitement par LAMICTAL les affecte avant de conduire ou d'utiliser une machine.
Les effets indésirables pour les indications d’épilepsie et de troubles bipolaires sont basés sur les données disponibles issues d’essais cliniques contrôlés et d’autres expériences cliniques et sont listés dans le tableau ci-dessous. Les catégories des fréquences proviennent des essais cliniques contrôlés (en monothérapie pour l’épilepsie (identifiées par une croix ) et pour les troubles bipolaires (identifiées par le symbole §)). Lorsque les catégories des fréquences diffèrent entre les données des essais cliniques de l’épilepsie et ceux des troubles bipolaires, la fréquence la plus élevée est mentionnée. Toutefois lorsqu’aucune donnée d’essais cliniques contrôlés n’est disponible, les catégories de fréquences étaient obtenues à partir d’autres essais cliniques.
La convention suivante a été utilisée pour la classification des effets indésirables : très fréquent (≥ 1/10), fréquent (≥ 1/100 à < 1/10), peu fréquent (≥ 1/1 000 à < 1/100), rare (≥ 1/10 000 à < 1/1 000), très rare (< 1/10 000), indéterminée (ne peut être estimé à partir des données disponibles).
|
Système organe |
Effets indésirables |
Fréquence |
|
Affections hématologiques et du système lymphatique |
Anomalies hématologiques1 incluant neutropénies, leucopénies, anémies, thrombopénies, pancytopénies, anémies aplasiques, agranulocytoses Lymphohistiocytose hémophagocytaire (LHH) (voir rubrique 4.4) Adénopathie1, Pseudolymphome |
Très rare
Très rare Indéterminée |
|
Affections du système immunitaire |
Syndrome d'hypersensibilité2 Hypogammaglobulinémie |
Très rare Indéterminée |
|
Affections psychiatriques |
Agressivité, irritabilité Confusion, hallucinations, tics (moteurs et/ou vocaux) Cauchemars |
Fréquent Très rare Indéterminée |
|
Affections du système nerveux |
Céphalées§ Somnolence§, sensations vertigineuses§, tremblements, insomnie, agitation§ |
Très fréquent Fréquent
|
|
Ataxie |
Peu fréquent |
|
|
Nystagmus, méningite aseptique (voir rubrique 4.4) |
Rare |
|
|
Instabilité, mouvements anormaux, aggravation de la maladie de Parkinson3, syndrome extrapyramidal, choréoathétose, augmentation de la fréquence des crises d’épilepsie |
Très rare |
|
|
Affections oculaires |
Diplopie, vision floue Conjonctivite |
Peu fréquent Rare |
|
Affections gastro-intestinales |
Nausées, vomissements, diarrhée, sécheresse buccale§ |
Fréquent |
|
Affections hépatobiliaires |
Insuffisance hépatique, dysfonctionnement hépatique4, augmentation des valeurs des tests hépatiques |
Très rare |
|
Affections de la peau et du tissu sous-cutané |
Eruptions cutanées5§ Alopécie, réaction de photosensibilité Erythème polymorphe, Syndrome de Stevens-Johnson§ Nécrolyse épidermique toxique Syndrome d’hypersensibilité médicamenteuse avec éosinophilie et symptômes systémiques2 |
Très fréquent Peu fréquent Rare
Très rare Très rare |
|
Affections musculo squelettiques et systémiques |
Arthralgie§ Réactions type lupus |
Fréquent Très rare |
|
Affections rénales et urinaires |
Néphrite tubulo-interstitielle, néphrite tubulo-interstitielle et uvéite |
Indéterminée |
|
Troubles généraux et anomalies au site d'administration |
Fatigue, douleur§, douleur du dos§ |
Fréquent |
Description des effets indésirables sélectionnés :
1 Les anomalies hématologiques et les adénopathies peuvent être ou non associées à un syndrome d’hypersensibilité médicamenteuse avec éosinophilie et symptômes systémiques (DRESS) / syndrome d'hypersensibilité (voir rubrique 4.4 et Affections du système immunitaire).
2 Des éruptions cutanées ont également été rapportées dans le cadre de ce syndrome, aussi connu sous le nom de DRESS. Cette maladie est associée à un tableau variable de symptômes systémiques incluant fièvre, adénopathies, oedèmes de la face et anomalies hématologiques, hépatiques et rénales. Ce syndrome d'expression clinique variable peut, rarement, conduire à une coagulation intra vasculaire disséminée et à une défaillance multiviscérale. Il est important de noter que des réactions précoces d'hypersensibilité (par exemple fièvre, adénopathies) peuvent être observées alors qu'une éruption cutanée n'est pas évidente. Si ces signes et symptômes surviennent, le patient doit alors être immédiatement examiné et LAMICTAL interrompu si une autre étiologie ne peut être établie (voir rubrique 4.4).
3 Ces effets ont été rapportés dans d’autres essais cliniques.
Des cas d'aggravation de symptômes parkinsoniens liés à la lamotrigine ont été rapportés chez des patients ayant une maladie de Parkinson préexistante, des effets extrapyramidaux et des choréoathétoses ont également été rapportés de façon isolée chez des patients n'ayant pas cette pathologie sous-jacente.
4 Un dysfonctionnement hépatique survient généralement en association avec des réactions d'hypersensibilité mais des cas isolés ont été rapportés sans signe manifeste d'hypersensibilité.
5 Dans des essais cliniques chez l’adulte, les éruptions cutanées sont survenues jusqu’à 8 à 12 % des patients prenant de la lamotrigine et chez 5 à 6 % des patients prenant un placebo. Les éruptions cutanées ont conduit à l’arrêt du traitement par la lamotrigine chez 2 % des patients. L'éruption, généralement maculopapuleuse en apparence, apparaît généralement dans les huit premières semaines de traitement et se résout à l’arrêt du traitement par LAMICTAL (voir rubrique 4.4).
Des éruptions cutanées graves pouvant mettre en jeu le pronostic vital, incluant le syndrome de Stevens-Johnson et la nécrolyse épidermique toxique (Syndrome de Lyell) et un syndrome d’hypersensibilité médicamenteuse avec éosinophilie et symptômes systémiques (syndrome DRESS) ont été rapportées. Bien que la majorité guérisse à l'arrêt du traitement par la lamotrigine, quelques patients ont des séquelles irréversibles et il y a eu de rares cas de décès associés (voir rubrique 4.4).
Le risque global d'éruptions cutanées, semble être fortement lié à :
· des doses initiales de lamotrigine élevées et dépassant le schéma d'escalade de dose recommandée (voir rubrique 4.2)
· l'utilisation concomitante de valproate (voir rubrique 4.2).
Il a été rapporté des cas de diminution de la densité minérale osseuse, d’ostéopénie, d’ostéoporose et de fractures chez des patients traités au long terme avec de la lamotrigine. Le mécanisme par lequel la lamotrigine affecte le métabolisme osseux n’a pas été identifié.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/
Des ingestions de doses massives excédant de 10 à 20 fois la dose thérapeutique maximale incluant des cas mortels ont été rapportées. Le surdosage a conduit à des symptômes comprenant nystagmus, ataxie, trouble de la conscience, crises convulsives tonico-cloniques et coma. Un élargissement du QRS (retard à la conduction intraventriculaire) et un allongement de l’intervalle QT ont également été observés chez les patients en surdosage. L’élargissement de plus de 100 ms de la durée du QRS peut être associé à une toxicité plus sévère.
Traitement
En cas de surdosage, il convient d'hospitaliser le patient et de lui administrer le traitement adéquat. Un traitement visant à diminuer l'absorption devra être mis en place (charbon activé), si cela est indiqué. Une prise en charge supplémentaire devra être instaurée selon l’état clinique du patient, en tenant compte des effets potentiels sur la conduction cardiaque (voir rubrique 4.4). L'utilisation d'une thérapie lipidique intraveineuse peut être envisagée pour le traitement de la cardiotoxicité qui ne répondant pas suffisamment au bicarbonate de sodium. Il n'y a pas de données concernant l'utilisation de l'hémodialyse comme traitement d'un surdosage. Chez six volontaires insuffisants rénaux, 20 % de la lamotrigine a été retiré de l'organisme pendant une session d'hémodialyse de 4 heures (voir rubrique 5.2).
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : autres anti épileptiques, code ATC : N03AX09
Mécanisme d’action
Les résultats d'études pharmacologiques suggèrent que la lamotrigine bloque préférentiellement et de façon voltage-dépendante les canaux sodiques activés. Cela inhibe l'activation répétitive et soutenue des neurones et inhibe la libération du glutamate (le neurotransmetteur qui joue un rôle clé dans la genèse des crises d'épilepsie). Ces effets contribuent probablement aux propriétés anti-convulsivantes de la lamotrigine.
A l'inverse, les mécanismes par lesquels la lamotrigine exerce son action thérapeutique sur les troubles bipolaires n'ont pas été établis, bien que les interactions canaux sodium voltage-dépendants soient probablement importantes.
Effets pharmacodynamiques
Dans les tests conçus pour évaluer les effets des médicaments sur le système nerveux central, les résultats obtenus en utilisant une dose de 240 mg de lamotrigine administrée à des volontaires sains n'ont pas différé du placebo, tandis qu'à la fois 1000 mg de phénytoïne et 10 mg de diazépam ont chacun atteint significativement la coordination motrice visuelle fine et les mouvements oculaires, augmenté le balancement du corps et produit des effets sédatifs subjectifs.
Dans une autre étude, des doses orales uniques de 600 mg de carbamazépine ont significativement atteint la coordination motrice visuelle fine et les mouvements oculaires, tout en augmentant le balancement du corps et le rythme cardiaque, alors que les résultats avec des doses de lamotrigine de 150 mg et 300 mg n'ont pas différé du placebo.
Etude de l'effet de la lamotrigine sur la conduction cardiaque
Une étude menée chez des volontaires adultes sains a évalué l'effet de doses répétées de lamotrigine (jusqu'à 400 mg/jour) sur la conduction cardiaque, évaluée par un ECG à 12 dérivations. Il n'y a pas eu d'effet cliniquement significatif de la lamotrigine sur l'intervalle QT par rapport au placebo.
Efficacité et sécurité cliniques
Prévention des épisodes thymiques chez les patients atteints de troubles bipolaires
L'efficacité de la lamotrigine dans la prévention des épisodes thymiques chez les patients atteints de trouble bipolaire de type I a été évaluée dans deux études.
L'étude SCAB2003 a été une étude multicentrique, randomisée, en double aveugle, double placebo, contrôlée contre placebo et lithium et à dose fixe, ayant évalué la prévention à long terme des rechutes et récurrences d'épisodes de dépression et/ou de manie chez les patients présentant un trouble bipolaire de type I et ayant présenté récemment ou présentant un épisode dépressif majeur.
Une fois stabilisés par de la lamotrigine administrée en monothérapie ou en association, les patients ont été randomisés dans l'un des cinq groupes de traitement : lamotrigine (50, 200, 400 mg/jour), lithium (taux sériques de 0,8 à 1,1 mMol/L) ou placebo pendant 76 semaines au maximum (18 mois). Le critère principal d'évaluation a été le "Délai d'intervention pour un épisode thymique (TIME)", l'intervention étant définie par un traitement pharmacologique complémentaire ou une sismothérapie (ou électroconvulsivothérapie, ECT). L'étude SCAB2006 a eu une méthodologie similaire à celle de l'étude SCAB2003, mais différente de l'étude SCAB2003 par l'évaluation de doses flexibles de lamotrigine (100 à 400 mg/jour) et par l'inclusion de patients présentant un trouble bipolaire de type I qui devaient avoir présenté récemment ou présentaient un épisode maniaque. Les résultats sont présentés dans le tableau 7.
Tableau 7 : Résumé des résultats des études ayant évalué l'efficacité de la lamotrigine dans la prévention des épisodes thymiques chez les patients présentant un trouble bipolaire de type I
|
'Proportion' de patients sans évènement à la semaine 76 |
||||||
|
Etude SCAB2003 |
Etude SCAB2006 |
|||||
|
Critère d'inclusion |
Episode dépressif majeur |
Episode maniaque majeur |
||||
|
Lamotrigine |
Lithium |
Placebo |
Lamotrigine |
Lithium |
Placebo |
|
|
Sans intervention |
0,22 |
0,21 |
0,12 |
0,17 |
0,24 |
0,04 |
|
Valeur de p (probabilité associée au test du log rank) |
0,004 |
0,006 |
- |
0,023 |
0,006 |
- |
|
Sans dépression |
0,51 |
0,46 |
0,41 |
0,82 |
0,71 |
0,40 |
|
Valeur de p (probabilité associée au test du log rank) |
0,047 |
0,209 |
- |
0,015 |
0,167 |
- |
|
Sans manie |
0,70 |
0,86 |
0,67 |
0,53 |
0,64 |
0,37 |
|
Valeur de p (probabilité associée au test du log rank) |
0,339 |
0,026 |
- |
0,280 |
0,006 |
- |
Dans des analyses portant sur le délai de survenue d'un premier épisode dépressif et le délai de survenue d'un premier épisode maniaque/hypomaniaque ou d'un épisode mixte, les patients traités par la lamotrigine ont eu des délais de survenue d'un premier épisode dépressif significativement plus longs que les patients sous placebo, et la différence entre les traitements pour le délai de survenue d'un premier épisode maniaque/hypomaniaque ou d'un épisode mixte n'a pas été statistiquement significative.
L'efficacité de la lamotrigine en association avec des thymorégulateurs n'a pas été suffisamment étudiée.
Enfants âgés de 1 à 24 mois
L'efficacité et la tolérance de la lamotrigine en association dans le traitement des crises partielles chez les enfants de 1 à 24 mois ont été évaluées dans un petit essai de sevrage en double aveugle contrôlé versus placebo. Le traitement a été initié chez 177 sujets selon un schéma d'augmentation des doses semblable à celui utilisé pour les enfants âgés de 2 à 12 ans. Comme les comprimés de 2 mg de lamotrigine correspondent au plus faible dosage disponible, ce schéma standard de posologie a été adapté dans certains cas durant la phase d'augmentation des doses (par exemple, en administrant un comprimé de 2 mg 1 jour sur 2 quand la dose calculée était inférieure à 2 mg). Les taux sériques ont été mesurés à la fin de la semaine 2 de titration et les doses suivantes étaient alors réduites ou restaient inchangées si la concentration dépassait 0,41 µg/mL, soit la concentration attendue chez les adultes à ce stade. Des réductions de doses allant jusqu'à 90 % ont été nécessaires chez certains patients à la fin de la semaine 2. Trente-huit patients répondeurs (diminution de la fréquence des crises > 40 %) ont été randomisés pour recevoir un placebo ou la lamotrigine. La proportion de sujets ayant présenté un échec au traitement a été de 84 % (16 sujets/19) dans le bras placebo et de 58 % (11 sujets/19) dans le bras lamotrigine. La différence n'a pas été statistiquement significative : 26,3 %, IC 95 % [-2,6 ; 50,2 %], p = 0,07.
Deux cent cinquante-six sujets au total, âgés de 1 à 24 mois, ont été exposés à la lamotrigine à des doses allant de 1 à 15 mg/kg/jour pendant 72 semaines au maximum. Le profil de tolérance de la lamotrigine chez ces enfants âgés de 1 mois à 2 ans a été similaire à celui d'enfants plus âgés à l'exception de l'aggravation cliniquement significative des crises (≥ 50 %) qui a été rapportée plus fréquemment chez les enfants de moins de 2 ans (26 %) comparé aux enfants plus âgés (14 %).
Syndrome de Lennox-Gastaut
Il n’existe pas de données sur la monothérapie dans les crises associées à un syndrome de Lennox-Gastaut.
Prévention des épisodes thymiques chez les enfants (10-12 ans) et adolescents (13-17 ans)
Une étude de sevrage multicentrique, randomisée avec groupes parallèles, contrôlée versus placebo et en double aveugle a évalué l'efficacité et la sécurité de la lamotrigine à libération immédiate comme traitement d’entretien en association pour retarder les épisodes thymiques chez les enfants et les adolescents (âgés de 10 à 17 ans) de sexe masculin et féminin chez qui un trouble bipolaire de type I avait été diagnostiqué et qui étaient en rémission ou présentaient une amélioration d'un épisode bipolaire au cours d’un traitement par lamotrigine en association avec un antipsychotique ou d'autres médicaments stabilisateurs de l'humeur. Le résultat de l'analyse primaire d'efficacité (délai d'apparition d'un événement bipolaire - TOBE) n'a pas atteint une significativité statistique (p = 0,0717), ainsi l'efficacité n'a pas été démontrée. De plus, les résultats concernant la sécurité ont montré un nombre de cas de comportements suicidaires accru chez les patients traités par la lamotrigine : 5% (4 patients) dans le bras lamotrigine comparativement à 0 dans le groupe placebo (voir rubrique 4.2).
5.2. Propriétés pharmacocinétiques
La lamotrigine est rapidement et complètement absorbée au niveau intestinal avec un effet de premier passage hépatique négligeable. Le pic plasmatique est atteint environ 2,5 heures après l'administration orale du produit. La nourriture retarde légèrement le pic de concentration plasmatique mais sans modifier la quantité absorbée.
Il existe une grande variation inter-individuelle des concentrations plasmatiques à l'état d'équilibre mais les concentrations pour un même individu varient rarement.
Distribution
Le taux de liaison de la lamotrigine aux protéines plasmatiques est de 55 % ; il est peu probable qu'un déplacement de la liaison de la lamotrigine aux protéines plasmatiques entraîne un effet toxique.
Le volume de distribution est de 0,92 à 1,22 L/kg.
Biotransformation
Les UDP-glucuronyltransférases ont été identifiées comme les enzymes responsables du métabolisme de la lamotrigine.
La lamotrigine induit son propre métabolisme de façon modérée et dose-dépendante.
D'autre part, la lamotrigine ne semble pas affecter la pharmacocinétique des autres AEs et les données suggèrent que les interactions entre la lamotrigine et les médicaments métabolisés par les enzymes du cytochrome P450 sont peu probables.
Élimination
La clairance plasmatique apparente chez le sujet sain est d'environ 30 mL/min. La clairance de la lamotrigine est initialement métabolique avec l'élimination consécutive de dérivés glucuronoconjugués dans les urines. Moins de 10 % sont excrétés inchangés dans les urines. Seulement 2 % environ des métabolites sont excrétés dans les fèces.
La clairance et la demi-vie d'élimination sont indépendantes de la dose administrée. La demi-vie plasmatique apparente chez le sujet sain est estimée à approximativement 33 heures (valeurs limites allant de 14 à 103 heures). Dans une étude chez des sujets atteints du syndrome de Gilbert, la clairance apparente moyenne a été réduite de 32 % par rapport au groupe contrôle, mais les valeurs sont restées dans les valeurs limites de la population générale.
La demi-vie de la lamotrigine est grandement affectée par les co-médications. La demi-vie moyenne est réduite approximativement à 14 heures avec des inducteurs de la glucuronisation comme la carbamazépine et la phénytoïne et augmente à 70 heures en moyenne quand la lamotrigine est administrée avec du valproate seul (voir rubrique 4.2).
Linéarité
La pharmacocinétique est linéaire jusqu'à 450 mg, correspondant à la plus haute dose unitaire testée.
Populations spéciales
Enfants
La clairance ajustée au poids du corps est plus grande chez les enfants que chez les adultes avec les valeurs les plus élevées chez les enfants de moins 5 ans. La demi-vie est généralement plus courte chez les enfants que chez les adultes avec une valeur moyenne d'approximativement 7 heures quand elle est administrée avec des médicaments inducteurs enzymatiques comme la carbamazépine et la phénytoïne et augmente à des valeurs moyennes de 45 à 50 heures quand elle est administrée avec du valproate seul (voir rubrique 4.2).
Nourrissons âgés de 2 à 26 mois
Chez 143 patients âgés de 2 à 26 mois, pesant de 3 à 16 kg, la clairance a été diminuée par rapport aux enfants plus âgés de même poids corporel, recevant des doses orales par kg de poids corporel semblables à celles utilisées pour des enfants âgés de plus de 2 ans. La demi-vie moyenne a été estimée à 23 heures chez les nourrissons de moins de 26 mois traités concomitamment par inducteur enzymatique, à 136 heures lors de la co-administration avec le valproate et à 38 heures chez les sujets traités sans inducteur/inhibiteur enzymatique associé. La variabilité inter-individuelle de la clairance orale a été élevée dans le groupe de patients de 2 à 26 mois (47 %). Les taux prévisibles de concentration sérique chez les nourrissons de 2 à 26 mois se sont généralement situés dans le même intervalle que ceux des enfants plus âgés, bien que des taux plus élevés de Cmax puissent être observés chez certains enfants avec un poids inférieur à 10 kg.
Sujets âgés
Les résultats d'une analyse pharmacocinétique de population incluant des patients épileptiques jeunes et âgés ayant participé aux mêmes essais cliniques, montrent que la clairance de la lamotrigine n'est pas modifiée de façon cliniquement significative. Après administration de doses uniques, la clairance apparente diminue de 12 % et passe de 35 mL/min chez les patients de 20 ans à 31 mL/min chez les patients de 70 ans. Après un traitement de 48 semaines, elle diminue de 10 % et passe de 41 mL/min chez les patients jeunes à 37 mL/min chez les patients âgés. De plus, les paramètres pharmacocinétiques de la lamotrigine ont été étudiés chez 12 sujets âgés sains après l'administration d'une dose unique de 150 mg.
La clairance moyenne chez les patients âgés (0,39 mL/min/kg) se situe dans l'intervalle des valeurs moyennes de clairance (0,31 à 0,65 mL/min/kg) obtenues au cours de 9 essais réalisés chez des adultes non-âgés, après administration d'une dose unique allant de 30 à 450 mg.
Insuffisants rénaux
Douze volontaires atteints d'insuffisance rénale chronique et six autres sujets sous hémodialyse ont chacun reçu une dose unique de 100 mg de lamotrigine. Les clairances moyennes ont été de 0,42 mL/min/kg (insuffisance rénale chronique), 0,33 mL/min/kg (entre les hémodialyses) et 1,57 mL/min/kg (pendant l'hémodialyse), comparées à 0,58 mL/min/kg chez les volontaires sains. Les demi-vies plasmatiques moyennes ont été de 42,9 heures (insuffisance rénale chronique), 57,4 heures (entre les hémodialyses) et 13,0 heures (pendant l'hémodialyse), comparées à 26,2 heures chez les volontaires sains.
En moyenne, environ 20 % (valeurs limites = 5,6 à 35,1) de la quantité totale de lamotrigine présente dans l'organisme a été éliminé pendant une session d'hémodialyse de 4 heures. Pour cette population de patients les doses initiales de lamotrigine doivent se baser sur les prises concomitantes de médicaments du patient ; des doses d'entretien réduites peuvent être efficaces pour les patients ayant une insuffisance rénale fonctionnelle significative (voir rubriques 4.2 et 4.4).
Insuffisants hépatiques
Une étude de pharmacocinétique en dose-unique a été réalisée chez 24 sujets ayant une insuffisance hépatique d'intensité variable et chez 12 volontaires sains faisant office de contrôle. La clairance apparente médiane de la lamotrigine a été de 0,31, 0,24 et 0,1 mL/min/kg chez des patients ayant respectivement une insuffisance hépatique de grade A, B ou C (Child-Pugh Classification) et de 0,34 mL/min/kg chez les volontaires sains de contrôle. Chez les patients ayant une insuffisance hépatique modérée ou sévère, la posologie initiale, l'escalade de doses et la posologie d'entretien devraient généralement être réduites (voir rubrique 4.2).
5.3. Données de sécurité préclinique
Dans les études sur la toxicité de reproduction et développementale chez les rongeurs et les lapins, aucun effet tératogène mais une réduction du poids fœtal et un retard de l'ossification du squelette ont été observés, à des niveaux d'exposition inférieurs ou similaires à l'exposition clinique attendue. Etant donné que des niveaux d'exposition supérieurs ne peuvent être testés chez l'animal en raison de la sévérité de la toxicité maternelle, le potentiel tératogénique de la lamotrigine n'a pas été caractérisé au-delà de l'exposition clinique.
Chez les rats, une augmentation de la mortalité fœtale et post-natale a été observée lorsque la lamotrigine a été administrée durant la phase tardive de la gestation et pendant la période post-natale précoce. Ces effets ont été observés à des niveaux inférieurs à l'exposition clinique attendue.
Chez des rats juvéniles, un effet sur l'apprentissage dans le test du labyrinthe de Biel, un léger retard dans la séparation balano-préputiale et la perméabilité vaginale ainsi qu'une diminution de la prise de poids corporel post-natale chez les animaux F1 ont été observés à des expositions inférieurs aux expositions thérapeutiques chez les adultes humains, basées sur la surface corporelle.
Les expériences animales n'ont pas révélé de baisse de la fertilité par la lamotrigine. La lamotrigine a réduit les taux d'acide folique fœtal chez les rats. Un déficit en acide folique est connu pour être associé à un risque accru de malformations congénitales chez l'animal comme chez les humains.
La lamotrigine a provoqué une inhibition dose-dépendante du courant à l'extrémité des canaux hERG dans les cellules rénales embryonnaires humaines. La CI50 a été environ 9 fois supérieure à la concentration maximale sans effet thérapeutique. La lamotrigine n'a pas provoqué de prolongation de l'intervalle QT chez l'animal à des expositions allant jusqu'à 9 fois la concentration maximale sans effet thérapeutique. Dans un essai clinique, il n'y a eu aucun effet cliniquement significatif de la lamotrigine sur l'intervalle QT chez des adultes volontaires sains (voir rubrique 5.1).
2 ans.
6.4. Précautions particulières de conservation
Pas de précautions particulières de conservation.
6.5. Nature et contenu de l'emballage extérieur
Plaquettes (PVC/PVdC/Aluminium) ou plaquettes avec sécurité enfant (PVC/PVdC/Aluminium/papier).
Boîte de 10, 14, 28, 30, 42, 50, 56, 60, 90, 98, 100, 196 ou 200 comprimés dispersibles ou à croquer.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Pas d’exigences particulières pour l’élimination.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
23 RUE FRANÇOIS JACOB
92500 RUEIL-MALMAISON
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 394 743 8 0 : 14 comprimés sous plaquette (PVC/PVdC/Aluminium)
· 34009 392 661 4 5 : 28 comprimés sous plaquette (PVC/PVdC/Aluminium)
· 34009 338 986 6 3 : 30 comprimés sous plaquette (PVC/PVdC/Aluminium)
· 34009 394 744 4 1 : 42 comprimés sous plaquette (PVC/PVdC/Aluminium)
· 34009 394 745 0 2 : 98 comprimés sous plaquette (PVC/PVdC/Aluminium)
· 34009 394 746 7 0 : 196 comprimés sous plaquette (PVC/PVdC/Aluminium)
· 34009 302 250 1 1 : 14 comprimés sous plaquettes avec sécurité enfant (PVC/PVdC/Aluminium/papier).
· 34009 302 250 2 8 : 28 comprimés sous plaquettes avec sécurité enfant (PVC/PVdC/Aluminium/papier).
· 34009 302 250 3 5 : 30 comprimés sous plaquettes avec sécurité enfant (PVC/PVdC/Aluminium/papier).
· 34009 302 250 4 2 : 42 comprimés sous plaquettes avec sécurité enfant (PVC/PVdC/Aluminium/papier).
· 34009 302 250 5 9 : 98 comprimés sous plaquettes avec sécurité enfant (PVC/PVdC/Aluminium/papier).
· 34009 302 250 6 6 : 196 comprimés sous plaquettes avec sécurité enfant (PVC/PVdC/Aluminium/papier).
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[À compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[À compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I
Informations importantes
Les informations importantes disponibles pour ce médicament sont les suivantes :
- Antiépileptiques pendant la grossesse entre 2013 et 2021 : une étude du GIS EPI-PHARE met en évidence une baisse importante de l'exposition au valproate et dérivés, mais moindre pour le topiramate et la carbamazépine
- Antiépileptiques et grossesse : mieux connaître les risques pour l'enfant à naître
- Lamotrigine (Lamictal et génériques) : rappel du bon usage afin de limiter le risque d'éruption cutanée grave en particulier au début du traitement
- Lamotrigine : attention au risque d'éruption cutanée grave en particulier au début du traitement
ANSM - Mis à jour le : 24/06/2025
LAMICTAL 100 mg, comprimé dispersible ou à croquer
lamotrigine
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que LAMICTAL 100 mg, comprimé dispersible ou à croquer et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant de prendre LAMICTAL100 mg, comprimé dispersible ou à croquer ?
3. Comment prendre LAMICTAL 100 mg, comprimé dispersible ou à croquer ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver LAMICTAL 100 mg, comprimé dispersible ou à croquer ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE LAMICTAL 100 mg, comprimé dispersible ou à croquer ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique - code ATC : N03AX09
LAMICTAL traite l'épilepsie en bloquant les signaux du cerveau qui déclenchent les crises d'épilepsie (convulsions).
· Chez les adultes et les enfants âgés de 13 ans et plus, LAMICTAL peut être utilisé seul ou avec d'autres médicaments, pour traiter l'épilepsie. LAMICTAL peut également être utilisé avec d'autres médicaments pour traiter les crises survenant dans une maladie appelée syndrome de Lennox-Gastaut.
· Chez les enfants âgés de 2 à 12 ans, LAMICTAL peut être utilisé avec d'autres médicaments, pour traiter ces maladies. Il peut être utilisé seul pour traiter un type d'épilepsie appelé crises d'absences typiques.
LAMICTAL traite également les troubles bipolaires.
Les personnes ayant des troubles bipolaires (parfois appelés maniaco-dépression) ont des variations d'humeur extrêmes, avec des périodes maniaques (excitation ou euphorie) alternant avec des périodes de dépression (profonde tristesse ou désespoir). Chez les adultes âgés de 18 ans et plus, LAMICTAL peut être utilisé seul ou avec d'autres médicaments, pour prévenir les périodes de dépression qui surviennent dans les troubles bipolaires. On ne sait pas encore comment LAMICTAL agit dans le cerveau pour avoir cet effet.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT DE PRENDRE LAMICTAL 100 mg, comprimé dispersible ou à croquer ?
Ne prenez jamais LAMICTAL 100 mg, comprimé dispersible ou à croquer :
· si vous êtes allergique (hypersensible) à la lamotrigine ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
Si vous êtes concerné :
è Parlez-en à votre médecin et ne prenez pas LAMICTAL.
Avertissements et précautions
Adressez-vous à votre médecin ou à votre pharmacien avant de prendre LAMICTAL :
· si vous avez des problèmes de reins
· si vous avez déjà développé une éruption cutanée après avoir pris de la lamotrigine ou tout autre médicament pour les troubles bipolaires ou l'épilepsie
· si vous avez présenté une éruption cutanée ou un coup de soleil après avoir pris de la lamotrigine et après vous être exposé au soleil ou à une lumière artificielle (par exemple, un solarium). Votre médecin vérifiera votre traitement et pourra vous conseiller d’éviter toute exposition au soleil ou de vous protéger contre le soleil (par exemple, utilisation d’un écran solaire et/ou port de vêtements de protection)
· si vous avez déjà développé une méningite après avoir pris de la lamotrigine (lisez le descriptif des symptômes dans la rubrique 4 de cette notice : effets indésirables rares)
· si vous prenez déjà un médicament contenant de la lamotrigine
· si vous souffrez du syndrome de Brugada, ou d’autres problèmes cardiaques. Le syndrome de Brugada est une maladie génétique entrainant une activité électrique anormale du cœur. Ces anomalies de l’électrocardiogramme (ECG), pouvant entrainer des arythmies (rythme cardiaque anormal), peuvent être déclenchées par la lamotrigine. Parlez-en à votre médecin si vous pensez avoir cette maladie.
Si vous êtes concerné :
è Parlez-en à votre médecin, il pourrait décider de diminuer la dose ou que LAMICTAL ne vous convienne pas.
Informations importantes concernant des réactions pouvant potentiellement mettre en jeu le pronostic vital
Un petit nombre de personnes prenant LAMICTAL présente une réaction allergique ou une réaction cutanée pouvant potentiellement mettre en jeu le pronostic vital, qui peut se transformer en problèmes plus graves si elle n'est pas traitée. Cela peut inclure le syndrome de Stevens-Johnson (SSJ), le syndrome de Lyell (nécrolyse épidermique toxique (NET)) et le syndrome d’hypersensibilité médicamenteuse avec éosinophilie et symptômes systémiques (DRESS). Vous devez connaître les symptômes à surveiller pendant la prise de LAMICTAL. Ce risque peut être associé à une variante génétique chez les personnes d'origine asiatique (principalement les Chinois Han et les Thaïlandais). Si vous êtes de cette origine et que vous avez déjà été testé comme porteur de cette variante génétique (HLA-B* 1502), discutez-en avec votre médecin avant de prendre LAMICTAL.
è Lisez la description de ces symptômes figurant dans la rubrique 4 de la notice sous le titre « Réactions pouvant potentiellement mettre en jeu le pronostic vital : demandez immédiatement l'aide d'un médecin.»
Lymphohistiocytose hémophagocytaire (LHH)
De rares cas de réactions du système immunitaire très graves ont été rapportés chez des patients traités par lamotrigine.
è Contactez immédiatement votre médecin ou pharmacien si vous ressentez l’un des symptômes suivant lors de la prise de lamotrigine : fièvre, éruption cutanée, symptômes neurologiques (ex. secousses ou tremblement, état confusionnel, troubles de la fonction cérébrale).
Pensées autodestructrices ou suicidaires
Les médicaments anti-épileptiques sont utilisés pour traiter plusieurs maladies, dont l'épilepsie et les troubles bipolaires. Les personnes ayant des troubles bipolaires peuvent parfois avoir des pensées autodestructrices ou suicidaires. Si vous avez des troubles bipolaires, ces pensées ont plus de chances de survenir :
· lorsque vous démarrez ce traitement pour la première fois
· si vous avez déjà eu des pensées autodestructrices ou suicidaires
· si vous avez moins de 25 ans.
Si vous avez des pensées ou des sentiments angoissants ou si vous remarquez que vous vous sentez plus mal ou que vous développez de nouveaux symptômes alors que vous prenez LAMICTAL :
è Consultez un médecin dès que possible ou rendez-vous à l'hôpital le plus proche pour obtenir de l'aide.
Vous pouvez trouver utile d’expliquer à un membre de la famille, à un soignant ou à un ami proche que vous pouvez devenir déprimé ou avoir des changements importants d'humeur et leur demander de lire cette notice. Vous pouvez leur demander de vous dire s’ils sont inquiets au sujet de votre dépression ou de vos changements de comportement.
Des pensées autodestructrices ou suicidaires ont également été observées chez un petit nombre de personnes traitées par des anti-épileptiques tels que LAMICTAL. Si vous avez ce type de pensées, contactez immédiatement votre médecin.
Si vous prenez LAMICTAL pour une épilepsie
Les crises dans certains types d'épilepsie peuvent de temps en temps s'aggraver ou se produire plus souvent alors que vous prenez LAMICTAL. Certains patients peuvent avoir des crises graves, qui peuvent provoquer des graves problèmes de santé. Si vos crises deviennent plus fréquentes ou si vous avez une crise grave alors que vous prenez LAMICTAL :
è Consultez un médecin dès que possible.
LAMICTAL ne doit jamais être donné à des personnes de moins de 18 ans pour traiter des troubles bipolaires. Les médicaments pour traiter la dépression ou d'autres problèmes mentaux de santé augmentent le risque de pensées et de comportements suicidaires chez les enfants et les adolescents de moins de 18 ans.
Enfants
Sans objet.
Autres médicaments et LAMICTAL 100 mg, comprimé dispersible ou à croquer
Informez votre médecin ou votre pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament, y compris un médicament à base de plantes ou obtenu sans ordonnance.
Votre médecin doit savoir si vous prenez d'autres médicaments pour traiter votre épilepsie ou vos problèmes de santé mentale. Ceci afin de s'assurer que vous prenez la dose correcte de LAMICTAL.
Ces médicaments incluent :
· l'oxcarbazépine, le felbamate, la gabapentine, le lévétiracétam, la prégabaline, le topiramate ou le zonisamide, utilisé pour traiter l'épilepsie
· le lithium, l'olanzapine ou l’aripiprazole, utilisé pour traiter des troubles psychiatriques
· le bupropion, utilisé pour traiter des troubles psychiatriques ou pour arrêter de fumer
· le paracétamol, utilisé pour traiter la douleur et la fièvre.
è Prévenez votre médecin si vous prenez l'un d'eux.
Certains médicaments peuvent interagir avec LAMICTAL ou peuvent augmenter la probabilité que certaines personnes en aient les effets indésirables. Ils incluent :
· le valproate, utilisé pour traiter l'épilepsie et des troubles psychiatriques
· la carbamazépine, utilisée pour traiter l'épilepsie et des troubles psychiatriques
· la phénytoïne, la primidone ou le phénobarbital, utilisé pour traiter l'épilepsie
· la rispéridone, utilisée pour traiter des troubles psychiatriques
· la rifampicine, qui est un antibiotique
· des médicaments utilisés pour traiter l'infection par le Virus de l'Immunodéficience Humaine (VIH) (une association de lopinavir et de ritonavir ou d’atazanavir et de ritonavir)
· les médicaments contenant des œstrogènes, y compris les contraceptifs hormonaux, comme la pilule (voir ci-dessous) et les thérapies hormonales substitutives (THS).
è Prévenez votre médecin si vous prenez, commencez à prendre ou arrêtez de prendre l'un d'entre eux.
Les contraceptifs hormonaux (comme la pilule) peuvent perturber l'action de LAMICTAL.
Votre médecin peut vous recommander d'utiliser un type particulier de contraceptif hormonal, ou une autre méthode de contraception, comme le préservatif, un diaphragme ou un stérilet. Si vous utilisez un contraceptif hormonal comme la pilule, votre médecin peut prélever des échantillons de votre sang pour contrôler le taux de LAMICTAL. Si vous prenez un contraceptif hormonal ou si vous envisagez de commencer à en prendre :
è Parlez-en à votre médecin, qui discutera avec vous des méthodes de contraception pouvant vous convenir.
LAMICTAL peut également perturber le mode d'action des contraceptifs hormonaux, bien qu'il soit peu probable qu'il en diminue leur efficacité. Si vous utilisez un contraceptif hormonal et si vous remarquez tout changement dans votre cycle menstruel, comme un saignement ou de légères pertes vaginales sanglantes entre les règles :
è Parlez-en à votre médecin. Ceux-ci peuvent être le signe que LAMICTAL perturbe le mode d'action de votre contraceptif.
Les THS peuvent perturber l’action de LAMICTAL
Si vous utilisez un traitement hormonal substitutif (THS) contenant des œstrogènes, votre médecin pourrait prélever des échantillons de votre sang pour contrôler le taux de LAMICTAL.
LAMICTAL 100 mg, comprimé dispersible ou à croquer avec des aliments et boissons
Sans objet.
è Si vous êtes enceinte, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou votre pharmacien avant de prendre ce médicament.
· Vous ne devez pas arrêter le traitement sans en avoir parlé à votre médecin. Cela est particulièrement important si vous avez une épilepsie.
· La grossesse peut modifier l'efficacité de LAMICTAL, de sorte que vous pourrez avoir besoin d'effectuer des prises de sang et votre dose de LAMICTAL pourrait être ajustée.
· Il existe un faible risque d’augmentation de malformations congénitales incluant des fentes labiales ou des fentes palatines, si LAMICTAL est pris au cours des 3 premiers mois de grossesse.
· Votre médecin peut vous conseiller de prendre un supplément en acide folique si vous envisagez une grossesse et pendant votre grossesse.
è Si vous allaitez ou envisagez d'allaiter, demandez conseil à votre médecin ou votre pharmacien avant de prendre ce médicament. La substance active de LAMICTAL passe dans le lait maternel et peut affecter votre bébé. Votre médecin discutera des risques et des bénéfices de l'allaitement si vous êtes traitées par LAMICTAL. Si vous décidez d’allaiter, il examinera régulièrement votre bébé en cas de somnolence, d’éruption cutanée ou d’une prise de poids insuffisante. Informez votre médecin si vous observez un de ces symptômes chez votre bébé.
Conduite de véhicules et utilisation de machines
LAMICTAL peut provoquer des sensations vertigineuses et une vision double.
è Ne conduisez pas et n'utilisez pas de machines à moins que vous ne soyez certain de ne pas être affecté.
Si vous avez une épilepsie, parlez à votre médecin de la conduite et de l'utilisation de machines.
Informations importantes concernant certains composants de LAMICTAL
LAMICTAL 100 mg, comprimé dispersible ou à croquer contient moins de 1 mmol (23 mg) de sodium par comprimé, c’est-à-dire qu’il est essentiellement « sans sodium ».
3. COMMENT PRENDRE LAMICTAL 100 mg, comprimé dispersible ou à croquer ?
Veillez à toujours prendre ce médicament en suivant exactement les indications de votre médecin ou de votre pharmacien. Vérifiez auprès de votre médecin ou pharmacien en cas de doute.
Quelle quantité de LAMICTAL prendre
Cela peut prendre un moment avant de trouver la meilleure dose de LAMICTAL pour vous. La dose que vous prendrez dépendra de :
· votre âge
· si vous prenez LAMICTAL avec d'autres médicaments
· si vous avez des problèmes de rein ou du foie.
Votre médecin vous prescrira pour commencer une dose faible et augmentera progressivement la dose sur quelques semaines jusqu'à ce que vous atteigniez la dose qui marche sur vous (appelée dose efficace). Ne prenez jamais plus de LAMICTAL que ce que votre médecin vous a indiqué.
La dose habituelle efficace de LAMICTAL pour les adultes et les enfants de 13 ans et plus est entre 100 mg et 400 mg par jour.
Pour les enfants entre 2 et 12 ans, la dose efficace dépend de leur poids corporel - habituellement, cela se situe entre 1 mg et 15 mg par kilogramme de poids corporel de l'enfant, jusqu'à une dose d’entretien maximale de 200 mg par jour.
LAMICTAL n'est pas recommandé chez les enfants âgés de moins de 2 ans.
Comment prendre votre dose de LAMICTAL
Prenez votre dose de LAMICTAL une ou deux fois par jour, selon les conseils de votre médecin. Il peut être pris avec ou sans nourriture.
· Prenez toujours la dose complète que votre médecin vous a prescrite. Ne prenez jamais une partie seulement d'un comprimé.
Votre médecin peut également vous conseiller de commencer ou d'arrêter d'autres médicaments, selon la maladie pour laquelle vous êtes traité et selon la façon dont vous répondez au traitement.
LAMICTAL comprimé dispersible ou à croquer peut être soit avalé en entier avec un peu d'eau, soit croqué, soit mélangé avec de l'eau pour obtenir un médicament liquide. Ne prenez jamais seulement une partie du liquide.
Ces comprimés sont présentés dans un emballage particulier pour éviter que les enfants ne retirent les comprimés hors de la plaquette.
Chaque alvéole comporte un numéro. Prenez chaque comprimé dans l’ordre en commençant par le comprimé numéro 1.
1. Séparez un comprimé : séparez une des alvéoles de la plaquette en la détachant selon les perforations.
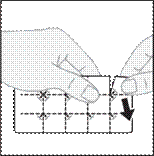
2. Décollez la pellicule extérieure : soulevez un coin à l’endroit indiqué par la flèche et retirez la pellicule extérieure de l’alvéole.
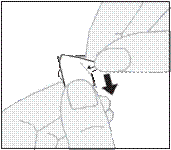
3. Sortez le comprimé : poussez doucement le comprimé à travers la couche d'aluminium.
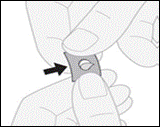
Pour croquer le comprimé :
Vous pouvez avoir besoin de boire un peu d'eau en même temps pour aider le comprimé à se dissoudre dans la bouche. Puis buvez encore un peu d'eau pour vous assurer que tout le médicament a été avalé.
Pour préparer un médicament liquide :
· Mettez le comprimé dans un verre avec au moins suffisamment d'eau pour recouvrir le comprimé entier.
· Au choix mélangez pour dissoudre ou attendez jusqu'à ce que le comprimé soit totalement dissout.
· Buvez tout le liquide.
· Ajoutez un peu plus d'eau dans le verre et buvez-la, pour vous assurer qu'il ne reste pas du médicament dans le verre.
Si vous avez pris plus de LAMICTAL100 mg, comprimé dispersible ou à croquer que vous n’auriez dû
è Contactez un médecin ou le service des urgences de l’hôpital le plus proche immédiatement. Si possible, montrez-leur la boîte de LAMICTAL.
Si vous avez pris trop de LAMICTAL vous avez plus de risques d’avoir des effets indésirables graves qui peuvent être mortels.
Quelqu'un qui a pris trop de LAMICTAL peut avoir l'un de ces symptômes :
· mouvements rapides et incontrôlables des yeux (nystagmus)
· maladresse et manque de coordination, perturbant l'équilibre (ataxie)
· modifications du rythme cardiaque (habituellement détectés à l’ECG)
· perte de connaissance, crises convulsives ou coma.
Si vous oubliez de prendre une seule dose de LAMICTAL 100 mg, comprimé dispersible ou à croquer
Ne prenez pas de comprimés supplémentaires pour compenser les comprimés que vous avez oublié de prendre. Prenez seulement votre prochaine dose à l’heure habituelle.
Dans le cas où vous oubliez de prendre plusieurs doses de LAMICTAL
è Demandez conseil à votre médecin sur comment recommencer à le prendre. Il est important pour vous de le faire.
Si vous arrêtez de prendre LAMICTAL 100 mg, comprimé dispersible ou à croquer
N'arrêtez pas LAMICTAL sans un avis :
Vous devez prendre LAMICTAL aussi longtemps que votre médecin le recommande. N'arrêtez pas tant que votre médecin ne vous le conseille pas.
Si vous prenez LAMICTAL pour une épilepsie
Pour arrêter de prendre LAMICTAL, il est important que la dose soit réduite progressivement, sur environ 2 semaines. Si vous arrêtez subitement de prendre LAMICTAL, votre épilepsie peut revenir ou s'aggraver.
Si vous prenez LAMICTAL pour des troubles bipolaires
LAMICTAL peut mettre du temps à agir, aussi il est peu probable que vous vous sentiez mieux tout de suite. Si vous arrêtez de prendre LAMICTAL, votre dose n'aura pas besoin d'être réduite progressivement. Mais si vous voulez arrêter de prendre LAMICTAL, vous devez toujours en parler en premier à votre médecin.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Réactions pouvant potentiellement mettre en jeu le pronostic vital : demandez immédiatement l'aide d'un médecin.
Un petit nombre de personnes prenant LAMICTAL présente une réaction allergique ou une réaction cutanée pouvant potentiellement mettre en jeu le pronostic vital, qui peut se transformer en problèmes plus graves si elle n'est pas traitée.
Ces symptômes ont plus de probabilité de survenir pendant les premiers mois de traitement par LAMICTAL, particulièrement si vous commencez par une dose trop élevée ou si votre dose est augmentée trop vite ou si vous prenez LAMICTAL avec un autre médicament appelé valproate. Les enfants ont plus de probabilité d'être touchés que les adultes, les parents doivent donc être particulièrement vigilants.
Les symptômes de ces réactions incluent :
· une éruption cutanée ou rougeur, qui peut se transformer en réaction cutanée grave ou pouvant parfois mettre en jeu le pronostic vital comme une éruption cutanée avec des lésions en forme de cibles (érythème polymorphe), une éruption cutanée étendue accompagnée de cloques et d'une desquamation, particulièrement autour de la bouche, du nez, des yeux et des parties génitales (syndrome de Stevens-Johnson), une desquamation étendue (plus de 30 % de la surface corporelle - nécrolyse épidermique toxique) ou une éruption cutanée étendue avec atteinte du foie, du sang ou d’autres organes (syndrome d’hypersensibilité médicamenteuse avec éosinophilie et symptômes systémiques aussi appelé syndrome d’hypersensibilité (DRESS))
· des ulcères de la bouche, de la gorge, du nez ou des organes génitaux
· une irritation de la bouche ou des yeux rouges ou enflés (conjonctivites)
· une température élevée (fièvre), des symptômes pseudo-grippaux ou une somnolence
· un gonflement autour du visage ou des ganglions gonflés au niveau du cou, de l'aisselle ou de l'aine
· des bleus ou des saignements inattendus ou les doigts qui deviennent bleus
· une gorge douloureuse ou plus d'infections que d'habitude (comme des rhumes)
· des augmentations des enzymes du foie observées dans les tests sanguins
· une augmentation d’un type de globules blancs (les éosinophiles)
· un gonflement des ganglions lymphatiques
· une atteinte d’autres organes comme le foie ou les reins.
Dans beaucoup de cas, ces symptômes seront les signes d'effets indésirables moins graves. Mais vous devez être conscient qu'ils peuvent potentiellement mettre en jeu le pronostic vital et peuvent se transformer en problèmes plus graves, comme la défaillance d'organes, s'ils ne sont pas traités. Si vous remarquez l'un de ces symptômes :
è Consultez immédiatement un médecin. Votre médecin peut décider d'effectuer des tests sur votre foie, vos reins ou votre sang et peut vous dire d'arrêter de prendre LAMICTAL. Dans le cas où vous avez développé le syndrome de Stevens-Johnson ou de nécrolyse épidermique toxique, votre médecin vous préviendra que vous ne devrez jamais plus utiliser la lamotrigine.
Lymphohistiocytose hémophagocytaire (LHH) (voir rubrique 2 : Quelles sont les informations à connaître avant de prendre Lamictal).
Effets indésirables très fréquents
Ils affectent plus d'1 personne sur 10 :
· maux de tête
· éruption cutanée.
Effets indésirables fréquents
Ils affectent jusqu'à 1 personne sur 10 :
· agressivité ou irritabilité
· envie de dormir
· sensation de vertiges
· frissons ou tremblements
· difficultés à dormir (insomnie)
· sensation d’agitation
· diarrhée
· bouche sèche
· nausées ou vomissements
· sensation de fatigue
· douleur du dos ou des articulations ou ailleurs.
Effets indésirables peu fréquents
Ils affectent jusqu'à 1 personne sur 100 :
· maladresse et manque de coordination (ataxie)
· vision double ou vision floue
· perte inhabituelle ou raréfaction des cheveux (alopécie)
· éruption cutanée ou coup de soleil après une exposition au soleil ou à la lumière artificielle (photosensibilité).
Effets indésirables rares
Ils affectent jusqu'à 1 personne sur 1 000 :
· éruption cutanée causant des rougeurs ou des cloques sur la peau, qui peuvent ressembler à des cibles avec un centre rouge sombre entouré d’un anneau rouge plus pâle (érythème polymorphe)
· une réaction cutanée mettant en jeu le pronostic vital (syndrome de Stevens-Johnson) : (voir également les informations au début de rubrique 4)
· un ensemble de symptômes survenant en même temps incluant :
fièvre, nausées, vomissements, maux de tête, raideur de la nuque et sensibilité extrême à la lumière. Cela peut être provoqué par une inflammation des membranes enveloppant le cerveau et la moelle épinière (méningite). Ces symptômes disparaissent habituellement à l’arrêt du traitement cependant s’ils continuent ou s’aggravent, contactez votre médecin
· mouvements rapides et incontrôlables des yeux (nystagmus)
· démangeaison des yeux, accompagnée d'écoulement et de croûtes sur les paupières (conjonctivite).
Effets indésirables très rares
Ils affectent jusqu'à 1 personne sur 10 000 :
· une réaction cutanée mettant en jeu le pronostic vital (nécrolyse épidermique toxique) : (voir également les informations en début de rubrique 4)
· syndrome d’hypersensibilité médicamenteuse avec éosinophilie et symptômes systémiques (DRESS) : (voir également les informations en début de rubrique 4)
· une température élevée (fièvre) : (voir également les informations en début de rubrique 4)
· gonflement autour du visage (œdème) ou des ganglions gonflés au niveau du cou, de l'aisselle ou de l'aine (adénopathie) : (voir aussi les informations en début de rubrique 4)
· modifications de la fonction du foie, qui peuvent se voir dans les analyses de sang ou insuffisance hépatique : (voir aussi les informations en début de rubrique 4)
· un trouble grave de la coagulation, qui peut provoquer de façon inattendue des saignements ou des bleus (coagulation intravasculaire disséminée) : (voir également les informations en début de rubrique 4)
· lymphohistiocytose hémophagocytaire (LHH) (voir rubrique 2 : Quelles sont les informations à connaître avant de prendre Lamictal)
· modifications qui peuvent se voir dans les analyses de sang, incluant une diminution du nombre de globules rouges (anémie), une diminution du nombre de globules blancs (leucopénie, neutropénie, agranulocytose), une diminution du nombre de plaquettes (thrombocytopénie), une diminution du nombre de tous ces types de cellules (pancytopénie) et affections de la moelle osseuse appelées anémie aplasique
· hallucinations (« voir » ou « entendre » des choses qui ne sont pas réellement là)
· confusion
· sensation d'instabilité ou de tremblements quand vous bougez
· mouvements corporels et/ou une répétition incontrôlable des sons ou des mots (tics), spasmes musculaires incontrôlables affectant les yeux, la tête et le torse (choréoathétose) ou tout mouvement corporel inhabituel comme des mouvements saccadés, des tremblements ou une raideur
· chez les personnes ayant déjà une épilepsie, les crises peuvent survenir plus souvent
· chez les personnes ayant une maladie de Parkinson, une aggravation des symptômes
· réaction de type lupus (symptômes incluant : douleur du dos ou des articulations qui peut parfois être accompagnée de fièvre et/ou d’une sensation de malaise général).
Autres effets indésirables
D'autres effets indésirables peuvent survenir chez un petit nombre de personnes mais leur fréquence exacte est inconnue :
· des troubles osseux, incluant l'ostéopénie, l'ostéoporose (amincissement des os) et des fractures ont été rapportés. Faites le point avec votre médecin ou votre pharmacien si vous êtes en cours de traitement antiépileptique à long terme ou si vous avez des antécédents d'ostéoporose ou en cas de prise de stéroïdes
· inflammation du rein (néphrite tubulo-interstitielle), ou inflammation à la fois du rein et de l’œil (néphrite tubulo-interstitielle et uvéite)
· cauchemars
· nodules ou plaques rouges sur la peau (pseudolymphome).
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou à votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER LAMICTAL 100 mg, comprimé dispersible ou à croquer ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur la plaquette, la boîte ou le flacon après {EXP}. La date de péremption fait référence au dernier jour de ce mois.
LAMICTAL ne requiert aucune condition particulière de conservation.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient LAMICTAL 100 mg, comprimé dispersible ou à croquer
· La substance active est :
Lamotrigine .................................................................................................................... 100,00 mg
Pour un comprimé dispersible ou à croquer.
· Les autres composants sont :
Carbonate de calcium, hydroxypropylcellulose faiblement substituée, silicate d'aluminium et de magnésium, carboxyméthylamidon sodique (type A), povidone K30, saccharine sodique, stéarate de magnésium, arôme cassis.
Qu’est-ce que LAMICTAL 100 mg, comprimé dispersible ou à croquer et contenu de l’emballage extérieur
Les comprimés dispersibles ou à croquer de LAMICTAL 100 mg sont carrés avec les angles arrondis. Ils sont marqués « GSCL7 » sur une face et « 100 » sur l'autre face.
Chaque boîte contient des plaquettes de 10, 14, 28, 30, 42, 50, 56, 60, 90, 98, 100, 196 ou 200 comprimés.
Titulaire de l’autorisation de mise sur le marché
23 RUE FRANÇOIS JACOB
92500 RUEIL-MALMAISON
Exploitant de l’autorisation de mise sur le marché
23 RUE FRANÇOIS JACOB
92500 RUEIL-MALMAISON
DELPHARM POZNAN SPOLKA AKCYJNA
UL. GRUNWALDZKA 189
60-322 POZNAN
POLOGNE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est
[À compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).