Dernière mise à jour le 30/03/2026
BECLOMETASONE/FORMOTEROL ZENTIVA 200/6 microgrammes/dose, solution pour inhalation en flacon pressurisé
Indications thérapeutiques
BECLOMETASONE/FORMOTEROL ZENTIVA est une solution pour inhalation en flacon pressurisé contenant deux substances actives qui sont inhalées par la bouche et administrées directement dans les poumons.
Les deux substances actives sont :
· Le dipropionate de béclométasone appartient à un groupe de médicaments appelés corticoïdes qui exercent un effet anti-inflammatoire et réduisent le gonflement et l'irritation dans vos poumons.
· Le fumarate de formotérol dihydraté appartient à un groupe de médicaments appelés « bronchodilatateurs de longue durée d'action » qui provoquent un relâchement des muscles des voies respiratoires et vous aident à respirer plus facilement.
L'association de ces deux substances actives facilite la respiration en soulageant les symptômes tels que l'essoufflement, les sifflements respiratoires et la toux chez les patients asthmatiques.
BECLOMETASONE/FORMOTEROL ZENTIVA est utilisé pour traiter l'asthme chez les adultes.
Si votre médecin vous a prescrit BECLOMETASONE/FORMOTEROL ZENTIVA, vous êtes probablement dans l’une des deux situations suivantes :
· votre asthme n'est pas correctement contrôlé par des corticoïdes inhalés et des bronchodilatateurs de courte durée d'action utilisés « à la demande » ou
· votre asthme répond bien aux corticoïdes et bronchodilatateurs de longue durée d'action.
Présentations
> 1 flacon pressurisé aluminium de 120 doses avec valve doseuse dans inhalateur en plastique polypropylène avec compteur de doses avec embout buccal
Code CIP : 34009 303 185 0 8
Déclaration de commercialisation : 23/01/2026
Cette présentation n'est pas agréée aux collectivités
- Prix hors honoraire de dispensation : 19,90 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 20,92 €
- Taux de remboursement :65 %
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 16/07/2025 | Inscription (CT) | Le service médical rendu par BECLOMETASONE/FORMOTEROL ZENTIVA 100/6 µg/dose et 200/6 µg/dose (béclométasone/formotérol), solution pour inhalation en flacon pressurisé, est important dans l’indication de l’AMM concernant l’asthme. |
| Modéré | Avis du 16/07/2025 | Inscription (CT) | Le service médical rendu par BECLOMETASONE/FORMOTEROL ZENTIVA 100/6 µg/dose (béclométasone/formotérol), solution pour inhalation en flacon pressurisé, est modéré dans l’indication de l’AMM concernant la BPCO. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 16/07/2025 | Inscription (CT) | Ces spécialités sont des hybrides qui n’apportent pas d’amélioration du service médical rendu (ASMR V) par rapport aux spécialités de référence INNOVAIR 100/6 µg/dose et 200/6 µg/dose (béclométasone/formotérol), solution en flacon pressurisé. |
ANSM - Mis à jour le : 06/10/2025
BECLOMETASONE/FORMOTEROL ZENTIVA 200/6 microgrammes/dose, solution pour inhalation en flacon pressurisé
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Dipropionate de béclométasone.......................................................................... 200 microgrammes
Fumarate de formotérol dihydraté............................................................................ 6 microgrammes
Pour une dose mesurée (en sortie du flacon pressurisé).
Cela équivaut à une dose délivrée (au travers de l'embout buccal) de 169,2 microgrammes de dipropionate de béclométasone et de 5,0 microgrammes de fumarate de formotérol dihydraté.
Excipient à effet notoire :
Ce médicament contient 9 mg d'alcool (éthanol anhydre) par bouffée (en sortie du flacon pressurisé).
Pour la liste complète des excipients, voir rubrique 6.1.
Solution pour inhalation en flacon pressurisé.
Solution incolore à jaunâtre.
4.1. Indications thérapeutiques
BECLOMETASONE/FORMOTEROL ZENTIVA est indiqué en traitement continu de l'asthme dans les situations où l'administration par voie inhalée d'un médicament associant un corticoïde et un bronchodilatateur bêta-2 agoniste de longue durée d'action est justifiée :
· chez les patients insuffisamment contrôlés par une corticothérapie inhalée et la prise d'un bronchodilatateur bêta-2 agoniste de courte durée d'action par voie inhalée « à la demande » ou
· chez les patients contrôlés par l'administration d'une corticothérapie inhalée associée à un traitement continu par bêta-2 agoniste de longue durée d'action par voie inhalée.
BECLOMETASONE/FORMOTEROL ZENTIVA est indiqué chez les adultes.
4.2. Posologie et mode d'administration
BECLOMETASONE/FORMOTEROL ZENTIVA ne doit pas être utilisé pour l’instauration d'un traitement de l'asthme. La posologie des composants de BECLOMETASONE/FORMOTEROL ZENTIVA est individuelle et doit être adaptée en fonction de la sévérité de la maladie. Cela doit être pris en compte non seulement lors de l'instauration d'un traitement avec des produits combinés, mais également lors de l’adaptation de la posologie. Si un patient doit recevoir une combinaison de doses autres que celles disponibles dans l'inhalateur combiné, des doses appropriées de bronchodilatateur bêta-2 agoniste et/ou de corticoïde doivent être prescrites individuellement.
Le dipropionate de béclométasone contenu dans BECLOMETASONE/FORMOTEROL ZENTIVA se caractérise par une distribution de particules de taille extrafine, ce qui entraîne une activité locale plus importante qu'avec une formulation de dipropionate de béclométasone non-extrafine (100 microgrammes de dipropionate de béclométasone en formulation extrafine sont équivalents à 250 microgrammes de dipropionate de béclométasone dans une formulation non-extrafine). Ainsi, la dose quotidienne totale de dipropionate de béclométasone administrée par BECLOMETASONE/ FORMOTEROL ZENTIVA devrait être inférieure à celle administrée avec une formulation non-extrafine.
Ceci doit être pris en considération en cas de passage d'une formulation de dipropionate de béclométasone non-extrafine à un traitement par BECLOMETASONE/FORMOTEROL ZENTIVA, et la dose de dipropionate de béclométasone devra être diminuée et adaptée aux besoins de chaque patient.
Posologies recommandées chez les adultes âgés de 18 ans et plus
Deux inhalations deux fois par jour.
La dose quotidienne maximale est de 4 inhalations.
BECLOMETASONE/FORMOTEROL ZENTIVA 200/6 microgrammes doit être utilisé uniquement en traitement continu de fond. Un dosage plus faible (dipropionate de béclométasone/formotérol 100/6 microgrammes) est disponible pour le traitement continu de fond de secours.
Il convient de conseiller aux patients d'avoir en permanence à disposition leur propre bronchodilatateur d’action rapide pour une utilisation de secours.
Les patients doivent être réévalués régulièrement par un médecin, afin que la posologie de BECLOMETASONE/FORMOTEROL ZENTIVA reste optimale et ne soit modifiée que sur avis médical. La dose doit être ajustée jusqu'à la dose la plus faible permettant de maintenir un contrôle efficace des symptômes. Lorsque le contrôle des symptômes à long terme est maintenu avec la posologie la plus faible recommandée, l'étape suivante pourrait inclure un test par corticoïde inhalé seul. BECLOMETASONE/FORMOTEROL ZENTIVA 200/6 microgrammes ne doit pas être utilisé pour la diminution progressive des doses par paliers, toutefois une concentration plus faible du composant dipropionate de béclométasone dans le même inhalateur est disponible pour la diminution progressive des doses par paliers (dipropionate de béclométasone/formotérol 100/6 microgrammes).
Les patients doivent être informés de la nécessité de prendre le traitement par BECLOMETASONE/FORMOTEROL ZENTIVA tous les jours, même lorsqu'ils sont asymptomatiques.
Population pédiatrique :
Posologie recommandée chez les enfants et adolescents âgés de moins de 18 ans
BECLOMETASONE/FORMOTEROL ZENTIVA 200/6 microgrammes ne doit pas être utilisé chez les enfants et adolescents âgés de moins de 18 ans.
Populations de patients particulières
Patients âgés :
Il n’est pas nécessaire d’adapter la dose chez les patients âgés.
Patients présentant une atteinte rénale et/ou hépatique :
Aucune donnée concernant l’utilisation du dipropionate de béclometasone/formotérol n’est disponible chez les patients présentant une insuffisance hépatique ou rénale (voir rubrique 5.2).
Mode d’administration
BECLOMETASONE/FORMOTEROL ZENTIVA est destiné à être inhalé.
Afin de garantir une administration correcte du médicament, un médecin ou un autre professionnel de santé doit montrer au patient comment utiliser correctement l'inhalateur. Une utilisation adaptée de l'aérosol-doseur pressurisé est essentielle à la réussite du traitement. Il convient de conseiller au patient de lire attentivement la notice d'information du patient et de suivre les instructions d'utilisation telles qu'elles figurent dans la notice.
Un compteur de doses au dos de l’inhalateur BECLOMETASONE/FORMOTEROL ZENTIVA indique le nombre de doses restantes. A chaque utilisation du dispositif, une bouffée est libérée et le compteur décompte une dose. Les patients doivent être informés qu’en cas de chute de l’inhalateur, un décompte accidentel du compteur de doses peut se produire.
Test de l’inhalateur
Avant la première utilisation de l'inhalateur ou en cas de non utilisation pendant 14 jours ou plus, le patient doit libérer préalablement une bouffée dans le vide afin de vérifier le bon fonctionnement du dispositif.
Après avoir testé le dispositif pour la première fois, le patient doit s’assurer que le compteur de doses affiche 120 doses.
Utilisation de l’inhalateur
Si l'inhalateur a été exposé à un froid intense, les patients doivent le réchauffer avec leurs mains pendant quelques minutes avant de l'utiliser. L'inhalateur ne doit jamais être réchauffé par des moyens artificiels.
Dans la mesure du possible, les patients doivent être debout ou assis en position verticale lors de l’inhalation.
1. Les patients doivent retirer le capuchon protecteur de l'embout buccal et vérifier que celui-ci est propre et exempt de poussière, de saleté ou de tout autre corps étranger.
2. Les patients doivent expirer aussi lentement et profondément que possible.
3. Les patients doivent tenir la cartouche à la verticale, le corps de la cartouche dirigé vers le haut, et placer les lèvres autour de l'embout buccal sans le mordre.
4. Dans le même temps, les patients doivent inspirer lentement et profondément par la bouche. Après avoir commencé à inspirer, ils doivent appuyer sur le haut de l'inhalateur pour libérer une bouffée.
5. Les patients doivent retenir leur souffle aussi longtemps que possible puis retirer l'inhalateur de la bouche et expirer lentement. Les patients ne doivent pas expirer dans l'inhalateur.
Pour inhaler une bouffée supplémentaire, le patient doit maintenir l'inhalateur en position verticale pendant environ une minute et répéter les étapes 2 à 5.
IMPORTANT : ne pas effectuer les étapes 2 à 5 trop rapidement.
Après utilisation, les patients doivent remettre le capuchon protecteur sur l’inhalateur et vérifier le compteur de doses.
Il est conseillé aux patients de se procurer un nouvel inhalateur lorsque le compteur ou l’indicateur de doses n’affiche plus que 20 doses. L’inhalateur ne doit plus être utilisé lorsque le compteur affiche 0 car les bouffées restant dans le dispositif peuvent ne pas délivrer la dose complète de traitement. Un nouvel inhalateur doit être utilisé.
Si un nuage sort de l'inhalateur ou de chaque côté de la bouche au cours de l'administration du produit, l'inhalation devra être recommencée à partir de l'étape 2.
Chez les patients présentant une faiblesse de préhension, la manipulation de l'appareil peut être facilitée en tenant l'inhalateur à deux mains. Dans ce cas, les index doivent être placés sur le haut de la cartouche de l'inhalateur et les deux pouces sur la base de l'inhalateur.
Les patients doivent se rincer la bouche ou se gargariser à l'eau ou encore se brosser les dents après l'inhalation (voir rubrique 4.4).
Nettoyage
Il est conseillé aux patients de lire attentivement la notice d'information du patient pour connaître les instructions de nettoyage. Pour le nettoyage régulier de l'inhalateur, les patients doivent retirer le capuchon de l'embout buccal et essuyer l'extérieur et l'intérieur de celui-ci à l’aide d’un chiffon ou un tissu sec. Ils ne doivent pas retirer la cartouche de l’inhalateur ni utiliser d'eau ou d'autres liquides pour nettoyer l'embout buccal.
Les patients qui éprouvent des difficultés à coordonner la pression sur le flacon avec l'inspiration de l'aérosol délivré peuvent utiliser la chambre d'inhalation AeroChamber Plus. Ils doivent recevoir des conseils de leur médecin, pharmacien ou infirmier/ère au sujet de l'utilisation et de l'entretien appropriés de l’inhalateur et de la chambre d'inhalation, et leur technique doit être vérifiée afin de garantir une administration optimale du médicament inhalé dans les poumons. Pour y parvenir, les patients qui utilisent AeroChamber Plus doivent respirer lentement et profondément à travers la chambre d'inhalation, sans attendre entre la pression et l'inhalation.
Hypersensibilité aux substances actives ou à l’un des excipients mentionnés à la rubrique 6.1.
4.4. Mises en garde spéciales et précautions d'emploi
Le dipropionate de béclometasone/formotérol doit être administré avec prudence (éventuellement sous surveillance avec enregistrement) chez les patients présentant les affections suivantes : arythmies cardiaques, en particulier bloc auriculo-ventriculaire du troisième degré et tachyarythmies (battements cardiaques accélérés et/ou irréguliers), sténose aortique sous-valvulaire idiopathique, cardiomyopathie hypertrophique obstructive, cardiopathie ischémique, insuffisance cardiaque sévère, hypertension artérielle sévère et anévrisme.
La prudence est également de mise chez les patients présentant un allongement de l'intervalle QTc, connu ou suspecté, qu'il soit congénital ou iatrogène (QTc > 0,44 seconde). Le formotérol lui-même peut induire un allongement de l'intervalle QTc.
La prudence est également recommandée en cas d'utilisation de BECLOMETASONE/FORMOTEROL ZENTIVA chez les patients présentant une thyrotoxicose, un diabète, un phéochromocytome et une hypokaliémie non traitée.
Une hypokaliémie pouvant entraîner des conséquences graves peut être observée lors d'un traitement par bêta-2 agoniste. Une prudence particulière est recommandée en cas d'asthme sévère, car cet effet peut être potentialisé par l'hypoxie. L'administration concomitante de médicaments ayant un effet hypokaliémiant tels que les dérivés xanthiques, les stéroïdes et les diurétiques peut induire une augmentation du risque d'hypokaliémie (voir rubrique 4.5). La prudence est également de mise en cas d'asthme instable pour lequel la prise des médicaments bronchodilatateurs utilisés « à la demande » est importante. Il est recommandé de surveiller la kaliémie dans ces situations.
L’inhalation de formotérol peut provoquer une augmentation de la glycémie. La glycémie doit donc être étroitement surveillée chez les patients diabétiques.
En cas d'anesthésie programmée avec des anesthésiques halogénés, l'administration de BECLOMETASONE/FORMOTEROL ZENTIVA doit être interrompue au moins 12 heures avant le début de l'anesthésie, en raison du risque d'arythmies.
Comme tous les médicaments inhalés contenant des corticoïdes, BECLOMETASONE/ FORMOTEROL ZENTIVA doit être administré avec prudence en cas de tuberculose pulmonaire évolutive ou quiescente et d'infection fongique ou virale des voies respiratoires.
Il est recommandé de ne pas interrompre brutalement un traitement par BECLOMETASONE/ FORMOTEROL ZENTIVA.
Les patients doivent consulter un médecin s’ils jugent le traitement inefficace. L'utilisation croissante de bronchodilatateurs à la demande indique une aggravation de la maladie sous-jacente et justifie une réévaluation du traitement de l'asthme. Une détérioration soudaine et progressive du contrôle de l'asthme est susceptible de mettre en danger la vie du patient, qui doit faire l'objet d'une évaluation médicale en urgence. Il convient d'envisager une augmentation de la corticothérapie, par voie inhalée ou orale, ou un traitement antibiotique en cas de suspicion d’infection.
Le traitement par dipropionate de béclometasone/formotérol ne doit pas être instauré pendant une exacerbation ou une aggravation significative ou une déstabilisation aiguë de l'asthme. Des événements indésirables graves liés à l'asthme ainsi que des exacerbations peuvent survenir au cours du traitement par dipropionate de béclometasone/formotérol. Les patients doivent être invités à poursuivre le traitement et à consulter un médecin si les symptômes de l'asthme restent insuffisamment contrôlés ou s'aggravent après l’instauration d’un traitement par BECLOMETASONE/ FORMOTEROL ZENTIVA.
Comme avec d'autres traitements par inhalation, un bronchospasme paradoxal peut survenir avec une augmentation immédiate des sifflements et de la rapidité de la respiration après l'administration. Ce phénomène doit être traité immédiatement par un bronchodilatateur inhalé à action rapide. Le traitement par BECLOMETASONE/FORMOTEROL ZENTIVA doit être interrompu immédiatement, le patient évalué et un autre traitement instauré si nécessaire.
BECLOMETASONE/FORMOTEROL ZENTIVA ne doit pas être utilisé en traitement de première intention de l'asthme.
Pour le traitement des crises d'asthme aiguës, les patients doivent être informés qu'ils doivent disposer en permanence de leur bronchodilatateur à action rapide.
Il convient de rappeler aux patients de prendre le dipropionate de béclométasone/formotérol quotidiennement, conformément à la prescription médicale, même en l’absence de symptômes.
Lorsque les symptômes de l'asthme ont été contrôlés, une diminution progressive de la dose de dipropionate de béclométasone/formotérol peut être envisagée. Il est primordial d’examiner régulièrement les patients pendant la durée de diminution du traitement. La dose efficace la plus faible de dipropionate de béclométasone/formotérol doit être utilisée (une concentration plus faible de dipropionate de béclométasone/formotérol 100 microgrammes/6 microgrammes est disponible, voir rubrique 4.2).
Les corticoïdes inhalés peuvent induire des effets systémiques, en particulier lorsqu'ils sont utilisés pendant longtemps et à doses élevées. Ces effets sont beaucoup moins susceptibles de se produire avec les corticoïdes inhalés qu'avec les corticoïdes oraux. Les effets systémiques possibles sont les suivants : syndrome de Cushing, symptômes cushingoïdes, freination surrénalienne, diminution de la densité minérale osseuse, retard de croissance chez les enfants et adolescents, cataracte et glaucome et, plus rarement, troubles psychologiques ou du comportement incluant hyperactivité psychomotrice, troubles du sommeil, anxiété, dépression ou agressivité (en particulier chez les enfants).
Par conséquent, il est primordial d'examiner régulièrement le patient et de diminuer la dose de corticoïde inhalé jusqu'à la dose minimale efficace pour le traitement de l'asthme.
Les données de pharmacocinétique en dose unique (voir rubrique 5.2) n'ont pas mis en évidence une exposition systémique du formotérol plus importante avec l'utilisation de la chambre d'inhalation AeroChamber Plus par rapport à l'inhalateur standard. Par ailleurs, l'exposition systémique du 17-monopropionate de béclométasone est diminuée alors que celle du dipropionate de béclométasone sous sa forme inchangée est plus importante. Etant donné que l'exposition systémique totale du dipropionate de béclometasone et de son métabolite actif reste inchangée, aucun risque accru d'effets systémiques n’est à prévoir avec l'utilisation de la chambre d'inhalation AeroChamber Plus.
L'administration au long cours de corticoïdes par voie inhalée à doses élevées peut provoquer une freination surrénalienne voire une insuffisance surrénalienne aiguë. Le risque est particulièrement élevé chez les enfants âgés de moins de 16 ans recevant/inhalant des doses de dipropionate de béclométasone supérieures aux doses préconisées. Les situations susceptibles de favoriser une insuffisance surrénalienne aigue sont notamment les suivantes : traumatisme, intervention chirurgicale, infection ou diminution trop rapide de la posologie. Les symptômes sont habituellement atypiques et peuvent inclure une anorexie, des douleurs abdominales, une perte de poids, une fatigue, des céphalées, des nausées, des vomissements, une hypotension, des troubles de la conscience, une hypoglycémie et des convulsions. Une corticothérapie de supplémentation par voie systémique doit être envisagée pendant toute la durée de la période de stress ou en cas d'intervention chirurgicale programmée.
La prudence est de mise lors du remplacement d'un traitement préalable par dipropionate de béclométasone/formotérol, notamment si un risque de freination surrénalienne par la corticothérapie systémique précédente est pressenti.
Les patients passant d’une corticothérapie orale à une corticothérapie inhalée peuvent présenter un risque de freination surrénalienne pendant une longue période. Les patients qui ont nécessité une corticothérapie d'urgence à doses élevées dans le passé ou qui ont reçu une corticothérapie inhalée prolongée et à doses élevées peuvent également être exposés à ce risque. Ce risque d'insuffisance surrénalienne persistante doit être gardé à l’esprit dans les situations d'urgence et d'intervention programmée susceptibles de générer un stress, et une corticothérapie appropriée doit être envisagée. L'ampleur de l'insuffisance surrénalienne peut nécessiter l'avis d'un spécialiste avant toute intervention programmée.
Les patients doivent être informés que BECLOMETASONE/FORMOTEROL ZENTIVA contient une petite quantité d'éthanol (environ 9 mg par bouffée). Cependant, à des doses normales, la quantité d'éthanol est négligeable et ne présente pas de risque pour les patients.
Ce médicament contient 9 mg d'alcool (éthanol) par bouffée. La quantité d'alcool contenue dans ce médicament équivaut à moins de 1 mL de bière ou 1 mL de vin. La faible quantité d'alcool contenue dans ce médicament n'est pas susceptible d'entraîner d'effet notable.
Il doit être conseillé aux patients de se rincer la bouche ou de se gargariser avec de l'eau ou encore de se brosser les dents après l’inhalation de la dose prescrite, afin de réduire le risque de candidose oropharyngée.
Troubles visuels
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Interactions pharmacocinétiques
Le dipropionate de béclométasone est très rapidement métabolisé par les enzymes estérases.
Le métabolisme de la béclométasone est moins dépendant du CYP3A que celui de certains autres corticoïdes, et les interactions sont en général peu probables. Néanmoins, en cas d’utilisation concomitante d’inhibiteurs puissants du CYP3A (par exemple, ritonavir, cobicistat), la possibilité d’effets systémiques ne peut être exclue. Il est donc conseillé d’être prudent et d’instaurer une surveillance adéquate en cas d’utilisation de ces agents.
Interactions pharmacodynamiques
Les bêta-bloquants peuvent diminuer voire inhiber l'effet du formotérol. Le dipropionate de béclométasone/formotérol ne doit donc pas être administré en association avec des bêta-bloquants (y compris sous forme de collyre), sauf nécessité absolue.
A l'inverse, l'utilisation concomitante d'autres produits bêta-adrénergiques peut entraîner un effet additif. Il convient donc d’être prudent en cas de prescription simultanée de formotérol et de théophylline ou d'autres médicaments bêta-adrénergiques.
Un traitement concomitant par quinidine, disopyramide, procaïnamide, phénothiazines, antihistaminiques, inhibiteurs de la monoamine oxydase et antidépresseurs tricycliques peut provoquer un allongement de l'intervalle QTc et augmenter le risque d'arythmie ventriculaire.
En outre, la L-dopa, la L-thyroxine, l'ocytocine et l'alcool peuvent perturber la tolérance cardiaque des bêta-2 sympathomimétiques.
Un traitement concomitant par des inhibiteurs de la monoamine oxydase ou par des médicaments dotés de propriétés similaires, tels que la furazolidone et la procarbazine, peut provoquer des réactions hypertensives.
Chez les patients recevant, de façon concomitante, une anesthésie par des hydrocarbures halogénés, le risque d'arythmie est augmenté.
Un traitement concomitant par des dérivés de la xanthine, des stéroïdes ou des diurétiques risque de potentialiser l'effet hypokaliémiant des bêta-2 agonistes (voir rubrique 4.4). Chez les patients traités par glycosides digitaliques, l'hypokaliémie peut augmenter le risque d'arythmie.
BECLOMETASONE/FORMOTEROL ZENTIVA contient de l'éthanol en petite quantité. Il existe un risque théorique d'interaction chez les patients particulièrement sensibles recevant du disulfirame ou du métronidazole.
4.6. Fertilité, grossesse et allaitement
Grossesse
Il n’existe aucune donnée ou preuve de la sécurité d'emploi du gaz propulseur HFC-134a chez la femme enceinte ou qui allaite. Toutefois, les études menées chez l’animal et portant sur l'effet du HFC-134a sur la reproduction et le développement embryofœtal n'ont révélé aucun effet indésirable cliniquement pertinent.
Il n'existe aucune donnée clinique pertinente concernant l’utilisation du dipropionate de béclométasone/formotérol chez la femme enceinte. Les études menées chez l’animal concernant l'association de dipropionate de béclométasone et de formotérol ont révélé une toxicité sur la reproduction après une exposition systémique élevée (voir rubrique 5.3). En raison de l'effet tocolytique des bêta-2 sympathomimétiques, la prudence est de mise au cours de la période précédant l'accouchement. L'utilisation du formotérol n’est pas recommandée pendant la grossesse et en particulier en fin de grossesse ou pendant l’accouchement, sauf en l'absence d'alternative et si la sécurité est bien établie.
Le dipropionate de béclométasone/formotérol ne doit être utilisé pendant la grossesse que si les bénéfices escomptés l'emportent sur les risques potentiels.
Il n'existe aucune donnée clinique pertinente concernant l’utilisation du dipropionate de béclométasone/formotérol chez la femme qui allaite.
Bien qu’on ne dispose d’aucune donnée recueillie chez l'animal, il est probable que le dipropionate de béclométasone, comme les autres corticoïdes, soit sécrété dans le lait.
Le passage du formotérol dans le lait humain n'est pas connu, mais sa présence a été détectée chez l'animal pendant l'allaitement.
L'administration du dipropionate de béclométasone/formotérol à des femmes qui allaitent ne doit être envisagée que si les bénéfices escomptés l'emportent sur les risques potentiels.
Une décision doit être prise soit d’interrompre l’allaitement soit d’interrompre/de s’abstenir du traitement par dipropionate de béclométasone/formotérol en prenant en compte le bénéfice de l’allaitement pour l’enfant au regard du bénéfice du traitement pour la femme.
Fertilité
Aucune donnée n’est disponible chez l'être humain. Dans des études animales menées chez le rat, la présence de dipropionate de béclométasone à doses élevées dans l'association a été associée à une diminution de la fertilité des femelles et à une embryotoxicité (voir rubrique 5.3).
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Etant donné que BECLOMETASONE/FORMOTEROL ZENTIVA contient du dipropionate de béclométasone et du formotérol, des effets indésirables dont la nature et la sévérité sont identiques à celles des effets indésirables de chacune des deux substances actives peuvent être attendus. L'administration concomitante des deux substances actives n'entraîne pas la survenue d'événements indésirables supplémentaires.
Les effets indésirables suivants ont été associés au dipropionate de béclométasone et au formotérol administrés en association fixe (dipropionate de béclométasone/formotérol) et en monothérapie, aux fréquences suivantes : très fréquent (≥ 1/10), fréquent (≥ 1/100, < 1/10), peu fréquent (≥ 1/1 000, < 1/100), rare (≥ 1/10 000, < 1/1 000), très rare (≤ 1/10 000), fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
Les effets indésirables fréquents et peu fréquents sont issus d'essais cliniques menés chez des patients asthmatiques et présentant une BPCO.
|
Classe de systèmes d’organes |
Effet indésirable |
Fréquence |
|
Infections et infestations |
Pharyngite, candidose orale |
Fréquent |
|
Grippe, mycose orale, candidose oropharyngée, candidose œsophagienne, candidose vulvovaginale, gastro-entérite, sinusite, rhinite, pneumonie* |
Peu fréquent |
|
|
Affections hématologiques et du système lymphatique |
Granulocytopénie |
Peu fréquent |
|
Thrombopénie |
Très rare |
|
|
Affections du système immunitaire |
Dermatite allergique |
Peu fréquent |
|
Réactions d'hypersensibilité, y compris érythème et œdème des lèvres, du visage, des yeux et du pharynx |
Very rare |
|
|
Affections endocriniennes |
Freination surrénalienne |
Très rare |
|
Troubles du métabolisme et de la nutrition |
Hypokaliémie, hyperglycémie |
Peu fréquent |
|
Affections psychiatriques |
Impatiences |
Peu fréquent |
|
Hyperactivité psychomotrice, troubles du sommeil, anxiété, dépression, agressivité, troubles du comportement (notamment chez l’enfant) |
Fréquence indéterminée |
|
|
Affections du système nerveux |
Céphalées |
Fréquent |
|
Tremblements, sensations vertigineuses |
Peu fréquent |
|
|
Affections oculaires |
Glaucome, cataracte |
Très rare |
|
Vision trouble (voir également rubrique 4.4) |
Fréquence indéterminée |
|
|
Affections de l’oreille et du labyrinthe |
Otosalpingite |
Peu fréquent |
|
Affections cardiaques |
Palpitations, allongement de l'intervalle QT corrigé à l’électrocardiogramme, modifications de l’électrocardiogramme, tachycardie, tachyarythmie, fibrillation auriculaire* |
Peu fréquent |
|
Extrasystoles ventriculaires, angine de poitrine |
Rare |
|
|
Affections vasculaires |
Hyperhémie, bouffées congestives |
Peu fréquent |
|
Affections respiratoires, thoraciques et médiastinales |
Dysphonie |
Fréquent |
|
Toux, toux productive, irritation de la gorge, crise d'asthme, gorge rouge |
Peu fréquent |
|
|
Bronchospasme paradoxal |
Rare |
|
|
Dyspnée, exacerbation de l'asthme |
Très rare |
|
|
Affections gastro-intestinales |
Diarrhée, bouche sèche, dyspepsie, dysphagie, sensation de brûlure des lèvres, nausées, dysgueusie |
Peu fréquent |
|
Affections de la peau et du tissu sous-cutané |
Prurit, rash, hyperhidrose, urticaire |
Peu fréquent |
|
Angiœdème |
Rare |
|
|
Affections musculosquelettiques et du tissu conjonctif |
Contractures musculaires, myalgies |
Peu fréquent |
|
Retard de croissance chez l'enfant et l'adolescent |
Très rare |
|
|
Affections du rein et des voies urinaires |
Néphrite |
Rare |
|
Troubles généraux et anomalies au site d’administration |
Œdème périphérique |
Très rare |
|
Investigations |
Protéine C réactive augmentée, numération plaquettaire augmentée, acides gras libres augmentés, insuline sanguine augmentée, corps cétoniques sanguins augmentés, cortisol sanguin diminué* |
Peu fréquent |
|
Pression artérielle augmentée |
Peu fréquent |
|
|
Pression artérielle diminuée |
Rare |
|
|
Densité osseuse diminuée |
Très rare |
* Un cas non grave de pneumonie liée au traitement par dipropionate de béclométasone/formotérol 100 microgrammes/6 microgrammes a été rapporté au cours d’un essai clinique pivot mené chez des patients présentant une BPCO. La diminution de la cortisolémie et la fibrillation auriculaire figurent parmi les autres effets indésirables observés avec le dipropionate de béclométasone/formotérol 100 microgrammes/6 microgrammes lors des essais cliniques portant sur la BPCO.
Comme avec les autres traitements utilisés en inhalation, un bronchospasme paradoxal peut survenir (voir rubrique 4.4).
Parmi les effets indésirables observés, ceux généralement associés au formotérol sont les suivants : hypokaliémie, céphalées, tremblements, palpitations, toux, contractures musculaires et allongement de l'intervalle QTc.
Les effets indésirables généralement associés à l’administration de dipropionate de béclométasone sont les suivants : mycose orale, candidose orale, dysphonie et irritation de la gorge.
Un gargarisme ou rinçage de la bouche à l'eau et un brossage des dents après l'utilisation du produit permettent de diminuer le risque de dysphonie et de candidose. Une candidose symptomatique peut être traitée par un antifongique topique, le traitement par dipropionate de béclométasone/formotérol étant poursuivi en même temps.
Les corticoïdes par voie inhalée (par exemple, dipropionate de béclométasone) peuvent avoir des effets systémiques, surtout en cas d'utilisation prolongée de doses élevées. Il peut s'agir des phénomènes suivants : freination surrénalienne, diminution de la densité minérale osseuse, retard de croissance chez l'enfant et l'adolescent, cataracte et glaucome (voir rubrique 4.4).
Des réactions d'hypersensibilité telles que rash, urticaire, prurit, érythème et œdème des yeux, du visage, des lèvres et de la gorge peuvent également survenir.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
Des doses cumulées allant jusqu'à douze bouffées de dipropionate de béclométasone/formotérol par voie inhalée (soit au total 1 200 microgrammes de dipropionate de béclométasone et 72 microgrammes de formotérol) administrées dans le cadre d'études chez des patients asthmatiques n'ont pas révélé d'effets perturbant sur les fonctions vitales ni entrainé d’événements indésirables graves ou sévères.
Un surdosage en formotérol peut entraîner des effets spécifiques des agonistes bêta-2 adrénergiques tels que nausées, vomissements, céphalées, tremblements, somnolence, palpitations, tachycardie, arythmies ventriculaires, allongement de l'intervalle QTc, acidose métabolique, hypokaliémie, hyperglycémie.
En cas de surdosage en formotérol, un traitement symptomatique et de soutien est indiqué. Les patients présentant des signes de gravité devront être hospitalisés. Le recours à des bêta-bloquants cardiosélectifs pourra être envisagé, mais avec une prudence extrême compte tenu du risque de bronchospasme induit par les bêta-bloquants. Une surveillance de la kaliémie est requise.
L'inhalation aiguë de doses de dipropionate de béclométasone supérieures aux doses recommandées peut provoquer une freination surrénalienne temporaire. Il n'y a pas lieu d'entreprendre un traitement spécifique, le retour à la normale de la fonction surrénalienne étant obtenu spontanément en quelques jours comme en témoignent les dosages plasmatiques du cortisol. Chez ces patients, le traitement doit être poursuivi aux doses adaptées pour le contrôle de l'asthme.
Le surdosage chronique en dipropionate de béclométasone inhalé expose au risque de freination surrénalienne (voir rubrique 4.4). Une surveillance des fonctions surrénaliennes peut être nécessaire. Le traitement devra être poursuivi à la dose adaptée pour le contrôle de l'asthme.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Mécanisme d’action et effets pharmacodynamiques
BECLOMETASONE/FORMOTEROL ZENTIVA contient du dipropionate de béclométasone et du formotérol. Ces deux substances actives ont des mécanismes d'action différents. Comme avec les autres médicaments par voie inhalée associant un corticoïde et un bêta-2 agoniste, les effets additifs des deux substances actives sont observés sur la réduction des exacerbations de l'asthme.
Dipropionate de béclométasone
Aux doses recommandées, le dipropionate de béclométasone inhalé exerce un effet anti-inflammatoire glucocorticoïde au niveau pulmonaire, ayant pour effet la réduction des symptômes et exacerbations de l'asthme avec des effets indésirables moindres qu'avec les corticoïdes par voie systémique.
Formotérol
Le formotérol est un agoniste bêta-2 adrénergique sélectif qui induit une relaxation des muscles lisses bronchiques en cas de bronchoconstriction. L'effet bronchodilatateur apparaît rapidement, en l'espace de 1 à 3 minutes après l'inhalation, et il persiste 12 heures après l'inhalation d'une dose unique.
Efficacité et sécurité clinique du dipropionate de béclométasone/formotérol
Lors d'essais cliniques menés chez des adultes, l'ajout de formotérol au dipropionate de béclométasone a amélioré les symptômes de l'asthme et la fonction pulmonaire et a réduit les exacerbations.
Au cours d’une étude menée pendant 24 semaines, l'effet du dipropionate de béclométasone/formotérol 100 microgrammes/6 microgrammes HFC sur la fonction pulmonaire a été au moins équivalent à celui de l'association de dipropionate de béclométasone et de formotérol administrés séparément et supérieur à celui du dipropionate de béclométasone utilisé en monothérapie.
L’efficacité du dipropionate de béclométasone/formotérol 200 microgrammes/6 microgrammes HFC, 2 bouffées deux fois par jour, a été évaluée sur la fonction pulmonaire au cours d’un essai pivot de 12 semaines par rapport à un traitement par dipropionate de béclometasone en monothérapie chez des patients asthmatiques mal contrôlés par un traitement antérieur (associations de corticoïdes inhalés à doses élevées ou à doses moyennes + bêta-agonistes de longue durée d’action). L’étude a démontré une supériorité du dipropionate de béclométasone/formotérol 200 microgrammes/6 microgrammes HFC par rapport au dipropionate de béclométasone HFC, en termes de variations par rapport à l'inclusion, du débit de pointe expiratoire matinal moyen pré-dose (différence moyenne ajustée : 18,53 L).
Au cours d’un essai pivot de 24 semaines, le profil de sécurité du dipropionate de béclométasone/ formotérol 200 microgrammes/6 microgrammes HFC, 2 bouffées deux fois par jour, a été comparable à celui d’une association fixe autorisée (fluticasone/salmétérol 500 microgrammes/50 microgrammes, 1 bouffée deux fois par jour). Aucun effet cliniquement pertinent n’a été observé avec le dipropionate de béclométasone/formotérol 200 microgrammes/6 microgrammes HFC sur l’axe hypothalamo-hypophyso-surrénalien après 6 mois de traitement.
Cette étude a révélé que le dipropionate de béclométasone/formotérol 200 microgrammes/ 6 microgrammes et l’association fixe autorisée n’étaient pas supérieurs au dipropionate de béclométasone non-extrafine en monothérapie (2 000 microgrammes/jour) en termes de modification du VEMS matinal pré-dose et du pourcentage de jours complets sans symptômes d'asthme.
5.2. Propriétés pharmacocinétiques
Une étude clinique a permis de comparer l'exposition systémique à chacune des substances actives de l'association fixe dipropionate de béclométasone/formotérol - dipropionate de béclométasone et formotérol - à celle obtenue après l'administration séparée de chacune des substances actives.
Au cours d’une étude pharmacocinétique menée chez des sujets sains traités par une dose unique de l'association fixe dipropionate de béclométasone/formotérol (4 bouffées de 100 microgrammes/ 6 microgrammes) ou par une dose unique de dipropionate de béclométasone CFC (4 bouffées de 250 microgrammes) et de formotérol HFC (4 bouffées de 6 microgrammes), l'aire sous la courbe (ASC) du principal métabolite actif du dipropionate de béclométasone (17-monopropionate de béclométasone) et sa concentration plasmatique maximale ont été réduites de 35 % et 19 % respectivement, avec l'association fixe, par rapport à la formulation non-extrafine de dipropionate de béclométasone CFC ; en revanche, la vitesse d'absorption était plus rapide (0,5 heure contre 2 heures) avec l'association fixe qu'avec la formulation non-extrafine de dipropionate de béclométasone CFC seul.
Pour le formotérol, les concentrations plasmatiques maximales étaient similaires après l'administration de l'association fixe et de chacune des substances actives administrées séparément et l'exposition systémique était légèrement plus élevée avec le dipropionate de béclométasone/formotérol que lorsque les produits étaient administrés séparément.
Il n’existe aucun élément évoquant l'existence d'interactions pharmacocinétiques ou pharmacodynamiques (systémiques) entre le dipropionate de béclométasone et le formotérol.
Une étude pharmacocinétique intégrant du charbon activé menée chez des volontaires sains a mis en évidence une biodisponibilité pulmonaire du 17-monopropionate de béclométasone proportionnelle à la dose avec le dipropionate de béclométasone/formotérol 200 microgrammes/6 microgrammes par rapport à la formulation 100 microgrammes/6 microgrammes pour l'ASC uniquement {le rapport moyen de biodisponibilité systémique de la formulation 200 microgrammes/6 microgrammes et du dosage 100 microgrammes/6 microgrammes était de 91,63 (intervalle de confiance à 90 % : 83,79 ; 100,20)}. Concernant le fumarate de formotérol, le rapport moyen de biodisponibilité systémique de la formulation 200 microgrammes/6 microgrammes et du dosage 100 microgrammes/6 microgrammes était de 86,15 [intervalle de confiance à 90 % : 75,94 ; 97,74].
Une autre étude pharmacocinétique n’intégrant pas de charbon activé menée chez des volontaires sains a mis en évidence une exposition systémique au 17-monopropionate de béclométasone proportionnelle à la dose avec la formulation de dipropionate de béclométasone/formotérol 200 microgrammes/6 microgrammes par rapport au dosage 100 microgrammes/6 microgrammes {le rapport moyen de biodisponibilité systémique de la formulation 200 microgrammes/6 microgrammes et du dosage 100 microgrammes/6 microgrammes était de 89,2 (intervalle de confiance à 90 % : 79,8 ; 99,7)}. L’exposition systémique totale du fumarate de formotérol, était inchangée ; {le rapport moyen de biodisponibilité systémique de la formulation 200 microgrammes/6 microgrammes et du dosage 100 microgrammes/6 microgrammes était de 102,2 [intervalle de confiance à 90 % : 90,4 ; 115,5)}.
Suite à l’utilisation de dipropionate de béclométasone/formotérol 200 microgrammes/6 microgrammes avec la chambre d'inhalation AeroChamber Plus chez des volontaires sains, une augmentation de la déposition pulmonaire du métabolite actif du dipropionate de béclométasone, le 17-monopropionate de béclométasone, de 25 % et du formotérol de 32 %, a été observée, tandis que l'exposition systémique totale a été légèrement réduite pour le 17-monopropionate de béclométasone (de 17 %) et le formotérol (de 17 %) et a augmenté pour le dipropionate de béclométasone sous sa forme inchangée (de 54 %).
Dipropionate de béclométasone
Le dipropionate de béclométasone est une pro-drogue dotée d'une faible affinité de fixation aux récepteurs des glucocorticoïdes et qui est hydrolysée par des enzymes estérases, donnant naissance à un métabolite actif, le 17-monopropionate de béclométasone, dont l'activité anti-inflammatoire topique est plus intense que celle de la pro-drogue dipropionate de béclométasone.
Absorption, distribution et biotransformation
Après inhalation, le dipropionate de béclométasone est rapidement absorbé par les poumons ; avant l'absorption, il est largement transformé en son métabolite actif, le 17-monopropionate de béclométasone, sous l'effet d'enzymes estérases présentes dans la plupart des tissus. La disponibilité systémique du métabolite actif est liée à l'absorption pulmonaire (36 %) et à l'absorption gastro-intestinale de la fraction déglutie. La biodisponibilité du dipropionate de béclométasone dégluti est négligeable, mais la transformation présystémique en 17-monopropionate de béclométasone aboutit à une résorption de 41 % sous la forme du métabolite actif.
L'exposition systémique augmente de façon approximativement linéaire avec la dose inhalée.
Après inhalation, la biodisponibilité absolue est d'environ 2 % de la dose nominale pour le dipropionate de béclométasone sous forme inchangée et 62 % pour le 17-monopropionate de béclométasone.
Après administration intraveineuse, la pharmacocinétique du dipropionate de béclométasone et de son métabolite actif se caractérise par une clairance plasmatique élevée (150 et 120 L/h respectivement), avec un volume de distribution à l'état d'équilibre faible pour le dipropionate de béclométasone (20 L) et une distribution tissulaire plus importante pour son métabolite actif (424 L).
Le taux de liaison aux protéines plasmatiques est modéré.
Elimination
Le dipropionate de béclométasone est essentiellement excrété par voie fécale, principalement sous la forme de métabolites polaires. L'excrétion rénale du dipropionate de béclométasone et de ses métabolites est négligeable. La demi-vie d'élimination terminale est de 0,5 heure pour le dipropionate de béclométasone et de 2,7 heures pour le 17-monopropionate de béclométasone.
Populations particulières
La pharmacocinétique du dipropionate de béclométasone n'a pas été étudiée chez des patients présentant une insuffisance rénale ou hépatique. Etant donné que le dipropionate de béclométasone est très rapidement métabolisé par les enzymes estérases présentes dans le liquide intestinal, le sérum, les poumons et le foie, donnant naissance à des produits plus polaires (21-monopropionate de béclométasone, 17-monopropionate de béclométasone et béclométasone), il n'y a pas lieu de penser qu'une insuffisance hépatique modifie la pharmacocinétique et le profil de sécurité du dipropionate de béclométasone.
Etant donné que ni le dipropionate de béclométasone ni ses métabolites n'ont été retrouvés dans les urines, il n'y pas lieu de considérer la possibilité d'une augmentation de l'exposition systémique chez les patients présentant une insuffisance rénale.
Formotérol
Absorption et distribution
Après inhalation, le formotérol est absorbé à la fois par les poumons et par le tractus gastro-intestinal. La fraction de la dose inhalée qui est déglutie après administration à l'aide d'un aérosol-doseur est comprise entre 60 % et 90 %. Au moins 65 % de la fraction déglutie sont absorbés par le tractus gastro-intestinal. Les concentrations plasmatiques maximales de la substance active sous forme inchangée sont atteintes en l'espace de 0,5 à 1 heure après l’administration orale. Le taux de liaison du formotérol aux protéines plasmatiques est de 61– 64 %, avec 34 % de liaison à l'albumine. Dans l’intervalle des concentrations atteintes aux doses thérapeutiques, aucun phénomène de saturation de la liaison n’a été observé. Après administration orale, la demi-vie d'élimination est de 2– 3 heures. L'absorption du formotérol est linéaire après l'inhalation de 12 à 96 microgrammes de fumarate de formotérol.
Biotransformation
Le formotérol est largement métabolisé et la voie de transformation métabolique consiste essentiellement en une conjugaison directe au niveau du groupe hydroxyle phénolique. Le conjugué d'acide glucuronique est inactif. La deuxième voie métabolique essentielle consiste en une O-déméthylation suivie d'une conjugaison au niveau du groupement phénolique 2'-hydroxyle. Les iso-enzymes CYP2D6, CYP2C19 et CYP2C9 du cytochrome P450 interviennent dans la O-déméthylation du formotérol. La transformation métabolique semble se dérouler essentiellement au niveau du foie. Aux concentrations thérapeutiques pertinentes, le formotérol n'induit pas d'inhibition des iso-enzymes du CYP450.
Elimination
L'excrétion urinaire cumulée du formotérol après une inhalation unique à partir d'un inhalateur de poudre sèche augmente de façon linéaire dans l’intervalle de doses allant de 12 à 96 microgrammes. En moyenne, 8 % et 25 % de la dose sont excrétés, respectivement, sous forme inchangée et sous forme de formotérol total. Au vu des concentrations plasmatiques enregistrées après l'inhalation d'une dose unique de 120 microgrammes chez 12 sujets sains, la demi-vie d'élimination terminale est en moyenne de 10 heures. Les énantiomères (R,R) et (S,S) représentent respectivement environ 40 % et 60 % du médicament excrété sous forme inchangée dans les urines. La proportion relative des deux énantiomères reste constante dans l’intervalle de doses étudié et rien n'indique une accumulation de l'un des énantiomères après administration répétée.
Après administration orale (40 à 80 microgrammes), 6 % à 10 % de la dose ont été retrouvés dans les urines sous forme de substance active inchangée chez des sujets sains ; jusqu'à 8 % de la dose étaient retrouvés sous forme du glucuronide.
Au total, 67 % d'une dose orale de formotérol sont excrétés dans les urines (essentiellement sous forme de métabolites) et le reste dans les selles. La clairance rénale du formotérol est de 150 mL/min.
Populations particulières
Insuffisance hépatique/rénale
La pharmacocinétique du formotérol n'a pas été étudiée chez des patients présentant une insuffisance hépatique ou rénale. Cependant, le formotérol étant principalement éliminé par métabolisation hépatique, une augmentation de l’exposition est attendue en cas de cirrhose hépatique sévère.
5.3. Données de sécurité préclinique
Les études menées chez le rat pour étudier la toxicité sur la reproduction ont montré des effets dose-dépendants. L'association a provoqué une réduction de la fertilité des femelles et une toxicité embryofœtale. Des doses élevées de corticoïdes administrées à des animaux gravides sont connues pour provoquer des anomalies du développement fœtal, notamment des fentes palatines et des retards de croissance intra-utérins, et les effets constatés avec l'association dipropionate de béclométasone/formotérol étaient donc probablement imputables au dipropionate de béclométasone. Ces effets n'ont été observés qu'à de fortes expositions systémiques au métabolite actif, le 17-monopropionate de béclométasone (200 fois les taux plasmatiques prévus en clinique). En outre, les études menées chez l’animal ont révélé un allongement de la durée de la gestation et de la mise-bas, ce qui s'explique par les effets tocolytiques connus des bêta-2 sympathomimétiques.
Ces effets ont été constatés à des taux plasmatiques maternels de formotérol inférieurs aux taux prévus chez les patients traités par dipropionate de béclométasone/formotérol.
Les études de génotoxicité menées avec l'association dipropionate de béclométasone/formotérol n'indiquent pas de potentiel mutagène. Aucune étude de carcinogénicité n'a été menée avec l'association proposée. Cependant, les données obtenues chez l'animal avec chacune des substances actives de l'association ne suggèrent aucun risque de carcinogénicité chez l’être humain.
Les études précliniques conventionnelles de sécurité pharmacologique, de toxicité en doses répétées, de génotoxicité, de carcinogénicité et de toxicité sur la reproduction concernant le gaz propulseur HFA-134a sans CFC n'ont pas révélé de risques particuliers pour l’être humain.
Norflurane (HFC-134a), éthanol anhydre, acide chlorhydrique.
21 mois.
6.4. Précautions particulières de conservation
Avant la délivrance au patient :
A conserver au réfrigérateur (entre 2 et 8 °C) pendant 18 mois maximum.
Après la délivrance au patient :
A conserver à une température ne dépassant pas 25 °C pendant 3 mois maximum.
La cartouche contient un liquide pressurisé. Ne pas exposer à des températures supérieures à 50 °C. Ne pas percer la cartouche.
6.5. Nature et contenu de l'emballage extérieur
La solution pour inhalation est contenue dans un flacon pressurisé en aluminium de 19 mL doté d'une valve doseuse, placé dans un inhalateur en plastique polypropylène avec compteur de doses, qui comprend un embout buccal et est muni d’un capuchon protecteur en plastique.
Présentations :
· 1 flacon pressurisé délivrant 120 doses ou
· 2 flacons pressurisés délivrant 120 doses chacun
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Pour les pharmacies
Inscrire sur la boîte la date de délivrance au patient.
Vérifier qu'il s'écoulera bien au moins 3 mois entre la date de délivrance du médicament au patient et la date de péremption imprimée sur l'emballage.
Elimination
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
35 RUE DU VAL DE MARNE
75013 PARIS
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 303 185 0 8 : 120 doses en flacon pressurisé (Aluminium), boîte de 1.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I
ANSM - Mis à jour le : 06/10/2025
Dipropionate de béclométasone/fumarate de formotérol dihydraté
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin, votre pharmacien ou votre infirmier/ère.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que BECLOMETASONE/FORMOTEROL ZENTIVA 200/6 microgrammes/dose, solution pour inhalation en flacon pressurisé et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser BECLOMETASONE/FORMOTEROL ZENTIVA 200/6 microgrammes/dose, solution pour inhalation en flacon pressurisé ?
3. Comment utiliser BECLOMETASONE/FORMOTEROL ZENTIVA 200/6 microgrammes/dose, solution pour inhalation en flacon pressurisé ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver BECLOMETASONE/FORMOTEROL ZENTIVA 200/6 microgrammes/dose, solution pour inhalation en flacon pressurisé ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE BECLOMETASONE/FORMOTEROL ZENTIVA 200/ 6 microgrammes/dose, solution pour inhalation en flacon pressurisé ET DANS QUELS CAS EST-IL UTILISE ?
BECLOMETASONE/FORMOTEROL ZENTIVA est une solution pour inhalation en flacon pressurisé contenant deux substances actives qui sont inhalées par la bouche et administrées directement dans les poumons.
Les deux substances actives sont :
· Le dipropionate de béclométasone appartient à un groupe de médicaments appelés corticoïdes qui exercent un effet anti-inflammatoire et réduisent le gonflement et l'irritation dans vos poumons.
· Le fumarate de formotérol dihydraté appartient à un groupe de médicaments appelés « bronchodilatateurs de longue durée d'action » qui provoquent un relâchement des muscles des voies respiratoires et vous aident à respirer plus facilement.
L'association de ces deux substances actives facilite la respiration en soulageant les symptômes tels que l'essoufflement, les sifflements respiratoires et la toux chez les patients asthmatiques.
BECLOMETASONE/FORMOTEROL ZENTIVA est utilisé pour traiter l'asthme chez les adultes.
Si votre médecin vous a prescrit BECLOMETASONE/FORMOTEROL ZENTIVA, vous êtes probablement dans l’une des deux situations suivantes :
· votre asthme n'est pas correctement contrôlé par des corticoïdes inhalés et des bronchodilatateurs de courte durée d'action utilisés « à la demande » ou
· votre asthme répond bien aux corticoïdes et bronchodilatateurs de longue durée d'action.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER BECLOMETASONE/FORMOTEROL ZENTIVA 200/6 microgrammes/dose, solution pour inhalation en flacon pressurisé ?
· si vous êtes allergique au dipropionate de béclométasone ou au fumarate de formotérol dihydraté ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
Avertissements et précautions
Adressez-vous à votre médecin, pharmacien ou infirmier/ère avant d’utiliser BECLOMETASONE/ FORMOTEROL ZENTIVA :
· Si vous souffrez de troubles cardiaques tels qu'une angine de poitrine (douleur cardiaque, douleur thoracique), si vous présentez une insuffisance cardiaque, un rétrécissement des artères, une maladie des valves cardiaques ou toute autre anomalie cardiaque connue.
· Si vous souffrez d’hypertension artérielle ou si vous savez que vous avez un anévrisme (dilatation anormale de la paroi d'un vaisseau sanguin).
· Si vous présentez des troubles du rythme cardiaque tels qu'une accélération ou une irrégularité des battements cardiaques, un pouls rapide ou des palpitations, ou si vous savez que votre électrocardiogramme est anormal.
· Si vous avez une glande thyroïde hyperactive.
· Si votre taux sanguin de potassium est faible.
· Si vous avez une maladie quelconque du foie ou des reins.
· Si vous êtes diabétique (si vous inhalez des doses élevées de formotérol, votre taux sanguin de glucose risque d'augmenter et il sera donc peut-être nécessaire de vérifier votre glycémie au début de l’utilisation de cet inhalateur et de temps à autre au cours du traitement).
· Si vous avez une tumeur de la glande surrénale (appelée phéochromocytome).
· Si vous devez subir une anesthésie : selon le type d'anesthésique utilisé, il peut être nécessaire d’interrompre le traitement par BECLOMETASONE/FORMOTEROL ZENTIVA au moins 12 heures avant l’anesthésie.
· Si vous êtes actuellement traité(e) ou avez déjà été traité(e) pour une tuberculose (TB) ou si vous présentez une infection pulmonaire virale ou fongique connue.
· Si vous devez éviter de consommer de l'alcool quelle qu'en soit la raison.
Si vous présentez l'une des caractéristiques mentionnées ci-dessus, prévenez toujours votre médecin avant d'utiliser BECLOMETASONE/FORMOTEROL ZENTIVA 200/6 microgrammes/ dose, solution pour inhalation en flacon pressurisé. Si vous avez ou avez eu des problèmes de santé, quels qu'ils soient, ou des allergies, ou si vous n'êtes pas certain(e) de savoir comment utiliser BECLOMETASONE/FORMOTEROL ZENTIVA, consultez votre médecin, une infirmière spécialisée dans le traitement de l'asthme ou votre pharmacien avant d'utiliser ce médicament.
Votre médecin pourra mesurer de temps en temps le taux de potassium dans votre sang, en particulier si votre asthme est sévère. Comme de nombreux bronchodilatateurs, BECLOMETASONE/ FORMOTEROL ZENTIVA peut provoquer une diminution brutale du taux de potassium sérique (hypokaliémie). En effet, la carence en oxygène dans le sang, associée à certains autres traitements que vous pouvez prendre en même temps que ce médicament, peuvent aggraver la diminution des taux de potassium.
Si vous utilisez des doses élevées de corticoïdes inhalés pendant une durée prolongée, il se peut que vous ayez davantage besoin de corticoïdes en cas de stress. Les situations de stress sont provoquées par exemple par une hospitalisation après un accident, un accident grave ou une intervention chirurgicale programmée. Dans une telle situation, votre médecin traitant déterminera s’il est nécessaire d'augmenter votre dose de corticoïdes et vous prescrira au besoin des comprimés ou des injections de stéroïdes.
Si vous devez vous rendre à l'hôpital, n'oubliez pas d'emporter tous vos médicaments et inhalateurs, y compris BECLOMETASONE/FORMOTEROL ZENTIVA et les médicaments ou comprimés obtenus sans ordonnance, dans leur emballage d'origine, si possible.
Contactez votre médecin si votre vision est trouble ou si vous présentez d'autres troubles visuels.
Enfants et adolescents
BECLOMETASONE/FORMOTEROL ZENTIVA ne doit pas être utilisé chez les enfants et adolescents âgés de moins de 18 ans tant qu’aucune donnée complémentaire n’est disponible.
Autres médicaments et BECLOMETASONE/FORMOTEROL ZENTIVA 200/6 microgrammes/ dose, solution pour inhalation en flacon pressurisé
Informez votre médecin ou pharmacien si vous utilisez, avez récemment utilisé ou pourriez utiliser tout autre médicament, y compris des médicaments obtenus sans ordonnance. En effet, ce médicament peut affecter la manière dont agissent certains autres médicaments. De même, certains médicaments peuvent affecter la manière dont BECLOMETASONE/FORMOTEROL ZENTIVA agit.
En particulier, informez votre médecin, votre pharmacien ou votre infirmier/ère si vous utilisez l'un des médicaments suivants :
· Certains médicaments peuvent augmenter les effets de ce médicament et il est possible que votre médecin souhaite vous surveiller attentivement si vous prenez ces médicaments (y compris certains médicaments pour traiter l’infection par le VIH : ritonavir, cobicistat).
· Médicaments bêta-bloquants. Les bêta-bloquants sont des médicaments utilisés pour traiter de nombreuses affections, notamment les problèmes cardiaques, l'hypertension artérielle et le glaucome (augmentation de la pression dans les yeux). Si vous devez utiliser des bêta-bloquants, y compris sous forme de collyre, l'effet du formotérol peut être réduit ou le formotérol peut ne pas fonctionner du tout.
· Les médicaments bêta-adrénergiques (médicaments qui agissent de la même manière que le formotérol) peuvent accentuer les effets du formotérol.
· Médicaments destinés au traitement des anomalies du rythme cardiaque (quinidine, disopyramide, procaïnamide).
· Médicaments destinés au traitement des réactions allergiques (antihistaminiques)
· Médicaments destinés au traitement des symptômes de dépression ou des troubles psychiques, tels que les inhibiteurs de la monoamine oxydase (par exemple, phénelzine et isocarboxazide), les antidépresseurs tricycliques (par exemple, amitryptiline et imipramine) et les phénothiazines.
· Médicaments destinés au traitement de la maladie de Parkinson (L-dopa).
· Médicaments destinés au traitement de l'insuffisance thyroïdienne (L-thyroxine).
· Médicaments contenant de l'ocytocine (provoquant des contractions utérines).
· Médicaments destinés au traitement des troubles mentaux, tels que les inhibiteurs de la monoamine oxydase (IMAO), y compris médicaments dotés de propriétés similaires comme la furazolidone et la procarbazine.
· Médicaments destinés au traitement des maladies cardiaques (digoxine).
· Autres médicaments utilisés pour le traitement de l'asthme (théophylline, aminophylline ou stéroïdes).
· Diurétiques.
Prévenez également votre médecin si vous devez subir une anesthésie générale pour une opération ou des soins dentaires.
BECLOMETASONE/FORMOTEROL ZENTIVA 200/6 microgrammes/dose, solution pour inhalation en flacon pressurisé avec des aliments et boissons
Sans objet.
Il n'existe aucune donnée clinique concernant l'utilisation de BECLOMETASONE/FORMOTEROL ZENTIVA pendant la grossesse.
BECLOMETASONE/FORMOTEROL ZENTIVA ne doit pas être utilisé si vous êtes enceinte, si vous pensez être enceinte, si vous planifiez une grossesse ou si vous allaitez, sauf si votre médecin vous l’a conseillé.
Conduite de véhicules et utilisation de machines
Il est peu probable que BECLOMETASONE/FORMOTEROL ZENTIVA affecte votre aptitude à conduire des véhicules et à utiliser des machines. Cependant, si vous présentez des effets indésirables tels que des sensations vertigineuses et/ou des tremblements, votre aptitude à conduire ou à utiliser des machines pourrait être affectée.
BECLOMETASONE/FORMOTEROL ZENTIVA 200/6 microgrammes/dose, solution pour inhalation en flacon pressurisé contient de l’alcool
Ce médicament contient 9 mg d'alcool (éthanol) par bouffée. La quantité d'alcool contenue dans une bouffée de ce médicament équivaut à moins de 1 mL de vin ou de bière. La faible quantité d'alcool contenue dans ce médicament n'est pas susceptible d'entraîner d'effet notable.
3. COMMENT UTILISER BECLOMETASONE/FORMOTEROL ZENTIVA 200/ 6 microgrammes/dose, solution pour inhalation en flacon pressurisé ?
Veillez à toujours utiliser ce médicament en suivant exactement les indications de votre médecin ou pharmacien. Vérifiez auprès de votre médecin ou pharmacien en cas de doute.
Votre médecin vous examinera régulièrement pour s'assurer que vous prenez la dose optimale de BECLOMETASONE/FORMOTEROL ZENTIVA. Votre médecin ajustera votre traitement à la dose la plus faible permettant de contrôler efficacement vos symptômes.
Posologie :
Adultes et personnes âgées :
La dose recommandée est de deux inhalations deux fois par jour.
La dose quotidienne maximale est de 4 inhalations.
Rappel : vous devez toujours avoir sur vous votre inhalateur « de secours » à action rapide pour traiter l'aggravation des symptômes de l'asthme ou une crise d'asthme soudaine.
Patients à risque :
Il n’est pas nécessaire d’adapter la dose si vous êtes une personne âgée. Aucune information n'est disponible concernant l'utilisation de ce médicament chez les personnes présentant des problèmes hépatiques ou rénaux.
Utilisation chez les enfants et adolescents âgés de moins de 18 ans :
Les enfants et adolescents âgés de moins de 18 ans ne doivent PAS prendre ce médicament.
BECLOMETASONE/FORMOTEROL ZENTIVA est efficace pour le traitement de l'asthme à une dose de dipropionate de béclométasone qui peut être inférieure à celle de certains autres inhalateurs contenant cette substance. Si vous utilisiez précédemment un inhalateur différent contenant du dipropionate de béclométasone, votre médecin vous indiquera quelle dose exacte de ce médicament vous devez prendre pour traiter votre asthme.
N'augmentez pas la dose.
Si vous avez l'impression que le médicament n'est pas très efficace, parlez-en à votre médecin avant d'augmenter la dose.
Si votre asthme s'aggrave :
Si vos symptômes s'aggravent ou sont difficiles à contrôler (par exemple, si vous utilisez plus fréquemment un autre inhalateur « de secours ») ou si votre inhalateur « de secours » ne soulage pas vos symptômes, consultez immédiatement votre médecin. Il se peut que votre asthme s'aggrave et que votre médecin doive ajuster votre dose de BECLOMETASONE/FORMOTEROL ZENTIVA ou vous prescrire un autre traitement.
Mode d’administration
BECLOMETASONE/FORMOTEROL ZENTIVA est destiné à être inhalé.
Ce médicament se présente sous la forme d’une cartouche pressurisée introduite dans un inhalateur en plastique muni d’un embout buccal. Un compteur de doses se trouve au dos de l’inhalateur, il vous indiquera le nombre de doses restantes. Chaque fois que vous appuyez sur la cartouche, une bouffée est libérée et une dose est décomptée. Attention à ne pas faire tomber le dispositif, cela risquerait de provoquer un décompte accidentel du compteur de doses.
Test de votre inhalateur
Avant d'utiliser l'inhalateur pour la première fois ou si vous ne l'avez pas utilisé pendant 14 jours ou plus, vous devez tester votre inhalateur pour vérifier son bon fonctionnement.
1. Retirez le capuchon protecteur de l’embout buccal.
2. Tenez l’inhalateur à la verticale, l’embout buccal dirigé vers le bas.
3. Tenez l’embout buccal éloigné de vous et appuyez fermement sur la cartouche pour libérer une bouffée.
4. Vérifiez le compteur de doses. Si vous testez votre inhalateur pour la première fois, le compteur de doses doit afficher 120 après l’essai.
Comment utiliser votre inhalateur
Dans la mesure du possible, vous devez être debout ou assis en position verticale lors de l'inhalation.
Avant de procéder à l’inhalation, vérifiez le compteur de doses : un chiffre compris entre « 1 » et « 120 » indique qu'il reste des doses. Si le compteur de doses affiche « 0 », cela signifie qu’il ne reste plus aucune dose ; jetez votre inhalateur et procurez-vous-en un nouveau.
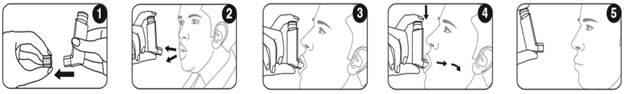
1. Retirez le capuchon protecteur de l'embout buccal et vérifiez que ce dernier est propre, non poussiéreux et exempt de saleté ou de tout autre corps étranger.
2. Expirez aussi lentement et profondément que possible.
3. Tenez la cartouche à la verticale, le corps de la cartouche dirigé vers le haut et enserrez l'embout buccal entre vos lèvres. Ne mordez pas l'embout buccal.
4. Inspirez lentement et profondément par la bouche et, juste après avoir commencé à inspirer, appuyez fermement sur le haut de l’inhalateur pour libérer une bouffée. Si vous n'avez pas suffisamment de force dans les mains, il peut vous être plus facile de tenir l'inhalateur des deux mains : tenez la partie supérieure de l'inhalateur entre vos deux index et la partie inférieure entre vos deux pouces.
5. Retenez votre respiration aussi longtemps que possible, puis retirez l'inhalateur de votre bouche et expirez lentement. N'expirez pas dans l'inhalateur.
Si vous devez inhaler une autre bouffée, maintenez l'inhalateur en position verticale pendant environ une minute, puis répétez les étapes 2 à 5.
Important : n’effectuez pas les étapes 2 à 5 trop rapidement.
Après utilisation, fermez l’inhalateur en remettant le capuchon protecteur et vérifiez le compteur de doses.
Pensez à vous procurer un nouvel inhalateur lorsque le compteur de doses affiche 20 doses. Arrêtez d’utiliser l’inhalateur lorsque le compteur de doses affiche 0. En effet, les bouffées restantes dans le dispositif peuvent ne pas délivrer la dose complète de traitement et vous devez commencer à utiliser un nouvel inhalateur.
Si vous voyez un « nuage » s'échapper du haut de l'inhalateur ou des côtés de votre bouche, cela signifie que BECLOMETASONE/FORMOTEROL ZENTIVA ne pénètre pas dans vos poumons comme il le devrait. Prenez une autre bouffée, en suivant les instructions à partir de l'étape 2.
Pour réduire le risque d'infection fongique dans la bouche et la gorge, rincez-vous la bouche, faites des gargarismes avec de l'eau, ou brossez-vous les dents chaque fois que vous utilisez votre inhalateur.
Si vous avez l'impression que l'effet de BECLOMETASONE/FORMOTEROL ZENTIVA est trop important ou insuffisant, parlez-en à votre médecin ou à votre pharmacien.
Si vous avez des difficultés à faire fonctionner l'inhalateur tout en inspirant, vous pouvez utiliser la chambre d'inhalation AeroChamber Plus. Demandez à votre médecin, ou pharmacien ou infirmier/ère de vous parler de l’utilisation de ce dispositif.
Il est important que vous lisiez la notice fournie avec votre chambre d'inhalation AeroChamber Plus et que vous suiviez attentivement les instructions d’utilisation et de nettoyage qui y figurent.
Nettoyage
Vous devez nettoyer votre inhalateur une fois par semaine.
Lors du nettoyage, n’enlevez pas la cartouche de l’inhalateur et n'utilisez pas d'eau ou d'autres liquides pour nettoyer votre inhalateur.
Pour nettoyer votre inhalateur :
1. Retirez le capuchon protecteur de l’embout buccal en le détachant de l'inhalateur.
2. Essuyez l’intérieur et l’extérieur de l’embout buccal et de l’inhalateur à l’aide d’un chiffon ou un tissu propre et sec.
3. Replacez le capuchon sur l’embout buccal.
Si vous avez utilisé plus de BECLOMETASONE/FORMOTEROL ZENTIVA 200/6 microgrammes/ dose, solution pour inhalation en flacon pressurisé que vous n’auriez dû
· L'utilisation d'une dose excessive de formotérol peut provoquer les effets suivants : nausées, vomissements, accélération de la fréquence des battements cardiaques, palpitations, troubles du rythme cardiaque, certaines formes de modifications de l'électrocardiogramme (enregistrement de l'activité électrique du cœur à l'aide d'un appareil électrocardiographe), maux de tête, tremblements, sensation de somnolence, excès d'acide dans le sang, diminution du taux sanguin de potassium et augmentation du taux sanguin de glucose. Votre médecin vous prescrira éventuellement des analyses de sang pour contrôler vos taux sanguins de potassium et de glucose.
· L'utilisation de doses excessives de dipropionate de béclométasone peut provoquer des perturbations de la fonction des glandes surrénales à court terme. Cependant, ces anomalies s'amélioreront en l'espace de quelques jours mais votre médecin devra peut-être effectuer des analyses de sang pour contrôler votre taux de cortisol sérique.
Si vous présentez l'un de ces symptômes, prévenez votre médecin.
Si vous oubliez d’utiliser BECLOMETASONE/FORMOTEROL ZENTIVA 200/6 microgrammes/ dose, solution pour inhalation en flacon pressurisé
Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre. Prenez-la dès que vous constatez l’oubli. Si l'heure de la dose suivante est proche, ne prenez pas la dose que vous avez oubliée, mais prenez la dose suivante à l'heure prévue.
Si vous arrêtez d’utiliser BECLOMETASONE/FORMOTEROL ZENTIVA 200/6 microgrammes/ dose, solution pour inhalation en flacon pressurisé
Ne diminuez pas la dose et n'arrêtez pas d’utiliser le traitement. Même si vous vous sentez mieux, n'arrêtez pas de prendre BECLOMETASONE/FORMOTEROL ZENTIVA et ne diminuez pas la dose. Si vous voulez le faire, parlez-en à votre médecin. Il est très important que vous utilisiez ce médicament régulièrement, même si vous ne présentez aucun symptôme.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin, à votre pharmacien ou à votre infirmier/ère.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Comme avec les autres traitements par inhalation, il existe un risque de survenue d'une aggravation de l'essoufflement et des sifflements respiratoires immédiatement après l’utilisation de ce médicament. Ce phénomène est appelé bronchospasme paradoxal. S'il se produit, vous devez immédiatement ARRETER d'utiliser BECLOMETASONE/FORMOTEROL ZENTIVA et utiliser aussitôt votre inhalateur « de secours » à action rapide pour traiter les symptômes d’essoufflement et de sifflements respiratoires. Vous devez immédiatement contacter votre médecin.
Informez immédiatement votre médecin en cas d’apparition de réactions d'hypersensibilité telles qu'allergies cutanées, démangeaisons, éruption cutanée, rougeur de la peau, gonflement de la peau ou des muqueuses, en particulier des yeux, du visage, des lèvres et de la gorge.
Les autres effets indésirables éventuels sont énumérés ci-dessous en fonction de leur fréquence.
Fréquent (pouvant affecter jusqu’à 1 personne sur 10) :
· infections fongiques (de la bouche et de la gorge) ;
· maux de tête ;
· enrouement ;
· maux de gorge.
Peu fréquent (pouvant affecter jusqu’à 1 personne sur 100)
· palpitations ;
· accélération inhabituelle du rythme cardiaque et trouble du rythme cardiaque ;
· certaines modifications de l'électrocardiogramme (ECG) ;
· augmentation de la pression artérielle ;
· symptômes pseudo-grippaux ;
· inflammation des sinus ;
· rhinite ;
· inflammation de l'oreille ;
· irritation de la gorge ;
· toux et toux productive ;
· crise d'asthme ;
· infections fongiques du vagin ;
· nausées ;
· sens du goût anormal ou altéré ;
· brûlure des lèvres ;
· bouche sèche ;
· troubles de la déglutition ;
· indigestion ;
· maux d'estomac ;
· diarrhée ;
· douleurs musculaires et crampes musculaires ;
· rougeur du visage et de la gorge ;
· augmentation du flux sanguin dans certains tissus de l’organisme ;
· transpiration excessive ;
· tremblements ;
· impatiences ;
· sensations vertigineuses ;
· urticaire ou éruption cutanée ;
· altération de certaines composantes du sang : diminution du nombre de globules blancs,
o augmentation du nombre de plaquettes,
o diminution du taux sanguin de potassium,
o augmentation de la glycémie,
o augmentation du taux sanguin d'insuline, d'acides gras libres et de cétones.
Les effets indésirables suivants ont également été rapportés chez les patients présentant une bronchopneumopathie chronique obstructive à une fréquence classée comme « peu fréquente » :
· pneumonie ; informez votre médecin si vous remarquez l’un des symptômes suivants : augmentation de la quantité de crachats, modification de la couleur des crachats, fièvre, augmentation de la toux, augmentation des problèmes respiratoires ;
· diminution du taux de cortisol dans le sang : ceci est dû à l’effet des corticoïdes sur votre glande surrénale ;
· battements de cœur irréguliers.
Rare (pouvant affecter jusqu’à 1 personne sur 1 000)
· oppression thoracique ;
· sensation d’omission d'un battement cardiaque ;
· diminution de la pression artérielle ;
· inflammation des reins ;
· gonflement de la peau et des muqueuses persistant pendant plusieurs jours.
Très rare (pouvant affecter jusqu’à 1 personne sur 10 000)
· aggravation de l'asthme ;
· essoufflement ;
· diminution du nombre de plaquettes sanguines ;
· gonflement des mains et des pieds.
L'utilisation de doses élevées de corticoïdes inhalés sur une longue période peut entraîner, dans de très rares cas, des effets systémiques. Ces effets comprennent :
· troubles du fonctionnement des glandes surrénales (adrénosuppression) ;
· augmentation de la pression dans vos yeux (glaucome) ;
· cataractes ;
· retard de croissance (ralentissement de la croissance chez les enfants et les adolescents) ;
· diminution de la densité minérale osseuse (amincissement des os).
Fréquence indéterminée (ne peut être estimée sur la base des données disponibles)
· troubles du sommeil ;
· dépression ou inquiétude ;
· nervosité ;
· surexcitation ou irritabilité.
Ces événements sont plus susceptibles de se produire chez les enfants.
· Vision trouble.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou à votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER BECLOMETASONE/FORMOTEROL ZENTIVA 200/ 6 microgrammes/dose, solution pour inhalation en flacon pressurisé ?
Tenir ce médicament hors de la vue et de la portée des enfants.
Avant la délivrance : conserver l'inhalateur au réfrigérateur (entre 2 et 8 °C).
Après la délivrance (date à laquelle votre pharmacien vous a délivré ce médicament) :
· N'utilisez pas ce médicament au-delà de 3 mois à compter de la date à laquelle votre pharmacien vous a délivré l'inhalateur et ne l'utilisez jamais après la date de péremption indiquée sur la boîte et l'étiquette après EXP. La date de péremption fait référence au dernier jour de ce mois.
· A conserver à une température ne dépassant pas 25 °C.
· Ne pas congeler.
· Si l'inhalateur a été exposé à un froid intense, réchauffez-le avec vos mains pendant quelques minutes avant de l'utiliser. Ne jamais le réchauffer par des moyens artificiels.
· Avertissement : la cartouche contient un liquide pressurisé. Ne pas exposer la cartouche à des températures supérieures à 50 °C. Ne pas percer la cartouche.
· Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
· Les substances actives sont :
Dipropionate de béclométasone.................................................................... 200 microgrammes
Fumarate de formotérol dihydraté...................................................................... 6 microgrammes
Pour une bouffée/dose mesurée (en sortie du flacon pressurisé).
Cela correspond à une dose délivrée par l'embout buccal de 169,2 microgrammes de dipropionate de béclométasone et de 5,0 microgrammes de fumarate de formotérol dihydraté.
· Les autres composants sont : éthanol anhydre, acide chlorhydrique et norflurane (gaz propulseur sans CFC).
Ce médicament contient des gaz à effet de serre fluorés.
Chaque inhalateur contient 10,24 g de norflurane (HFC-134a) correspondant à 0,015 tonne d'équivalent CO2 (potentiel de réchauffement global PRG = 1430)
BECLOMETASONE/FORMOTEROL ZENTIVA est contenu dans un flacon pressurisé en aluminium de 19 mL doté d'une valve doseuse, placé dans un inhalateur en plastique polypropylène avec compteur de doses, qui comprend un embout buccal et est muni d’un capuchon protecteur en plastique.
Présentations :
· 1 flacon pressurisé délivrant 120 doses ou
· 2 flacons pressurisés délivrant 120 doses chacun
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
35 RUE DU VAL DE MARNE
75013 PARIS
Exploitant de l’autorisation de mise sur le marché
35 RUE DU VAL DE MARNE
75013 PARIS
DE KEYSERLEI 60C BUS 1301
2018 ANTWERP
BELGIQUE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).