Dernière mise à jour le 30/06/2025
DOLIPRANE ADULTES 1000 mg, suppositoire
Indications thérapeutiques
Classe pharmacothérapeutique – code ATC : N02BE01
DOLIPRANE est un antalgique (calme la douleur) et un antipyrétique (fait baisser la fièvre).
La substance active de ce médicament est le paracétamol.
Il est utilisé pour traiter la douleur et/ou la fièvre, par exemple en cas de maux de tête, d’état grippal, de douleurs dentaires, de courbatures, de règles douloureuses.
Cette présentation est réservée à l’adulte et à l’enfant à partir de 50 kg (soit à partir d’environ 15 ans). Lire attentivement la rubrique « Posologie ».
Pour les enfants pesant moins de 50 kg, il existe d’autres présentations de paracétamol dont le dosage est plus adapté. N’hésitez pas à demander conseil à votre médecin ou à votre pharmacien.
Présentations
> film(s) thermosoudé(s) PVC polyéthylène de 8 suppositoire(s)
Code CIP : 330 474-6 ou 34009 330 474 6 7
Déclaration de commercialisation : 19/09/1988
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 1,46 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 2,48 €
- Taux de remboursement :65%
Documents de bon usage du médicament
- Prise en charge de la fièvre chez l’enfant
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Octobre 2016
- Prise en charge médicamenteuse de la douleur chez l'enfant : alternatives à la codéine
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Février 2016
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 01/04/2015 | Renouvellement d'inscription (CT) | Le service médical rendu par les spécialités DOLIPRANE, GELUPRANE et PARACETAMOL ZENTIVA reste important dans les indications de l’AMM. |
Amélioration du service médical rendu (ASMR)
Pas d'ASMR disponible pour ce médicament (plus d'informations dans l'aide )
ANSM - Mis à jour le : 20/06/2025
DOLIPRANE ADULTES 1000 mg, suppositoire
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Paracétamol....................................................................................................................... 1000 mg
Pour un suppositoire.
Pour la liste complète des excipients, voir rubrique 6.1.
Suppositoire.
4.1. Indications thérapeutiques
Traitement symptomatique des douleurs d'intensité légère à modérée et/ou des états fébriles.
Cette présentation est réservée à l'adulte et à l’enfant à partir de 50 kg (soit à partir d’environ 15 ans).
4.2. Posologie et mode d'administration
Posologie
Attention : cette présentation contient 1000 mg de paracétamol par unité : ne pas prendre 2 unités à la fois.
La posologie unitaire usuelle est de 1 suppositoire à 1000 mg par prise, à renouveler en cas de besoin au bout de 4 heures minimum. En cas de diarrhées, l’administration du suppositoire n’est pas recommandée.
Il n’est généralement pas nécessaire de dépasser 3 g de paracétamol par jour, soit 3 suppositoires par jour. Cependant, en cas de douleurs plus intenses, la posologie maximale peut être augmentée jusqu’à 4 g par jour, soit 4 suppositoires par jour.
Toujours respecter un intervalle de 4 heures entre les prises.
Doses maximales recommandées : voir rubrique 4.4.
Fréquence d’administration
Les prises systématiques permettent d’éviter les oscillations de douleur ou de fièvre :
· chez l'adulte, elles doivent être espacées de 4 heures minimum.
Insuffisance rénale
En cas d'insuffisance rénale sévère (clairance de la créatinine inférieure à 10 ml/mn), l'intervalle entre deux prises devra être augmenté et sera au minimum de 8 heures.
La dose totale de paracétamol ne devra pas excéder 3 g par jour soit 3 suppositoires.
Autres situations cliniques
La dose journalière efficace la plus faible doit être envisagée, sans excéder 60 mg/kg/jour (sans dépasser 3 g/j) dans les situations suivantes :
· poids < 50 kg,
· insuffisance hépatocellulaire légère à modérée,
· alcoolisme chronique,
· déshydratation,
· réserves basses en glutathion telles que par exemple malnutrition chronique, jeûne, amaigrissement récent, sujet âgé de plus de 75 ans ou de plus de 65 ans et polypathologique, hépatite virale chronique et VIH, mucoviscidose, cholémie familiale (maladie de Gilbert).
Mode d’administration
Voie rectale.
Durée d’administration
L’administration par voie rectale doit être la plus courte possible en raison du risque de toxicité locale.
· Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
· Insuffisance hépatique sévère.
· Antécédent récent de rectite, d’anite ou de rectorragie.
4.4. Mises en garde spéciales et précautions d'emploi
En raison de la dose unitaire par suppositoire (1000 mg), cette présentation n’est pas adaptée à l'enfant de moins de 15 ans.
Pour éviter un risque de surdosage :
· vérifier l'absence de paracétamol dans la composition d'autres médicaments,
· respecter les doses maximales recommandées.
Dose maximale recommandée
A titre informatif
Chez l’enfant de moins de 40 kg, la dose totale de paracétamol ne doit pas dépasser 80 mg/kg/jour (voir rubrique 4.9)
Chez l’enfant de 41 à 50 kg, la dose totale de paracétamol ne doit pas excéder 3 g par jour (voir rubrique 4.9).
Chez l’adulte et l’enfant de plus de 50 kg, LA DOSE TOTALE DE PARACETAMOL NE DOIT PAS EXCEDER 4 GRAMMES PAR JOUR (voir rubrique 4.9).
Avec les suppositoires, il y a un risque de toxicité locale, d’autant plus fréquent et intense que la durée du traitement est prolongée, le rythme d’administration est élevé et la posologie forte. En conséquence, l’administration d’un suppositoire n’est pas conseillée au‑delà de 4 fois par jour, et la durée de traitement par voie rectale doit être la plus courte possible.
Précautions d’emploi
En cas de diarrhée, la forme suppositoire n’est pas adaptée.
L’administration de paracétamol peut exceptionnellement entrainer une toxicité hépatique, même à doses thérapeutiques, après un traitement de courte durée et chez des patients sans antécédents de troubles hépatiques (voir rubrique 4.8).
Le paracétamol est à utiliser avec précaution sans dépasser 3 g/jour dans les situations suivantes (voir rubrique 4.2) :
· poids < 50 kg,
· insuffisance hépatocellulaire légère à modérée,
· insuffisance rénale sévère (clairance de la créatinine < 30 ml/min (voir rubrique 5.2)),
· alcoolisme chronique,
· déshydratation,
· réserves basses en glutathion telles que par exemple malnutrition chronique, jeûne, amaigrissement récent, sujet âgé de plus de 75 ans ou de plus de 65 ans et polypathologique, hépatite virale chronique et VIH, mucoviscidose, cholémie familiale (maladie de Gilbert),
· allergie à l’aspirine et/ou aux anti‑inflammatoires non stéroïdiens (AINS).
La consommation de boissons alcoolisées pendant le traitement est déconseillée.
En cas de sevrage récent d’un alcoolisme chronique, le risque d’atteinte hépatique est majoré.
En cas de découverte d’une hépatite virale aiguë, il convient d’arrêter le traitement.
Des cas d’acidose métabolique à trou anionique élevé (AMTAE) due à une acidose pyroglutamique ont été rapportés chez les patients atteints de maladies graves telles qu’une insuffisance rénale sévère et un sepsis, ou chez les patients souffrant de malnutrition ou d’autres sources de déficit en glutathion (par exemple, l’alcoolisme chronique), qui ont été traités par du paracétamol à une dose thérapeutique pendant une période prolongée ou par une association de paracétamol et de flucloxacilline. En cas de suspicion d’AMTAE due à une acidose pyroglutamique, il est recommandé d’arrêter immédiatement le paracétamol et d’effectuer une surveillance étroite. La mesure de la 5-oxoproline urinaire peut être utile pour identifier l’acidose pyroglutamique comme cause sous-jacente de l’AMTAE chez les patients présentant de multiples facteurs de risque.
Chez l’enfant, la posologie devra être ajustée en fonction du poids (voir rubrique 4.2).
Chez un enfant traité par 60 mg/kg/jour de paracétamol, l’association d’un autre antipyrétique n’est justifiée qu’en cas d’inefficacité.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Associations faisant l’objet de précautions d’emploi
+ Anticoagulants oraux : warfarine et autres antivitamines K (AVK)
Risque d’augmentation de l’effet de la warfarine et des autres AVK et du risque hémorragique en cas de prise de paracétamol aux doses maximales (4 g/j) pendant au moins 4 jours. Contrôle biologique incluant un contrôle plus fréquent de l’INR. Adaptation éventuelle de la posologie de la warfarine et des autres AVK pendant le traitement par le paracétamol et après son arrêt.
+ Flucloxacilline
Des précautions doivent être prises lorsque le paracétamol est utilisé en même temps que la flucloxacilline, car une prise concomitante a été associée à une acidose métabolique à trou anionique élevé due à une acidose pyroglutamique, en particulier chez les patients présentant des facteurs de risque (voir rubrique 4.4).
+ Médicaments hépatotoxiques
La toxicité du paracétamol peut être augmentée chez les patients traités par des médicaments potentiellement hépatotoxiques ou par des médicaments inducteurs enzymatiques du cytochrome P450, tels que les médicaments anti‑épileptiques (tels que phénobarbital, phénytoïne, carbamazépine, topiramate), la rifampicine ou en cas de prise concomitante d’alcool. L’induction du métabolisme entraine une production importante du métabolite hépatotoxique du paracétamol. L’hépatotoxicité se produit si la quantité de ce métabolite dépasse les capacités de liaison au glutathion.
Interactions avec les examens paracliniques
La prise de paracétamol peut fausser le dosage de la glycémie par la méthode à la glucose oxydase‑péroxydase en cas de concentrations anormalement élevées.
La prise de paracétamol peut fausser le dosage de l’acide urique sanguin par la méthode à l’acide phosphotungstique.
4.6. Fertilité, grossesse et allaitement
Grossesse
Les études effectuées chez l'animal n'ont pas mis en évidence d'effet tératogène ou fœtotoxique du paracétamol.
Une vaste quantité de données portant sur les femmes enceintes démontrent l’absence de toute malformation ou de toute toxicité fœtale/néonatale. Les études épidémiologiques consacrées au neurodéveloppement des enfants exposés au paracétamol in utero produisent des résultats non concluants.
Si cela s’avère nécessaire d’un point de vue clinique, le paracétamol peut être utilisé pendant la grossesse. Cependant il doit être utilisé à la dose efficace la plus faible, pendant la durée la plus courte et le moins fréquemment possible au cours de la grossesse.
Allaitement
Le paracétamol est excrété dans le lait maternel. A doses thérapeutiques, l'administration de ce médicament est possible pendant l'allaitement.
Fertilité
En raison du mécanisme d’action potentiel sur les cyclo-oxygénases et la synthèse de prostaglandines, le paracétamol pourrait altérer la fertilité chez la femme, par un effet sur l’ovulation réversible à l’arrêt du traitement.
Des effets sur la fertilité des mâles ont été observés dans une étude chez l'animal. La pertinence de ces effets chez l'homme n'est pas connue.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Sans objet.
Affections du système immunitaire :
Rare : réactions d’hypersensibilité à type de choc anaphylactique, œdème de Quincke. Leur survenue impose l’arrêt définitif de ce médicament et des médicaments apparentés.
Affections de la peau et des tissus sous‑cutanés :
Rare : érythème, urticaire, rash cutané ont été rapportés.
De très rares cas d’effets indésirables cutanés graves ont été rapportés.
Fréquence indéterminée : érythème pigmenté fixe.
En cas de survenue d’au moins un des effets indésirables mentionnés ci-dessus, ce médicament doit être définitivement arrêté.
Affections hématologiques et du système lymphatique :
Très exceptionnels : thrombopénie, leucopénie et neutropénie.
Fréquence indéterminée : agranulocytose, anémie hémolytique chez les patients présentant un déficit en glucose‑6‑phosphate‑déshydrogénase.
Affections hépatobiliaires :
Fréquence indéterminée : augmentation des transaminases, atteinte hépatique cytolytique, hépatite aiguë, hépatite massive en particulier lors d’une utilisation dans une situation à risque (voir rubrique 4.4 Précautions d’emploi).
Affections respiratoires, thoraciques et médiastinales :
Fréquence indéterminée : bronchospasme (voir rubrique 4.4).
Affections du métabolisme et de la nutrition :
Fréquence indéterminée : acidose métabolique à trou anionique élevé (des cas d’acidose métabolique à trou anionique élevé due à une acidose pyroglutamique ont été rapportés chez des patients présentant des facteurs de risque et prenant du paracétamol (voir rubrique 4.4). Une acidose pyroglutamique peut survenir chez ces patients en raison des faibles taux de glutathion).
LIEES A LA FORME PHARMACEUTIQUE
Irritation rectale et anale.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance ‑ Site internet : https://signalement.social-sante.gouv.fr/
Le risque d'une intoxication grave peut être particulièrement élevé chez les sujets âgés, chez les jeunes enfants, chez les patients avec une atteinte hépatique, en cas d'alcoolisme chronique, chez les patients souffrant de réserves basses en glutathion telles que la malnutrition chronique (voir rubrique 4.2), le jeûne , l’amaigrissement récent, le vieillissement, les virus de l’hépatite virale chronique et du VIH, la cholémie familiale (Maladie de Gilbert) ainsi que les patients traités de façon concomitante par des médicaments inducteurs enzymatiques. Dans ces cas, l'intoxication peut être mortelle.
Symptômes
Nausées, vomissements, anorexie, pâleur, douleurs abdominales apparaissent généralement dans les 24 premières heures.
Un surdosage de paracétamol peut provoquer une cytolyse hépatique susceptible d'entrainer une insuffisance hépatocellulaire, un saignement gastro-intestinal, une acidose métabolique, une encéphalopathie, un coma et le décès.
Des cas de coagulation intravasculaire disséminée ont été observés dans un contexte de surdosage au paracétamol.
En cas de surdosage aigu, il peut être observé dans les 12 à 48 heures une augmentation des transaminases hépatiques, de la lactico-déshydrogénase, de la bilirubine et une diminution du taux de prothrombine.
Le surdosage peut également entrainer une pancréatite, une hyperamylasémie, une insuffisance rénale aiguë et une pancytopenie.
Conduite d’urgence
· Transfert immédiat en milieu hospitalier.
· Prélever un tube de sang pour faire le dosage plasmatique initial de paracétamol. Ce dosage sera à interpréter en fonction du délai entre l’heure supposée de la prise et l’heure de prélèvement. La concentration plasmatique de paracétamol doit être mesurée au moins 4 heures après la prise (les concentrations mesurées avant ne sont pas fiables).
· Evacuation rapide du produit ingéré par lavage gastrique, de préférence dans les 4 heures suivant la prise orale.
· Le traitement du surdosage comprend classiquement l'administration aussi précoce que possible de l'antidote N-acétylcystéine par voie I.V. ou voie orale si possible avant la dixième heure. Bien que la N-acétylcystéine soit plus efficace lorsqu’elle est initiée avant la dixième heure, elle conserve un certain degré de protection même si elle est administrée au cours des 48 premières heures suivant la prise. Dans ce cas, le traitement par N-acétylcystéine devra être prolongé.
· Traitement symptomatique.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : AUTRES ANALGESIQUES ET ANTI‑PYRETIQUES‑ANILIDES, code ATC : N02BE01
N : Système nerveux central.
Mécanisme d’action
Le paracétamol a un mécanisme d’action central et périphérique.
5.2. Propriétés pharmacocinétiques
Absorption
Par voie rectale, l'absorption du paracétamol est moins rapide que par voie orale. Elle est toutefois totale. Les concentrations plasmatiques maximales sont atteintes 2 à 3 heures après administration.
Distribution
Le paracétamol se distribue rapidement dans tous les tissus. Les concentrations sont comparables dans le sang, la salive et le plasma. La liaison aux protéines plasmatiques est faible.
Biotransformation
Le paracétamol est métabolisé essentiellement au niveau du foie. Les 2 voies métaboliques majeures sont la glycuroconjugaison et la sulfoconjugaison. Cette dernière voie est rapidement saturable aux posologies supérieures aux doses thérapeutiques. Une voie mineure, catalysée par le cytochrome P450, est la formation d’un intermédiaire réactif (le N‑acétyl benzoquinone imine) qui, dans les conditions normales d’utilisation, est rapidement détoxifié par le glutathion réduit et éliminé dans les urines après conjugaison à la cystéine et à l’acide mercaptopurique. En revanche, lors d’intoxications massives, la quantité de ce métabolite toxique est augmentée.
Elimination
L’élimination est essentiellement urinaire. 90% de la dose administrée est éliminée par le rein en 24 heures, principalement sous forme glycuroconjuguée (60 à 80%) et sulfoconjuguée (20 à 30%).
Moins de 5% est éliminé sous forme inchangée.
La demi‑vie d’élimination est de 4 à 5 heures.
Variations physiopathologiques
Insuffisance rénale : en cas d'insuffisance rénale sévère (clairance de la créatinine inférieure à 30 ml/min), l'élimination du paracétamol et de ses métabolites est retardée.
Sujet âgé : la capacité de conjugaison n'est pas modifiée.
5.3. Données de sécurité préclinique
Aucune étude conventionnelle s’appuyant sur les normes actuellement admises pour évaluer la toxicité pour la reproduction et le développement n’est disponible.
Glycérides hémi‑synthétiques solides (Witepsol).
Sans objet.
2 ans.
6.4. Précautions particulières de conservation
A conserver à l’abri de la chaleur.
6.5. Nature et contenu de l'emballage extérieur
8 suppositoires sous film thermosoudé (PVC – PE).
6.6. Précautions particulières d’élimination et de manipulation
Pas d’exigences particulières.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
157 AVENUE CHARLES DE GAULLE
92200 NEUILLY-SUR-SEINE
FRANCE
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 330 474 6 7 : 8 suppositoires sous film thermosoudé (PVC – PE)
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Sans objet.
Médicament non soumis à prescription médicale.
ANSM - Mis à jour le : 20/06/2025
DOLIPRANE ADULTES 1000 mg, suppositoire
Paracétamol
Vous devez toujours utiliser ce médicament en suivant scrupuleusement les informations fournies dans cette notice ou par votre médecin ou votre pharmacien.
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Adressez‑vous à votre pharmacien pour tout conseil ou information.
· Si vous ressentez un quelconque effet indésirable, parlez‑en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
· Vous devez vous adresser à votre médecin si vous ne ressentez aucune amélioration ou si vous vous sentez moins bien après 3 jours en cas de fièvre ou 5 jours en cas de douleurs.
· Ne laissez pas ce médicament à la portée des enfants.
1. Qu'est‑ce que DOLIPRANE ADULTES 1000 mg, suppositoire et dans quels cas est‑il utilisé ?
2. Quelles sont les informations à connaître avant d’utiliser DOLIPRANE ADULTES 1000 mg, suppositoire ?
3. Comment utiliser DOLIPRANE ADULTES 1000 mg, suppositoire ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver DOLIPRANE ADULTES 1000 mg, suppositoire ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE DOLIPRANE ADULTES 1000 mg, suppositoire ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique – code ATC : N02BE01
DOLIPRANE est un antalgique (calme la douleur) et un antipyrétique (fait baisser la fièvre).
La substance active de ce médicament est le paracétamol.
Il est utilisé pour traiter la douleur et/ou la fièvre, par exemple en cas de maux de tête, d’état grippal, de douleurs dentaires, de courbatures, de règles douloureuses.
Cette présentation est réservée à l’adulte et à l’enfant à partir de 50 kg (soit à partir d’environ 15 ans). Lire attentivement la rubrique « Posologie ».
Pour les enfants pesant moins de 50 kg, il existe d’autres présentations de paracétamol dont le dosage est plus adapté. N’hésitez pas à demander conseil à votre médecin ou à votre pharmacien.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER DOLIPRANE ADULTES 1000 mg, suppositoire ?
N’utilisez jamais DOLIPRANE ADULTES 1000 mg, suppositoire :
· Si vous êtes allergique au paracétamol ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
· Si vous avez une maladie grave du foie.
· Si vous avez a eu récemment une inflammation anale ou rectale ou des saignements du rectum.
|
Ce médicament contient du paracétamol. D'autres médicaments en contiennent. Vérifiez que vous ne prenez pas d'autres médicaments contenant du paracétamol, y compris si ce sont des médicaments obtenus sans prescription. Ne les associez pas, afin de ne pas dépasser la dose quotidienne recommandée. (voir « Posologie » et « Si vous avez utilisé plus de DOLIPRANE ADULTES 1000 mg, suppositoire que vous n’auriez dû ») |
Avertissements et précautions
Adressez‑vous à votre médecin ou pharmacien avant d’utiliser DOLIPRANE ADULTES 1000 mg, suppositoire.
Faites attention avec DOLIPRANE
· Si la douleur persiste plus de 5 jours, ou la fièvre plus de 3 jours, ou en cas d’efficacité insuffisante ou de survenue de tout autre signe, ne continuez pas le traitement sans l’avis de votre médecin.
· La prise de paracétamol peut entrainer des troubles du fonctionnement du foie.
· Vous devez demander l’avis de votre médecin avant de prendre ce médicament :
o Si vous pesez moins de 50 kg,
o Si vous avez une maladie du foie ou une maladie grave des reins,
o Si vous buvez fréquemment de l’alcool ou que vous avez arrêté de boire de l’alcool récemment,
o Si vous souffrez de déshydratation,
o Si vous souffrez par exemple de malnutrition chronique, si vous êtes en période de jeûne, si vous avez perdu beaucoup de poids récemment, si vous avez plus de 75 ans ou si vous avez plus de 65 ans et que vous présentez des maladies de longue durée, si vous êtes atteint du virus du SIDA ou d’une hépatite virale chronique, si vous souffrez de mucoviscidose (maladie génétique et héréditaire caractérisée notamment par des infections respiratoires graves), ou encore si vous êtes atteint de la maladie de Gilbert (maladie héréditaire associée à une augmentation du taux de bilirubine dans le sang).
o si vous êtes allergique à l’aspirine et/ou aux anti‑inflammatoires non stéroïdiens
· La consommation de boissons alcoolisées pendant le traitement est déconseillée.
· En cas de sevrage récent d’un alcoolisme chronique, le risque d’atteinte hépatique est majoré.
· En cas d’administration chez un enfant, la dose dépend de son poids (voir rubrique « comment utiliser DOLIPRANE ADULTES 1000 mg, suppositoire ? »).
· En cas d’hépatite virale aiguë, arrêtez votre traitement et consultez votre médecin.
Pendant le traitement par DOLIPRANE ADULTES 1000 mg, suppositoire, informez immédiatement votre médecin :
· Si vous avez des maladies graves, y compris une insuffisance rénale grave ou un sepsis (lorsque des bactéries et leurs toxines circulent dans le sang, entraînant des lésions au niveau des organes), ou si vous êtes atteint de malnutrition, d’alcoolisme chronique ou si vous prenez également de la flucloxacilline (un antibiotique). Une affection grave appelée acidose métabolique (une anomalie du sang et des fluides corporels) a été signalée chez les patients qui prennent régulièrement du paracétamol pendant une période prolongée ou qui prennent du paracétamol en association avec de la flucloxacilline. Les symptômes de l’acidose métabolique peuvent inclure : de graves difficultés respiratoires avec une respiration rapide et profonde, une somnolence, une envie de vomir (nausée) et des vomissements.
Analyses de sang
Prévenez votre médecin si vous utilisez DOLIPRANE et que vous devez faire un test sanguin car ce médicament peut fausser les résultats de votre taux d’acide urique (uricémie) et de sucre (glycémie) dans le sang.
EN CAS DE DOUTE NE PAS HESITER A DEMANDER L’AVIS DE VOTRE MEDECIN OU DE VOTRE PHARMACIEN.
Enfants
Sans objet.
Autres médicaments et DOLIPRANE ADULTES 1000 mg, suppositoire
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
Ne prenez pas d’autres médicaments contenant du paracétamol. Vous risqueriez un surdosage.
Si vous suivez un traitement anticoagulant par voie orale (par warfarine ou antivitamines K (AVK)), l’utilisation de DOLIPRANE ADULTES 1000 mg, suppositoire aux doses maximales (4 g/jour) pendant plus de 4 jours nécessite une surveillance renforcée des examens biologiques dont notamment de l’INR. Dans ce cas, consultez votre médecin.
La toxicité du paracétamol peut être augmentée, si vous prenez :
· des médicaments potentiellement toxiques pour le foie,
· des médicaments qui favorisent la production du métabolite toxique du paracétamol tels que les médicaments anti‑épileptiques (phénobarbital, phénytoïne, carbamazépine, topiramate),
· de la rifampicine (un antibiotique),
· en même temps de l’alcool.
DOLIPRANE ADULTES 1000 mg, suppositoire avec des aliments, boissons et de l’alcool
La consommation de boissons alcoolisées pendant le traitement est déconseillée.
Grossesse, allaitement et fertilité
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
Au besoin, ce médicament peut être utilisé pendant la grossesse et l’allaitement. Vous devez utiliser la dose la plus faible possible qui permette de soulager la douleur et/ou la fièvre et la prendre pendant la durée la plus courte possible. Contactez votre médecin ou votre sage-femme si la douleur et/ou la fièvre ne diminuent pas ou si vous devez prendre le médicament plus fréquemment.
Fertilité
Il est possible que le paracétamol puisse altérer la fertilité des femmes, de façon réversible à l'arrêt du traitement.
Conduite de véhicules et utilisation de machines
Sans objet.
3. COMMENT UTILISER DOLIPRANE ADULTES 1000 mg, suppositoire ?
Respectez toujours la dose prescrite par votre médecin. En cas de doute, consultez votre médecin ou votre pharmacien.
En raison du risque d’irritation rectale, l’administration de suppositoire doit être la plus courte possible, ne doit pas dépasser 4 suppositoires par jour et sera remplacée dès que possible par un traitement par voie orale.
En cas de diarrhée, la forme suppositoire n’est pas adaptée.
Cette présentation est réservée à l’adulte et à l’enfant pesant plus de 50 kg (soit à partir d’environ 15 ans).
Pour les enfants ayant un poids inférieur à 50 kg, il existe d’autres présentations de paracétamol dont le dosage est plus adapté. N’hésitez pas à demander conseil à votre médecin ou à votre pharmacien.
Posologie chez l’adulte et l’enfant à partir de 50 kg (soit à partir d’environ 15 ans)
La dose habituelle est de 1 suppositoire par prise, à renouveler au bout de 6 à 8 heures. En cas de besoin, la prise peut être répétée au bout de 4 heures minimum.
|
Attention : cette présentation contient 1000 mg de paracétamol par suppositoire : n’utilisez jamais 2 suppositoires à la fois. |
Dose de paracétamol à ne jamais dépasser
· Chez un adulte ou un enfant pesant plus de 50 kg :
Il n’est généralement pas nécessaire de dépasser 3 grammes de paracétamol par jour (soit 3 suppositoires par jour).
Cependant, si vous avez des douleurs plus intenses, et uniquement sur les conseils de votre médecin, la dose totale peut être augmentée jusqu’à 4 grammes de paracétamol par jour (soit 4 suppositoires par jour).
NE JAMAIS PRENDRE PLUS DE 4 GRAMMES DE PARACETAMOL PAR JOUR (en tenant compte de tous les médicaments contenant du paracétamol dans leur formule).
· Situations particulières :
La dose maximale journalière ne doit pas dépasser 60 mg/kg/jour (sans dépasser 3 g/jour) dans les situations suivantes :
o si vous pesez moins de 50 kg,
o si vous avez une maladie du foie ou une maladie grave des reins,
o si vous buvez fréquemment de l’alcool ou que vous avez arrêté de boire de l’alcool récemment,
o si vous souffrez de déshydratation,
o si vous souffrez par exemple de malnutrition chronique, si vous êtes en période de jeûne, si vous avez perdu beaucoup de poids récemment, si vous avez plus de 75 ans ou si vous avez plus de 65 ans et que vous avez des maladies de longue durée, si vous êtes atteint du virus du SIDA ou d’une hépatite virale chronique, si vous souffrez de mucoviscidose (maladie génétique et héréditaire caractérisée notamment par des infections respiratoires graves), ou encore si vous êtes atteint de la maladie de Gilbert (maladie héréditaire associée à une augmentation du taux de bilirubine dans le sang).
EN CAS DE DOUTE, DEMANDEZ CONSEIL A VOTRE MEDECIN OU A VOTRE PHARMACIEN.
Mode et voie d'administration
Ce médicament est utilisé par voie rectale.
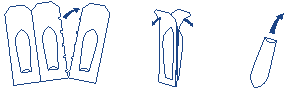
|
Détacher un suppositoire selon les pointillés |
Écarter les 2 bords pour ouvrir |
Sens d’introduction du suppositoire (le bout plat en premier pour éviter son rejet) |
Fréquence d'administration
Des prises régulières permettent d’éviter que la douleur ou la fièvre ne revienne : voir rubrique « Posologie ».
Chez l'enfant, les prises doivent être régulièrement espacées, y compris la nuit, de préférence de 6 heures, et d'au moins 4 heures.
Chez l'adulte, les prises doivent être espacées de 4 heures minimum.
En cas de maladie grave des reins (insuffisance rénale sévère), vous devez attendre au moins 8 heures entre chaque prise.
Si vous avez l'impression que l'effet de DOLIPRANE est trop fort ou trop faible, consultez votre médecin ou votre pharmacien.
Durée du traitement
Sauf avis médical, la durée du traitement est limitée :
· à 5 jours en cas de douleurs,
· à 3 jours en cas de fièvre
Si la douleur persiste plus de 5 jours ou la fièvre plus de 3 jours, si elles s'aggravent, ne pas continuer le traitement sans l'avis de votre médecin.
Si vous avez utilisé plus de DOLIPRANE ADULTES 1000 mg, suppositoire que vous n’auriez dû
Consultez immédiatement votre médecin ou votre pharmacien ou les urgences médicales.
Le surdosage peut être à l’origine d’une maladie du foie (insuffisance hépatique), d’un saignement gastro-intestinal, d’une maladie du cerveau (encéphalopathie), d’un coma, voire d’un décès, et notamment chez les populations plus à risque telles que les jeunes enfants, les personnes âgées et dans certaines situations (maladie du foie, alcoolisme, malnutrition chronique, ainsi que chez les patients traités de façon concomitante par des médicaments inducteurs enzymatiques). Dans les 24 premières heures, les principaux symptômes d’intoxication sont : nausées, vomissements, perte d’appétit, douleurs abdominales, pâleur.
Le surdosage peut également entrainer : une atteinte du pancréas (pancréatite), une hyperamylasémie (augmentation du taux d’amylase dans le sang), une maladie des reins (insuffisance rénale aiguë), et un problème de sang dans lequel les globules rouges, les globules blancs et les plaquettes sont tous réduits en nombre ce qui entraine :
· une fatigue, un souffle court et une pâleur ;
· des infections fréquentes accompagnées de fièvre et de frissons importants, des maux de gorge ou des ulcères de la bouche ;
· une tendance à saigner ou à présenter des ecchymoses spontanées, des saignements de nez.
De rare cas de formation de caillots sanguins (coagulation intravasculaire disséminée) ont été observés dans le contexte d’un surdosage au paracetamol
Si vous oubliez d’utiliser DOLIPRANE ADULTES 1000 mg, suppositoire
Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre.
Si vous arrêtez d’utiliser DOLIPRANE ADULTES 1000 mg, suppositoire
Sans objet.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
· Rarement, une réaction allergique peut survenir :
o boutons et/ou des rougeurs sur la peau,
o urticaire,
o brusque gonflement du visage et du cou pouvant entrainer une difficulté à respirer (œdème de Quincke),
o malaise brutal avec baisse importante de la pression artérielle (choc anaphylactique).
Si une allergie survient, vous devez immédiatement arrêter d’utiliser ce médicament et consulter rapidement votre médecin. À l’avenir, vous ne devrez plus jamais prendre de médicaments contenant du paracétamol.
· De très rares cas d’effets indésirables cutanés graves ont été rapportés.
· Exceptionnellement, ce médicament peut diminuer le nombre de certaines cellules du sang : globules blancs (leucopénie, neutropénie), plaquettes (thrombopénie) pouvant se manifester par des saignements du nez ou des gencives. Dans ce cas, consultez un médecin.
· Autres effets indésirables possibles (dont la fréquence ne peut être estimée sur la base de données disponibles) : troubles du fonctionnement du foie, affection grave qui peut rendre le sang et les fluides corporels plus acides (appelée acidose métabolique) chez les patients atteints d’une maladie grave et utilisant du paracétamol (voir rubrique 2), diminution importante de certains globules blancs pouvant provoquer des infections graves (agranulocytose), destruction des globules rouges dans le sang (anémie hémolytique chez les patients présentant un déficit en glucose‑6‑phosphate‑deshydrogénase), éruption cutanée en plaques rouges arrondies avec démangeaison et sensation de brûlure, laissant des tâches colorées et pouvant apparaître aux mêmes endroits en cas de reprise du médicament (érythème pigmenté fixe), difficulté à respirer (bronchospasme). Dans ce cas, arrêtez le traitement et consultez un médecin.
· Avec la forme suppositoire, il y a un risque d’irritation rectale ou anale (voir la rubrique « Faites attention avec Doliprane »).
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez‑en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance ‑ Site internet : https://signalement.social-sante.gouv.fr/
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER DOLIPRANE ADULTES 1000 mg, suppositoire ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur la boite.
A conserver à l’abri de la chaleur.
Ne jetez aucun médicament au tout‑à‑l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient DOLIPRANE ADULTES 1000 mg, suppositoire
· La substance active est :
Paracétamol................................................................................................................. 1000 mg
Pour un suppositoire.
· Les autres composants sont : glycérides hémi‑synthétiques solides.
Qu’est-ce que DOLIPRANE ADULTES 1000 mg, suppositoire et contenu de l’emballage extérieur
Ce médicament se présente sous forme de suppositoire. Chaque boîte contient 8 suppositoires.
Titulaire de l’autorisation de mise sur le marché
157 AVENUE CHARLES DE GAULLE
92200 NEUILLY-SUR-SEINE
FRANCE
Exploitant de l’autorisation de mise sur le marché
OPELLA HEALTHCARE FRANCE SAS
157 AVENUE CHARLES DE GAULLE
92200 NEUILLY-SUR-SEINE
FRANCE
OPELLA HEALTHCARE INTERNATIONAL SAS
1360 RUE EDOUARD BRANLY
14100 LISIEUX
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
Conseil d’éducation sanitaire :
QUE FAIRE EN CAS DE FIEVRE :
La température normale du corps est variable d’une personne à l’autre et comprise entre 36,5°C et 37,5°C. Une élévation au‑delà de 38°C est considérée comme une fièvre, mais il est déconseillé de traiter la fièvre avec un médicament en dessous de 38,5°C.
Ce médicament est destiné à l’adulte et l’enfant à partir de 50 kg (soit à partir d’environ 15 ans).
Si les troubles que la fièvre entraîne sont trop gênants, vous pouvez prendre ce médicament qui contient du paracétamol en respectant les doses indiquées.
Pour éviter tout risque de déshydratation, pensez à boire fréquemment.
Avec ce médicament, la fièvre doit baisser rapidement, néanmoins :
· si d’autres signes apparaissent,
· si la fièvre persiste plus de 3 jours ou si elle s’aggrave,
· si les maux de tête deviennent violents, ou en cas de vomissements,
CONSULTEZ IMMEDIATEMENT VOTRE MEDECIN.
QUE FAIRE EN CAS DE DOULEUR :
L'intensité de la perception de la douleur et la capacité à lui résister varient d'une personne à l'autre.
· S'il n'y a pas d’amélioration au bout de 5 jours de traitement,
· si la douleur est violente, inattendue et survient de façon brutale (notamment une douleur forte dans la poitrine) et/ou au contraire revient régulièrement,
· si elle s’accompagne d'autres signes comme un état de malaise général, de fièvre, un gonflement inhabituel de la zone douloureuse, une diminution de la force dans un membre,
· si elle vous réveille la nuit,
CONSULTEZ IMMEDIATEMENT VOTRE MEDECIN.