Dernière mise à jour le 30/03/2026
NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée
Présentations
> 1 crayon polyéthylène basse densité (PEBD) avec bâton pour application cutanée
Code CIP : 34009 302 509 9 0
Déclaration de commercialisation : 28/08/2024
Cette présentation n'est pas agréée aux collectivités
Service médical rendu (SMR)
Pas de SMR disponible pour ce médicament ( plus d'informations dans l'aide )
Amélioration du service médical rendu (ASMR)
Pas d'ASMR disponible pour ce médicament (plus d'informations dans l'aide )
ANSM - Mis à jour le : 17/06/2022
NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Nitrate d’argent...................................................................................................................... 63,3 g
Pour 100 g de bâton pour application cutanée
Pour la liste complète des excipients, voir rubrique 6.1.
Bâton pour application cutanée
4.1. Indications thérapeutiques
NITRATE D’ARGENT COOPER 63,3 % est indiqué dans le traitement local des bourgeons charnus.
4.2. Posologie et mode d'administration
USAGE EXTERNE EXCLUSIVEMENT – MEDICAMENT DESTINE A UN SEUL PATIENT.
Ce médicament doit être utilisé sous contrôle d’un professionnel de santé.
L’utilisation en pédiatrie est réservée au personnel médical.
L’application doit se limiter strictement à la zone à traiter.
Le temps d’application est de 1 minute maximum.
La fréquence d'application est de 1 à 3 applications espacées d'au moins 24 h.
Un même crayon peut servir pour le traitement d’un patient pendant maximum 3 jours de traitement.
Mode d’administration
Voie cutanée.
Précautions à prendre avant l’administration du médicament
Avant utilisation, s’assurer que la mine n’est pas fêlée ou cassée en secouant légèrement le crayon. Ne pas utiliser un crayon qui est tombé du fait du risque de fêlure de la mine.
Pour tout soin d’un bourgeon charnu au pourtour d’un orifice (trachée, oreille ), le patient doit être en position assise afin d’effectuer le soin dans les meilleures conditions de sécurité.
· Enlever le capuchon et tenir le crayon uniquement avec les parties plastiques, ne pas toucher la mine avec les doigts.
· Humecter la mine avec une goutte d’eau (ne pas utiliser de solution saline). Pour ce faire, déposer la goutte d’eau sur un verre renversé propre, puis plonger la mine dans la goutte d’eau. Ne jamais utiliser la langue pour humecter la mine. Ne pas mettre directement le crayon sous l’eau du robinet.
· Maintenir le crayon horizontalement au-dessus d’un mouchoir jetable pour protéger la peau saine, les surfaces et éviter l’entrée d’eau dans le crayon.
· Appliquer la mine humidifiée du crayon perpendiculairement à la zone à traiter conformément au schéma ci-dessous, en prenant soin de ne pas déborder sur les tissus sains.
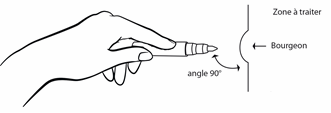
· Assurez-vous que l’eau couvre toute la zone à traiter et laisser sécher.
· Ne pas appliquer une pression trop forte sur la zone à traiter et ne pas exercer un effet levier pour éviter que la mine ne se casse.
· En cas de rupture de la mine, assurez-vous que tous les morceaux sont récupérés. Envelopper les morceaux de la mine dans un mouchoir en papier sec et les mettre à la poubelle.
· Bien essuyer la mine après utilisation à l’aide d’un mouchoir en papier propre que vous jetterez immédiatement à la poubelle.
· Remettre le capuchon pour protéger la mine.
Pour les instructions concernant la manipulation du médicament, voir la rubrique 6.6.
Hypersensibilité connue au nitrate d’argent ou au nitrate de potassium.
Ne pas appliquer sur les muqueuses.
4.4. Mises en garde spéciales et précautions d'emploi
Mises en garde spéciales :
Ce médicament doit être utilisé sous contrôle d’un professionnel de santé.
L’utilisation en pédiatrie est réservée au personnel médical.
Ne pas appliquer près des yeux, sur les muqueuses (génitales, buccale, nasale), et la peau saine en raison de l’action corrosive de ce médicament.
Ce médicament peut provoquer des brûlures de la peau et entraîner un risque de perforation des muqueuses. Il doit être manipulé avec précaution.
Précautions d'emploi :
Ne pas déborder sur les tissus sains. Protéger la peau saine située sur le pourtour du site d’application par exemple avec de la vaseline.
L’eau qui a touché la mine peut tacher la plupart des surfaces, y compris la peau saine, le mobilier et les vêtements. Utiliser un mouchoir en papier propre et sec pour protéger les surfaces et recueillir l’eau qui peut tomber de la mine.
La mine du crayon est fragile, manipuler le crayon avec précaution.
Ne pas appliquer une pression trop forte sur la zone à traiter et ne pas exercer un effet levier pour éviter que la mine ne se casse (voir rubrique 6.6).
La rupture de la mine peut être à l’origine d’effets indésirables graves (nécrose pulmonaire) lors de l’utilisation du produit chez les patients trachéotomisés ou trachéostomisés (risque de chute de la mine dans la trachée).
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Aucune étude d’interaction n’a été réalisée.
4.6. Fertilité, grossesse et allaitement
Grossesse
Il n’existe pas de données sur l’utilisation du nitrate d’argent chez la femme enceinte. Les effets du nitrate d’argent sur la fertilité, la reproduction et le développement fœtal n’ont pas été évalués de façon satisfaisante chez l'animal. Cependant le passage transcutané du nitrate d’argent dans la circulation systémique est très limité (voir section 5.3).
NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée ne doit être utilisé qu’après avis médical chez la femme enceinte.
Allaitement
L’excrétion dans le lait maternel du nitrate d’argent n’est pas connue. Aucun effet indésirable n’est prévisible chez le nourrisson ou l’enfant allaité puisque l’exposition systémique de la mère allaitante au nitrate d’argent est négligeable. Le nitrate d’argent peut être utilisé pendant l’allaitement.
Fertilité
Les effets sur la fertilité n'ont pas été évalués.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Les effets indésirables de NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée sont listés ci-dessous selon la base de données MedDRA et par Classes de Systèmes d’Organes et par fréquence. Les fréquences sont définies en utilisant la classification suivante : Très fréquent (≥ 1/10) ; fréquent (≥ 1/100 ; < 1/10) ; peu fréquent (≥ 1/1 000 ; < 1/100) ; rare (≥ 1/10 000 ; < 1/1 000), très rare (< 1/10 000), indéterminée (ne peut être estimée sur la base des données disponibles).
|
SOC (MedDRA) |
Fréquence |
Effet indésirable |
|
Troubles du système immunitaire |
Indéterminée |
Réactions d’hypersensibilité, Réactions cutanées localisées. |
|
Affections de la peau et du tissu sous-cutané |
Indéterminée |
Taches cutanées (brunes à noires)*. Décoloration cutanée |
|
Troubles généraux et anomalies au site d’administration |
Indéterminée |
Brûlure de la peau saine non protégée autour du site d’application |
|
Affections respiratoires, thoraciques et médiastinales |
Indéterminée |
Nécrose pulmonaire, toux sévère |
|
Problèmes de produit |
indéterminée |
Rupture du dispositif |
* L’application chronique du nitrate d’argent sur les tissus conjonctifs ou sur les plaies ouvertes peut provoquer une affection nommée argyrie. Il s’agit d’une accumulation de l’argent métal ou de ses composés dans les tissus conjonctifs, qui donne lieu à une coloration noire bleutée locale ou générale. La coloration peut persister indéfiniment ou ne disparaître que très lentement. Les cas d’argyrie se présentent dans des situations exceptionnelles au cours d’un usage prolongé de nitrate d’argent.
La coloration au site d’application est une conséquence de l’application du produit et ne peut être évitée.
Les taches sur la peau saine disparaissent habituellement en quelques jours.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr
Des quantités excessives, ou l'utilisation incorrecte de ce médicament lors de l’application en topique, peuvent donner lieu à des cas de brûlures ou de coloration de la peau.
En cas de contact avec les yeux, il faut laver immédiatement et abondamment avec de l’eau. Si possible, enlevez les lentilles de contact et demandez un avis de spécialiste.
En cas d’intoxication accidentelle par ingestion, les symptômes sont liés à la nature corrosive du nitrate d'argent. Il peut apparaitre des douleurs dans la bouche, sialorrhée, diarrhée, nausées, vomissements, coma ou des convulsions.
Le traitement de l'empoisonnement accidentel ou intentionnel par ingestion doit être entrepris sans délai.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : DERIVES ARGENTIQUES, code ATC : D08AL01
Ce médicament agit comme agent caustique, utilisé comme cautérisant chimique.
Aucune étude clinique n’a été réalisée avec le bâton au nitrate d’argent à la concentration de 63,3%.
5.2. Propriétés pharmacocinétiques
Aucune étude pharmacocinétique n’a été réalisée avec le bâton au nitrate d’argent à la concentration de 63 ,3%.
5.3. Données de sécurité préclinique
Etant donné que le passage transcutané du nitrate d’argent est très faible après application sur la peau et que la durée du traitement recommandée est courte, aucun effet indésirable systémique n’est attendu après application sur la peau de NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée.
In vitro, testé sur bactéries (test d’Ames), l’argent n’est pas mutagène. Testé sur cellules de mammifère, l’argent est génotoxique et produit des cassures de l’ADN par un mécanisme mal connu et probablement lié à ses propriétés pharmacologiques.
Le potentiel cancérigène du nitrate d’argent après application sur la peau n’a pas été évalué chez l’animal. Sur la base des données disponibles, l’argent n’est pas classé comme cancérigène pour l’homme. De plus, la durée du traitement avec NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée étant très court, le risque cancérigène lié à l’application de ce produit est négligeable.
Les effets du nitrate d’argent sur la fertilité, la reproduction et le développement fœtal n'ont pas été évalués de façon satisfaisante chez l’animal.
Le nitrate d’argent ne modifie pas la fertilité du rat mâle après administration orale chronique.
Administré par voie systémique pendant la gestation chez la souris, l’argent ne s’accumule pas dans les tissus de l’embryon ou du fœtus. Chez le rat après administration de nanoparticules d’argent pendant toute la gestation et le début de la lactation, aucun effet indésirable sur l’ensemble des paramètres de la reproduction n’a été mis en évidence. Les données disponibles suggèrent que l’argent passe la barrière placentaire.
L’excrétion du nitrate d’argent dans le lait maternel n’est pas connue. L'exposition systémique de la femme allaitante au nitrate d’argent étant très limitée après application topique, le passage dans le lait maternel peut être considéré comme très faible et aucun effet indésirable chez le nourrisson/enfant allaité n’est attendu.
Le nitrate d’argent à forte concentration est irritant et corrosif pour la peau et les yeux.
Le nitrate d’argent colore la peau après application topique.
Le nitrate d’argent peut causer de la sensibilisation cutanée et des réactions allergiques.
Les utilisations proposées du nitrate d'argent par les patients ne devraient pas présenter de risque significatif pour l’environnement.
Ne pas utiliser en présence de solutions salines.
3 ans.
6.4. Précautions particulières de conservation
A conserver à une température ne dépassant pas 25°C.
Conserver le crayon soigneusement fermé à l’abri de la lumière et de l’humidité.
La mine blanche noircit à la lumière, cela n’affecte en rien ses propriétés.
6.5. Nature et contenu de l'emballage extérieur
Bâton pour application cutanée, constitué d’une mine montée sur un support en polyéthylène basse densité bleu fermé par un capuchon en polyéthylène basse densité bleu.
Boîte de 1.
6.6. Précautions particulières d’élimination et de manipulation
Ce médicament est destiné au traitement d’un seul patient.
Instructions de manipulation :
Le crayon est composé d’un support en plastique sur lequel est fixée une mine (bâton) recouverte par un capuchon.
Avant utilisation, s’assurer que la mine n’est pas fêlée ou cassée en secouant légèrement le crayon. Ne pas utiliser un crayon qui est tombé du fait du risque de fêlure de la mine.
· Enlever le capuchon
· Tenir le crayon uniquement avec les parties plastiques, ne pas toucher la mine avec les doigts.
· Protéger la peau saine située sur le pourtour du site d’application par exemple avec de la vaseline.
· Humecter la mine avec une goutte d’eau (ne pas utiliser de solution saline). Pour ce faire, déposer la goutte d’eau sur un verre renversé propre, puis plonger la mine dans la goutte d’eau. Ne jamais utiliser la langue pour humecter la mine. Ne pas mettre directement le crayon sous l’eau du robinet.
· Maintenir le crayon horizontalement au-dessus d’un mouchoir en papier propre pour protéger la peau saine, les surfaces et éviter l’entrée d’eau dans le crayon.
· Appliquer la mine humidifiée perpendiculairement à la zone à traiter en prenant soin de ne pas laisser d’eau de la mine toucher quoi que ce soit d’autre. Assurez-vous que l’eau couvre toute la zone à traiter et laisser sécher. Ne pas déborder sur les tissus sains.
· Ne pas appliquer une pression trop forte sur la zone à traiter et ne pas exercer un effet levier pour éviter que la mine ne se casse.
· L’eau qui a touché la mine peut tacher la plupart des surfaces, y compris la peau saine, le mobilier et les vêtements. Utiliser un mouchoir en papier propre et sec pour protéger les surfaces et recueillir l’eau qui peut tomber de la mine.
· En cas de rupture de la mine, assurez-vous que tous les morceaux sont récupérés. Envelopper les morceaux de la mine dans un mouchoir en papier sec et les mettre à la poubelle.
· Bien essuyer la mine après utilisation à l’aide d’un mouchoir en papier propre que vous jetterez immédiatement à la poubelle.
· Remettre le capuchon pour protéger la mine.
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
COOPERATION PHARMACEUTIQUE FRANCAISE
PLACE LUCIEN AUVERT
77020 MELUN CEDEX
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 302 509 9 0 : Bâton pour application cutanée ; boîte de 1
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I
ANSM - Mis à jour le : 17/06/2022
NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée
Nitrate d’argent
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que NITRATE D’ARGENTCOOPER 63,3 %, bâton pour application cutanée et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée ?
3. Comment utiliser NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : DERIVES ARGENTIQUES - code ATC : D08AL01
Ce médicament est préconisé dans le traitement local des bourgeons charnus.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée ?
N’utilisez jamais NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée :
· si vous êtes allergique (hypersensible) au nitrate d’argent ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
· sur les muqueuses (bouche, muqueuses génitales, nez )
Avertissements et précautions
Adressez-vous à votre médecin ou votre infirmier/ère avant d’utiliser NITRATE D’ARGENT COOPER 63,3 %.
Ce médicament peut provoquer des brûlures de la peau et entrainer un risque de perforation des muqueuses. Il doit être manipulé avec précaution.
Ce médicament doit être utilisé sous contrôle d’un professionnel de santé.
Ne pas ingérer. En cas d’ingestion accidentelle, consultez immédiatement un médecin ou allez aux urgences d’un hôpital et montrez l’étui et la notice.
Ne pas appliquer près des yeux. En cas de contact avec les yeux, lavez-les immédiatement et abondamment avec de l’eau. Enlevez les lentilles de contact si vous en portez et si elles peuvent être facilement retirées. Continuez à rincer puis consultez un spécialiste.
Une coloration noire ou brune à l’endroit où a été appliqué le crayon est normale.
Si la mine du crayon au nitrate d’argent est accidentellement en contact avec la peau saine environnante, il peut causer des taches, des brûlures ou une décoloration de la peau.
Appliquer une couche de vaseline sur la peau autour de la zone à traiter pour la protéger de tout contact accidentel avec le produit.
Précautions d’emploi
La mine du crayon est fragile, manipulez le crayon avec précaution.
Ne pas appuyer trop fort et appliquer le crayon perpendiculairement à la zone à traiter pour éviter que la mine ne se casse. Voir le chapitre 3 pour les instructions de manipulation.
La rupture de la mine peut être à l’origine d’effets indésirables graves (nécrose pulmonaire) lors de l’utilisation du produit chez les patients trachéotomisés ou trachéostomisés (risque de chute de la mine dans la trachée).
Enfants et adolescents
L’utilisation en pédiatrie est réservée au personnel médical.
Autres médicaments et NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée
Informez votre médecin ou votre pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée avec des aliments, des boissons et de l’alcool
Sans objet.
Ce médicament ne doit être utilisé qu’après avis médical pendant la grossesse et l'allaitement.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou à votre pharmacien avant d’utiliser ce médicament.
Conduite de véhicules et utilisation de machines
Sans objet.
NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée contient
Sans objet.
3. COMMENT UTILISER NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée ?
Veillez à toujours utiliser ce médicament en suivant exactement les indications de votre médecin ou de votre pharmacien. Vérifiez auprès de votre médecin ou de votre pharmacien en cas de doute.
USAGE EXTERNE EXCLUSIVEMENT – MEDICAMENT DESTINE A UN SEUL PATIENT
Posologie
Appliquer une couche de vaseline sur la peau autour du bourgeon charnu pour la protéger du contact avec le produit.
1 application strictement limitée à la zone à traiter pendant maximum 1 minute par jour pendant 1 à 3 jours.
Le crayon est composé d’un support en plastique sur lequel est fixée une mine recouverte par un capuchon.
Pour tout soin d’un bourgeon charnu au pourtour d’un orifice (trachée, oreille ), le patient doit être en position assise afin d’effectuer le soin dans les meilleures conditions de sécurité.
· Enlever le capuchon
· Tenir le crayon uniquement avec les parties plastiques, ne pas toucher la mine avec les doigts.
· Avant utilisation, protéger la peau saine autour du site d’application avec de la vaseline.
· Avant utilisation, secouer légèrement le crayon pour s’assurer que la mine n’est pas fêlée ou cassée. Ne pas utiliser un crayon qui est tombé du fait du risque de fêlure de la mine. Eliminer tous les morceaux cassés de la mine avec des pincettes, un essuie-tout ou un mouchoir en papier sec pour éviter le contact avec la peau.
· Humecter la mine avec une goutte d’eau (ne pas utiliser de solution saline). Pour ce faire, déposer la goutte d’eau sur un verre renversé propre, puis plonger la mine dans la goutte d’eau. Ne jamais utiliser la langue pour humecter la mine. Ne pas mettre directement le crayon sous l’eau du robinet.
· Maintenir le crayon horizontalement au-dessus d’un mouchoir jetable pour protéger la peau saine, les surfaces et éviter l’entrée d’eau dans le crayon.
· Appliquer la mine du crayon perpendiculairement à la zone à traiter conformément au schéma ci-dessous et sans exercer de pression, en prenant soin de ne pas déborder sur les tissus sains.
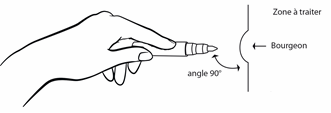
· Prendre soin de ne pas laisser d’eau de la mine toucher quoi que ce soit d’autre. Assurez-vous que l’eau couvre toute la zone à traiter et laisser sécher.
· L’eau qui a touché la mine peut tacher la plupart des surfaces, y compris la peau saine, le mobilier et les vêtements. Utilisez un mouchoir en papier propre et sec pour protéger les surfaces et recueillir l’eau qui peut tomber de la mine.
· En cas de rupture de la mine, assurez-vous que tous les morceaux sont récupérés. Envelopper les morceaux de la mine du crayon dans un mouchoir en papier sec et les mettre à la poubelle.
· Bien essuyer la mine après utilisation à l’aide d’un mouchoir en papier propre que vous jetterez immédiatement à la poubelle.
· Remettre le capuchon pour protéger la mine.
L’utilisation en pédiatrie est réservée au personnel médical.
Si vous avez utilisé plus de NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée que vous n’auriez dû
Consultez immédiatement votre médecin ou votre pharmacien.
Si vous oubliez d’utiliser NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée
Ne prenez pas de dose double pour compenser l’application que vous avez oubliée de faire.
Si vous arrêtez d’utiliser NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée
Sans objet.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Effets indésirables rapportés au cours de l’utilisation de ce médicament pour lesquels la fréquence est indéterminée :
· Possibles réactions allergiques à l’un des composants, et en particulier des réactions cutanées locales.
· Brûlure de la peau saine non protégée autour du site d’application.
· Taches (brunes à noires) de la peau
· Décoloration de la peau
· Toux sévère, nécrose pulmonaire
· Rupture du dispositif
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: https://signalement.social-sante.gouv.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur le conditionnement extérieur après EXP. La date de péremption fait référence au dernier jour de ce mois.
A conserver à une température ne dépassant pas 25°C.
Conserver le crayon soigneusement fermé à l’abri de la lumière et de l’humidité.
La mine blanche noircit à la lumière, cela n’affecte en rien ses propriétés.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient NITRATE D’ARGENT COOPER 63,3 %, bâton pour application cutanée
· La substance active est :
Nitrate d’argent................................................................................................................. 63,3 g
pour 100 g de bâton pour application cutanée
· L’autre composant est : Nitrate de potassium.
Ce médicament se présente sous forme d’un bâton pour application cutanée.
Boîte de 1 bâton.
Titulaire de l’autorisation de mise sur le marché
COOPERATION PHARMACEUTIQUE FRANCAISE
PLACE LUCIEN AUVERT
77020 MELUN CEDEX
Exploitant de l’autorisation de mise sur le marché
COOPERATION PHARMACEUTIQUE FRANCAISE
PLACE LUCIEN AUVERT
77020 MELUN CEDEX
COOPERATION PHARMACEUTIQUE FRANCAISE
PLACE LUCIEN AUVERT
77020 MELUN CEDEX
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Sans objet.
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).