Dernière mise à jour le 02/03/2026
BRIMONIDINE/TIMOLOL BIOGARAN 2 mg/mL + 5 mg/mL, collyre en solution
Indications thérapeutiques
Classe pharmacothérapeutique - code ATC : S01ED51
BRIMONIDINE/TIMOLOL BIOGARAN est un collyre antiglaucomateux. Il contient deux substances actives différentes (la brimonidine et le timolol) qui diminuent la pression élevée dans l’œil. La brimonidine appartient au groupe de médicaments appelés agonistes des récepteurs alpha2-adrénergiques. Le timolol appartient au groupe de médicaments appelés bêta-bloquants.
BRIMONIDINE/TIMOLOL BIOGARAN est prescrit pour abaisser la pression intraoculaire quand l’effet produit par un collyre contenant uniquement un bêta-bloquant n’est pas suffisant.
Votre œil contient un liquide aqueux limpide qui nourrit l'intérieur de l'œil. Ce liquide est constamment évacué de l'œil et un nouveau liquide est produit pour le remplacer. Si le liquide ne peut pas être évacué suffisamment vite, la pression intraoculaire augmente, ce qui risque d'endommager la vue. BRIMONIDINE/TIMOLOL BIOGARAN agit en réduisant la production de liquide et également en augmentant la quantité de liquide évacué. Cela diminue la pression à l’intérieur de l’œil.
Présentations
> 1 flacon(s) polyéthylène basse densité (PEBD) compte-gouttes (incorporé) de 5 ml
Code CIP : 34009 302 558 3 4
Déclaration de commercialisation : 01/02/2023
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 5,54 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 6,56 €
- Taux de remboursement :65 %
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 14/09/2022 | Inscription (CT) | Le service médical rendu par BRIMONIDINE/TIMOLOL BIOGARAN (brimonidine/timolol) 2 mg/ml + 5 mg/ml, collyre en solution, est important dans l’indication de l’AMM. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 14/09/2022 | Inscription (CT) | BRIMONIDINE/TIMOLOL BIOGARAN (brimonidine/timolol) 2 mg/ml + 5 mg/ml, collyre en solution est un hybride qui n’apporte pas d’amélioration du service médical rendu (ASMR V) par rapport à la spécialité de référence COMBIGAN (brimonidine/timolol) 2 mg/ml + 5 mg/ml, collyre en solution. |
ANSM - Mis à jour le : 04/07/2022
BRIMONIDINE/TIMOLOL BIOGARAN 2 mg/mL + 5 mg/mL, collyre en solution
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
sous forme de 2,0 mg de tartrate de brimonidine
Timolol................................................................................................................................. 5,0 mg
sous forme de 6,8 mg de maléate de timolol
Pour 1 mL de collyre en solution.
Excipients à effet notoire : chlorure de benzalkonium, phosphates.
Pour la liste complète des excipients, voir rubrique 6.1.
Collyre en solution.
Solution limpide, jaune-verdâtre.
4.1. Indications thérapeutiques
4.2. Posologie et mode d'administration
Posologie recommandée chez les adultes (y compris chez les patients âgés)
La dose recommandée est d'une goutte de BRIMONIDINE/TIMOLOL BIOGARAN dans l'œil ou les yeux affectés deux fois par jour, les instillations devant être effectuées à 12 heures d'intervalle environ.
Utilisation chez les insuffisants rénaux ou hépatiques
BRIMONIDINE/TIMOLOL BIOGARAN n'a pas été étudié chez les patients atteints d'insuffisance rénale ou d'insuffisance hépatique. En conséquence, il doit être utilisé avec précaution chez ces patients.
Population pédiatrique
BRIMONIDINE/TIMOLOL BIOGARAN est contre-indiqué chez les nouveau-nés et les nourrissons (moins de 2 ans) (voir rubriques 4.3; 4.4; 4.8 et 4.9).
La sécurité et l'efficacité de BRIMONIDINE/TIMOLOL BIOGARAN n'ont pas été établies chez les enfants et les adolescents (2 à 17 ans), son utilisation est donc déconseillée chez ces patients (voir rubriques 4.4, 4.8 et 4.9).
Mode d’administration
Comme c'est le cas avec tous les collyres, afin de réduire une possible absorption systémique, il est recommandé de comprimer le sac lacrymal au niveau du canthus interne (point d'occlusion) ou de fermer les paupières pendant deux minutes. Ceci doit être fait immédiatement après l'instillation de chaque goutte. Cette pratique vise à minimiser les effets secondaires systémiques et à favoriser l'action locale du collyre.
Afin de prévenir une contamination de l’œil ou de la solution, éviter tout contact de l'embout avec une autre surface.
En cas d'utilisation concomitante de plusieurs médicaments ophtalmiques à usage local, chacun doit être administré à un intervalle d'au moins 5 minutes.
· Hypersensibilité aux substances actives ou à l’un des excipients mentionnés à la rubrique 6.1.
· Hyperréactivité des bronches y compris asthme bronchique ou antécédents d'asthme bronchique, broncho-pneumopathie chronique obstructive grave.
· Bradycardie sinusale, syndrome de dysfonctionnement sinusal, bloc sino-auriculaire, bloc auriculo-ventriculaire du deuxième ou troisième degré non contrôlé par un stimulateur cardiaque, insuffisance cardiaque manifeste, choc cardiogénique.
· Utilisation chez les nouveau-nés et les nourrissons (moins de 2 ans) (voir rubrique 4.8).
· Patients prenant un inhibiteur de la monoamine oxydase (IMAO).
· Patients prenant des antidépresseurs qui affectent la transmission noradrénergique (antidépresseurs tricycliques et miansérine par exemple).
4.4. Mises en garde spéciales et précautions d'emploi
Lors des essais cliniques, quelques patients ont présenté des réactions de type allergique oculaire avec l’association brimonidine/timolol (conjonctivite allergique et blépharite allergique). Une conjonctivite allergique a été observée chez 5,2% des patients. Sa survenue se situait en général entre le 3ème et le 9ème mois et entraînait un arrêt du traitement dans 3,1% des cas. Une blépharite allergique a été peu fréquemment rapportée (<1%). En cas de réaction allergique, le traitement par BRIMONIDINE/TIMOLOL BIOGARAN doit être interrompu.
Des réactions oculaires d’hypersensibilité retardée ont été rapportées lors de l’utilisation d’une solution ophtalmique de tartrate de brimonidine à 0,2%, certaines étant associées à une augmentation de la PIO.
L’association brimonidine/timolol n’a pas été étudiée chez patients atteints de glaucome à angle fermé.
Effets systémiques
Comme d’autres agents ophtalmiques à usage local, une absorption systémique de BRIMONIDINE/TIMOLOL BIOGARAN est possible. Aucune augmentation de l’absorption systémique de chacune des substances actives n’a été observée. En raison de la présence d'un composant bêta-adrénergique, le timolol, des effets indésirables cardiovasculaires, pulmonaires et autres effets indésirables similaires à ceux rapportés avec les bêta-bloquants par voie générale, sont susceptibles de se produire. L’incidence des effets indésirables systémiques après une administration ophtalmique topique est plus faible qu’après une administration systémique. Pour réduire l'absorption systémique, voir rubrique 4.2.
Troubles cardiaques
Après administration de timolol, des réactions cardiaques ont été rapportées, y compris, rarement, des décès associés à une insuffisance cardiaque. Les patients souffrant de maladies cardiovasculaires (par ex. maladie coronarienne, angor de Prinzmetal ou insuffisance cardiaque) et sous traitement hypotenseur par des bêta-bloquants doivent être évalués de manière approfondie, et un traitement par d'autres substances actives doit être envisagé. Les patients atteints de maladies cardiovasculaires doivent être surveillés afin de dépister tout signe d’altération de leur maladie et d’effets indésirables.
En raison de leur effet négatif sur le temps de conduction, les bêta-bloquants doivent être administrés avec précaution aux patients atteints de bloc cardiaque du premier degré.
Comme avec les bêta-bloquants par voie générale, un sevrage progressif s’impose si une interruption du traitement est requise chez des patients atteints d’une coronaropathie pour éviter le développement de troubles du rythme, un infarctus du myocarde ou une mort subite.
Troubles vasculaires
Il convient de traiter avec prudence les patients atteints de troubles/perturbations sévères de la circulation périphérique (i.e. les formes sévères de la maladie de Raynaud ou du syndrome de Raynaud).
Troubles respiratoires
Des réactions respiratoires, dont des décès dus à un bronchospasme chez des patients asthmatiques, ont été rapportées après l’administration de certains bêta-bloquants ophtalmiques.
BRIMONIDINE/TIMOLOL BIOGARAN doit être utilisé avec prudence chez les patients atteints de broncho-pneumopathie chronique obstructive (BPCO) légère/modérée et uniquement si le bénéfice potentiel l’emporte sur le risque potentiel.
Hypoglycémie/diabète
Les inhibiteurs bêta-adrénergiques doivent être administrés avec prudence chez les patients ayant une tendance à l’hypoglycémie spontanée et chez les patients atteints de diabète instable, car les bêta-bloquants peuvent masquer les signes et symptômes d’hypoglycémie aiguë.
Hyperthyroïdisme
Les bêta-bloquants risquent également de masquer les signes d’hyperthyroïdie.
BRIMONIDINE/TIMOLOL BIOGARAN doit être utilisé avec précaution chez les patients atteints d'acidose métabolique et de phéochromocytome non traité.
Maladies de la cornée
Les bêta-bloquants ophtalmiques peuvent provoquer une sécheresse oculaire. Les patients atteints de maladies de la cornée doivent être traités avec prudence.
Autres agents bêta-bloquants
L'effet sur la pression intraoculaire ou les effets connus du blocage bêta-adrénergique systémique peuvent être potentialisés lorsque le timolol est administré à des patients recevant déjà un agent bêta-bloquant systémique. La réponse de ces patients doit être étroitement surveillée. L'utilisation de deux bêta-bloquants à usage topique n'est pas recommandée (voir rubrique 4.5).
Réactions anaphylactiques
Durant un traitement par des bêta-bloquants, les patients qui ont des antécédents d’atopie ou de réaction anaphylactique grave à divers allergènes peuvent se montrer plus sensibles aux expositions répétées à ces allergènes ou réfractaires à l’adrénaline aux doses habituellement utilisées pour le traitement des réactions anaphylactiques.
Décollements de la choroïde
Des décollements de la choroïde ont été décrits après administration de traitement suppresseur de la sécrétion de l’humeur aqueuse (par exemple : timolol, acétazolamide) suite à une intervention chirurgicale de filtration.
Anesthésie chirurgicale
Les préparations ophtalmologiques de bêta-bloquants peuvent bloquer les effets bêta-agonistes systémiques de l'adrénaline, par exemple. L'anesthésiste doit être informé que le patient suit un traitement par timolol.
Chlorure de benzalkonium
Le conservateur contenu dans BRIMONIDINE/TIMOLOL BIOGARAN, le chlorure de benzalkonium, peut entraîner une irritation oculaire, des symptômes de sécheresse oculaire et peut endommager le film lacrymal et la surface cornéenne en cas d’utilisation prolongée. Les porteurs de lentilles de contact doivent les retirer avant d’effectuer l’instillation et attendre 15 minutes au moins avant de les remettre. Le chlorure de benzalkonium est susceptible de décolorer les lentilles de contact souples. Ne pas utiliser en présence de lentilles souples.
BRIMONIDINE/TIMOLOL BIOGARAN doit être utilisé avec précautions chez les patients atteints de sécheresse oculaire et chez les patients dont l’état de la cornée peut être endommagé. Les patients doivent faire l’objet d’un suivi en cas d’utilisation prolongée.
Phosphate
BRIMONIDINE/TIMOLOL BIOGARAN contient du phosphate, qui peut entraîner dans de rares cas des taches opaques sur la cornée en raison d’une accumulation de calcium pendant le traitement.
Population pédiatrique
Les enfants de 2 ans ou plus, en particulier ceux âgés de 2 à 7 ans et/ou de poids inférieur ou égal à 20 kg, doivent être traités avec précaution et étroitement surveillés en raison de l'incidence élevée et de la sévérité de la somnolence. La sécurité et l'efficacité de l’association brimonidine/timolol chez les enfants et les adolescents (2 à 17 ans) n'ont pas été établies (voir rubriques 4.2 et 4.8).
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Aucune étude d'interaction n'a été menée avec l’association fixe brimonidine/timolol. Bien qu’aucune étude spécifique d’interactions médicamenteuses n’ait été conduite avec BRIMONIDINE/TIMOLOL BIOGARAN, la possibilité théorique d’observer un effet additif ou une potentialisation avec les dépresseurs du système nerveux central (alcool, barbituriques, opiacés, sédatifs ou anesthésiques) doit être prise en considération.
Des effets additifs ayant pour conséquence une hypotension et/ou une bradycardie marquée peuvent en théorie se produire quand une solution ophtalmique contenant un bêta-bloquants est administrée en association avec des inhibiteurs calciques, des bêta-bloquants adrénergiques, des antiarythmiques (incluant l’amiodarone), des glucosides digitaliques, des parasympathomimétiques ou la guanéthidine. De plus, une hypotension a été rapportée dans de très rares cas (<1 sur 10 000) après l’instillation de brimonidine. La prudence est donc recommandée quand BRIMONIDINE/TIMOLOL BIOGARAN est administré en association avec des antihypertenseurs par voie générale.
Des mydriases résultant de l'utilisation concomitante de bêta-bloquants ophtalmiques et d'adrénaline (épinéphrine) ont été occasionnellement rapportées.
Les bêta-bloquants sont susceptibles d’augmenter l’effet hypoglycémiant des antidiabétiques. Les bêta-bloquants peuvent en outre masquer les signes et symptômes d’hypoglycémie (voir rubrique 4.4).
L’hypertension induite par un arrêt brutal de la clonidine peut être potentialisée par la prise de bêta-bloquants.
Une potentialisation du blocage bêta-adrénergique systémique (par ex. une baisse de la fréquence cardiaque, dépression) a été décrite au cours d’un traitement associant des inhibiteurs du CYP2D6 (par exemple : quinidine, fluoxétine, paroxétine) et du timolol.
L’utilisation concomitante d’un bêta-bloquant et d’anesthésiques peut atténuer la tachycardie de compensation et augmenter le risque d’hypotension (voir rubrique 4.4) : par conséquent l'anesthésiste doit être informé que le patient est traité par BRIMONIDINE/TIMOLOL BIOGARAN.
Une surveillance doit être exercée en cas d’utilisation de BRIMONIDINE/TIMOLOL BIOGARAN avec des produits de contraste iodés ou lors d’une administration intraveineuse de lidocaïne.
La cimétidine, l’hydralazine et l’alcool peuvent augmenter les concentrations plasmatiques de timolol.
Aucune donnée n’est disponible sur les taux de catécholamines circulantes après administration de BRIMONIDINE/TIMOLOL BIOGARAN. La prudence est néanmoins recommandée chez les patients qui prennent des médicaments susceptibles de modifier le métabolisme et le captage des amines circulantes, par exemple la chlorpromazine, le méthylphénidate et la réserpine.
La prudence est conseillée lors de la mise en œuvre (ou du changement de la dose) d’un traitement concomitant par voie générale (indépendamment de la forme pharmaceutique) pouvant interagir avec les agonistes a-adrénergiques ou interférer sur leur activité, c’est à dire des agonistes ou antagonistes des récepteurs adrénergiques (par exemple : isoprénaline ou prazosine).
Bien qu’aucune étude spécifique d’interactions médicamenteuses n’ait été menée avec l’association brimonidine/timolol, il faut envisager la possibilité théorique d’un effet additif sur la baisse de la PIO avec les prostamides, les prostaglandines, les inhibiteurs de l’anhydrase carbonique et la pilocarpine.
La brimonidine est contre-indiquée chez les patients traités par inhibiteurs de la monoamine oxydase (MAO) et chez les patients sous antidépresseurs affectant la transmission noradrénergique (par exemple : antidépresseurs tricycliques et miansérine) (voir rubrique 4.3). Les patients qui ont reçu un traitement par IMAO devront respecter un délai de 14 jours avant de débuter un traitement avec BRIMONIDINE/TIMOLOL BIOGARAN.
4.6. Fertilité, grossesse et allaitement
Grossesse
Il n’y a pas de donnée pertinente concernant la sécurité d’utilisation de l’association fixe brimonidine/timolol chez la femme enceinte. BRIMONIDINE/TIMOLOL BIOGARAN ne doit pas être utilisé au cours de la grossesse à moins d’une nécessité absolue. Pour réduire l'absorption systémique, voir rubrique 4.2.
Tartrate de brimonidine
Il n’existe pas de données pertinentes sur l’utilisation du tartrate de brimonidine chez la femme enceinte. Les études chez l’animal ont mis en évidence une toxicité sur la reproduction à de fortes doses maternotoxiques (voir rubrique 5.3). Le risque potentiel pour l'homme n'est pas connu.
Timolol
Les études chez l'animal ont mis en évidence une toxicité sur la reproduction à des doses significativement supérieures à celles utilisées lors des pratiques cliniques (voir rubrique 5.3). Les études épidémiologiques n’ont pas mis en évidence de signe de malformation mais ont montré un risque de retard de croissance intra-utérin après une exposition à des bêta-bloquants par voie orale.
De plus, des signes et symptômes évocateurs d’un blocage bêta-adrénergique (par ex.: bradycardie, hypotension, détresse respiratoire et hypoglycémie) ont été observés chez le nouveau-né lorsque les bêta-bloquants étaient administrés avant l’accouchement. Si BRIMONIDINE/TIMOLOL BIOGARAN est administré avant l’accouchement, le nouveau-né doit être étroitement surveillé durant les premiers jours de sa vie.
Tartrate de brimonidine
Il n’a pas été établi si la brimonidine est excrétée dans le lait de la femme, mais elle est excrétée dans le lait des rates allaitantes.
Timolol
Les bêta-bloquants sont excrétés dans le lait maternel. Cependant, aux doses thérapeutiques du timolol en collyre, il est peu probable que des quantités suffisamment importantes soient présentes dans le lait maternel pour provoquer des symptômes cliniques de blocage bêta-adrénergique chez le nourrisson. Pour réduire l'absorption systémique, voir rubrique 4.2.
BRIMONIDINE/TIMOLOL BIOGARAN ne doit pas être utilisé par la femme qui allaite.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
D’après des données cliniques obtenues sur une période de 12 mois, les effets indésirables d’origine médicamenteuse les plus fréquemment rapportés ont été une hyperémie conjonctivale (chez approximativement 15 % des patients) et des sensations de brûlure oculaire (chez approximativement 11 % des patients). Dans la majorité des cas, ces réactions ont été légères et elles ont entraîné un arrêt du traitement chez seulement 3,4 % et 0,5 % des patients, respectivement.
Les effets indésirables d’origine médicamenteuse suivants ont été reportés durant les essais cliniques menés avec l’association brimonidine/timolol:
Dans chaque catégorie, les effets indésirables sont présentés dans l’ordre décroissant de gravité. Pour classer la fréquence des effets indésirables les terminologies suivantes ont été utilisées : très fréquents (³ 1/10) ; fréquents (³ 1/100, < 1/10) ; peu fréquents (³ 1/1 000, < 1/100); rares (³ 1/10 000, < 1/1 000) ; très rares (<1/10 000) ; fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
Affections oculaires
Très fréquents : hyperhémie conjonctivale, sensations de brûlure.
Fréquents : sensations de picotement dans l’œil, conjonctivite allergique, érosion de la cornée, kératite ponctuée superficielle, prurit oculaire, folliculose conjonctivale, troubles de la vision, blépharite, épiphora, sécheresse oculaire, écoulement oculaire, douleur oculaire, irritation oculaire, sensation de corps étranger dans l’œil.
Peu fréquents : diminution de l’acuité visuelle, œdème conjonctival, conjonctivite folliculaire, blépharite allergique, conjonctivite, corps flottants du vitré, asthénopie, photophobie, hypertrophie papillaire, douleurs de la paupière, blanchiment conjonctival, œdème de la cornée, infiltrats cornéens, décollement du vitré.
Affections psychiatriques
Fréquents : dépression.
Affections du système nerveux
Fréquents : somnolence, céphalées.
Peu fréquents : vertiges, syncope.
Affections cardiaques
Peu fréquents : insuffisance cardiaque congestive, palpitations.
Affections vasculaires
Fréquents : hypertension.
Affections respiratoires, thoraciques et médiastinales
Peu fréquents : rhinite, sécheresse nasale.
Affections gastro-intestinales
Fréquents : sécheresse buccale.
Peu fréquents : dysgueusie, nausées, diarrhée.
Affections de la peau et des tissus sous-cutanés
Fréquents : œdème des paupières, prurit des paupières, érythème des paupières.
Peu fréquents : eczéma allergique de contact.
Troubles généraux et anomalies au site d’administration
Fréquents : asthénie.
Les effets indésirables suivants ont été rapportés depuis la commercialisation de l’association brimonidine/timolol.
Affections oculaires :
Fréquence indéterminée : vision floue
Affections cardiaques :
Fréquence indéterminée : arythmie, bradycardie, tachycardie.
Affections vasculaires :
Fréquence indéterminée : hypotension.
Affections de la peau et des tissus sous-cutanés
Fréquence indéterminée : érythème facial
D’autres effets indésirables ont été rapportés avec l’un des composants, et sont également susceptibles d’être observés avec BRIMONIDINE/TIMOLOL BIOGARAN :
Brimonidine
Affections oculaires : iritis, iridocyclite (uvéite antérieure), myosis.
Affections psychiatriques : insomnie.
Affections respiratoires, thoraciques et médiastinales : symptômes respiratoires supérieurs, dyspnée.
Affections gastro-intestinales : symptômes gastro-intestinaux.
Troubles généraux et anomalies au site d’administration : réactions allergiques générales.
Troubles de la peau et des tissus sous-cutanés : réactions cutanées incluant érythème, œdème facial, prurit, rash et vasodilatation.
Population pédiatrique
Dans des cas où la brimonidine a été utilisée dans le cadre du traitement médical d'un glaucome congénital, des symptômes de surdosage à la brimonidine tels que perte de conscience, léthargie, somnolence, hypotension, hypotonie, bradycardie, hypothermie, cyanose, pâleur, dépression respiratoire et apnée ont été rapportés chez des nouveau-nés et nourrissons (moins de 2 ans) qui avaient reçu de la brimonidine (voir rubrique 4.3).
De nombreux et sévères cas de somnolence ont été rapportés chez les enfants de 2 ans ou plus, en particulier ceux âgés de 2 à 7 ans et/ou de poids inférieur ou égal à 20kg (voir rubrique 4.4).
Timolol
Comme c'est le cas avec d'autres produits ophtalmiques à usage local, BRIMONIDINE/TIMOLOL BIOGARAN (brimonidine/timolol) peut passer dans la circulation systémique. L’absorption de timolol peut provoquer des effets indésirables similaires à ceux observés avec les bêta-bloquants systémiques.
L’incidence des effets indésirables systémiques après une administration ophtalmique locale est plus faible qu’après une administration systémique. Pour réduire l'absorption systémique, voir rubrique 4.2.
Les effets indésirables supplémentaires qui ont été observés avec les bêta-bloquants ophtalmiques et qui peuvent éventuellement se produire aussi avec BRIMONIDINE/TIMOLOL BIOGARAN sont listés ci-après :
Affections du système immunitaire : Réactions allergiques systémiques incluant angiœdème, urticaire, éruption cutanée localisée et généralisée, prurit, anaphylaxie.
Troubles du métabolisme et de la nutrition : Hypoglycémie.
Affections psychiatriques : Insomnie, cauchemars, perte de mémoire, hallucinations.
Affections du système nerveux : Accident cérébrovasculaire, ischémie cérébrale, aggravation des signes et symptômes de myasthénie grave, paresthésie.
Affections oculaires : Kératite, décollement de la choroïde après chirurgie filtrante (voir rubrique 4.4), baisse de la sensibilité cornéenne, érosion cornéenne, ptosis, diplopie.
Affections cardiaques : Douleurs thoraciques, œdème, bloc auriculo-ventriculaire, arrêt cardiaque, défaillance cardiaque.
Affections vasculaires : Phénomène de Raynaud, refroidissement des mains et des pieds.
Affections respiratoires, thoraciques et médiastinales : Bronchospasme (surtout chez des patients présentant une maladie bronchospastique préexistante), dyspnée, toux.
Affections gastro-intestinales : dyspepsie, douleurs abdominales, vomissements.
Affections de la peau et du tissu sous-cutané : Alopécie, éruption psoriasiforme ou aggravation du psoriasis, éruption cutanée.
Affections musculo-squelettiques et systémiques : Myalgie.
Affections des organes de reproduction et du sein : Dysfonctionnements sexuels, baisse de la libido.
Troubles généraux et anomalies au site d’administration : Asthénie.
Effets indésirables rapportés avec les collyres contenant du phosphate
Des cas de calcification cornéenne ont été très rarement rapportés en association avec l'utilisation de collyre contenant du phosphate chez certains patients présentant des altérations significatives de la cornée.
Déclaration des effets indésirables suspectés.
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.signalement-sante.gouv.fr.
Brimonidine
Surdosage ophtalmique (adultes)
Parmi les cas reçus, les évènements rapportés faisaient généralement partie des effets indésirables connus.
Surdosage systémique résultant d'une ingestion accidentelle (Adultes)
Il existe peu d’information concernant l’ingestion accidentelle de brimonidine chez l’adulte. Le seul effet indésirable rapporté à ce jour a été l’hypotension. L’épisode hypotensif a été suivi par une hypertension rebond. Les cas rapportés de surdosage oral avec d’autres agonistes alpha2-adrénergiques ont mentionné des symptômes tels que : hypotension, asthénie, vomissements, léthargie, sédation, bradycardie, arythmies, myosis, apnée, hypotonie, hypothermie, dépression respiratoire et convulsions.
Population pédiatrique :
Plusieurs rapports d'effets indésirables graves consécutifs à l'ingestion accidentelle de brimonidine en collyre par des enfants ont été publiés ou rapportés. Les sujets ont présenté des symptômes de dépression du système nerveux central, typiquement coma temporaire, ou faible niveau de conscience, léthargie, somnolence, hypotonie, bradycardie, hypothermie, pâleur, dépression respiratoire et apnée, ayant nécessité une admission aux soins intensifs avec intubation si nécessaire. Un rétablissement complet a été rapporté chez tous les sujets, en général dans les 6 à 24 heures.
Timolol
Les symptômes d’un surdosage par le timolol par voie générale incluent : bradycardie, hypotension, bronchospasme, céphalées, vertiges et arrêt cardiaque. Une étude clinique a indiqué que le timolol n’est pas éliminé facilement par dialyse.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Mécanisme d’action
BRIMONIDINE/TIMOLOL BIOGARAN contient deux substances actives : le tartrate de brimonidine et le maléate de timolol. Ces deux composants diminuent la pression intraoculaire (PIO) élevée par des mécanismes d’action complémentaires ; cet effet combiné résulte en une baisse additionnelle de la PIO comparée à celle induite par l’un ou l’autre principe actif en monothérapie. BRIMONIDINE/TIMOLOL BIOGARAN a un délai d’action rapide.
Le tartrate de brimonidine est un agoniste des récepteurs alpha2-adrénergiques qui est 1 000 fois plus sélectif pour les récepteurs adrénergiques de type alpha2 que pour ceux de type alpha1. Cette sélectivité résulte en l’absence de mydriase et de vasoconstriction des microvaisseaux associée aux xénogreffes de rétine humaine.
On pense que le tartrate de brimonidine diminue la PIO en augmentant l'écoulement de l'humeur aqueuse par la voie uvéosclérale et en réduisant la production d'humeur aqueuse.
Le timolol est un inhibiteur non sélectif des récepteurs bêta1- et bêta2-adrénergiques qui n’a pas d’activité sympathomimétique intrinsèque significative ni d’action dépressive directe sur le myocarde ou d’effet anesthésique local (stabilisateur des membranes). Le timolol abaisse la PIO en réduisant la production d’humeur aqueuse. Son mécanisme d’action n’est pas clairement élucidé, mais il est probable qu’il fasse intervenir une inhibition de l’augmentation de la synthèse d’AMP cyclique induite par une stimulation bêta-adrénergique endogène.
Efficacité et sécurité clinique
Dans trois études cliniques contrôlées en double insu, l’association brimonidine/timolol (deux fois par jour) a produit une baisse additionnelle de la PIO diurne moyenne cliniquement significative par rapport à celles observées avec le timolol (deux fois par jour) ou la brimonidine (deux ou trois fois par jour) en monothérapie.
Dans une étude conduite sur des patients dont la PIO était insuffisamment contrôlée par une monothérapie de 3 semaines minimum des baisses additionnelles de PIO diurne moyenne atteignant respectivement 4,5 ; 3,3 et 3,5 mmHg, ont été observées durant les 3 mois de traitement par l’association brimonidine/timolol (deux fois par jour), timolol (deux fois par jour) et brimonidine (deux fois par jour). Dans cette étude, une baisse additionnelle significative de la PIO au creux a pu être démontrée pour la brimonidine mais pas pour le timolol, cependant une tendance positive a été observée à tous les autres points. Dans les données poolées des 2 autres études, une supériorité statistique versus timolol a été démontrée à tous les points.
De plus, la baisse de PIO produite par l’association brimonidine/timolol a été constamment non-inférieure à celle observée avec un traitement associant la brimonidine et le timolol (deux fois par jour dans tous les cas).
Il a été démontré que la baisse de PIO produite par l’association brimonidine/timolol a été maintenue durant les études en double insu allant jusqu’à 12 mois.
5.2. Propriétés pharmacocinétiques
Association fixe brimonidine/timolol
Les concentrations plasmatiques en brimonidine et timolol ont été déterminées durant une étude croisée comparant les monothérapies à l’association brimonidine/timolol chez des sujets sains. Aucune différence statistiquement significative des aires sous la courbe (ASC) de la brimonidine et du timolol n’a été détectée entre l’association brimonidine/timolol et les deux monothérapies. Chez les patients traités par l’association brimonidine/timolol, les Cmax plasmatiques moyennes en brimonidine et timolol ont été respectivement de 0,0327 et 0,406 ng/mL.
Brimonidine
Chez l’homme, les concentrations plasmatiques en brimonidine mesurées après l’administration oculaire d’un collyre en solution à 0,2 % sont basses. La brimonidine est peu métabolisée dans l’œil humain, et son taux de liaison aux protéines plasmatiques humaines est d’environ 29 %. La demi-vie systémique apparente moyenne est voisine de 3 heures après administration oculaire chez l’homme.
La brimonidine est bien absorbée et rapidement éliminée après une administration orale chez l’homme. La majeure partie de la dose (environ 74 % de la dose) est excrétée dans l’urine sous la forme de métabolites en cinq jours ; la forme inchangée de la brimonidine n’est pas détectée dans l’urine. Des études menées in vitro sur les foies animal et humain ont indiqué que le métabolisme fait largement intervenir l’aldéhyde-oxydase et le cytochrome P450. En conséquence, l’élimination systémique semble être principalement due à un métabolisme hépatique.
La brimonidine est liée de façon importante et réversible à la mélanine dans les tissus oculaires, sans effets indésirables quelconques. L’accumulation n’a pas lieu en l'absence de mélanine.
La brimonidine ne subit pas un métabolisme important dans l’œil humain.
Timolol
Le pic des concentrations en timolol a atteint 898 ng/mL dans l’humeur aqueuse, une heure après l’administration oculaire d’un collyre en solution à 0,5 % chez des sujets subissant une chirurgie de la cataracte. Une partie de la dose passe dans la circulation générale où elle est métabolisée de façon importante par le foie. La demi-vie plasmatique du timolol est de l’ordre de 7 heures. Le timolol est partiellement métabolisé dans le foie et excrété par les reins avec ses métabolites. Le taux de liaison du timolol aux protéines plasmatiques est faible.
5.3. Données de sécurité préclinique
Le profil de sécurité oculaire et systémique de chaque principe actif est bien établi. Les données non-cliniques issues des études de sécurité pharmacologique, de toxicologie en administration répétée, de génotoxicité et de cancérogénicité n’ont pas révélé de risque particulier pour l’homme. Des études supplémentaires de toxicité oculaire à doses répétées ont aussi indiqué que l’association brimonidine/timolol ne présente pas de risque particulier pour l’homme.
Brimonidine
Le tartrate de brimonidine n’induit aucun effet tératogène chez l’animal, mais provoque des avortements chez le lapin et un retard de croissance postnatale chez le rat pour des expositions systémiques respectivement d’environ 37 et 134 fois plus élevées que celles utilisées pour le traitement chez l’homme.
Timolol
Dans les études chez l’animal, les bêta-bloquants ont montré qu’ils pouvaient réduire le flux sanguin ombilical, réduire la croissance fœtale, retarder l’ossification et augmenter la mortalité fœtale et post natale mais sans tératogénicité. Avec le timolol, on a observé, à de fortes doses maternelles, une embryotoxicité (résorption) chez le lapin et une fœtotoxicité (retard de l’ossification) chez le rat. Il n’a pas été mis en évidence de malformation fœtale lors d’études de tératogénicité chez la souris, le rat et le lapin, à des doses de timolol par voie orale allant jusqu’à 4200 fois la dose quotidienne de l’association brimonidine/timolol chez l’homme.
Chlorure de benzalkonium, phosphate monosodique monohydraté, phosphate disodique heptahydraté, acide chlorhydrique ou hydroxyde de sodium (pour l’ajustement du pH), eau purifiée.
2 ans.
Après première ouverture, le médicament doit être conservé maximum 28 jours.
6.4. Précautions particulières de conservation
Ce médicament ne nécessite pas de précautions particulières de conservation.
6.5. Nature et contenu de l'emballage extérieur
5 mL en flacon en polyéthylène basse densité (PEBD) blanc muni d’un compte-goutte (PEBD) et d’un bouchon en polyéthylène haute densité (PEHD) ; boîte de 1 ou 3.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Pas d’exigences particulières pour l’élimination.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
15 boulevard charles de gaulle
92700 colombes
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 302 558 3 4 : 5 mL en flacon (PEBD). Boîte de 1.
· 34009 302 558 5 8 : 5 mL en flacon (PEBD). Boîte de 3.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I.
ANSM - Mis à jour le : 04/07/2022
BRIMONIDINE/TIMOLOL BIOGARAN 2 mg/mL + 5 mg/mL, collyre en solution
Tartrate de brimonidine / Timolol
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin, votre pharmacien ou votre infirmier/ère.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que BRIMONIDINE/TIMOLOL BIOGARAN 2 mg/mL + 5 mg/mL, collyre en solution et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d’utiliser BRIMONIDINE/TIMOLOL BIOGARAN 2 mg/mL + 5 mg/mL, collyre en solution ?
3. Comment utiliser BRIMONIDINE/TIMOLOL BIOGARAN 2 mg/mL + 5 mg/mL, collyre en solution ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver BRIMONIDINE/TIMOLOL BIOGARAN 2 mg/mL + 5 mg/mL, collyre en solution ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE BRIMONIDINE/TIMOLOL BIOGARAN 2 mg/mL + 5 mg/mL, collyre en solution ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique - code ATC : S01ED51
BRIMONIDINE/TIMOLOL BIOGARAN est un collyre antiglaucomateux. Il contient deux substances actives différentes (la brimonidine et le timolol) qui diminuent la pression élevée dans l’œil. La brimonidine appartient au groupe de médicaments appelés agonistes des récepteurs alpha2-adrénergiques. Le timolol appartient au groupe de médicaments appelés bêta-bloquants.
BRIMONIDINE/TIMOLOL BIOGARAN est prescrit pour abaisser la pression intraoculaire quand l’effet produit par un collyre contenant uniquement un bêta-bloquant n’est pas suffisant.
Votre œil contient un liquide aqueux limpide qui nourrit l'intérieur de l'œil. Ce liquide est constamment évacué de l'œil et un nouveau liquide est produit pour le remplacer. Si le liquide ne peut pas être évacué suffisamment vite, la pression intraoculaire augmente, ce qui risque d'endommager la vue. BRIMONIDINE/TIMOLOL BIOGARAN agit en réduisant la production de liquide et également en augmentant la quantité de liquide évacué. Cela diminue la pression à l’intérieur de l’œil.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER BRIMONIDINE/TIMOLOL BIOGARAN 2 mg/mL + 5 mg/mL, collyre en solution ?
N’utilisez jamais BRIMONIDINE/TIMOLOL BIOGARAN 2 mg/mL + 5 mg/mL, collyre en solution
· Si vous êtes allergique au tartrate de brimonidine, au timolol, aux bêta-bloquants ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
Les symptômes d'une réaction allergique peuvent se traduire par des gonflements du visage, des lèvres et de la gorge, une respiration pénible, un malaise, un souffle coupé, une démangeaison ou une rougeur autour des yeux.
· Si vous souffrez ou avez souffert par le passé d’une maladie respiratoire quelle qu'elle soit, par exemple d’asthme, de bronchite obstructive chronique sévère (maladie pulmonaire grave pouvant entraîner des difficultés à respirer et/ou une toux persistante).
· Si vous avez des problèmes cardiaques, par exemple une fréquence cardiaque basse, un bloc cardiaque, des troubles du rythme cardiaque (sauf si contrôlés par un stimulateur cardiaque),
· Si vous prenez un inhibiteur de la monoamine oxydase (IMAO) ou certains autres antidépresseurs.
Avertissements et précautions
Adressez-vous à votre médecin, pharmacien ou votre infirmier/ère avant d’utiliser BRIMONIDINE/TIMOLOL BIOGARAN.
Informez votre médecin si vous êtes dans l'une des situations suivantes :
· si vous présentez ou si vous avez présenté dans le passé :
o une maladie cardiaque coronarienne (les symptômes comprennent des douleurs thoraciques ou une oppression dans la poitrine, des difficultés respiratoires ou des suffocations), une insuffisance cardiaque ou une pression sanguine basse,
o des perturbations du rythme cardiaque comme un ralentissement du rythme cardiaque,
o des problèmes respiratoires, de l’asthme ou une broncho-pneumopathie chronique obstructive,
o une mauvaise circulation du sang (comme la maladie de Raynaud ou le syndrome de Raynaud),
o un diabète car le timolol peut masquer les signes et les symptômes de faibles taux de sucre dans le sang,
o un hyperfonctionnement de la thyroïde car le timolol peut en masquer les signes et symptômes,
o des troubles des reins ou du foie,
o une tumeur de la glande surrénale,
o une intervention chirurgicale oculaire destinée à diminuer la pression dans votre œil.
· si vous présentez ou si vous avez eu dans le passé une forme quelconque d’allergie (par exemple un rhume des foins, un eczéma) ou une réaction allergique sévère, il sera éventuellement nécessaire d’augmenter la dose d’adrénaline habituellement utilisée pour maîtriser une réaction allergique grave.
· en cas de réaction allergique oculaire,
· avant toute anesthésie chirurgicale, veuillez indiquer à votre médecin que vous prenez BRIMONIDINE/TIMOLOL BIOGARAN, car le timolol peut modifier les effets de certains médicaments utilisés pendant l’anesthésie.
Enfants et adolescents
BRIMONIDINE/TIMOLOL BIOGARAN ne doit pas être utilisé chez l’enfant de moins de 2 ans et son utilisation est déconseillée chez les enfants âgés de 2 à 17 ans.
Autres médicaments et BRIMONIDINE/TIMOLOL BIOGARAN 2 mg/mL + 5 mg/mL, collyre en solution
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament, même s’il n’est pas lié à votre problème oculaire, y compris un médicament obtenu sans ordonnance.
L’action de BRIMONIDINE/TIMOLOL BIOGARAN peut affecter ou être affectée par l’action d’autres médicaments que vous prenez, y compris par d’autres collyres prescrits en cas de glaucome.
Il existe plusieurs médicaments susceptibles d’interférer avec BRIMONIDINE/TIMOLOL BIOGARAN, il est important que vous préveniez votre médecin si vous prenez :
· un médicament contre la douleur,
· un médicament pour vous aider à dormir ou pour traiter l’anxiété,
· un médicament contre la pression sanguine élevée (hypertension),
· un médicament pour des problèmes cardiaques (par exemple rythme cardiaque anormal) comme des bêta-bloquants, la digoxine, ou la quinidine (utilisée pour traiter les problèmes cardiaques et certains types de paludisme),
· un médicament pour traiter le diabète ou un taux élevé de sucre dans le sang,
· un médicament pour traiter la dépression comme la fluoxétine ou la paroxétine,
· un autre collyre afin de réduire la pression oculaire élevée (glaucome),
· un médicament pour traiter les réactions allergiques graves,
· un médicament ayant un impact sur certaines hormones comme l’adrénaline ou la dopamine,
· un médicament ayant un impact sur les muscles des vaisseaux sanguins,
· un médicament pour traiter les brûlures d’estomac ou les ulcères de l’estomac.
Si la dose d’un des médicaments que vous prenez habituellement est modifiée ou si vous consommez régulièrement de l’alcool, informez votre médecin.
Si vous devez subir une anesthésie, informez votre médecin ou votre dentiste que vous prenez BRIMONIDINE/TIMOLOL BIOGARAN.
BRIMONIDINE/TIMOLOL BIOGARAN 2 mg/mL + 5 mg/mL, collyre en solution avec des aliments, des boissons et de l’alcool
Sans objet.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
N’utilisez pas BRIMONIDINE/TIMOLOL BIOGARAN si vous êtes enceinte à moins que votre médecin ne le recommande.
N’utilisez pas BRIMONIDINE/TIMOLOL BIOGARAN si vous allaitez. Le timolol peut passer dans le lait maternel. Pendant la période d’allaitement, demandez conseil à votre médecin avant de prendre un médicament.
Conduite de véhicules et utilisation de machines
BRIMONIDINE/TIMOLOL BIOGARAN peut provoquer une somnolence, une fatigue et une vision trouble chez certains patients. Ne conduisez pas un véhicule et n’utilisez pas des machines jusqu'à ce que vous ayez retrouvé une vue normale.
BRIMONIDINE / TIMOLOL BIOGARAN 2 mg/mL + 5 mg/mL, collyre en solution contient du chlorure de benzalkonium et des phosphates
Ce médicament contient 0,05 mg de chlorure de benzalkonium pour 1 mL de collyre.
Le chlorure de benzalkonium peut être absorbé par les lentilles de contact souples et changer leur couleur. Retirez les lentilles de contact avant application et attendez au moins 15 minutes avant de les remettre.
Le chlorure de benzalkonium peut également provoquer une irritation des yeux, surtout si vous souffrez du syndrôme de l’œil sec ou de troubles de la cornée (couche transparente à l’avant de l’œil). En cas de sensation anormale, de picotements ou de douleur dans les yeux après avoir utilisé ce médicament, contactez votre médecin.
Ce médicament contient 10,6 mg de phosphates pour 1 mL de collyre.
Si vous souffrez de dommages sévères de la cornée (couche transparente située à l’avant de l’œil), les phosphates peuvent causer, dans de très rares cas, des troubles de la vision en raison de l’accumulation de calcium pendant le traitement (nuage).
3. COMMENT UTILISER BRIMONIDINE/TIMOLOL BIOGARAN 2 mg/mL + 5 mg/mL, collyre en solution ?
La dose recommandée est d’une goutte instillée dans l’œil à traiter deux fois par jour à 12 heures d’intervalle environ. Ne modifiez pas la dose et n’arrêtez pas le traitement sans consulter votre médecin.
Si vous utilisez BRIMONIDINE/TIMOLOL BIOGARAN en même temps qu’un autre collyre, attendez 5 minutes au moins entre l’instillation de BRIMONIDINE/TIMOLOL BIOGARAN et celle de l’autre médicament.
Utilisation chez les enfants et les adolescents
BRIMONIDINE/TIMOLOL BIOGARAN ne doit pas être utilisé chez les enfants de moins de 2 ans. Il est déconseillé d'utiliser BRIMONIDINE/TIMOLOL BIOGARAN chez les enfants et les adolescents (âgés de 2 à 17 ans).
Mode d’administration
N’utilisez pas le flacon si le sceau d’inviolabilité qui recouvre le col du flacon a été endommagé avant la première ouverture.
Lavez-vous les mains avant d’ouvrir le flacon. Inclinez la tête légèrement en arrière et regardez vers le haut.
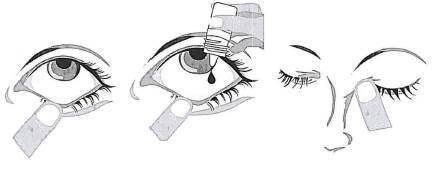
1. Tirez délicatement la paupière inférieure vers le bas jusqu'à ce qu'une petite poche soit formée.
2. Retournez le flacon à l'envers et appuyez dessus pour en libérer une goutte dans chacun des yeux à traiter.
3. Relâchez la paupière inférieure et gardez l’œil fermé.
4. Maintenez l’œil fermé et comprimez le sac lacrymal au niveau de l’angle interne de l’œil (point d’occlusion) pendant deux minutes. Ceci permet d’éviter que BRIMONIDINE/TIMOLOL BIOGARAN ne se diffuse ailleurs que dans l’œil.
Si une goutte tombe à côté de votre œil, répétez la procédure.
Pour éviter toute contamination, ne laissez pas la pointe du flacon toucher votre œil ou quoi que ce soit. Remettez le bouchon en place sur le flacon aussitôt après l'avoir utilisé.
Si vous avez utilisé plus de BRIMONIDINE / TIMOLOL BIOGARAN 2 mg/mL + 5 mg/mL, collyre en solution que vous n’auriez dû
Adultes
Si vous utilisez plus de BRIMONIDINE/TIMOLOL BIOGARAN que vous n’auriez dû, il est peu probable que ceci entraîne des effets néfastes. Instillez la goutte suivante à l'heure habituelle. Si vous êtes inquiet, parlez-en à votre médecin ou à votre pharmacien.
Nouveau-nés et enfants
Quelques cas de surdosage ont été rapportés chez des nouveau-nés traités par brimonidine (l’un des composants de BRIMONIDINE/TIMOLOL BIOGARAN) dans le cadre d’un glaucome congénital. Les signes observés comprennent une somnolence, une mollesse, une température corporelle basse, une pâleur, et des difficultés respiratoires. Si l’un de ces signes se manifeste, consultez immédiatement votre médecin.
Adultes et enfants
Consultez immédiatement votre médecin si vous avez avalé accidentellement BRIMONIDINE/TIMOLOL BIOGARAN.
Si vous oubliez d’utiliser BRIMONIDINE / TIMOLOL BIOGARAN 2 mg/mL + 5 mg/mL, collyre en solution
Si vous oubliez d’utiliser BRIMONIDINE/TIMOLOL BIOGARAN, instillez une seule goutte dans chaque œil à traiter dès que vous vous rendez compte de votre oubli et ensuite reprenez votre traitement comme d'habitude. Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre.
Si vous arrêtez d’utiliser BRIMONIDINE / TIMOLOL BIOGARAN 2 mg/mL + 5 mg/mL, collyre en solution
BRIMONIDINE/TIMOLOL BIOGARAN doit être utilisé tous les jours pour être efficace.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin, à votre pharmacien ou à votre infirmier/ère.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Si vous développez l'un des effets indésirables suivants, contactez votre médecin immédiatement :
· défaillance cardiaque (par exemple douleur thoracique) ou battements cardiaque irréguliers
· diminution ou augmentation du rythme cardiaque ou tension basse (hypotension)
Les effets indésirables suivants peuvent survenir avec BRIMONIDINE/TIMOLOL BIOGARAN :
Affectant l’œil / les yeux
Très fréquent (pouvant affecter plus de 1 patient sur 10)
· Rougeur de l'œil ou sensation de brûlure.
Fréquent (pouvant affecter jusqu’à 1 patient sur 10)
· Picotements ou douleur au niveau de l’œil.
· Réaction allergique au niveau de l'œil ou de la peau avoisinante.
· Petite érosion à la surface de l'œil (avec ou sans inflammation).
· Gonflement, rougeur ou inflammation des paupières.
· Irritation, ou sensation de corps étranger dans l'œil.
· Démangeaisons des yeux et des paupières.
· Follicules ou points blancs sur la couche transparente qui recouvre la surface de l’œil.
· Trouble de la vision.
· Larmoiement.
· Sécheresse oculaire.
· Œil (yeux) collé(s).
Peu fréquent (pouvant affecter jusqu’à 1 patient sur 100)
· Difficulté à voir nettement.
· Gonflement ou inflammation de la couche transparente qui recouvre la surface de l’œil.
· Yeux fatigués.
· Sensibilité à la lumière.
· Douleur des paupières.
· Blanchiment de la couche transparente qui recouvre la surface de l’œil.
· Gonflements ou points d’inflammation sous la surface de l’œil.
· Corps flottants devant les yeux.
Fréquence indéterminée (ne pouvant être estimée sur la base des données disponibles)
· Vision floue.
Affectant le corps
Très fréquents (pouvant affecter plus de 1 patient sur 10)
· Pression sanguine élevée.
· Dépression.
· Somnolence.
· Maux de tête.
· Sécheresse buccale.
· Faiblesse généralisée.
Peu fréquent (pouvant affecter jusqu’à 1 patient sur 100)
· Défaillance cardiaque.
· Irrégularité du rythme cardiaque.
· Sensation de vertige.
· Evanouissements.
· Sécheresse nasale.
· Perturbation du goût.
· Nausées.
· Diarrhée.
Fréquence indéterminée (ne pouvant être estimée sur la base des données disponibles)
· Augmentation ou diminution de la fréquence cardiaque.
· Pression sanguine basse.
· Rougeur du visage.
Certains de ces effets peuvent être dus à une allergie à l'un des composants de ce collyre.
D’autres effets indésirables ont été rapportés avec la brimonidine ou le timolol, et ils sont donc également susceptibles de se produire avec BRIMONIDINE/TIMOLOL BIOGARAN.
Les effets indésirables suivants ont été observés avec la brimonidine :
· inflammation à l’intérieur de l’œil, rétrécissement des pupilles, difficultés d’endormissement, symptômes grippaux, essoufflement, symptômes au niveau de l’estomac et de la digestion, réactions allergiques généralisées, réactions cutanées incluant rougeur, gonflement du visage, démangeaisons, rash et dilatation des vaisseaux sanguins.
Comme les autres médicaments ophtalmiques à usage local, BRIMONIDINE/TIMOLOL BIOGARAN passe dans le sang, L’absorption du timolol, un bêta-bloquant contenu dans BRIMONIDINE/TIMOLOL BIOGARAN, peut provoquer des effets indésirables similaires à ceux observés avec les bêta-bloquants « intraveineux » et/ou « oraux ». La probabilité de présenter des effets indésirables après une administration ophtalmique est plus faible qu’après une administration orale ou intraveineuse, par exemple.
Les effets indésirables listés ci-après comprennent les réactions observées avec la classe des bêta-bloquants utilisés dans le traitement des maladies oculaires :
· Réactions allergiques généralisées incluant gonflement sous la peau (pouvant se produire au niveau du visage ou des membres et pouvant obstruer le passage de l’air résultant dans des difficultés à avaler ou à respirer), urticaire (ou éruption cutanée qui démange), éruption cutanée localisée ou généralisée, démangeaisons, réactions allergiques sévères pouvant engager le pronostic vital.
· Faible taux de sucre dans le sang.
· Difficultés à s’endormir (insomnies), cauchemars, perte de mémoire, hallucinations
· Accident vasculaire cérébral, diminution du flux sanguin vers le cerveau, aggravation des signes et symptômes de la myasthénie grave (augmentation de la faiblesse musculaire), sensation de picotements.
· Inflammation de la cornée, séparation de l’une des couches en dessous de la rétine qui contient des vaisseaux sanguins après une chirurgie filtrante (opération destinée à réduire la pression dans l’œil) pouvant causer des troubles visuels, diminution de la sensibilité de la cornée, érosion de la cornée (dommages de la couche superficielle du globe oculaire), affaissement de la paupière (fermant l’œil à moitié), vision double.
· Douleur thoracique, œdèmes (accumulation de liquides), irrégularités du rythme ou de la fréquence cardiaque, trouble du rythme cardiaque, attaque cardiaque, insuffisance cardiaque.
· Phénomène de Raynaud, froideur des mains et des pieds.
· Rétrécissement des voies respiratoires au niveau du poumon (particulièrement chez les patients présentant des maladies respiratoires), difficultés à respirer, toux.
· Indigestion, douleurs abdominales, vomissements.
· Chute de cheveux, éruption cutanée de couleur blanche-argentée (rash psoriasiforme) ou aggravation d’un psoriasis, éruption cutanée.
· Douleur musculaire non liée à de l’exercice.
· Dysfonctionnements sexuels, baisse de la libido.
· Faiblesse/fatigue musculaire.
Autres effets indésirables rapportés avec les collyres contenant du phosphate
Des cas de calcification cornéenne ont été très rarement rapportés lors de l’utilisation de collyres contenant du phosphate chez certains patients présentant des altérations significatives de la cornée.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou à votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.signalement-sante.gouv.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER BRIMONIDINE/TIMOLOL BIOGARAN 2 mg/mL + 5 mg/mL, collyre en solution ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’emballage. La date de péremption fait référence au dernier jour de ce mois.
Ce médicament ne nécessite pas de précautions particulières de conservation.
Après première ouverture, le médicament doit être conservé maximum 28 jours.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient BRIMONIDINE/TIMOLOL BIOGARAN 2 mg/mL + 5 mg/mL, collyre en solution
· Les substances actives sont :
Brimonidine...................................................................................................................... 1,3 mg
sous forme de 2 mg de tartrate de brimonidine
Timolol............................................................................................................................... 5 mg
sous forme de 6,8 mg de maléate de timolol
pour 1 mL de collyre en solution.
· Les autres composants sont : chlorure de benzalkonium, phosphate monosodique monohydraté, phosphate disodique heptahydraté, acide chlorhydrique ou hydroxyde de sodium (pour l’ajustement du pH) et eau purifiée.
Ce médicament se présente sous forme de collyre en solution dans un flacon compte-goutte. La solution est jaune-verdâtre et limpide
Chaque flacon de 5 mL de collyre contient approximativement 150 gouttes de collyre.
Chaque boîte contient 1 ou 3 flacons (PEBD) avec compte-goutte (PEBD) et bouchon à vis (PEHD).
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
15 BOULEVARD CHARLES DE GAULLE
92700 COLOMBES
Exploitant de l’autorisation de mise sur le marché
15 BOULEVARD CHARLES DE GAULLE
92700 COLOMBES
THESI POUSI-XATZI
AGIOU LOUKA
19002 PAIANIA ATTIKI
GRECE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).