Dernière mise à jour le 28/04/2026
NORADRENALINE TARTRATE KALCEKS 2 mg/mL, solution à diluer pour perfusion
Indications thérapeutiques
Classe pharmacothérapeutique : Agents adrénergiques et dopaminergiques, Code ATC : C01CA03.
NORADRENALINE TARTRATE KALCEKS contient la substance active noradrénaline et agit comme vasoconstricteur (provoque le rétrécissement des vaisseaux sanguins).
NORADRENALINE TARTRATE KALCEKS est utilisé chez les adultes en cas d'urgence pour augmenter la pression artérielle à des niveaux normaux.
Présentations
> 10 ampoule(s) de 8 ml
Code CIP : 34009 550 739 2 5
Déclaration de commercialisation : 12/01/2023
Cette présentation est agréée aux collectivités
> 10 ampoule(s) de 4 ml
Code CIP : 34009 550 739 0 1
Déclaration de commercialisation : 12/01/2023
Cette présentation est agréée aux collectivités
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 14/12/2022 | Inscription (CT) | Le service médical rendu par NORADRENALINE TARTRATE KALCEKS 2 mg/mL (tartrate de noradrénaline) est important dans l’indication de l’AMM. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 14/12/2022 | Inscription (CT) | Ces spécialités sont un euro-générique qui n’apporte pas d’amélioration du service médical rendu (ASMR V) par rapport aux autres spécialités à base de noradrénaline au même dosage et dans la même indications déjà inscrites. |
Autres informations
- Titulaire de l'autorisation : AS KALCEKS
- Conditions de prescription et de délivrance :
- liste I
- réservé à l'usage en situation d'urgence selon l'article R5121-96 du code de la santé publique
- réservé à l'usage HOSPITALIER
- Statut de l'autorisation : Valide
- Type de procédure : Procédure décentralisée
- Code CIS : 6 994 886 5
ANSM - Mis à jour le : 26/06/2024
NORADRENALINE TARTRATE KALCEKS 2 mg/mL, solution à diluer pour perfusion
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Equivalent à noradrénaline................................................................................................... 1,00 mg
Pour 1 mL de solution à diluer pour perfusion.
Chaque ampoule de 2 mL de solution à diluer pour perfusion contient du tartrate de noradrénaline, équivalent à 2 mg de noradrénaline.
Chaque ampoule de 4 mL de solution à diluer pour perfusion contient du tartrate de noradrénaline, équivalent à 4 mg de noradrénaline.
Chaque ampoule de 5 mL de solution à diluer pour perfusion contient du tartrate de noradrénaline, équivalent à 5 mg de noradrénaline.
Chaque ampoule de 8 mL pour solution à diluer pour perfusion contient du tartrate de noradrénaline, équivalent à 8 mg de noradrénaline.
Chaque ampoule de 10 mL pour solution à diluer pour perfusion contient du tartrate de noradrénaline, équivalent à 10 mg de noradrénaline.
Une fois dilué comme recommandé, chaque mL contient du tartrate de noradrénaline, équivalent à 40 microgrammes de noradrénaline.
Excipient à effet notoire :
8 mL de solution à diluer pour perfusion contient 26,4 mg (ou 1,12 mmol) de sodium.
10 mL de solution à diluer pour perfusion contient 33 mg (ou 1,40 mmol) de sodium.
Pour la liste complète des excipients, voir rubrique 6.1.
Solution à diluer pour perfusion (solution à diluer stérile).
Solution limpide, incolore ou jaunâtre, pratiquement exempte de particules visibles.
Le pH compris entre 3,0 et 4,0.
Osmolalité : 260 à 310 mOsm/kg.
4.1. Indications thérapeutiques
NORADRENALINE TARTRATE KALCEKS 2 mg/mL, solution à diluer pour perfusion est recommandé chez les adultes dans le traitement d'urgence pour la restauration de la pression artérielle en cas d'hypotension aiguë.
4.2. Posologie et mode d'administration
Adultes
Ajouter 2 mL de NORADRENALINE TARTRATE KALCEKS à 48 mL de glucose 50 mg/mL (5 %) (ou autres solutions de dilution mentionnées à la rubrique 6.6) pour l'administration par pompe à seringue.
La concentration finale de la solution pour perfusion est de 80 mg/l de tartrate de noradrénaline, ce qui équivaut à 40 mg/l de noradrénaline. Si d'autres dilutions sont utilisées, vérifiez soigneusement le calcul avant de commencer le traitement.
Taux initial de perfusion
La vitesse initiale de perfusion doit être comprise entre 10 mL/h et 20 mL/h (0,16 mL/min à 0,32 mL/min). Cela équivaut à 0,8 mg/h à 1,6 mg/h de tartrate de noradrénaline (ou 0,4 mg/h à 0,8 mg/h de noradrénaline).
Ajustement de la dose
Une fois la perfusion de noradrénaline est établie, la dose doit être ajustée en fonction de l'effet observé sur la pression artérielle. Il existe une grande variabilité inter-individuelle de la dose requise pour atteindre et maintenir la tension artérielle normale. L'objectif doit être d'établir une pression artérielle systolique basse (100 à 120 mmHg) ou d'atteindre une pression artérielle moyenne adéquate (> 65-80 mmHg - selon l'état du patient).
Tableau 1 : Ajustement de la dose de solution de noradrenaline pour perfusion
|
Solution pour perfusion de noradrénaline 40 mg/l(40 µg/mL) de noradrénaline base |
|||
|
Poids du patient |
Posologie (µg/kg/min) de noradrénaline |
Posologie (mg/h) de noradrénaline |
Débit de perfusion (mL/h) |
|
40 kg
|
0,05 |
0,12 |
3,0 |
|
0,1 |
0,24 |
6,0 |
|
|
0,25 |
0,60 |
15,0 |
|
|
0,5 |
1,2 |
30,0 |
|
|
1 |
2,4 |
60 |
|
|
50 kg |
0,05 |
0,15 |
3,75 |
|
0,1 |
0,3 |
7,5 |
|
|
0,25 |
0,75 |
18,75 |
|
|
0,5 |
1,5 |
37,5 |
|
|
1 |
3 |
75 |
|
|
60 kg |
0,05 |
0,18 |
4,5 |
|
0,1 |
0,36 |
9 |
|
|
0,25 |
0,9 |
22,5 |
|
|
0,5 |
1,8 |
45 |
|
|
1 |
3,6 |
90 |
|
|
70 kg |
0,05 |
0,21 |
5,25 |
|
0,1 |
0,42 |
10,5 |
|
|
0,25 |
1,05 |
26,25 |
|
|
0,5 |
2,1 |
52,5 |
|
|
1 |
4,2 |
105 |
|
|
80 kg |
0,05 |
0,24 |
6 |
|
0,1 |
0,48 |
12 |
|
|
0,25 |
1,2 |
30 |
|
|
0,5 |
2,4 |
60 |
|
|
1 |
4,8 |
120 |
|
|
90 kg |
0,05 |
0,27 |
6,75 |
|
0,1 |
0,54 |
13,5 |
|
|
0,25 |
1,35 |
33,75 |
|
|
0,5 |
2,7 |
67,5 |
|
|
1 |
5,4 |
135 |
|
Durée du traitement et surveillance
La noradrénaline doit être poursuivie jusqu'à ce que la pression artérielle et la perfusion tissulaire soient maintenues à un niveau adéquat sans traitement. Le patient doit être surveillé attentivement pendant toute la durée du traitement à la noradrénaline. La noradrénaline ne doit être administrée que par des professionnels de la santé qui connaissent son utilisation et qui disposent des installations appropriées pour surveiller adéquatement le patient.
Arrêt du traitement
Les perfusions doivent être réduites progressivement, en évitant un sevrage brutal qui peut entraîner une hypotension aiguë.
Insuffisance hépatique/rénale
Il n'existe aucune expérience de traitement chez les patients atteints d'insuffisance hépatique ou rénale.
Patients âgés
En général, des précautions doivent être prises lors de l’ajustement de la dose pour un patient âgé, en commençant par la partie inférieure de la gamme de dosage afin de refléter la plus grande fréquence de diminution de la fonction hépatique, rénale ou cardiaque et de maladie concomitante ou d'autres traitements médicamenteux.
Population pédiatrique
L'efficacité et la sécurité de la noradrénaline chez les enfants de moins de 18 ans n'ont pas encore été établies. Aucune donnée n'est disponible.
Mode d’administration
Voie d'administration
Voie intraveineuse après dilution.
NORADRENALINE TARTRATE KALCEKS doit être dilué et doit être administré par un cathéter veineux central. La perfusion doit avoir un débit contrôlé à l'aide d'une pompe à seringue ou d'une pompe à perfusion ou d'un compte-gouttes.
Pour les instructions relatives à la dilution du médicament avant l'administration, voir rubrique 6.6.
Hypersensibilité à la substance active ou à l'un des excipients mentionnés à la rubrique 6.1.
Hypotension due à un déficit du volume sanguin (hypovolémie).
Ne pas utiliser avec les anesthésiques cyclopropane et halothane. Pour les interactions, voir rubrique 4.5.
L'utilisation d'amines vasopressives pendant l'anesthésie au cyclopropane ou à l'halothane peut provoquer des arythmies cardiaques graves. En raison de la possibilité d'augmenter le risque de fibrillation ventriculaire, la noradrénaline doit être utilisée avec précaution chez les patients qui reçoivent ces substances ou tout autre agent de sensibilisation cardiaque ou chez les patients qui présentent une hypoxie ou une hypercapnie profonde.
L'administration dans les veines des membres inférieurs des personnes âgées et des patients souffrant de maladies occlusives dues à une éventuelle vasoconstriction doit être évitée (voir rubrique 4.4).
4.4. Mises en garde spéciales et précautions d'emploi
La noradrénaline est contre-indiquée chez les patients présentant une hypotension due à une hypovolémie, sauf en cas d'urgence pour maintenir la perfusion des artères coronaires et cérébrales jusqu'à ce qu’une thérapie de remplacement du volume sanguin puisse être mise en place.
La noradrénaline ne doit être utilisée qu’en association avec un remplacement approprié du volume sanguin.
Si la noradrénaline est administrée de façon continue pour maintenir la pression artérielle en l'absence de remplacement du volume sanguin, les symptômes suivants peuvent survenir : vasoconstriction périphérique et viscérale sévère, diminution de la perfusion rénale et du débit urinaire, mauvaise circulation sanguine systémique malgré une pression artérielle "normale", hypoxie tissulaire et acidose lactique. Le remplacement du volume sanguin peut être administré avant et/ou en même temps que cet agent ; toutefois, si le sang total ou le plasma sanguin est indiqué pour augmenter le volume sanguin, il faut l'administrer séparément (par exemple, s'il est administré simultanément, utiliser des tubes en Y et des récipients individuels).
Une administration prolongée de tout vasopresseur puissant peut entraîner une diminution du volume plasmatique qui doit être corrigée en continu par un remplissage hydro-électrolytique approprié. Si les volumes plasmatiques ne sont pas corrigés, soit une hypotension peut réapparaître à l'arrêt de la noradrénaline, soit la pression artérielle peut être maintenue au risque d'une sévère vasoconstriction périphérique et viscérale (par exemple, diminution de la perfusion rénale) associée à une diminution du flux sanguin et de la perfusion tissulaire, entraînant une hypoxie tissulaire et une acidose lactique ultérieures et une possible lésion ischémique ; une gangrène des extrémités a rarement été signalée.
Lors de la perfusion de noradrénaline, la pression artérielle et le débit doivent être vérifiés fréquemment pour éviter l'hypertension, qui peut être associée à la bradycardie ainsi qu'aux maux de tête et à l'ischémie périphérique, y compris, rarement, la gangrène des extrémités. L'extravasation peut provoquer une nécrose tissulaire locale (voir la section « Extravasation » ci-dessous).
Une attention particulière doit être maintenue chez les patients présentant un dysfonctionnement majeur du ventricule gauche associé à une hypotension aiguë. Un traitement de soutien doit être initié en même temps que l'évaluation diagnostique. La noradrénaline doit être réservée aux patients présentant un choc cardiogénique et une hypotension réfractaire, en particulier ceux qui ne présentent pas de résistance vasculaire systémique élevée.
La survenue de troubles du rythme cardiaque pendant le traitement doit entraîner une réduction de la dose.
Des arythmies cardiaques peuvent survenir lorsque la noradrénaline est utilisée en association avec des agents sensibilisateurs cardiaques, et peuvent être plus probables chez les patients souffrant d'hypoxie ou d'hypercapnie.
Une attention particulière doit être maintenue chez les patients présentant une thrombose vasculaire coronarienne, mésentérique ou périphérique, car la noradrénaline peut accroître l'ischémie et étendre la zone d'infarctus, à moins que, de l'avis du médecin traitant, l'administration de noradrénaline soit nécessaire pour sauver la vie. Des précautions identiques doivent être prises chez les patients souffrant d'hypotension suite à un infarctus du myocarde, chez les patients présentant une angine, en particulier l’angine de Prinzmetal, et chez les patients souffrant de diabète, d'hypertension ou d'hyperthyroïdie (voir rubrique 4.8).
Des précautions particulières doivent être prises chez les patients présentant une insuffisance hépatique, une dysfonction rénale sévère, des cardiopathies ischémiques et une pression intracrânienne élevée. Les surdoses ou les doses conventionnelles chez les personnes hypersensibles (par exemple les patients hyperthyroïdiens) peuvent provoquer une hypertension sévère accompagnée de violents maux de tête, de photophobie, de douleurs rétrosternales lancinantes, de pâleur, de transpiration intense et de vomissements. L'hypertension peut éventuellement entraîner un œdème pulmonaire aigu, une arythmie ou un arrêt cardiaque.
Des précautions doivent être prises chez les diabétiques car la noradrénaline augmente le taux de glucose dans le sang (en raison de l'action glycogénolytique dans le foie et de l'inhibition de la libération d'insuline par le pancréas).
Les personnes âgées peuvent être particulièrement sensibles aux effets de la noradrénaline en raison de la fréquence plus élevée de dysfonctionnement hépatique, rénale ou cardiaque et de maladie concomitante ou autre traitement médicamenteux.
L'utilisation de la noradrénaline chez les enfants n'est pas recommandée (voir les rubriques 4.2 et 5.2).
La noradrénaline ne doit être utilisée que par des médecins familiarisés avec les indications sélectives de son utilisation.
Lorsque cela est indiqué, une thérapie appropriée de remplacement du sang ou des liquides, ainsi que l'adoption de la position couchée avec élévation des jambes, doivent être instituées et maintenues avant et/ou pendant la thérapie avec ce produit. Lors de la perfusion de noradrénaline, la pression artérielle et le débit doivent être vérifiés fréquemment pour éviter l'hypertension. Il est donc souhaitable d'enregistrer la pression artérielle toutes les deux minutes à partir du début de l'administration jusqu'à l'obtention de la pression artérielle souhaitée, puis toutes les cinq minutes par la suite, si l'administration doit être poursuivie. Le débit doit être surveillé en permanence et le patient ne doit jamais être laissé sans surveillance lorsqu'il reçoit de noradrénaline. L'hypertension peut éventuellement entraîner un œdème pulmonaire aigu, une arythmie ou un arrêt cardiaque.
La perfusion de noradrénaline doit être arrêtée progressivement, car un arrêt soudain peut entraîner une chute catastrophique de la pression artérielle.
Extravasation
Le site de perfusion doit être vérifié fréquemment pour s'assurer de l’écoulement du liquide de perfusion. Des précautions doivent être prises pour éviter l'extravasation de la noradrénaline dans les tissus, car une nécrose peut en résulter en raison de l'action vasoconstrictrice du médicament. Un blanchiment le long de la veine perfusée, parfois sans extravasation évidente, a été attribué à une constriction du vasa vasorum avec une perméabilité accrue de la paroi de la veine, permettant une certaine fuite. En de rares occasions, cela peut entrainer une mue superficielle des cellules nécrosées, en particulier lors de la perfusion dans les veines des jambes chez les patients âgés ou chez ceux qui souffrent d'une maladie vasculaire oblitérante. En cas de blanchiment, il faut envisager de changer le site de perfusion à intervalles réguliers pour permettre aux effets de la vasoconstriction locale de s'atténuer.
IMPORTANT - Antidote pour l'ischémie d'extravasation
Pour prévenir l'envasement et la nécrose dans les zones où l'extravasation a eu lieu, la zone doit être infiltrée le plus rapidement possible avec 10 mL à 15 mL de solution saline contenant de 5 mg à 10 mg de phentolamine, un agent bloquant adrénergique. Une seringue munie d'une fine aiguille hypodermique doit être utilisée avec la solution infiltrée généreusement dans toute la zone, ce qui est facilement identifiable par son aspect froid, dur et pâle. Un blocage sympathique avec de la phentolamine provoque des changements hyperémiques locaux immédiats et visibles si la zone est infiltrée dans les 12 heures. En cas d’extravasation, la perfusion doit être arrêtée et la zone doit être infiltrée avec de la phentolamine immédiatement.
Excipients
Ce médicament contient moins de 1 mmol de sodium (23 mg) par ampoules de 1 mL, 2 mL, 4 mL ou 5 mL de solution à diluer pour perfusion, c'est-à-dire qu’il est essentiellement « sans sodium ».
Ce médicament contient 26,4 mg (1,12 mmol) de sodium par ampoule de 8 mL de solution à diluer pour perfusion, ce qui équivaut à 1,32 % de l’apport alimentaire quotidien maximal recommandé par l’OMS de 2 g de sodium par adulte.
Ce médicament contient 33 mg (1,40 mmol) de sodium par ampoule de 10 mL de solution à diluer pour perfusion, ce qui équivaut à 1,65 % de l’apport alimentaire quotidien maximal recommandé par l’OMS de 2 g de sodium par adulte.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
· Anesthésiques volatils halogénés : arythmie ventriculaire sévère (augmentation de l'excitabilité cardiaque).
· Antidépresseurs imipraminiques : hypertension paroxystique avec possibilité d'arythmie (inhibition de l'entrée des sympathomimétiques dans les fibres sympathiques).
· Antidépresseurs sérotoninergiques-adrénergiques : hypertension paroxystique avec possibilité de troubles du rythme (inhibition de l'entrée des sympathomimétiques dans les fibres sympathiques).
· Glycosides digitaliques.
· Lévodopa.
· Chlorhydrate de chlorphéniramine, chlorhydrate de tripelennamine et désipramine : augmentent significativement la toxicité de la noradrénaline.
· Antihistaminiques, car certains peuvent bloquer l'absorption des catécholamines par les tissus périphériques et augmenter la toxicité de la noradrénaline injectée.
L'utilisation d'amines vasopressives avec du cyclopropane, de l'halothane, du chloroforme, de l'enflurane ou d'autres anesthésiques halogénés peut provoquer de graves arythmies cardiaques. En raison de la possibilité d'augmenter le risque de fibrillation ventriculaire, la noradrénaline doit être utilisée avec précaution chez les patients qui reçoivent ces produits ou tout autre agent de sensibilisation cardiaque ou qui présentent une hypoxie ou une hypercapnie profonde.
Associations faisant l’objet de précautions d'emploi
· Inhibiteurs non sélectifs de la monoamine oxydase (MAO) : augmentation de l'action pressive du sympathomimétique, le plus souvent modérée. A n’utiliser que sous contrôle médicale strict.
· Inhibiteurs sélectifs de la MAO-A : par extrapolation à partir des inhibiteurs non sélectifs de la MAO, risque d'augmentation de l'action pressive. A n’utiliser que sous contrôle médicale strict.
· Linézolide : par extrapolation à partir d'inhibiteurs MAO non sélectifs : risque d'augmentation de l'action pressive. A n’utiliser que sous contrôle médicale strict.
La noradrénaline doit être utilisée avec une précaution particulière chez les patients recevant des inhibiteurs de la MAO ou dans les 14 jours suivant l'arrêt de ce traitement.
Les effets de la noradrénaline peuvent être renforcés par la guanéthidine, le guanadrel, la réserpine, le méthyldopa ou les antidépresseurs tricycliques, l'amphétamine, le doxapram, le mazindol, les alcaloïdes rauwolfia.
La noradrénaline doit être utilisée avec précaution avec des alpha et bêta-bloquants, pouvant provoquer une hypertension sévère.
La noradrénaline doit être utilisée avec précaution avec les médicaments suivants pouvant provoquer des effets cardiaques accrus : hormones thyroïdiennes, glycosides cardiaques, antiarythmiques.
Les alcaloïdes de l'ergot (mésylates ergoloïdes, ergotamine, dihydroergotamine, ergométrine, méthylergométrine et méthysergide) ou l'ocytocine peuvent augmenter les effets vasopresseurs et vasoconstricteurs.
L'administration concomitante de propofol et de noradrénaline peut conduire au syndrome de perfusion du propofol (PRIS).
Desmopressine ou vasopressine : son effet antidiurétique est diminué.
Le lithium diminue l'effet de la noradrénaline.
Les solutions pour perfusion de noradrénaline ne doivent pas être mélangées avec d'autres médicaments (sauf ceux mentionnés à la rubrique 6.6).
4.6. Fertilité, grossesse et allaitement
Grossesse
La noradrénaline peut altérer la perfusion placentaire et induire une bradycardie fœtale. Elle pourrait également exercer un effet contractile sur l'utérus de la femme enceinte et conduire à une asphyxie fœtale en fin de grossesse. Ces risques possibles pour le fœtus doivent toutefois êtres comparés au bénéfice potentiel apporté à la mère.
Il n’est pas connu si ce médicament est excrété dans le lait maternel. Comme de nombreux médicaments sont excrétés dans le lait maternel, des précautions doivent être prises lorsque la noradrénaline est administrée à une femme qui allaite.
Fertilité
Aucune étude n'a été réalisée pour recueillir des données sur la fertilité pour la noradrénaline.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Le tableau 2 liste les effets indésirables qui ont été observés à la suite d'un traitement à la noradrénaline. Ces données ont été recueillies en grande partie à partir de déclarations spontanées et, en raison des problèmes de calcul de la fréquence des déclarations spontanées, la fréquence des effets indésirables énumérés est "inconnue" (ne peut être estimée à partir des données disponibles). Les effets indésirables sont répertoriés par ordre décroissant de fréquence par Système Classe-organe (SCO).
Tableau 2 : Effets indésirables signalés avec la noradrénaline par le biais de la déclaration spontanée
|
Système Classe-organe (SCO) |
Effets indésirables |
|
Troubles psychiatriques |
Anxiété, insomnie, confusion, faiblesse, état psychotique |
|
Troubles du système nerveux |
Céphalées transitoires, tremblements |
|
Troubles cardiaques |
Bradycardie1, arythmie, modification de l'électrocardiogramme, tachycardie, choc cardiogénique, cardiomyopathie d'effort, palpitations, augmentation de la contractilité du muscle cardiaque résultant de l'effet bêta-adrénergique sur le cœur (inotrope et chronotrope) |
|
Troubles vasculaires |
Hypertension, ischémie périphérique2, y compris gangrène des extrémités, diminution du volume plasmatique en cas d'utilisation prolongée, lésion ischémique due à une action vasoconstrictrice puissante pouvant entraîner une sensation de froid et une pâleur au niveau des membres |
|
Troubles gastro-intestinaux |
Nausées, vomissements |
|
Troubles de la peau et des tissus sous-cutanés |
Pâleur, scarification de la peau, couleur bleuâtre de la peau, bouffées de chaleur ou rougeurs de la peau, éruption cutanée, urticaire ou démangeaisons |
|
Troubles rénaux et urinaires |
Rétention d'urine |
|
Troubles respiratoires, thoraciques et médiastinaux |
Dyspnée |
|
Troubles généraux et anomalies au site d'administration |
Extravasation, nécrose au site d'injection |
1 Bradycardie, probablement due à un réflexe d'augmentation de la pression artérielle
2 Ischémie, due à une puissante action vasoconstrictrice et à une hypoxie tissulaire
L'administration continue d'un vasopresseur pour maintenir la pression artérielle en l'absence de remplissage vasculaire peut provoquer les symptômes suivants :
· vasoconstriction viscérale et périphérique sévère,
· diminution du flux sanguin rénal
· diminution de la production d'urine
· hypoxie
· augmentation des taux de lactate sérique.
En cas d'hypersensibilité ou de surdosage, les effets suivants peuvent apparaître plus fréquemment : hypertension, photophobie, douleur rétrosternale, douleur pharyngée, pâleur, sudation intense et vomissements.
L'effet vasopresseur (résultant de l'action adrénergique sur les vaisseaux) peut être réduit par l'administration concomitante d'un agent alpha-bloquant (mésilate de phentolamine) alors que l'administration d'un agent bêta-bloquant (propranolol) peut entraîner une réduction de l'effet stimulant du produit sur le cœur et une augmentation de l'effet hypertenseur (par la réduction de la dilatation artériolaire), résultant de la stimulation adrénergique bêta 1.
L'administration prolongée de tout vasopresseur puissant peut entraîner une déplétion du volume plasmatique qui doit être continuellement corrigée par une thérapie appropriée de remplacement de l'eau et des électrolytes. Si les volumes plasmatiques ne sont pas corrigés, l'hypotension peut réapparaître lorsque la perfusion de noradrénaline est interrompue, ou la pression artérielle peut être maintenue avec le risque d'une vasoconstriction périphérique et viscérale sévère accompagnée d'une diminution du flux sanguin.
Une hypertension peut se produire, qui peut être associée à une bradycardie ainsi qu'à des céphalées et à une ischémie périphérique, y compris une gangrène des extrémités.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.signalement-sante.gouv.fr.
Symptômes
Un surdosage peut entraîner des maux de tête, une hypertension sévère, une bradycardie réflexe, une augmentation marquée des résistances périphériques et un débit cardiaque diminué. Cela peut s'accompagner de maux de tête violents, d'hémorragies cérébrales, de photophobie, de douleurs rétrosternales, de pâleur, de fièvre, de transpiration intense, d'œdème pulmonaire et de vomissements.
Traitement
En cas de surdosage accidentel, comme le montre l'élévation excessive de la pression artérielle, il faut interrompre le médicament jusqu'à ce que l'état du patient se stabilise.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : Agents adrénergiques et dopaminergiques, Code ATC : C01CA03.
La noradrénaline apporte une très puissante stimulation des récepteurs alpha et un effet plus modéré sur les récepteurs bêta-1. La noradrénaline provoque une vasoconstriction généralisée, sauf pour les vaisseaux coronaires qu'elle dilate indirectement en augmentant la consommation d'oxygène. Il en résulte une augmentation de la force et (en l'absence d'inhibition vagale) de la vitesse de contraction du myocarde. La résistance périphérique augmente, et les pressions diastolique et systolique sont augmentées.
Les effets vasculaires de la noradrénaline aux doses habituellement utilisées en clinique résultent de la stimulation simultanée des récepteurs alpha et bêta-adrénergiques du cœur et du système vasculaire. Sauf dans le cœur, son action se fait principalement sur les récepteurs alpha. Il en résulte une augmentation de la force et (en l'absence d'inhibition vagale) de la vitesse de contraction du myocarde. La résistance périphérique augmente et les pressions diastolique et systolique sont relevées.
5.2. Propriétés pharmacocinétiques
Absorption
· Sous-cutanée : Faible
· Voie Orale : La noradrénaline est rapidement inactivée dans le tractus gastro-intestinal suite à une administration orale.
· Suite à une administration intraveineuse, la noradrénaline a une demi-vie plasmatique d'environ 1 à 2 minutes.
Distribution
La noradrénaline est rapidement éliminée du plasma par la recapture et le métabolisme cellulaire. Elle ne traverse pas facilement la barrière hémato-encéphalique.
Biotransformation
· Méthylation par la catéchol-O-méthyltransférase
· Désamination par la monoamine oxydase (MAO)
· Le métabolite ultime de ces deux voies de biotransformation est l'acide 4-hydroxy-3-méthoxymandélique
· Les métabolites intermédiaires comprennent la normétanéphrine et l'acide 3,4-dihydroxymandélique.
Élimination
La noradrénaline est principalement éliminée sous forme de glucuronoconjugués ou de sulfoconjugués des métabolites dans l'urine.
Jusqu'à 16 % d'une dose intraveineuse est excrétée sous forme inchangée dans l'urine avec les métabolites méthylés et désaminés sous forme libre et conjuguée.
Population pédiatrique
Aucune donnée sur l'expérience des études pharmacocinétiques dans les groupes d'âge pédiatriques n'est disponible.
5.3. Données de sécurité préclinique
La noradrénaline peut nuire à la perfusion placentaire et induire une bradycardie fœtale. Elle peut également exercer un effet contractile sur l'utérus de la femme enceinte et entraîner une asphyxie fœtale en fin de grossesse.
Ce médicament ne doit pas être mélangé avec d'autres médicaments, sauf ceux mentionnés à la rubrique 6.6.
Fermé :
1mL, 2 mL : 18 mois
4 mL, 5 mL, 8 mL, 10 mL : 2 ans
Durée de conservation après ouverture de l'ampoule
Une fois l’ampoule ouverte, la solution diluée doit être préparée immédiatement.
Durée de vie après dilution
La stabilité physico-chimique a été démontrée pendant 48 heures à 25°C et 2 - 8°C à la dilution à 4 mg/l et 40 mg/l de noradrénaline base dans une solution de chlorure de sodium à 9 mg/mL (0,9 %) ou une solution de glucose à 50 mg/mL (5 %), ou une solution de chlorure de sodium à 9 mg/mL (0,9 %) avec du glucose à 50 mg/mL (5 %).
D’un point de vue microbiologique, la solution diluée doit être utilisée immédiatement. En cas d’utilisation non immédiate, les durées et les conditions de conservation avant utilisation relèvent de la seule responsabilité de l’utilisateur et ne doivent normalement pas dépasser 24 heures entre 2 et 8°C, à moins que la dilution n'ait eu lieu dans des conditions aseptiques contrôlées et validées.
6.4. Précautions particulières de conservation
A conserver à une température ne dépassant pas 25°C.
Conserver les ampoules dans l’emballage extérieur, à l’abri de la lumière.
Pour les conditions de conservation du médicament après dilution, voir la rubrique 6.3.
6.5. Nature et contenu de l'emballage extérieur
1 mL, 2 mL, 4 mL, 5 mL, 8 mL ou 10 mL de solution en ampoules en verre incolore munies d’un système d’ouverture OPC (One Point Cut).
Les ampoules sont emballées dans une doublure et placées dans une boîte en carton.
Boîte de 5 ou 10 ampoules.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Pour usage unique seulement. Jeter tout contenu non utilisé.
La solution doit être inspectée visuellement avant utilisation. La solution ne doit pas être utilisée si elle contient des particules/solides visibles.
Ne pas utiliser la solution pour perfusion si celle-ci est de couleur marron.
Diluer avant utilisation dans :
· une solution de glucose à 50 mg/mL (5 %) ou
· une solution de chlorure de sodium à 9 mg/mL (0,9 %) ou
· une solution de chlorure de sodium à 9 mg/mL (0,9 %) avec du glucose à 50 mg/mL (5 %).
Ajouter soit 2 mL de solution à diluer à 48 mL de solution de glucose 50 mg/mL (5 %) (ou l'une des autres solutions susmentionnées pour la dilution) pour l'administration par pompe à seringue, soit ajouter 20 mL de solution à diluer à 480 mL de solution de glucose 50 mg/mL (5 %) (ou l'une des autres solutions susmentionnées pour la dilution) pour l'administration par compte-gouttes. Dans les deux cas, la concentration finale de la solution pour perfusion est de 40 mg/l de noradrénaline base (ce qui est équivalent à 80 mg/l de tartrate de noradrénaline). Des dilutions différentes de 40 mg/l de noradrénaline base peuvent aussi être utilisées (voir rubrique 4.2). En cas d’utilisation d’une dilution différente de 40 mg/l de noradrénaline base, vérifier attentivement le calcul du débit de perfusion avant le début du traitement.
Ce médicament est compatible avec les poches pour perfusion en chlorure de polyvinyle (PVC), en acétate d'éthyle et de vinyle (EVA) ou en polyéthylène (PE).
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation locale en vigueur.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
KRUSTPILS IELA 71E,
RĪGA, LV‑1057,
LETTONIE
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 550 738 1 9 : 1 mL en ampoule (verre). Boîte de 5.
· 34009 550 738 3 3 : 2 mL en ampoule (verre). Boîte de 5.
· 34009 550 738 4 0 : 4 mL en ampoule (verre). Boîte de 5.
· 34009 550 738 5 7 : 5 mL en ampoule (verre). Boîte de 5.
· 34009 550 738 6 4 : 8 mL en ampoule (verre). Boîte de 5.
· 34009 550 738 7 1 : 10 mL en ampoule (verre). Boîte de 5.
· 34009 550 738 8 8 : 1 mL en ampoule (verre). Boîte de 10.
· 34009 550 738 9 5 : 2 mL en ampoule (verre). Boîte de 10.
· 34009 550 739 0 1 : 4 mL en ampoule (verre). Boîte de 10.
· 34009 550 739 1 8 : 5 mL en ampoule (verre). Boîte de 10.
· 34009 550 739 2 5 : 8 mL en ampoule (verre). Boîte de 10.
· 34009 550 739 3 2 : 10 mL en ampoule (verre). Boîte de 10.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
Date de première autorisation:{JJ mois AAAA}
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
{JJ mois AAAA}
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Médicament réservé à l’usage hospitalier.
Réservé à l'usage en situation d'urgence selon l'article R5121-96 du code de la santé publique.
ANSM - Mis à jour le : 26/06/2024
NORADRENALINE TARTRATE KALCEKS 2 mg/mL, solution à diluer pour perfusion
Tartrate de noradrénaline
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre infirmier/ère.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que NORADRENALINE TARTRATE KALCEKS 2 mg/mL, solution à diluer pour perfusion et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser NORADRENALINE TARTRATE KALCEKS 2 mg/mL, solution à diluer pour perfusion ?
3. Comment utiliser NORADRENALINE TARTRATE KALCEKS 2 mg/mL, solution à diluer pour perfusion ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver NORADRENALINE TARTRATE KALCEKS 2 mg/mL, solution à diluer pour perfusion ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE NORADRENALINE TARTRATE KALCEKS 2 mg/mL, solution à diluer pour perfusion ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : Agents adrénergiques et dopaminergiques, Code ATC : C01CA03.
NORADRENALINE TARTRATE KALCEKS contient la substance active noradrénaline et agit comme vasoconstricteur (provoque le rétrécissement des vaisseaux sanguins).
NORADRENALINE TARTRATE KALCEKS est utilisé chez les adultes en cas d'urgence pour augmenter la pression artérielle à des niveaux normaux.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER NORADRENALINE TARTRATE KALCEKS 2 mg/mL, solution à diluer pour perfusion ?
N’utilisez jamais NORADRENALINE TARTRATE KALCEKS :
· si vous êtes allergique à la noradrénaline ou à l'un des autres composants contenus dans ce médicament (mentionnés dans la rubrique 6)
· si vous souffrez d'hypotension causée par un faible volume sanguin
· si vous recevez certains anesthésiques tels que l'halothane ou le cyclopropane (cela peut augmenter le risque de battements cardiaques irréguliers).
Avertissements et précautions
Adressez-vous à votre médecin ou à votre infirmier/ère avant de recevoir de la noradrénaline :
· si vous êtes diabétiques
· si vous avez une insuffisance hépatique
· si vous avez des troubles rénaux graves
· si vous souffrez d'hypertension artérielle
· si vous avez une glande thyroïde trop active
· si vous avez un faible taux d'oxygène dans le sang
· si vous présentez des niveaux élevés de dioxyde de carbone dans le sang
· si vous avez une pression élevée à l'intérieur du crâne (pression intracrânienne)
· si vous avez des caillots ou des obstructions dans les vaisseaux sanguins qui alimentent le cœur, les intestins ou d'autres parties du corps
· si vous souffrez d'hypotension à la suite d'une crise cardiaque
· si vous avez un type d'angine (douleur thoracique) appelé angine de Prinzmetal
· si vous souffrez d'un dysfonctionnement majeur du ventricule gauche (une maladie cardiaque)
· si vous avez eu récemment un infarctus du myocarde
· si vous souffrez de troubles du rythme cardiaque (votre cœur bat trop vite, trop lentement ou irrégulièrement), vous aurez besoin d'une dose réduite
· si vous êtes âgé(e)s
Enfants et adolescents
L'efficacité et la sécurité de la noradrénaline chez les enfants de moins de 18 ans n'ont pas été établies. Son utilisation chez les enfants n'est donc pas recommandée.
Autres médicaments et NORADRENALINE TARTRATE KALCEKS 2 mg/mL, solution à diluer pour perfusion
Informez votre médecin ou votre infirmier/ère si vous utilisez, avez récemment utilisé ou pourriez utiliser tout autre médicament. C'est particulièrement important si vous utilisez ou avez récemment utilisé l'un des médicaments suivants :
· les médicaments pour traiter la dépression appelés "inhibiteurs de la monoamine oxydase" qui sont actuellement pris ou qui l'ont été au cours des 14 derniers jours
· les médicaments pour traiter la dépression appelés "antidépresseurs tricycliques", par exemple l'imipramine ou la désipramine
· les médicaments adrénergiques-sérotoninergiques, utilisés par exemple dans le traitement de l'asthme et des maladies cardiaques
· linézolide (un antibiotique)
· les anesthésiques (en particulier les gaz anesthésiques tels que le cyclopropane, l'halothane, le chloroforme, l'enflurane)
· les médicaments pour traiter l'hypertension artérielle (par exemple, guanéthidine, réserpine, méthyldopa, alpha et bêta-bloquants)
· des médicaments pour traiter les troubles du rythme cardiaque
· glycosides cardiaques (pour traiter les maladies cardiaques)
· lévodopa (pour traiter la maladie de Parkinson)
· les hormones thyroïdiennes
· l'ocytocine (utilisée pour améliorer les contractions utérines)
· les antihistaminiques (pour le traitement des allergies)
· amphétamine
· doxapram (pour les troubles respiratoires)
· mazindol (pour traiter l'obésité)
· les médicaments pour traiter la migraine (alcaloïdes de l'ergot)
· le lithium (pour traiter certains troubles mentaux)
L'utilisation de noradrénaline avec du propofol (un anesthésique) peut conduire au syndrome de perfusion du propofol (SPP), une maladie grave qui touche les patients sous sédatifs au propofol dans les unités de soins intensifs. Votre médecin constaterait des troubles du métabolisme de votre corps à partir d'analyses sanguines et cela pourrait entraîner une insuffisance rénale, une défaillance cardiaque et la mort.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin avant que ce médicament ne vous soit administré. La noradrénaline peut être nocive pour le foetus. Votre médecin décidera si vous devez recevoir de la noradrénaline.
Aucune information n’est disponible sur l’excrétion de ce médicament dans le lait maternel. Comme de nombreux médicaments sont excrétés dans le lait maternel, des précautions doivent être prises lorsque la noradrénaline est administrée à une femme qui allaite.
Conduite de véhicules et utilisation de machines
Aucune information n'est disponible. Il n'est donc pas recommandé de conduire ou de faire fonctionner des machines.
NORADRENALINE TARTRATE KALCEKS contient du sodium
Ce médicament contient moins de 1 mmol de sodium (23 mg) par ampoules de 1 mL, 2 mL, 4 mL ou 5 mL de solution à diluer pour perfusion, c'est-à-dire qu’il est essentiellement « sans sodium »
Ce médicament contient 26,4 mg de sodium (composant principal du sel de cuisine/table) par ampoule de 8 mL de solution à diluer pour perfusion. Cela équivaut à 1,32 % de l’apport alimentaire quotidien maximal recommandé de sodium pour un adulte.
Ce médicament contient 33 mg de sodium (composant principal du sel de cuisine/table) par ampoule de 10 mL de solution à diluer pour perfusion, Cela équivaut à 1,65 % de l’apport alimentaire quotidien maximal recommandé de sodium pour un adulte.
3. COMMENT UTILISER NORADRENALINE TARTRATE KALCEKS 2 mg/mL, solution à diluer pour perfusion ?
La dose initiale de noradrénaline dépendra de votre état de santé. La dose habituelle se situe entre 0,4 mg et 0,8 mg de noradrénaline par heure. Votre médecin déterminera la dose correcte pour vous. Après la dose initiale, votre médecin évaluera votre réponse et ajustera la dose en conséquence.
Votre médecin surveillera votre tension artérielle et votre volume sanguin.
Si vous avez utilisé plus de NORADRENALINE TARTRATE KALCEKS que vous n’auriez dû
Il est peu probable que vous en receviez trop, car ce médicament vous sera administré à l'hôpital. Toutefois, si vous avez des inquiétudes, parlez-en à votre médecin ou à votre infirmier/ère.
En cas de surdosage avec la noradrénaline, les symptômes qui peuvent être observés sont : une hypertension artérielle sévère, un rythme cardiaque lent, de violents maux de tête, une sensibilité à la lumière, des douleurs dans la poitrine, des saignements dans le cerveau, une pâleur, de la fièvre, une transpiration intense et des vomissements, du liquide dans les poumons provoquant un essoufflement.
Si vous oubliez d’utiliser NORADRENALINE TARTRATE KALCEKS
Sans objet.
Si vous arrêtez d’utiliser NORADRENALINE TARTRATE KALCEKS
Sans objet.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Informez immédiatement votre médecin ou votre infirmier/ère si vous avez :
· des démangeaisons soudaines (urticaire), un gonflement des mains, des pieds, des chevilles, du visage, des lèvres, de la bouche ou de la gorge (qui peut entraîner des difficultés à avaler ou à respirer), la sensation que vous allez vous évanouir
· une douleur et/ou un gonflement au point d'injection.
Informez votre médecin ou votre infirmier/ère dès que possible si vous avez :
· anxiété, insomnie, confusion, faiblesse, état psychotique
· maux de tête, tremblements
· diminution ou augmentation du rythme cardiaque
· un rythme cardiaque anormal
· modification de l'électrocardiogramme
· un type d'insuffisance circulatoire potentiellement mortellement grave appelé « choc cardiogénique ».
· faiblesse du muscle cardiaque due à un stress physique ou émotionnel intense, palpitations, augmentation de la contractilité du muscle cardiaque
· hypertension artérielle, diminution de l'apport d'oxygène à certains organes (hypoxie)
· une mauvaise circulation sanguine aux mains et aux pieds (peut provoquer un refroidissement, une pâleur et/ou des douleurs dans les membres)
· gangrène (mort des tissus)
· la réduction du volume du plasma sanguin
· les difficultés respiratoires
· pâleur, scarification de la peau, couleur bleuâtre de la peau, bouffées de chaleur ou rougeurs de la peau, éruption cutanée, urticaire ou démangeaisons
· nausées, vomissements
· la rétention d'urine
· une irritation ou une ulcération au point d'injection
En cas d'hypersensibilité ou de surdosage, les effets suivants peuvent apparaître plus fréquemment : très haute pression artérielle, sensibilité ou intolérance anormale à la lumière, douleur derrière le sternum, douleur pharyngée, pâleur, transpiration intense et vomissements.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou à votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.signalement-sante.gouv.fr
5. COMMENT CONSERVER NORADRENALINE TARTRATE KALCEKS 2 mg/mL, solution à diluer pour perfusion ?
Tenir ce médicament hors de la vue et de la portée des enfants.
A conserver à une température ne dépassant pas 25°C.
Conserver les ampoules dans l’emballage extérieur, à l’abri de la lumière.
Durée de conservation après ouverture de l'ampoule
Une fois ouverte, la solution diluée doit être préparée immédiatement.
Durée de vie après dilution
La stabilité physico-chimique a été démontrée pendant 48 heures à 25°C et 2 - 8°C à la dilution à 4 mg/l et 40 mg/l de noradrénaline base dans une solution de chlorure de sodium à 9 mg/mL (0,9 %) ou une solution de glucose à 50 mg/mL (5 %), ou une solution de chlorure de sodium à 9 mg/mL (0,9 %) avec du glucose à 50 mg/mL (5 %).
D’un point de vue microbiologique, la solution diluée doit être utilisée immédiatement. En cas d’utilisation non immédiate, les durées et les conditions de conservation avant utilisation relèvent de la seule responsabilité de l’utilisateur et ne devraient normalement pas dépasser 24 heures entre 2 et 8 °C, à moins que la dilution n'ait eu lieu dans des conditions aseptiques contrôlées et validées.
N'utilisez pas ce médicament après la date de péremption qui est indiquée sur l'étiquette du carton et de l'ampoule après EXP. La date de péremption se réfère au dernier jour du mois.
Ne jetez aucun médicament dans les eaux usées ou dans les ordures ménagères. Demandez à votre pharmacien comment jeter les médicaments que vous n'utilisez plus. Ces mesures contribueront à protéger l'environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient NORADRENALINE TARTRATE KALCEKS
· La substance active est :
Tartrate de noradrénaline ............................................................................................... 2,00 mg
Pour 1 mL de solution
Chaque ampoule de 2 mL de solution à diluer pour perfusion contient du tartrate de noradrénaline, équivalent à 2 mg de noradrénaline.
Chaque ampoule de 4 mL de solution à diluer pour perfusion contient du tartrate de noradrénaline, équivalent à 4 mg de noradrénaline.
Chaque ampoule de 5 mL de solution à diluer pour perfusion contient du tartrate de noradrénaline, équivalent à 5 mg de noradrénaline.
Chaque ampoule de 8 mL de solution à diluer pour perfusion contient du tartrate de noradrénaline, équivalent à 8 mg de noradrénaline.
Chaque ampoule de 10 mL de solution à diluer pour perfusion contient du tartrate de noradrénaline, équivalent à 10 mg de noradrénaline.
· Les autres composants sont :
Chlorure de sodium, acide chlorhydrique (pour l'ajustement du pH), eau pour préparations injectables.
Solution limpide, incolore ou jaunâtre, pratiquement exempte de particules visibles.
Boîte de : 5 ou 10 ampoules
Tous les formats d'emballage ne peuvent pas être commercialisés.
Titulaire de l’autorisation de mise sur le marché
KRUSTPILS IELA 71E
RĪGA, LV‑1057
LETTONIE
Exploitant de l’autorisation de mise sur le marché
84 QUAI JOSEPH GILLET
69004 LYON
KRUSTPILS IELA 71E
RĪGA, LV‑1057
LETTONIE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[À compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
Les informations suivantes sont destinées exclusivement aux professionnels de la santé :
Mode d'administration
Voie intraveineuse après dilution.
Ne pas utiliser non dilué.
Incompatibilités
Il a été rapporté que les solutions pour perfusion contenant du tartrate de noradrénaline sont incompatibles avec les substances suivantes : sels de fer, alcalis et agents oxydants, barbituriques, chlorphéniramine, chlorothiazide, nitrofurantoïne, novobiocine, phénytoïne, bicarbonate de sodium, iodure de sodium, streptomycine, sulfadiazine, sulfafurazole.
Ce médicament ne doit pas être mélangé avec d'autres médicaments, sauf ceux mentionnés ci-dessous.
Instructions pour la dilution
A usage unique. Jeter tout contenu non utilisé.
La solution doit être inspectée visuellement avant utilisation. Le médicament ne doit pas être utilisé si la solution contient des particules/solides visibles. N'utilisez pas la solution pour perfusion si celle-ci est de couleur marron.
Diluer avant utilisation dans :
· une solution de glucose à 50 mg/mL (5 %) ou
· une solution de chlorure de sodium à 9 mg/mL (0,9 %) ou
· une solution de chlorure de sodium à 9 mg/mL (0,9 %) avec du glucose à 50 mg/mL (5 %).
Ajouter soit 2 mL de solution à diluer à 48 mL de solution de glucose 50 mg/mL (5 %) (ou l'une des autres solutions susmentionnées pour la dilution) pour l'administration par pompe à seringue, soit ajouter 20 mL de solution à diluer à 480 mL de solution de glucose 50 mg/mL (5 %) (ou l'une des autres solutions susmentionnées pour la dilution) pour l'administration par compte-gouttes. Dans les deux cas, la concentration finale de la solution pour perfusion est de 40 mg/l de noradrénaline base (ce qui est équivalent à 80 mg/l de tartrate de noradrénaline). Des dilutions différentes de 40 mg/l de noradrénaline base peuvent aussi être utilisées. En cas d’utilisation d’une dilution différente de 40 mg/l de noradrénaline base, vérifier attentivement le calcul du débit de perfusion avant le début du traitement.
Ce médicament est compatible avec les poches pour perfusion en chlorure de polyvinyle (PVC), en acétate d'éthyle et de vinyle (EVA) ou en polyéthylène (PE).
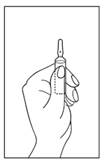
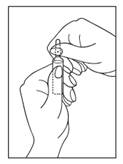
Instruction d'ouverture de l'ampoule
1) Tourner l'ampoule avec la pointe colorée vers le haut. S'il y a de la solution dans la partie supérieure de l'ampoule, taper doucement avec votre doigt pour faire passer toute la solution dans la partie inférieure de l'ampoule.
2) Utiliser les deux mains pour ouvrir ; tout en tenant la partie inférieure de l'ampoule dans une main, utiliser l'autre main pour casser la partie supérieure de l'ampoule dans la direction opposée au point coloré (voir les photos ci-dessous).
|
|
|
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation locale en vigueur.