
ANSM - Mis à jour le : 17/01/2025
GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie
Acétate de glatiramère
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
2. Quelles sont les informations à connaître avant d'utiliser GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie ?
3. Comment utiliser GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie?
6. Contenu de l’emballage et autres informations.

GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie est un médicament, indiqué dans le traitement des formes rémittentes de sclérose en plaques (SEP). Il modifie la manière dont fonctionne le système immunitaire de votre corps et il est classé comme agent immunomodulateur. On attribue les symptômes de la sclérose en plaques (SEP) à un dysfonctionnement du système immunitaire de l’organisme. Il en résulte une inflammation sous forme de plaques au niveau du cerveau et de la moelle épinière.
GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie est utilisé pour réduire le nombre de poussées de SEP. Son efficacité n’a pas été démontrée si vous présentez une forme de SEP sans poussées ou avec peu de poussées.
GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie peut n’avoir aucun effet sur la durée ou la sévérité d’une poussée de SEP dont vous souffrez.

N’utilisez jamais GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie :
· si vous êtes allergique à l’acétate de glatiramère ou à l’un des autres composants contenus dans ce médicament (mentionnés dans la rubrique 6).
Avertissements et précautions
Adressez-vous à votre médecin ou pharmacien avant d’utiliser GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie :
· si vous avez une insuffisance rénale ou des troubles cardiaques, car vous serez probablement soumis à des examens réguliers.
· si vous avez ou avez eu des troubles hépatiques (y compris ceux dus à la consommation d’alcool).
GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie peut provoquer des réactions allergiques sévères qui peuvent parfois menacer le pronostic vital. Ces réactions peuvent survenir peu de temps après l’administration, mais également plusieurs mois voire plusieurs années après le début du traitement, et ce même si les précédentes administrations n’ont pas entraîné de réaction allergique.
Les signes et symptômes de réactions allergiques et de réactions post-injection peuvent être identiques. Votre médecin vous expliquera quels sont les signes d’une réaction allergique.
Enfants
GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie ne doit pas être utilisé chez l'enfant de moins de 18 ans.
Personnes âgées
GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie n'a pas été spécifiquement étudié chez le sujet âgé. Demandez conseil à votre médecin.
Autres médicaments et GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie avec des aliments, boissons et de l’alcool
Sans objet.
Si vous êtes enceinte, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil et avis auprès de votre médecin à propos d’un traitement par GLATIRAMER VIATRIS 40 mg/ml solution injectable en seringue préremplie pendant la grossesse.
GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie peut être utilisé pendant la grossesse sur avis de votre médecin.
Des données limitées chez l'homme n'ont montré aucun effet négatif de l'acétate de glatiramère sur les nouveau-nés/nourrissons allaités. GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie peut être utilisé pendant l'allaitement.
Conduite de véhicules et utilisation de machines
GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie n’est pas connu pour influencer l’aptitude à conduire des véhicules ou à utiliser des machines.
GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie contient
Sans objet.

Chez l'adulte, la dose recommandée est d’une seringue préremplie (40 mg d'acétate de glatiramère) administrée sous la peau (par voie sous-cutanée) trois fois par semaine, à au moins 48 heures d’intervalle, par exemple les lundi, mercredi et vendredi. Il est recommandé d’administrer le médicament les mêmes jours chaque semaine.
Il est très important d’injecter correctement GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie :
· Uniquement dans le tissu situé sous la peau (tissu sous-cutané) (voir “Instructions d’utilisation”, ci- dessous).
· En respectant la dose indiquée par votre médecin. Prenez uniquement la dose prescrite par votre médecin.
· N’utilisez jamais la même seringue plus d’une fois. Jetez tout produit inutilisé ou déchet.
· Ne mélangez pas ou n’administrez pas en même temps le contenu des seringues préremplies de GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie avec un autre produit.
· Si la solution contient des particules, ne l’utilisez pas. Utilisez une nouvelle seringue.
La première fois que vous utilisez GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie, vous recevrez des instructions complètes et serez supervisé par un médecin ou une infirmière. Ils resteront près de vous pendant que vous réaliserez votre injection et pendant les 30 minutes suivant l'injection afin de s'assurer que vous n'avez aucun problème.
Instructions d’utilisation
Lisez attentivement ces instructions avant d’utiliser GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie.
Avant l’injection, vérifiez que vous avez tout ce dont vous avez besoin :
· Une seringue préremplie de GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie dans son conditionnement individuel (plaquette).
· Le récipient destiné à la récupération des seringues et des aiguilles usagées.
· Pour chaque injection, ne sortez de la boîte qu'une seule plaquette contenant une seringue préremplie. Laissez les autres seringues dans la boîte.
· Si votre seringue a été conservée au réfrigérateur, sortez la plaquette contenant la seringue au moins 20 minutes avant votre injection, afin que la solution atteigne la température ambiante.
Lavez soigneusement vos mains à l’eau et au savon.
Si vous souhaitez utiliser un dispositif d’injection pour effectuer votre injection, le dispositif MYJECT peut être utilisé avec GLATIRAMER VIATRIS. Le dispositif MYJECT n’est approuvé que dans le cadre d’une utilisation avec GLATIRAMER VIATRIS et n’a pas été testé avec d’autres produits. Veuillez consulter le mode d'emploi fourni avec le dispositif d’injection MYJECT.
Choisissez un site d'injection se situant dans les zones, selon les schémas.
Vous disposez de sept zones possibles où injecter le médicament :
· Zone 1 : Région du ventre (abdomen) autour du nombril. Evitez d’injecter à moins de 5 cm autour du nombril,
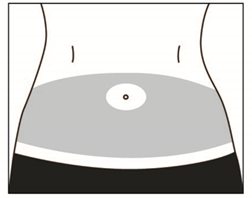
· Zone 2 et 3 : Cuisses (au-dessus des genoux),
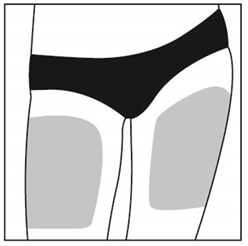
· Zone 4, 5, 6 et 7 : Arrière de la partie supérieure des bras, et de la partie supérieure des hanches (en dessous de la taille).
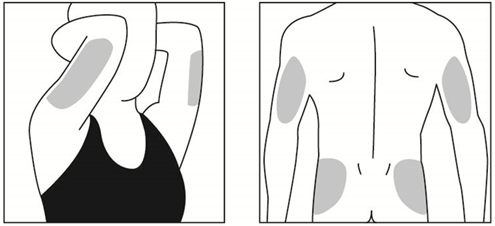
Chaque zone d'injection comporte plusieurs sites d'injection. Choisissez un site d'injection différent chaque jour. Cela réduira le risque d’irritation ou de douleur au site d’injection. Alternez les sites d’injection dans une même zone. N'utilisez pas le même site à chaque fois.
Remarque : n’injectez pas à un endroit qui est douloureux ou décoloré ou qui comporte une induration. Il est recommandé de respecter un ordre planifié de rotation des sites d’injection et de noter les sites utilisés dans un agenda. Vous aurez peut-être des difficultés à injecter dans certaines zones de votre corps (comme la partie arrière de vos bras), et pourriez avoir besoin d’aide.
Comment réaliser l’injection :
· Retirez la seringue de son emballage de protection en décollant le film qui recouvre la plaquette.
· Retirez l'embout de protection de l'aiguille, ne retirez pas l’embout avec votre bouche ou avec vos dents.
· Pincez doucement la peau entre le pouce et l’index de la main libre (Figure 1).
· Insérez l’aiguille dans la peau de la manière décrite sur la Figure 2.
· Injectez le médicament en enfonçant complètement le piston de manière régulière, jusqu’à ce que la seringue soit vide.
· Enlevez d’une manière droite la seringue et l’aiguille.
· Jetez la seringue dans le récipient de récupération des déchets. Ne jetez pas les seringues usagées dans la poubelle de la maison mais dans le récipient spécifique résistant à la perforation, selon la recommandation de votre médecin ou votre infirmier/ère.
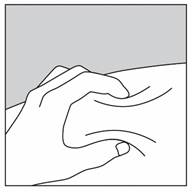

Figure 1 Figure 2
Si vous avez l'impression que l'effet de GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie est trop fort ou trop faible, parlez-en à votre médecin.
Si vous avez utilisé plus de GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie que vous n’auriez dû :
Consultez immédiatement votre médecin.
Si vous oubliez d’utiliser GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie :
Utilisez le traitement dès que vous réalisez votre oubli ou dès que vous le pouvez, puis ne faites pas d’injection le jour suivant. N’utilisez pas de dose double pour compenser la dose individuelle oubliée. Si possible, respectez à nouveau la fréquence régulière d’administration la semaine suivante.
Si vous arrêtez d’utiliser GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie :
N’interrompez pas votre traitement par GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie sans consulter votre médecin.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.

Réactions allergiques (hypersensibilité, réaction anaphylactique)
Une réaction allergique grave à ce médicament peut se produire peu de temps après l’administration. Il s’agit d’un effet indésirable peu fréquent. Ces réactions peuvent également survenir plusieurs mois voire plusieurs années après le début du traitement par GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie, même si les précédentes administrations n’ont pas entraîné de réaction allergique.
Arrêtez d’utiliser GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie et prévenez immédiatement votre médecin ou rendez-vous dans le service médical d'urgence de l’hôpital le plus proche, si vous constatez la survenue soudaine de l'un des effets indésirables suivants :
· éruption cutanée étendue (boutons rouges ou urticaire),
· gonflement des paupières, du visage, des lèvres, de la bouche, de la gorge ou de la langue,
· essoufflement soudain, difficultés pour respirer ou respiration sifflante,
· convulsions (crises),
· difficultés à avaler ou à parler,
· syncope, étourdissement ou évanouissement,
· état de choc.
Autres réactions suivant l’injection (réactions immédiates post-injection)
Certaines personnes peuvent présenter un ou plusieurs des symptômes suivants, dans les minutes suivant l'injection de GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie. Ces réactions sont généralement sans gravité et disparaissent habituellement au bout de 30 minutes.
Toutefois, si les symptômes suivants durent plus de 30 minutes, avertissez immédiatement votre médecin ou rendez-vous dans le service d’urgence de l’hôpital le plus proche :
· rougeur du torse ou du visage (vasodilatation),
· difficulté respiratoire (dyspnée),
· douleur dans la poitrine,
· battements cardiaques rapides et forts (palpitations, tachycardie).
Problèmes hépatiques
Des problèmes hépatiques ou une aggravation des problèmes hépatiques, y compris une insuffisance hépatique (certains cas nécessitant une transplantation hépatique) peuvent rarement se produire avec GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie.
Contactez immédiatement votre médecin si vous présentez des symptômes, tels que :
· nausées,
· perte d'appétit,
· urine de couleur foncée et selles pâles,
· jaunissement de la peau ou de la partie blanche de l’œil,
· saignements apparaissant plus facilement que d'habitude.
D’une façon générale, les effets indésirables rapportés chez les patients traités par l’acétate de glatiramère 40 mg/ml trois fois par semaine ont également été rapportés chez les patients traités par l’acétate de glatiramère 20 mg/ml (voir liste ci-dessous).
Les effets indésirables suivants ont été rapportés avec l’acétate de glatiramère :
Très fréquent (pouvant affecter plus de 1 personne sur 10) :
· infections, grippe,
· anxiété, dépression,
· maux de tête,
· nausées,
· éruption cutanée,
· douleur des articulations ou du dos,
· sensation de faiblesse, réactions cutanées au site d'injection incluant rougeur de la peau, douleur, formation de papules, démangeaisons, gonflement des tissus, inflammation et hypersensibilité (ces réactions au site d'injection ne sont pas inhabituelles et diminuent généralement avec le temps),
· douleur non spécifique.
Fréquent (pouvant affecter jusqu’à 1 personne sur 10) :
· inflammation des voies respiratoires, grippe intestinale, bouton de fièvre, otite, nez qui coule, abcès dentaires, mycose vaginale,
· tumeur cutanée non maligne (néoplasme non malin de la peau), tumeurs des tissus (néoplasme),
· gonflement des ganglions lymphatiques,
· réactions allergiques,
· perte d’appétit, prise de poids,
· nervosité,
· altération du goût, hypertonicité musculaire, migraine, problèmes d’élocution, syncope, tremblements,
· vision double, problèmes oculaires,
· affection de l’oreille,
· toux, rhume des foins,
· problèmes au niveau de l’anus ou du rectum, constipation, caries dentaires, indigestion, difficultés à avaler, incontinence fécale, vomissements,
· anomalie des tests de la fonction hépatique,
· ecchymoses, transpiration excessive, démangeaisons, affections de la peau, urticaire,
· douleur dans le cou,
· besoin d’uriner impérieux ou fréquent, incapacité à vider complètement votre vessie,
· frissons, gonflement du visage, amincissement du tissu sous-cutané au site d’injection, réaction locale, œdème périphérique dû à l’accumulation de liquide, fièvre.
Peu fréquent (pouvant affecter jusqu'à 1 personne sur 100) :
· abcès, inflammation de la peau et des tissus mous sous-cutanés, furoncles, zona, inflammation des reins,
· cancer de la peau,
· modification du nombre de globules blancs (augmentation ou diminution), augmentation du volume de la rate, diminution du nombre de plaquettes, modification de la forme des globules blancs,
· augmentation de volume ou hyperactivité de la thyroïde,
· faible tolérance à l'alcool, goutte, augmentation des graisses (lipides) dans le sang, augmentation du taux de sodium dans le sang, diminution de la ferritine dans le sang,
· rêves étranges, confusion, euphorie, hallucinations (voir, entendre, sentir, gouter ou ressentir des choses qui n’existent pas), agressivité, altération de l’humeur, modification de la personnalité, tentative de suicide,
· engourdissement et douleur de la main (syndrome du canal carpien), troubles mentaux, crises (convulsions), troubles de l'écriture et de la lecture, troubles musculaires, troubles du mouvement, spasmes musculaires, inflammation des nerfs, anomalie des connections neuromusculaires entraînant un fonctionnement musculaire anormal, mouvements involontaires rapides des yeux, paralysie, impossibilité de relever le pied (sciatique paralysante), état inconscient (stupeur), déficit du champ visuel,
· cataracte, lésion de la cornée, sécheresse oculaire, saignement oculaire, paupière tombante, dilatation de la pupille, atteinte du nerf optique entraînant des troubles de la vue,
· augmentation des battements cardiaques, battements cardiaques lents ou rapides,
· varices,
· apnée, saignement de nez, respiration anormalement rapide ou profonde (hyperventilation), sensation de gorge serrée, troubles pulmonaires, sensation d’étouffement,
· inflammation du côlon ou de l’intestin, polypes du côlon, éructations, ulcère de l'œsophage, inflammation des gencives, saignement rectal, augmentation de volume des glandes salivaires
· calculs biliaires, augmentation du volume du foie,
· gonflement de la peau et des tissus mous, éruption cutanée de contact, nodules cutanés rouges et douloureux, nodules cutanés,
· gonflement, inflammation et douleur des articulations (arthrite ou ostéoarthrite), inflammation du liquide synovial (existant dans certaines articulations) et douleurs, douleur au flanc, diminution de la masse musculaire,
· sang dans les urines, calculs rénaux, affection des voies urinaires, urines anormales,
· gonflement des seins, difficultés à obtenir une érection, descente d’organes pelviens (prolapsus pelvien), érection prolongée, troubles de la prostate, test de Papanicolaou anormal (frottis vaginal anormal), troubles des testicules, saignement vaginal, troubles vaginaux,
· kyste, sensation de gueule de bois, température corporelle inférieure à la normale (hypothermie), inflammation non spécifique, destruction des tissus au site d'injection, problèmes au niveau des muqueuses,
· troubles après une vaccination.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.

Tenir ce médicament hors de la vue et de la portée des enfants.
A conserver au réfrigérateur (entre 2°C et 8°C).
Les seringues préremplies de GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie peuvent être conservées, une seule fois, jusqu’à un mois hors du réfrigérateur, entre 15°C et 25°C. Après un mois, toute seringue préremplie de GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie non utilisée et toujours dans son emballage d’origine doit être remise au réfrigérateur.
Ne pas congeler.
Conserver les seringues préremplies dans l’emballage, à l’abri de la lumière.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’étiquette et l’emballage extérieur après EXP. Les deux premiers chiffres indiquent le mois et les quatre derniers chiffres indiquent l’année. La date de péremption fait référence au dernier jour de ce mois.
Jeter toute seringue contenant des particules.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.

Ce que contient GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie 
· La substance active est : l’acétate de glatiramère.
1 ml de solution injectable (le contenu d’une seringue préremplie) contient 40 mg d’acétate de glatiramère.
· Les autres composants sont :
Mannitol et eau pour préparations injectables.
Qu’est-ce que GLATIRAMER VIATRIS 40 mg/ml, solution injectable en seringue préremplie et contenu de l’emballage extérieur 
Si la solution contient des particules, jetez-la et recommencez. Utilisez une nouvelle seringue.
3 seringues préremplies.
12 seringues préremplies.
36 (3x12) seringues préremplies.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché 
1 BIS PLACE DE LA DEFENSE – TOUR TRINITY
92400 COURBEVOIE
Exploitant de l’autorisation de mise sur le marché 
1 BIS PLACE DE LA DEFENSE – TOUR TRINITY
92400 COURBEVOIE
C/ CASTELLÓ No.1
POL. LAS SALINAS
08830 SANT BOI DE LLOBREGAT
ESPAGNE
Ou
SYNTHON BV
MICROWEG 22,
6545 CM NIJMEGEN
PAYS-BAS
Noms du médicament dans les Etats membres de l'Espace Economique Européen 
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen et au Royaume-Uni (Irlande du Nord) sous les noms suivants : Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
L’auto-injecteur réutilisable est autorisé dans les Etats membres de l'Espace Economique Européen et au Royaume-Uni (Irlande du Nord) sous les noms suivants :
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est : 
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
|
| Plan du site | Accessibilité | Contact | Téléchargement | Declaration de confidentialité | Service-Public.fr | Legifrance | Gouvernement.fr |