Dernière mise à jour le 08/01/2026
OXYCODONE SANDOZ 10 mg, gélule
Indications thérapeutiques
Classe pharmacothérapeutique : analgésique opioïde, Code ATC : N02AA05.
Ce médicament est un analgésique opioïde (destiné à soulager la douleur).
OXYCODONE SANDOZ est utilisé chez les adultes et les adolescents à partir de 12 ans pour le traitement des douleurs intenses qui ne peuvent être correctement traitées que par des analgésiques forts, notamment les douleurs cancéreuses.
Présentations
> plaquette(s) PVC PVDC aluminium de 14 gélule(s)
Code CIP : 34009 300 688 9 2
Déclaration de commercialisation : 11/09/2018
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 2,00 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 3,02 €
- Taux de remboursement :65%
Documents de bon usage du médicament
- Prévenir le risque de surdose d’opioïdes
Auteur : Haute autorité de santé
Type : Fiche Bon Usage du Médicament
Date de mise à jour :Avril 2023
- Prise en charge médicamenteuse de la douleur chez l'enfant : alternatives à la codéine
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Février 2016
- Les médicaments des accès douloureux paroxystiques du cancer
Auteur : Haute autorité de santé
Type : Fiche Bon Usage du Médicament
Date de mise à jour :Juin 2014
Service médical rendu (SMR)
Amélioration du service médical rendu (ASMR)
Ce médicament étant un générique, l'ASMR n'a pas été évalué par la commission de la transparence (CT), il est possible de se référer à la /aux spécialité(s) de référence du groupe générique auquel appartient ce médicament (cliquez ici pour aller à la rubrique des groupes génériques)
Autres informations
- Titulaire de l'autorisation : SANDOZ
- Conditions de prescription et de délivrance :
- prescription en toutes lettres sur ordonnance sécurisée
- prescription limitée à 4 semaines
- stupéfiants
- Statut de l'autorisation : Valide
- Type de procédure : Procédure nationale
- Code CIS : 6 974 635 8
ANSM - Mis à jour le : 18/02/2025
OXYCODONE SANDOZ 10 mg, gélule
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chlorhydrate d’oxycodone................................................................................................... 10,0 mg
équivalant à oxycodone base........................................................................................................ 9,0 mg
Pour la liste complète des excipients, voir rubrique 6.1.
Gélule blanche (corps) et marron (tête), de taille 4, avec une impression « 10 » (corps) et « OXY » (tête).
4.1. Indications thérapeutiques
OXYCODONE SANDOZ est indiqué chez les adultes et les adolescents à partir de 12 ans dans le traitement des douleurs sévères qui ne peuvent être correctement traitées que par des analgésiques opioïdes forts, en particulier dans les douleurs d'origine cancéreuse.
4.2. Posologie et mode d'administration
Réservé à l'adulte et à l’adolescent à partir de 12 ans.
Comme pour tous les médicaments antalgiques, la posologie doit être adaptée à l'intensité de la douleur et à la réponse efficacité-tolérance du patient. Les traitements antalgiques antérieurs et concomitants du patient, son poids corporel et son sexe (des concentrations plasmatiques plus élevées sont produites chez les femmes) doivent également être pris en considération lors de la détermination de la posologie.
En règle générale, la dose efficace la plus faible pour l'analgésie doit être choisie pour la durée la plus courte possible.
Posologie initiale
Patients recevant des opioïdes forts pour la première fois
Utiliser le dosage 5 mg toutes les 4 à 6 heures.
Patients antérieurement traités par des opioïdes forts
La dose initiale est à déterminer en fonction de l'équivalent de la dose quotidienne de morphine prise antérieurement.
A titre indicatif et en absence d'équivalence clairement établie, le rapport d'équianalgésie est le suivant : 10 mg d'oxycodone par voie orale sont équivalents à 20 mg de morphine orale. La dose d'oxycodone sera donc environ la moitié de la dose de morphine administrée précédemment.
Cependant, la variabilité inter-patients nécessite que chaque patient soit soigneusement titré à la dose appropriée. Initialement, une dose inférieure à l’équivalence peut être recommandée.
Patients âgés, patients amaigris
L'administration d'oxycodone doit être prudente. Débuter le traitement à la dose la plus faible, 5 mg toutes les 4 à 6 heures afin de minimiser l’incidence des effets indésirables. La dose sera ensuite ajustée individuellement en fonction de l'état clinique du patient.
Patients présentant une insuffisance hépatique, une insuffisance rénale
L’initiation du traitement doit suivre une approche conservatrice chez ces patients. La posologie initiale recommandée chez l'adulte doit être réduite de 50 % (par exemple une posologie journalière totale de 10 mg par voie orale chez les patients naïfs d’opioïdes), et chaque patient doit faire l'objet d’une titration permettant un contrôle analgésique adéquat conformément à sa situation clinique.
Adaptation de la posologie
Elle se justifie lorsque les doses antérieurement prescrites se révèlent insuffisantes.
Fréquence de l'évaluation
Il ne faut pas s'attarder sur une posologie qui s'avère inefficace. Le patient doit donc être vu de manière rapprochée jusqu'à ce que la douleur soit contrôlée. Dans la pratique, une évaluation quotidienne est recommandée en début de traitement.
Augmentation de la dose
Si la douleur n'est pas contrôlée, il convient d'augmenter les doses de 25 à 50 % :
· soit en réduisant l'intervalle entre les prises (si la douleur est contrôlée au début mais pas en fin d'intervalle),
· soit en augmentant la dose à chaque prise (si la douleur n'est contrôlée à aucun moment de l'intervalle entre 2 prises).
Dans ce processus d'ajustement de dose, il n'y a pas de limite supérieure tant que les effets indésirables sont contrôlés.
Changement de forme pharmaceutique
En cas de passage d'une forme à libération immédiate à une forme à libération prolongée, la posologie quotidienne sera inchangée.
En cas de passage d’une forme orale à une forme parentérale et à titre indicatif le rapport d’équianalgésie suivant doit être respecté : 2 mg d’oxycodone par voie orale est équivalent à 1 mg d’oxycodone par voie parentérale. Cependant, la variabilité inter-patients nécessite que chaque patient soit soigneusement titré à la dose appropriée.
Objectifs et arrêt du traitement
Avant d’instaurer un traitement par OXYCODONE SANDOZ, une stratégie thérapeutique comprenant la durée et les objectifs du traitement, ainsi qu’un plan d’arrêt du traitement, doivent être convenus avec le patient, conformément aux directives de prise en charge de la douleur. Au cours du traitement, le médecin et le patient doivent s’entretenir régulièrement afin d’évaluer la nécessité de poursuivre le traitement, d’envisager son interruption et d’adapter les doses si nécessaire. Lorsqu’un patient n’a plus besoin d’un traitement à l’oxycodone, il peut être conseillé de diminuer progressivement la dose pour prévenir les symptômes de sevrage. En l’absence d’un contrôle adéquat de la douleur, il convient de réfléchir à la survenue possible d’une hyperalgésie, d’une tolérance et d’une progression de la maladie sous-jacente (voir rubrique 4.4).
Adolescent à partir de 12 ans
Posologie initiale :
La dose initiale habituelle pour les patients naïfs d'opioïdes et les patients présentant une douleur sévère non contrôlée par des opioïdes faibles est de 5 mg d’OXYCODONE SANDOZ à intervalles de 6 heures. La dose doit ensuite être progressivement augmentée, si nécessaire, de façon journalière jusqu'à ce qu'un contrôle suffisant de la douleur soit obtenu.
Au cours de ce processus, l'intervalle entre les doses d’OXYCODONE SANDOZ peut être réduit à 4 heures si nécessaire sans dépasser 6 prises par jour.
Les patients ayant déjà été traités par opioïdes peuvent avoir une dose initiale plus élevée en fonction de leur prise antérieure.
Enfants de moins de 12 ans
La sécurité et l'efficacité de l'oxycodone chez les enfants de moins de 12 ans n'ont pas encore été établies.
Mode d’administration
Voie orale.
Avec les formes à libération immédiate, la posologie quotidienne totale est généralement divisée en plusieurs doses équivalentes administrées toutes les 4 à 6 heures.
OXYCODONE SANDOZ peut aussi être utilisé pour le traitement des accès douloureux non contrôlés par le traitement de fond (en particulier chez les patients traités par oxycodone à libération prolongée).
Durée du traitement :
L’oxycodone ne doit pas être utilisé plus longtemps que nécessaire.
Ce médicament ne doit jamais être utilisé dans les cas suivants :
· hypersensibilité connue à l’oxycodone, ou à l’un des excipients mentionnés à la rubrique 6.1,
· bronchopneumopathie chronique obstructive sévère,
· asthme bronchique sévère,
· dépression respiratoire sévère avec hypoxie,
· taux élevé de dioxyde de carbone dans le sang,
· iléus paralytique,
· cœur pulmonaire chronique,
· allaitement,
· association à la buprénorphine, la nalbuphine, la pentazocine, la naltrexone, le nalméfène et l’oxybate de sodium (voir rubrique 4.5).
4.4. Mises en garde spéciales et précautions d'emploi
L'oxycodone n'est pas indiqué dans le traitement des pharmacodépendances majeures aux opiacés.
Dépression respiratoire
Le principal risque en cas d’abus d'opioïdes est la dépression respiratoire.
Les opioïdes peuvent provoquer des troubles respiratoires liés au sommeil, notamment une apnée centrale du sommeil (ACS) et une hypoxémie liée au sommeil, pouvant conduire à des éveils nocturnes et une somnolence diurne. L’utilisation d’opioïdes peut augmenter le risque d’ACS d'une manière dose-dépendante chez certains patients. Les opioïdes peuvent également provoquer l’aggravation d’une apnée du sommeil préexistante (voir rubrique 4.8). Chez les patients qui présentent une ACS, une réduction de la dose totale d’opioïdes doit être envisagée.
Abus et usage détourné
L’oxycodone est un opioïde stupéfiant qui peut donner lieu à un usage abusif et à un usage détourné chez des personnes à risque. L’usage détourné de formes orales par injection parentérale peut entraîner des effets indésirables graves pouvant être fatals. L’oxycodone doit être utilisé avec précaution chez les patients présentant ou ayant présenté des troubles d’usage de substance, y compris d’alcool.
Trouble d’utilisation d’opioïde (abus et dépendance)
Une accoutumance (tolérance) et une dépendance physique et/ou psychologique peuvent apparaître lors de l’administration répétée d’opioïdes comme l’oxycodone.
L’utilisation répétée d’OXYCODONE SANDOZ peut conduire à un trouble d’utilisation d’opioïde (TUO). Une dose plus élevée et une durée plus longue du traitement par opioïdes peuvent augmenter le risque de développer un TUO. L’abus ou le mésusage intentionnel d’OXYCODONE SANDOZ peut entraîner un surdosage et/ou le décès. Le risque de développement d’un TUO est accru chez les patients ayant des antécédents personnels ou familiaux (parents ou fratrie) de troubles d’utilisation d’opioïde (y compris de troubles liés à l’utilisation d’alcool), en cas de tabagisme actif ou chez les patients ayant des antécédents personnels d’autres troubles de la santé mentale (par exemple, dépression majeure, anxiété et troubles de la personnalité).
Avant d’instaurer un traitement par OXYCODONE SANDOZ et pendant le traitement, les objectifs du traitement et un plan d’arrêt doivent être convenus avec le patient (voir rubrique 4.2). Avant et pendant le traitement, le patient doit également être informé des risques et des signes de TUO. En cas d’apparition de ces signes, il doit être conseillé au patient de contacter son médecin.
Les patients devront être surveillés afin de détecter tout signe de comportements de recherche compulsive du produit (par exemple, demande de renouvellement trop précoce de la prescription). Dans ce cadre, les opioïdes et les médicaments psychoactifs (tels que les benzodiazépines) utilisés en concomitance devront être passés en revue. Pour les patients présentant des signes et symptômes de TUO, une consultation auprès d’un addictologue devra être envisagée.
Tolérance, dépendance et syndrome de sevrage
En cas d’utilisation prolongée et répétée, le patient peut développer une tolérance au médicament et avoir besoin d’augmenter progressivement les doses pour maintenir l’analgésie. Une demande pressante et réitérée nécessite de réévaluer fréquemment l’état du patient et le traitement.
L'utilisation prolongée de ce médicament peut entraîner une dépendance physique et un syndrome de sevrage peut apparaître lors d'un arrêt brutal du traitement. Le syndrome de sevrage est caractérisé par les symptômes suivants : bâillements, anxiété, irritabilité, frissons, mydriase, bouffées de chaleur, tremblements, sudation, larmoiement, rhinorrhée, agitation, convulsions, insomnie, nausées, vomissements, crampes abdominales, diarrhées et arthralgies.
L’apparition d’un syndrome de sevrage sera évitée par une diminution progressive des doses.
Troubles respiratoires liés au sommeil
Les opioïdes peuvent provoquer des troubles respiratoires liés au sommeil, tels que l’apnée centrale du sommeil (ACS) et l’hypoxémie liée au sommeil. L’utilisation d’opioïdes augmente de façon dose-dépendante le risque d’ACS. Chez les patients présentant une ACS, une diminution de la dose totale d’opioïdes doit être envisagée.
La prise concomitante d’alcool et d’OXYCODONE SANDOZ doit être évitée car elle peut entraîner une augmentation des effets indésirables d’OXYCODONE SANDOZ.
Ce médicament contient moins de 1 mmol (23 mg) de sodium par gélule, c’est-à-dire qu’il est essentiellement « sans sodium ».
Ce médicament est généralement deconseillé pendant la grossesse (voir rubrique 4.6).
Précautions d'emploi
L'oxycodone doit être utilisé avec précaution dans les cas suivants :
Hypovolémie
En cas d'hypovolémie, l'oxycodone peut induire un collapsus. L'hypovolémie sera donc corrigée avant l'administration d'oxycodone.
Insuffisance rénale
L'élimination rénale de l'oxycodone, sous la forme d'un métabolite actif, impose de débuter le traitement à posologie réduite, en adaptant par la suite, comme chez tout patient, les doses ou la fréquence d'administration à l'état clinique. Chez les patients atteints d’insuffisance rénale sévère en initiation de traitement par l’oxycodone, il est recommandé de débuter le traitement par une dose initiale de 5 mg toutes les 4 à 6 heures.
Lorsque l'étiologie de la douleur est traitée simultanément
Il convient alors d'adapter les doses d'oxycodone aux résultats du traitement appliqué.
Chez l'insuffisant respiratoire et en cas de syndrome d’apnée du sommeil
La fréquence respiratoire sera surveillée attentivement. La somnolence constitue un signe d'appel d'une décompensation.
Il importe de diminuer les doses d'oxycodone lorsque d'autres traitements antalgiques d'action centrale sont prescrits simultanément, car cela favorise l'apparition brutale d'une insuffisance respiratoire.
Risques liés à l’utilisation concomitante de médicaments sédatifs tels que les benzodiazépines ou autres médicaments apparentés :
L’utilisation concomitante d’OXYCODONE SANDOZ et de sédatifs tels que les benzodiazépines ou autres médicaments apparentés peut entraîner une sédation, une dépression respiratoire, un coma et la mort. En raison de ces risques, la prescription concomitante avec ces médicaments sédatifs doit être réservée aux patients pour lesquels d’autres options thérapeutiques ne sont pas possibles.
Si la décision de prescrire OXYCODONE SANDOZ en même temps que des médicaments sédatifs est prise, la dose efficace la plus faible doit être utilisée et la durée du traitement doit être aussi courte que possible. Les patients doivent être suivis de près pour surveiller la survenue de signes et symptômes de dépression respiratoire et de sédation.
A cet égard, il est fortement recommandé d’informer les patients et leurs soignants afin qu’ils connaissent ces symptômes (voir rubrique 4.5).
Chez les patients présentant une insuffisance hépatique
L’administration d’oxycodone doit être prudente et accompagnée d’une surveillance clinique. Chez les patients atteints d’insuffisance hépatique sévère en initiation de traitement par l’oxycodone, il est recommandé de débuter le traitement par une dose initiale de 5 mg toutes les 4 à 6 heures.
Chez les personnes âgées ou fragilisées
Leur sensibilité particulière aux effets antalgiques des opioïdes forts, mais aussi à leurs effets indésirables centraux (confusion) ou d'ordre digestif, associée à une baisse physiologique de la fonction rénale, doit inciter à la prudence, en instaurant notamment le traitement à la dose la plus faible, et en augmentant très progressivement la posologie.
Les co-prescriptions, lorsqu'elles comportent des antidépresseurs tricycliques notamment, augmentent a fortiori la survenue d'effets indésirables comme la confusion ou la constipation.
Une pathologie urétro-prostatique, fréquente dans cette population, expose au risque de rétention urinaire.
L'usage de l'oxycodone ne doit pas pour autant être restreint chez la personne âgée dès lors qu'il s'accompagne de ces précautions.
Constipation
Il est impératif de rechercher et de prendre en charge une constipation ou un syndrome occlusif avant et pendant le traitement.
Traumatisme crânien
En raison du risque d'augmentation de la pression intracrânienne, l'utilisation d'oxycodone au cours des douleurs chroniques devra être prudente.
Troubles mictionnels
Il existe un risque de dysurie ou de rétention d'urine, principalement en cas d'adénome prostatique ou de sténose urétrale.
Chez les patients présentant une atteinte du tractus biliaire, une pancréatite, des troubles inflammatoires intestinaux, un myxœdème, une hypothyroïdie, une insuffisance adrénocorticale, une maladie d’Addison, une hypotension, une psychose toxique, un delirium tremens, un alcoolisme, une hypertrophie de la prostate.
L'administration d'oxycodone doit être prudente et accompagnée d'une surveillance clinique.
Affections hépatobiliaires
L’oxycodone peut provoquer un dysfonctionnement et des spasmes du sphincter d’Oddi, ce qui accroît le risque de symptômes des voies biliaires et de pancréatite. L’oxycodone doit donc être administré avec précaution chez les patients atteints de pancréatite et de maladies des voies biliaires.
Hyperalgésie
Une hyperalgésie ne répondant pas à une augmentation supplémentaire de la dose d’oxycodone peut exceptionnellement apparaitre, en particulier à hautes doses. Il peut être nécessaire de réduire la dose d’oxycodone ou de changer d’opioïde.
Sportifs
L'attention des sportifs doit être attirée sur le fait que cette spécialité contient du chlorhydrate d'oxycodone et que ce principe actif est inscrit sur la liste des substances dopantes.
Ce médicament devrait être utilisé avec précaution en situations pré-opératoires, dans les 12-24 heures post-opératoires et jusqu'à la confirmation médicale de la reprise du transit intestinal.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Il faut prendre en compte le fait que de nombreux médicaments ou substances peuvent additionner leurs effets dépresseurs du système nerveux central et contribuer à diminuer la vigilance. Il s'agit des dérivés morphiniques (analgésiques, antitussifs et traitements de substitution), des neuroleptiques, des barbituriques, des benzodiazépines, des anxiolytiques autres que les benzodiazépines (par exemple le méprobamate), des hypnotiques, des antidépresseurs sédatifs (amitriptyline, doxépine, miansérine, mirtazapine, trimipramine), des antihistaminiques H1 sédatifs, des antihypertenseurs centraux, des IMAO, du baclofène et du thalidomide.
Associations contre-indiquées (voir rubrique 4.3)
+ Morphiniques agonistes-antagonistes (buprénorphine, nalbuphine, pentazocine)
Diminution de l'effet antalgique par blocage compétitif des récepteurs, avec risque d'apparition d'un syndrome de sevrage.
+ Morphiniques antagonistes partiels (nalméfène, naltrexone)
Risque de diminution de l’effet antalgique.
+ Oxybate de sodium
Risque majoré de dépression respiratoire, pouvant être fatale en cas de surdosage.
Associations déconseillées (voir rubrique 4.4)
+ Consommation d'alcool
Majoration par l'alcool de l'effet sédatif des analgésiques morphiniques.
L'altération de la vigilance peut rendre dangereuses la conduite de véhicules et l'utilisation de machines.
Eviter la prise de boissons alcoolisées et de médicaments contenant de l'alcool.
+ Médicaments sédatifs tels que les benzodiazépines ou les médicaments apparentés
L'utilisation concomitante d'opioïdes avec des médicaments sédatifs tels que les benzodiazépines ou les médicaments apparentés augmente le risque de sédation, de dépression respiratoire, de coma et de décès en raison d’un effet dépresseur additif sur le système nerveux central. La dose et la durée de l'utilisation concomitante doivent être limitées (voir rubrique 4.4).
+ Inhibiteurs puissants du CYP3A4 tels que certains macrolides (clarithromycine, érythromycine, télithromycine), azolés antifongiques (fluconazole, kétoconazole, itraconazole, voriconazole, posaconazole) et inhibiteurs de protéases boostés par ritonavir ou cobicistat, bocéprévir
Majoration des effets indésirables, notamment respiratoires, de l’oxycodone par diminution de son métabolisme hépatique par l’inhibiteur. Surveillance clinique et adaptation éventuelle de la posologie d’oxycodone pendant le traitement par l’inhibiteur enzymatique et après son arrêt.
+ Le jus de pamplemousse, inhibiteur du CYP3A4, administré à raison de 200 mL trois fois par jour pendant cinq jours, a augmenté l’ASC de l’oxycodone administré par voie orale. En moyenne, l’ASC était environ 1,7 fois plus élevée (intervalle de 1,1 à 2,1).
+ Crizotinib
Risque de majoration de la toxicité de l’oxycodone par diminution de son métabolisme et/ou augmentation de sa biodisponibilité par le crizotinib.
+ Idélalisib
Augmentation des concentrations plasmatiques du substrat par diminution de son métabolisme hépatique par l’idélalisib.
+ Inducteurs enzymatiques (rifampicine, rifabutine, carbamazépine, enzalutamide, dabrafénib, phénytoïne, primidone, phénobarbital, éfavirenz, eslicarbamazépine, oxcarbazépine)
Diminution des concentrations plasmatiques de l’oxycodone par augmentation de sa clairance. Une adaptation de la posologie d’oxycodone peut être envisagée.
La rifampicine, un inducteur du CYP3A4, administrée à raison de 600 mg une fois par jour pendant sept jours, a réduit l’ASC de l’oxycodone administré par voie orale. En moyenne, l’ASC était réduite d’environ 86 %.
+ Millepertuis
Diminution des concentrations plasmatiques de l’oxycodone par augmentation de sa clairance. Une adaptation de la posologie d’oxycodone peut être envisagée.
Le millepertuis, un inducteur du CYP3A4, administré à raison de 300 mg trois fois par jour pendant quinze jours, a réduit l’ASC de l’oxycodone administré par voie orale. En moyenne, l’ASC était réduite d’environ 50 % (intervalle de 37 à 57 %).
Associations à prendre en compte
+ Médicaments sérotoninergiques
L’administration concomitante de l’oxycodone et d’agents sérotoninergiques, tels qu’un inhibiteur sélectif de la recapture de la sérotonine (ISRS) ou un inhibiteur de la recapture de la sérotonine et de la noradrénaline (IRSN) peut entraîner une toxicité sérotoninergique. Les symptômes de la toxicité sérotoninergique peuvent inclure des modifications de l’état mental (par ex., agitation, hallucinations, coma), une instabilité du système nerveux autonome (par ex., tachycardie, pression artérielle labile, hyperthermie), des anomalies neuromusculaires (par ex., hyperréflexie, manque de coordination, rigidité) et/ou des symptômes gastro-intestinaux (par ex., nausées, vomissements, diarrhée). L’oxycodone doit être utilisé avec prudence et il peut être nécessaire de diminuer la posologie chez les patients utilisant ces médicaments.
+ Autres analgésiques morphiniques agonistes (alfentanil, codéine, dextromoramide, dihydrocodéine, fentanyl, hydromorphone, morphine, péthidine, phénopéridine, rémifentanil, sufentanil, tramadol)
Risque majoré de dépression respiratoire, pouvant être fatale en cas de surdosage.
+ Antitussifs morphine-like (dextrométorphane, noscapine, pholcodine)
Risque majoré de dépression respiratoire, pouvant être fatale en cas de surdosage.
+ Antitussifs morphiniques vrais (codéine, éthylmorphine)
Risque majoré de dépression respiratoire, pouvant être fatale en cas de surdosage.
+ Barbituriques
Risque majoré de sédation et de dépression respiratoire pouvant entraîner coma et décès, notamment chez le sujet âgé. Il convient de limiter autant que possible les doses et la durée de l’association.
+ Autres médicaments sédatifs
Majoration de la dépression centrale. L'altération de la vigilance peut rendre dangereuses la conduite de véhicules et l'utilisation de machines.
Risque important d'akinésie colique, avec constipation sévère.
4.6. Fertilité, grossesse et allaitement
Grossesse
Les études chez l'animal n'ont pas mis en évidence d'effet tératogène. En l'absence d'effet tératogène chez l'animal, un effet malformatif dans l'espèce humaine n'est pas attendu. En effet, à ce jour, les substances responsables de malformations dans l'espèce humaine se sont révélées tératogènes chez l'animal au cours d'études bien conduites sur deux espèces.
En clinique, il n'existe pas actuellement de données suffisamment pertinentes pour évaluer un éventuel effet malformatif ou fœtotoxique du chlorhydrate d'oxycodone lorsqu'il est administré pendant la grossesse.
En fin de grossesse, des posologies élevées, même en traitement bref, sont susceptibles d'entraîner une dépression respiratoire chez le nouveau-né.
Au cours des trois derniers mois de la grossesse, la prise chronique de chlorhydrate d'oxycodone par la mère, et cela quelle que soit la dose, peut être à l'origine d'un syndrome de sevrage chez le nouveau-né avec irritabilité, vomissements, convulsions et létalité accrue.
En conséquence, l'utilisation du chlorhydrate d'oxycodone est déconseillée au cours de la grossesse.
En fin de grossesse, en cas de prises ponctuelles élevées, de traitement chronique, voire de toxicomanie, une surveillance néo-natale doit être envisagée, afin de prévenir les risques de dépression respiratoire ou de syndrome de sevrage chez l'enfant.
L'oxycodone peut être excrété dans le lait maternel et engendrer une dépression respiratoire du nouveau-né. En conséquence, l'oxycodone est contre-indiqué au cours de l'allaitement.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Les effets indésirables les plus fréquents aux doses habituelles sont la constipation, la somnolence, des sensations vertigineuses, des maux de tête, un prurit, des nausées et vomissements.
En cas d'administration chronique, la constipation ne régresse pas spontanément et doit donc être prise en charge. En revanche, somnolence, nausées et vomissements sont en règle générale transitoires et leur persistance doit faire rechercher une cause associée.
Tous ces effets, et notamment la constipation, sont prévisibles et doivent donc être anticipés afin d'optimiser le traitement. Ils peuvent nécessiter une thérapeutique correctrice.
L’incidence des effets indésirables classés par classe de systèmes organes est présentée ci-dessous. La définition des catégories de fréquences de survenue est la suivante :
Très fréquent (≥ 1/10)
Fréquent (≥ 1/100, < 1/10)
Peu fréquent (≥ 1/1000, < 1/100)
Rare (≥ 1/10 000, < 1/1000)
Très rare (< 1/10 000)
Fréquence indéterminée (ne pouvant être estimée à partir des données disponibles)
Affections du système immunitaire
Peu fréquent : hypersensibilité.
Fréquence indéterminée : réaction anaphylactique.
Troubles du métabolisme et de la nutrition
Fréquent : diminution de l’appétit.
Peu fréquent : déshydratation.
Affections psychiatriques
Fréquent : anxiété, état confusionnel, dépression, insomnie, nervosité, troubles de la pensée, cauchemars, plus spécialement chez le sujet âgé, avec éventuellement hallucinations.
Peu fréquent : agitation, labilité émotionnelle, troubles de l’humeur, hallucinations, diminution de la libido, pharmacodépendance* (voir rubrique 4.4).
Fréquence indéterminée : agressivité.
Affections du système nerveux
Très fréquent : somnolence, sensations vertigineuses, céphalées.
Fréquent : tremblements, augmentation de la pression intracrânienne, qu’il convient de traiter dans un premier temps.
Peu fréquent : amnésie, convulsions, hypertonie, hypoesthésie, contractions musculaires involontaires, troubles du langage, syncope, paresthésies, dysgueusie.
Fréquence indéterminée : hyperalgésie, léthargie, syndrome d’apnée du sommeil (voir rubrique 4.4).
Affections oculaires
Peu fréquent : troubles de la vision, myosis.
Affections de l’oreille et du labyrinthe
Peu fréquent : vertiges.
Affections cardiaques
Peu fréquent : palpitations (dans un contexte de syndrome de sevrage).
Rare : bradycardie.
Affections vasculaires
Peu fréquent : vasodilatation.
Rare : hypotension, hypotension orthostatique.
Affections respiratoires, thoraciques et médiastinales
Fréquent : dyspnée.
Peu fréquent : dépression respiratoire.
Fréquence indéterminée : syndrome d’apnée centrale du sommeil (voir rubrique 4.4).
Affections gastro-intestinales
Très fréquent : constipation, nausées, vomissements.
Fréquent : douleur abdominale, diarrhée, sécheresse de la bouche, dyspepsie.
Peu fréquent : dysphagie, flatulences, éructations, iléus.
Fréquence indéterminée : caries dentaires.
Affections hépatobiliaires
Peu fréquent : augmentation des enzymes hépatiques.
Fréquence indéterminée : cholestase, colique biliaire, dysfonctionnement du sphincter d’Oddi.
Affections de la peau et du tissu sous-cutané
Très fréquent : prurit.
Fréquent : éruption cutanée, hyperhidrose.
Peu fréquent : sécheresse de la peau.
Rare : urticaire.
Affections du rein et des voies urinaires
Peu fréquent : rétention urinaire.
Affections des organes de reproduction et du sein
Peu fréquent : troubles de l’érection.
Fréquence indéterminée : aménorrhée.
Affections endocriniennes
Fréquence indéterminée : hypogonadisme.
Troubles généraux et anomalies au site d’injection
Fréquent : asthénie.
Peu fréquent : frissons, syndrome de sevrage, malaise, œdème, œdème périphérique, tolérance au médicament, soif.
Fréquence indéterminée : syndrome de sevrage médicamenteux du nouveau-né, fatigue.
*Pharmacodépendance
L’utilisation répétée d’OXYCODONE SANDOZ peut entraîner une pharmacodépendance, même à des doses thérapeutiques. Le risque de pharmacodépendance peut varier en fonction des facteurs de risque individuels du patient, de la posologie et de la durée du traitement opioïde (voir rubrique 4.4).
Population pédiatrique
La fréquence, le type et la sévérité des effets indésirables chez les adolescents (âgés de 12 à 18 ans) semblent similaires à ceux observés chez les adultes (voir rubrique 5.1).
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
Symptômes
Les signes d'un surdosage en oxycodone sont : une dépression respiratoire, un myosis, une hypotonie musculaire, une hypotension, un œdème pulmonaire, une bradycardie, une somnolence pouvant évoluer vers un état de stupeur ou de coma, pouvant être fatal dans les cas les plus graves.
La somnolence constitue un signe d’appel précoce de la décompensation respiratoire.
Une leucoencéphalopathie toxique a été observée en cas de surdosage d’oxycodone.
Conduite d'urgence
Ventilation assistée, avant réanimation cardio-respiratoire en service spécialisé. L'évacuation du contenu gastrique peut être utile pour éliminer le produit non absorbé.
En cas de surdosage massif, traitement par la naloxone par voie intraveineuse.
Chez les sujets physiquement dépendants à l'oxycodone, la naloxone doit être administrée avec précaution, car elle peut provoquer une réversion brutale ou totale des effets opioïdes, et provoquer des douleurs ou un syndrome de sevrage aigu.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : analgésique opioïde, Code ATC: N02AA05.
(N: système nerveux central)
L'oxycodone est un agoniste opioïde pur.
Son action antalgique est similaire qualitativement à celle de la morphine. L'effet thérapeutique est principalement analgésique, anxiolytique, antitussif et sédatif.
Système endocrinien
Les opioïdes ont une action pharmacologique sur l'axe hypothalamo-hypophysaire ou gonadique. Certaines modifications ont été observées telles qu'une augmentation de la prolactinémie et une diminution du cortisol plasmatique et de la testostérone. Ces modifications hormonales peuvent se manifester par des symptômes cliniques.
Autres effets pharmacologiques
Les études animales et in vitro indiquent différents effets des opioïdes naturels, tels que la morphine, sur les composantes du système immunitaire. La conséquence clinique de ces observations n'est pas connue.
Population pédiatrique
Dans l'ensemble, les données de sécurité obtenues avec l'oxycodone dans les études cliniques, pharmacodynamiques et pharmacocinétiques montrent que l'oxycodone est généralement bien toléré chez les patients pédiatriques, avec seulement des effets indésirables mineurs affectant principalement le système gastro-intestinal et le système nerveux. Tous les effets indésirables rapportés étaient conformes au profil de sécurité connu de l'oxycodone ainsi que à celui d'autres opioïdes puissants comparables.
Il n'existe pas de données d'essais cliniques sur l'utilisation à long terme chez les adolescents âgés de 12 à 18 ans.
5.2. Propriétés pharmacocinétiques
Absorption
A partir des formulations à libération immédiate, les concentrations maximales sont généralement atteintes en 1 heure.
Distribution
Après absorption, l’oxycodone est distribué dans tout le corps. Environ 45 % est lié aux protéines plasmatiques.
Métabolisme
L'oxycodone est métabolisé dans le foie via le CYP3A4 et le CYP2D6 en noroxycodone, oxymorphone et noroxymorphone qui sont ensuite glucuronidés.
La noroxycodone et la noroxymorphone sont les principaux métabolites circulants. La noroxycodone est un agoniste opioïde mu faible. La noroxymorphone est un puissant agoniste opioïde mu ; cependant, elle ne traverse pas la barrière hémato-encéphalique d’une façon significative. L'oxymorphone est un puissant agoniste opioïde mu mais est présent à de très faibles concentrations après administration d'oxycodone.
Aucun de ces métabolites ne contribue de manière significative à l'effet analgésique de l'oxycodone.
La demi-vie d'élimination plasmatique est d'environ 4,5 heures. Le principe actif et ses métabolites sont excrétés dans l'urine et les selles. Les concentrations plasmatiques d'oxycodone ne sont que nominalement affectées par l'âge, étant supérieur de 15 % chez les sujets âgés par rapport aux sujets jeunes.
Les femmes ont en moyenne des concentrations plasmatiques d'oxycodone jusqu'à 25 % plus élevées que les hommes sur une base de poids corporel ajusté.
Par rapport aux sujets normaux, les patients présentant une insuffisance hépatique légère à sévère peuvent avoir des concentrations plasmatiques plus élevées d'oxycodone et de noroxycodone, et des concentrations plasmatiques plus faibles d'oxymorphone. Il peut y avoir une augmentation de la demi-vie d'élimination de l'oxycodone, et cela peut s'accompagner d'une augmentation des effets du médicament.
Par rapport aux sujets normaux, les patients présentant une insuffisance rénale légère à sévère peuvent avoir des concentrations plasmatiques plus élevées d'oxycodone et de ses métabolites. Il peut y avoir une augmentation de la demi-vie d'élimination de l'oxycodone, et cela peut s'accompagner d'une augmentation des effets du médicament.
5.3. Données de sécurité préclinique
Toxicologie de la reproduction et du développement
Chez le rat, l'oxycodone n'a eu aucun effet sur la fertilité mâle, la fertilité femelle, ou le développement embryonnaire précoce à des doses allant jusqu’à 8 mg/kg/jour (équivalant à une dose de 1,3 mg/kg/jour chez l'Homme). Aucune malformation n’était rapportée chez le rat et le lapin traités au cours de l’organogénèse jusqu’aux doses respectives de 8 et 125 mg/kg/jour (équivalant à des doses de 1,3 et 40,3 mg/kg chez l'Homme.
Dans une étude de développement pré et postnatal chez le rat, une diminution du poids corporel des petits de la génération F1 était observée à la dose de 6 mg/kg/jour (équivalant à 1,0 mg/kg chez l'Homme) provoquant une diminution du poids et de la prise alimentaire des génitrices.
Génotoxicité
Les résultats des études in vitro et in vivo indiquent que le risque génotoxique de l'oxycodone pour l'Homme est minime ou absent aux concentrations systémiques d'oxycodone obtenues thérapeutiquement. L'oxycodone n'était pas génotoxique dans un essai de mutagénicité bactérienne ou dans un test de micronoyau in vivo chez la souris. L'oxycodone a produit une réponse positive dans le test in vitro du lymphome de souris en présence d'une activation métabolique S9 du foie de rat à des doses supérieures à 25 µg/mL. Deux essais d'aberration chromosomique in vitro avec des lymphocytes humains ont donné des résultats de clastogénicité équivoques.
Carcinogénicité
La carcinogénicité a été évaluée dans une étude de gavage oral de 2 ans menée sur des rats Sprague-Dawley.
L'oxycodone n'a pas augmenté l'incidence des tumeurs chez les rats mâles et femelles à des doses allant jusqu'à 6 mg / kg / jour, ce qui équivaut à une dose de 1,0 mg / kg chez l'homme. Les doses étaient limitées par les effets pharmacologiques de l'oxycodone liés aux opioïdes.
Cellulose microcristalline, stéarate de magnésium.
Enveloppe de la gélule
Dioxyde de titane (E171), oxyde de fer rouge (E172), oxyde de fer jaune (E172), indigotine (E132), laurylsulfate de sodium, gélatine.
Encre noire d'impression
Gommes laques, oxyde de fer noir (E172), propylèneglycol, hydroxyde de potassium, solution concentrée d’ammoniaque.
2 ans.
6.4. Précautions particulières de conservation
A conserver à une température ne dépassant pas 30°C.
6.5. Nature et contenu de l'emballage extérieur
14, 20, 28, 30, 50 et 56 gélules sous plaquettes (PVC/PVDC/Aluminium).
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Pas d’exigences particulières.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
49 AVENUE GEORGES POMPIDOU
92300 LEVALLOIS-PERRET
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 300 688 9 2 : 14 gélules sous plaquettes (PVC/PVDC/Aluminium).
· 34009 300 689 0 8 : 20 gélules sous plaquettes (PVC/PVDC/Aluminium).
· 34009 300 689 1 5 : 28 gélules sous plaquettes (PVC/PVDC/Aluminium).
· 34009 300 689 2 2 : 30 gélules sous plaquettes (PVC/PVDC/Aluminium).
· 34009 300 689 3 9 : 50 gélules sous plaquettes (PVC/PVDC/Aluminium).
· 34009 300 689 5 3 : 56 gélules sous plaquettes (PVC/PVDC/Aluminium).
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Stupéfiant.
Prescription sur ordonnances sécurisées.
Prescription limitée à 28 jours.
ANSM - Mis à jour le : 18/02/2025
OXYCODONE SANDOZ 10 mg, gélule
Chlorhydrate d’oxycodone
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou à votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que OXYCODONE SANDOZ 10 mg, gélule et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant de prendre OXYCODONE SANDOZ 10 mg, gélule ?
3. Comment prendre OXYCODONE SANDOZ 10 mg, gélule ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver OXYCODONE SANDOZ 10 mg, gélule ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE OXYCODONE SANDOZ 10 mg, gélule ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : analgésique opioïde, Code ATC : N02AA05.
Ce médicament est un analgésique opioïde (destiné à soulager la douleur).
OXYCODONE SANDOZ est utilisé chez les adultes et les adolescents à partir de 12 ans pour le traitement des douleurs intenses qui ne peuvent être correctement traitées que par des analgésiques forts, notamment les douleurs cancéreuses.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT DE PRENDRE OXYCODONE SANDOZ 10 mg, gélule ?
Ne prenez jamais OXYCODONE SANDOZ 10 mg, gélule dans les cas suivants :
· si vous êtes allergique à la substance active, le chlorhydrate d'oxycodone ou à l'un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6,
· si vous souffrez d’une maladie pulmonaire sévère, associée à un rétrécissement des voies respiratoires (bronchopneumopathie chronique obstructive ou BPCO),
· si vous souffrez d’un asthme bronchique sévère,
· si votre respiration n’est pas en mesure d’apporter suffisamment d’oxygène dans le sang et d’éliminer le gaz carbonique par votre corps (dépression respiratoire sévère avec hypoxie),
· si le taux de gaz carbonique dans votre sang est trop élevé,
· si vous souffrez de dysfonctionnements intestinaux avec occlusion intestinale (iléus paralytique),
· si vous souffrez de problèmes cardiaques à la suite d'une insuffisance pulmonaire chronique (cœur pulmonaire),
· si vous allaitez,
· si vous êtes traité(e) par des médicaments morphiniques tels que ceux contenant de la buprénorphine, de la nalbuphine, de la pentazocine (substances ayant des propriétés comparables à celles de l'oxycodone) ainsi que par des médicaments contenant de la naltrexone, du nalméfène et de l’oxybate de sodium.
Avertissements et précautions
Adressez-vous à votre médecin ou à votre pharmacien avant de prendre OXYCODONE SANDOZ, gélule.
Tolérance, dépendance et addiction
Le risque de devenir dépendant(e) ou addict(e) varie d’une personne à l’autre. Vous risquez davantage de devenir dépendant(e) ou addict(e) à OXYCODONE SANDOZ si :
· vous ou une personne de votre famille avez déjà consommé de façon abusive ou été dépendant(e) à l’alcool, à des médicaments sur ordonnance ou à des substances illicites (« addiction »),
· vous fumez,
· vous avez déjà présenté des troubles de l’humeur (dépression, anxiété ou trouble de la personnalité) ou si vous avez été suivi(e) par un psychiatre pour d’autres troubles de la santé mentale.
Ce médicament contient de l’oxycodone qui est un médicament opioïde. Il peut entraîner une dépendance et/ou une addiction.
Ce médicament contient de l’oxycodone qui est un médicament opioïde. L’utilisation répétée d’analgésiques opioïdes peut entraîner une diminution de l’efficacité du médicament (vous vous y habituez, ce que l’on appelle la tolérance). L’utilisation répétée d’OXYCODONE SANDOZ peut également entraîner une dépendance, un abus et une addiction, ce qui peut conduire à un surdosage potentiellement mortel. Le risque que ces effets secondaires surviennent peut augmenter avec une dose plus élevée et une durée d’utilisation plus longue.
La dépendance ou l’addiction peut vous donner l’impression que vous ne contrôlez plus la quantité de médicament que vous devez prendre ou la fréquence à laquelle vous devez le prendre. Vous pouvez ressentir le besoin de continuer à prendre votre médicament, même s’il ne vous aide pas à soulager votre douleur.
Si vous remarquez l’un des signes suivants pendant que vous prenez OXYCODONE SANDOZ, cela peut être le signe que vous êtes devenu(e) dépendant(e) ou addict(e) :
· vous avez besoin de prendre le médicament pendant une durée plus longue que celle indiquée par votre médecin,
· vous avez besoin de prendre plus que la dose recommandée,
· vous utilisez le médicament pour des raisons autres que celles prescrites, par exemple pour rester calme ou pour vous aider à dormir,
· vous avez tenté à plusieurs reprises, sans succès, d’arrêter d’utiliser le médicament ou d’en contrôler son utilisation,
· lorsque vous arrêtez de prendre le médicament, vous vous sentez mal, et vous vous sentez mieux lorsque vous reprenez le médicament (« effets de sevrage »).
Si vous remarquez l’un de ces signes, parlez-en à votre médecin pour discuter de la meilleure approche de traitement pour vous, y compris le moment approprié pour arrêter et la façon d’arrêter en toute sécurité (voir rubrique 3, « Si vous arrêtez de prendre OXYCODONE SANDOZ 10 mg, gélule »).
Troubles respiratoires liés au sommeil
OXYCODONE SANDOZ peut provoquer des troubles respiratoires liés au sommeil, tels que l’apnée du sommeil (pauses respiratoires pendant le sommeil) et l’hypoxémie liée au sommeil (faible taux d’oxygène dans le sang). Les symptômes associés peuvent inclure des pauses respiratoires pendant le sommeil, des réveils nocturnes dus à un essoufflement, des difficultés à rester endormi(e) ou une somnolence excessive pendant la journée. Si vous ou une personne de votre entourage remarquez ces symptômes, contactez votre médecin. Une réduction de la dose pourra être envisagée par votre médecin.
Mises en garde spéciales
Ce médicament peut entraîner une dépendance physique et psychique.
Votre médecin accompagnera ce traitement d’une surveillance adaptée à son utilisation.
L’oxycodone est un opioïde stupéfiant qui peut donner lieu à un usage abusif et à un usage détourné chez des personnes à risque. Si son utilisation est indispensable, elle doit être utilisée avec précaution chez les patients présentant ou ayant présenté des troubles d’usage de substance, y compris d’alcool.
L’augmentation progressive des doses, lorsqu’elle est nécessaire et même si elles sont élevées, n’expose pas le plus souvent au risque d’apparition d’une accoutumance. Si malgré l’augmentation de la dose l’effet du médicament est insuffisant, adressez-vous à votre médecin pour réévaluer le traitement.
En cas de traitement prolongé et répété par l’oxycodone, il est impératif de ne pas arrêter brutalement le traitement, car cela expose à la survenue d’un syndrome de sevrage (voir rubrique « 4. Quels sont les effets indésirables éventuels ? »).
Ce médicament est généralement déconseillé pendant la grossesse.
Précautions d’emploi
Ce médicament doit être utilisé avec précaution :
· chez les personnes âgées, ou fragilisées,
· si vous avez un myxœdème (troubles thyroïdiens, accompagnés d’une peau sèche, froide et d’un gonflement au niveau du visage et des membres),
· si votre glande thyroïde ne produit pas assez d’hormones (insuffisance thyroïdienne),
· si vous avez un traumatisme crânien,
· si vous avez une diminution du volume total de sang (hypovolémie),
· si vous souffrez d’insuffisance respiratoire (diminution de la capacité à respirer),
· si vous souffrez d’une maladie chronique du foie (insuffisance hépatique), d’une affection du pancréas,
· si vous souffrez d’une inflammation du pancréas (pancréatite),
· si vous souffrez de troubles inflammatoires intestinaux,
· si vous souffrez de problèmes biliaires,
· si vous souffrez d’insuffisance rénale,
· si la taille de votre prostate est anormalement augmentée ou si vous avez des difficultés à uriner,
· si vous souffrez de constipation (signalez toute constipation à votre médecin pour qu’il vous donne un traitement adapté),
· si vos glandes surrénales ne produisent pas assez d’hormones (insuffisance des glandes surrénales ou maladie d’Addison),
· si votre tension est trop basse (hypotension),
· si vous souffrez d’alcoolisme ou de delirium tremens,
· si vous souffrez de troubles mentaux induits par une substance ou par une infection (psychose toxique),
· si vous ressentez une douleur anormalement intense (hyperalgésie).
Si vous devez subir une opération chirurgicale, informez votre médecin que vous prenez ce médicament.
Contactez votre médecin si vous ressentez de fortes douleurs abdominales supérieures pouvant irradier vers le dos, des nausées, des vomissements ou de la fièvre, car il pourrait s’agir de symptômes liés à l’inflammation du pancréas (pancréatite) et des voies biliaires.
Autres médicaments et OXYCODONE SANDOZ 10 mg, gélule
Ce médicament ne doit pas être associé à la buprénorphine, la nalbuphine ou la pentazocine, ainsi qu’à la naltrexone, au nalméfène et à l’oxybate de sodium.
L'utilisation concomitante d’OXYCODONE SANDOZ et de médicaments sédatifs tels que les benzodiazépines ou les médicaments apparentés augmente le risque de somnolence, de difficultés respiratoires (dépression respiratoire), de coma et peut être mortelle. Pour cette raison, l'utilisation concomitante ne doit être envisagée que lorsque d'autres options de traitement ne sont pas possibles.
Le risque de survenue d’effets indésirables augmente avec la prise d’antidépresseurs (tels que le citalopram, la duloxétine, l’escitalopram, la fluoxétine, la fluvoxamine, la paroxétine, la sertraline, la venlafaxine). Ces médicaments peuvent interagir avec l’oxycodone et vous pourriez présenter des symptômes, tels que des contractions rythmiques involontaires des muscles, y compris les muscles qui contrôlent les mouvements des yeux, une agitation, une transpiration excessive, des tremblements, une exagération des réflexes, une augmentation du tonus musculaire, une température corporelle supérieure à 38 °C. Contactez votre médecin si vous manifestez de tels symptômes.
Si vous prenez ou avez pris récemment un autre médicament, y compris un médicament obtenu sans ordonnance parlez-en à votre médecin ou à votre pharmacien, et notamment des médicaments agissant sur le système nerveux central et pouvant avoir un effet sédatif :
· autres médicaments utilisés pour traiter les douleurs modérées à intenses (analgésiques opioïdes),
· médicaments utilisés pour traiter les troubles psychiques (neuroleptiques),
· médicaments utilisés pour traiter l’anxiété (tranquillisants),
· médicaments utilisés pour traiter la dépression (antidépresseurs),
· médicaments utilisés pour traiter les troubles du sommeil (hypnotiques, sédatifs),
· médicaments utilisés pour traiter les allergies (antihistaminiques),
· inhibiteurs de la monoamine oxydase (médicaments utilisés pour traiter la dépression ou la maladie de Parkinson),
· médicaments utilisés pour traiter les contractures musculaires (myorelaxants),
· médicaments antitussifs dérivés de la morphine.
Prévenez également votre médecin si vous prenez un des médicaments suivants, qui peuvent augmenter les effets indésirables d’OXYCODONE SANDOZ ou diminuer son efficacité ; dans ce cas, votre médecin vous surveillera étroitement et adaptera éventuellement la dose d’OXYCODONE SANDOZ :
· antibiotiques macrolides tels que la clarithromycine, l’érythromycine et la télithromycine (médicaments pour traiter les infections bactériennes),
· antifongiques azolés tels que le fluconazole, le kétoconazole, l’itraconazole, le voriconazole et le posaconazole (médicaments pour traiter les infections dues à des champignons),
· inhibiteurs de protéases tels que le ritonavir et le cobicistat (médicaments utilisés dans le traitement du SIDA),
· crizotinib, idélalisib (médicaments utilisés dans le traitement de certains cancers),
· bocéprévir (médicament utilisé dans le traitement de l’hépatite C),
· inducteurs enzymatiques tels que la rifampicine, la rifabutine, la carbamazépine, l’enzalutamide, le dabrafénib, la phénytoïne, le primidone, le phénobarbital, l’éfavirenz, l’eslicarbamazépine, l’oxcarbazépine,
· médicaments contenant du millepertuis,
· les médicaments atropiniques.
Informez également votre médecin si vous prenez, avez récemment pris ou pourriez prendre un des médicaments suivants :
· autres médicaments utilisés pour traiter la douleur tels que l’alfentanil, la codéine, le dextromoramide, la dihydrocodéine, le fentanyl, l’hydromorphone, la morphine, la péthidine, la phénopéridine, le rémifentanil, le sufentanil, le tramadol,
· médicaments utilisés pour le traitement de la toux tels que le dextrométhorphane, la noscapine, la pholcodine, la codéine et l’éthylmorphine,
· médicaments utilisés pour traiter les troubles psychiques (psychotropes) tels que les benzodiazépines et apparentés,
· médicaments utilisés pour traiter les troubles du sommeil (hypnotiques) tels que les barbituriques.
OXYCODONE SANDOZ 10 mg, gélule avec des aliments et des boissons
La consommation d’alcool avec la prise d’OXYCODONE SANDOZ peut vous rendre plus somnolent ou augmenter la probabilité d’effets secondaires graves tels qu’une respiration superficielle avec un risque d’arrêt respiratoire et de perte de connaissance. Il est fortement déconseillé de boire de l’alcool pendant le traitement par OXYCODONE SANDOZ.
Le jus de pamplemousse contient une ou plusieurs substances qui peuvent modifier la façon dont votre corps utilise certains médicaments, dont OXYCODONE SANDOZ. Il faut éviter de boire du jus de pamplemousse pendant le traitement par OXYCODONE SANDOZ.
Grossesse et allaitement
Ce médicament est déconseillé pendant la grossesse.
Ce médicament est contre-indiqué chez la femme qui allaite.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou à votre pharmacien avant de prendre ce médicament.
Sportifs
Attention, ce médicament contient du chlorhydrate d’oxycodone qui est inscrit sur la liste des substances dopantes.
Conduite de véhicules et utilisation de machines
Vous pouvez avoir la sensation d'être plus endormi que d'habitude, notamment en début de traitement, lors d'augmentation de posologie et en cas d'association avec d'autres médicaments.
Soyez très prudent. Ne pas conduire sans l'avis d'un professionnel de santé.
OXYCODONE SANDOZ 10 mg, gélule contient du sodium
Ce médicament contient moins de 1 mmol (23 mg) de sodium par gélule c’est-à-dire qu’il est essentiellement « sans sodium ».
3. COMMENT PRENDRE OXYCODONE SANDOZ 10 mg, gélule ?
Avant le début du traitement et régulièrement au cours du traitement, votre médecin discutera avec vous de ce que vous pouvez attendre de l’utilisation d’OXYCODONE SANDOZ, quand et pendant combien de temps vous devez le prendre, quand contacter votre médecin et quand vous devez l’arrêter (voir également « Si vous arrêtez de prendre OXYCODONE SANDOZ 10 mg, gélule »).
Posologie
Adulte et adolescents à partir de 12 ans
La posologie initiale est de 5 mg toutes les 6 heures. L’intervalle entre les prises peut être réduit à 4 heures si besoin sans dépasser 6 prises par jour.
Veillez à toujours prendre ce médicament en suivant exactement les instructions de cette notice ou les indications de votre médecin ou de votre pharmacien. Vérifiez auprès de votre médecin ou de votre pharmacien en cas de doute. Cependant, la posologie dépendra de l'intensité de votre douleur et peut varier en fonction des personnes. Les doses doivent être adaptées à chaque personne et faire l'objet d'une évaluation régulière par le médecin.
Une augmentation de l'intensité de la douleur peut nécessiter une augmentation de la dose quotidienne. Veuillez suivre les instructions de votre médecin ou de votre pharmacien.
Si vous avez l'impression que l'effet d’OXYCODONE SANDOZ est trop fort ou si vous ressentez toujours des douleurs, consultez votre médecin ou votre pharmacien.
La sécurité et l'efficacité d’OXYCODONE SANDOZ n'ont pas été suffisamment testées chez les enfants de moins de 12 ans. Par conséquent, le traitement par OXYCODONE SANDOZ n'est pas recommandé chez les enfants de moins de 12 ans.
Mode d'administration
Prenez toujours OXYCODONE SANDOZ, gélule par voie orale.
Chaque plaquette contient des gélules dans des alvéoles séparées par des perforations (voir figure 1).
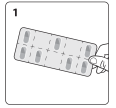
N’appuyez pas sur la gélule pour la sortir de l’alvéole, car cela risque de l’écraser (voir figure 2).
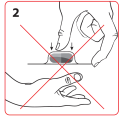
Découpez une seule alvéole de la plaquette en suivant les pointillés (voir figure 3).
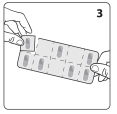
Décollez délicatement la feuille de couverture à partir du coin non scellé afin de prendre la gélule (voir figure 4).
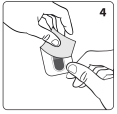
Fréquence d'administration
Ce médicament doit être pris en plusieurs prises journalières, espacées par un intervalle de 4 à 6 heures.
Suivez toujours les instructions de votre médecin.
Durée du traitement
La posologie d’OXYCODONE SANDOZ doit être ajustée fréquemment. Vous devez par conséquent consulter votre médecin régulièrement.
Tout changement ou interruption du traitement doit être effectué selon les recommandations de votre médecin.
Si vous avez pris plus d’OXYCODONE SANDOZ 10 mg, gélule que vous n’auriez dû
Consultez immédiatement votre médecin ou votre pharmacien.
Les personnes qui ont pris une dose trop importante peuvent ressentir une somnolence importante et une sensation de malaise. Des difficultés à respirer peuvent également survenir et entraîner une perte de conscience et un coma nécessitant une prise en charge d'urgence à l'hôpital. Un surdosage peut aussi entraîner une maladie du cerveau (appelée leucoencéphalopathie toxique). Un antidote peut être administré par injection pour arrêter les effets indésirables graves. Si vous demandez une consultation médicale, pensez à prendre cette notice et les gélules restantes pour les montrer à votre médecin.
Si vous oubliez de prendre OXYCODONE SANDOZ 10 mg, gélule
Ne prenez pas de dose double pour compenser celle que vous avez oublié de prendre.
Prenez la dose suivante à l'heure habituelle. Continuez le traitement selon les recommandations de votre médecin ou de votre pharmacien.
Si vous arrêtez de prendre OXYCODONE SANDOZ 10 mg, gélule
Vous ne devez pas arrêter brutalement ce traitement sauf dans le cas ou votre médecin le décide. Si vous souhaitez arrêter le traitement parlez-en à votre médecin. Il vous donnera les recommandations appropriées, habituellement en diminuant les doses progressivement afin que vous n'ayez pas d'effet indésirable.
Si vous avez d'autres questions sur l'utilisation de ce médicament, demandez plus d'informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Les effets indésirables très fréquents (peuvent concerner plus de 1 patient sur 10) sont :
· constipation, qu'il convient de traiter,
· somnolence, nausées et vomissements, qui régressent après un certain temps,
· sensations vertigineuses, prurit, maux de tête.
Les effets indésirables fréquents (peuvent concerner entre 1 et 10 patients sur 100) sont :
· diminution de l’appétit,
· anxiété, état confusionnel, dépression, insomnie, nervosité, troubles de la pensée, cauchemars, plus spécialement chez le sujet âgé, avec éventuellement hallucinations (perception anormale d’un objet qui n’existe pas dans la réalité),
· tremblements, augmentation de la pression intracrânienne se traduisant par des maux de tête voire des vomissements,
· difficultés à respirer (dyspnée),
· douleurs abdominales, diarrhée, sécheresse de la bouche, douleurs au niveau de l’estomac (dyspepsies),
· éruption cutanée, transpiration excessive (hyperhidrose),
· asthénie.
Les effets indésirables peu fréquents (peuvent concerner entre 1 et 10 patients sur 1000) sont :
· réaction allergique (hypersensibilité),
· déshydratation,
· agitation, changement rapide et important de l’humeur (labilité émotionnelle), troubles de l’humeur, hallucinations, diminution de la libido, dépendance au médicament (voir rubrique « Mises en gardes spéciales »),
· troubles de la mémoire (amnésie), convulsions, tonus musculaire trop élevé (hypertonie), diminution de la sensibilité au toucher (hypoesthésie), contractions musculaires involontaires, troubles du langage, malaise (syncope), sensations de fourmillements ou d’engourdissements dans les membres (paresthésies), troubles du goût (dysgueusie),
· troubles de la vision, rétrécissement de la pupille (myosis),
· vertiges,
· palpitations (en cas de syndrome de sevrage),
· dilatation des vaisseaux sanguins (vasodilatation),
· respiration lente et peu profonde (dépression respiratoire),
· difficultés à avaler (dysphagie), flatulences, rots, occlusion intestinale (iléus),
· augmentation des enzymes hépatiques,
· sécheresse de la peau,
· rétention urinaire,
· troubles de l’érection,
· frissons, syndrome de sevrage, malaise, gonflement des mains, des chevilles et des pieds (œdème, œdème périphérique), accoutumance au médicament (tolérance), soif.
Les effets indésirables rares (peuvent concerner entre 1 et 10 patients sur 10 000) sont :
· ralentissement des battements du cœur (bradycardie),
· pression artérielle basse (hypotension), étourdissements au passage à la position debout (hypotension orthostatique),
· éruption cutanée qui démange.
Les effets indésirables suivants sont de fréquence indéterminée :
· apnée du sommeil (pauses respiratoires pendant le sommeil),
· réaction allergique sévère (réaction anaphylactique),
· agressivité,
· douleur anormalement intense (hyperalgésie), léthargie,
· problèmes respiratoires pendant le sommeil (syndrome d’apnée du sommeil),
· caries dentaires,
· diminution de sécrétion de la bile (cholestase), douleur au niveau du foie (colique biliaire),
· absence de règles (aménorrhée),
· insuffisance en hormones sexuelles (hypogonadisme),
· syndrome de sevrage chez le nouveau-né,
· fatigue,
· problème affectant une valve des intestins qui peut provoquer une douleur abdominale haute sévère (dysfonctionnement du sphincter d’Oddi).
En cas d’arrêt brutal de ce médicament, un syndrome de sevrage peut apparaître dont les symptômes sont : bâillements, anxiété, irritabilité, insomnie, frissons, dilatation des pupilles, bouffées de chaleur, tremblements, sueurs, larmoiement, écoulement nasal, nausées, vomissement, perte d’appétit, douleurs abdominales, diarrhée, douleurs musculaires ou articulaires, agitation et convulsions.
Si vous remarquez des effets indésirables non mentionnés dans cette notice, ou si certains effets indésirables deviennent graves, veuillez en informer votre médecin ou votre pharmacien.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER OXYCODONE SANDOZ 10 mg, gélule ?
Tenir ce médicament hors de la vue et de la portée des enfants. Un surdosage accidentel chez l’enfant est dangereux et pourrait être fatal.
Conserver ce médicament dans un lieu de conservation fermé à clé, sûr et sécurisé, où d’autres personnes ne peuvent pas y accéder. Il peut nuire gravement, voire être fatal aux personnes auxquelles il n’a pas été prescrit.
N’utilisez pas ce médicament après la date de péremption indiquée sur la boîte. La date de péremption fait référence au dernier jour de ce mois.
A conserver à une température ne dépassant pas 30°C.
Ne jetez aucun médicament au tout-à-l’égout ni avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient OXYCODONE SANDOZ 10 mg, gélule
· La substance active est :
Chlorhydrate d'oxycodone................................................................................................... 10,0 mg
équivalant à oxycodone base........................................................................................................ 9,0 mg
Pour une gélule.
· Les autres composants sont :
Contenu de la gélule
Cellulose microcristalline, stéarate de magnésium.
Enveloppe de la gélule
Dioxyde de titane (E171), oxyde de fer rouge (E172), oxyde de fer jaune (E172), indigotine (E132), laurylsulfate de sodium, gélatine.
Encre noire d'impression
Gommes laques, oxyde de fer noir (E172), propylèneglycol, hydroxyde de potassium, solution concentrée d’ammoniaque.
Qu’est-ce que OXYCODONE SANDOZ 10 mg, gélule et contenu de l’emballage extérieur
Ce médicament se présente sous forme de gélule, blanche (corps) et marron (tête), de taille 4, avec une impression « 10 » (corps) et « OXY » (tête).
Boîtes de 14, 20, 28, 30, 50 et 56 gélules.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
49 AVENUE GEORGES POMPIDOU
92300 LEVALLOIS-PERRET
Exploitant de l’autorisation de mise sur le marché
SANDOZ
9 PLACE MARIE-JEANNE BASSOT
92300 LEVALLOIS-PERRET
REYKJAVIKURVEGUR 78,
220 HAFNARFJÖRDUR
ISLANDE
ou
BALKANPHARMA DUPNITSA AD
3 SAMOKOVSKO SHOSSE STR.
DUPNITSA 2600
BULGARIE
ou
SALUTAS PHARMA GMBH
OTTO-VON-GUERICKE ALLEE 1
39179 BARLEBEN
ALLEMAGNE
ou
LEK PHARMACEUTICALS D.D.
VEROVSKOVA ULICA 57
1526 LJUBLJANA
SLOVENIE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).