Dernière mise à jour le 02/03/2026
ZOMACTON 10 mg/ml, poudre et solvant pour solution injectable
Indications thérapeutiques
Classe pharmacothérapeutique - code ATC : H01AC01.
ZOMACTON contient une substance, la somatropine connue en tant qu’hormone de croissance. L’hormone de croissance est naturellement produite dans le corps et joue un rôle important dans la croissance. La somatropine contenue dans ZOMACTON est synthétisée par un site de fabrication pharmaceutique.
ZOMACTON est préconisé pour le traitement à long terme des enfants présentant :
· un retard de croissance lié à un déficit de sécrétion de l’hormone de croissance,
· un retard de croissance lié au syndrome de Turner (maladie génétique qui affecte les filles).
Présentations
> 1 flacon(s) en verre de poudre - 1 seringue(s) préremplie(s) en verre de 1 ml de solvant
Code CIP : 370 840-3 ou 34009 370 840 3 1
Déclaration de commercialisation : 12/06/2008
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 252,22 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 253,24 €
- Taux de remboursement :100%
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 22/07/2015 | Renouvellement d'inscription (CT) | Le service médical rendu par ZOMACTON reste important dans : • le traitement à long terme des enfants atteints d'un retard de croissance lié à un déficit en hormone de croissance normale endogène • le traitement de la petite taille chez les enfants atteints du syndrome de Turner, confirmé par analyse chromosomique. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| IV (Mineur) | Avis du 07/12/2011 | Réévaluation SMR | ZOMACTON apporte une amélioration du service médical rendu mineure (ASMR IV) dans la prise en charge du syndrome de Turner. |
| V (Inexistant) | Avis du 06/09/2006 | Inscription (CT) | Cette spécialité est un complément de gamme qui n'apporte pas d'amélioration du service médical rendu. |
Autres informations
- Titulaire de l'autorisation : FERRING SAS
- Conditions de prescription et de délivrance :
- liste I
- prescription initiale hospitalière annuelle
- prescription réservée aux spécialistes et services ENDOCRINOLOGIE
- prescription réservée aux spécialistes et services MALADIES METABOLIQUES
- prescription réservée aux spécialistes et services PEDIATRIE
- Statut de l'autorisation : Valide
- Type de procédure : Procédure de reconnaissance mutuelle
- Code CIS : 6 912 283 2
ANSM - Mis à jour le : 28/09/2021
ZOMACTON 10 mg/ml, poudre et solvant pour solution injectable
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Somatropine*..................................................................................... 10 mg/ml après reconstitution
Pour un flacon.
* Produite sur cellules d’Escherichia coli par la technique de l’ADN recombinant.
Pour la liste complète des excipients, voir rubrique 6.1.
Poudre et solvant pour solution injectable.
ZOMACTON est une poudre lyophilisée blanche à blanc cassé. Le solvant dans la seringue est limpide et incolore.
4.1. Indications thérapeutiques
· dans le traitement à long terme des enfants présentant un retard de croissance lié à un déficit de sécrétion de l’hormone de croissance.
· dans le traitement à long terme d’un retard de croissance lié au syndrome de Turner, confirmé par l’analyse chromosomique.
4.2. Posologie et mode d'administration
Un traitement par ZOMACTON doit être réalisé seulement sous la responsabilité d'un médecin spécialiste qualifié, ayant l’expérience du suivi des patients présentant un déficit en hormone de croissance.
La posologie de ZOMACTON doit être adaptée à chaque patient.
La durée du traitement, en général de plusieurs années, dépend du bénéfice thérapeutique maximal obtenu.
L’administration sous-cutanée d’hormone de croissance peut entraîner une raréfaction ou une augmentation du tissu adipeux au site d’injection. Il est donc préférable d’alterner les sites d’injection.
Déficit de sécrétion de l’hormone de croissance
En général, la dose recommandée est de 0,17 à 0,23 mg/kg de poids corporel par semaine (soit environ 4,9 mg/m² à 6,9 mg/m² de surface cutanée) répartie en 6 à 7 injections S.C par semaine (soit une injection quotidienne de 0,02 à 0,03 mg/kg de poids corporel ou 0,7 à 1,0 mg/m² de surface cutanée).
La dose totale hebdomadaire de 0,27 mg/kg ou 8 mg/m² de surface cutanée ne devra pas être dépassée (soit jusqu’à 0,04 mg/kg/jour).
Syndrome de Turner
En général, la posologie recommandée est de 0,33 mg/kg de poids corporel par semaine (approximativement 9,86 mg/m² de surface corporelle) répartie en 6 à 7 injections S.C par semaine (soit une injection quotidienne de 0,05 mg/kg de poids corporel ou 1,40 à 1,63 mg/m² de surface cutanée).
Pour les instructions pour l’utilisation et la manipulation, voir rubrique 6.6.
Mode d’administration
La dose requise de ZOMACTON 10 mg/ml est administrée au moyen d’une seringue ordinaire.
La solution limpide et incolore doit ensuite être administrée par voie sous-cutanée.
Après la reconstitution, les étapes suivantes doivent être effectuées pour l'injection :
1. Les mains doivent être lavées.
2. Le haut du flacon doit être essuyé avec un tampon imbibé d'alcool pour éviter la contamination du contenu. Ne touchez pas le bouchon en caoutchouc après le nettoyage.
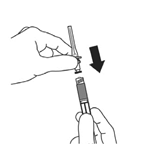
3. Retournez le flacon en gardant le haut de l'aiguille sous la surface du médicament. Tirez doucement sur le piston jusqu'à ce que la quantité prescrite de médicament remplisse la seringue. Si vous n'avez pas assez de médicament pour une dose complète, reconstituez un nouveau flacon pour compléter la différence.
4. Avec l'aiguille toujours dans le flacon retourné, tapotez doucement la seringue pour enlever les bulles d'air.
5. Retirez l'aiguille du flacon et remettez soigneusement le capuchon de l'aiguille jusqu'à ce que vous soyez prêt à injecter.
6. Nettoyer soigneusement le site d'injection avec un tampon imbibé d'alcool.
7. Vérifiez que la dose correcte est dans la seringue.
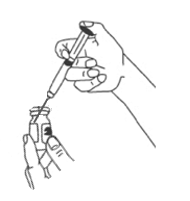
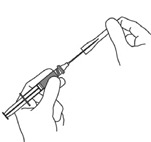
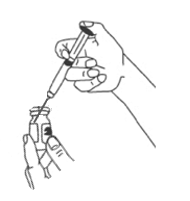
8. Retirez le capuchon de l'aiguille et tenez la seringue comme vous tenez un crayon.
9. Avec votre main libre, pincez doucement la peau autour du site d'injection entre vos doigts.
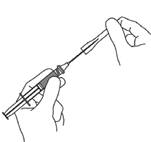
10. Insérez l'aiguille dans le tissu sous-cutané à un angle de 45° à 90° pour réduire l'inconfort.
11. En maintenant la seringue en place, tirez le piston (s'il y a du sang dans la seringue, cela signifie que vous avez pénétré dans un vaisseau sanguin. N'injectez pas ZOMACTON. Retirez l'aiguille, jetez toutes les fournitures et revenez à l'étape 1. Choisissez et nettoyez un nouveau site d'injection). Si aucune trace de sang n'apparaît, poussez lentement le piston jusqu'à ce que la seringue soit vide.
12. Retirez rapidement l'aiguille et appliquez une pression sur le site d'injection avec une compresse de gaze stérile. Jetez l'aiguille et la seringue dans votre conteneur pour objets tranchants.
Ne partagez pas vos seringues, aiguilles ou flacons avec qui que ce soit. Vous pouvez leur donner une infection ou en contracter une.
Pour les instructions concernant la reconstitution du médicament avant administration, voir rubrique 6.6.
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
La somatropine ne doit pas être administrée en cas de tumeur active. Les tumeurs intracrâniennes doivent être inactives et le traitement anti-tumoral doit être terminé avant la mise en place du traitement par l’hormone de croissance. Le traitement doit être arrêté en cas de développement de tumeur.
La somatropine ne doit pas être utilisée pour stimuler la croissance chez les enfants dont les épiphyses sont soudées.
Le traitement par la somatropine est contre-indiqué chez les patients présentant un état critique aigu, souffrant de complications secondaires à une intervention à cœur ouvert, à une intervention chirurgicale abdominale, à un poly-traumatisme, à une insuffisance respiratoire aiguë ou un état similaire.
Chez les enfants souffrant d’une maladie rénale chronique, le traitement par la somatropine devra être interrompu en cas de transplantation rénale.
4.4. Mises en garde spéciales et précautions d'emploi
La dose quotidienne maximale recommandée ne doit pas être dépassée (voir rubrique 4.2).
De très rares cas de myosite ont été observés et pourraient être liés au métacrésol employé comme conservateur. En cas de myalgie ou de douleur disproportionnée au site d’injection, la possibilité d’une myosite doit être envisagée et, si elle est confirmée, il conviendra d’utiliser une formulation de ZOMACTON sans métacrésol.
Patients avec un syndrome de Prader-Willi
ZOMACTON n’est pas indiqué dans le traitement à long terme des enfants qui ont un déficit de croissance lié à un syndrome de Prader-Willi, confirmé par caryotype sauf en cas d’un déficit en hormone de croissance associé. Des cas d’apnée du sommeil et de mort subite survenant après l’initiation d’un traitement par l’hormone de croissance ont été rapportés chez des enfants ayant un syndrome de Prader-Willi qui présentaient un ou plusieurs facteurs de risque suivants : obésité sévère, antécédents d’obstruction des voies respiratoires ou d’apnée du sommeil ou infection respiratoire d’origine non identifiée.
Hypertension intracrânienne
De rares cas d’hypertension intracrânienne bénigne ont été décrits. En présence de céphalées sévères ou récurrentes, de troubles visuels et de nausées/vomissements, un examen du fond d’œil est recommandé afin de rechercher un éventuel œdème papillaire. Si celui-ci est confirmé, le diagnostic d’hypertension intracrânienne bénigne doit être considéré et il convient alors d’arrêter le traitement par l’hormone de croissance (voir également rubrique 4.8). A ce jour, il n’y a pas suffisamment de données pour orienter la décision clinique chez les patients ayant une hypertension intracrânienne normalisée. Si le traitement par hormone de croissance est ré-institué, une surveillance attentive des signes d’hypertension intracrânienne s’impose.
Leucémie
Des cas de leucémie ont été rapportés chez un petit nombre de patients présentant un déficit en hormone de croissance, dont certains avaient été traités par somatropine. Néanmoins, il n’a pas été montré d’augmentation de l’incidence de la leucémie chez les patients traités par l’hormone de croissance et ne présentant pas de facteurs de prédisposition.
Développement d’anticorps
Comme avec tous les produits contenant de la somatropine, un faible pourcentage de patients peut développer des anticorps anti-somatropine. La capacité de liaison de ces anticorps est faible et ils n’ont pas d’effet sur le taux de croissance. La recherche d'anticorps anti-somatropine doit être effectuée chez tout patient non-répondeur au traitement.
Hypothyroïdie
L’hormone de croissance augmente la conversion extra-thyroïdienne de T4 en T3 et peut, en tant que telle, révéler une hypothyroïdie infraclinique. La surveillance de la fonction thyroïdienne devra donc être effectuée chez tous les patients. Chez les patients présentant une insuffisance hypophysaire, un traitement substitutif standard doit être étroitement surveillé lors de l’administration du traitement par la somatropine.
Patients diabétiques
La somatropine pouvant induire une résistance à l’insuline, la recherche d’une éventuelle intolérance au glucose doit être effectuée. Chez les patients diabétiques, la dose d'insuline peut nécessiter un ajustement après l’instauration du traitement par la somatropine. Chez les patients souffrant de diabète ou d'intolérance au glucose, une surveillance étroite doit être mise en place pendant le traitement par la somatropine. ZOMACTON doit aussi être utilisé avec précaution chez les patients ayant des antécédents familiaux de diabète.
Patients avec lésions intracrâniennes
Chez les sujets présentant un déficit en hormone somatotrope secondaire à une lésion intracrânienne, il est recommandé de faire des examens réguliers pour surveiller la possibilité d’une évolution ou d’une récidive de la lésion. Chez les patients ayant survécu à un cancer infantile, une augmentation du risque d’un second néoplasme a été rapporté chez ceux traités par la somatropine lors de leur premier néoplasme. Les tumeurs intracrâniennes, en particulier les méningiomes, chez les patients traités par radiothérapie au début de leur premier néoplasme, étaient les tumeurs plus fréquemment observées en second néoplasme.
Dans l’un ou l’autre cas, il convient d’arrêter l’administration de ZOMACTON.
Chez les patients ayant des antécédents d’affections malignes, l’apparition de signes et symptômes de récidive doivent être très attentivement surveillés.
Scoliose
Une scoliose peut progresser chez les enfants au cours d’une croissance rapide. Les signes de scoliose doivent être surveillés au cours du traitement par l’hormone de croissance.
Patients présentant des désordres endocriniens
Des luxations de la tête fémorale peuvent apparaître plus fréquemment chez les sujets présentant des désordres endocriniens. Tout patient traité par ZOMACTON et développant une claudication ou se plaignant d’une douleur de la hanche ou du genou doit être examiné par un médecin.
Patients souffrant de complications suite à une intervention chirurgicale
Les effets du traitement par l’hormone de croissance ont été étudiés dans le cadre de deux essais contrôlés versus placebo conduits chez 522 patients adultes gravement malades souffrant de complications à la suite d’une intervention chirurgicale abdominale ou à cœur ouvert, de poly-traumatismes accidentels ou d’une insuffisance respiratoire aiguë.
La mortalité a été supérieure (42 % contre 19 %) chez les patients traités par des hormones de croissance (à des doses comprises entre 5,3 et 8 mg/jour) comparativement aux patients ayant reçu un placebo. D’après ces informations, de tels patients ne doivent pas être traités par l’hormone de croissance. En l’absence de données sur l’innocuité de l’hormone de croissance de substitution chez les patients présentant une maladie grave aiguë, il convient d’évaluer les bénéfices pouvant être attendus de la poursuite du traitement avec ses risques potentiels.
Pancréatite
Bien que rare, une pancréatite doit être envisagée chez les patients traités par la somatropine qui ont des douleurs abdominales, en particulier chez les enfants.
L'initiation du traitement par la somatropine peut entraîner une inhibition de la 11βHSD-1 et réduire les concentrations sériques de cortisol. Chez les patients traités par la somatropine, une insuffisance surrénale centrale (secondaire) non diagnostiquée auparavant peut être découverte et un traitement substitutif par glucocorticoïde peut être nécessaire. De plus, les patients traités par glucocorticoïde pour une insuffisance surrénalienne préalablement diagnostiquée peuvent nécessiter une augmentation de leurs doses d'entretien ou de stress, après le début du traitement par la somatropine (voir rubrique 4.5).
Traçabilité
Afin d'améliorer la traçabilité des médicaments biologiques, le nom et le numéro de lot du produit administré doivent être clairement enregistrés.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
L'hormone de croissance diminue la conversion de la cortisone en cortisol et peut mettre en évidence une insuffisance surrénale centrale non encore diagnostiquée ou rendre inefficaces de faibles doses des glucocorticoïdes (voir rubrique 4.4).
Des doses élevées d’androgènes, d’œstrogènes ou de stéroïdes anabolisants peuvent accélérer la maturation osseuse et aller ainsi à l’encontre de la croissance staturale du patient.
La somatropine pouvant entraîner une résistance à l'insuline, on peut être amené à modifier la posologie de l'insuline chez les sujets qui reçoivent ZOMACTON.
Les données fournies par une étude d’interaction conduite chez des adultes présentant un déficit en hormone de croissance suggèrent que l’administration de somatropine pourrait augmenter la clairance de substances connues pour être métabolisées par les isoenzymes du cytochrome P450. En particulier, la clairance des substances métabolisées par le cytochrome P450 3A4 (telles que les stéroïdes sexuels, les corticostéroïdes, les antiépileptiques et la ciclosporine) pourrait être augmentée, entraînant une baisse de leur taux plasmatique. On ne connaît pas la signification clinique de ces observations.
4.6. Fertilité, grossesse et allaitement
Grossesse
Il n’existe pas de données sur l’utilisation de ZOMACTON chez la femme enceinte. Il n’existe pas de données sur l’utilisation de ZOMACTON pendant la gestation chez l’animal. (Voir rubrique 5.3)
En conséquence, ZOMACTON n’est pas recommandé pendant la grossesse et chez la femme en âge de procréer n’utilisant pas de contraception.
Aucune étude clinique avec les produits contenant de la somatropine n’a été menée chez la femme qui allaite.
En l’absence de données sur la possibilité d’excrétion de la somatropine dans le lait maternel, des précautions doivent donc être prises lors de l’administration de produits contenant de la somatropine chez les femmes qui allaitent.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
L'administration sous-cutanée d’hormone de croissance peut entraîner une raréfaction ou une augmentation du tissu adipeux au site d'injection, ainsi qu’une hémorragie ponctuelle et un bleu au site d’injection.
|
Classes de Système d’Organes |
Très fréquent (≥ 1/10) |
Fréquent (≥ 1/100, < 1/10) |
Peu fréquent (≥ 1/1 000, < 1/100) |
Rare (≥ 1/10 000, < 1/1 000) |
Très rare (< 1/10 000) |
|
Affections hématologiques et du système lymphatique |
|
|
Anémie |
|
|
|
Affections cardiaques |
|
|
Tachycardie, (adulte) hypertension |
(enfant) hypertension |
|
|
Affections de l’oreille et du labyrinthe |
|
|
Vertige |
|
|
|
Affections endocriniennes |
|
Hypothyroïdie |
|
|
|
|
Affections oculaires |
|
|
œdème papillaire, diplopie |
|
|
|
Affections gastro-intestinales |
|
|
Vomissements, douleur abdominale, flatulence, nausée |
Diarrhées |
|
|
Troubles généraux et anomalies au site d’administration |
(adulte) œdème, (adulte) œdème périphérique |
(enfant) œdème, (enfant) œdème périphérique, réactions au site d’injection, asthénie |
Faiblesse, atrophie au site d’injection, saignement au site d’injection, masse au site d’injection, hypertrophie |
|
|
|
Affections du système immunitaire |
|
Formation d’anticorps |
|
|
|
|
Investigations |
|
|
|
Test de la fonction rénale anormal |
|
|
Troubles du métabolisme et de la nutrition |
(adulte) hyperglycémie modérée |
(enfant) diminution de la tolérance au glucose |
Hypoglycémie, hyperphosphatémie |
Diabète de type II |
|
|
Affections musculo-squelettiques et systémiques |
(adulte) arthralgie, (adulte) myalgie |
(enfant) arthralgie, (enfant) myalgie, (adulte) raideurs dans les extrémités |
Atrophie musculaire, douleur osseuse, syndrome du canal carpien, (enfant) raideurs dans les extrémités |
|
|
|
Tumeurs bénignes, malignes et non précisées |
|
|
Tumeurs malignes, tumeurs |
|
(enfant) leucémie |
|
Affection du système nerveux |
(adulte) céphalée, (adulte) paresthésie |
Maux de tête, hypertonie, (adulte) insomnie |
Somnolence, nystagmus |
Neuropathie, augmentation de la pression intracrânienne, (enfant) insomnie, (enfant) paresthésie |
|
|
Affections psychiatriques |
|
|
Trouble de la personnalité |
|
|
|
Affections du rein et des voies urinaires |
|
|
Incontinence urinaire, hématurie, polyurie, besoin fréquent d’uriner/pollakiurie, urine anormale |
|
|
|
Affections des organes de reproduction et du sein |
|
|
Pertes génitales, gynécomastie |
|
|
|
Affections de la peau et du tissu sous-cutané |
|
|
Lipodystrophie, atrophie de la peau, dermatite exfoliative, urticaire, hirsutisme, hypertrophie de la peau |
|
|
La survenue de pancréatite a été rapportée après commercialisation, lors de traitement par hormone de croissance (de fréquence indéterminée).
Anticorps anti-somatropine : La protéine somatropine peut donner lieu à la formation d'anticorps. La détermination du pourcentage de la population traitée chez laquelle des anticorps ont été identifiés dépend du produit concerné. Leur capacité de liaison et leurs dosages sont généralement faibles, sans conséquence clinique. Toutefois, la recherche d'anticorps anti-somatropine doit être effectuée en cas d'absence de réponse à la somatropine.
Leucémie : Des cas de leucémies (très rares) ont été rapportés chez les enfants présentant un déficit en hormone de croissance, dont certains traités par la somatropine, et ont été inclus dans l’expérience post-commercialisation. Toutefois, l’augmentation de l’incidence de la leucémie sans facteur de prédisposition n’a pas été montrée.
Des cas de luxation de la tête fémorale et de la maladie de Legg-Calve-Perthes ont été rapportés chez des enfants traités par l’hormone de croissance. La luxation de la tête fémorale survient plus fréquemment en cas de désordres endocriniens et la maladie de Legg-Calve-Perthes en cas de petite taille. En revanche, on ne sait pas si la fréquence de ces 2 maladies est plus élevée ou non lors d’un traitement avec la somatropine. Un inconfort, une douleur au niveau de la hanche et du genou doivent évoquer leur diagnostic.
D’autres réactions indésirables peuvent être considérées comme un effet de classe, comme l’hyperglycémie en raison de la diminution de la sensibilité à l’insuline, la baisse du taux de thyroxine libre et l’éventuelle hypertension intracrânienne bénigne.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www. signalement-sante.gouv.fr.
On ne doit pas dépasser la posologie recommandée de ZOMACTON.
Bien qu'il n'ait pas été rapporté de surdosage avec ZOMACTON, on peut supposer qu’un surdosage pourrait entraîner une hypoglycémie initiale, suivie d'une hyperglycémie.
Les effets d’une administration répétée à long terme des doses supérieures à celles qui sont recommandées, sont inconnus. Cependant, une telle administration peut conduire à des signes et symptômes similaires aux effets connus de l’excès d’hormone de croissance chez l’homme (par ex. acromégalie).
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : somatropine et analogues, code ATC : H01AC01.
Propriétés pharmacodynamiques
Du fait de la similitude de ZOMACTON avec l’hormone de croissance humaine d’origine hypophysaire (h-GH) en ce qui concerne la séquence des acides aminés, la longueur de la chaîne (191 A.A.) et le profil pharmacocinétique, on peut s'attendre à des effets pharmacologiques semblables à ceux de l'hormone endogène.
Mécanisme d'action
Croissance osseuse
L’hormone de croissance entraîne une croissance harmonieuse du squelette chez l'homme. Chez des enfants présentant un déficit confirmé en h-GH, l’administration de ZOMACTON a provoqué une accélération linéaire de la croissance. L’augmentation de la taille observée après administration de ZOMACTON est due à un effet de l’hormone au niveau des cartilages de conjugaison des os longs.
Chez les enfants n’ayant pas une concentration de h-GH suffisante, ZOMACTON entraîne une accélération de la croissance, et une élévation des concentrations de IGF-1 (Insulin-like Growth Factor/Somatomedine-C) semblable à celle observée après un traitement par h-GH. On a également observé une augmentation de la concentration moyenne des phosphatases alcalines sériques.
Croissance tissulaire
En réponse à l’administration de l’hormone de croissance, on observe également une augmentation de la taille des autres tissus, proportionnelle à l’augmentation du poids corporel.
Ces modifications comportent : une croissance accrue du tissu conjonctif, de la peau et des annexes ; un développement du muscle squelettique en augmentant à la fois le nombre et la taille des cellules musculaires; la croissance du thymus ; une augmentation du volume du foie avec prolifération des cellules et une légère augmentation de la taille des gonades, des surrénales et de la thyroïde.
La croissance disproportionnée de la peau et des os plats et une maturation sexuelle accélérée n’ont pas été rapportées en association avec le traitement par l’hormone de croissance.
Métabolisme protéique, glucidique et lipidique
L’hormone de croissance a un effet d’épargne sur les protides, avec augmentation du transport des acides aminés dans les tissus. Ces deux actions se conjuguent pour augmenter la synthèse des protéines. Le catabolisme glucidique et la lipogenèse sont diminués sous l’action de l’hormone de croissance.
A dose élevée, ou en l'absence d'insuline, l’hormone de croissance agit comme un agent diabétogène, entraînant des effets typiquement observés au cours du jeûne (c’est-à-dire intolérance aux glucides, inhibition de la lipogenèse, mobilisation des graisses et production de corps cétoniques).
Métabolisme des sels minéraux
Les concentrations en sodium, potassium et phosphore sont maintenues après traitement par l’hormone de croissance. L’élimination accrue de calcium par le rein est compensée par l’augmentation de son absorption intestinale. Les concentrations sériques en calcium ne sont pas significativement modifiées chez les sujets recevant ZOMACTON ou la h-GH. Une élévation de la concentration sérique des phosphates inorganiques a été observée après administration de ZOMACTON ou de h-GH. L’accumulation de ces électrolytes traduit une augmentation des besoins au cours de la synthèse tissulaire.
5.2. Propriétés pharmacocinétiques
24 sujets adultes sains ont reçu la somatropine à la dose de 1,67 mg par injection sous-cutanée . Le pic de la concentration plasmatique d’environ 17 ng/ml est retrouvé environ 4 heures après l’administration. Le volume apparent de distribution (V/F) de la somatropine était de 48 litres, la clairance apparente (CL/F) était de 15 L/h et une demi-vie terminale de 2,2 heures a été observée.
Les données provenant d’autres produits contenant de la somatropine suggèrent que la biodisponibilité de la somatropine administrée par voie sous-cutanée est environ de 80 % chez l’adulte sain et que le foie aussi bien que les reins sont des organes importants pour le catabolisme des protéines et l’élimination du produit.
5.3. Données de sécurité préclinique
La somatropine obtenue par génie génétique est identique à l’hormone de croissance humaine endogène. Elle possède les mêmes propriétés biologiques et est habituellement administrée aux doses physiologiques. En conséquence, en l’absence d’effet attendu, aucune étude de toxicité générale, de toxicité sur la fonction de la reproduction, en carcinogenèse n’a été effectuée.
Mannitol
Phosphate disodique dodécahydraté
Phosphate monosodique dihydraté.
Solvant
Métacrésol
Eau pour préparations injectables.
3 ans.
Après reconstitution la solution peut être conservée au maximum pendant 28 jours entre 2 °C et 8 °C (au réfrigérateur), à l’abri de la lumière.
Après reconstitution, le flacon doit être conservé en position verticale.
6.4. Précautions particulières de conservation
À conserver au réfrigérateur (entre 2 °C et 8 °C) dans l’emballage extérieur, à l’abri de la lumière.
Pour les conditions de conservation du médicament après reconstitution, voir la rubrique 6.3.
6.5. Nature et contenu de l'emballage extérieur
ZOMACTON est fourni dans différents emballages selon les pays :
Nécessaires pour une utilisation en injection avec aiguille :
Poudre : en flacon (verre de type I), muni d’un bouchon (caoutchouc, polymère halobutyle), avec une bague de sertissage en aluminium et un capuchon amovible (plastique).
Solvant : seringue (verre de type I) avec un capuchon d’embout (caoutchouc, polymère halobutyle), un bouchon-piston (caoutchouc, polymère halobutyle).
Boîtes de 1, 3, 5.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Reconstitution
La poudre doit être exclusivement reconstituée en introduisant dans le flacon, le solvant fourni dans la seringue.
Une description générale de la reconstitution et du procédé d’administration est détaillée ci-dessous. La reconstitution doit être réalisée selon les règles de bonne pratique, en particulier dans le respect des conditions d’asepsie.
1. Se laver les mains.
2. Enlevez le capuchon de protection en plastique jaune du flacon.
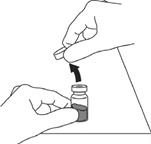
3. Passez une solution antiseptique sur le haut du flacon ou un tampon imbibé d’alcool afin d’éviter la contamination du contenu. Ne touchez pas le bouchon en caoutchouc après le nettoyage.
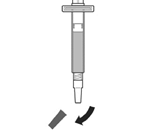
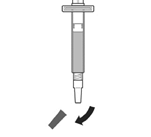
4. Prenez la seringue préremplie avec le solvant. Enlevez le capuchon gris. Fixez l'aiguille de reconstitution à la seringue préremplie. Retirez le capuchon de l'aiguille.
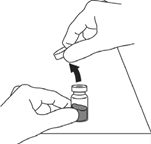
5. Placez l’aiguille au centre du bouchon en caoutchouc propre et dans le flacon et injecter lentement le solvant dans le flacon en dirigeant le jet du liquide contre la paroi en verre afin d’éviter la formation de mousse.
6. Jetez la seringue et l'aiguille dans un conteneur pour objets tranchants
7. Faire tourner le flacon en rotations douces durant quelques minutes jusqu’à la dissolution complète du contenu. Ne pas secouer. Ceci pourrait provoquer la dénaturation de la substance active.
8. Si la solution reste trouble ou contient des particules, elle ne doit pas être utilisée. En cas de trouble après réfrigération, le médicament doit être amené à température de la pièce. Si l’aspect trouble persiste, jeter le flacon et le contenu.
Le contenu doit être limpide et incolore après reconstitution.
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
|
Reconstitution avec une seringue ordinaire
|
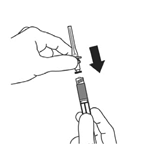
Etape 5
Le flacon doit être tourné par rotations douces jusqu’à dissolution complète et obtention d’une solution limpide et incolore.
Après reconstitution, placez le flacon de ZOMACTON en position verticale dans le réfrigérateur entre 2°C et 8°C.
Evitez de secouer vigoureusement le mélange. Si la solution reste trouble ou contient des particules, le flacon et son contenu doivent être jetés. En cas de trouble après réfrigération, la solution doit être amenée à température de la pièce. Si le trouble persiste encore, jetez le flacon et son contenu.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
7, RUE JEAN-BAPTISTE CLEMENT
94250 GENTILLY
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34 009 370 840 3 1 : 10 mg de poudre en flacon (verre de type I), avec un bouchon (polymère halobutylique), muni d’une bague de sertissage (aluminium) et d’une capsule « Flip-off » (plastique) + 1 ml de solvant en seringue préremplie (verre de type I) munie d’un bouchon-piston (polymère halobutylique)- Boîte de 1.
· 34 009 375 471 6 1 : 10 mg de poudre en flacon (verre de type I), avec un bouchon (polymère halobutylique), muni d’une bague de sertissage (aluminium) et d’une capsule « Flip-off » (plastique) + 1 ml de solvant en seringue préremplie (verre de type I) munie d’un bouchon-piston (polymère halobutylique)- Boîte de 3.
· 34 009 375 472 2 2 : 10 mg de poudre en flacon (verre de type I), avec un bouchon (polymère halobutylique), muni d’une bague de sertissage (aluminium) et d’une capsule « Flip-off » (plastique) + 1 ml de solvant en seringue préremplie (verre de type I) munie d’un bouchon-piston (polymère halobutylique)- Boîte de 5.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I.
Médicament soumis à prescription initiale hospitalière annuelle réservée aux spécialistes en pédiatrie ou en endocrinologie et maladies métaboliques exerçant dans les services spécialisés en pédiatrie ou en endocrinologie et maladies métaboliques.
ANSM - Mis à jour le : 28/09/2021
ZOMACTON 10 mg/ml, poudre et solvant pour solution injectable
Somatropine
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que ZOMACTON 10 mg/ml, poudre et solvant pour solution injectable et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser ZOMACTON 10 mg/ml, poudre et solvant pour solution injectable ?
3. Comment utiliser ZOMACTON 10 mg/ml, poudre et solvant pour solution injectable ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver ZOMACTON 10 mg/ml, poudre et solvant pour solution injectable ?
6. Contenu de l’emballage et autres informations.
Dans cette notice le « vous » fait référence à vous ou à l’enfant ou l’adolescent dont vous prenez soin.
1. QU’EST-CE QUE ZOMACTON 10 mg/ml, poudre et solvant pour solution injectable ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique - code ATC : H01AC01.
ZOMACTON contient une substance, la somatropine connue en tant qu’hormone de croissance. L’hormone de croissance est naturellement produite dans le corps et joue un rôle important dans la croissance. La somatropine contenue dans ZOMACTON est synthétisée par un site de fabrication pharmaceutique.
ZOMACTON est préconisé pour le traitement à long terme des enfants présentant :
· un retard de croissance lié à un déficit de sécrétion de l’hormone de croissance,
· un retard de croissance lié au syndrome de Turner (maladie génétique qui affecte les filles).
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER ZOMACTON 10 mg/ml, poudre et solvant pour solution injectable ?
N’utilisez jamais ZOMACTON 10 mg/ml, poudre et solvant pour solution injectable :
· si vous êtes allergique à la somatropine ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
· chez les enfants dont la croissance osseuse est terminée (épiphyses soudées).
· si vous avez une tumeur active (cancer), n’utilisez pas ZOMACTON et informez en votre médecin. Avant de commencer votre traitement par ZOMACTON, les tumeurs doivent être inactives et vous devez avoir fini votre traitement anti-tumoral.
· si vous êtes gravement malade en raison de complications suite à une intervention chirurgicale à cœur ouvert ou abdominale, un poly-traumatisme accidentel, ou une insuffisance respiratoire aiguë.
· chez les enfants souffrant d’une maladie chronique rénale en cas de transplantation rénale.
Avertissements et précautions
Un traitement par ZOMACTON doit être réalisé uniquement sous la responsabilité d'un médecin spécialiste qualifié, ayant l’expérience du suivi des patients présentant un déficit en hormone de croissance.
Adressez-vous à votre médecin ou pharmacien avant d’utiliser ZOMACTON 10 mg/ml, poudre et solvant pour solution injectable :
· ZOMACTON contient un conservateur dénommé, métacrésol. De très rares cas d’inflammation musculaire ont été observés et pourraient être liés au métacrésol. En cas de douleur musculaire ou de douleur au site d’injection, prévenez votre médecin.
· Les enfants souffrant du syndrome de Prader-Willi ne doivent pas être traités avec ZOMACTON, sauf en cas de déficit en hormone de croissance avéré.
· Si vous avez des antécédents familiaux de diabète sucré, la mesure de la concentration du sucre dans le sang doit être faite régulièrement par votre médecin.
· Si vous êtes diabétique, un contrôle strict du glucose sanguin est recommandé et une adaptation de la dose d’insuline peut être nécessaire afin de maintenir le contrôle du diabète. Votre médecin vous indiquera si cela est nécessaire.
· Si votre déficit en hormone de croissance est secondaire à un problème cérébral (lésion dans le cerveau), il est recommandé de surveiller attentivement la possibilité d’une évolution ou d’une récidive de la lésion. En cas de confirmation, votre médecin vous indiquera s’il convient d’arrêter le traitement par ZOMACTON.
· Si vous avez des antécédents d’affections graves telles qu’un cancer, le traitement par ZOMACTON peut entraîner la récidive ou l’aggravation de la maladie. Par conséquent, si vous remarquez un symptôme qui vous préoccupe, vous devez en parler à votre médecin immédiatement.
· Si vous avez un traitement substitutif par des glucocorticoïdes, vous devez consulter votre médecin régulièrement, car la dose des glucocorticoïdes peut nécessiter un ajustement.
· Le traitement par ZOMACTON peut conduire à des taux bas d’hormone thyroïde qu’il conviendra, si nécessaire, de traiter également. Pour ce contrôle, votre médecin doit effectuer régulièrement des tests pour s’assurer que votre thyroïde fonctionne bien.
· Certains enfants atteints d’un déficit en hormone de croissance ont développé une leucémie (augmentation du nombre de globules blancs), qu’ils aient ou non été traités par hormone de croissance. Toutefois, une incidence accrue de la leucémie chez les personnes traitées par hormone de croissance sans facteurs prédisposants n’a pas été démontrée. Aucun lien de cause à effet n’a été établi avec le traitement par hormone de croissance.
· Si vous souffrez de complications suite à une intervention chirurgicale, à un traumatisme ou à une insuffisance respiratoire aiguë.
· Si vous devez subir une intervention ou si vous êtes accidentellement blessé ou gravement malade, votre médecin peut réévaluer votre traitement.
· ZOMACTON peut entrainer une inflammation du pancréas, provoquant de fortes douleurs abdominales et dorsales. Contactez votre médecin si vous ou votre enfant ressentez des maux d’estomac après avoir pris ZOMACTON.
Au cours du traitement par ZOMACTON, vous devez prévenir votre médecin ou contacter le service des urgences le plus proche en cas de survenue :
· de maux de tête sévères ou répétés,
· de troubles visuels,
· de nausées et/ou vomissements.
Veuillez consulter le médecin dès que vous ressentez une douleur à un membre ou à la hanche ou au genou.
Enfants
Sans objet.
Autres médicaments et ZOMACTON 10 mg/ml, poudre et solvant pour solution injectable
Informez votre médecin ou pharmacien si vous utilisez, avez récemment utilisé ou pourriez utiliser tout autre médicament y compris les médicaments obtenus sans ordonnance.
Veuillez indiquer à votre médecin ou votre pharmacien :
· Si vous prenez un traitement par stéroïdes en raison d’un déficit associé en ACTH (hormone adréno-corticotrope). En cours de traitement par ZOMACTON, le traitement par stéroïdes doit être habituellement ajusté.
· Si vous prenez des doses élevées d’androgènes, d’œstrogènes ou de stéroïdes anabolisants car ils peuvent réduire le gain de taille finale.
· Si vous prenez des médicaments prescrits régulièrement tels que les stéroïdes, les traitements pour l’épilepsie ou les immunosuppresseurs.
· Si vous êtes en cours de traitement par l’insuline, on peut être amené à modifier la posologie de l'insuline afin de maintenir le contrôle de la glycémie. Votre médecin vous indiquera si cela est nécessaire.
ZOMACTON 10 mg/ml, poudre et solvant pour solution injectable avec des aliments et boissons
Sans objet.
Ce médicament ne doit pas être utilisé au cours de la grossesse ou en cas d’allaitement.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
Conduite de véhicules et utilisation de machines
ZOMACTON n’a pas d’influence sur l’aptitude à conduire des véhicules ou à utiliser des machines.
3. COMMENT UTILISER ZOMACTON 10 mg/ml, poudre et solvant pour solution injectable ?
Votre médecin ou infirmier(ère) vous précisera la dose qui vous convient exactement. La dose est administrée par injection sous-cutanée (sous la peau) à l’aide d’une seringue.
Posologie
Déficit en hormone de croissance chez l’enfant
Le médecin calculera la dose exacte qui vous convient en fonction de votre poids (kg). La dose usuelle recommandée est de 0,17 à 0,23 mg/kg de poids corporel par semaine, en 6 à 7 injections par semaine, soit une injection de 0,02 à 0,03 mg/kg de poids corporel par jour.
La dose totale de 0,27 mg/kg par semaine, soit jusqu’à 0,04 mg/kg/jour, ne devra pas être dépassée.
Syndrome de Turner (chez les filles uniquement)
Le médecin calculera la dose exacte qui vous convient en fonction de votre poids (kg). La posologie usuelle recommandée est de 0,33 mg/kg de poids corporel par semaine, en 6 à 7 injections par semaine soit une injection de 0,05 mg/kg de poids corporel par jour.
Instructions pour la reconstitution
Reconstitution
ZOMACTON est fourni sous forme de poudre et doit être reconstitué exclusivement avec le solvant (liquide) fourni.
La solution pour injection à 10 mg/ml est préparée en reconstituant la poudre ZOMACTON dans 1 ml de solvant à l’aide d’une seringue préremplie comme décrit ci-après.
1. Les mains doivent être lavées.
2. Retirez le capuchon protecteur en plastique jaune du flacon.
3. Le haut du flacon doit être essuyé avec une solution antiseptique ou un tampon imbibé d'alcool pour éviter la contamination du contenu. Ne touchez pas le bouchon en caoutchouc après le nettoyage.
4. Prenez la seringue préremplie de solvant. Retirez le capuchon gris. Fixez l'aiguille de reconstitution à la seringue préremplie. Retirez le capuchon de l'aiguille.
5. Placez l'aiguille au centre du bouchon en caoutchouc propre et dans le flacon et injecter lentement le solvant dans le flacon en dirigeant le jet de liquide contre la paroi en verre afin d'éviter la formation de mousse.
6. Jetez la seringue dans un conteneur pour objets tranchants
7. Agiter doucement le flacon plusieurs fois jusqu'à ce que le contenu soit complètement dissous. Ne secouez pas.
8. Si la solution est trouble ou contient des particules, elle ne doit pas être utilisée. En cas de trouble après réfrigération, laisser le produit se réchauffer à température ambiante. Si le trouble persiste, jetez le flacon et son contenu.
Le contenu doit être clair et incolore après reconstitution.
|
|
Reconstitution avec une seringue ordinaire
|
|
|
||||||||
|
|
|||||||||
Etape 5
Le flacon doit être tourné par rotations douces jusqu’à dissolution complète et obtention d’une solution limpide et incolore.
Après reconstitution, placez le flacon de ZOMACTON en position verticale dans le réfrigérateur entre 2°C et 8°C.
Evitez de secouer vigoureusement le mélange. Si la solution reste trouble ou contient des particules, le flacon et son contenu doivent être jetés. En cas de trouble après réfrigération, la solution doit être amenée à température de la pièce. Si le trouble persiste encore, jetez le flacon et son contenu
Administration
La dose requise de ZOMACTON 10 mg/ml est administrée avec une seringue classique comme indiqué par votre professionnel de santé à l’hôpital.
Après la reconstitution, les étapes suivantes doivent être effectuées pour l'injection :
1. Les mains doivent être lavées.
2. Le haut du flacon doit être essuyé avec un tampon imbibé d'alcool pour éviter la contamination du contenu. Ne touchez pas le bouchon en caoutchouc après le nettoyage.
3. Retournez le flacon en gardant le haut de l'aiguille sous la surface du médicament. Tirez doucement sur le piston jusqu'à ce que la quantité prescrite de médicament remplisse la seringue. Si vous n'avez pas assez de médicament pour une dose complète, reconstituez un nouveau flacon pour combler la différence.
4. Avec l'aiguille toujours dans le flacon retourné, tapotez doucement la seringue pour enlever les bulles d'air.
5. Retirez l'aiguille du flacon et remettez soigneusement le capuchon de l'aiguille jusqu'à ce que vous soyez prêt à injecter.
6. Nettoyer soigneusement le site d'injection avec un tampon imbibé d'alcool.
7. Vérifiez que la dose correcte est dans la seringue.
8. Retirez le capuchon de l'aiguille et tenez la seringue comme vous tenez un crayon.
9. Avec votre main libre, pincez doucement la peau autour du site d'injection entre vos doigts.
10. Insérez l'aiguille dans le tissu sous-cutané à un angle de 45° à 90° pour réduire l'inconfort.
11. En maintenant la seringue en place, tirez le piston (s'il y a du sang dans la seringue, cela signifie que vous avez pénétré dans un vaisseau sanguin. N'injectez pas ZOMACTON. Retirez l'aiguille, jetez toutes les fournitures et revenez à l'étape 1. Choisissez et nettoyez un nouveau site d'injection). Si aucune trace de sang n'apparaît, poussez lentement le piston jusqu'à ce que la seringue soit vide.
12. Retirez rapidement l'aiguille et appliquez une pression sur le site d'injection avec une compresse de gaze stérile. Jetez l'aiguille et la seringue dans votre conteneur pour objets tranchants.
Ne partagez pas vos seringues, aiguilles ou flacons avec qui que ce soit. Vous pouvez leur donner une infection ou en contracter une.
Tout produit non utilisé ou déchet doit être éliminé conformément aux exigences locales.
Si vous avez utilisé plus de ZOMACTON 10 mg/ml, poudre et solvant pour solution injectable que vous n’auriez dû
Un surdosage avec ZOMACTON pourrait entraîner une faible concentration de sucre dans le sang (hypoglycémie initiale), suivie d'une forte concentration de sucre dans le sang (hyperglycémie).
Si vous, ou quelqu’un d’autre, avez utilisé une dose trop forte de ZOMACTON, consultez un médecin ou le service d’urgence le plus proche dès que possible. Les effets de l’administration répétée de doses supérieures à celles qui sont recommandées, sont inconnus.
Si vous oubliez d’utiliser ZOMACTON 10 mg/ml, poudre et solvant pour solution injectable
Si une injection a été oubliée, ne vous inquiétez pas. Continuez comme d’habitude et prenez la prochaine dose normalement.
Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre.
Vous pouvez vous sentir en état d’hypoglycémie (faible concentration de sucre sanguin) qui provoque des vertiges, un état confusionnel ou des troubles visuels. Bien que l’efficacité du traitement à long terme ne doit pas être affectée, vous devez consulter votre médecin si ces symptômes surviennent.
Si vous arrêtez d’utiliser ZOMACTON 10 mg/ml, poudre et solvant pour solution injectable
Sans objet.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
L’administration sous-cutanée d’hormone de croissance peut entraîner une raréfaction ou une augmentation du tissu graisseux aussi bien qu’un saignement ponctuel ou une ecchymose (coloration pourpre de la peau) au site d’injection. Il est donc préférable d’alterner les sites d’injection.
Dans de rares cas, les patients ont présenté une douleur ou une éruption prurigineuse au site d’injection.
Effets indésirables très fréquents (pouvant affecter plus de 1 personne sur 10) :
Chez l’adulte seulement :
· gonflement dû à une rétention d’eau, surtout au niveau des pieds et des mains (œdème)
· légère élévation du taux de sucre dans le sang (hyperglycémie)
· douleur articulaire (arthralgie)
· douleur musculaire (myalgie)
· maux de tête
· engourdissement, fourmillements, sensation de brûlure (paresthésie)
Effets indésirables fréquents (pouvant affecter jusqu’à 1 personne sur 10) :
Chez l’adulte et l’enfant :
· hypothyroïdie
· une réaction immunitaire à l’hormone de croissance, révélée lors d’une analyse de sang (formation d’anticorps)
· maux de tête
· augmentation du tonus musculaire (hypertonie)
Chez l’enfant seulement :
· gonflement dû à une rétention d’eau, surtout au niveau des pieds et des mains (œdème, œdème périphérique)
· réactions au site d’injection
· faiblesse (asthénie)
· diminution de la tolérance au glucose
· douleur articulaire (arthralgie)
· douleur musculaire (myalgie)
Chez l’adulte seulement :
· raideur dans les jambes et/ou les bras
· difficulté à s’endormir et/ou à dormir (insomnie)
Effets indésirables peu fréquents (pouvant affecter jusqu’à 1 personne sur 100) :
Chez l’adulte et l’enfant :
· anémie
· accélération du rythme cardiaque (tachycardie)
· sensation de tournis, trouble de l’équilibre (vertige)
· vision double (diplopie)
· œdème papillaire
· vomissements, douleur abdominale, flatulence, nausée
· faiblesse
· atrophie, saignement, induration au site d’injection, hypertrophie
· diminution du taux de sucre dans le sang (hypoglycémie)
· hyperphosphatémie
· atrophie musculaire
· douleur osseuse
· syndrome du canal carpien
· tumeur maligne, tumeur
· besoin de sommeil (somnolence)
· mouvement oculaire involontaire (nystagmus)
· trouble de la personnalité
· incontinence urinaire, hématurie, polyurie, besoin fréquent d’aller uriner, urine anormale
· réactions au site d’injection (dont lipodystrophie, atrophie de la peau, dermatite exfoliative, urticaire, hirsutisme, hypertrophie de la peau)
· Gonflement des seins (gynécomastie)
Chez l’enfant seulement :
· raideur dans les jambes et/ou les bras
Chez l’adulte seulement :
· élévation de la pression sanguine (hypertension)
Effets indésirables rares ( pouvant affecter jusqu’à 1 personne sur 1 000) :
Chez l’adulte et l’enfant :
· diarrhée
· test de la fonction rénale anormal
· diabète sucré de type II
· picotements ou engourdissement dans certaines parties du corps (neuropathie)
· excès liquidien autour du cerveau (maux de tête répétés ou sévères, vision trouble et nausée et/ou vomissements)
Chez l’enfant :
· élévation de la pression sanguine (hypertension)
· difficulté à s’endormir et/ou à dormir (insomnie)
· engourdissement, fourmillements, sensation de brûlure (paresthésie)
Effets indésirables très rares ( pouvant affecter jusqu’à 1 personne sur 10 000) :
Chez l’enfant seulement :
· leucémie (l’incidence semble similaire à celle observée chez les enfants dans la population générale)
Si vous remarquez des effets indésirables non mentionnés dans cette notice, ou si certains effets indésirables mentionnés deviennent graves, veuillez en informer votre médecin ou votre pharmacien.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: www. signalement-sante.gouv.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER ZOMACTON 10 mg/ml, poudre et solvant pour solution injectable ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’emballage. La date de péremption fait référence au dernier jour de ce mois.
A conserver au réfrigérateur (entre 2 °C et 8 °C). Conserver dans l’emballage extérieur, à l’abri de la lumière.
Une fois la poudre dissoute dans le liquide fourni (reconstituée), conserver le flacon en position verticale entre 2 °C et 8 °C (au réfrigérateur). Après mélange, la solution doit être utilisée dans les 28 jours. Vous devez jeter toute solution restante dans le flacon à la fin de cette période.
Si le mélange est trouble au moment où vous le sortez du réfrigérateur, amener la solution à température ambiante. Si le mélange est encore trouble ou se colore, jetez le flacon et son contenu.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient ZOMACTON 10 mg/ml, poudre et solvant pour solution injectable
· La substance active est :
Somatropine.................................................................... 10 mg (10 mg/ml après reconstitution)
· Les autres composants sont :
o Poudre : mannitol, phosphate disodique dodécahydraté, phosphate monosodique dihydraté.
o Solvant : métacrésol, eau pour préparation injectable.
Ce médicament se présente sous forme d'une poudre et d'un solvant pour solution injectable (poudre fournie en flacon et le solvant en seringue).
La poudre est blanche à blanc cassé. Une fois dissoute dans le solvant fourni une solution incolore est obtenue.
ZOMACTON se présente en boîtes de 1,3 et 5 et se compose de : 10 mg de somatropine en flacon et 1 ml de solvant en seringue.
Titulaire de l’autorisation de mise sur le marché
7, RUE JEAN-BAPTISTE CLEMENT
94250 GENTILLY
Exploitant de l’autorisation de mise sur le marché
7, RUE JEAN-BAPTISTE CLEMENT
94250 GENTILLY
WITTLAND 11
24109 KIEL
ALLEMAGNE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les États membres de l'Espace économique européen et au Royaume-Uni (Irlande du Nord) sous les noms suivants :: Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
< {MM/AAAA}>< {mois AAAA}.>
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).