Dernière mise à jour le 28/04/2026
FUCITHALMIC 1 POUR CENT, gel ophtalmique
Indications thérapeutiques
Classe pharmacothérapeutique - code ATC : Antibiotiques - code ATC : S01AA13
Ce médicament est destiné à l'œil et se présente sous forme de gel ophtalmique. Il contient un antibiotique, l'acide fusidique, qui agit en tuant certaines bactéries responsables d'infections.
Ce médicament est indiqué dans le traitement local de certaines infections de l'œil et des paupières : conjonctivites, kératites (inflammation de la cornée d'origine bactérienne), ulcères de la cornée, blépharites (inflammation des paupières d'origine bactérienne) et orgelets (infection d'une glande située dans la paupière se présentant habituellement comme une pustule centrée sur un cil).
Présentations
> 1 tube(s) aluminium polyéthylène de 3 g
Code CIP : 331 913-3 ou 34009 331 913 3 7
Déclaration de commercialisation : 19/01/1990
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 2,58 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 3,60 €
- Taux de remboursement :65%
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 07/09/2016 | Renouvellement d'inscription (CT) | Le service médical rendu par FUCITHALMIC reste important dans l’indication de l’AMM. |
Amélioration du service médical rendu (ASMR)
Pas d'ASMR disponible pour ce médicament (plus d'informations dans l'aide )
ANSM - Mis à jour le : 13/02/2026
FUCITHALMIC 1 POUR CENT, gel ophtalmique
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Pour 100 g.
Excipient(s) à effet notoire : chlorure de benzalkonium : 0,10 mg/g.
Pour la liste complète des excipients, voir rubrique 6.1.
4.1. Indications thérapeutiques
Il convient de tenir compte des recommandations officielles concernant l'utilisation appropriée des antibactériens.
4.2. Posologie et mode d'administration
Posologie
Une goutte dans le sac conjonctival inférieur matin et soir.
Mode d'administration
Voie ophtalmique uniquement.
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1
4.4. Mises en garde spéciales et précautions d'emploi
Les lentilles de contact ne doivent pas être portées pendant le traitement avec FUCITHALMIC, le produit contenant de fines particules pouvant entrainer des lésions de la cornée avec le port de lentilles.
Les lentilles de contact peuvent être utilisées 12 heures après la fin du traitement.
FUCITHALMIC contient du chlorure de benzalkonium qui peut provoquer une irritation des yeux et une décoloration des lentilles de contact.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
4.6. Fertilité, grossesse et allaitement
Grossesse
Les études chez l’animal n'ont montré aucun effet délétère direct ou indirect sur la reproduction. Il existe des données limitées sur l'utilisation de l'acide fusidique chez la femme enceinte.
En raison du bénéfice thérapeutique attendu, l'utilisation d'acide fusidique peut être envisagée pendant la grossesse si nécessaire, malgré des données cliniques limitées.
Allaitement
Les données suggèrent un passage d'acide fusidique dans le lait maternel. Par mesure de précaution, il est préférable d'éviter d'utiliser de l'acide fusidique pendant l'allaitement.
Fertilité
Aucune étude clinique sur les effets de l'acide fusidique sur la fertilité n'a été menée. Les études précliniques chez le rat n'ont montré aucun effet de l'acide fusidique sur la fertilité.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Cependant FUCITHALMIC est susceptible de provoquer une vision floue après son application et les patients doivent en tenir compte.
L'estimation de la fréquence des effets indésirables repose sur une analyse groupée des données issues des essais cliniques et des déclarations spontanées.
Sur la base des données groupées, issues des essais cliniques incluant 2499 patients atteints d'infections oculaires, dont une conjonctivite aiguë, ayant reçu FUCITHALMIC, la fréquence des effets indésirables était de 11,3%.
Les réactions indésirables les plus fréquemment rapportées au cours du traitement sont des manifestations au niveau du site d'application telles que douleur, prurit et irritation/gêne, survenant chez environ 8,5% des patients, suivi de la vision floue, rapportée chez environ 1,2% des patients. L'angioœdème a été signalé chez quelques patients après le marketing.
Les effets indésirables sont classés par système d'organes (SOC) selon la convention MedDRA, en commençant par les plus fréquemment rapportés. Au sein de chaque groupe de fréquence, les effets indésirables sont présentés suivant un ordre décroissant de gravité.
Très fréquent (≥1/10),
Fréquent (≥1/100 à <1/10),
Peu fréquent (≥1/1 000 à <1/100),
Rare (≥1/10 000 à <1/1 000),
Très rare (<1/10 000),
Fréquence indéterminée (ne peut pas être estimée à partir des données disponibles).
|
Classification par système organe |
Fréquence |
Effets indésirables |
|
Affections du système immunitaire |
Peu fréquent |
Hypersensitivité (y compris rash, angiodème et urticaire) |
|
Affections oculaires |
Fréquent |
Vision floue (transitoire) |
|
Peu fréquent |
Oedème des paupières, augmentation du larmoiement |
|
|
Rare |
Aggravation de la conjonctivite |
|
|
Troubles généraux et manifestations au niveau du site d'application |
Fréquent |
Douleur au niveau du site d’application (y compris brûlure, picotements) Prurit au niveau du site d’application, gêne/irritation au niveau du site d’application |
Population pédiatrique :
Le profil de sécurité observé est le même chez les enfants et les adultes.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
La quantité totale d'acide fusidique contenue dans un tube de 5 g de FUCITHALMIC (50 mg) ne dépasse pas la dose quotidienne totale, approuvée pour les produits contenant de l’acide fusidique par voie orale. La concentration des excipients est trop faible pour constituer un risque pour la sécurité. Par conséquent, un surdosage est peu probable.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : Antibiotiques, code ATC : S01AA13.
Antibiotiques de structure stéroïdienne, de la famille des fusidanines.
Mécanisme d’action
Antibiotique actif sur la synthèse des protéines.
Les concentrations critiques séparent les souches sensibles des souches de sensibilité intermédiaire et ces dernières, des résistantes :
S £ 2 mg/l et R > 16 mg/l.
La prévalence de la résistance acquise peut varier en fonction de la géographie et du temps pour certaines espèces. Il est donc utile de disposer d'informations sur la prévalence de la résistance locale, surtout pour le traitement d'infections sévères. Ces données ne peuvent apporter qu'une orientation sur les probabilités de la sensibilité d'une souche bactérienne à cet antibiotique.
Lorsque la variabilité la prévalence de la résistance en France est connue pour une espèce bactérienne, elle est indiquée dans le tableau ci-dessous :
|
Catégories |
Fréquence de résistance acquise en France (> 10%) (valeurs extrêmes) |
|
ESPÈCES SENSIBLES |
|
|
Aérobies à Gram positif |
|
|
Staphylococcus aureus |
|
|
Staphylococcus non-aureus |
5 - 20 % |
|
Anaérobies |
|
|
Clostridium difficile |
|
|
Clostridium perfringens |
|
|
Peptostreptococcus |
|
|
Propionibacterium acnes |
|
|
ESPÈCES MODÉRÉMENT SENSIBLES |
|
|
(in vitro de sensibilité intermédiaire) |
|
|
Aérobies à Gram positif |
|
|
Streptococcus |
|
|
ESPÈCES RÉSISTANTES |
|
|
Aérobies à Gram négatif |
|
|
Acinetobacter |
|
|
Entérobactéries |
|
|
Pseudomonas |
Ce spectre correspond à celui des formes systémiques de l'acide fusidique. Avec les présentations pharmaceutiques locales, les concentrations obtenues in situ sont très supérieures aux concentrations plasmatiques. Quelques incertitudes demeurent sur la cinétique des concentrations in situ, sur les conditions physico-chimiques locales qui peuvent modifier l'activité de l'antibiotique et sur la stabilité du produit in situ.
FUCITHALMIC possède une activité antibactérienne sur la plupart des germes rencontrés dans les infections oculaires externes.
5.2. Propriétés pharmacocinétiques
La forme gel de FUCITHALMIC assure un temps de contact prolongé avec l'œil d'au moins 12 heures.
Les études de pharmacocinétique ont montré, après instillation d'une goutte, que les concentrations d'acide fusidique sont thérapeutiques jusqu'à la 12ème heure.
En conséquence l'instillation deux fois par jour suffit pour obtenir des concentrations thérapeutiques d'acide fusidique.
L'acide fusidique pénètre bien dans l'humeur aqueuse.
5.3. Données de sécurité préclinique
3 ans.
6.4. Précautions particulières de conservation
A utiliser dans les 15 jours après ouverture du tube.
6.5. Nature et contenu de l'emballage extérieur
Tube (PE/Alu/PE) de 3 ou 5 g.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Pas d'exigences particulières.
Tout produit non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
Unit 17, Northwood House
Northwood Crescent
Northwood
Dublin 9 D09 V504
IRLANDE
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 331 913 3 7 ou 331 913-3 : 3 g en tube (PE/Alu/PE).
· 34009 331 111 4 4 ou 331 111-4 : 5 g en tube (PE/Alu/PE).
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I
ANSM - Mis à jour le : 13/02/2026
FUCITHALMIC 1 POUR CENT, gel ophtalmique
Acide fusidique
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que FUCITHALMIC 1 POUR CENT, gel ophtalmique et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser FUCITHALMIC 1 POUR CENT, gel ophtalmique ?
3. Comment utiliser FUCITHALMIC 1 POUR CENT, gel ophtalmique ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver FUCITHALMIC 1 POUR CENT, gel ophtalmique ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE FUCITHALMIC 1 POUR CENT, gel ophtalmique ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique - code ATC : Antibiotiques - code ATC : S01AA13
Ce médicament est destiné à l'œil et se présente sous forme de gel ophtalmique. Il contient un antibiotique, l'acide fusidique, qui agit en tuant certaines bactéries responsables d'infections.
Ce médicament est indiqué dans le traitement local de certaines infections de l'œil et des paupières : conjonctivites, kératites (inflammation de la cornée d'origine bactérienne), ulcères de la cornée, blépharites (inflammation des paupières d'origine bactérienne) et orgelets (infection d'une glande située dans la paupière se présentant habituellement comme une pustule centrée sur un cil).
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER FUCITHALMIC 1 POUR CENT, gel ophtalmique ?
N’utilisez jamais FUCITHALMIC 1 POUR CENT, gel ophtalmique :
· si vous êtes allergique à l’acide fusidique ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
· EN CAS DE DOUTE, IL EST INDISPENSABLE DE DEMANDER L'AVIS DE VOTRE MEDECIN OU DE VOTRE PHARMACIEN.
Avertissements et précautions
Adressez-vous à votre médecin ou votre pharmacien d’utiliser FUCITHALMIC 1 POUR CENT, gel ophtalmique.
· Ne pas porter de lentilles de contact durant l’utilisation de ce médicament,
· Ne pas utiliser FUCITHALMIC trop longtemps car les bactéries ne pourront plus être tuées par l'antibiotique,
· Utilisez toujours FUCITHALMIC tout le temps que votre médecin vous l’a demandé.
Autres médicaments et FUCITHALMIC 1 POUR CENT, gel ophtalmique
Informez votre médecin ou votre pharmacien si vous utilisez, avez récemment utilisé ou pourriez utiliser tout autre médicament, y compris les médicaments obtenus sans ordonnance.
FUCITHALMIC 1 POUR CENT, gel ophtalmique avec des aliments et des boissons
Sans objet.
Grossesse, allaitement et fertilité
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou votre pharmacien avant de prendre ce médicament.
Grossesse :
Aucun effet n'est attendu pendant la grossesse, car l'exposition systémique à Fucithalmic est insignifiante.
FUCITHALMIC peut être utilisé pendant la grossesse.
Allaitement :
Aucun effet sur l'allaitement du nouveau-né/nourrisson n'est attendu, puisque l'exposition systémique à l'acide fusidique de la femme allaitante est négligeable. FUCITHALMIC peut être utilisé pendant l'allaitement.
Fertilité :
Aucun effet sur les femmes en âge de procréer n’est attendu, car l'exposition systémique à FUCITHALMIC est négligeable.
Conduite de véhicules et utilisation de machines
FUCITHALMIC a peu ou pas d’effet sur la capacité à conduire et à utiliser des machines. Cependant, une vision trouble transitoire ou d'autres troubles visuels peuvent survenir et affecter l'aptitude à conduire ou à utiliser des machines. En cas de vision trouble après instillation, le patient doit attendre que sa vision redevienne normale avant de conduire un véhicule ou d'utiliser une machine.
FUCITHALMIC 1 POUR CENT, gel ophtalmique contient du chlorure de benzalkonium
Informations importantes concernant certains ingrédients :
Durant le traitement par FUCITHALMIC, les lentilles de contact ne doivent pas être portées.
FUCITHALMIC 1 POUR CENT, gel ophtalmique contient 10 mg de chlorure de benzalkonium pour 100 g de produit. Le chlorure de benzalkonium peut être absorbé par les lentilles de contact souples et changer leur couleur. Les lentilles de contact ne doivent pas être utilisées pendant le traitement par FUCITHALMIC, voir rubrique "Avertissements et précautions".
Le chlorure de benzalkonium peut également provoquer une irritation des yeux, surtout si vous souffrez du syndrome de l’œil sec ou de troubles de la cornée (couche transparente à l’avant de l’œil). En cas de sensation anormale, de picotements ou de douleur dans les yeux après avoir utilisé ce médicament, contactez votre médecin.
3. COMMENT UTILISER FUCITHALMIC 1 POUR CENT, gel ophtalmique ?
Ce médicament vous a été personnellement prescrit dans une situation précise :
· il ne peut être adapté à un autre cas ;
· ne pas le réutiliser sans avis médical ;
· ne pas le conseiller à une autre personne.
A titre indicatif, la posologie usuelle est la suivante :
1 goutte le matin et 1 goutte le soir, dans l'œil ou les yeux atteints.
Mode et voie d’administration
Se laver toujours les mains avant d'utiliser FUCITHALMIC.
Cette image vous montrera comment utiliser votre médicament. Il peut être utile de regarder dans un miroir.
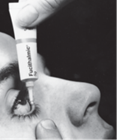
Ne retirez le bouchon du tube que lorsque vous êtes prêt à utiliser le médicament. Il est important que la pointe du tube ne touche pas vos yeux.
Inclinez la tête en arrière. Tirez doucement la paupière inférieure. Tenez le tube au-dessus de votre œil et levez les yeux, comme indiqué sur l'image.
Pressez une goutte dans votre paupière inférieure ou si les deux yeux sont infectés, mettez une goutte dans les deux yeux. La goutte apparaîtra comme une chute épaisse. Il deviendra plus liquide dans votre œil et vous devriez toujours voir clairement.
Après avoir utilisé votre médicament, une poudre blanche pourrait apparaître autour de votre œil. Cela peut se produire lorsque les gouttes se dessèchent. Ceci est tout à fait normal et ne vous en inquiétez pas. Vous pouvez l’essuyer avec du coton.
Utilisation chez les enfants et les adolescents
Lorsque le médicament est destiné à un enfant, vous pouvez mettre les gouttes lorsqu’qu'il est endormi ou allongé, si cela est plus facile.
Si vous avez utilisé plus de FUCITHALMIC 1 POUR CENT, gel ophtalmique que vous n’auriez dû
Si vous appliquez accidentellement trop de gouttes dans l'œil ou qu'une petite quantité de gouttes est accidentellement avalée, il est peu probable que cela vous fasse du mal. Si une plus grande quantité de gouttes est accidentellement avalée, ou si vous êtes inquiet, contactez votre médecin, votre pharmacien ou un service des urgences pour obtenir des conseils.
Si vous oubliez d’utiliser FUCITHALMIC 1 POUR CENT, gel ophtalmique
Si vous arrêtez d’utiliser FUCITHALMIC 1 POUR CENT, gel ophtalmique
Consultez toujours votre médecin si vous envisagez d’arrêter le traitement.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Effets secondaires importants à surveiller :
Avec l'administration de ce médicament, les effets suivants ont été observés :
Fréquent (peut toucher jusqu'à 1 personne sur 10)
· Vision floue temporaire,
· sensation de brûlure,
· picotements des yeux,
· démangeaisons,
· irritation/gêne oculaire.
Peu fréquent (peut toucher jusqu'à 1 personne sur 100)
· réactions allergiques telles que rash, gonflement du visage et urticaire,
· gonflement des paupières (œdème),
· larmoiement.
Rare (peut affecter jusqu'à 1 sur 1000 personnes)
· aggravation de la conjonctivite.
Effets indésirables supplémentaires chez les enfants et les adolescents
Les effets indésirables attendus sont similaires à ceux observés chez l’adulte.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: https://signalement.social-sante.gouv.fr/.
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER FUCITHALMIC 1 POUR CENT, gel ophtalmique ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’emballage. La date de péremption fait référence au dernier jour de ce mois.
Ne pas utiliser au-delà de 15 jours après première ouverture du tube.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient FUCITHALMIC 1 POUR CENT, gel ophtalmique
· La substance active est :
Acide fusidique................................................................................................................ 1,00 g
Pour 100 g.
· Les autres composants sont :
Chlorure de benzalkonium, édétate disodique, mannitol, carbomère (carbopol 974P), solution d'hydroxyde de sodium, eau pour préparations injectables.
Qu’est-ce que FUCITHALMIC 1 POUR CENT, gel ophtalmique et contenu de l’emballage extérieur
Ce médicament se présente sous forme de gel ophtalmique. Tube de 3 ou 5 g.
Titulaire de l’autorisation de mise sur le marché
Unit 17, Northwood House
Northwood Crescent
Northwood
Dublin 9 D09 V504
IRLANDE
Exploitant de l’autorisation de mise sur le marché
CENTRE SPECIALITES PHARMACEUTIQUES
76-78 AVENUE DU MIDI
63800 COURNON D’AUVERGNE
CASHEL ROAD
DUBLIN 12
IRLANDE
ou
cenexi hsc
2 rue louis pasteur
14200 herouville-saint-clair
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
Conseil d’éducation sanitaire :
QUE SAVOIR SUR LES ANTIBIOTIQUES ?
Les antibiotiques sont efficaces pour combattre les infections dues aux bactéries. Ils ne sont pas efficaces contre les infections dues aux virus.
Aussi, votre médecin a choisi de vous prescrire cet antibiotique parce qu’il convient précisément à votre cas et à votre maladie actuelle.
Les bactéries ont la capacité de survivre ou de se reproduire malgré l’action d’un antibiotique. Ce phénomène est appelé résistance : il rend certains traitements antibiotiques inactifs.
La résistance s’accroît par l’usage abusif ou inapproprié des antibiotiques.
Vous risquez de favoriser l’apparition de bactéries résistantes et donc de retarder votre guérison ou même de rendre inactif ce médicament, si vous ne respectez pas :
· la dose à prendre,
· les moments de prise,
· et la durée de traitement.
En conséquence, pour préserver l’efficacité de ce médicament :
1- N’utilisez un antibiotique que lorsque votre médecin vous l’a prescrit.
2- Respectez strictement votre ordonnance.
3- Ne réutilisez pas un antibiotique sans prescription médicale même si vous pensez combattre une maladie apparemment semblable.
4- Ne donnez jamais votre antibiotique à une autre personne, il n’est peut-être pas adapté à sa maladie.
5- Une fois votre traitement terminé, rapportez à votre pharmacien toutes les boîtes entamées pour une destruction correcte et appropriée de ce médicament.