
ANSM - Mis à jour le : 16/06/2025
NEFOPAM ARROW 20 mg/2 mL, solution injectable
Chlorhydrate de néfopam
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin, votre pharmacien ou votre infirmier/ère.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que NEFOPAM ARROW 20 mg/2 mL, solution injectable et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d’utiliser NEFOPAM ARROW 20 mg/2 mL, solution injectable ?
3. Comment utiliser NEFOPAM ARROW 20 mg/2 mL, solution injectable ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver NEFOPAM ARROW 20 mg/2 mL, solution injectable ?
6. Contenu de l’emballage et autres informations.

Classe pharmacothérapeutique : autres analgésiques et antipyrétiques - code ATC : N02BG06.
Traitement symptomatique de la douleur aiguë, notamment de la douleur post-opératoire.

N’utilisez jamais NEFOPAM ARROW 20 mg/2 mL, solution injectable :
· si vous êtes allergique au chlorhydrate de néfopam ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6 ;
· dans les cas suivants :
o glaucome à angle fermé (augmentation de la pression à l'intérieur de l'œil) ;
o difficultés pour uriner d'origine prostatique ;
o convulsions ou antécédents de convulsion ;
o enfants de moins de 15 ans.
Avertissements et précautions
Adressez-vous à votre médecin, pharmacien ou votre infirmier/ère avant d’utiliser NEFOPAM ARROW 20 mg/2 mL, solution injectable.
Il existe un risque de dépendance avec NEFOPAM ARROW.
En cas d’utilisation conjointe d’un médicament dérivé de la morphine, l’arrêt brutal de ce médicament dérivé de la morphine peut provoquer un syndrome de sevrage, NEFOPAM ARROW n’étant pas un médicament dérivé de la morphine.
Utiliser ce médicament avec précaution :
· en cas d’insuffisance hépatique ;
· en cas d’insuffisance rénale ;
· chez les patients présentant une pathologie cardiovasculaire en raison de l’effet tachycardisant de ce médicament (augmentation de la fréquence cardiaque) ;
· en raison de ses effets anticholinergiques, le traitement par NEFOPAM ARROW est déconseillé chez le sujet âgé.
Autres médicaments et NEFOPAM ARROW 20 mg/2 mL, solution injectable
Informez votre médecin ou pharmacien si vous utilisez, avez récemment utilisé ou pourriez utiliser tout autre médicament.
NEFOPAM ARROW peut interagir avec d’autres médicaments.
NEFOPAM ARROW 20 mg/2 mL, solution injectable avec des aliments, boissons et de l’alcool
Sans objet.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
L’effet de ce médicament pendant la grossesse ou l’allaitement étant mal connu, l’utilisation de ce médicament est déconseillée en cas de grossesse et d’allaitement.
Conduite de véhicules et utilisation de machines
En raison d’un risque éventuel de somnolence, les conducteurs et utilisateurs de machine devront être vigilants.
NEFOPAM ARROW 20 mg/2 mL, solution injectable contient du sodium
Ce médicament contient moins de 1 mmol (23 mg) de sodium par ampoule, c’est-à-dire qu’il est essentiellement « sans sodium ».
Ce médicament contient 31,38 mg de sodium (composant principal du sel de cuisine/table) par dose maximale de 6 ampoules. Cela équivaut à 1,57% de l’apport alimentaire quotidien maximal recommandé de sodium pour un adulte.

Veillez à toujours utilisez ce médicament en suivant exactement les indications de votre médecin. Vérifiez auprès de votre médecin ou pharmacien en cas de doute.
Posologie
La posologie est strictement individuelle.
Elle est généralement de 1 ampoule (voie IV ou voie IM) par prise, à renouveler jusqu'à 6 ampoules par jour si nécessaire.
Mode et voie d'administration
NEFOPAM ARROW peut être administré par voie intramusculaire (IM) profonde ou en perfusion intraveineuse (IV) lente (de plus de 15 minutes).
Par voie intraveineuse, il est nécessaire d'être allongé pour éviter la survenue d'effets indésirables tels que nausées, vertiges et sueurs.
Comment ouvrir les ampoules de NEFOPAM ARROW ?
![]()
Les ampoules de NEFOPAM ARROW sont des ampoules de type O.P.C (One Point Cut).
La tête de l’ampoule se compose d’un point coloré bleu et d’un anneau coloré bleu.
La partie rétrécie entre la tête et le corps de l’ampoule comporte une zone de prédécoupe, quelques millimètres en-dessous du point coloré, permettant son ouverture.
· Tapotez la tête de l’ampoule avec votre doigt si du liquide est présent pour le faire descendre.
· Tenez l’ampoule vers le haut, inclinée à 45 degrés, le point coloré dirigé vers l’extérieur.
· Mettez une compresse au niveau de la tête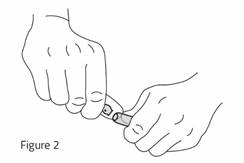 de l’ampoule.
de l’ampoule.
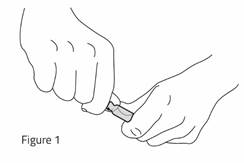
· Positionnez le centre de votre pouce au niveau de la partie rétrécie et votre index replié sur la tête de l’ampoule (au niveau du point coloré). Placez l’autre main pour que les deux pouces soient collés en tenant fermement le bas de l’ampoule (voir la Figure 1).
· Exercez une pression ferme avec le pouce au niveau de la partie rétrécie (effet de levier) tout en résistant avec l’index replié (point d’appui) pour détacher la tête de l’ampoule (voir la Figure 2).
· Si l'ampoule ne se casse pas correctement (présence de particules de verre), ne l’utilisez pas. Une autre ampoule doit être utilisée.
Fréquence d'administration
Les injections pourront être renouvelées toutes les 6 heures (voie IM) ou toutes les 4 heures (voie IV).
Durée du traitement
La durée du traitement prescrit par votre médecin doit être scrupuleusement respectée.
Si vous avez utilisé plus de de NEFOPAM ARROW 20 mg/2 mL, solution injectable que vous n'auriez dû
Sans objet.
Si vous oubliez d’utiliser NEFOPAM ARROW 20 mg/2 mL, solution injectable
Lorsqu'une injection a été omise, il n'est pas nécessaire d'augmenter d'autant la dose suivante.
Si vous arrêtez d’utiliser NEFOPAM ARROW 20 mg/2 mL, solution injectable
L'arrêt du traitement n'entraîne pas de syndrome de sevrage (état de privation ou de manque ressenti après l'arrêt de certains médicaments avec réapparition ou aggravation des troubles).
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin, à votre pharmacien ou à votre infirmier/ère.

Les effets indésirables les plus fréquemment rapportés sont : vertiges, nausées avec ou sans vomissements, somnolence, sueurs.
Il a été également observé des troubles tels que bouche sèche, accélération du rythme cardiaque, palpitations, rétention d'urine.
Plus rarement ont été rapportés excitabilité, irritabilité, malaise, hallucination, abus, pharmacodépendance, convulsion, réactions allergiques (éruption cutanée, œdème de Quincke, choc anaphylactique…).
D’autres effets indésirables de fréquence indéterminée (ne peut être estimée sur la base de données disponibles) ont également été observés : coma, confusion, douleur au site d’injection.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou à votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.

Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’emballage ou l’ampoule après EXP. La date de péremption fait référence au dernier jour de ce mois.
Ce médicament ne nécessite pas de précautions particulières de conservation.
Après ouverture/reconstitution/dilution : le produit doit être utilisé immédiatement.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.

Ce que contient NEFOPAM ARROW 20 mg/2 mL, solution injectable 
· La substance active est :
Chlorhydrate de néfopam....................................................................................................... 20 mg
Pour une ampoule de 2 mL
· Les autres composants sont : phosphate monosodique dihydraté, phosphate disodique dodécahydraté, eau pour préparations injectables.
Qu’est-ce que NEFOPAM ARROW 20 mg/2 mL, solution injectable et contenu de l’emballage extérieur 
Il est disponible en boite de 5 et 20 ampoules (verre transparent) de 2 mL.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché 
VAULT 14, LEVEL 2
VALLETTA WATERFRONT
FLORIANA, FRN 1914
MALTE
Exploitant de l’autorisation de mise sur le marché 
ARROW GENERIQUES
26 AVENUE TONY GARNIER
69007 LYON
LYONER STRAΒE 14
60528 FRANKFURT
ALLEMAGNE
ou
ESSETI FARMACEUTICI S.R.L
VIA CAMPOBELLO 15
POMEZIA, 00071
ITALIE
ou
PHARMADOX HEALTHCARE LTD
KW20A KORDIN INDUSTRIAL PARK
PAOLA, PLA 3000
MALTE
ou
ARROW GENERIQUES
26 AVENUE TONY GARNIER
69007 LYON
Noms du médicament dans les Etats membres de l'Espace Economique Européen 
Sans objet.
La dernière date à laquelle cette notice a été révisée est : 
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
|
| Plan du site | Accessibilité | Contact | Téléchargement | Declaration de confidentialité | Service-Public.fr | Legifrance | Gouvernement.fr |