Dernière mise à jour le 30/06/2025
LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion
Indications thérapeutiques
Classe pharmacothérapeutique : Anesthésiques locaux, amide, code ATC N01B B10.
LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion appartient à une famille de médicaments appelée anesthésiques locaux. Ce type de médicament est utilisé pour anesthésier certaines parties du corps ou pour soulager la douleur.
Chez les adultes et les adolescents (âgés de 12 ans et plus) :
LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion s'utilise en tant qu'anesthésique local pour anesthésier certaines parties du corps avant une chirurgie lourde (par exemple, pour une anesthésie péridurale en vue d'une césarienne) ou une chirurgie légère.
Il est également utilisé pour soulager la douleur :
· après une chirurgie lourde,
· pendant l'accouchement.
Enfants (âgés de moins de 12 ans)
LEVOBUPIVACAINE KABI peut également être utilisé chez l’enfant pour anesthésier certaines parties
du corps avant une chirurgie et pour soulager la douleur après une chirurgie légère telle qu’une cure
de hernie inguinale.
LEVOBUPIVACAINE KABI n’a pas été étudié chez l’enfant de moins de 6 mois.
Présentations
> 5 ampoule(s) polypropylène de 10 ml
Code CIP : 586 934-6 ou 34009 586 934 6 5
Déclaration de commercialisation : 19/11/2015
Cette présentation n'est pas agréée aux collectivités
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 01/07/2015 | Inscription (CT) | Le service médical rendu par LEVOBUPIVACAINE KABI est important dans les indications de son AMM. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 01/07/2015 | Inscription (CT) | Ces spécialités sont des génériques qui n’apportent pas d’amélioration du service médical rendu (ASMR V) par rapport au princeps CHIROCAINE. |
Autres informations
- Titulaire de l'autorisation : FRESENIUS KABI FRANCE SA
- Conditions de prescription et de délivrance :
- liste I
- réservé à l'usage HOSPITALIER
- Statut de l'autorisation : Valide
- Type de procédure : Procédure décentralisée
- Code CIS : 6 863 739 1
ANSM - Mis à jour le : 26/04/2024
LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion.
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
1 ml de solution contient 2,5 mg de lévobupivacaïne sous forme de chlorhydrate de lévobupivacaïne.
Une ampoule de 10 ml contient 25 mg de lévobupivacaïne sous forme de chlorhydrate de lévobupivacaïne.
Excipient(s) à effet notoire :
Ce médicament contient 3,6 mg de sodium par ml ce qui équivaut à 0,18 % de l’apport alimentaire quotidien maximal recommandé par l’OMS de 2 g de sodium par adulte.
Pour la liste complète des excipients, voir rubrique 6.1.
Solution injectable/pour perfusion.
Solution incolore, limpide.
pH 4,0 à 6,0.
Osmolarité : 271 – 372 mOsmol/L.
4.1. Indications thérapeutiques
Adultes et adolescent (≥ 12 ans)
· Anesthésie chirurgicale :
o Majeure : péridurale (y compris césarienne), intrathécale, périneurale (bloc nerveux périphérique).
o Mineure : infiltration locale.
· Traitement de la douleur
o Perfusion péridurale continue ou administration par bolus unique ou répété pour le traitement de la douleur, en particulier douleurs post-opératoires ou de l'accouchement.
Enfants (< 12 ans)
Analgésie par infiltration (blocs ilioinguinal/iliohypogastrique).
Aucune donnée n’est disponible pour la population pédiatrique dont l’âge est inférieur à 6 mois.
4.2. Posologie et mode d'administration
La lévobupivacaïne devra être administrée uniquement par, ou sous la responsabilité d'un médecin ayant l'expérience nécessaire.
Le tableau ci-dessous donne, à titre indicatif, les posologies administrées pour les blocs les plus couramment utilisés. Pour l'analgésie (administration par voie péridurale pour le traitement de la douleur), il est recommandé d'utiliser les concentrations et les posologies les plus faibles. Pour une anesthésie plus profonde ou prolongée, associée à un bloc moteur important (anesthésie péridurale ou bloc péribulbaire), les concentrations plus élevées peuvent être utilisées. Une aspiration soigneuse avant et pendant l'injection est recommandée dans le but de prévenir toute injection intravasculaire.
Les données de sécurité d’un traitement par lévobupivacaïne pendant une période excédant 24 heures sont limitées. Afin de minimiser le risque de complications neurologiques sévères, il est recommandé de surveiller étroitement le patient et la durée d’administration de lévobupivacaïne (voir rubrique 4.4).
Dose maximale
La dose maximale dépend de la taille et de l'état clinique du patient ainsi que de la concentration de l'anesthésique et de la zone et voie d'administration. Des variations interindividuelles du délai d'installation et de la durée du bloc peuvent exister. L'expérience acquise au cours des études cliniques montre que le délai d'installation d'un bloc sensitif adapté à la chirurgie est de 10 à 15 minutes après administration péridurale et le temps de régression de 6 à 9 heures.
La dose maximale recommandée en injection unique est de 150 mg. Pour une intervention longue, lorsqu'un bloc moteur et sensitif prolongé est nécessaire, des doses supplémentaires peuvent être requises. La dose maximale recommandée sur une période de 24 h est de 400 mg. Pour le traitement des douleurs post-opératoires, la dose ne doit pas dépasser 18,75 mg/heure.
Obstétrique
Dans les césariennes, la concentration utilisée ne doit pas dépasser 5 mg/ml (voir rubrique 4.3). La dose maximale recommandée est de 150 mg.
Pour l'analgésie obstétricale par perfusion péridurale, la dose ne doit pas dépasser 12,5 mg/heure.
Population pédiatrique
Chez l'enfant (<12 ans), la dose maximale recommandée pour l'analgésie par infiltration (blocs ilioinguinal/iliohypogastrique) est de 1,25 mg/kg/côté.
La dose maximale doit être ajustée en fonction de la taille, du poids et de l’état clinique du patient/de l’enfant.
L'efficacité et la tolérance de la lévobupivacaïne chez l'enfant n'ont pas été établies dans les autres indications.
Populations particulières
Chez les patients fragilisés, âgés ou présentant une pathologie aiguë, les doses de lévobupivacaïne devront être réduites en fonction de leur état clinique.
Dans la prise en charge des douleurs post-opératoires, les doses administrées au cours de la chirurgie doivent être prises en compte.
Il n'y a pas de données pertinentes chez le patient insuffisant hépatique (voir rubriques 4.4 et 5.2).
Tableau de doses
Adultes et adolescents (≥ 12 ans)
|
Concentration (mg/ml)1 |
Dose |
Bloc Moteur |
||
|
Anesthésie chirurgicale Bolus péridural (lent)2 pour chirurgie Adulte |
5,0 – 7,5 |
10-20 ml (50-150 mg) |
Modéré à complet |
|
|
Injection péridurale lente3 pour césariennes |
5,0 |
15-30 ml (75-150 mg) |
Modéré à complet |
|
|
Intrathécale |
5,0 |
3 ml (15 mg) |
Modéré à complet |
|
|
Bloc nerveux périphérique |
2,5-5,0 |
1-40 ml (2,5-150 mg max.) |
Modéré à complet |
|
|
Infiltration locale Adulte |
2,5 |
1-60 ml (2,5-150 mg max.) |
Sans objet |
|
|
Traitement de la douleur4 Analgésie pendant l’accouchement (bolus péridural5) |
2,5 |
6-10 ml (15-25 mg) |
Faible à modéré |
|
|
Analgésie pendant l’accouchement (perfusion péridurale) |
1,256 |
4-10 ml/h (5-12,5 mg/h) |
Faible à modéré |
|
|
Douleur post-opératoire |
1,256 2,5 |
10-15 ml/h (12,5-18,75 mg/h) 5-7,5 ml/h (12,5-18,75 mg/h) |
Faible à modéré |
|
1 La lévobupivacaïne est disponible en solutions injectables à 2,5 et 5,0 mg/ml.
2 Administré en 5 minutes (voir aussi texte).
3 Administré en 15 à 20 minutes.
4 Dans les cas où la lévobupivacaïne est associée à d'autres produits tels que les opiacés pour le traitement de la douleur, la dose de lévobupivacaïne devra être réduite et il sera préférable d'utiliser une concentration faible (par exemple : 1,25 mg/ml).
5 L'intervalle minimum recommandé entre les injections est de 15 minutes.
6 Pour les informations sur la dilution, voir rubrique 6.6.
Population pédiatrique (< 12 ans)
|
|
Concentration (mg/ml)1 |
Dose |
Bloc moteur |
|
Bloc ilioinguinal/ Bloc iliohypogastrique chez les enfants < 12 ans2 |
2,5
5.0 |
0,5 ml/kg/côté (1,25 mg/Kg/côté) 0,25 ml/kg/côté (1,25 mg/kg/côté) |
Sans objet
|
1 La lévobupivacaïne est disponible en solutions injectables à 2,5 et 5,0 mg/ml.
2 Aucune donnée disponible pour la population pédiatrique avant 6 mois.
Mode d’administration
LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion est indiqué pour l’utilisation péridurale, intrathécale, périneurale (blocs nerveux périphériques) et pour l’infiltration (se reporter au tableau des doses ci-dessus).
L'aspiration devra être répétée avant et pendant l'administration de la dose principale, qui devra être injectée lentement ou à doses croissantes, à une vitesse de 7,5 à 30 mg/min, tout en surveillant étroitement les fonctions vitales du patient et en maintenant le contact verbal avec lui.
Si des symptômes de toxicité apparaissent, l'injection devra être arrêtée immédiatement.
Pour les instructions concernant la dilution du médicament avant administration, voir la rubrique 6.6.
Les contre-indications générales liées à l'anesthésie locorégionale, quel que soit l'anesthésique local utilisé, doivent être prises en compte.
Les solutions de lévobupivacaïne sont contre-indiquées pour l'anesthésie locorégionale intraveineuse (Bloc de Bier).
Les solutions de lévobupivacaïne sont contre-indiquées chez les patients ayant une hypotension sévère (choc cardiogénique ou hypovolémique).
Les solutions de lévobupivacaïne sont contre-indiquées pour l'utilisation en bloc paracervical en obstétrique (voir rubrique 4.6).
4.4. Mises en garde spéciales et précautions d'emploi
Toutes les techniques d’anesthésie locorégionale avec la lévobupivacaïne doivent être réalisées dans des locaux bien équipés, par un personnel formé et expérimenté dans les techniques d’anesthésie locorégionale, capable de diagnostiquer et de traiter les éventuels effets indésirables pouvant survenir.
La lévobupivacaïne peut provoquer des réactions allergiques aiguës, des effets cardiovasculaires et des lésions neurologiques (voir rubrique 4.8).
La lévobupivacaïne doit être utilisée avec prudence lors d'une anesthésie locorégionale chez les patients présentant une altération de la fonction cardiovasculaire telle qu’une arythmie cardiaque sévère (voir rubrique 4.3).
Chez les patients ayant une maladie du système nerveux central, l’introduction d’anesthésiques locaux par voie péridurale ou intrathécale dans le système nerveux central peut potentiellement exacerber cette maladie. Par conséquent, une évaluation clinique doit être réalisée lorsqu’une anesthésie péridurale ou intrathécale est envisagée chez ce type de patients.
Anesthésie péridurale
Lors de l’administration péridurale de lévobupivacaïne, les solutions concentrées (0,5 % - 0,75%) doivent être administrées à doses croissantes de 3 à 5 ml avec des intervalles entre les doses suffisants pour permettre de détecter des signes de toxicité liés à une injection intravasculaire ou intrathécale accidentelle. Des cas sévères de bradycardie, d’hypotension et de dépression respiratoire avec arrêt cardiaque (dont certains ont été fatals) ont été rapportés avec des anesthésiques locaux, incluant la lévobupivacaïne. Lorsqu’une dose importante doit être injectée, par exemple lors d’un bloc péridural, il est recommandé d’administrer une dose test de 3 à 5 ml avec de la lidocaïne adrénalinée. Une injection intravasculaire accidentelle peut être identifiée par une accélération transitoire de la fréquence cardiaque et une injection intrathécale accidentelle par des signes de rachianesthésie.
Des aspirations à l’aide d’une seringue doivent être réalisées avant et pendant chaque injection supplémentaire dans les techniques par cathéter en continu (intermittent). Une injection intravasculaire est toujours possible même si les aspirations de sang sont négatives. Au cours de l’anesthésie péridurale, il est recommandé d’administrer une dose test initiale et de surveiller les effets avant d’administrer la dose thérapeutique.
L'anesthésie péridurale peut provoquer une hypotension et une bradycardie quel que soit l'anesthésique local utilisé. Tous les patients doivent disposer d'une voie d’abord intraveineuse. Un équipement de réanimation ainsi qu'un personnel qualifié doivent être disponibles, de même que des solutés de remplissage, des vasopresseurs, des anesthésiques ayant des propriétés anticonvulsivantes, des myorelaxants et de l’atropine (voir rubrique 4.9).
Analgésie péridurale
Il a été observé après commercialisation des cas de syndrome de la queue de cheval et des événements indiquant une neurotoxicité transitoire associés à l’administration de lévobupivacaïne pendant 24 heures ou plus lors d’une analgésie péridurale (voir rubrique 4.8). Ces effets ont été plus sévères et ont conduit dans certains cas à des séquelles permanentes lorsque la lévobupivacaïne était administrée pendant plus de 24 heures. Par conséquent, la perfusion de lévobupivacaïne sur une période dépassant 24 heures doit être soigneusement évaluée et ne doit être utilisée que si le bénéfice pour le patient est clairement supérieur au risque.
Il est primordial d’effectuer une aspiration du sang ou du liquide céphalo-rachidien (le cas échéant) avant l’injection de tout anesthésique local, qu’il s’agisse de la dose initiale ou des doses suivantes, afin d’éviter une injection intravasculaire ou intrathécale. Cependant, une aspiration négative n’écarte pas la possibilité d’une injection intravasculaire ou intrathécale. La lévobupivacaïne doit être utilisée avec prudence chez les patients recevant d’autres anesthésiques locaux ou des médicaments apparentés sur le plan de la structure aux anesthésiques locaux à liaison amide car les effets toxiques de ces médicaments sont additifs.
Principaux blocs nerveux régionaux
Le patient devra disposer d’une voie d’abord intraveineuse fonctionnelle. Il est recommandé d’utiliser la plus petite dose d’anesthésique local qui produit une anesthésie efficace afin d’éviter des concentrations plasmatiques élevées et des effets indésirables graves. L’injection rapide de grands volumes d’anesthésique local devra être évitée et l’utilisation de doses fractionnées (croissantes) est recommandée lorsque cela est réalisable.
Injection au niveau de la tête et du cou
L’injection de petites doses d’anesthésiques locaux injectés au niveau de la tête et du cou et bloc des ganglions stellaires, peut produire des réactions indésirables semblables aux signes de toxicité systémique observés avec des injections intravasculaires accidentelles de doses plus importantes. Les techniques d’injection nécessitent le plus grand soin. Les réactions peuvent être dues à une injection intraartérielle de l’anesthésique local avec un flux rétrograde vers la circulation cérébrale. Elles peuvent être aussi dues à une ponction de la gaine du nerf optique lors du bloc rétrobulbaire avec diffusion de l’anesthésique local le long de l’espace sous-dural vers l’encéphale. Ces blocs nécessitent un monitorage des fonctions circulatoires et respiratoires et une surveillance constante des patients. Un équipement de réanimation et un personnel compétent pour la prise en charge des effets indésirables doivent être immédiatement disponibles.
Utilisation en chirurgie ophtalmique
Les médecins qui réalisent des blocs rétrobulbaires doivent être informés que des arrêts respiratoires ont été observés suite à une injection d’anesthésique local. Avant tout bloc rétrobulbaire, comme pour toute technique locorégionale, il faut s’assurer de la disponibilité immédiate de l’équipement, des médicaments et du personnel compétent pour la prise en charge d’une dépression ou d’un arrêt respiratoire, de convulsions ou d’une dépression ou stimulation cardiaque. Comme pour toutes les autres techniques d’anesthésie, les patients doivent être sous surveillance constante après un bloc ophtalmique afin de détecter les signes de ces réactions indésirables.
Chondrolyse
Il a été rapporté après commercialisation des cas de chondrolyse chez les patients recevant une perfusion post-opératoire intra-articulaire continue d'anesthésiques locaux, y compris la ropivacaïne. La majorité des cas de chondrolyse rapportés ont concerné l’articulation de l'épaule. Du fait de nombreux facteurs et des incohérances dans la littérature scientifique concernant le mécanisme d’action, la causalité n’a pas été établie. La perfusion intra-articulaire continue n’est pas une indication pour la lévobupivacaine.
Populations particulières
Patients fragilisés, âgés ou présentant une pathologie aiguë : la lévobupivacaïne doit être utilisée avec prudence (voir rubrique 4.2).
Insuffisance hépatique : la lévobupivacaïne étant métabolisée par le foie, elle doit être utilisée avec prudence chez les patients souffrant de troubles hépatiques ou d'une réduction du débit sanguin hépatique comme chez les patients alcooliques ou cirrhotiques (voir rubrique 5.2).
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
La lévobupivacaïne doit être utilisée avec prudence chez les patients recevant des antiarythmiques ayant une activité anesthésique locale (par exemple : méxilétine ou antiarythmiques de classe III), car leurs effets toxiques peuvent être additifs.
Il n'a pas été réalisé d'études cliniques évaluant l'association de lévobupivacaïne et d'adrénaline.
4.6. Fertilité, grossesse et allaitement
Grossesse
Les solutions de lévobupivacaïne sont contre-indiquées pour l'utilisation en bloc paracervical en obstétrique. En se basant sur l'expérience acquise avec la bupivacaïne, il est possible qu'une bradycardie fœtale survienne après un bloc paracervical (voir rubrique 4.3).
Pour la lévobupivacaïne, il n'y a pas de données cliniques sur les grossesses exposées au premier trimestre. Les études conduites chez l'animal, au cours desquelles l'exposition systémique était de même ordre que celle obtenue en clinique, n'ont pas mis en évidence d'effet tératogène mais ont révélé une toxicité embryo-fœtale (voir rubrique 5.3). Les conséquences dans l'espèce humaine ne sont pas connues. Par conséquent, la lévobupivacaïne ne doit pas être utilisée en début de grossesse sauf en cas de nécessité absolue.
Toutefois, à ce jour, les données cliniques relatives à l'utilisation de la bupivacaïne en chirurgie obstétricale (au terme de la grossesse ou pour l'accouchement) sont nombreuses et n'ont pas mis en évidence de fœtotoxicité.
Il n'y a pas de données disponibles sur l'excrétion de la lévobupivacaïne et de ses métabolites dans le lait maternel humain. Comme pour la bupivacaïne, il est probable que la lévobupivacaïne soit faiblement excrétée dans le lait maternel. Par conséquent, l'allaitement est possible après une anesthésie locale.
Fertilité
Les données permettant d’évaluer l’impact de la lévobupivacaine sur la fertilité sont absentes ou très limitées.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Les effets indésirables observés avec la lévobupivacaïne sont comparables à ceux connus pour la classe de médicaments à laquelle il appartient.
Les effets indésirables les plus fréquemment rapportés sont : hypotension, nausées, anémie, vomissements, étourdissements, céphalées, fièvre, douleur liée à la procédure, douleur dorsale et détresse fœtale en utilisation obstétrique (voir tableau ci-dessous).
Les effets indésirables rapportés spontanément ou observés au cours d’essais cliniques sont présentés dans le tableau ci-dessous. Au sein de chaque classe de système-organe, les effets indésirables sont présentés par fréquence, selon la convention suivante : très fréquents (≥ 1/10), fréquents (≥ 1/100, < 1/10), peu fréquents (≥ 1/1000, < 1/100), rare (≥ 1/10000 à < 1/1000), fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
|
Classe de système-organe |
Fréquence |
Effet indésirable |
|
Affections hématologiques et du système lymphatique |
Très fréquent |
Anémie |
|
Affections du système immunitaire |
Fréquence indéterminée |
Réactions allergiques (dans des cas graves choc anaphylactique) Hypersensibilité |
|
Affections du système nerveux |
Fréquent |
Etourdissements Céphalées |
|
Fréquence indéterminée |
Convulsions Perte de conscience Somnolence Syncope Paresthésie Paraplégie Paralysie1 |
|
|
Affections oculaires |
Fréquence indéterminée |
Vision trouble Ptose2 Myosis2 Enophtalmie2 |
|
Affections cardiaques |
Fréquence indéterminée |
Bloc auriculo-venticulaire Arrêt cardiaque Tachyarythmie ventriculaire Tachychardie Bradycardie |
|
Affections vasculaires |
Très fréquent |
Hypotension |
|
Fréquence indéterminée |
Vasodilation2 |
|
|
Affections respiratoires, thoraciques et médiastinales |
Fréquence indéterminée |
Arrêt respiratoire Œdème laryngé Apnée Eternuements |
|
Affections gastro-intestinales |
Très fréquent |
Nausées |
|
Fréquent |
Vomissements |
|
|
Fréquence indéterminée |
Hypoesthésie orale Perte de contrôle sphinctérien1 |
|
|
Affections de la peau et du tissu sous-cutané |
Fréquence indéterminée |
Angiœdeme Urticaire Prurit Hyperhidrose Anhidrose2 Erythème |
|
Affections musculo-squelettiques et systémiques |
Fréquent |
Douleurs dorsales |
|
Fréquence indéterminée |
Contractions musculaires Faiblesse musculaire |
|
|
Affections du rein et des voies urinaires |
Fréquence indéterminée |
Dysfonctionnement vésical1 |
|
Affections gravidiques puerpérales et périnatales |
Fréquent |
Détresse fœtale |
|
Affections des organes de reproduction et du sein |
Fréquence indéterminée |
Priapisme1 |
|
Troubles généraux et anomalies au site d’administration |
Fréquent |
Fièvre |
|
Investigations |
Fréquence indéterminée |
Diminution du débit cardiaque Modifications de l'ECG |
|
Lésions, intoxications et complications liées aux procédures |
Fréquent |
Douleur liée à la procédure |
1 Peut être un signe ou symptôme d’un syndrome de la queue de cheval (voir ci-dessous texte complémentaire de la rubrique 4.8).
2 Peut être un signe ou symptôme d’un syndrome de Horner transitoire (voir ci-dessous texte complémentaire de la rubrique 4.8).
Les effets indésirables sont rares avec les anesthésiques locaux à liaison amide, mais ils peuvent survenir suite à un surdosage ou à une injection intravasculaire accidentelle et peuvent être graves.
Une sensibilité croisée au sein du groupe des anesthésiques locaux à liaison amide a été rapportée (voir rubrique 4.3).
Une injection intrathécale accidentelle d’anesthésiques locaux peut entraîner une anesthésie rachidienne haute.
Les effets cardiovasculaires sont liés à la dépression de la conduction cardiaque, à une réduction de l'excitabilité et de la contractibilité du myocarde. Généralement, ces symptômes sont précédés par des signes majeurs de toxicité neurologique (c’est-à-dire des convulsions) mais, dans de rares cas, l'arrêt cardiaque peut se produire sans prodromes neurologiques.
Les lésions neurologiques sont rares mais bien connues comme conséquence de l'anesthésie loco-régionale, particulièrement l’anesthésie péridurale et rachidienne. Elles peuvent être dues à une lésion directe de la moelle épinière ou des nerfs rachidiens, au syndrome de l'artère spinale antérieure, à l'injection d'une substance irritante ou d'une solution non stérile. Ces lésions sont rarement permanentes.
Des cas de faiblesse prolongée ou de troubles sensoriels, dont certains ont pu être permanents, ont été rapportés en association avec l’administration de lévobupivacaïne. Il est difficile de déterminer si les effets à long terme ont été dus à une toxicité du médicament ou à un traumatisme non détecté pendant l’intervention chirurgicale ou à d’autres facteurs mécaniques, tels que l’insertion et la manipulation d’un cathéter.
Des cas de syndrome de la queue de cheval ou de signes ou symptômes de lésion potentielle de la base de la moelle épinière ou des racines des nerfs rachidiens (incluant paresthésie, faiblesse ou paralysie des membres inférieurs, incontinence fécale et/ou urinaire et priapisme) associés à l’administration de lévobupicavaïne ont été rapportés. Ces effets ont été plus graves et dans certains cas non réversibles lorsque la lévobupivacaïne a été administrée pendant plus de 24 heures (voir rubrique 4.4).Cependant, il n’est pas possible de déterminer si ces événements sont dus à un effet de la lévobupicavaïne, à un traumatisme mécanique de la moelle épinière ou des racines nerveuses rachidiennes, ou à une collection de sang à la base du rachis.
Des cas de syndrome de Horner transitoire (ptose, myosis, énophtalmie, sudation et/ou vasodilatation unilatérale) ont été rapportés en association avec l’utilisation d’anesthésiques locorégionaux incluant la lévobupicavaïne. Cet événement se résout après l’arrêt du traitement.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/
L'injection intravasculaire accidentelle d'anesthésiques locaux peut donner lieu à des réactions toxiques immédiates. En cas de surdosage, le pic de concentration plasmatique peut n'être atteint qu'après un délai de 2 heures suivant l'administration, en fonction du site d'injection, les signes de toxicité pouvant donc apparaître de façon retardée. Les effets du médicament peuvent être prolongés.
Les effets indésirables systémiques liés à un surdosage ou à une injection intravasculaire accidentelle décrits avec les anesthésiques locaux de longue durée d'action, affectent à la fois le système cardiovasculaire et le SNC.
Effets sur le SNC
Les convulsions seront traitées immédiatement par administration IV de thiopental ou de diazépam à la dose requise. Le thiopental et le diazépam possèdent également un effet dépresseur sur le système nerveux central ainsi que sur les fonctions respiratoire et cardiaque. Leur utilisation peut donc entraîner une apnée. Les agents provoquant un bloc neuro-musculaire ne pourront être utilisés que si le clinicien est capable d'effectuer une intubation trachéale et de prendre en charge un patient totalement paralysé.
Si elles ne sont pas traitées rapidement, les convulsions, l'hypoxie et l'hypercapnie qui s'en suivent ainsi que la dépression myocardique liée aux effets cardiaques de l'anesthésique local, peuvent provoquer une arythmie, une fibrillation ventriculaire ou un arrêt cardiaque.
Effets cardiovasculaires
L'hypotension peut être évitée ou limitée par des mesures préventives telles que le remplissage vasculaire et/ou l’utilisation de vasopresseurs. Si une hypotension survient, elle sera prise en charge par administration intraveineuse d'un soluté cristalloïde ou colloïde et/ou par administration de doses croissantes de vasopresseur tel que l'éphédrine (5-10 mg). Tout facteur associé d'hypotension devra être rapidement pris en charge.
En cas de survenue d'une bradycardie sévère, un traitement par atropine (0,3 à 1 mg) assure en général le retour du rythme cardiaque à un niveau acceptable.
Une arythmie cardiaque sera prise en charge de façon appropriée et une fibrillation ventriculaire sera traitée par cardioversion.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : Anesthésiques locaux, amide, code ATC N01B B10.
La lévobupivacaïne est un anesthésique local et un analgésique de longue durée d'action. Elle bloque la conduction des nerfs sensitifs et moteurs principalement par action sur les canaux sodiques de la membrane cellulaire, mais aussi en bloquant les canaux potassiques et calciques. De plus, la lévobupivacaïne interfère sur la transmission et la conduction de l'influx nerveux vers d’autres organes, ce qui peut donner lieu à des effets indésirables au niveau du système cardiovasculaire et du SNC.
La dose de lévobupivacaïne est exprimée sous forme de base alors que la dose de bupivacaïne racémique est exprimée sous forme de chlorhydrate. Par comparaison avec la bupivacaïne, les solutions de lévobupivacaïne contiennent environ 13% de plus de substance active. Dans les études cliniques, aux mêmes concentrations nominales, l’effet clinique de la lévobupivacaïne est similaire à celui de la bupivacaïne.
Dans une étude de pharmacologie clinique sur le nerf cubital, la lévobupivacaïne a eu une puissance égale à celle de la bupivacaïne.
Les données de sécurité concernant l’administration de lévobupivacaïne pendant des périodes excédant 24 heures sont limitées.
5.2. Propriétés pharmacocinétiques
Chez l'Homme, la distribution de la lévobupivacaïne, après administration IV, est essentiellement similaire à celle de la bupivacaïne.
La concentration plasmatique de lévobupivacaïne après administration à dose thérapeutique dépend de la dose et de la voie d'administration; l'absorption à partir du site d'administration dépend de la vascularisation tissulaire. Les informations issues des études cliniques montrent la mise en place d’un bloc satisfaisant pour une chirurgie en 10 à 15 minutes après une administration péridural avec une levée en 6 à 9 heures.
Après administration de 40 mg de lévobupivacaïne par voie intraveineuse, la demi-vie moyenne était d'environ 80 ± 22 minutes, la Cmax de 1,4 ± 0,2 µg/ml et l'ASC de 70 ± 27 µg.min/ml.
La Cmax moyenne et l'ASC (0-24 h) étaient approximativement proportionnelles à la dose après administration péridurale de 75 mg (0,5%) et 112,5 mg (0,75%) et après administration de 1 mg/kg (0,25%) et 2 mg/kg (0,5%) pour un bloc du plexus brachial. Après administration péridurale de 112,5 mg (0,75%), les valeurs de la Cmax moyenne et de l'ASC étaient de 0,58 µg/ml et 3,56 µg.h/ml respectivement.
Distribution
La liaison aux protéines plasmatiques chez l'Homme a été étudiée in vitro et a été évaluée à plus de 97% pour des concentrations allant de 0,1 à 1,0 µg/ml.
Le volume de distribution après administration intraveineuse était de 67 litres.
Biotransformation
Il n'y pas de données pertinentes chez l'insuffisant hépatique (voir rubrique 4.4).
La lévobupivacaïne subit une importante métabolisation et il n'est pas retrouvé de lévobupivacaïne sous forme inchangée dans les urines ou les fèces. La 3-hydroxylévobupivacaïne, métabolite principal de la lévobupivacaïne, est excrétée dans les urines sous forme de glucurono et sulfo - conjugués. Les études in vitro ont montré que les isoformes CYP3A4 et CYP1A2 interviennent dans le métabolisme de la lévobupivacaïne en desbutyl-lévobupivacaïne et en 3-hydroxylévobupivacaïne respectivement. Ces études indiquent que le métabolisme de la lévobupivacaïne est essentiellement similaire à celui de la bupivacaïne.
Il n'existe aucune preuve de racémisation in vivo de la lévobupivacaïne.
Elimination
Il n'y pas de données chez l'insuffisant rénal. La lévobupivacaïne est très fortement métabolisée et il n'y a pas d'excrétion de lévobupivacaïne sous forme inchangée dans les urines.
La clairance plasmatique totale moyenne et la demi-vie terminale de la lévobupivacaïne étaient de 39 litres/heure et de 1,3 heures respectivement.
Après administration intraveineuse, l'élimination de la lévobupivacaïne est quantitativement importante, avec une quantité totale moyenne d'environ 95% retrouvés dans les urines (71%) et les fèces (24%) en 48 heures.
5.3. Données de sécurité préclinique
La lévobupivacaïne ne s'est pas montrée génotoxique lors d'une série de tests standards évaluant le pouvoir mutagène et clastogène. Aucune étude de carcinogénicité n'a été réalisée.
Ce médicament ne doit pas être mélangé à d’autres médicaments à l’exception de ceux mentionnés dans la rubrique 6.6.
2 ans.
Après première ouverture : le produit doit être utilisé immédiatement.
Après dilution :
La stabilité physico-chimique de la solution de lévobupivacaïne diluée dans du chlorure de sodium 9 mg/ml (0,9%) à une concentration finale de 0,625 mg/ml et 1,25 mg/ml respectivement a été démontrée pendant 30 jours à une température comprise entre 2°C et 8°C ou entre 20°C et 25°C.
La stabilité physico-chimique de la solution de lévobupivacaïne diluée dans du chlorure de sodium 9 mg/ml (0,9%) à une concentration finale de 0,625 mg/ml et 1,25 mg/ml respectivement a été démontrée :
· avec le chlorhydrate de clonidine à 8,4 µg/ml, le sulfate de morphine à 50 µg/ml et le citrate de fentanyl à 2 à 4 µg/ml pendant 30 jours à une température comprise entre 2°C et 8°C ou entre 20°C et 25°C,
· avec du sufentanil ajouté à la concentration de 0,4 µg/ml pendant 30 jours à une température comprise entre 2°C et 8°C ou 7 jours à une température comprise entre 20°C et 25°C.
Toutefois, d’un point de vue microbiologique, le produit doit être utilisé immédiatement. En cas d’utilisation non immédiate, la durée et les conditions de conservation avant utilisation relèvent de la seule responsabilité de l'utilisateur et ne devraient pas dépasser 24 heures entre 2°C et 8°C, sauf en cas de préparation du mélange en conditions d'asepsie dûment validées et contrôlées.
6.4. Précautions particulières de conservation
Ce médicament ne nécessite pas de précautions particulières de conservation.
Pour les conditions de conservation du médicament après dilution et première ouverture, voir la rubrique 6.3.
6.5. Nature et contenu de l'emballage extérieur
10 ml en ampoule (polypropylène) avec suremballage stérile. Boîte de 5, 10 ou 20 ampoules.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
A usage unique. Les spécialités en ampoules sont destinées aux voies péridurale, intrathécale, périneurale et aux infiltrations. Toute solution non utilisée doit être jetée.
Ne pas utiliser si le conditionnement extérieur est endommagé.
La solution/dilution doit être vérifiée visuellement avant utilisation. Seules les solutions limpides sans particule visible seront utilisées.
Le conditionnement sous suremballage stérile doit être utilisé quand la stérilité extérieure de l'ampoule est nécessaire. La surface de l'ampoule n'est pas stérile si le suremballage stérile est percé.
Les solutions standards de lévobupivacaïne seront diluées avec une solution injectable de chlorure de sodium à 9 mg/ml (0,9%), en respectant les règles usuelles d’asepsie.
Il a été montré que la clonidine à 8,4 µg/ml, la morphine à 0,05 mg/ml et le fentanyl à 2-4 µg/ml étaient compatibles à la lévobupivacaïne dans une solution injectable de chlorure de sodium à 9 mg/ml (0,9%).
Pour la durée de conservation du produit dilué, se reporter à la rubrique 6.3.
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
5 PLACE DU MARIVEL
92316 SEVRES CEDEX
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 586 934 6 5 : 10 ml en ampoule (polypropylène). Boîte de 5.
· 34009 586 935 2 6: 10 ml en ampoule (polypropylène). Boîte de 10.
· 34009 586 936 9 4: 10 ml en ampoule (polypropylène). Boîte de 20.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[À compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[À compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I
Médicament réservé à l’usage hospitalier.
ANSM - Mis à jour le : 26/04/2024
LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion
Chlorhydrate de lévobupivacaïne
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin, votre pharmacien ou votre infirmier/ère.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion ?
3. Comment utiliser LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : Anesthésiques locaux, amide, code ATC N01B B10.
LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion appartient à une famille de médicaments appelée anesthésiques locaux. Ce type de médicament est utilisé pour anesthésier certaines parties du corps ou pour soulager la douleur.
Chez les adultes et les adolescents (âgés de 12 ans et plus) :
LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion s'utilise en tant qu'anesthésique local pour anesthésier certaines parties du corps avant une chirurgie lourde (par exemple, pour une anesthésie péridurale en vue d'une césarienne) ou une chirurgie légère.
Il est également utilisé pour soulager la douleur :
· après une chirurgie lourde,
· pendant l'accouchement.
Enfants (âgés de moins de 12 ans)
LEVOBUPIVACAINE KABI peut également être utilisé chez l’enfant pour anesthésier certaines parties
du corps avant une chirurgie et pour soulager la douleur après une chirurgie légère telle qu’une cure
de hernie inguinale.
LEVOBUPIVACAINE KABI n’a pas été étudié chez l’enfant de moins de 6 mois.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion ?
N’utilisez jamais LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion :
· si vous êtes allergique à la lévobupivacaïne, à tout autre anesthésique local similaire ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
· si votre pression artérielle est très basse.
· pour anesthésier une région du corps par injection intraveineuse de LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion.
· pour soulager la douleur par injection dans la région du col de l'utérus au cours des premiers stades du travail lors de l’accouchement (bloc paracervical).
Avertissements et précautions
Adressez-vous à votre médecin, pharmacien ou votre infirmier/ère avant d’utiliser LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion.
Avant que LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion ne vous soit administré, informez votre médecin si vous présentez l'une des maladies ou conditions ci-dessous. Il vous faudra peut-être être suivi(e) plus étroitement ou recevoir une dose plus faible :
· si vous souffrez d'une maladie cardiaque ;
· si vous souffrez de maladies du système nerveux ;
· si vous êtes faible ou malade ;
· si vous êtes âgé(e) ;
· si vous souffrez d'une maladie du foie.
Enfants
Sans objet.
Autres médicaments et LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion
Informez votre médecin ou votre infirmière si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
Particulièrement si vous prenez des médicaments pour :
· les troubles du rythme cardiaque (par exemple la mexilétine),
· les mycoses (par exemple le kétoconazole), en raison de l'influence possible sur la vitesse d'élimination de LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion par l'organisme,
· l'asthme (par exemple la théophylline), en raison de l'influence possible sur la vitesse d'élimination de LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion par l'organisme.
LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion avec des aliments
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin avant de prendre ce médicament.
LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion ne doit pas être administré pour soulager la douleur par injection dans la région du col de l'utérus au cours de l'accouchement (bloc paracervical).
Les effets de LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion sur le fœtus au cours des premiers stades de la grossesse ne sont pas connus. Par conséquent, LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion ne doit pas être utilisé pendant le premier trimestre de grossesse, sauf en cas de nécessité.
On ne sait pas si la lévobupivacaïne passe dans le lait maternel. Cependant la lévobupivacaïne est probablement excrétée en petites quantités seulement dans le lait maternel, comme c'est le cas pour un médicament similaire. Il est, par conséquent, possible d'allaiter après l'administration d'un anesthésique local.
Conduite de véhicules et utilisation de machines
L'utilisation de LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion peut avoir un effet important sur la capacité à conduire des véhicules et à utiliser des machines. Vous ne devez ni conduire, ni utiliser de machine jusqu'à disparition totale des effets de LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion et des effets immédiats de l'opération. Avant de quitter l'hôpital, demandez conseil à ce sujet à votre médecin ou à votre infirmière qui vous soigne.
LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion contient du sodium.
Ce médicament contient 3,6 mg de sodium (composant principal du sel de cuisine/table) par ml. Cela équivaut à 0,18 % de l’apport alimentaire quotidien maximal recommandé de sodium pour un adulte.
3. COMMENT UTILISER LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion ?
Posologie
La quantité et la fréquence à laquelle LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion vous sera administré dépendra de la raison de son utilisation mais également de votre état de santé, de votre âge et de votre poids. La dose la plus faible pouvant entraîner une anesthésie de la région visée sera utilisée. Cette dose sera déterminée avec soin par votre médecin.
L'utilisation de LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion pour soulager la douleur pendant le travail ou en cas d'accouchement par césarienne (péridurale) nécessite une attention particulière quant à la dose utilisée.
Veillez à toujours utiliser ce médicament en suivant exactement les instructions de cette notice ou les indications de votre médecin, pharmacien ou infirmier/ère. Vérifiez auprès de votre médecin, pharmacien ou infirmier/ère en cas de doute.
Si une quantité trop importante de LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion vous est administrée, les symptômes suivants peuvent apparaître: engourdissement de la langue, étourdissements, vision trouble, contractions musculaires, difficultés respiratoires sévères (y compris arrêt respiratoire), voire convulsions. Si vous remarquez l'un de ces symptômes, dites-le immédiatement à votre médecin. Une dose trop forte de LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion peut parfois entraîner une hypotension, une accélération, un ralentissement ou une modification du rythme cardiaque. Votre médecin devra éventuellement vous administrer d'autres médicaments pour soulager ces symptômes.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez à votre médecin ou votre infirmière.
Si vous oubliez d’utiliser LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion
Si vous arrêtez d’utiliser LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion
Sans objet.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez à votre médecin ou votre infirmière.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Si vous présentez l’un des effets indésirables suivants, veuillez en informer immédiatement votre médecin ou votre infirmière. Certains effets indésirables de LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion peuvent être graves.
Très fréquents : (peut affecter plus d’1 personne sur 10)
· fatigue ou faiblesse, essoufflement, pâleur (ce sont des signes d’anémie),
· pression artérielle basse,
· nausées.
Fréquents : (peut affecter jusqu’à 1 personne sur 10)
· étourdissements,
· maux de tête,
· vomissements,
· problèmes pour le fœtus (détresse fœtale),
· douleur au niveau du dos,
· température corporelle élevée (fièvre),
· douleur après l’opération.
Fréquence inconnue : (fréquence ne pouvant être estimée sur la base des données disponibles)
· réactions allergiques graves (hypersensibilité) qui peuvent provoquer des difficultés respiratoires sévères, une difficulté à avaler, une urticaire, et une pression artérielle très basse,
· réactions allergiques (hypersensibilité) sous forme de rougeurs de la peau et démangeaisons, éternuements, transpiration excessive, accélération du rythme cardiaque, syncope ou gonflement de la face, des lèvres, de la bouche, de la langue ou de la gorge,
· perte de conscience,
· somnolence,
· vision trouble,
· arrêt respiratoire,
· bloc cardiaque ou arrêt cardiaque,
· fourmillements localisés,
· engourdissement de la langue,
· faiblesse ou contractions musculaires,
· incontinence urinaire ou fécale,
· paralysie,
· crises (convulsions),
· fourmillements, engourdissement ou autre sensation anormale,
· érection du pénis prolongée qui peut être douloureuse,
· troubles nerveux pouvant inclure une chute de la paupière, une pupille (centre noir de l’œil) rétrécie, les yeux enfoncés dans les orbites, une transpiration et/ou une rougeur sur un côté du visage.
L’accélération, le ralentissement, l’irrégularité ou les modifications du rythme cardiaque détectées par ECG sont des effets indésirables qui ont été également signalés.
Dans de rares cas, certains effets indésirables peuvent durer longtemps ou devenir permanents.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou à votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: https://signalement.social-sante.gouv.fr/
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’étiquette après EXP. La date de péremption fait référence au dernier jour de ce mois.
Ce médicament sera conservé pour vous par votre médecin.
Après première ouverture : le produit doit être utilisé immédiatement.
La solution ne doit pas être utilisée si elle contient des particules visibles.
Ce médicament ne nécessite pas de précautions particulières de conservation.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion
· La substance active est : lévobupivacaïne (sous forme de chlorhydrate)
1 ml de solution contient 2,5 mg de lévobupivacaïne (sous forme de chlorhydrate de lévobupivacaïne). Une ampoule de 10 ml contient 25 mg de lévobupivacaïne (sous forme de chlorhydrate de lévobupivacaïne).
· Les autres composants sont : Chlorure de sodium, hydroxyde de sodium, acide chlorhydrique et eau pour préparations injectables.
Ce médicament contient un excipient à effet notoire (le sodium). Voir rubrique 2 pour plus d’informations.
pH 4,0 – 6,0.
Osmolarité : 271 – 372 mOsmol/L.
Ce médicament se présente sous forme de solution limpide et incolore en ampoule de polypropylène avec suremballage stérile. Chaque ampoule contient 10 ml de solution. Boîtes de 5, 10 ou 20 ampoules.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
5 PLACE DU MARIVEL
92316 SEVRES CEDEX
Exploitant de l’autorisation de mise sur le marché
FRESENIUS KABI FRANCE
5 PLACE DU MARIVEL
92316 SÈVRES CEDEX
Svinesundsveien 80
1788 Halden
NORVEGE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[À compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
Les informations suivantes sont destinées exclusivement aux professionnels de santé :
LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion
Instructions pour l’utilisation et la manipulation
LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion est à usage unique. Toute solution non utilisée doit être éliminée. Ne pas utiliser si le conditionnement extérieur est endommagé.
Il convient de procéder à une vérification visuelle de la solution/dilution avant utilisation. Seules les solutions limpides sans particules peuvent être utilisées.
Le conditionnement sous suremballage stérile doit être utilisé quand la stérilité extérieure de l’ampoule est nécessaire. La surface de l'ampoule n'est pas stérile si le suremballage stérile est percé.
Les solutions standards de lévobupivacaïne seront diluées avec une solution injectable de chlorure de sodium à 9 mg/ml (0,9%), de façon aseptique.
Il a été démontré que la clonidine à 8,4 µg/ml, la morphine à 0,05 mg/ml, le fentanyl à 2-4 µg/ml et le sufentanil à 0,4 µg/ml étaient compatibles avec la lévobupivacaïne dans le chlorure de sodium à 9 mg/ml (0,9%) en solution injectable.
Après première ouverture : le produit doit être utilisé immédiatement.
Après dilution :
La stabilité physico-chimique a été démontrée de lévobupivacaïne diluée dans du chlorure de sodium 9 mg/ml (0,9%) à une concentration finale de 0,625 mg/ml et 1,25 mg/ml respectivement a été démontrée pendant 30 jours à une température de 2°C et 8°C ou entre 20°C et 25°C.
La stabilité physico-chimique de la solution de lévobupivacaïne diluée dans du chlorure de sodium 9 mg/ml (0,9%) à une concentration finale de 0,625 mg/ml et 1,25 mg/ml respectivement a été démontrée :
· avec chlorhydrate de clonidine à 8,4 µg/ml, sulfate de morphine à 50 µg/ml et citrate de fentanyl à 2 à 4 µg/ml pendant 30 jours à une température comprise entre 2°C et 8°C ou entre 20°C - 25°C.
· avec du sufentanil ajouté à la concentration de 0,4 µg/ml pendant 30 jours à une température comprise entre 2°C et 8°C ou 7 jours à une température comprise entre 20°C et 25°C.
Toutefois, d’un point de vue microbiologique, le produit doit être utilisé immédiatement. En cas d’utilisation non immédiate, la durée et les conditions de conservation avant utilisation relèvent de la seule responsabilité de l’utilisateur et ne devraient pas dépasser 24 heures entre 2°C et 8°C, sauf en cas de préparation du mélange en conditions d’asepsie dûment validées et contrôlées.
LEVOBUPIVACAINE KABI 2,5 mg/ml, solution injectable/pour perfusion ne doit pas être mélangé à d’autres médicaments à l’exception de ceux mentionnés ci-dessus. La lévobupivacaïne peut précipiter si elle est diluée dans des solutions alcalines telles que le bicarbonate de sodium.
Les données de sécurité concernant l’administration de lévobupivacaïne pendant des périodes excédant 24 heures sont limitées.
Mode d’administration
La lévobupivacaïne devra être administrée uniquement par, ou sous la surveillance d'un médecin ayant la formation et l'expérience nécessaires.
Veuillez-vous référer au résumé des caractéristiques du produit pour les informations concernant la posologie.
Une aspiration soigneuse avant et pendant l'injection est recommandée dans le but de prévenir toute injection intravasculaire.
L'aspiration devra être répétée avant et pendant l'administration de la dose principale en dose bolus, qui devra être injectée lentement et à doses croissantes, à une vitesse de 7,5 à 30 mg/min, tout en surveillant étroitement les fonctions vitales du patient et en maintenant le contact verbal avec lui.
Si des symptômes de toxicité apparaissent, l'injection devra être arrêtée immédiatement.
|
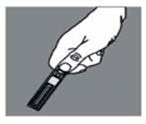
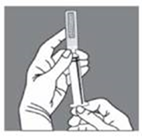
1. Lisez attentivement l’étiquette. Secouez vers le bas la solution présente dans le col de l’ampoule. |
|
|
|
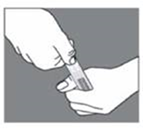
2. Tenez l’ampoule dans la paume de la main au niveau du col de l’ampoule. Maintenez la flèche sur la tête de l’ampoule entre le pouce et l’index (avec le pouce opposé à vous). TOURNEZ RAPIDEMENT ET BRUSQUEMENT VERS VOUS (dans le sens opposé des aiguilles d’une montre) |
|
|
|
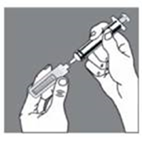
3. Enfoncez fermement l’embout conique Luer de la seringue dans l’ampoule. |
|
|
|
4. |
|
|
|
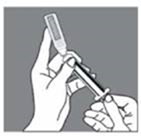
5. Poussez doucement l’ampoule vers vous avec l’index et videz lentement son contenu, en faisant particulièrement attention au début. |
|
|