Dernière mise à jour le 01/12/2025
MULTIBIC 4 mmol/l POTASSIUM, solution pour hémodialyse/hémofiltration
Indications thérapeutiques
MULTIBIC 4 mmol/l POTASSIUM est une solution d’épuration extra-rénale continue pour éliminer les toxines urémiques issues du métabolisme de l’organisme chez des personnes atteintes d’une défaillance rénale aigue. Il est utilisé chez les patients présentant des lésions rénales ainsi que dans le traitement de l’intoxication médicamenteuse ou toxique. Le type de solution prescrite dépend de la quantité de potassium (un sel) dans votre sang. Votre médecin vérifiera régulièrement votre taux de potassium.
Composition en substances actives
-
Petit compartiment ( Composition pour 1000 ml )
- > chlorure de potassium 5,964 g
- > chlorure de calcium dihydraté 4,410 g
- glucose anhydre20 g
- sous forme de : glucose monohydraté22 g
- > chlorure de magnésium hexahydraté 2,033 g
- > chlorure de sodium 6,453 g
- > bicarbonate de sodium 3,104 g
Présentations
> 2 poches bicompartimentées - petit compartiment polytéréphtalate polyamide polyoléfine de 250 ml - grand compartiment polytéréphtalate polyamide polyoléfine de 4750 ml équipées d’un connecteur HF, d’un connecteur luer-lock et d’un port d’injection
Code CIP : 346 954-2 ou 34009 346 954 2 1
Déclaration de commercialisation : 14/06/2010
Cette présentation est agréée aux collectivités
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 31/03/2010 | Inscription (CT) | Le service médical rendu par ces spécialités est important dans l'insuffisance rénale aiguë nécessitant une hémofiltration en continu. |
| Important | Avis du 23/01/2008 | Inscription (CT) | Le service médical rendu par cette spécialité est important dans l'indication : Insuffisance rénale aiguë nécessitant une hémofiltration en continu. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 31/03/2010 | Inscription (CT) | Absence d'amélioration du service médical rendu (ASMR V). |
| V (Inexistant) | Avis du 23/01/2008 | Inscription (CT) | La spécialité MULTIBIC 4 mmol/l POTASSIUM n’apporte pas d’amélioration du service médical rendu (ASMR V) par rapport aux autres solutions d’hémofiltration de la gamme. |
ANSM - Mis à jour le : 05/03/2025
MULTIBIC 4 mmol/l POTASSIUM solution pour hémodialyse/hémofiltration
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
MULTIBIC 4 mmol/l POTASSIUM est présenté en poche bi-compartimentée : un compartiment de 4750 mL contenant la solution alcaline de bicarbonate, l’autre compartiment de 250 mLmL contenant la solution acide à base de glucose et d’électrolytes.
AVANT RECONSTITUTION :
1000 mL de solution contiennent :
Solution acide à base de glucose et d’électrolytes (petit compartiment)
Chlorure de potassium.......................................................................................................... 5,964 g
Chlorure de calcium dihydraté............................................................................................... 4,410 g
Chlorure de magnésium hexahydraté..................................................................................... 2,033 g
Glucose monohydraté........................................................................................................... 22,00 g
(Glucose)........................................................................................................................... (20,00 g)
K+.................................................................................................................................... 80 mmol/l
Ca2+.................................................................................................................................. 30 mmol/l
Mg2+................................................................................................................................. 10 mmol/l
Cl-.................................................................................................................................. 162 mmol/l
Glucose.......................................................................................................................... 111 mmol/l
Solution alcaline de bicarbonate (grand compartiment)
Chlorure de sodium.............................................................................................................. 6,453 g
Bicarbonate de sodium......................................................................................................... 3,104 g
Na+................................................................................................................................. 147 mmol/l
Cl-.................................................................................................................................. 110 mmol/l
HCO3-.............................................................................................................................. 37 mmol/l
APRES RECONSTITUTION :
1000 mL de la solution prête à l’emploi contiennent :
Chlorure de potassium........................................................................................................ 0,2982 g
Chlorure de sodium.............................................................................................................. 6,136 g
Bicarbonate de sodium......................................................................................................... 2,940 g
Chlorure de calcium dihydraté.............................................................................................. 0,2205 g
Chlorure de magnésium hexahydraté.................................................................................... 0,1017 g
Glucose monohydraté........................................................................................................... 1,100 g
(Glucose) .......................................................................................................................... (1,000 g)
K+................................................................................................................................... 4,0 mmol/l
Na+............................................................................................................................ 140,00 mmol/l
Ca2+................................................................................................................................. 1,5 mmol/l
Mg2+.............................................................................................................................. 0,50 mmol/l
Cl-.................................................................................................................................. 113 mmol/l
HCO3-.............................................................................................................................. 35 mmol/l
Glucose......................................................................................................................... 5,55 mmo/ll
Pour la liste complète des excipients, voir rubrique 6.1.
Solution pour hémodialyse/hémofiltration.
La solution prête à l’emploi est limpide et incolore.
Osmolarité théorique : 300 mOsm/L
pH » 7,4
4.1. Indications thérapeutiques
MULTIBIC 4 mmol/l POTASSIUM est indiqué par voie intraveineuse comme solution de substitution pour l’hémofiltration et l’hémodiafiltration et comme solution de dialyse pour l’hémodialyse et l'hémodiafiltration.
Pour utilisation chez les patients :
· présentant une insuffisance rénale chronique, pour lesquels un traitement temporaire est indiqué, par exemple pendant un séjour en soins intensifs.
· pour lesquels une épuration extra-rénale continue est indiquée dans le cadre du traitement d’une intoxication par des substances toxiques solubles dans l’eau, filtrables/dialysables.
MULTIBIC 4 mmol/l POTASSIUM est indiqué chez l’adulte.
4.2. Posologie et mode d'administration
L’épuration extra-rénale continue nécessitant la prescription de ce médicament doit être réalisée sous la responsabilité d'un médecin connaissant la technique.
En cas d’insuffisance rénale aiguë chez un adulte de poids corporel de 70 kg, une épuration extra-rénale continue à la dose de 2000 mL/h de MULTIBIC 4 mmol/l POTASSIUM est indiquée pour éliminer les déchets métaboliques, en fonction du statut métabolique du patient. La posologie doit être adaptée à la corpulence du patient.
Chez les patients présentant une insuffisance rénale chronique, sauf indication clinique contraire, la dose de MULTIBIC 4 mmol/l POTASSIUM devrait être d’au moins un tiers du poids corporel pour chaque séance, avec 3 séances par semaine. L’augmentation du volume administré par semaine ou la répartition de ce volume hebdomadaire sur plus de 3 séances par semaine peut être nécessaire.
Pour le traitement des intoxications aiguës, la dose et la durée de l’hémodialyse, de l’hémofiltration ou de l’hémodiafiltration dépendent du produit toxique et de sa concentration ainsi que de la sévérité des symptômes cliniques et doivent être adaptées individuellement par le médecin en fonction de l’état du patient.
Il n'est pas recommandé de dépasser la dose maximale de 75 litres par jour.
Population pédiatrique
La sécurité et l’efficacité de MULTIBIC 4 mmol/l POTASSIUM chez les enfants n’ont pas encore été établies (voir rubriques 4.4 et 5.1).
Mode d’administration
Pour utilisation par voie intraveineuse et hémodialyse.
Pour les instructions d'utilisation, voir rubrique 6.6
Les contre-indications liées à la solution sont les suivantes :
· Hypersensibilité aux substances actives ou à l’un des excipients mentionnés à la rubrique 6.1 ;
· Hyperkaliémie ;
· Alcalose métabolique.
Les contre-indications liées à la technique sont les suivantes :
· Débit sanguin inadapté à partir de l’accès vasculaire ;
· Anticoagulation systémique associée à un sur-risque d’hémorragie élevé.
4.4. Mises en garde spéciales et précautions d'emploi
Ne pas utiliser avant d’avoir mélangé les 2 solutions.
Avant utilisation, la solution MULTIBIC 4 mmol/l POTASSIUM doit être réchauffé approximativement à la température du corps à l'aide d'un réchauffeur approprié et ne doit pas être utilisée si la température de la solution est inférieure à la température ambiante.
Le réchauffement de la solution prête à l’emploi à la température corporelle doit être contrôlé attentivement en vérifiant que la solution prête à l’emploi est claire et sans particules.
La formation d'un précipité blanc de carbonate de calcium a été rarement observée dans les tubulures lors de l'utilisation de la solution prête à l’emploi, plus particulièrement aux abords de la pompe et du réchauffeur de cette solution prête à l’emploi.
L'apparition de tels précipités peut survenir en particulier si la température de la solution prête à l’emploi en amont de la pompe excède déjà 30°C.
En conséquence, la solution prête à l’emploi dans les tubulures doit faire l'objet d'une surveillance visuelle étroite à intervalles de 30 minutes durant une séance d’épuration extra-rénale continue afin de s'assurer que cette solution dans les tubulures est limpide et exempte de précipité. Les précipités peuvent apparaître, en général, plusieurs heures après le début du traitement. Si un précipité est détecté, la solution prête à l’emploi et les lignes utilisées pour l’épuration extra-rénale continue doivent être immédiatement remplacées et le patient doit être surveillé étroitement.
La kaliémie doit être contrôlée régulièrement avant et pendant l’épuration extra-rénale continue. La kaliémie du patient ainsi que son évolution doivent être surveillés en cours de traitement.
En cas d’hypokaliémie, une supplémentation en potassium et/ou un changement de la solution d’hémodialyse/d’hémofiltration pour une solution à concentration accrue en potassium peut être nécessaire.
En cas d'hyperkaliémie, il est indiqué d'augmenter la dose et/ou d'utiliser une solution d’hémodialyse/d’hémofiltration ayant une concentration réduite en potassium. Dans ces situations, le recours aux mesures de thérapie intensive peut s'avérer nécessaire.
La natrémie doit être vérifiée régulièrement avant et pendant le traitement par la solution d’hémodialyse/hémofiltration pour contrôler le risque lié à l’hypo/hypernatrémie. La normalisation de l'hypo/hypernatrémie doit être effectuée soigneusement afin d'éviter la survenue d’effets indésirables dus aux changements trop rapides de la natrémie. La concentration en sodium de MULTIBIC peut être modifiée par dilution avec une quantité d'eau pour préparations injectables adéquate ou par ajout d'une quantité adéquate de solution concentrée de chlorure de sodium.
De plus, les paramètres suivants doivent être contrôlés avant et pendant l’épuration extra-rénale continue : calcémie, magnésémie, phosphatémie, glycémie, équilibre acido-basique, urémie et créatininémie, poids corporel et bilan hydrique (pour le diagnostic précoce d'un trouble de l’hydratation par excès ou défaut).
L’hémodialyse, l’hémofiltration, ou l’hémodiafiltration peuvent entrainer l’élimination de substances cliniquement important non compensées par ce médicament. Cette élimination de nutriments essentiels doit être compensée par un régime alimentaire adéquat, des compléments alimentaires ou une nutrition parentérale adaptée.
Population pédiatrique
Aucune étude chez l’enfant n’a été réalisée. L’utilisation de ce médicament n’est pas recommandée chez l’enfant jusqu’à l’obtention de données supplémentaires (voir section 4.2 et 5.1).
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Aucune étude d’interaction n’a été réalisée.
Un dosage correct de MULTIBIC 4 mmol/l POTASSIUM ainsi qu’une surveillance stricte des paramètres cliniques et des signes vitaux éviteront les risques d’interactions avec d’autres médicaments.
Les interactions suivantes sont possibles :
· Les effets toxiques des digitaliques peuvent être masqués par une hyperkaliémie, une hypermagnésémie et une hypocalcémie. La correction de ces électrolytes par épuration extra-rénale continue peut précipiter l’apparition de signes et symptômes d’intoxication digitalique avec, par exemple, une arythmie cardiaque.
· Les solutions de substitution électrolytiques, la nutrition parentérale et autres solutions de perfusion habituellement prescrites en soins intensifs, interagissent avec la composition sérique et le bilan hydrique du patient. Ceci doit être considéré en cas d’administration d’une épuration extra-rénale continue.
· Une épuration extra-rénale continue peut réduire la concentration sérique de certains médicaments, tels que les médicaments avec faible capacité de liaison aux protéines, avec faible volume de distribution, avec poids moléculaire inférieur au point de coupure de l’hémofiltre et les médicaments qui sont adsorbés sur l’hémofiltre. Une vérification du dosage de tels médicaments peut être nécessaire.
4.6. Fertilité, grossesse et allaitement
Grossesse
Il n’existe pas de données ou il existe des données limitées sur l’utilisation de MULTIBIC 4 mmol/l POTASSIUM chez la femme enceinte. Les études effectuées chez l’animal sont insuffisantes pour permettre de conclure sur la toxicité sur la reproduction (voir rubrique 5.3.).
MULTIBIC 4 mmol/l POTASSIUM ne doit pas être utilisé pendant la grossesse à moins que la situation clinique de la femme ne justifie le traitement par épuration extra-rénale continue.
Il n’existe pas de données suffisantes sur l’excrétion de MULTIBIC 4 mmol/l POTASSIUM et/ou de ses métabolites dans le lait maternel. L’allaitement n’est pas recommandé pendant le traitement par MULTIBIC 4 mmol/l POTASSIUM.
Fertilité
Aucune donnée n’est disponible.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Les effets indésirables peuvent provenir du mode de traitement lui-même ou peuvent être induits par le médicament :
Tableau listant les effets indésirables :
|
Classe de systèmes d’organes (SOC) |
Effet indésirable |
Fréquence |
|
Affections vasculaires |
Hypertension |
La fréquence exacte de ces événements est indéterminée (ne peut être estimée sur la base des données disponibles). |
|
Hypotension |
||
|
Affections gastro-intestinales |
Nausées |
|
|
Vomissements |
||
|
Affections musculosquelettiques et du tissu conjonctif |
Crampes musculaires |
Les effets indésirables suivants peuvent être liés au traitement :
|
Effet indésirable |
Fréquence |
|
|
Troubles du métabolisme et de la nutrition |
Hyper- ou hypohydratation |
La fréquence exacte de ces événements est indéterminée (ne peut être estimée sur la base des données disponibles). |
|
Troubles électrolytiques (par exemple, hypokaliémie) |
||
|
Hypophosphatémie |
||
|
Hyperglycémie |
||
|
Alcalose métabolique |
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.signalement-sante.gouv.fr
Lorsque la solution est utilisée selon la prescription, aucun cas grave de surdosage n’a été rapporté.
D'ailleurs, l’administration du médicament peut être arrêtée à n’importe quel moment.
Si l’équilibre des fluides n’est pas calculé et surveillé correctement, une hyperhydratation ou une déshydratation sévères peuvent apparaître, accompagnées de troubles circulatoires. Ces troubles peuvent se traduire par une modification de la pression sanguine, de la pression veineuse centrale, du débit cardiaque et de la pression artérielle pulmonaire. En cas d’hyperhydratation, des accidents congestifs cardiaques et/ou une congestion pulmonaire peuvent se produire.
En cas d’hyperhydratation, l’ultrafiltration nette de liquides doit être augmentée sur le dispositif utilisé pour l’épuration extra-rénale continue. En cas de déshydratation sévère, l’ultrafiltration nette de liquides par le dispositif d’épuration extra-rénale continue doit être diminuée ou interrompue ; de façon alternative, une réanimation liquidienne peut être instaurée pour rétablir le statut d’hydratation.
L’administration d’un grand volume peut entraîner des désordres électrolytiques et des modifications de l’équilibre acido-basique. Par exemple, un excès de bicarbonate peut apparaître, si un volume trop important de solution pour hémodialyse/hémofiltration est administré. Ceci peut entraîner éventuellement une alcalose métabolique, une diminution du calcium ionisé ou une tétanie.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : Solutions pour hémofiltration, code ATC : B05ZB
Mécanisme d’action
Principes de base de l’hémofiltration, l’hémodialyse et l’hémodiafiltration :
Pendant l’hémofiltration, l’eau et les solutés, tels que les toxines urémiques, les électrolytes et le bicarbonate, sont épurés par ultrafiltration. L’ultrafiltrat est remplacé par une solution d’hémofiltration ayant une composition équilibrée en électrolytes et en tampon.
Pendant l’hémodialyse, l’eau et les solutés tels que les toxines urémiques, les électrolytes, le bicarbonate et autres petites molécules sont échangées par diffusion entre le sang du patient et la solution d’hémodialyse. La direction et l’importance du processus de diffusion dépendent des gradients de concentration significatifs entre sang et la solution pour hémodialyse.
Dans l’hémodiafiltration, les principes de base de l’hémofiltration et l’hémodialyse sont combinés.
Ce médicament est une solution au tampon bicarbonate, administrée par voie intraveineuse ou pour utilisation comme solution d’hémodialyse pour la correction de l’homéostasie hydro-électrolytique pendant une épuration extra-rénale continue, par exemple pour le traitement de l’insuffisance rénale aiguë. Les électrolytes Na+, K+, Mg2+, Ca2+, Cl- et le bicarbonate sont indispensables pour le maintien et la correction du bilan liquidien et des électrolytes (volume sanguin, équilibre osmotique, équilibre acido-basique).
Population pédiatrique
Aucune étude chez l’enfant n’a été réalisée. L’utilisation de ce médicament n’est pas recommandée chez l’enfant jusqu’à l’obtention de données supplémentaires (voir section 4.2 et 4.4).
5.2. Propriétés pharmacocinétiques
Ce médicament doit seulement être administrée par voie intraveineuse ou utilisé comme solution d’hémodialyse.
Distribution / Biotransformation / Élimination
La distribution des électrolytes et du bicarbonate est régulée selon les besoins, l’état métabolique et la fonction rénale résiduelle. Les substances actives de ce médicament ne sont pas métabolisées, excepté le glucose. L’élimination de l’eau et des électrolytes dépend des besoins cellulaires, de l’état métabolique, de la fonction rénale résiduelle et des autres voies d’élimination des fluides (par exemple, voie intestinale, voie respiratoire et voie cutanée).
5.3. Données de sécurité préclinique
Aucune donnée de sécurité préclinique n’est disponible.
Petit compartiment : eau pour préparations injectables, acide chlorhydrique 25 %
Grand compartiment : eau pour préparations injectables, dioxyde de carbone, dihydrogénophosphate de sodium dihydraté.
2 ans
Conditions de conservation après avoir mélangé les 2 compartiments (solution prête à l’emploi) :
La stabilité physico-chimique en cours d'utilisation de la solution prête à l'emploi a été démontrée sur 48 heures à 30°C. Il n’est pas recommandé de conserver la solution prête à l’emploi plus de 48 heures, durée de traitement incluse, ou à une température à l'entrée de la pompe supérieure à 30°C.
D’un point de vue microbiologique, une fois connectée au circuit d’hémofiltration, d’hémodialyse ou d’hémodiafiltration et compte-tenu de la présence de bicarbonate, le médicament doit être utilisé immédiatement.
6.4. Précautions particulières de conservation
Ne pas conserver à une température inférieure à 4°C.
6.5. Nature et contenu de l'emballage extérieur
Poche bi-compartimentée avec 4750 mL (solution alcaline de bicarbonate) + 250 mL (solution acide à base de glucose et d’électrolytes) = 5000 mL (solution prête à l’emploi).
Le film de la poche est composé de polyéthylène téréphtalate, SiOx, polyamide et polyoléfine.
Chaque poche est équipée d’un connecteur HF, d’un connecteur Luer lock et d’un port d’injection, et est recouverte d’un film protecteur.
Taille du conditionnement :
2 poches de 5 000 mL.
6.6. Précautions particulières d’élimination et de manipulation
La solution prête à l’emploi ne peut être utilisée que si elle est limpide et incolore et si la poche et les connecteurs sont intacts et non endommagés.
Pour usage unique seulement. Jeter les quantités non utilisées.
La solution pour hémodialyse/hémofiltration doit être administrée en 3 étapes :
1. Retirer le film protecteur et inspecter minutieusement la poche.
Le film protecteur doit être retiré seulement immédiatement avant l’administration.
Les poches peuvent parfois être endommagées durant le transport du fabricant au centre de soins ou dans le centre de soins lui-même. Cela peut entraîner une contamination et une prolifération microbienne ou fongique dans la solution. Il est donc nécessaire de mirer soigneusement la poche et la solution avant de mélanger.
Il est indispensable de contrôler soigneusement la qualité du connecteur, des soudures ou des angles des poches en raison du risque possible de contamination.
2. Mélanger les deux compartiments
Les deux compartiments de la poche - le compartiment bicarbonate et le compartiment d’électrolytes et de glucose - sont mélangés immédiatement avant utilisation pour obtenir la solution prête à l’emploi.
|
|
|
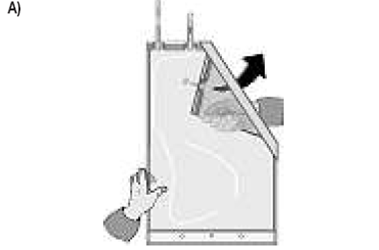
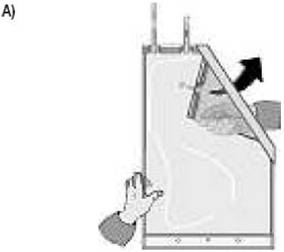
Déplier le petit compartiment |
|
|
|
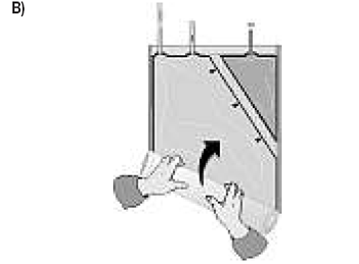
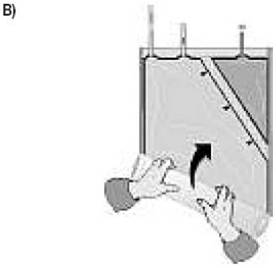
Rouler la poche de la solution en commençant par le coin inverse au petit compartiment |
|
|
|
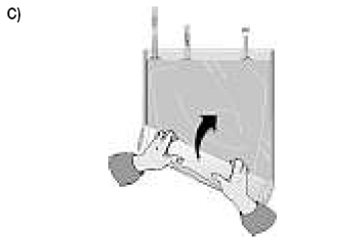
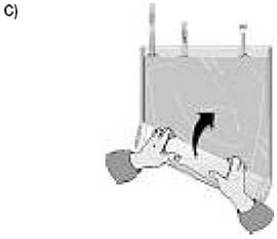
Jusqu’à ouverture de la thermo-soudure sur toute sa longueur et le mélange complet des deux solutions. |
Après mélange des deux solutions, il faut vérifier l'ouverture complète de la thermo-soudure, la limpidité et la clarté de la solution mélangée, l'absence de fuite sur la poche.
Connexion de la poche au circuit extracorporel
Connecter la poche au circuit extracorporel à l’aide d’une technique aseptique et conformément au mode d'emploi du dispositif choisi pour l'EERC. Retirer le capuchon du connecteur HF ou du connecteur Luer-Lock en effectuant un mouvement de torsion et de traction et, à l’aide d’une technique aseptique, raccorder le connecteur mâle de la tubulure de remplacement au récepteur femelle de la poche. Vérifier que les parties mâle et femelle s'emboîtent correctement et que la connexion est bien serrée.
Ensuite, casser le cône du connecteur femelle de la poche en avant puis en arrière pour déclencher l'écoulement. Vérifier que le liquide s'écoule sans difficulté au cours de l'utilisation.
3. Utilisation de la solution prête à l’emploi.
La solution prête à l’emploi doit être utilisée immédiatement ou dans les 48 heures suivant le mélange.
Tout ajout à la solution prête à l’emploi doit être réalisé seulement après avoir mélangé correctement la solution prête à l’emploi. Après ajout d'une substance, la solution prête à l’emploi doit de nouveau être correctement mélangée avant utilisation.
Le mélange d’une solution de chlorure de sodium (concentration entre 3 % et 30 % de chlorure de sodium ; jusqu’à 250 mmol de chlorure de sodium pour 5 litres de solution MULTIBIC) et d’eau pour préparation injectable (jusqu’à 1250 mL pour 5 litres de solution MULTIBIC) sont compatibles avec ce médicament.
Sauf indication contraire, la solution prête à l’emploi doit être réchauffée à 36,5°C – 38,0°C, immédiatement avant l’utilisation. La température est déterminée en fonction des besoins cliniques et de l’équipement utilisé.
Pas d’exigences particulières pour l’élimination
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
FRESENIUS MEDICAL CARE DEUTSCHLAND GmbH
ELSE-KRÖNER-STRAßE 1
61352 BAD HOMBURG V.D.H.
ALLEMAGNE
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 346 954 2 1 : 5 L en poche (Polyéthylène téréphtalate, SiOx, polyamide et polyoléfine). Boîte de 2.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Sans objet.
ANSM - Mis à jour le : 05/03/2025
MULTIBIC 4 mmol/l POTASSIUM solution pour hémodialyse/hémofiltration
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre infirmier/ère.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que MULTIBIC 4 mmol/l POTASSIUM solution pour hémodialyse/hémofiltration et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser MULTIBIC 4 mmol/l POTASSIUM solution pour hémodialyse/hémofiltration ?
3. Comment utiliser MULTIBIC 4 mmol/l POTASSIUM solution pour hémodialyse/hémofiltration ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver MULTIBIC 4 mmol/l POTASSIUM solution pour hémodialyse/hémofiltration ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE MULTIBIC 4 mmol/l POTASSIUM solution pour hémodialyse/hémofiltration ET DANS QUELS CAS EST-IL UTILISE ?
MULTIBIC 4 mmol/l POTASSIUM est une solution d’épuration extra-rénale continue pour éliminer les toxines urémiques issues du métabolisme de l’organisme chez des personnes atteintes d’une défaillance rénale aigue. Il est utilisé chez les patients présentant des lésions rénales ainsi que dans le traitement de l’intoxication médicamenteuse ou toxique. Le type de solution prescrite dépend de la quantité de potassium (un sel) dans votre sang. Votre médecin vérifiera régulièrement votre taux de potassium.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER MULTIBIC 4 mmol/l POTASSIUM solution pour hémodialyse/hémofiltration ?
N’utilisez jamais MULTIBIC 4 mmol/l POTASSIUM solution pour hémodialyse/hémofiltration:
· Si vous êtes allergique aux substances actives ou à l’un des composants contenus dans ce médicament, mentionnés dans la rubrique 6.
· Si vous avez une hyperkaliémie (votre taux de potassium est très élevé).
· Si vous êtes en alcalose métabolique (un état ou il y a trop de bicarbonate dans le sang).
· Si vous ne pouvez pas obtenir un débit sanguin suffisant à travers l’hémofiltre (filtre utilisé dans la filtration du sang).
· Si vous avez un risque élevé d'hémorragie causée par un médicament utilisé pour empêcher la coagulation dans l’hémofiltre.
Avertissements et précautions
Adressez-vous à votre médecin avant d’utiliser MULTIBIC 4 mmol/l POTASSIUM.
· Ne doit être utilisé qu’après mélange des 2 solutions dans la poche bi-compartimentée (2 compartiments)
· Ne doit pas cas être utilisé si la température de la solution est inférieure à la température ambiante.
· Les tubulures utilisées pour l'administration de la solution prête à l’emploi doivent être surveillées toutes les 30 minutes. Si un précipité (matière solide) est détecté dans ces tubulures, la poche et les tubulures doivent être immédiatement remplacées et le patient doit être soigneusement surveillé.
· Votre médecin vérifiera votre état d’hydratation (la quantité d’eau dans votre corps), les taux de potassium, de sodium, d’autres sels, de certains produits de dégradation, and votre taux de sucre dans le sang. Votre médecin vous conseillera également sur votre régime alimentaire.
Enfants
L’utilisation de MULTIBIC 4 mmol/l POTASSIUM chez les enfants n’a pas été établie.
Autres médicaments et MULTIBIC 4 mmol/l POTASSIUM solution pour hémodialyse/hémofiltration
Informez votre médecin si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
Les interactions suivantes peuvent se produire :
· Les effets toxiques des digitaliques (médicaments pour le traitement de maladies cardiaques).
· Les solutions de substitution électrolytiques, la nutrition parentérale et autres solutions de perfusion. Leur effet sur la concentration sérique dans le sang et les liquides doit être pris en considération lors de l’utilisation de ce traitement.
· Cette thérapie peut réduire la concentration sérique de certains médicaments. Un ajustement des doses peut être nécessaire.
MULTIBIC 4 mmol/l POTASSIUM solution pour hémodialyse/hémofiltration avec des aliments et boissons
Sans objet
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
Il n’existe pas ou peu de données sur l’utilisation de MULTIBIC 4 mmol/l POTASSIUM au cours de la grossesse et de l’allaitement.
Ce médicament doit être utilisé uniquement si votre médecin considère que celui-ci est nécessaire.
L’allaitement n’est pas recommandé pendant le traitement avec MULTIBIC 4 mmol/l POTASSIUM.
Conduite de véhicules et utilisation de machines
Sans objet.
MULTIBIC 4 mmol/l POTASSIUM solution pour hémodialyse/hémofiltration contient
Sans objet
3. COMMENT UTILISER MULTIBIC 4 mmol/l POTASSIUM solution pour hémodialyse/hémofiltration ?
MULTIBIC 4 mmol/l POTASSIUM sera donné à l’hôpital ou à la clinique. Votre médecin saura comment utiliser ce médicament.
Si vous avez d’autres questions sur l’utilisation de ce traitement, demandez plus d’informations à votre médecin.
Si vous avez utilisé plus de MULTIBIC 4 mmol/l POTASSIUM solution pour hémodialyse/hémofiltration que vous n'auriez dû
Sans objet.
Si vous oubliez d'utiliser MULTIBIC 4 mmol/l POTASSIUM solution pour hémodialyse/hémofiltration
Sans objet.
Si vous arrêtez d'utiliser MULTIBIC 4 mmol/l POTASSIUM solution pour hémodialyse/hémofiltration
Sans objet.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Comme tous les médicaments, ce médicament peut provoquer des effets indésirables, mais ils ne surviennent pas systématiquement chez tout le monde.
Les effets indésirables de MULTIBIC 4 mmol/l POTASSIUM incluent :
· Nausées (se sentir malade)
· Vomissement (être malade)
· Crampes musculaires
· Changement de pression sanguine
Certains effets indésirables peuvent être causés par trop ou pas assez de liquide. Ces effets sont :
· Essoufflement
· Gonflement des chevilles et jambes
· Déshydration (par exemple vertiges, crampes musculaires, sensation de soif)
· Désordres électrolytiques (par exemple une concentration anormale de sel dans le sang),
La fréquence exacte de chaque évènement est indéterminée (ne peut être estimée sur la base des données disponibles).
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: www.signalement-sante.gouv.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER MULTIBIC 4 mmol/l POTASSIUM solution pour hémodialyse/hémofiltration ?
Tenir ce médicament hors de la vue et de la portée des enfants.
Ne pas conserver à une température inférieure à 4°C.
Conditions de conservation après le mélange des 2 compartiments :
La solution prête à l'emploi ne doit pas être conservée à une température supérieure à 30°C et doit être utilisée dans un délai de 48 heures maximum.
N’utilisez pas ce médicament après la date de péremption indiquée sur la poche après EXP. La date de péremption fait référence au dernier jour de ce mois.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient MULTIBIC 4 mmol/l POTASSIUM solution pour hémodialyse/hémofiltration
· Les substances actives sont : chrorure de potassium, chlorure de sodium, bicarbonate de sodium, chlorure de calcium dihydraté, chlorure de magnésium hexahydraté, glucose monohydraté.
· Les autres ingrédients sont : eau pour injection, acide chlorhydrique 25 %, dioxyde de carbone et dihydrogénophosphate de sodium dihydraté.
Ce médicament se présente sous la forme d’une poche bi-compartimentée (deux compartiments contenant des solutions différentes). Le mélange des 2 solutions dans les compartiments résulte en la solution prête à l’emploi.
Chaque poche contient 5000 mL de solution au total. La solution prête à l’emploi est claire et incolore.
Chaque poche est équipée d’un connecteur HF, d’un connecteur Luer-Lock et d’un port d’injection, et recouverte d’un film protecteur.
Taille de l’emballage :
2 poches de 5000 mL.
Titulaire de l’autorisation de mise sur le marché
FRESENIUS MEDICAL CARE DEUTSCHLAND GmbH
ELSE-KRÖNER STRAßE 1
61352 BAD HOMBURG V.D.H.
ALLEMAGNE
Exploitant de l’autorisation de mise sur le marché
FRESENIUS MEDICAL CARE
PARC MEDICIS
47, AVENUE DES PEPINIERES
F - 94832 FRESNES CEDEX
FRESENIUS MEDICAL CARE DEUTSCHLAND GmbH
FRANKFURTER STRAßE 6-8
66606 ST. WENDEL
ALLEMAGNE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
< {MM/AAAA}>< {mois AAAA}.>
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
Les informations destinées exclusivement aux professionnels de santé se trouvent à la fin de cette notice.
Informations destinées exclusivement aux professionnels de santé :
1000 mL de la solution prête à l'emploi contiennent :
Chlorure de potassium...................................................................................................... 0,2982 g
Chlorure de sodium.............................................................................................................. 6,136 g
Bicarbonate de sodium......................................................................................................... 2,940 g
Chlorure de calcium dihydraté.............................................................................................. 0,2205 g
Chlorure de magnésium hexahydraté.................................................................................... 0,1017 g
Sous forme de glucose monohydraté.................................................................................... 1,100 g
(Glucose)........................................................................................................................... (1,000 g)
K+.................................................................................................................................. 4,0 mmol/l
Na+................................................................................................................................. 140 mmol/l
Ca2+................................................................................................................................. 1,5 mmol/l
Mg2+.............................................................................................................................. 0,50 mmol/l
Cl-.................................................................................................................................. 113 mmol/l
HCO3-.............................................................................................................................. 35 mmol/l
Glucose......................................................................................................................... 5,55 mmol/l
pH » 7,4
Osmolarité théorique (Osmol. Theor.): 300 mOsm/L
La solution prête à l’emploi ne peut être utilisée que si elle est limpide et incolore et si la poche et les connecteurs sont intacts et non endommagés.
Pour usage unique seulement. Jeter les quantités non utilisées.
Instructions concernant la manipulation et l'élimination
La solution pour hémofiltration doit être administrée en 3 étapes :
1. Retirer le suremballage et inspecter minutieusement la poche.
Le film protecteur doit être retiré seulement immédiatement avant l'utilisation de la solution.
Les poches peuvent parfois être, occasionnellement, endommagées durant le transport du fabricant au centre de soins ou dans le centre de soins lui-même. Cela peut entraîner une contamination et une prolifération microbienne ou fongique dans la solution. Il est donc nécessaire de mirer soigneusement la poche et la solution avant utilisation.
Il est indispensable de contrôler soigneusement la qualité du connecteur, des soudures ou des angles des poches.
2. Mélanger les deux compartiments
Les deux compartiments de la poche sont mélangés immédiatement avant utilisation pour obtenir la solution prête à l'emploi.
|
|
|
Déplier le petit compartiment |
|
|
|
Rouler la poche en commençant par le coin inverse au petit compartiment |
|
|
|
... Jusqu'à ouverture de la thermo-soudure sur toute sa longueur et le mélange complet des deux solutions. |
Après mélange intégral des deux solutions, vous devez vérifier l'ouverture complète de la thermo-soudure, la limpidité et la clarté de la solution, l'absence de fuite sur la poche.
3. Utilisation de la solution prête à l'emploi.
La solution prête à l’emploi doit être utilisée immédiatementou dans les 48 heures maximum après le mélange.
Tout ajout à la solution prête à l’emploi doit être réalisé seulement après avoir mélangé correctement la solution prête à l’emploi. Après ajout d'une substance, la solution prête à l’emploi doit de nouveau être correctement mélangée avant de l’utiliser.
Tout ajout de solution de chlorure de sodium (jusqu’à 30 %) ou alternativement d’eau pour préparation injectable sont compatibles avec ce médicament et peuvent être utilisées pour ajuster la concentration en sodium si besoin dans le but de limiter les variations rapides de la concentration en sodium dans le cas d’hyper ou hyponatrémie grave.
Pour plus de détails merci de vous référer au Résumé des Caractéristiques du Produit.
Sauf indication contraire, la solution prête à l'emploi doit être réchauffée à 36,5°C - 38,0°C, immédiatement avant la perfusion. La température exacte doit être déterminée en fonction des besoins cliniques et de l'équipement utilisé.