Dernière mise à jour le 08/01/2026
BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose
Ce médicament n'est ou ne sera bientôt plus disponible sur le marché.
Si vous prenez actuellement ce médicament, il vous est recommandé d'en parler avec votre médecin
ou avec votre pharmacien qui pourra vous orienter vers un autre traitement.
Indications thérapeutiques
Classe pharmacothérapeutique : AGONISTES SELECTIFS BETA 2 ADRENERGIQUES
Code ATC : R03AC03
Ce médicament est un bêta2 mimétique à action rapide et de courte durée.
C'est un broncho-dilatateur (il augmente le calibre des bronches).
Il s'administre par voie inhalée à l'aide d'un appareil pour nébulisation (nébuliseur).
L'usage de ce médicament par ce mode d'administration doit être réservé au traitement des crises d'asthme graves et des poussées aiguës au cours de la bronchite chronique obstructive, lorsque ces situations nécessitent l'inhalation de fortes doses.
BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose ne doit pas être utilisé seul pour le traitement régulier de l’asthme ou d’autres problèmes respiratoires. Si vous utilisez BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose tous les jours, votre médecin devrait également vous avoir prescrit un autre type de médicament comme des corticoïdes inhalés qui aident à réduire le gonflement et l’inflammation dans vos poumons.
Présentations
> 20 récipient(s) unidose(s) polyéthylène suremballée(s)/surpochée(s) de 2 ml
Code CIP : 365 732-1 ou 34009 365 732 1 5
Déclaration d'arrêt de commercialisation : 29/05/2025
Cette présentation n'est pas agréée aux collectivités
- Prix hors honoraire de dispensation : 5,40 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 6,42 €
- Taux de remboursement :65%
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 30/11/2016 | Inscription (CT) | Le service médical rendu par BRICANYL 5 mg/2 ml, solution pour inhalation par nébuliseur en récipient unidose est important dans les indications de l’AMM. |
| Important | Avis du 16/03/2016 | Renouvellement d'inscription (CT) | Le service médical rendu par BRICANYL TURBUHALER 500 µg/dose reste important dans : • le traitement symptomatique de la crise d’asthme. • le traitement symptomatique des exacerbations au cours de la maladie asthmatique ou de la bronchite chronique obstructive lorsqu’’il existe une composante réversible. • la prévention de l’asthme d’effort. • le test de réversibilité de l’obstruction bronchique lors des explorations fonctionnelles respiratoires. Le service médical rendu par BRICANYL 5 mg/2 ml reste important dans : • le traitement symptomatique des asthmes aigus graves. • le traitement des poussées aiguës des broncho-pneumopathies chroniques obstructives de l’adulte. Le service médical rendu par BRICANYL 0,5 mg/1 ml, solution injectable en ampoule, reste important dans : • le traitement symptomatique de l’asthme aigu grave de l’adulte et de l’enfant de plus de 2 ans par voie S.C. • le traitement de l’asthme aigu grave de l’adulte (état de mal asthmatique). |
| Insuffisant | Avis du 16/03/2016 | Renouvellement d'inscription (CT) | Le service médical rendu par BRICANYL 0,5 mg/1 ml, solution injectable en ampoule, reste insuffisant dans le traitement à court terme du travail prématuré sans complication. |
| Modéré | Avis du 16/03/2016 | Renouvellement d'inscription (CT) | Le service médical rendu par BRICANYL LP 5 mg, comprimé à libération prolongée, reste modéré. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 30/11/2016 | Inscription (CT) | Cette spécialité est un complément de gamme qui n’apporte pas d’amélioration du service médical rendu (ASMR V) par rapport à la présentation déjà inscrite. |
Autres informations
- Titulaire de l'autorisation : ASTRAZENECA
- Conditions de prescription et de délivrance :
- liste I
- prescription réservée aux spécialistes et services PEDIATRIE
- prescription réservée aux spécialistes et services PNEUMOLOGIE
- réservé à l'usage en situation d'urgence selon l'article R5121-96 du code de la santé publique
- réservé à une structure d'assistance médicale mobile ou de rapatriement sanitaire
- Statut de l'autorisation : Valide
- Type de procédure : Procédure nationale
- Code CIS : 6 824 217 7
ANSM - Mis à jour le : 25/09/2023
BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Sulfate de terbutaline ............................................... ...................................................... 5,0 mg
Pour un flacon de 2 mL
Pour la liste complète des excipients, voir rubrique 6.1.
4.1. Indications thérapeutiques
· Traitement symptomatique des asthmes aigus graves.
· Traitement des poussées aiguës des bronchopneumopathies chroniques obstructives de l’adulte.
en association avec un traitement anti-inflammatoire continu comme les corticoïdes inhalés ou les antagonistes du récepteur aux leucotriènes.
Remarque : l’asthme aigu grave nécessite une hospitalisation en unité de soins intensifs.
Une oxygénothérapie et une corticothérapie par voie systémique doivent être associées au traitement bronchodilatateur.
4.2. Posologie et mode d'administration
Adulte : 5 mg à 10 mg soit 1 à 2 doses de 2 mL par nébulisation
Enfant et nourrisson : 0,1 à 0,2 mg/kg par nébulisation
Toute dose entamée doit être utilisée dans les 24 heures.
La nébulisation peut être renouvelée toutes les 20 à 30 minutes en fonction du résultat clinique et de la tolérance du traitement.
Mode d’administration
Cette solution de terbutaline doit être administrée par voie inhalée à l’aide d’un appareil pour nébulisation (nébuliseur).
NE PAS INJECTER - NE PAS AVALER
Se conformer au mode d’emploi de l’appareil utilisé.
Diluer la quantité nécessaire de terbutaline dans du sérum physiologique de façon à obtenir un volume total de 4 à 5 mL.
Le mélange obtenu est pulsé par un débit d’air ou d’oxygène (6 à 8 litres/minutes) pendant environ 10 à 15 minutes durant lesquelles le patient respire à son rythme habituel.
La technique d’utilisation par le patient doit être vérifiée régulièrement.
Après inhalation, la solution inutilisée restant dans la cuve de l’appareil doit être jetée.
· Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
4.4. Mises en garde spéciales et précautions d'emploi
L’administration de terbutaline à l’aide d’un nébuliseur doit être réservée aux situations aiguës graves nécessitant l’inhalation d’une posologie élevée de produit par voie inhalée.
Ces situations nécessitent une surveillance médicale avec possibilité de mise en place d’une réanimation (abord veineux et assistance respiratoire) ; une oxygénothérapie et corticothérapie par voie systémique doivent généralement y être associées.
Il est nécessaire d'associer un traitement anti-inflammatoire continu comme les corticoïdes inhalés ou les antagonistes du récepteur aux leucotriènes chez les patients avec un asthme persistant pour lesquels un traitement continu par bêta2 mimétiques est requis.
Les patients doivent être informés qu’ils doivent poursuivre le traitement de fond anti-inflammatoire qui leur a été est prescrit même si les symptômes et leur utilisation de BRICANYL 5mg/2 mL en solution pour inhalation par nébuliseur diminuent. Une diminution de la réponse habituellement obtenue sur les symptômes avec le traitement est le signe d’une aggravation de l’asthme qui nécessite une consultation médicale afin de réévaluer le traitement de l’asthme.
L'utilisation excessive de bêta-agonistes de courte durée d'action peut masquer la progression de la maladie sous-jacente et contribuer à la détérioration du contrôle de l'asthme, entraînant un risque accru d'exacerbations sévères d’asthme et de mortalité.
En cas d’utilisation de terbutaline en traitement de secours « à la demande » plus de deux fois par semaine, le traitement de fond doit être réévalué et ajusté en raison du risque d’utilisation excessive de terbutaline.
L'attention des sportifs sera attirée sur le fait que cette spécialité contient un principe actif pouvant induire une réaction positive des tests pratiqués lors de contrôles antidopage.
Des effets cardiovasculaires peuvent être observés avec les médicaments sympathomimétiques, y compris BRICANYL. Les cas issus de la littérature et de l’expérience post-commercialisation ont mis en évidence la survenue de rares cas d’ischémie myocardique en lien avec l’utilisation des bêta2-mimétiques. Les patients traités par BRICANYL et présentant des pathologies cardiaques sévères (cardiopathie ischémique, arythmie ou insuffisance cardiaque sévère) doivent être informés de prendre un avis médical s’ils ressentent une douleur thoracique ou tout autre symptôme témoignant d’une aggravation de leur pathologie cardiaque. Une attention particulière doit être apportée aux symptômes tels qu’une dyspnée ou une douleur thoracique car ceux-ci peuvent être d’origine respiratoire ou cardiaque.
Précautions particulières d’emploi
En cas d’infection bronchique ou de bronchorrhée abondante, un traitement approprié est nécessaire afin de favoriser la diffusion optimale du produit dans les voies respiratoires.
Ce médicament doit être administré avec prudence en cas d’hyperthyroïdie, en cas d’affection cardiovasculaire, notamment cardiomyopathie obstructive, troubles coronariens, troubles du rythme, hypertension artérielle, et en cas de diabète sucré.
Les bêta-2-mimétiques à forte dose peuvent être à l’origine d’une hypokaliémie pouvant favoriser la survenue de troubles du rythme cardiaque. Une surveillance de la kaliémie est recommandée dans la mesure du possible, en particulier lors de l’administration simultanée de thérapeutiques hypokaliémiantes, en cas d’hypoxie ou chez les sujets chez qui le risque de survenue de torsades de pointes est majoré (QT long ou traitements susceptibles d’augmenter le QTc).
Les bêta-bloquants (y compris ceux sous forme de collyres) peuvent inhiber partiellement ou totalement l’effet des bêta2stimulants.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
+ Halothane
En cas d’intervention obstétricale, majoration de l'inertie utérine avec risque hémorragique ; par ailleurs, risque de survenue de troubles du rythme ventriculaire graves, par augmentation de la réactivité cardiaque.
Interrompre le traitement par bêta-2 mimétiques si l'anesthésie doit se faire sous halothane.
Associations faisant l'objet de précautions d’emploi
+ Antidiabétiques
Elévation de la glycémie par effet bêta-stimulant.
Renforcer la surveillance sanguine et urinaire. Passer éventuellement à l'insuline.
+ Agents entrainant une déplétion potassique
En raison de l'effet hypokaliémiant des bêta2‑mimétiques, l'administration concomitante d’agents entraînant une déplétion potassique connus pour aggraver le risque d'hypokaliémie, comme les diurétiques, la digoxine, les méthyl‑xanthines et les corticostéroïdes doit être effectuée avec prudence après une évaluation minutieuse des bénéfices et des risques avec une attention particulière pour l'augmentation du risque d'arythmies cardiaques résultant d'une hypokaliémie (voir rubrique 4.4). L’hypokaliémie prédispose également à la toxicité de la digoxine.
4.6. Fertilité, grossesse et allaitement
Grossesse
En clinique, il existe un recul important, avec un nombre suffisant de grossesses documentées, pour que l’on puisse conclure à l’innocuité de la terbutaline pendant la grossesse.
En conséquence, la terbutaline par voie inhalée peut être administrée en cas de grossesse.
Lors de l’administration pendant la grossesse :
Une accélération du rythme cardiaque foetal peut être observée parallèlement à la tachycardie maternelle. Il est exceptionnel de la voir persister à la naissance.
De même, les valeurs de la glycémie post-natale ne sont qu’exceptionnellement perturbées.
BRICANYL 5 mg/2 mL en solution pour inhalation par nébuliseur, utilisé dans le traitement de l’asthme et des autres pathologies pulmonaires, est un agent tocolytique et doit donc être utilisé avec prudence en fin de grossesse.
En cas d’administration avant accouchement tenir compte de l’effet vasodilatateur périphérique des bêta2 mimétiques.
Les bêta2 mimétiques passent dans le lait maternel.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
La gravité des effets indésirables dépend du dosage et de la voie d’administration. La terbutaline prescrite en inhalation est peu probable de produire des effets systémiques significatifs en administration aux doses recommandées. La plupart de ces effets sont caractéristiques des amines sympathomimétiques. La majorité de ces effets ont été spontanément réversibles au cours des deux premières semaines de traitement.
|
Fréquence |
Classe de Système d’Organe |
Effets indésirables |
|
Très fréquents (> 1/10) |
Affections du système nerveux |
Céphalées Tremblements des extrémités |
|
Fréquents (< 1/1000 et > 1/100) |
Affections cardiaques |
Tachycardie Palpitations |
|
Affections musculo- squelettiques et systémiques |
Crampes musculaires |
|
|
Troubles du métabolisme et de la nutrition |
Hypokaliémie, augmentation de la glycémie |
|
|
Rares (< 1/1000 et > 1/10000) |
Affections du métabolisme et de la nutrition |
Acidose lactique |
|
Indéterminée* |
Affections cardiaques |
Troubles du rythme cardiaque, en particulier fibrillation auriculaire, tachycardie supraventriculaire et extrasystoles auriculaires ou ventriculaires, ischémie myocardique |
|
Affections gastro-intestinales |
Nausées |
|
|
Affections psychiatriques |
Troubles du sommeil et troubles du comportement : agitation, nervosité, hyperactivité |
|
|
Affections respiratoires, thoraciques et médiastinales |
Bronchospasme**, toux** |
|
|
Affections de la peau et tissu sous-cutané |
Éruption cutanée érythémateuse, urticaire, exanthème |
* Signalé spontanément dans les données post-commercialisation ; la fréquence est donc considérée comme indéterminée.
** Comme avec d’autres produits inhalés, possibilité de survenue de toux et rarement de bronchospasme paradoxal à la suite de l’inhalation du produit. Dans ce cas, il conviendra d’interrompre ce traitement et de prescrire d’autres thérapeutiques ou d’autre forme d’administration.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
En cas de surdosage : sont majorés le risque de tachycardie et arythmie cardiaque, modifications tensionnelles, tremblements, sueurs, agitation, nausées, hypokaliémie.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : AGONISTES SELECTIFS BETA 2 ADRENERGIQUES
Code ATC : R03AC03.
Bronchodilatateur bêta2 mimétique à action rapide et de courte durée par voie inhalée.
La terbutaline est un agoniste sélectif des récepteurs bêta2.
Après inhalation, la terbutaline exerce une action stimulante sur les récepteurs bêta2 du muscle lisse bronchique assurant ainsi une bronchodilatation rapide, significative en quelques minutes, persistant pendant 4 à 6 heures.
5.2. Propriétés pharmacocinétiques
Après nébulisations répétées, les concentrations plasmatiques observées aux doses thérapeutiques ne sont pas négligeables mais restent inférieures à celles observées per os ou en injection.
Il n’y a pas de corrélation entre le taux sanguin et la courbe d’efficacité.
Après résorption pulmonaire, la terbutaline est faiblement liée aux protéines plasmatiques.
Elle est métabolisée dans le foie en dérivés sulfo et conjugués, éliminés dans les urines.
5.3. Données de sécurité préclinique
Chlorure de sodium, édétate de sodium, acide chlorhydrique, eau pour préparations injectables.
Sans objet.
Avant ouverture du sachet : 3 ans.
Après ouverture du sachet : 3 mois.
6.4. Précautions particulières de conservation
A conserver à une température inférieure à 25°C et à l'abri de la lumière.
Une fois le sachet protecteur ouvert, les doses doivent être maintenues dans le sachet et utilisées dans les trois mois. Notez en clair la date d'ouverture du sachet.
La dose entamée doit être utilisée dans les 24 heures.
6.5. Nature et contenu de l'emballage extérieur
2 mL en récipient unidose (PE). Sachet (Aluminium/Polyéthylène/Polyester) de cinq récipients unidoses.
6.6. Précautions particulières d’élimination et de manipulation
Pas d’exigences particulières
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
ASTRAZENECA
TOUR CARPE DIEM
31 PLACE DES COROLLES
92400 COURBEVOIE
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 365 732 1 5 : 2 mL en récipient unidose (PE), boîte de 20.
· 34009 366 675 1 8 : 2 mL en récipient unidose (PE), boîte de 25.
· 34009 365 733 8 3 : 2 mL en récipient unidose (PE), boîte de 50.
· 34009 365 734 4 4 : 2 mL en récipient unidose (PE), boîte de 100.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
<{JJ mois AAAA}>
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I.
Médicament à prescription réservée aux spécialistes en pneumologie ou en pédiatrie. Médicament pouvant être administré par tout médecin intervenant en situation d’urgence ou dans le cadre d’une structure d’assistance médicale ou de rapatriement sanitaire (article R 5121-96 du code de la santé publique)
Ce médicament n'est ou ne sera bientôt plus disponible sur le marché.
Si vous prenez actuellement ce médicament, il vous est recommandé d'en parler avec votre médecin
ou avec votre pharmacien qui pourra vous orienter vers un autre traitement.
ANSM - Mis à jour le : 25/09/2023
BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose
Sulfate de terbutaline
Veuillez lire attentivement cette notice avant d’utiliser ce médicament car elle contient des informations importantes pour vous.
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose ?
3. Comment utiliser BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : AGONISTES SELECTIFS BETA 2 ADRENERGIQUES
Code ATC : R03AC03
Ce médicament est un bêta2 mimétique à action rapide et de courte durée.
C'est un broncho-dilatateur (il augmente le calibre des bronches).
Il s'administre par voie inhalée à l'aide d'un appareil pour nébulisation (nébuliseur).
L'usage de ce médicament par ce mode d'administration doit être réservé au traitement des crises d'asthme graves et des poussées aiguës au cours de la bronchite chronique obstructive, lorsque ces situations nécessitent l'inhalation de fortes doses.
BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose ne doit pas être utilisé seul pour le traitement régulier de l’asthme ou d’autres problèmes respiratoires. Si vous utilisez BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose tous les jours, votre médecin devrait également vous avoir prescrit un autre type de médicament comme des corticoïdes inhalés qui aident à réduire le gonflement et l’inflammation dans vos poumons.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose ?
N’utilisez jamais BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose :
· si vous êtes allergique à la terbutaline ou à l’un des autres composants contenus dans ce médicament, mentionnés à la rubrique 6.
En cas de survenue de majoration de la gêne respiratoire à la suite de l’inhalation de ce produit, il est préférable de ne pas renouveler la prise de ce médicament, signalez le au médecin.
EN CAS DE DOUTE, IL EST INDISPENSABLE DE DEMANDER L'AVIS DE VOTRE MEDECIN.
Avertissements et précautions
Mises en garde spéciales
EN CAS DE DOUTE NE PAS HESITER A DEMANDER L’AVIS DE VOTRE MEDECIN.
Précautions d’emploi
Ce produit, actif en inhalation doit atteindre l’extrémité des petites bronches. En cas d’encombrement (par des mucosités abondantes) ou d’infection, son efficacité peut être diminuée. Un traitement adapté sera instauré en complément.
En cas de maladie du coeur, de maladie de la glande thyroïde, d’hypertension artérielle, de diabète, prévenir le médecin afin qu’il détermine les modalités de prescription et de surveillance les plus adaptées à votre cas.
NE JAMAIS LAISSER A LA PORTEE DES ENFANTS.
Enfants et adolescents
Sans objet.
Autres médicaments et BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose
AFIN D'EVITER D'EVENTUELLES INTERACTIONS ENTRE PLUSIEURS MEDICAMENTS IL FAUT SIGNALER SYSTEMATIQUEMENT TOUT AUTRE TRAITEMENT EN COURS A VOTRE MEDECIN OU A VOTRE PHARMACIEN, en particulier les antidiabétiques oraux.
BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose avec des aliments et des boissons
Sans objet.
Ce médicament dans les conditions normales d’utilisation, peut être utilisé, pendant la grossesse
BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose, lorsqu’il est utilisé tous les jours et non en cas de besoin, doit être utilisé avec prudence en fin de grossesse car il provoque un relâchement de l’utérus.
En cas de grossesse ou d’allaitement demander conseil à votre médecin.
Sportifs
Sportifs, attention cette spécialité contient un principe actif pouvant induire une réaction positive des tests pratiqués lors des contrôles antidopage.
Conduite de véhicules et utilisation de machines
Sans objet.
BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose contient :
Sans objet.
3. COMMENT UTILISER BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose ?
Adulte : 5 mg à 10 mg soit 1 à 2 doses par nébulisation
Enfant et nourrisson : 0,1 à 0,2 mg/kg par nébulisation
Mode d’administration
Voie inhalée exclusivement.
NE PAS INJECTER - NE PAS AVALER
Cette solution de terbutaline doit être administrée par voie inhalée à l’aide d’un appareil pour nébulisation (nébuliseur). La nébulisation est une technique d’inhalation qui fait appel à un appareil générateur d’aérosol utilisant de l’air comprimé ou de l’oxygène (6 à 8 litres/minutes).
L’appareillage complet se compose :
· d’une source de pression, le compresseur, qui sert à pulvériser la suspension médicamenteuse,
· du nébuliseur proprement dit, récipient en plastique dans lequel on verse la suspension à nébuliser,
· d’un masque facial, relié au nébuliseur par une tubulure à adapter au visage du patient ou d’un embout buccal.
L’efficacité de ce médicament est en partie dépendante du bon usage de l’appareil de nébulisation. Il convient donc de lire très attentivement le mode d’emploi de l’appareil.
1ère étape : préparation
|
|
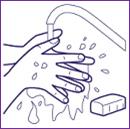
1. Se laver les mains avec de l’eau et du savon.
|
|
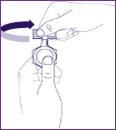
2. Prendre une unidose de BRICANYL Solution pour inhalation par nébuliseur. |
|
|
3. Ouvrir l’unidose
|
|
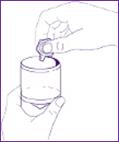
4. Verser la quantité prescrite dans la cuve du nébuliseur. |
Si nécessaire, en fonction du volume de la cuve, le produit peut être dilué dans le sérum physiologique stérile.
2ème étape : pendant la nébulisation
|
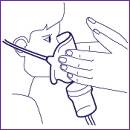
5. Serrez l’embout buccal entre les lèvres ou adapter le masque sur le visage (pour les enfants). 6. Mettre l’appareil en marche 7. Respirez au rythme habituel. La nébulisation ne devra pas excéder 10 à 15 mn.
|
3ème étape : après la nébulisation
|
|
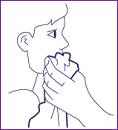
8. Ne pas oublier de rincer à l’eau la bouche et son pourtour. 9. Après inhalation, la solution inutilisée restant dans la cuve du nébuliseur doit être jetée.
|
|
|
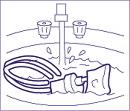
10. Laver à l’eau savonneuse le réservoir du nébuliseur et le masque.
|
|
11. Rincer puis sécher le tout soigneusement.
|
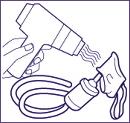
12. Nettoyer régulièrement la tubulure et le filtre à air d’arrivée au compresseur.
Après chaque utilisation, pensez à l’entretien du matériel.
Une dose unitaire entamée doit être utilisée dans les 24 heures.
Fréquence d'administration
En milieu hospitalier, la nébulisation peut être renouvelée toutes les 20 à 30 minutes si nécessaire en fonction du résultat clinique.
BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur doit être utilisé selon les besoins plutôt que régulièrement.
Consultez immédiatement un médecin si vos symptômes d’asthme (toux, essoufflement, respiration sifflante ou oppression thoracique) s’aggravent ou si vous vous sentez trop essoufflé quand vous parlez, mangez ou dormez.
Vous devez contacter votre médecin dès que possible si vous avez besoin de doses de BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur plus élevées que d’habitude pour soulager vos problèmes respiratoires. Vous pourriez alors avoir besoin de médicaments supplémentaires pour contrôler votre asthme.
Si vous utilisez BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur plus de deux fois par semaine pour traiter vos symptômes d’asthme, cela indique un asthme mal contrôlé et une augmentation du risque de crises sévères d’asthme (aggravation de l’asthme) et de graves complications pouvant mettre en jeu le pronostic vital ou même être fatales. Vous devez contacter votre médecin dès que possible pour réévaluer votre traitement de l’asthme.
Si vous utilisez quotidiennement un médicament contre l’inflammation des poumons, par exemple un « corticoïde inhalé », il est important de continuer à l’utiliser régulièrement, même si vous vous sentez mieux.
Si vous avez utilisé plus de BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose que vous n’auriez dû
Sans objet.
Si vous oubliez d’utiliser BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose
Si vous arrêtez d’utiliser BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose
Sans objet.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Les effets suivants peuvent être observés aux doses thérapeutiques :
· Très fréquemment : tremblements des extrémités, maux de tête
· Fréquemment : Tachycardie, palpitations, crampes musculaires, diminution du taux de potassium dans le sang ou augmentation transitoire de la glycémie
· Fréquence indéterminée* : Troubles du rythme cardiaque, nausées, agitation, nervosité, hyperactivité, toux ou bronchospasme, troubles du sommeil, urticaire, éruption cutanée/rougeur de la peau.
* Signalé spontanément dans les données post-commercialisation ; la fréquence est donc considérée comme indéterminée.
Comme avec d'autres produits inhalés, rarement possibilité de survenue de toux ou de majoration de la gêne respiratoire à la suite de l'inhalation du produit. Dans ce cas ce traitement devra être interrompu et une autre thérapeutique devra être envisagée.
EN CAS DE DOUTE NE PAS HESITER A PREVENIR LE MEDECIN.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur le conditionnement extérieur. La date de péremption fait référence au dernier jour de ce mois.
Ce médicament doit être conservé à une température inférieure à 25°C et à l'abri de la lumière.
Une fois le sachet protecteur ouvert, les doses doivent être maintenues dans le sachet et utilisées dans les trois mois. Notez en clair la date d’ouverture du sachet.
La dose entamée doit être utilisée dans les 24 heures.
Si nécessaire, mises en garde contre certains signes visibles de détérioration :
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient BRICANYL 5 mg/2 mL, solution pour inhalation par nébuliseur en récipient unidose
· La substance active est :
Sulfate de terbutaline ............................................................................................................ 5,0 mg
Pour un flacon
· Les autres composants sont :
Chlorure de sodium, édétate de sodium, acide chlorhydrique, eau pour préparations injectables.
Ce médicament se présente sous forme de solution pour inhalation par nébuliseur. Boîte de 20, 25, 50 ou 100 récipients unidoses de 2 mL.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
TOUR CARPE DIEM
31 PLACE DES COROLLES
92400 COURBEVOIE
Exploitant de l’autorisation de mise sur le marché
ASTRAZENECA
TOUR CARPE DIEM
31 PLACE DES COROLLES
92400 COURBEVOIE
FORSKARGATAN 18
SE-151 36 SÖDERTÄLJE
SUEDE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
< {MM/AAAA}>< {mois AAAA}.>
Sans objet.
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).