Dernière mise à jour le 28/04/2026
VISTABEL 4 UNITES ALLERGAN/0,1 ml, poudre pour solution injectable
Indications thérapeutiques
VISTABEL est un myorelaxant d'action périphérique.
VISTABEL agit en bloquant les impulsions nerveuses dirigées vers tous les muscles dans lesquels il a été injecté. Ceci empêche les muscles de se contracter en entraînant une paralysie temporaire et réversible.
VISTABEL est utilisé, chez l’adulte, pour l’amélioration temporaire de l’apparence des rides suivantes :
· des rides verticales situées entre les sourcils, observées lors du froncement des sourcils et/ou,
· des rides en forme d’éventail (pattes d'oie) situées au coin des yeux observées lors d’un sourire forcé et/ou,
· des rides du front observées lors du haussement des sourcils,
lorsque la sévérité des rides du visage entraîne un retentissement psychologique important.
Présentations
> 1 flacon(s) en verre de 50 UI
Code CIP : 364 696-1 ou 34009 364 696 1 7
Déclaration de commercialisation : 22/11/2004
Cette présentation n'est pas agréée aux collectivités
> 1 flacon(s) en verre de 100 UI
Code CIP : 34009 301 622 5 5
Déclaration de commercialisation : 02/05/2019
Cette présentation n'est pas agréée aux collectivités
Service médical rendu (SMR)
Pas de SMR disponible pour ce médicament ( plus d'informations dans l'aide )
Amélioration du service médical rendu (ASMR)
Pas d'ASMR disponible pour ce médicament (plus d'informations dans l'aide )
Autres informations
- Titulaire de l'autorisation : ABBVIE
- Conditions de prescription et de délivrance :
- liste I
- prescription réservée aux spécialistes et services CHIRURGIE DE LA FACE ET DU COU
- prescription réservée aux spécialistes et services CHIRURGIE MAXILLO-FACIALE
- prescription réservée aux spécialistes et services CHIRURGIE PLASTIQUE, RECONSTRUCTRICE ET ESTHETIQUE
- prescription réservée aux spécialistes et services DERMATOLOGIE
- prescription réservée aux spécialistes et services OPHTALMOLOGIE
- réservé à l'usage professionnel selon l'article R.5121-80 du code de la santé publique
- Statut de l'autorisation : Valide
- Type de procédure : Procédure de reconnaissance mutuelle
- Code CIS : 6 815 077 5
ANSM - Mis à jour le : 02/02/2026
VISTABEL 4 UNITÉS ALLERGAN / 0,1 ml, poudre pour solution injectable
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Toxine botulinique de type A*........................ 4 Unités ALLERGAN par 0,1 ml de solution reconstituée
* (de Clostridium botulinum)
Les Unités ALLERGAN ne sont pas interchangeables avec les autres préparations de toxine botulinique
Flacon de 50 Unités.
Flacon de 100 Unités.
Pour la liste complète des excipients, voir rubrique 6.1.
Poudre pour solution injectable.
Poudre blanche.
VISTABEL se présente sous la forme d'un fin dépôt blanc qui peut être difficile à voir dans le fond du flacon.
4.1. Indications thérapeutiques
VISTABEL est indiqué dans l’amélioration temporaire de l’apparence :
· des rides verticales intersourcilières modérées à sévères observées lors du froncement maximal des sourcils (rides glabellaires) et/ou,
· des rides canthales latérales modérées à sévères (pattes d’oie) observées lors d’un sourire forcé et/ou,
· des rides du front modérées à sévères observées lors de l’élévation maximale des sourcils,
lorsque la sévérité des rides du visage entraîne un retentissement psychologique important chez les patients adultes.
4.2. Posologie et mode d'administration
Veuillez-vous référer aux recommandations spécifiques pour chaque indication ci-dessous.
Les doses de toxine botulinique ne sont pas interchangeables d’un produit à un autre. Les doses recommandées en Unités ALLERGAN diffèrent des autres préparations de toxine botulinique.
Patients âgés
Les données cliniques de phase 3 avec VISTABEL sont limitées chez les patients âgés de plus de 65 ans (voir rubrique 5.1).
Aucun ajustement posologique particulier n’est requis chez les personnes âgées.
Population pédiatrique
Chez les sujets de moins de 18 ans, la sécurité et l’efficacité de VISTABEL dans le traitement des rides glabellaires modérées à sévères observées lors du froncement des sourcils, des rides canthales latérales modérées à sévères observées lors d’un sourire forcé ou des rides du front observées lors de l’élévation maximale des sourcils n’ont pas été démontrées.
L’utilisation de VISTABEL n’est pas recommandée chez les personnes de moins de 18 ans (voir rubrique 4.4).
Mode d’administration
Le traitement par VISTABEL doit être administré par des médecins ayant les qualifications adéquates, ayant une bonne expérience du traitement et utilisant le matériel approprié.
VISTABEL, après reconstitution, ne doit être utilisé que pour une seule séance d’injection(s) par patient.
L’excédent de produit non utilisé doit être éliminé conformément à la rubrique 6.6. Des précautions particulières doivent être prises pour la préparation et l’administration du produit ainsi que pour l’inactivation et l’élimination de la solution reconstituée non utilisée (voir rubriques 4.4 et 6.6).
Le volume d’injection recommandé par site musculaire est de 0,1 ml. Voir également le tableau de dilution rubrique 6.6.
Pour les instructions concernant l’utilisation, la manipulation et l’élimination des flacons, voir rubrique 6.6.
Une attention particulière doit être portée afin de s’assurer que VISTABEL ne soit pas injecté dans un vaisseau sanguin, lors de son injection dans les rides verticales intersourcilières (dites rides glabellaires) observées lors du froncement des sourcils, ou dans les rides canthales latérales (dites de la patte d’oie) observées lors d’un sourire forcé ou dans les rides du front observées lors de l’élévation maximale des sourcils (voir rubrique 4.4).
L’intervalle entre deux traitements ne doit pas être inférieur à trois mois.
Instructions d’administration pour les rides glabellaires observées lors du froncement des sourcils
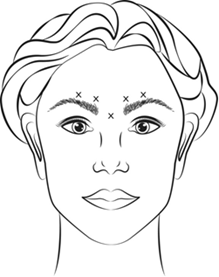
VISTABEL, après reconstitution (50 Unités/1,25 ml ou 100 Unités/2,5 ml), est injecté à l’aide d’une aiguille stérile de 30 gauges. On injecte 0,1 ml (4 Unités) dans chacun des 5 sites d’injection (voir figure 1) : deux injections dans chaque muscle corrugator et une injection dans le muscle procerus, soit une dose totale de 20 Unités.
Avant injection, le pouce ou l’index doit être placé fermement sous le rebord orbitaire afin d’éviter l’extravasation sous le rebord orbitaire. L’aiguille devra être orientée vers le haut et vers la ligne médiane lors de l’injection. Afin de réduire les risques de ptôse de la paupière, la dose maximum de 4 Unités par site d’injection ainsi que le nombre de sites d’injection ne doivent pas être dépassés. De plus, les injections à proximité du muscle releveur de la paupière supérieure doivent être évitées, en particulier chez les patients dotés d'importants complexes musculaires abaisseurs des sourcils (depressor supercilii). Les injections dans le muscle corrugator doivent être faites dans la partie centrale de ce muscle, à une distance d’au moins un centimètre au-dessus de l’arcade sourcilière.
Figure 1 :
Une amélioration de la sévérité des rides glabellaires, observées lors du froncement des sourcils, apparaît, en général, en une semaine après le traitement. L’effet du traitement a été démontré jusqu'à 4 mois après injection.
Instructions d’administration pour les rides canthales latérales observées lors d’un sourire forcé
VISTABEL, après reconstitution (50 Unités/1,25 ml ou 100 Unités/2,5 ml), est injecté à l’aide d’une aiguille stérile de 30 gauges. On injecte 0,1 ml (4 Unités) dans chacun des 3 sites d’injection (6 sites d’injection au total) dans le muscle oculaire orbiculaire latéral, soit une dose totale de 24 Unités dans un volume total de 0,6 ml (12 Unités par côté).
Afin de réduire les risques de ptôse de la paupière, la dose maximum de 4 Unités par site d’injection ainsi que le nombre de sites d’injection ne doivent pas être dépassés. De plus, les injections devront être faites de façon temporale par rapport à l’orbite, en s’assurant de respecter une distance de sécurité par rapport au muscle contrôlant l’élévation de la paupière.
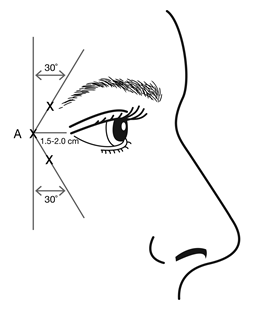
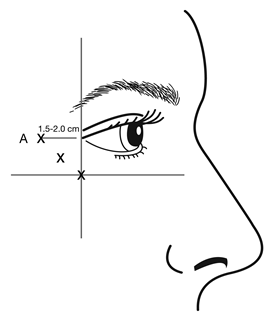
Les injections doivent être administrées avec le biseau de l’aiguille vers le haut et orientées à l’opposé de l’œil. La première injection (A) doit être effectuée à environ 1,5 à 2,0 cm de façon temporale au canthus latéral et juste temporale à l’orbite. Si les rides de la région de la patte d’oie se situent au-dessus et en-dessous du canthus latéral, injecter tel que schématisé dans la figure 2. Sinon, si les rides de la région de la patte d’oie se situent principalement sous le canthus latéral, injecter tel que schématisé dans la figure 3.
|
Figure 2 : |
Figure 3 : |
|
|
|
Pour un traitement simultané des rides glabellaires et de la patte d’oie, la dose est de 24 Unités pour les rides de la patte d’oie observées lors d’un sourire forcé et de 20 Unités pour les rides glabellaires observées lors du froncement des sourcils (voir Instructions d’administration pour les rides glabellaires, et figure 1), pour une dose totale de 44 Unités dans un volume total de 1,1 ml.
L’amélioration de la sévérité des rides de la patte d’oie observées lors d’un sourire forcé, telle qu’évaluée par l’investigateur est survenue en une semaine après le traitement. L’effet a été démontré pendant une durée médiane de 4 mois après l’injection.
Instructions d’administration pour les rides du front observées lors de l’élévation maximale des sourcils
VISTABEL, après reconstitution (50 Unités/1,25 ml ou 100 Unités/2,5 ml) est injecté à l’aide d’une aiguille stérile de 30 gauges. On injecte 0,1 ml (4 Unités) dans chacun des 5 sites d’injection dans le muscle frontal, soit une dose totale de 20 Unités dans un volume total de 0,5 ml (voir figure 4).
La dose totale pour le traitement simultané des rides du front (20 Unités) et des rides glabellaires (20 Unités) est de 40 Unités/1,0 ml.
Pour déterminer l’emplacement des sites d'injection appropriés dans le muscle frontal, le rapport entre la taille du front du patient et la répartition de l’activité du muscle frontal doit être évalué.
Les lignes horizontales de traitement, listées ci-dessous, doivent être localisées en palpant légèrement le front au repos et lors de l’élévation maximale des sourcils :
· Bord supérieur de l’activité du muscle frontal : environ 1 cm au-dessus du pli supérieur du front
· Ligne inférieure de traitement : à mi-distance entre le bord supérieur de l’activité du muscle frontal et le sourcil, au moins 2 cm au-dessus du sourcil
· Ligne supérieure de traitement : à mi-distance entre le bord supérieur de l’activité du muscle frontal et la ligne inférieure de traitement
Les 5 injections doivent être pratiquées à l’intersection des lignes de traitement horizontales et des repères verticaux suivants :
· Sur la ligne inférieure de traitement, au niveau de la ligne médiane du visage et à 0,5 - 1,5 cm du milieu de la ligne de fusion temporale (crête temporale) repérée par palpation; recommencez pour l’autre côté.
· Sur la ligne supérieure de traitement, à mi-distance entre les sites latéral et médian de la ligne inférieure de traitement ; recommencez pour l’autre côté.
Figure 4 :
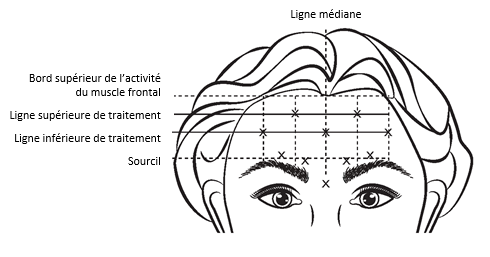
L’amélioration de la sévérité des rides du front observées lors de l’élévation maximale des sourcils est survenue en une semaine après le traitement. L’effet a été démontré pendant environ 4 mois après l’injection.
Pour un traitement simultané des rides glabellaires et des rides de la patte d’oie, la dose totale est de 64 Unités, réparties en 20 Unités pour les rides du front, 20 Unités pour les rides glabellaires (voir Instructions d’administration pour les rides glabellaires, et figure 1), et 24 Unités pour les rides de la patte d’oie (voir Instructions d’administration pour les rides de la patte d’oie, et figures 2 et 3).
Informations générales
En cas d’échec au traitement après une première séance, c’est-à-dire en l’absence, un mois après injection, d’amélioration significative par rapport au bilan initial, il y a lieu :
· d’analyser les causes de l’échec, qui peuvent être diverses : erreur dans les muscles injectés, technique d’injection, formation d’anticorps neutralisant la toxine, dose insuffisante ;
· de réévaluer la pertinence du traitement par la toxine botulinique de type A.
En l’absence d’effets indésirables survenus après la première séance de traitement, effectuer si besoin une seconde séance avec un intervalle d’au moins trois mois entre les deux séances.
Pour les rides glabellaires observées lors du froncement des sourcils, en cas de dose insuffisante, effectuer une deuxième séance d’injection en ajustant la dose totale jusqu’à 40 ou 50 Unités, en tenant compte de l’échec précédent.
L’efficacité et la sécurité d’emploi des injections répétées de VISTABEL au-delà de 12 mois n’ont pas été évaluées.
· Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
· Myasthénie grave ou syndrome de Lambert-Eaton.
· Infection au point d’injection.
4.4. Mises en garde spéciales et précautions d'emploi
Ce médicament contient moins de 1 mmol de sodium (23 mg) par flacon, c'est-à-dire qu'il est essentiellement "sans sodium".
Il est nécessaire d'étudier avec pertinence l'anatomie du patient, et toutes altérations de celle-ci, dues à de précédentes interventions chirurgicales avant d’administrer VISTABEL et l’injection dans des structures anatomiques fragilisées doit être évitée.
La posologie recommandée et la fréquence d’administration de VISTABEL ne doivent pas être dépassées.
Très rarement une réaction anaphylactique peut survenir après injection de toxine botulinique. On disposera donc d’épinéphrine (adrénaline) ou de tout autre moyen utilisable en cas de choc anaphylactique.
Les patients avec des troubles neuromusculaires non identifiés peuvent présenter un risque accru d’effets systémiques cliniquement significatifs tels qu’une dysphagie sévère et une atteinte de la fonction respiratoire à des doses habituellement utilisées de toxine botulinique de type A. Dans certains cas, la dysphagie a duré plusieurs mois et a nécessité la mise en place d’une sonde d’alimentation gastrique (voir rubrique 4.3).
La prudence s’impose lorsque VISTABEL est utilisé chez les patients atteints de sclérose latérale amyotrophique ou présentant un trouble neuromusculaire périphérique.
Des effets indésirables, pouvant être liés à la diffusion de la toxine à distance du site d’administration, ont été très rarement rapportés après traitement par la toxine botulinique (voir rubrique 4.8). Les patients traités à doses thérapeutiques peuvent présenter une faiblesse musculaire excessive. Les difficultés à respirer ou à avaler sont graves et peuvent conduire au décès. L’injection de VISTABEL n’est pas recommandée chez les patients ayant des antécédents de dysphagie ou de pneumopathie d’inhalation.
Les patients et leur entourage doivent être avisés de consulter immédiatement un médecin s’il survenait des troubles de la déglutition, de l’élocution ou de la respiration.
L’administration de doses trop rapprochées, ou trop élevées, peut augmenter le risque de formation d’anticorps. La formation d’anticorps peut mener à un échec du traitement par la toxine botulinique de type A même dans d’autres indications.
Comme pour toute injection, une douleur localisée, une inflammation, des paresthésies, une hypoesthésie, une sensibilité, un gonflement/œdème, un érythème, une infection locale, un saignement et/ou une ecchymose ont été associées à l’injection. La douleur et/ou l'anxiété liées à l'injection avec une aiguille ont entraîné des réactions vasovagales telles qu’une hypotension symptomatique transitoire et une syncope.
La prudence s’impose lorsque VISTABEL est utilisé en présence d’une inflammation au(x) site(s) d’injection proposé(s) ou lorsque le muscle cible présente une atrophie ou une faiblesse excessive.
Il faut s’assurer que VISTABEL ne soit pas injecté dans un vaisseau sanguin lors de l’injection dans les rides glabellaires observées lors du froncement des sourcils, ou lors de l’injection dans les rides de la patte d’oie observées lors d’un sourire forcé, ou lors de l’injection dans les rides du front observées lors de l’élévation maximale des sourcils, voir rubrique 4.2.
Il existe un risque de ptôse de la paupière suite au traitement, voir rubrique 4.2 pour les instructions d’administration pour minimiser ce risque.
Patients âgés
Les données issues des études cliniques de phase 3 sur l’utilisation de VISTABEL chez les patients âgés de plus de 65 ans sont limitées.
Population pédiatrique
L’utilisation de VISTABEL n’est pas recommandée chez les personnes de moins de 18 ans.
Traçabilité
Afin d’améliorer la traçabilité des médicaments biologiques, le nom et le numéro de lot du produit administré doivent être clairement enregistrés
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
L’effet lié à l’administration de différents sérotypes de toxine botulinique de façon concomitante ou à quelques mois d’intervalle chacun, n’est pas connu. Une faiblesse neuromusculaire excessive peut être exacerbée par l’administration d’une autre toxine botulinique avant la disparition des effets de la toxine botulinique administrée précédemment.
Aucun test spécifique n’a été effectué pour vérifier la possibilité d’interactions avec d’autres médicaments. Aucune autre interaction cliniquement significative n’a été décrite dans cette indication.
4.6. Fertilité, grossesse et allaitement
Grossesse
Il n’existe pas d’études appropriées sur l’utilisation de la toxine botulinique de type A chez la femme enceinte. Les études effectuées chez l’animal ont mis en évidence une toxicité sur la reproduction (voir rubrique 5.3). Le risque potentiel chez l’homme est inconnu. VISTABEL n'est pas recommandé pendant la grossesse ni chez la femme en âge de procréer n’utilisant pas de contraception.
Il n’y a pas de données permettant de savoir si VISTABEL est excrété dans le lait maternel. L’utilisation de VISTABEL est déconseillée durant l’allaitement.
Fertilité
Il n’existe pas de données sur les effets de l’utilisation de la toxine botulinique de type A sur la fertilité des femmes en âge de procréer. Les études conduites chez des rats mâles et femelles ont montré des diminutions de la fertilité (Voir rubrique 5.3).
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
a) Général
Dans les essais cliniques contrôlés conduits sur les rides glabellaires observées lors du froncement des sourcils, des effets indésirables considérés comme étant reliés à VISTABEL par l’investigateur ont été rapportés chez 23,5 % (placebo : 19,2%) des patients. Lors du premier cycle de traitement des études pivots contrôlées conduites dans les rides de la patte d’oie observées lors d’un sourire forcé, ce type d’effets indésirables a été rapporté chez 7,6% des patients traités par 24 Unités (pour le traitement des rides de la patte d’oie uniquement) et 6,2% des patients traités par 44 Unités (24 Unités pour le traitement des rides de la patte d’oie administrées simultanément avec 20 Unités pour les rides glabellaires) par comparaison avec 4,5% des patients dans le groupe placebo.
Lors du premier cycle de traitement des essais cliniques conduits sur les rides du front observées lors de l’élévation maximale des sourcils, des effets indésirables considérés comme étant reliés à VISTABEL par l’investigateur ont été rapportés chez 20,6 % des patients traités par 40 Unités (20 Unités dans le muscle frontal et 20 Unités dans le complexe glabellaire), et 14,3 % des patients traités par 64 Unités (20 Unités dans le muscle frontal, 20 Unités dans le complexe glabellaire et 24 Unités dans la zone des rides canthales latérales), par comparaison avec 8,9 % des patients du groupe placebo.
Des effets indésirables peuvent être associés au traitement, à la technique d’injection ou aux deux. En général, les effets indésirables s’observent dans les premiers jours qui suivent l’injection et sont transitoires. La plupart des effets secondaires rapportés étaient d’intensité légère à modérée.
L’action pharmacologique attendue de la toxine botulinique est une faiblesse musculaire locale. Cependant, une faiblesse des muscles adjacents et/ou des muscles distants du site d’injection a été rapportée. L'apparition d'une ptôse de la paupière qui peut être due à la technique d'injection correspondrait à l'action pharmacologique de VISTABEL. Comme pour toute injection, on peut observer une douleur/brûlure/piqûre, un œdème et/ou un hématome liés à l'injection. Une fièvre et un syndrome grippal ont également été rapportés après injection de toxine botulinique.
b) Effets indésirables – fréquence
Les effets indésirables sont classés par Système Organe Classe et par fréquence définie comme suit : très fréquent (≥ 1/10) ; fréquent (≥ 1/100, < 1/10) ; peu fréquent (≥ 1/1000, < 1/100) ; rare (≥ 1/10 000, < 1/1000) ; très rare (< 1/10 000).
Rides glabellaires
Les effets indésirables suivants ont été rapportés dans des études cliniques en double aveugle, contrôlées versus placebo, après injection de VISTABEL 20 Unités dans le traitement des rides glabellaires uniquement :
|
Système Organe Classe |
Effets indésirables |
Fréquence |
|
Infections et infestations |
Infections |
Peu fréquent |
|
Affections psychiatriques |
Anxiété |
Peu fréquent |
|
Affections du système nerveux |
Céphalées, paresthésies |
Fréquent |
|
Vertiges |
Peu fréquent |
|
|
Affections oculaires |
Ptôse de la paupière |
Fréquent |
|
Blépharite, douleur oculaire, trouble visuel (incluant vision trouble) |
Peu fréquent |
|
|
Affections gastro-intestinales |
Nausées |
Fréquent |
|
Sécheresse buccale |
Peu fréquent |
|
|
Affections de la peau et du tissu sous-cutané |
Erythème, sensation de tension cutanée |
Fréquent |
|
Œdème (visage, paupière, périorbital), réaction de photosensibilité, prurit, sécheresse cutanée |
Peu fréquent |
|
|
Affections musculo-squelettiques et du tissu conjonctif |
Faiblesse musculaire localisée |
Fréquent |
|
Contractions musculaires, effet Méphisto (élévation latérale des sourcils) |
Peu fréquent |
|
|
Troubles généraux et anomalies au site d’administration |
Douleur faciale, œdème au site d’injection, ecchymoses, douleur au site d’injection, irritation au site d’injection |
Fréquent |
|
Syndrome grippal, asthénie, fièvre |
Peu fréquent |
Rides de la patte d’oie avec ou sans rides glabellaires
Les effets indésirables suivants ont été rapportés dans des études cliniques en double aveugle, contrôlées versus placebo, après injection de VISTABEL dans le traitement des rides de la patte d’oie, avec ou sans traitement des rides glabellaires :
|
Système Organe Classe |
Effets indésirables |
Fréquence |
|
Affections oculaires |
Œdème de la paupière |
Peu fréquent |
|
Troubles généraux et anomalies au site d’administration |
Hématome au site d'injection* |
Fréquent |
|
Hémorragie au site d'injection* |
Peu fréquent |
|
|
Douleur au site d'injection* |
Peu fréquent |
|
|
Paresthésie au site d'injection |
Peu fréquent |
* effets indésirables liés à la procédure
Rides du front et rides glabellaires avec ou sans rides de la patte d’oie
Les effets indésirables suivants ont été rapportés dans des études cliniques en double aveugle, contrôlées versus placebo, après injection de VISTABEL dans le traitement simultané des rides du front et des rides glabellaires, avec ou sans traitement des rides de la patte d’oie :
|
Système Organe Classe |
Effets indésirables |
Fréquence |
|
Affections du système nerveux |
Céphalées |
Fréquent |
|
Affections oculaires |
Ptôse de la paupière1 |
Fréquent |
|
Affections de la peau et du tissu sous-cutané |
Constriction de la peau, |
Fréquent |
|
Ptôse du sourcil2 |
Fréquent |
|
|
Affections musculo-squelettiques et du tissu conjonctif |
Effet Méphisto (élévation latérale des sourcils) |
Fréquent |
|
Troubles généraux et anomalies au site d’administration |
Contusion au site d’injection* |
Fréquent |
|
Hématome au site d'injection* |
Fréquent |
|
|
Douleur au site d'injection* |
Peu fréquent |
1 Le délai médian d’apparition de la ptôse de la paupière était de 9 jours après le traitement.
2 Le délai médian d’apparition de la ptôse du sourcil était de 5 jours après le traitement.
* Effets indésirables liés à la procédure.
Aucun changement n’a été observé dans le profil de sécurité global suite à une administration répétée.
c) Données de commercialisation (fréquence indéterminée)
Les événements indésirables ou effets indésirables médicalement pertinents suivants ont été décrits depuis la mise sur le marché du produit pour le traitement des rides glabellaires, des rides de la patte d’oie et d'autres indications thérapeutiques :
|
Système Organe Classe |
Effets indésirables |
|
Affections du système immunitaire |
Réaction anaphylactique, angioedème, maladie sérique, urticaire |
|
Troubles métaboliques et nutritionnels |
Anorexie |
|
Affections du système nerveux |
Atteinte du plexus brachial, dysphonie, dysarthrie, parésie faciale, hypoesthésie, faiblesse musculaire, myasthénie grave, neuropathie périphérique, paresthésies, radiculopathie, syncope, paralysie faciale |
|
Affections oculaires |
Glaucome à angle fermé (lors du traitement du blépharospasme), ptôse de la paupière, lagophtalmie, strabisme, vision trouble, trouble visuel, œil sec, œdème de la paupière |
|
Affections de l’oreille et du labyrinthe |
Hypoacousie, bourdonnements d’oreille, vertiges |
|
Affections respiratoires, thoraciques et médiastinales |
Pneumopathie d’inhalation, dyspnée, bronchospasme, dépression respiratoire, insuffisance respiratoire |
|
Affections gastro-intestinales |
Douleurs abdominales, diarrhée, sécheresse buccale, dysphagie, nausées, vomissements |
|
Affections de la peau et du tissu sous-cutané |
Alopécie, ptôse du sourcil, dermatite psoriasiforme, érythème polymorphe, hyperhidrose, madarose, prurit, éruptions cutanées |
|
Affections musculo-squelettiques et du tissu conjonctif |
Atrophie musculaire, myalgie, contractions musculaires localisées / contractions musculaires involontaires |
|
Troubles généraux et anomalies au site d’administration |
Atrophie par dénervation, malaise, fièvre |
Des effets indésirables pouvant être liés à la diffusion de la toxine à distance du site d’administration ont été très rarement rapportés après traitement par la toxine botulinique (faiblesse musculaire, dysphagie, constipation ou pneumopathie d’inhalation pouvant être fatale) (voir rubrique 4.4).
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
La dose, le site d’injection et les propriétés sous-jacentes des tissus sont à prendre en considération lors d’un surdosage en VISTABEL. Il n’a été enregistré aucun cas de toxicité systémique résultant d’une injection accidentelle de toxine botulinique de type A. Des doses excessives peuvent entraîner une paralysie neuromusculaire locale, ou à distance, généralisée et profonde. Aucun cas d’ingestion de toxine botulinique de type A n'a été rapporté.
Les signes de surdosage ne s’observent pas immédiatement après l’injection. En cas d’injection ou d’ingestion accidentelle, le patient doit être mis sous observation médicale pendant plusieurs jours, afin de rechercher d’éventuels signes et symptômes de faiblesse générale ou de paralysie musculaire.
Si un patient présente des symptômes d’intoxication par la toxine botulinique de type A (faiblesse générale, ptôse de la paupière, diplopie, dysphagie et dysphonie ou paralysie des muscles respiratoires), il convient d’envisager son hospitalisation.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : autres myorelaxants à action périphérique, code ATC : M03AX01.
La toxine botulinique de type A (neurotoxine de Clostridium botulinum) bloque la libération périphérique d’acétylcholine au niveau des terminaisons cholinergiques présynaptiques en clivant la protéine SNAP-25, protéine nécessaire à l’ancrage et à la libération de l’acétylcholine par les vésicules situées au sein des terminaisons nerveuses, entraînant une dégénérescence des terminaisons nerveuses et ainsi une paralysie.
Après injection, il se produit une liaison rapide et extrêmement forte de la toxine à des récepteurs cellulaires de surface spécifiques. Cette étape est suivie d’un passage de la toxine à travers la membrane présynaptique par endocytose. Enfin, la toxine est libérée dans le cytoplasme. Cette dernière étape s’accompagne d’une inhibition progressive de la libération d’acétylcholine, les signes cliniques sont visibles au bout de 2-3 jours, le pic d’effet étant observé 5 à 6 semaines après l’injection.
Le rétablissement après injection intramusculaire se produit normalement en l’espace de 12 semaines après l’injection, lorsque les terminaisons nerveuses rétablissent leurs connexions avec les plaques basales.
Données cliniques
Rides glabellaires
537 patients présentant des rides glabellaires d’intensité modérée à sévère au maximum du froncement ont été inclus dans les études cliniques.
Les injections de VISTABEL ont diminué de façon significative la sévérité des rides glabellaires observées lors du froncement des sourcils jusqu’à 4 mois, les critères d’évaluations utilisés étant le jugement par l’investigateur de la sévérité des rides de la glabelle au maximum du froncement et de l’estimation par le patient du changement global dans l’apparence de ses rides glabellaires observées lors du froncement des sourcils. Aucun des critères d’évaluation clinique n’a inclus une mesure objective de l’impact psychologique. Trente jours après l’injection, 80 % (325/405) des patients traités par VISTABEL ont été considérés par l’investigateur comme répondeurs (rides d’intensité légère ou absence de rides lors du froncement des sourcils) comparés aux 3 % (4/132) des patients traités par le placebo. Lors de cette même visite à 30 jours après l’injection, 89 % (362/405) des patients traités par VISTABEL ont estimé qu’ils présentaient une amélioration modérée ou importante, comparés aux 7 % (9/132) des patients traités par le placebo.
Les injections de VISTABEL ont également réduit de façon significative la sévérité des rides de la glabelle au repos. Sur les 537 patients, 39 % (210/537) avaient des rides de la glabelle modérées à sévères au repos (15% n’avaient aucune ride au repos). Parmi ces patients, 74 % (119/161) d’entre eux traités par VISTABEL ont été considérés comme répondeurs au traitement (absence de rides ou rides d’intensité légère) 30 jours après l’injection, comparés aux 20% (10/49) des patients traités par le placebo.
Les données cliniques de phase 3 avec VISTABEL sont limitées chez les patients âgés de plus de 65 ans. Seulement 6,0 % (32/537) des patients avaient plus de 65 ans et les résultats d’efficacité étaient inférieurs dans cette population.
Rides de la patte d’oie
1 362 patients présentant des rides de la patte d’oie modérées à sévères observées lors d’un sourire forcé, soit seules (N = 445, Étude 191622-098) soit associées à des rides glabellaires modérées à sévères observées lors du froncement des sourcils (N= 917, Étude 191622-099), ont été inclus.
Les injections de VISTABEL ont réduit de manière significative la sévérité des rides de la patte d’oie observées lors d’un sourire forcé par comparaison au placebo à tous les temps d’évaluation (p < 0,001) pendant une durée allant jusqu’à 5 mois. Ceci a été mesuré par la proportion de patients présentant une sévérité des rides de la patte d’oie cotée en absence de rides ou rides d’intensité légère observées lors d’un sourire forcé dans les deux études pivots, jusqu’au jour 150 (à la fin de l’étude) dans l’étude 191622-098 et au jour 120 (à la fin du premier cycle de traitement) dans l’étude 191622-099. Les évaluations faites par les patients comme celles faites par les investigateurs ont montré que la proportion de patients présentant une sévérité cotée « absence de rides » ou « rides d’intensité légère » pour les rides de la patte d’oie observées lors d’un sourire forcé était plus importante chez les patients présentant des rides de la patte d’oie modérées observées lors d’un sourire forcé à l’inclusion, par comparaison à des rides de la patte d’oie sévères observées lors d’un sourire forcé à l’inclusion. Le Tableau 1 résume les résultats au jour 30, temps d’évaluation du critère d’efficacité principal.
Dans l’étude 191622-104 (extension de l’étude 191622-099), 101 patients précédemment randomisés dans le groupe placebo ont été inclus pour recevoir un premier traitement à la dose de 44 Unités. Les patients traités par VISTABEL ont présenté un bénéfice statistiquement significatif sur le critère d’efficacité principal par comparaison au placebo 30 jours après administration du premier traitement actif. Le taux de réponse était similaire au groupe 44 Unités 30 jours après administration du premier traitement actif dans l’étude 191622-099. Un total de 123 patients a reçu 4 cycles de traitement de 44 Unités de VISTABEL pour le traitement simultané des rides de la patte d’oie observées lors d’un sourire forcé et des rides glabellaires observées lors du froncement des sourcils.
Tableau 1. Jour 30 : Évaluation par l’investigateur et le patient des rides de la patte d’oie observées lors d’un sourire forcé – Taux de répondeurs (% de patients ayant présenté une sévérité des rides de la patte d’oie cotée « absence de rides » ou « rides d’intensité légère »)
|
Étude clinique |
Dose |
VISTABEL |
Placebo |
VISTABEL |
Placebo |
|
Évaluation de l’investigateur |
Évaluation du patient |
||||
|
191622-098 |
24 Unités (rides de la patte d’oie) |
66,7 %* (148/222) |
6,7 % (15/223) |
58,1 %* (129/222) |
5,4 % (12/223) |
|
191622-099 |
24 Unités (rides de la patte d’oie) |
54,9 %* (168/306) |
3,3 % (10/306) |
45,8 %* (140/306) |
3,3 % (10/306) |
|
44 Unités (24 Unités rides de la patte d’oie & 20 Unités rides glabellaires) |
59,0 %* (180/305) |
3,3 % (10/306) |
48,5 %* (148/305) |
3,3 % (10/306) |
|
*p < 0,001 (VISTABEL vs placebo)
Des améliorations par rapport à l’inclusion dans l’évaluation par les patients de l’apparence des rides de la patte d’oie observées lors d’un sourire forcé ont été observées pour VISTABEL (24 Unités et 44 Unités) par comparaison au placebo, au jour 30 et pour tous les temps d’évaluation suivant chaque cycle de traitement dans les deux études pivots (p < 0,001).
Le traitement par VISTABEL 24 Unités a également réduit de façon significative la sévérité des rides de la patte d’oie au repos. Parmi les 528 patients traités, 63 % (330/528) avaient des rides de la patte d’oie modérées à sévères au repos à l’inclusion. Parmi ceux-ci, 58 % (192/330) des patients traités par VISTABEL ont été considérés comme répondeurs au traitement (sévérité cotée « absence de rides » ou « rides d’intensité légère ») 30 jours après l’injection, par comparaison avec 11 % (39/352) des patients traités par placebo.
Les patients ont également observé des améliorations concernant leur âge et leur attrait avec VISTABEL (24 Unités et 44 Unités) par comparaison au placebo en utilisant le questionnaire sur les rides faciales (FLO-11) au temps d’évaluation du critère d’efficacité principal au jour 30 (p < 0,001) et à tous les temps d’évaluation suivants dans les deux études pivots.
Dans les études pivots, 3,9 % des patients (53/1362) étaient âgés de 65 ans et plus. 36 % des patients de ce groupe d’âge étaient répondeurs au traitement, évalué par l’investigateur (au jour 30) pour VISTABEL (24 Unités et 44 Unités). Lors de l’analyse par groupe d’âge ≤ 50 ans et > 50 ans, les deux populations ont démontré des améliorations statistiquement significatives par comparaison au placebo. La réponse au traitement par VISTABEL 24 Unités, évaluée par l’investigateur, était inférieure dans le groupe de patients > 50 ans à celle du groupe de patients ≤ 50 ans (42,0 % et 71,1 %, respectivement).
La réponse au traitement par VISTABEL globale pour les rides de la patte d’oie observées lors d’un sourire forcé était inférieure (60 %) à celle obtenue après traitement des rides glabellaires observées lors du froncement des sourcils (80 %).
916 patients traités avec VISTABEL (517 patients à 24 Unités et 399 patients à 44 Unités) ont eu des prélèvements pour analyse de la formation d’anticorps. Aucun patient n’a développé d’anticorps neutralisants.
Rides du front
822 patients présentant des rides du front et des rides glabellaires modérées à sévères observées à la contraction maximale, soit seules (N = 254, étude 191622-142) soit associées à des rides de la patte d’oie modérées à sévères observées lors d’un sourire forcé (N = 568, étude 191622-143), ont été inclus dans la population principale d’analyse de tous les critères d’efficacité principaux et secondaires. Dans les études cliniques, les rides du front étaient traitées en même temps que les rides glabellaires.
La proportion de patients présentant une sévérité cotée « absence de rides » ou « rides d’intensité légère » pour les rides du front observées lors de l’élévation maximale des sourcils après les injections de VISTABEL, évaluée par les patients et les investigateurs, était supérieure à celle des patients du groupe placebo au jour 30, critère d’efficacité principal (Tableau 2). La proportion de patients obtenant une amélioration d’au moins 1 grade de la sévérité des rides du front au repos par rapport à l’inclusion, et la proportion de patients obtenant une sévérité cotée « absence de rides » ou « rides d’intensité légère » pour les rides supérieures du visage à la contraction maximale sont également présentées.
Tableau 2. Jour 30 : Évaluation par l’investigateur et le patient des rides du front et des rides supérieures du visage à la contraction maximale et au repos
|
Étude clinique |
Critère d’évaluation |
VISTABEL |
Placebo |
VISTABEL |
Placebo |
|
Évaluation de l’investigateur |
Évaluation du patient |
||||
|
Étude 191622-142 40 U (20 U rides du front + 20 U rides glabellaires) |
Rides du front à la contraction maximalea |
94,8 % |
1,7 % |
87,6 % |
0,0 % |
|
p < 0,0005 |
p < 0,0005 |
||||
|
Rides du front au reposb |
86,2 % |
22,4 % |
89,7 % (174/194) |
10,2 % (6/59) |
|
|
p < 0,0001 |
p < 0,0001 |
||||
|
Étude 191622-143 40 U (20 U rides du front + 20 U rides glabellaires) |
Rides du front à la contraction maximalea |
90,5 % |
2,7 % |
81,5 % |
3,6 % |
|
p < 0,0005 |
p < 0,0005 |
||||
|
Rides du front au reposb |
84,1 % |
15,9 % |
83,6 % (184/220) |
17,4 % (19/109) |
|
|
p < 0,0001 |
p < 0,0001 |
||||
|
Étude 191622-143 64 U (20 U rides du front + 20 U rides glabellaires + 24 U rides de la patte d’oie) |
Rides du front à la contraction maximalea |
93,6 % |
2,7 % |
88,9 % |
3,6 % |
|
p < 0,0005 |
p < 0,0005 |
||||
|
Rides supérieures du visage à la contraction maximalec |
56,6 % |
0,9 % |
sans objet
|
||
|
p < 0,0001 |
|||||
a Proportion de patients présentant une sévérité cotée « absence de rides » ou « rides d’intensité légère » pour les rides du front lors de l’élévation maximale des sourcils.
b Proportion de patients présentant une amélioration d’au moins 1 grade par rapport à l’inclusion pour la sévérité des rides du front au repos.
c Proportion de répondeurs définie comme un même patient présentant une sévérité cotée « absence de rides » ou « rides d'intensité légère » pour les rides du front, les rides glabellaires et les rides de la patte d’oie pour chaque région du visage à la contraction maximale
Les injections de VISTABEL ont significativement réduit la sévérité des rides du front observées lors de l’élévation maximale des sourcils par comparaison au placebo pendant une durée allant jusqu’à 6 mois (p < 0,05) : Ceci a été évalué par la proportion de patients présentant une sévérité des rides du front cotée « absence de rides » ou « rides d’intensité légère » lors de l’élévation maximale des sourcils dans les deux études pivots, jusqu’au jour 150 dans l’étude 191622-142 (21,6 % des patients ayant reçu VISTABEL contre 0 % des patients ayant reçu le placebo) et au jour 180 dans l’étude 191622-143 (6,8 % des patients ayant reçu VISTABEL contre 0 % des patients ayant reçu le placebo).
Lorsque les 3 zones étaient traitées simultanément dans l’étude 191622-143 (groupe VISTABEL 64 U), les injections de VISTABEL ont réduit de façon significative la sévérité des rides glabellaires pendant une durée allant jusqu’à 6 mois (5,5 % des patients ayant reçu VISTABEL contre 0 % des patients du groupe placebo), la sévérité des rides canthales latérales pendant une durée allant jusqu’à 6 mois (3,4 % des patients ayant reçu VISTABEL contre 0 % des patients du groupe placebo), et la sévérité des rides du front pendant une durée jusqu’à 6 mois (9,4 % des patients ayant reçu VISTABEL contre 0 % des patients du groupe placebo).
Au total, 116 et 150 patients ont reçu sur un an 3 cycles de VISTABEL 40 Unités (20 Unités pour les rides du front et 20 Unités pour les rides glabellaires) et 64 Unités (20 unités pour les rides du front, 20 Unités pour les rides glabellaires et 24 Unités pour les rides de la patte d’oie), respectivement. Le taux de réponse pour l’amélioration des rides du front était similaire pour tous les cycles de traitement.
D'après le questionnaire FLO-11, des améliorations de la perception des patients de la gêne occasionnée par les rides du front, du fait de paraître plus vieux que leur âge réel, et de leur attrait ont été observées chez une proportion de patients significativement plus importante (p < 0,001) dans les groupes de patients traités par VISTABEL 40 Unités (20 Unités pour les rides du front et 20 Unités pour les rides glabellaires) et VISTABEL 64 Unités (20 Unités pour les rides du front, 20 Unités pour les rides glabellaires et 24 Unités pour les rides de la patte d'oie) que dans le groupe placebo au temps d’évaluation principal (J30) dans les études 191622-142 et 191622-143.
D'après le questionnaire de satisfaction sur les rides du visage (FLSQ), 78,1 % (150/192) des patients de l’étude 191622-142 et 62,7 % (138/220) des patients de l’étude 191622-143 ont rapporté des améliorations du retentissement sur le plan émotionnel et sur l’apparence (défini par des items liés au fait de se sentir plus âgé, à la mauvaise estime de soi, et au fait de paraître fatigué, triste ou en colère) dans le groupe traité par VISTABEL 40 Unités (20 Unités pour les rides du front et 20 Unités pour les rides glabellaires) contre 19,0 % (11/58) des patients du groupe placebo de l’étude 191622-142 et 18,9 % (21/111) des patients du groupe placebo de l’étude 191622-143, au jour 30 (p < 0,0001 dans les deux études).
D'après ce même questionnaire (FLSQ), 90,2 % (174/193) des patients de l’étude 191622-142 et 79,2 % (175/221, 40 Unités) et 86,4 % (203/235, 64 Unités) des patients de l’étude 191622-143 ont indiqué qu'ils étaient « très satisfaits »/« globalement satisfaits » de VISTABEL 40 Unités ou 64 Unités, par rapport aux patients du groupe placebo (1,7 % [1/58] et 3,6 % [4/110] dans les études 191622-142 et 191622-143, respectivement), au temps d’évaluation principal (jour 60) (p < 0,0001 dans les deux études).
Dans les études pivots, 3,7 % (22/587) des patients étaient âgés de 65 ans et plus. 86,7 % (13/15) des patients de ce groupe d’âge étaient répondeurs au traitement par VISTABEL, selon l’évaluation de l’investigateur (au jour 30), contre 28,6 % (2/7) pour le placebo. Les taux de répondeurs dans ce sous-groupe traité par VISTABEL étaient similaires à ceux de la population globale, mais la significativité statistique n’a pas été atteinte et les comparaisons avec le placebo sont difficiles du fait du faible nombre de patients.
5.2. Propriétés pharmacocinétiques
a) Caractéristiques générales de la substance active :
Après injection, les études de distribution chez le rat mettent en évidence une diffusion musculaire lente de la neurotoxine botulinique radiomarquée à l'iode 125 dans le muscle gastrocnémien. Elle est suivie d'une métabolisation systémique rapide et d'une excrétion urinaire. La quantité de radioactivité dans le muscle a diminué avec une demi-vie de 10 heures environ. Au point d'injection, les éléments radioactifs étaient liés à de grosses molécules protéiques, tandis que dans le plasma, la radioactivité était liée à de petites molécules. Cela suggère une métabolisation systémique rapide du substrat. Dans les 24 heures suivant l'administration, 60 % de la radioactivité se retrouve dans les urines. La toxine est probablement métabolisée par des protéases et par les composants moléculaires recyclés par les voies métaboliques normales.
En raison de la nature de ce produit, il n'a pas été conduit d'étude pharmacocinétique classique (ADME) : Absorption, Distribution, Métabolisation, Elimination.
b) Caractéristiques chez les patients :
On estime qu'aux doses thérapeutiques, VISTABEL se caractérise par une faible distribution systémique. Des études cliniques électromyographiques à fibre unique ont mis en évidence une augmentation de l'activité électrophysiologique neuromusculaire dans les muscles distants du point d'injection, sans aucun signe/symptôme clinique associé.
5.3. Données de sécurité préclinique
Des études de toxicité aiguë, de toxicité à doses répétées, de tolérance locale, de mutagénicité, d’antigénicité et de compatibilité sanguine n’ont pas montré d’effets indésirables locaux ou systémiques inhabituels à des niveaux de doses cliniquement pertinentes.
Albumine humaine, chlorure de sodium.
3 ans.
Après reconstitution, une utilisation immédiate de la solution est recommandée. Toutefois, la stabilité physicochimique a été démontrée pendant 24 heures entre 2°C et 8°C.
6.4. Précautions particulières de conservation
A conserver au réfrigérateur (2°C - 8°C).
Pour les conditions de conservation du médicament après reconstitution, voir la rubrique 6.3.
6.5. Nature et contenu de l'emballage extérieur
Poudre en flacon (verre de type I) muni d'un bouchon (caoutchouc chlorobutyl) et d'une bague (aluminium).
Flacon de 50 Unités ALLERGAN de toxine botulinique de type A - Boîte de 1 ou 2 flacons.
Flacon de 100 Unités ALLERGAN de toxine botulinique de type A - Boîte de 1 ou 2 flacons.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
La reconstitution doit être effectuée selon les règles de bonnes pratiques, en particulier le respect de l’asepsie.
VISTABEL doit être reconstitué avec une solution stérile sans conservateur de sérum physiologique (solution injectable de chlorure de sodium à 0,9 pour cent). Comme indiqué dans le tableau de dilution ci-dessous, le volume adéquat de solution saline stérile sans conservateur (solution injectable de chlorure de sodium à 0,9 pour cent) doit être prélevé dans une seringue afin d’obtenir une solution reconstituée à une concentration de 4 Unités/0,1 ml :
|
Flacon |
Quantité de solvant ajoutée (solution stérile sans conservateur de sérum physiologique (solution injectable de chlorure de sodium à 0,9 pour cent)) |
Dose obtenue |
|
50 Unités |
1,25 ml |
4,0 |
|
100 Unités |
2,5 ml |
4,0 |
La partie centrale du bouchon en caoutchouc doit être nettoyée à l’alcool.
Afin d’éviter la dénaturation de VISTABEL, injecter lentement le solvant dans le flacon et effectuer délicatement des rotations avec le flacon afin d’éviter la formation de bulles. Le flacon ne doit pas être utilisé si la dépression n’entraîne pas l’aspiration du solvant à l’intérieur du flacon. Une fois reconstituée, la solution obtenue doit être contrôlée visuellement avant utilisation. Seule une solution limpide, incolore ou jaune très pâle exempte de particules peut être utilisée.
Il est impératif que VISTABEL ne soit utilisé que pour le traitement d’un seul patient, au cours d’une seule séance.
Procédure à suivre pour une élimination en toute sécurité des flacons, seringues et matériels utilisés :
Immédiatement après utilisation, la solution reconstituée non utilisée de VISTABEL dans le flacon et/ou dans la seringue doit être inactivée, avant élimination, en ajoutant environ 2 ml d’une solution diluée d’hypochlorite de sodium à 1 ou 0,5% (solution de Dakin) et doit être éliminée conformément à la réglementation en vigueur.
Les flacons, seringues et matériels utilisés qui ne doivent pas être vidés doivent ensuite être placés dans des récipients adaptés et éliminés comme déchet biologique médical conformément à la réglementation en vigueur.
Recommandations en cas d’incident lors de la manipulation de la toxine botulinique
|
En cas d’incident lors d’une manipulation du produit qu’il soit à l’état de poudre ou reconstitué, les mesures appropriées décrites ci-dessous doivent être mises en route immédiatement. · La toxine botulinique est très sensible à la chaleur et à certains agents chimiques. · Toute projection doit être essuyée : · soit avec un matériel absorbant imbibé d’une solution d’hypochlorite de sodium (eau de Javel) en cas de produit sec, · soit avec un matériel absorbant sec en cas de produit reconstitué. · Les surfaces contaminées seront nettoyées avec un matériel absorbant imbibé d’une solution d’hypochlorite de sodium puis séchées. · En cas de bris de flacon, procéder comme indiqué ci-dessus au ramassage méticuleux des particules de verre et du produit, en évitant les coupures cutanées. · En cas de projection, laver avec une solution d’hypochlorite de sodium puis rincer abondamment à l’eau. · En cas de projection oculaire, rincer abondamment avec de l’eau ou avec une solution ophtalmique de rinçage oculaire. · En cas de blessure du manipulateur (coupure, autopiqûre), procéder comme ci-dessus et prendre les mesures médicales appropriées en fonction de la dose injectée. |
Ces instructions pour l’utilisation, la manipulation et l’élimination doivent être scrupuleusement suivies.
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
5/13 BOULEVARD DE LA REPUBLIQUE
92100 BOULOGNE-BILLANCOURT
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 364 696 1 7 : poudre en flacon de 50 UNITES ALLERGAN (verre type I) muni d’un bouchon (caoutchouc) et d’une bague (aluminium) ; boîte de 1.
· 34009 301 622 5 5 : poudre en flacon de 100 UNITES ALLERGAN (verre type I) muni d’un bouchon (caoutchouc) et d’une bague (aluminium) ; boîte de 1.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I
Médicament à prescription réservée aux spécialistes en chirurgie plastique, reconstructrice et esthétique, en dermatologie et en chirurgie de la face et du cou et chirurgie maxillo-faciale et en ophtalmologie.
Médicament réservé à l’usage professionnel selon l’article R.5121-80 du code de la santé publique.
ANSM - Mis à jour le : 02/02/2026
VISTABEL 4 UNITÉS ALLERGAN / 0,1 ml, poudre pour solution injectable
Toxine botulinique de type A
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que VISTABEL 4 UNITÉS ALLERGAN / 0,1 ml, poudre pour solution injectable et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser VISTABEL 4 UNITÉS ALLERGAN / 0,1 ml, poudre pour solution injectable ?
3. Comment utiliser VISTABEL 4 UNITÉS ALLERGAN / 0,1 ml, poudre pour solution injectable ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver VISTABEL 4 UNITÉS ALLERGAN / 0,1 ml, poudre pour solution injectable ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE VISTABEL 4 UNITÉS ALLERGAN / 0,1 ml, poudre pour solution injectable ET DANS QUELS CAS EST-IL UTILISE ?
VISTABEL est un myorelaxant d'action périphérique.
VISTABEL agit en bloquant les impulsions nerveuses dirigées vers tous les muscles dans lesquels il a été injecté. Ceci empêche les muscles de se contracter en entraînant une paralysie temporaire et réversible.
VISTABEL est utilisé, chez l’adulte, pour l’amélioration temporaire de l’apparence des rides suivantes :
· des rides verticales situées entre les sourcils, observées lors du froncement des sourcils et/ou,
· des rides en forme d’éventail (pattes d'oie) situées au coin des yeux observées lors d’un sourire forcé et/ou,
· des rides du front observées lors du haussement des sourcils,
lorsque la sévérité des rides du visage entraîne un retentissement psychologique important.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER VISTABEL 4 UNITÉS ALLERGAN / 0,1 ml, poudre pour solution injectable ?
N’utilisez jamais VISTABEL 4 UNITÉS ALLERGAN / 0,1 ml, poudre pour solution injectable
· Si vous êtes allergique à la toxine botulinique de type A ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6
· Si vous souffrez de faiblesse musculaire grave ou de syndrome de Lambert-Eaton (maladies chroniques affectant les muscles)
· Si vous avez une infection au point d’injection.
Avertissements et précautions
Adressez-vous à votre médecin ou votre pharmacien avant d’utiliser VISTABEL.
Des effets indésirables, pouvant être liés à la diffusion de la toxine à distance du site d’administration, ont été très rarement rapportés après traitement par la toxine botulinique (faiblesse musculaire, difficultés à avaler ou aliments solides ou liquides détournés dans les voies respiratoires).
Les patients recevant les doses recommandées peuvent présenter une faiblesse musculaire excessive.
Consultez immédiatement votre médecin si, à la suite du traitement, vous avez des difficultés à avaler, à parler ou à respirer.
· L’utilisation de VISTABEL n’est pas recommandée chez les patients ayant des antécédents de dysphagie (difficultés à avaler) et de « fausses routes ».
· L’utilisation de VISTABEL n’est pas recommandée chez les personnes de moins de 18 ans.
· L’administration de doses trop rapprochées, ou trop élevées, peut augmenter le risque de formation d’anticorps. La formation d’anticorps peut mener à un échec du traitement par la toxine botulinique de type A même dans d’autres indications. Pour limiter ce risque, l’intervalle entre deux traitements ne doit pas être inférieur à trois mois.
· Très rarement une réaction allergique peut survenir après l'injection de toxine botulinique.
· Une chute de la paupière peut survenir après le traitement.
Informez votre médecin si :
· vous avez eu des problèmes dans le passé lors de précédentes injections de toxine botulinique ;
· vous ne constatez pas d'amélioration de vos rides un mois après votre première séance d'injection ;
· vous êtes atteint de sclérose latérale amyotrophique ou présentez un trouble neuromusculaire périphérique ;
· vous avez une inflammation au niveau des muscles où l’injection doit être effectuée ;
· les muscles dans lesquels votre médecin va faire l’injection sont faibles ou atrophiés ;
· vous avez été opéré ou blessé au niveau de la tête, du cou ou de la poitrine ;
· vous allez bientôt être opéré.
Autres médicaments et VISTABEL 4 UNITÉS ALLERGAN / 0,1 ml, poudre pour solution injectable
L’utilisation de toxine botulinique n’est pas recommandée en association avec les aminosides, la spectinomycine, ou d’autres médicaments pouvant interférer avec la transmission neuromusculaire.
Informez votre médecin si on vous a récemment injecté un médicament contenant de la toxine botulinique (substance active de VISTABEL), car cela pourrait augmenter l’effet de VISTABEL de façon excessive.
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
VISTABEL 4 UNITÉS ALLERGAN / 0,1 ml, poudre pour solution injectable avec des aliments, boissons et de l’alcool
Sans objet.
L’utilisation de VISTABEL n’est pas recommandée pendant la grossesse et chez les femmes en âge de procréer n’utilisant pas de contraception.
VISTABEL n’est pas recommandé durant l’allaitement.
Contactez votre médecin si vous êtes enceinte, prévoyez une grossesse ou devenez enceinte pendant le traitement. Votre médecin vous conseillera sur la poursuite ou non du traitement.
Demandez conseil à votre médecin ou à votre pharmacien avant de prendre tout médicament.
Conduite de véhicules et utilisation de machines
L'attention est attirée, notamment chez les conducteurs de véhicules et les utilisateurs de machines, sur les risques de faiblesse musculaire et/ou généralisée, de vertiges et de troubles de la vision liés à l'emploi de ce médicament, pouvant rendre dangereuse la conduite de véhicules ou l'utilisation de machines.
Ne conduisez pas ou n'utilisez pas de machines tant que ces symptômes n'ont pas disparu.
VISTABEL 4 UNITÉS ALLERGAN / 0,1 ml, poudre pour solution injectable contient du sodium
Ce médicament contient moins de 1 mmol de sodium (23 mg) par flacon, c’est-à-dire qu'il est essentiellement « sans sodium ».
3. COMMENT UTILISER VISTABEL 4 UNITÉS ALLERGAN / 0,1 ml, poudre pour solution injectable ?
Le traitement par VISTABEL doit être administré par des médecins ayant les qualifications nécessaires, ayant une bonne expérience du traitement et utilisant le matériel approprié.
Rides verticales situées entre les sourcils observées lors du froncement des sourcils
VISTABEL est injecté dans les muscles (usage intramusculaire), directement dans la zone à traiter entre les sourcils.
La dose recommandée est de 20 Unités.
Vous recevrez une injection dans chacun des 5 sites d’injection de vos muscles, le volume recommandé d’injection est de 0,1 ml (4 Unités) de VISTABEL.
Une amélioration des rides situées entre les sourcils observées au froncement des sourcils survient en général dans la semaine qui suit le traitement. Le pic d’effet étant observé 5 à 6 semaines après l’injection. L’effet du traitement a été démontré jusqu’à 4 mois après injection.
Rides en forme d’éventail au coin des yeux (pattes d’oie) observées lors d’un sourire forcé
VISTABEL est injecté directement dans la zone à traiter au coin de chaque œil.
La dose recommandée est de 24 Unités.
Vous recevrez une injection dans chacun des 6 sites d’injection de vos muscles (3 sites d’injection au coin de chaque œil), le volume d’injection de VISTABEL recommandé est de 0,1 ml (4 Unités).
Une amélioration de la sévérité des rides en forme d’éventail situées au coin des yeux observées lors d’un sourire forcé survient généralement dans la semaine qui suit le traitement. L’effet du traitement a été démontré jusqu’à 4 mois après injection.
Rides du front observées lors du haussement des sourcils
VISTABEL est injecté directement dans le muscle de la zone du front à traiter.
La dose recommandée est de 20 Unités.
Vous recevrez une injection dans chacun des 5 sites d’injection, le volume recommandé d’injection est de 0,1 ml (4 Unités) de VISTABEL.
La dose totale pour le traitement des rides du front (20 Unités) conjointement avec les rides glabellaires (20 Unités) est de 40 Unités.
L’amélioration de la sévérité des rides du front observées lors du haussement des sourcils survient généralement dans la semaine qui suit le traitement. L’effet du traitement a été démontré jusqu'à 4 mois après injection.
Informations générales
Si vous êtes traité(e) pour les rides en forme d’éventail situées au coin des yeux, observées lors d’un sourire forcé, en même temps que les rides verticales situées entre les sourcils, observées lors du froncement des sourcils, vous recevrez une dose totale de 44 Unités.
Si vous êtes traité(e) simultanément pour les rides de ces trois régions du visage (rides en forme d’éventail situées au coin des yeux, observées lors d’un sourire forcé, rides verticales situées entre les sourcils, observées lors du froncement des sourcils, et rides du front, observées lors du haussement des sourcils), vous recevrez une dose totale de 64 Unités.
L’intervalle entre deux traitements ne doit pas être inférieur à trois mois.
L’efficacité et la sécurité des injections répétées de VISTABEL après 12 mois n’ont pas été évaluées.
Si vous avez utilisé plus de VISTABEL 4 UNITÉS ALLERGAN / 0,1 ml, poudre pour solution injectable que vous n’auriez dû
Sans objet.
Si vous oubliez d’utiliser VISTABEL 4 UNITÉS ALLERGAN / 0,1 ml, poudre pour solution injectable
Si vous arrêtez d’utiliser VISTABEL 4 UNITÉS ALLERGAN / 0,1 ml, poudre pour solution injectable
Sans objet.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
En général, les effets indésirables surviennent dans les premiers jours suivant l’injection et sont transitoires. La plupart des effets indésirables rapportés sont d’intensité légère à modérée.
Environ 1 patient sur 4 peut présenter un effet indésirable après une injection de VISTABEL pour le traitement des rides verticales situées entre les sourcils observées lors du froncement des sourcils. Environ 8 % des patients peuvent présenter des effets indésirables après une injection de VISTABEL pour le traitement des rides en forme d’éventail situées au coin des yeux observées lors d’un sourire forcé quand elles sont traitées seules ou en même temps que les rides verticales situées entre les sourcils observées lors du froncement des sourcils. Environ 20 % des patients peuvent présenter des effets indésirables après une injection de VISTABEL pour le traitement des rides du front observées lors du haussement des sourcils, quand elles sont traitées en même temps que les rides verticales situées entre les sourcils observées lors du froncement des sourcils. Environ 14 % des patients peuvent présenter des effets indésirables lors du traitement des rides du front et des rides verticales, quand elles sont traitées en même temps que les rides en forme d’éventail situées au coin des yeux observées lors d’un sourire forcé.
Ces effets indésirables peuvent être liés au traitement, à la technique d’injection ou les deux. Une chute de la paupière, pouvant être liée à la technique d’injection, est compatible avec l’action de relaxation musculaire locale de VISTABEL.
Des effets indésirables, pouvant être liés à la diffusion de la toxine à distance du site d’administration, ont été très rarement rapportés après traitement par la toxine botulinique (faiblesse musculaire, difficultés à avaler, constipation ou pneumonie due à des aliments solides ou liquides détournés dans les voies respiratoires, pouvant être fatale). L’injection de VISTABEL n’est pas recommandée chez les patients ayant des antécédents de dysphagie (difficulté à avaler) ou de « fausses routes ».
SI VOUS PRÉSENTEZ DES DIFFICULTÉS POUR RESPIRER, AVALER OU PARLER APRÈS AVOIR REÇU VISTABEL, CONTACTEZ IMMÉDIATEMENT VOTRE MÉDECIN.
Si vous présentez une urticaire ou un gonflement notamment gonflement du visage ou de la gorge, une respiration sifflante, une sensation de faiblesse et d’essoufflements, contactez immédiatement votre médecin.
Une diffusion de la toxine botulinique dans les muscles voisins est possible lorsque de fortes doses sont injectées, en particulier dans la région du cou.
Comme pour toute injection, une douleur/brûlure/piqûre, un gonflement et/ou un hématome au point d’injection sont possibles. Parlez-en à votre médecin si cela vous inquiète.
Le risque de présenter un effet indésirable est décrit selon les catégories suivantes :
|
Fréquent |
Peut affecter jusqu’à une personne sur 10 |
|
Peu fréquent |
Peut affecter jusqu’à une personne sur 100 |
Injections pour l’amélioration temporaire des rides verticales situées entre les sourcils
|
Fréquents |
Maux de tête, engourdissements, chute de la paupière, nausée (se sentir malade), rougeurs de la peau, sensation de tension cutanée, faiblesse musculaire localisée, douleur au niveau du visage, gonflement au site d’injection, douleur au site d’injection, ecchymoses (bleus), irritation au site d’injection |
|
Peu fréquents |
Infection, anxiété, vertiges, inflammation de la paupière, douleur au niveau de l’œil, troubles de la vision, vision floue, bouche sèche, gonflement (visage, paupière, ou autour de l’œil), sensibilité à la lumière, démangeaisons, peau sèche, contraction musculaire, syndrome grippal, faiblesse, fièvre, effet Méphisto (élévation de la partie externe des sourcils). |
Injections pour l’amélioration temporaire des rides en forme d’éventail situées au coin des yeux, lorsqu’elles sont traitées seules ou en même temps que les rides verticales situées entre les sourcils observées lors du froncement des sourcils
|
Fréquent |
Hématome au site d'injection* |
|
Peu fréquents |
Gonflement de la paupière, saignement au site d'injection*, douleur au site d'injection*, picotement ou engourdissement au site d’injection |
*Certains de ces effets indésirables peuvent être liés à la procédure d’injection.
Injections pour l’amélioration temporaire des rides du front et des rides verticales situées entre les sourcils observées lors du froncement des sourcils, lorsqu’elles sont traitées seules ou en même temps que les rides en forme d’éventail situées au coin des yeux
|
Fréquents |
Maux de tête, chute de la paupière1, sensation de tension cutanée, chute du sourcil2, ecchymoses (bleus) au site d'injection*, hématome au site d’injection*, effet Méphisto (élévation de la partie externe des sourcils). |
|
Peu fréquents |
Douleur au site d'injection* |
1 Le délai médian d’apparition de la chute de la paupière était de 9 jours après le traitement.
2 Le délai médian d’apparition de la chute du sourcil était de 5 jours après le traitement.
* Effets indésirables liés à la procédure.
La liste suivante décrit d’autres effets indésirables rapportés pour VISTABEL, depuis sa commercialisation dans le traitement des rides glabellaires, des rides de la patte d’oie et autres indications :
· réactions allergiques sévères (gonflement sous la peau, difficulté pour respirer)
· urticaire
· perte de l’appétit
· lésion nerveuse
· difficultés pour bouger le bras et l’épaule
· problèmes d’élocution et de voix
· faiblesse des muscles du visage
· diminution de la sensibilité de la peau
· faiblesse musculaire
· maladie chronique des muscles (myasthénie grave)
· engourdissement
· douleur ou faiblesse partant de la colonne vertébrale
· évanouissement
· affaissement des muscles d’un côté du visage
· augmentation de la pression intraoculaire
· chute de la paupière
· strabisme (yeux qui louchent)
· difficulté à fermer complètement les yeux
· vision floue, difficultés pour voir clairement
· diminution de l’audition
· bourdonnements dans les oreilles
· sensation de vertiges ou de tête qui tourne
· pneumopathie d’inhalation (inflammation du poumon causée par une inhalation accidentelle de nourriture, de liquide, de salive ou de vomi)
· essoufflement
· problèmes respiratoires, détresse respiratoire et/ou insuffisance respiratoire
· douleur abdominale
· diarrhée
· bouche sèche
· difficultés pour avaler
· nausée
· vomissements
· perte de cheveux
· chute du sourcil
· lésion cutanée évoquant un psoriasis (apparition de plaques rouges, épaisses, sèches, qui s’écaillent)
· différents types d’éruptions cutanées avec des taches rouges
· transpiration excessive
· perte de cils
· démangeaisons
· urticaire
· perte de masse musculaire
· douleur musculaire
· perte/diminution de l’innervation du muscle injecté
· malaise
· sensation de malaise généralisée
· fièvre
· œil sec
· contractions musculaires localisées / contractions musculaires involontaires
· gonflement de la paupière
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER VISTABEL 4 UNITÉS ALLERGAN / 0,1 ml, poudre pour solution injectable ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur le flacon après EXP. La date de péremption fait référence au dernier jour de ce mois.
A conserver au réfrigérateur (entre +2°C et +8°C).
Après reconstitution, une utilisation immédiate de la solution injectable est recommandée, toutefois elle peut être conservée pendant 24 heures au réfrigérateur (entre 2°C et 8°C).
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient VISTABEL 4 UNITÉS ALLERGAN / 0,1 ml, poudre pour solution injectable
· La substance active est : toxine botulinique de type A de Clostridium botulinum, 4 UNITÉS ALLERGAN par 0,1 ml de solution reconstituée.
Les UNITÉS ALLERGAN ne sont pas interchangeables avec les autres préparations de toxine botulinique.
· Les autres composants sont : l’albumine humaine et le chlorure de sodium.
VISTABEL se présente sous la forme d'une fine poudre blanche pour solution injectable qui peut être difficile à voir dans le fond du flacon en verre transparent. Avant injection, la poudre doit être dissoute dans une solution stérile sans conservateur de sérum physiologique (solution injectable de chlorure de sodium à 0,9 pour cent). Chaque flacon contient soit 50 soit 100 UNITÉS ALLERGAN de toxine botulinique de type A.
Chaque boîte contient 1 ou 2 flacon(s).
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
5/13 BOULEVARD DE LA REPUBLIQUE
92100 BOULOGNE-BILLANCOURT
Exploitant de l’autorisation de mise sur le marché
ABBVIE
5/13 BOULEVARD DE LA REPUBLIQUE
ALLERGAN PHARMACEUTICALS IRELAND
CASTLEBAR ROAD
WESTPORT-CO. MAYO
IRLANDE
Ou
ABBVIE DEUTSCHLAND GMBH & CO. KG
KNOLLSTRASSE
67061 LUDWIGSHAFEN
ALLEMAGNE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site internet de l’ANSM (France).
----------------------------------------------------------------------------------------------------------------------------------------
Les informations suivantes sont destinÉes exclusivement aux professionnels de santÉ :
Les unités de toxine botulinique ne sont pas interchangeables d’un produit à l’autre. Les doses recommandées en UNITÉS ALLERGAN sont différentes de celles des autres préparations de toxine botulinique.
VISTABEL est utilisé pour l’amélioration temporaire de l’apparence :
· des rides verticales modérées à sévères situées entre les sourcils, observées lors du froncement des sourcils (rides glabellaires) et/ou,
· des rides en forme d’éventail modérées à sévères situées au coin des yeux (pattes d’oie) observées lors d’un sourire forcé et/ou,
· des rides du front modérées à sévères observées lors de l’élévation maximale des sourcils,
lorsque la sévérité des rides du visage entraîne un retentissement psychologique important chez le patient adulte.
La reconstitution doit être effectuée selon les règles de bonnes pratiques, en particulier le respect de l’asepsie. VISTABEL doit être reconstitué avec une solution stérile sans conservateur de sérum physiologique (solution injectable sans conservateur de chlorure de sodium à 0,9 %). Pour un flacon de 50 Unités, 1,25 ml de solution stérile sans conservateur de sérum physiologique (solution injectable sans conservateur de chlorure de sodium à 0,9 pour cent) doit être prélevé dans une seringue afin d’obtenir une solution injectable reconstituée à une concentration de 4 Unités/0,1 ml ; pour un flacon de 100 Unités, 2,5 ml de solution stérile sans conservateur de sérum physiologique (solution injectable sans conservateur de chlorure de sodium à 0,9 pour cent) doivent être prélevés dans une seringue afin d’obtenir une solution injectable reconstituée à une concentration de 4 Unités/ 0,1 ml :
|
Flacon |
Quantité de solvant ajoutée (solution stérile sans conservateur de sérum physiologique (solution injectable de chlorure de sodium à 0,9 pour cent)) |
Dose obtenue |
|
50 Unités |
1,25 ml |
4,0 |
|
100 Unités |
2,5 ml |
4,0 |
La partie centrale du bouchon en caoutchouc doit être nettoyée à l’alcool.
Afin d’éviter la dénaturation de VISTABEL, injecter lentement le solvant dans le flacon et effectuer délicatement des rotations avec le flacon afin d’éviter la formation de bulles. Le flacon ne doit pas être utilisé si la dépression n’entraîne pas l’aspiration du solvant à l’intérieur du flacon. Une fois reconstituée, la solution injectable obtenue doit être contrôlée visuellement avant utilisation afin de vérifier qu’elle est limpide, incolore ou jaune très pâle et qu’elle ne contient pas de particules.
Il est impératif que VISTABEL ne soit utilisé que pour le traitement d’un seul patient, au cours d’une seule séance.
Avant injection pour le traitement des rides glabellaires (rides verticales situées entre les sourcils, modérées à sévères observées lors du froncement des sourcils), le pouce ou l’index doit être placé fermement sous le rebord orbitaire afin d’éviter l’extravasation sous le rebord orbitaire. L’aiguille devra être orientée vers le haut et vers la ligne médiane lors de l’injection. Afin de réduire le risque de ptôse de la paupière, la dose maximale de 4 Unités par site d’injection ainsi que le nombre de sites d’injection ne doivent pas être dépassés. De plus, les injections à proximité du muscle releveur de la paupière supérieure doivent être évitées, en particulier chez les patients dotés d'importants complexes abaisseurs des sourcils (depressor supercilii). Les injections dans le muscle corrugator doivent être faites dans la partie centrale de ce muscle, à une distance d’au moins un centimètre au-dessus de l’arcade sourcilière.
Les injections pour le traitement des rides de la patte d’oie (rides canthales latérales modérées à sévères observées lors d’un sourire forcé) doivent être administrées avec le biseau de l’aiguille vers le haut et orientées à l’opposé de l’œil. Afin de réduire les risques de ptôse de la paupière, la dose maximum de 4 Unités par site d’injection ainsi que le nombre de site d’injection ne doivent pas être dépassés. De plus, les injections devront être faites de façon temporale par rapport à l’orbite, en s’assurant de respecter une distance de sécurité par rapport au muscle contrôlant l’élévation de la paupière.
La dose totale pour le traitement des rides du front (20 Unités) conjointement avec les rides glabellaires (20 Unités) est de 40 Unités/1,0 ml. Lors de la détermination de l’emplacement des sites d’injection appropriés au niveau du muscle frontal, veuillez évaluer le rapport entre la taille du front du patient et la répartition de l’activité du muscle frontal.
Procédure à suivre pour une élimination en toute sécurité des flacons, seringues et matériels utilisés
Immédiatement après utilisation, la solution injectable reconstituée non utilisée de VISTABEL dans le flacon et/ou dans la seringue doit être inactivée, avant élimination, en ajoutant environ 2 ml d’une solution diluée d’hypochlorite de sodium à 0,5 % ou 1 % et doit être éliminée conformément à la réglementation en vigueur.
Les flacons, seringues et matériels utilisés qui ne doivent pas être vidés doivent ensuite être placés dans des récipients adaptés et éliminés conformément à la réglementation en vigueur.
Recommandations en cas d’incident lors de la manipulation de la toxine botulinique
En cas d’incident lors d’une manipulation du produit qu’il soit à l’état de poudre ou reconstitué, les mesures appropriées décrites ci-dessous doivent être mises en route immédiatement.
· Toute projection doit être essuyée : soit avec un matériel absorbant imbibé d’une solution d’hypochlorite de sodium (eau de Javel) en cas de produit sec, soit avec un matériel absorbant sec en cas de produit reconstitué.
· Les surfaces contaminées seront nettoyées avec un matériel absorbant imbibé d’une solution d’hypochlorite de sodium (eau de Javel) puis séchées.
· En cas de bris de flacon, procéder comme indiqué ci-dessus et ramasser méticuleusement les particules de verre et du produit, en évitant les coupures cutanées.
· En cas de projection sur la peau, laver avec une solution d’hypochlorite de sodium (solution d’eau de Javel) puis rincer abondamment à l’eau.
· En cas de projection oculaire, rincer abondamment avec de l’eau ou avec une solution de rinçage oculaire.
· En cas de blessure du manipulateur (coupure, autopiqûre), procéder comme ci-dessus et prendre les mesures médicales appropriées en fonction de la dose injectée.
Identification du produit
Afin de vérifier que le produit que vous avez reçu sous le nom de VISTABEL est bien un authentique produit AbbVie, recherchez des signes d’inviolabilité figurant sur les boîtes VISTABEL, ainsi qu’un pelliculage holographique sur l’étiquette du flacon. Afin de visualiser le pelliculage holographique, examinez le flacon sous une lampe de bureau ou sous une source de lumière fluorescente. Faîtes tourner le flacon d’avant en arrière entre vos doigts et recherchez des lignes horizontales multicolores et vérifiez la présence de l’inscription « abbvie » entre ces lignes horizontales multicolores.
N’utilisez pas le produit et contactez AbbVie pour obtenir plus d’informations si les lignes horizontales multicolores ou l’inscription « abbvie » sont absentes de l’étiquette du flacon.
De plus, deux vignettes détachables sont incluses sur l’étiquette du flacon de VISTABEL indiquant chacune le numéro de lot et la date de péremption du produit que vous avez reçu. Ces vignettes peuvent être décollées et placées dans le dossier clinique de votre patient à des fins de traçabilité. Il est à noter qu’une fois la vignette retirée de l’étiquette du flacon, le mot « UTILISÉ » apparaît, vous apportant une preuve supplémentaire que vous utilisez un authentique flacon de VISTABEL.