Dernière mise à jour le 02/03/2026
ANDROGEL 16,2 mg/g, gel transdermique
Indications thérapeutiques
Classe pharmacothérapeutique - code ATC : G03BA03 Testostérone
Ce médicament contient de la testostérone, hormone masculine naturellement produite dans l'organisme.
Ce médicament est utilisé chez l’homme adulte pour remplacer la testostérone afin de traiter divers problèmes de santé dus au manque de testostérone (hypogonadisme masculin). Ce diagnostic doit être confirmé par deux dosages séparés de la testostérone dans le sang, ainsi que par la présence de symptômes tels que :
· impuissance,
· infertilité,
· diminution de la libido,
· fatigue,
· humeur dépressive,
· perte osseuse due aux faibles taux d’hormones,
· régression des caractères sexuels masculins,
· diminution de la masse maigre,
· dysfonction érectile.
Présentations
> 1 récipient(s) multidose(s) polypropylène avec poche doublée polyéthylène basse densité (PEBD) avec pompe(s) doseuse(s)
Code CIP : 34009 300 537 0 6
Déclaration de commercialisation : 14/02/2018
Cette présentation n'est pas agréée aux collectivités
Service médical rendu (SMR)
Pas de SMR disponible pour ce médicament ( plus d'informations dans l'aide )
Amélioration du service médical rendu (ASMR)
Pas d'ASMR disponible pour ce médicament (plus d'informations dans l'aide )
Autres informations
- Titulaire de l'autorisation : BESINS HEALTHCARE France
- Conditions de prescription et de délivrance :
- liste I
- prescription initiale réservée à certains spécialistes
- prescription réservée aux médecins compétents en NUTRITION
- prescription réservée aux spécialistes en MEDECINE ET BIOLOGIE DE LA REPRODUCTION - ANDROLOGIE
- prescription réservée aux spécialistes et services DIABETOLOGIE
- prescription réservée aux spécialistes et services ENDOCRINOLOGIE
- prescription réservée aux spécialistes et services GYNECOLOGIE
- prescription réservée aux spécialistes et services UROLOGIE
- renouvellement non restreint
- Statut de l'autorisation : Valide
- Type de procédure : Procédure décentralisée
- Code CIS : 6 809 723 7
ANSM - Mis à jour le : 04/02/2026
ANDROGEL 16,2 mg/g, gel transdermique
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Un gramme de gel contient 16,2 mg de testostérone. Une action sur la pompe délivre 1,25 g de gel contenant 20,25 mg de testostérone.
Excipient à effet notoire : ce médicament contient 0,9 g d’alcool (éthanol) dans chaque dose de 1,25 g de gel.
Pour la liste complète des excipients, voir rubrique 6.1.
Gel transparent ou légèrement opalescent, incolore.
4.1. Indications thérapeutiques
Ce médicament est indiqué chez l’adulte dans le traitement substitutif d'un hypogonadisme masculin quand le déficit en testostérone a été confirmé cliniquement et biologiquement (voir 4.4 Mises en garde spéciales et précautions d’emploi).
4.2. Posologie et mode d'administration
Adulte et sujet âgé
La posologie recommandée est de deux pressions sur la pompe (soit 40,5 mg de testostérone) appliquées une fois par jour, environ à la même heure, de préférence le matin. La dose quotidienne sera adaptée par le médecin en fonction de la réponse clinique ou biologique de chaque patient, sans dépasser quatre pressions sur la pompe, soit 81 mg de testostérone par jour. L'ajustement de la posologie devra être effectué par paliers d’une pression sur la pompe.
La dose doit être déterminée sur la base des concentrations sanguines matinales en testostérone avant l’administration. L'état d'équilibre des concentrations sanguines de testostérone est atteint environ à partir du 2e jour du traitement par ce médicament. L'adaptation de la posologie se fait en fonction de la testostéronémie, mesurée le matin avant l’application du produit, une fois l’état d’équilibre atteint. Les concentrations sanguines en testostérone doivent être évaluées périodiquement pour s’assurer que la dose reçue par le patient est adéquate. La posologie peut être diminuée si la testostéronémie dépasse le niveau souhaité. Si la concentration est faible, la posologie peut être augmentée par étapes sans dépasser 81 mg de testostérone (quatre pressions sur la pompe).
Le traitement doit être arrêté si la testostéronémie dépasse constamment la plage normale à la dose quotidienne la plus faible de 20,25 mg (1,25 g de gel, soit une pression sur la pompe) ou si une testostéronémie normale n’est pas obtenue avec la dose la plus élevée de 81 mg (5 g de gel, soit quatre pressions sur la pompe).
Patients souffrant d’une insuffisance rénale ou hépatique sévère
Veuillez consulter la rubrique 4.4 Mises en garde particulières et précautions d’emploi.
Population pédiatrique
Aucune donnée n’est disponible.
Utilisation chez la femme
Ce médicament n’est pas indiqué chez la femme.
Mode d’administration
Utilisation transdermique.
Le gel doit être appliqué par le patient lui-même, sur une peau propre, sèche et saine, sur les épaules, et les bras.
Le gel doit être étalé simplement en couche mince sur la peau. Il n’est pas nécessaire de frotter la peau. Laisser sécher le gel au moins 3 à 5 minutes avant de s’habiller.
· Se laver soigneusement les mains à l'eau et au savon après avoir appliqué le gel,
· Lorsque le gel est sec, couvrir le(s) site(s) d’application avec un vêtement propre (par exemple un t-shirt).
Après avoir appliqué ce médicament, le patient doit attendre au moins 1 heure avant de prendre une douche ou un bain.
Ne pas appliquer le gel sur les organes génitaux, la quantité importante d'alcool dans le gel pouvant entraîner une irritation locale.
Avant d’obtenir une première dose complète, il est nécessaire d’amorcer la pompe du réservoir. Pour ce faire, le réservoir étant en position verticale, appuyez lentement et complètement sur le piston à trois reprises. Éliminez le gel issu des trois premières pressions en toute sécurité. L’amorçage de la pompe est uniquement nécessaire avant la première dose.
Après l’amorçage, appuyer complètement sur le piston pour délivrer 1,25 g de ce médicament dans la paume de la main et appliquer le gel sur les épaules et les bras.
Avant tout contact physique étroit avec une autre personne (adulte ou enfant), laver le site d'application avec de l'eau et du savon une fois le délai recommandé (au moins 1 heure) écoulé et recouvrir à nouveau de vêtements propres.
Pour plus d'informations concernant le lavage après application, voir rubrique 4.4 (sous-section Transfert peau à peau).
Ce médicament est contre-indiqué en cas de :
· Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1,
· Cancer de la prostate ou carcinome mammaire, suspecté ou confirmé.
4.4. Mises en garde spéciales et précautions d'emploi
En raison de la variabilité des résultats entre les différents laboratoires, tous les dosages doivent être effectués par le même laboratoire pour un sujet donné.
Avant d'instaurer un traitement à base de testostérone, les patients devraient subir impérativement un examen approfondi afin d'écarter tout risque de cancer de la prostate préexistant. Une surveillance attentive et régulière de la prostate et des seins devra être conduite selon les méthodes recommandées (toucher rectal et dosage du PSA - antigène spécifique de la prostate) au moins une fois par an chez tout patient suivant un traitement par la testostérone et deux fois par an chez les sujets âgés et les patients à risque (facteurs cliniques ou familiaux).
Les androgènes peuvent accélérer l'évolution d'un cancer de la prostate infraclinique ou d'une hyperplasie bénigne de la prostate.
Ce médicament doit être utilisé avec prudence chez les patients ayant un cancer avec un risque d'hypercalcémie (et d'hypercalciurie associée), liée à des métastases osseuses. Il est recommandé d’assurer un suivi régulier de la calcémie chez ces patients.
Chez les patients atteints d'insuffisance cardiaque, hépatique ou rénale sévère ou de pathologies cardiaques ischémiques, le traitement par la testostérone pourrait entraîner des complications sévères caractérisées par un œdème, avec ou sans insuffisance cardiaque congestive. Dans ce cas, le traitement doit être interrompu immédiatement. De plus, un traitement par diurétique pourrait être requis.
La testostérone peut entraîner une élévation de la pression artérielle. Par conséquent ce médicament doit être utilisé avec prudence chez les hommes présentant une hypertension.
Troubles de la coagulation
La testostérone doit être utilisée avec prudence chez les patients souffrant de thrombophilie ou présentant des facteurs de risque de thromboembolie veineuse (TEV) car des évènements thromboemboliques ont été rapportés chez ces patients sous traitement par testostérone, lors d’études et de suivi post commercialisation (par exemple : thrombose veineuse profonde, embolie pulmonaire, thrombose oculaire). Chez les patients atteints de thrombophilie, des cas de TEV ont été rapportés même sous traitement anticoagulant. Par conséquent, la poursuite du traitement par la testostérone après un premier événement thrombotique doit être évaluée attentivement. En cas de poursuite du traitement, d'autres mesures doivent être prises afin de réduire au maximum le risque de TEV.
Les taux de testostérone doivent être contrôlés avant le début du traitement, puis à intervalles réguliers pendant le traitement. Les cliniciens doivent ajuster la posologie à chaque patient, afin de s’assurer que les taux de testostérone sont maintenus à un niveau eugonadique.
Chez les patients suivant un traitement androgénique au long cours, les paramètres biologiques suivants doivent être contrôlés régulièrement : taux d’hémoglobine, hématocrite (pour détecter une polyglobulie), fonction hépatique et bilan lipidique.
Actuellement, il n'existe pas de consensus quant aux valeurs de référence de la testostéronémie en fonction de l'âge. La diminution des taux sériques physiologiques de la testostérone avec l'âge doit être prise en compté.
Ce médicament doit être utilisé avec prudence chez les patients souffrant d'épilepsie et de migraine car leur état pourrait être aggravé.
Il a été rapporté dans la littérature des risques d'augmentation d'apnée du sommeil lors de traitement par les esters de testostérone chez les sujets traités pour hypogonadisme, en particulier chez les sujets à risques présentant une obésité ou une pathologie respiratoire chronique.
Une amélioration de la sensibilité à l'insuline peut être observée chez les patients traités par androgènes et peut nécessiter une diminution de la posologie des antidiabétiques (voir rubrique 4.5). Un suivi de la glycémie et du taux en HbA1c est conseillé aux patients traités par androgènes.
Certains signes cliniques de type : irritabilité, nervosité, prise de poids, érections prolongées ou fréquentes peuvent témoigner d'une androgénisation trop intense et nécessitent une adaptation posologique.
En cas de réaction sévère au niveau du site d’application, le traitement doit être reconsidéré et arrêté si nécessaire.
Une gynécomastie peut parfois se développer et persister chez les patients traités par androgènes pour hypogonadisme.
Ce médicament ne doit pas être utilisé chez la femme en raison de possibles effets virilisants.
Si aucune précaution n’est prise, un transfert de testostérone à une autre personne peut se produire à tout moment après l’administration lors d'un contact physique étroit avec la zone d'application du gel, induisant une augmentation du taux sérique de testostérone et de possibles effets indésirables (par exemple, augmentation de la pilosité sur le visage et/ou le corps, mue de la voix, irrégularités du cycle menstruel chez la femme, puberté prématurée et développement des organes génitaux chez l’enfant) en cas de contact répété (androgénisation accidentelle).
Ce produit contient de l'éthanol : chez les nouveau-nés (nouveau-nés prématurés et à terme), des concentrations élevées d'éthanol peuvent provoquer des réactions locales graves et une toxicité systémique en raison d'une absorption importante par une peau qui est immature (en particulier sous occlusion).
Les femmes enceintes doivent éviter tout contact avec les sites d'application de ce médicament. En cas de grossesse de sa partenaire, le patient devra être d’autant plus vigilant quant aux précautions d’utilisation décrites ci-dessus (voir également rubrique 4.6).
Ce médicament contient 0,9 g d'alcool (éthanol) dans chaque dose de de 1,25 g de gel. Cela peut provoquer une sensation de brûlure sur une peau endommagée.
Ce médicament contient de l’éthanol pour faciliter le passage transdermique et est inflammable.
Des précautions doivent être prises pour éviter les sources de chaleur/flammes nues lors de l’administration du produit, jusqu'à ce que le gel soit sec sur la peau.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Anticoagulants oraux
Des modifications de l’effet anticoagulant (augmentation de l'effet de l'anticoagulant oral par modification de la synthèse hépatique des facteurs de la coagulation et inhibition compétitive au niveau des liaisons aux protéines plasmatiques), un contrôle plus fréquent du taux de prothrombine et une mesure du rapport international normalisé (INR) est recommandé. Les patients sous anticoagulants oraux nécessitent une surveillance attentive particulièrement au début ou à l'arrêt du traitement par androgènes.
Corticostéroïdes
L'administration concomitante de testostérone et d'ACTH ou de corticostéroïdes peut augmenter le risque d'apparition d'œdèmes. Par conséquent, ces médicaments doivent être administrés avec prudence, en particulier chez les patients souffrant de maladie cardiaque, rénale ou hépatique.
Analyses de laboratoire
Interaction avec les analyses de laboratoire : les androgènes peuvent diminuer les taux de globuline fixant la thyroxine (TBG), entraînant une réduction des concentrations sériques de T4 et une augmentation du captage sur résine de la T3 et de la T4. Néanmoins, les taux d'hormones thyroïdiennes libres restent inchangés et sans manifestation clinique d'insuffisance thyroïdienne.
Médicament pour le diabète
Des modifications de la sensibilité à l’insuline, de la tolérance au glucose, du contrôle glycémique, de la glycémie et du taux d'hémoglobine ont été rapportées avec les androgènes. Chez les patients diabétiques, les médicaments antidiabétiques pourraient nécessiter une réduction de la dose (voir rubrique 4.4).
L’application d’un écran solaire ou d’une lotion ne réduit pas l’efficacité du médicament.
4.6. Fertilité, grossesse et allaitement
Fertilité
La spermatogenèse peut être supprimée de façon réversible par ce médicament.
Grossesse
Ce médicament est destiné exclusivement aux hommes.
Ce médicament n'est pas indiqué chez la femme enceinte.
Les femmes enceintes doivent éviter tout contact avec ce médicament (voir rubrique 4.4) en raison des effets indésirables virilisants sur le fœtus. En cas de contact peau à peau accidentel, se laver soigneusement avec de l'eau et du savon dès que possible
Allaitement
Ce médicament n'est pas indiqué chez la femme allaitante.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Les effets sur l'aptitude à conduire des véhicules et à utiliser des machines n'ont pas été étudiés.
Les effets indésirables listés ci-après sont basés sur les données issues de la période post-autorisation de mise sur le marché de ce médicament, les essais cliniques et les effets de classe.
Résumé du profil de sécurité
À la posologie journalière recommandée, les effets indésirables les plus fréquemment observés ont été des réactions cutanées au site d’application (érythème, acné, sécheresse cutanée), de l’anxiété et de l’asthénie.
Tableau des effets indésirables
Les effets indésirables rapportés dans les études cliniques et issus de la période post-commercialisation via les déclarations spontanées et les cas publiés sont listés ci-dessous.
Les effets indésirables sont listés selon les catégories suivantes de fréquence : très fréquent (≥ 1/10), fréquent (≥ 1/100 à < 1/10), peu fréquent (≥ 1/1 000 à < 1/100), rare (≥ 1/10 000 à < 1/1 000), très rare (< 1/10 000), fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
|
Classe de systèmes d’organes MedRA |
Effets indésirables - Termes préférentiels |
||||
|
Fréquent (≥ 1/100, < 1/10) |
Peu fréquent (≥ 1/1 000 à < 1/100) |
Rare (≥ 1/10 000 à < 1/1 000) |
Très rare (< 1/10 000) |
Fréquence indéterminée (ne peut être estimée sur la base des données disponibles) |
|
|
Tumeurs bénignes, malignes et non précisées (incl. kystes et polypes) |
|
|
Néoplasie hépatique |
|
Cancer de la prostate |
|
Troubles du métabolisme et de la nutrition |
|
|
|
|
Gain de poids, modifications des électrolytes (rétention de sodium, chlorure, potassium, calcium, phosphate inorganique et eau) lors de posologie élevée et/ou de traitement prolongé |
|
Affections psychiatriques |
Troubles de l’humeur, symptômes émotionnels |
|
|
|
Nervosité, dépression, hostilité |
|
Affections du système nerveux |
Vertiges, paresthésie, amnésie, hyperesthésie, maux de tête |
|
|
|
|
|
Affections vasculaires |
Hypertension |
Hypertension maligne, bouffées de chaleur/rougissement, phlébite |
|
|
|
|
Affections respiratoires, thoraciques et médiastinales |
|
|
|
|
Apnée du sommeil |
|
Affections gastro-intestinales |
Diarrhée |
Douleur buccale, distension abdominale |
|
|
|
|
Affections hépatobiliaires |
|
|
|
Jaunisse, anomalies des tests de la fonction hépatique |
|
|
Affections de la peau et du tissus sous-cutanée |
Alopécie, urticaire |
Acné, hirsutisme, rash, sécheresse de la peau, séborrhée, lésions cutanées, dermatite de contact, modifications de la couleur des cheveux, hypersensibilité au site d’application, prurit au site d’application |
|
|
Réactions cutanées2 |
|
Affections musculo-squelettiques et systémiques |
|
|
|
|
Crampes musculaires |
|
Affections du rein et des voies urinaires |
|
|
|
|
Obstruction urinaire |
|
Affections des organes de reproduction et du sein |
Gynécomastie1 |
Troubles au niveau des mamelons, anomalies de la prostate, douleurs testiculaires, augmentation de la fréquence des érections |
Priapisme |
|
Perturbation de la libido, les thérapies à haute dose de testostérone interrompent ou réduisent fréquemment et réversiblement la spermatogénèse et donc la taille des testicules |
|
Troubles généraux et anomalies au site d'administration |
Réaction au site d’application |
Œdème qui prend le godet |
|
|
Asthénie, malaise, œdème, réactions d’hypersensibilité, augmentation de la survenue de rétention d’eau et d’œdème3. |
|
Investigations |
Modifications des tests en laboratoire (polyglobulie, lipides), augmentation de l’hématocrite, augmentation du taux d’hémoglobine, augmentation de la numération des globules rouges |
PSA accru |
|
|
|
1. Peut se développer et persister chez les patients traités pour hypogonadisme par la testostérone.
2. Réactions cutanées, en raison de l'alcool contenu dans le produit, des applications fréquentes sur la peau peuvent provoquer des irritations et un dessèchement de la peau
3. Une dose élevée ou une administration à long terme de testostérone augmente parfois les cas de rétention d'eau et d'œdème.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
Le taux sérique de testostérone devrait être dosé si les signes cliniques indiquent une surexposition aux androgènes. Des rashs cutanés au site d’application ont également été rapportés dans des cas de surdosage avec ce médicament.
Traitement
Le traitement du surdosage consiste à laver le site d’application immédiatement et d’arrêter le traitement si cela est conseillé par le médecin traitant.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : Androgènes, code ATC : G03B A03.
Les androgènes endogènes, principalement la testostérone, sécrétés par les testicules et son principal métabolite, la DHT, sont responsables du développement des organes génitaux externes et internes et du maintien des caractères sexuels secondaires (développement de la pilosité, mue de la voix, apparition de la libido). Les androgènes ont également un effet sur l'anabolisme protidique, le développement de la musculature squelettique et de la distribution de la graisse corporelle, la réduction de l'élimination urinaire d'azote, de sodium, de potassium, de chlorures, de phosphore et d'eau.
La testostérone diminue la sécrétion hypophysaire de gonadotrophines.
Les effets de la testostérone sur certains organes cibles ne se manifestent qu'après conversion au niveau périphérique de la testostérone en œstradiol, qui se lie alors aux récepteurs nucléaires des œstrogènes des cellules cibles, par exemple, dans l'hypophyse, le tissu adipeux, le cerveau, l'os et les cellules de Leydig dans le testicule.
5.2. Propriétés pharmacocinétiques
L'absorption percutanée de la testostérone après administration de ce médicament varie entre 1 % et 8,5 %.
Après absorption percutanée, la testostérone diffuse dans la circulation générale à des taux relativement constants au cours du nycthémère.
La concentration sérique de testostérone augmente dès la première heure après l'application pour atteindre l'état d'équilibre à partir du deuxième jour. Les variations quotidiennes du taux de testostérone sont alors d'amplitude similaire à celles observées au cours du rythme circadien de la testostérone endogène. La voie percutanée évite ainsi les pics de distribution sanguine induits par les injections. Elle n'entraîne pas de concentrations hépatiques supra-physiologiques du stéroïde, contrairement à l'androgénothérapie par voie orale.
L’administration de 2,5 g de ce médicament produit une augmentation moyenne du taux de testostérone plasmatique d’environ 2,2 ng/ml (7,7 nmol/l).
À l'arrêt du traitement, la décroissance du taux de testostérone commence environ 24 h après la dernière administration. Le retour au taux de base s'effectue en environ 72 à 96 heures après la dernière administration.
Les principaux métabolites actifs de la testostérone sont la dihydrotestostérone et l'œstradiol.
La testostérone est principalement éliminée dans l’urine sous forme de métabolites conjugués, une faible quantité étant éliminée sous forme inchangée dans les fèces.
Au cours de l’étude de phase III, menée à double insu, à la fin d’une période de traitement de 112 jours, pendant laquelle la dose de ce médicament pouvait être déterminée sur la base des concentrations en testostérone totale, 81,6 % (IC 75,1-87,0 %) des hommes avaient une concentration en testostérone totale dans la plage normale des jeunes hommes eugonadiques (300 -1 000 ng/dl). Chez les patients prenant une dose quotidienne de ce médicament, la moyenne (±ET) de la concentration quotidienne en testostérone au jour 112 (Cav) était de 561 (±259) ng/dl, la Cmax moyenne était de 845 (±480) ng/dl et la Cmin moyenne était de 334 (±155) ng/dl. Les concentrations correspondantes au jour 182 (période de double insu) étaient Cav 536 (±236) ng/dl, Cmax moyenne 810 (±497) ng/dl et Cmin moyenne 330 (±147) ng/dl.
Au cours de l’étude de phase III, menée en ouvert, à la fin d’une période de traitement de 264 jours, pendant laquelle la dose de ce médicament pouvait être déterminée sur la base de la concentration totale en testostérone, 77 % (IC 69,8-83,2 %) des hommes avaient une concentration totale en testostérone dans la plage normale des jeunes hommes eugonadiques (300 -1 000 ng/dl).
Chez les patients prenant une dose quotidienne de ce médicament, la moyenne (±ET) de la concentration quotidienne en testostérone au jour 266 (Cav) était de 459 (±218) ng/dl, la Cmax moyenne était de 689 (±414) ng/dl et la Cmin moyenne était de 305 (±121) ng/dl. Les concentrations correspondantes au jour 364 (extension de la période en ouvert) étaient Cav 454 (±193) ng/dl, Cmax moyenne 698 (±382) ng/dl et Cmin moyenne 302 (±126) ng/dl.
5.3. Données de sécurité préclinique
Les hormones sexuelles sont connues pour faciliter le développement de certaines tumeurs induites par des agents carcinogènes connus. L’importance de ces résultats et le risque réel pour l’être humain n’ont pas été élucidés.
Il a été rapporté que l’administration de testostérone exogène supprimait la spermatogenèse chez le rat, le chien et les primates non humains, cette suppression étant réversible à l’arrêt du traitement.
Carbomère 980, myristate d’isopropyle, éhanol à 96 %, hydroxyde de sodium, eau purifiée.
3 ans.
6.4. Précautions particulières de conservation
Ce médicament ne nécessite pas de précautions particulières de conservation.
6.5. Nature et contenu de l'emballage extérieur
Récipient multidose (comportant un réservoir en polypropylène avec une poche doublée en LDPE) et une pompe doseuse qui contient 88 g de gel et délivre au minimum 60 doses.
Tailles de l’emballage extérieur :
· 1 récipient par boîte en carton
· Boîtes de 1, 2,3 ou 6 récipients.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Pas d’exigences particulières.
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
BESINS HEALTHCARE FRANCE
3 RUE DU BOURG L’ABBE
75003 PARIS
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 300 537 0 6 : Récipient multidose (comportant un réservoir en polypropylène avec une poche doublée en LDPE). Boite de 1 récipient.
· 34009 300 537 1 3 : Récipient multidose (comportant un réservoir en polypropylène avec une poche doublée en LDPE). Boite de 2 récipients.
· 34009 550 190 1 5 : Récipient multidose (comportant un réservoir en polypropylène avec une poche doublée en LDPE). Boite de 3 récipients.
· 34009 550 190 2 2 : Récipient multidose (comportant un réservoir en polypropylène avec une poche doublée en LDPE). Boite de 6 récipients.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
<{JJ mois AAAA}>
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I
Prescription initiale réservée aux spécialistes en endocrinologie – diabétologie – nutrition, en urologie, en gynécologie ou en médecine et biologie de la reproduction – andrologie.
Renouvellement non restreint.
ANSM - Mis à jour le : 04/02/2026
ANDROGEL 16,2 mg/g, gel transdermique
Testostérone
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
· « Ce médicament » fera référence à ANDROGEL 16,2 mg/g, gel transdermique dans cette notice.
1. Qu'est-ce que ANDROGEL 16,2 mg/g, gel transdermique et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser ANDROGEL 16,2 mg/g, gel transdermique ?
3. Comment utiliser ANDROGEL 16,2 mg/g, gel transdermique?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver ANDROGEL 16,2 mg/g, gel transdermique ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE ANDROGEL 16,2 mg/g, gel transdermique ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique - code ATC : G03BA03 Testostérone
Ce médicament contient de la testostérone, hormone masculine naturellement produite dans l'organisme.
Ce médicament est utilisé chez l’homme adulte pour remplacer la testostérone afin de traiter divers problèmes de santé dus au manque de testostérone (hypogonadisme masculin). Ce diagnostic doit être confirmé par deux dosages séparés de la testostérone dans le sang, ainsi que par la présence de symptômes tels que :
· impuissance,
· infertilité,
· diminution de la libido,
· fatigue,
· humeur dépressive,
· perte osseuse due aux faibles taux d’hormones,
· régression des caractères sexuels masculins,
· diminution de la masse maigre,
· dysfonction érectile.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER ANDROGEL 16,2 mg/g, gel transdermique ?
Qui peut utiliser ce médicament :
· Seuls les hommes peuvent utiliser ce médicament.
· Les hommes jeunes de moins de 18 ans ne doivent pas utiliser ce médicament.
· Ce médicament ne doit pas être utilisé chez la femme quel que soit son âge.
· Ne laissez pas les femmes (spécialement les femmes enceintes ou allaitantes) ou les enfants entrer en contact avec ce médicament ou la zone cutanée sur laquelle ce médicament a été appliqué.
N’utilisez jamais ce médicament :
· si vous présentez un cancer de la prostate ou une suspicion de cancer de la prostate
· si vous vous présentez un cancer du sein ou une suspicion de cancer du sein
· si vous êtes allergique (hypersensible) à la testostérone ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
Avertissements et précautions
Adressez-vous à votre médecin ou pharmacien avant d’utiliser ce médicament.
Avant de démarrer tout traitement avec ce médicament, votre déficit en testostérone doit être clairement démontré par des signes cliniques (régression des caractères masculins, diminution de la masse maigre, faiblesse ou fatigue, désir sexuel/libido diminué(e), incapacité à obtenir/maintenir une érection, etc.) et confirmé par des examens biologiques. Votre médecin fera les tests nécessaires avant utilisation de ce médicament ainsi que les contrôles de suivi en effectuant des analyses de sang périodiques.
Si une des situations ci-dessous s’appliquent à vous (ou si vous n’êtes pas surs), informez votre médecin avant d’utiliser ce médicament car son utilisation pourrait aggraver ces troubles :
· vous avez des difficultés à uriner en raison d'une hypertrophie de la prostate
· vous avez un cancer des os - votre médecin vérifiera votre taux de calcium
· vous avez une pression artérielle élevée ou si vous êtes traité pour une pression artérielle élevée, car ce médicament peut provoquer une augmentation de la pression artérielle
· vous avez une maladie cardiaque, hépatique ou rénale grave, car le traitement par ce médicament peut entraîner de graves complications sous forme de rétention d'eau dans votre corps, parfois accompagnée d'une insuffisance cardiaque (congestive) (surcharge de liquide dans le cœur)
· vous avez une maladie cardiaque ischémique (qui affecte l'apport sanguin au cœur)
· problèmes de coagulation sanguine
o thrombophilie (une anomalie de la coagulation du sang qui augmente le risque de thrombose, formation de caillots sanguins dans les vaisseaux sanguins)
o facteurs qui augmentent le risque de formation de caillots sanguins dans une veine : antécédents de caillots sanguins dans une veine, tabagisme, obésité, cancer, immobilisation, si un membre de votre famille proche a eu un caillot sanguin dans une jambe, un poumon ou un autre organe à un âge jeune (par exemple, avant environ 50 ans), ou à mesure que votre âge augmente.
o comment reconnaître un caillot sanguin : gonflement douloureux d'une jambe ou changement soudain de la couleur de la peau qui par exemple devient pâle, rouge ou bleue, essoufflement soudain, toux soudaine et inexpliquée pouvant faire cracher du sang ou douleur soudaine dans la poitrine, sensation d’étourdissement importante ou vertige, douleur intense à l’estomac, perte de vision brutale. Consultez immédiatement un médecin si vous présentez l'un de ces symptômes.
· vous souffrez d'épilepsie
· vous avez des migraines
· vous avez des difficultés à respirer pendant votre sommeil - ces symptômes sont plus susceptibles de se produire si vous êtes en surpoids ou si vous avez des problèmes pulmonaires de longue durée
Les androgènes peuvent augmenter le risque de grossissement de la prostate (hypertrophie bénigne de la prostate) ou de cancer de la prostate. Des examens réguliers de la prostate devront être réalisés avant le début et pendant le traitement conformément aux prescriptions de votre médecin.
En cas de réaction cutanée sévère, le traitement doit être reconsidéré et arrêté si nécessaire.
Ce médicament ne doit pas être utilisé chez les femmes en raison de ses effets potentiellement virilisants (comme le développement de la pilosité sur le visage ou sur le corps, la mue de la voix ou des modifications du cycle menstruel).
Informations sur la surveillance complémentaire
Les contrôles sanguins suivants doivent être effectués par votre médecin avant et pendant le traitement : taux de testostérone dans le sang, numération globulaire complète.
Vous ferez l'objet de contrôles réguliers (au moins une fois par an et deux fois par an si vous êtes âgé ou si votre médecin vous considère comme un patient à risque) pendant le traitement.
Si vous recevez un traitement de substitution à la testostérone sur de longues périodes, vous risquez de développer une augmentation anormale du nombre de globules rouges dans votre sang (polycythémie). Vous devrez effectuer des analyses sanguines régulières pour vérifier que cela ne se produit pas.
Enfants et adolescents
En raison de l’absence d’information clinique chez les garçons de moins de 18 ans, ce médicament n’est pas recommandé chez les enfants.
Transfert possible de testostérone
Pour éviter un tel transfert, les précautions suivantes sont recommandées :
· Lavez-vous soigneusement les mains à l'eau et au savon après avoir appliqué le gel,
· Lorsque le gel est sec, couvrez le(s) site(s) d’application avec un vêtement (par exemple un t-shirt). Après avoir appliqué ce médicament, le patient doit attendre au moins 1 heure avant de prendre une douche ou un bain.
· Lavez soigneusement le site d'application avec de l'eau et du savon afin d’enlever tout résidu de testostérone avant tout contact physique ou, si cela n’est pas possible, mettez un vêtement comme une chemise ou un t-shirt couvrant la zone d’application durant le contact.
Les patients utilisant ce produit susceptibles d'être en contact physique étroit avec des enfants doivent faire preuve de prudence, car la testostérone peut traverser les vêtements. Veillez à respecter la technique d'application (voir la section 3 de cette notice) en cas de contact physique avec des enfants, notamment en couvrant le site d'application avec des vêtements propres une fois le gel sec. De plus, lavez le site d'application avec du savon une fois le délai recommandé (au moins 1 heure) écoulé et recouvrez-le de vêtements propres avant tout contact physique avec des enfants.
Si vous pensez qu'un transfert de testostérone à une autre personne (homme, femme ou enfant) a pu se produire, cette personne doit :
· laver immédiatement à l'eau et au savon la surface cutanée concernée,
· signaler à un médecin l'apparition de signes tels que de l’acné, une modification de la croissance ou du système pileux du visage ou du corps, une mue de la voix, des modifications du cycle menstruel.
· Chez les enfants, les signes d’une puberté prématurée et d’un agrandissement des organes génitaux sont à surveiller.
Il est préférable de respecter un délai d'au moins 1 heure avant la prise d'un bain ou d'une douche.
Autres médicaments et ce médicament
Informez votre médecin pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament, notamment :
· des anticoagulants oraux (utilisés pour fluidifier le sang)
· des corticostéroïdes (médicaments utilisés pour réduire l’inflammation)
· de l’insuline (médicament utilisé pour contrôler la glycémie chez les diabétiques). Vous pourriez être amené à diminuer votre dose d’insuline lors de l’utilisation de ce médicament.
Si une des situations ci-dessus s’applique (ou si vous n’êtes pas surs), informez votre médecin ou votre pharmacien avant d’utiliser ce médicament.
Ces médicaments peuvent nécessiter l'ajustement des doses de ce médicament.
Ce médicament avec des aliments
Sans objet.
Grossesse et allaitement
Ce médicament n'est pas indiqué chez la femme.
La production de sperme peut être supprimée de manière réversible avec ce médicament.
Si votre partenaire tombe enceinte, vous devez suivre les conseils concernant l'évitement du transfert du gel de testostérone.
Sportifs
L’attention des sportifs est attirée sur le fait que ce médicament contient un principe actif (testostérone) pouvant induire une réaction positive des tests pratiqués lors des contrôles antidopage.
Conduite de véhicules et utilisation de machines
Ce médicament n'a pas d'influence sur l'aptitude à conduire ou à utiliser des machines.
Ce médicament contient 0,9 g d'alcool (éthanol) ans chaque dose de 1,25 g de gel. Cela peut provoquer une sensation de brûlure sur une peau endommagée.
3. COMMENT UTILISER ANDROGEL 16,2 mg/g, gel transdermique ?
Ce médicament est réservé à l’homme adulte.
Veillez à toujours utiliser ce médicament en suivant exactement les indications de votre médecin. Vérifiez auprès de votre médecin ou pharmacien en cas de doute.
Première utilisation de la pompe
Avant d’utiliser la pompe pour la première fois, vous devez la préparer à l’utilisation comme suit :
· Retirez le capuchon du réservoir pour révéler le piston,
· Appuyez sur le piston à trois reprises,
· N’utilisez pas le gel issu de ces trois pressions sur le piston. Cette dose doit être éliminée de façon sûre.
· Votre pompe est désormais prête à l’emploi. Vous n’aurez plus besoin de l’amorcer à nouveau.
À chaque fois que vous appuierez sur le piston, la pompe délivrera 1,25 g de gel.
La dose recommandée est de 2 pressions appliquées une fois par jour, environ à la même heure, de préférence le matin. La dose sera éventuellement adaptée par votre médecin sans toutefois dépasser 4 pressions par jour.
Votre médecin vous indiquera le nombre de pressions sur le piston à réaliser pour obtenir la dose de gel correcte dans votre cas. Le tableau ci-dessous vous donne plus d’informations à ce sujet.
|
Nombre de pressions |
Quantité de gel |
Quantité de testostérone appliquée sur la peau |
|
1 |
1,25 |
20,25 |
|
2 |
2,5 |
40,5 |
|
3 |
3,75 |
60,75 |
|
4 |
5,0 |
81,0 |
Le gel doit être délicatement étalé en couche mince sur une peau propre, sèche et saine, sur les deux épaules et les deux bras. Ne le faites pas pénétrer dans la peau en frottant. Laissez le gel sécher au moins 3 à 5 minutes avant de vous habiller. Lavez-vous les mains à l'eau et au savon après l'application. N’appliquez pas le gel sur les organes génitaux (pénis et testicules), la quantité importante d'alcool dans le gel pouvant entraîner une irritation locale.
Après avoir actionné la pompe comme décrit ci-dessus, le gel est prêt à être utilisé.
Comment appliquer le gel
Le gel doit être appliqué par le patient lui-même.
1. Appuyez une fois sur le piston pour distribuer le gel dans la paume de la main.
2. Sélectionnez une zone de peau propre, sèche et saine sur l'épaule et le haut du bras (voir les zones identifiées sur l'image ci-dessous).
3. À l'aide de vos doigts, étalez doucement le gel uniformément sur une épaule et le haut du bras. Ne le frottez pas sur la peau.
4. Si vous utilisez 2 pressions, répétez les étapes 1, 2 et 3 sur l'autre épaule et le haut du bras.
5. Si vous utilisez 3 pressions ou plus, appliquez jusqu'à 2 pompes sur la première épaule et le haut du bras et jusqu'à 2 pompes sur l'autre épaule et le haut du bras.
6. Après avoir appliqué le gel, lavez-vous les mains à l'eau et au savon.
7. Vous devez laisser le gel sécher complètement avant de vous habiller.
Ne pas appliquer sur les zones génitales (pénis et testicules) car la forte teneur en alcool peut provoquer une irritation locale.
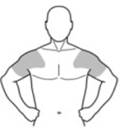
Les patients doivent être informés que d'autres personnes (adultes ou enfants) ne doivent pas entrer en contact avec la zone du corps où le gel a été appliqué.
Une fois le gel séché, couvrez le site d'application avec un vêtement propre (comme un t-shirt)
Avant tout contact physique étroit avec une autre personne (adulte ou enfant), lavez le site d'application avec de l'eau et du savon une fois le délai recommandé (au moins 1 heure) écoulé et recouvrez-le à nouveau avec un vêtement propre.
Le gel doit être administré par le patient lui-même, sur une peau propre, sèche et saine sur les deux épaules ou les deux bras.
Si vous utilisez plus de ce médicament que vous n'auriez dû
Demandez conseil à votre médecin ou à votre pharmacien. Il pourra vous être conseillé de laver immédiatement le site d'application et votre médecin pourra vous conseiller d'arrêter le traitement.
Les signes suivants peuvent indiquer que vous prenez une dose trop importante du produit et vous devez contacter votre médecin :
· irritabilité
· nervosité
· prise de poids
· érections fréquentes ou prolongées
Ces symptômes peuvent signifier que votre dose de ce médicament est trop élevée et votre médecin peut devoir ajuster votre dose (voir Mises en garde et précautions, rubrique 2).
Si vous oubliez d’utiliser ce médicament :
Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre. Appliquez la dose suivante à l’heure habituelle.
Si vous arrêtez d’utiliser ce médicament :
N'arrêtez pas votre traitement par ce médicament sans en avoir préalablement parlé à votre médecin.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Effets indésirables fréquents (jusqu’à 1 personne sur 10)
· troubles de l’humeur,
· symptômes émotionnels (sautes d’humeur, troubles affectifs, colère, agressivité, impatience, insomnie, rêves anormaux et augmentation de la libido),
· vertiges,
· paresthésie,
· amnésie,
· hyperesthésie,
· maux de tête,
· hypertension,
· diarrhée,
· alopécie,
· urticaire,
· gynécomastie,
· réaction au site d’application,
· modifications des tests en laboratoire (polyglobulie, lipides),
· augmentation de l’hématocrite,
· augmentation du taux d’hémoglobine,
· augmentation de la numération des globules rouges.
Effets indésirables peu fréquents (jusqu’à 1 personne sur 100)
· hypertension maligne,
· bouffées de chaleur/rougissement,
· phlébite,
· douleur buccale,
· distension abdominale,
· acné,
· hirsutisme,
· rash,
· sécheresse de la peau,
· séborrhée,
· lésions cutanées,
· dermatite de contact,
· modifications de la couleur des cheveux,
· hypersensibilité au site d’application,
· prurit au site d’application,
· troubles au niveau des mamelons,
· anomalies de la prostate,
· douleurs testiculaires,
· augmentation de la fréquence des érections,
· œdème qui prend le godet,
· PSA accru.
Effets indésirables rares (jusqu’à 1 personne sur 1000)
· néoplasie hépatique,
· priapisme.
Effets indésirables très rares (jusqu’à 1 personne sur 10 000)
· jaunisse
· obstruction des voies urinaires
Fréquence indéterminée (ne peut être estimée sur la base des données disponibles) :
· cancer de la prostate
· asthénie,
· nervosité,
· dépression,
· hostilité,
· apnée du sommeil,
· obstruction urinaire
· crampes musculaires
· perturbation de la libido,
· les thérapies à haute dose de testostérone interrompent ou réduisent fréquemment et réversiblement la spermatogénèse et donc la taille des testicules
· malaise,
· œdème,
· réactions d’hypersensibilité,
· gain de poids,
· modifications des électrolytes (rétention de sodium, chlorure, potassium, calcium, phosphate inorganique et eau) lors de posologie élevée et/ou de traitement prolongé,
· réactions cutanées (en raison de l'alcool contenu dans le produit, des applications fréquentes sur la peau peuvent provoquer des irritations et un dessèchement de la peau),
· augmentation de la survenue de rétention d’eau et d’œdème.
En raison de la présence d'alcool, des applications fréquentes sur la peau peuvent provoquer des irritations et une sécheresse de la peau.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER ANDROGEL 16,2 mg/g, gel transdermique ?
Ce médicament ne nécessite pas de précautions particulières de conservation.
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur la boite et le flacon. La date de péremption fait référence au dernier jour de ce mois.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
· La substance active est : testostérone
· Les autres composants sont :
Carbomère 980, myristate d’isopropyle, éthanol à 96 %, hydroxyde de sodium et eau purifiée.
Qu’est-ce que ce médicament et contenu de l’emballage extérieur
Ce médicament est un gel incolore présenté dans un récipient multidose à pompe doseuse contenant 88 g de gel et délivre un minimum de 60 doses.
Ce médicament est disponible en boîte de 1,2, 3 ou 6 récipients.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
3 RUE DU BOURG L’ABBE
75003 PARIS
Exploitant de l’autorisation de mise sur le marché
BESINS HEALTHCARE FRANCE
75009 PARIS
LABORATOIRES BESINS INTERNATIONAL
13 RUE PERIER
92120 MONTROUGE
ou
BESINS MANUFACTURING BELGIUM
GROOT-BIJGAARDENSTRAAT 128
1620 DROGENBOS
BELGIQUE
ou
BESINS MANUFACTURING ESPAÑA S.L.
POLIGONO INDUSTRIAL EL PITARCO
PARCELA 4
50450 MUEL (ZARAGOZA)
ESPAGNE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[à compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).