Dernière mise à jour le 08/01/2026
MIFLASONE 400 microgrammes, poudre pour inhalation en gélule
Indications thérapeutiques
Classe pharmacothérapeutique : GLUCOCORTICOIDE PAR VOIE INHALEE, ANTIASTHMATIQUE - code ATC : R03BA01
MIFLASONE est une poudre pour inhalation contenue dans une gélule. La poudre est administrée par voie inhalée à l'aide du dispositif (Aerolizer) fourni à cet effet.
La substance active contenue dans Milflasone est le dipropionate de béclométasone,
Le dipropionate de béclométasone est un corticoïde (également appelé corticostéroïde).
Dans quels cas est-il utilisé ?
Votre médecin vous a prescrit MIFLASONE pour le traitement de fond quotidien de votre asthme.
MIFLASONE est utilisé pour diminuer l’inflammation de vos poumons réduisant ainsi les symptômes de l’asthme. Il doit être utilisé régulièrement et quotidiennement. Il ne sera efficace qu’après plusieurs jours de traitement et seulement si vous respectez bien le nombre de doses et de prises indiquées par votre médecin. Il ne doit pas être interrompu sans avis médical, même en cas d'amélioration très nette des symptômes
Attention: ce médicament n'est pas un bronchodilatateur.
Il ne permet pas le traitement de la crise d'asthme.
MIFLASONE n’apporte pas de soulagement immédiat, et est notamment sans action sur la crise d’asthme déclarée.
Si vous faites une crise d’asthme, ou si vous éprouvez une gêne respiratoire, vous devez utiliser un autre médicament contenant un bronchodilatateur (bêta-2 mimétique d’action rapide et de courte durée) qui s’administre également par inhalation, et que votre médecin vous aura prescrit pour traiter les symptômes aigus d'asthme. Le soulagement habituellement obtenu avec le bronchodilatateur bêta2 mimétique par voie inhalée doit alors être observé rapidement.
Présentations
> plaquette(s) PVC-Aluminium PVDC avec inhalateur(s) de 60 gélule(s)
Code CIP : 356 595-5 ou 34009 356 595 5 2
Déclaration de commercialisation : 11/03/2002
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 8,47 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 9,49 €
- Taux de remboursement :65%
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 03/05/2017 | Renouvellement d'inscription (CT) | Le service médical rendu par MIFLASONE reste important dans l’indication de l’AMM. |
Amélioration du service médical rendu (ASMR)
Pas d'ASMR disponible pour ce médicament (plus d'informations dans l'aide )
ANSM - Mis à jour le : 20/09/2019
MIFLASONE 400 microgrammes, poudre pour inhalation en gélule
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Dipropionate de béclométasone........................................................................................ 400,00 µg
Quantité correspondant à béclométasone base....................................................................... 314 µg
Pour une gélule.
Excipient à effet notoire : lactose (pouvant contenir des traces de protéines de lait).
Pour la liste complète des excipients, voir rubrique 6.1.
Poudre pour inhalation en gélule.
4.1. Indications thérapeutiques
Traitement continu anti-inflammatoire de l'asthme persistant*.
*L'asthme persistant se définit par l'existence de symptômes diurnes plurihebdomadaires et/ou de symptômes nocturnes plus de 2 fois par mois.
Remarque:
Cette spécialité est particulièrement adaptée aux sujets chez qui il a été mis en évidence une mauvaise synchronisation main/poumon nécessaire pour une utilisation correcte des aérosols doseurs classiques sans chambre d'inhalation.
4.2. Posologie et mode d'administration
La dose initiale sera déterminée selon la sévérité de l’asthme avant traitement.
La posologie est strictement individuelle. La dose initiale sera déterminée selon la sévérité de l'asthme avant traitement et sera ensuite ajustée en fonction des résultats individuels.
· dans l'asthme persistant léger à modéré la dose initiale préconisée se situe entre :
o chez l'adulte : 400 et 1 000 microgrammes par jour à répartir en deux prises par jour,
o chez l'enfant : 200 et 500 microgrammes par jour à répartir en deux prises par jour.
· dans l'asthme persistant sévère la dose initiale préconisée est :
o chez l'adulte : 2000 microgrammes par jour,
o chez l'enfant : 1 000 microgrammes par jour.
Après plusieurs jours (ou semaines) de ce traitement lorsque l'état clinique du patient est amélioré, que les symptômes ont régressé et que l'asthme est contrôlé, la posologie minimale efficace devra être recherchée.
La dose totale quotidienne maximale ne doit pas dépasser 2000 microgrammes/jour chez l’adulte et 1000 microgrammes/jour chez l’enfant.
En cas d’asthme instable, la dose quotidienne pourra être administrée en 3 à 4 prises en fonction de l’état clinique du patient.
En cas d'utilisation d'une autre spécialité à base de béclométasone par voie inhalée, la posologie devra être réajustée individuellement.
Population pédiatrique
Il n'a pas été réalisé d'étude clinique chez l'enfant avec Miflasone. La possibilité d’utilisation de l'inhalateur Aerolizer dépend de la capacité de l’enfant à utiliser correctement ce dispositif. Ce dispositif n'est pas adapté pour l'administration aux enfants de moins de 6 ans.
Mode d’administration
Inhalation par distributeur avec embout buccal.
LES GELULES NE DOIVENT PAS ETRE AVALEES.
Leur contenu doit être administré par voie inhalée uniquement avec le dispositif d’inhalation Aerolizer fourni à cet effet dans la boite.
Pour une utilisation correcte, les patients doivent être formés à l’utilisation correcte de l’inhalateur en suivant les recommandations de la notice. Il est souhaitable que le médecin s'assure par lui-même du bon usage de l'appareil par le patient.
Mode d'emploi
1. Retirer le capuchon de protection.
2. Ouvrir le logement destiné à placer la gélule en tenant fermement le socle et faire pivoter l'embout buccal dans le sens de la flèche.
3. Avec des doigts bien secs, placer la gélule dans le logement prévu à cet effet (ne pas introduire la gélule dans l’embout buccal).
Important : sortir la gélule de son emballage au dernier moment.
4. Refermer l'inhalateur en remettant l'embout buccal dans sa position initiale jusqu’au déclic.
5. Pour libérer la poudre de la gélule, appuyer à fond sur les 2 boutons poussoirs latéraux en même temps en maintenant l'inhalateur en position verticale, puis relâcher. Cette opération a pour but de percer la gélule à ses extrémités afin que la poudre puisse être libérée lors de l'inspiration au travers de l'embout buccal. Il peut en résulter la formation de petits fragments de gélule composés de gélatine non nocive.
6. Expirer à fond à l'extérieur du dispositif.
7. Placer l'embout dans la bouche et serrer les lèvres, maintenir la tête droite, inspirer rapidement et profondément par la bouche.
NB: un léger vrombissement continu doit être entendu lorsque la gélule tournoie dans son logement. Si ce n’est pas le cas, vérifier que la gélule est bien en place.
8. Retirer l'inhalateur de la bouche en retenant sa respiration aussi longtemps que possible puis, respirer normalement. Ouvrir l'inhalateur pour vérifier qu'il ne reste plus de poudre dans la gélule. S'il reste de la poudre, renouveler l'inhalation.
9. Après utilisation, sortir la gélule vide de son logement, replacer l'embout buccal et remettre le capuchon de protection.
Afin de limiter le risque de candidose oropharyngée, il doit être recommandé aux patients de bien se rincer la bouche à l’eau après chaque inhalation du produit, en recrachant l’eau de rinçage (voir rubriques 4.4 et 4.8).
Entretien du dispositif d'inhalation
Nettoyer l'embout buccal et le logement de la gélule avec un linge sec afin d'enlever tout résidu de poudre.
Ne jamais laver l’inhalateur à l’eau.
Erreur d’administration
Des cas de patients ayant avalé par erreur des gélules de Miflasone au lieu de les placer dans le dispositif d’inhalation Aerolizer ont été rapportés. Dans la majorité des cas, ces ingestions n’ont pas entraîné d’effets indésirables. En cas d'inefficacité du traitement, il convient de vérifier que le patient n'avale pas les gélules au lieu d'en inhaler le contenu à l'aide de l'inhalateur prévu à cet effet.
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
4.4. Mises en garde spéciales et précautions d'emploi
Si en dépit d'un traitement bien conduit une dyspnée paroxystique survient, on doit avoir recours à un bronchodilatateur bêta-2 mimétique par voie inhalée d'action rapide et de courte durée pour traiter les symptômes aigus. Il conviendra d'en informer le patient et de lui préciser qu'une consultation médicale immédiate est nécessaire si, dans ce cas, le soulagement habituellement obtenu n'est pas rapidement observé après inhalation du bronchodilatateur bêta-2 mimétique.
Si un patient développe en quelques jours une augmentation rapide de sa consommation en bronchodilatateurs bêta-2 mimétiques d'action rapide et de courte durée par voie inhalée, il faut craindre (surtout si les valeurs du débitmètre de pointe s'abaissent et/ou deviennent irrégulières) une décompensation de l'asthme et la possibilité d'une évolution vers un asthme aigu grave (état de mal asthmatique). Le médecin devra prévenir le patient de la nécessité dans ce cas, d'une consultation immédiate. La conduite thérapeutique devra alors être réévaluée.
En cas de déstabilisation de l’asthme, ou de contrôle insuffisant des exacerbations d’asthme malgré des doses maximales de corticoïdes par voie inhalée, un traitement par corticothérapie par voie générale en cure courte doit être envisagé. Il est alors nécessaire de maintenir la corticothérapie inhalée associée au traitement par voie générale.
Le patient doit être averti que l'amélioration de son état clinique ne doit pas conduire à une modification de son traitement, en particulier à l'arrêt de la corticothérapie par voie inhalée, sans avis médical.
En cas d’infection bronchique ou de bronchorrhée abondante, un traitement approprié est nécessaire afin de favoriser la diffusion optimale du produit dans les voies respiratoires.
La prudence est requise en cas de tuberculose pulmonaire active ou quiescente, d’infection mycosique pulmonaire, l’instauration d’une surveillance étroite et d’un traitement adapté s’impose.
Risque de pneumonie : une augmentation de l’incidence des cas de pneumonie, ayant ou non nécessité une hospitalisation, a été observée chez les patients présentant une bronchopneumopathie chronique obstructive (BPCO) et recevant une corticothérapie inhalée. Bien que cela ne soit pas formellement démontré dans toutes les études cliniques disponibles, ce risque semble augmenter avec la dose de corticoïde administrée. Les données disponibles ne permettent pas de considérer que le niveau du risque de survenue de pneumonie varie en fonction du corticostéroïde inhalé utilisé. Il convient de rester vigilant chez les patients présentant une BPCO, les symptômes de pneumonie pouvant s'apparenter aux manifestations cliniques d'une exacerbation de BPCO. Le tabagisme, un âge avancé, un faible indice de masse corporelle (IMC) ainsi que la sévérité de la BPCO sont des facteurs de risques de survenue de pneumonie.
La corticothérapie inhalée peut entrainer une candidose oropharyngée pouvant nécessiter un traitement antifongique et un arrêt de la corticothérapie inhalée (voir également rubrique 4.2).
Une dysphonie peut apparaître. Elle est réversible à l’arrêt du traitement ou après réduction des doses et/ou après mise au repos de la voix (voir rubrique 4.8).
Comme avec les autres produits inhalés, un bronchospasme peut survenir se manifestant par une majoration des sibilants, une dyspnée et une toux immédiatement après la prise du médicament. Le bronchospasme sera traité avec un bronchodilatateur d’action rapide qui devra être administré immédiatement. Le traitement par MIFLASONE devra être arrêté immédiatement et la conduite thérapeutique sera réévaluée pour envisager, si nécessaire, les alternatives thérapeutiques.
La corticothérapie par voie inhalée peut entraîner des effets systémiques, en particulier lors de traitements à fortes doses ou prolongés. La survenue de ces effets avec la voie inhalée est beaucoup moins probable qu’au cours d’une corticothérapie orale. Les effets systémiques possibles sont : syndrome de Cushing ou tableau cushingoïde, amincissement cutané, ecchymoses, insuffisance surrénalienne, retard de croissance chez les enfants et les adolescents, diminution de la densité osseuse, cataracte et glaucome et plus rarement, troubles psychologiques et du comportement comprenant hyperactivité psychomotrice, troubles du sommeil, anxiété, dépression ou agressivité (en particulier chez l’enfant). Il est important de toujours rechercher la posologie minimale efficace de corticoïdes inhalés permettant d'obtenir le contrôle des symptômes d'asthme.
Des troubles visuels peuvent apparaitre lors d'une corticothérapie par voie systémique ou locale. En cas de vision floue ou d'apparition de tout autre symptôme visuel apparaissant au cours d'une corticothérapie, un examen ophtalmologique est requis à la recherche notamment d'une cataracte, d'un glaucome, ou d'une lésion plus rare telle qu'une choriorétinopathie séreuse centrale, décrits avec l'administration de corticostéroïdes par voie systémique ou locale.
Il convient de garder en mémoire les effets potentiels sur la densité minérale osseuse en particulier chez les patients recevant de fortes doses de corticoïdes par voie inhalée au long cours et présentant des facteurs de risque d’ostéoporose.
Les patients ayant nécessité de fortes doses de corticostéroïdes en urgence ou ayant reçu une corticothérapie inhalée au long cours aux posologies maximales recommandées, peuvent développer une insuffisance surrénalienne. Ces patients sont susceptibles de présenter des signes et des symptômes d’insuffisance surrénalienne lors de situation de stress sévère. Les signes d’une insuffisance surrénale aigue peuvent être non spécifiques : anorexie, douleurs abdominales, perte de poids, fatigue, céphalées, nausées, vomissements, perte de connaissance, convulsions, hypotension et hypoglycémie. Une corticothérapie de supplémentation devra être envisagée dans les situations susceptibles de déclencher un stress ou en cas de chirurgie programmée.
L’administration conjointe de corticoïdes par voie inhalée chez les asthmatiques sous corticothérapie orale au long cours (patients corticodépendants) ne dispense pas des précautions nécessaires lors d’une réduction des doses de corticoïde par voie orale. Celles-ci seront diminuées très progressivement et le sevrage devra être effectué sous surveillance médicale attentive (à la recherche de l’apparition de signes d’insuffisance surrénale aiguë ou subaiguë) qui peut persister pendant une période prolongée après l’arrêt de la corticothérapie par voie générale.
Lors du remplacement d'une corticothérapie orale par une corticothérapie inhalée, l’effet corticoïde systémique est diminué ce qui peut entrainer la réapparition de symptômes allergiques (tels que rhinite, eczéma) et/ou rhumatologiques (telles que des douleurs musculaires et articulaires). Un traitement spécifique devra être instauré. Une insuffisance glucocorticostéroïde doit être suspectée si, dans de rares cas, les symptômes suivants apparaissent : fatigue, céphalée, nausée et vomissements. Une augmentation temporaire des doses de corticoïdes oraux peut alors parfois être nécessaire.
Ce médicament contient du lactose. Le lactose est déconseillé chez les patients présentant une intolérance au galactose, un déficit en lactase de Lapp ou un syndrome de malabsorption du glucose ou du galactose (maladies héréditaires rares). De plus, le lactose peut contenir des traces de protéines de lait pouvant déclencher des réactions allergiques chez les patients allergiques aux protéines de lait (voir rubriques 4.3).
Population pédiatrique
La croissance des enfants recevant une corticothérapie inhalée au long cours doit être surveillée régulièrement. En cas de ralentissement de la croissance, le traitement devra être réévalué en vue de réduire les doses du corticoïde inhalé. Il conviendra de soigneusement peser les bénéfices attendus d’une corticothérapie face aux risques éventuels de ralentissement de la croissance. L’avis d’un spécialiste pneumo-pédiatre peut être requis.
Sportif
L'attention des sportifs sera attirée sur le fait que cette spécialité contient un principe actif pouvant induire une réaction positive des tests pratiqués lors des contrôles antidopage.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
+ Inhibiteurs du CYP 3A
Le métabolisme de la béclométasone est moins dépendant du CYP3A que celui de certains autres corticostéroïdes, et les interactions sont en général peu probables ; néanmoins, en cas d'utilisation concomitante d'inhibiteurs puissants du CYP3A (exemple: ritonavir, cobicistat), la possibilité d'effets systémiques ne peut être exclue et il est donc conseillé d'être prudent et d'appliquer une surveillance adéquate en cas d'utilisation concomitante de ces produits.
4.6. Fertilité, grossesse et allaitement
Grossesse
Chez l'animal, l'expérimentation a mis en évidence un effet tératogène des corticoïdes variable selon les espèces (voir rubrique 5.3).
Cependant, chez l’Homme, les études épidémiologiques n'ont décelé aucun risque malformatif lié à la prise de corticoïdes lors du premier trimestre bien qu'il existe un passage transplacentaire.
Lors de maladies chroniques nécessitant un traitement tout au long de la grossesse, un léger retard de croissance intra-utérin est possible. Une insuffisance surrénale néo-natale a été exceptionnellement observée après corticothérapie à dose élevée par voie systémique.
Ce médicament peut être prescrit au cours de la grossesse si besoin et en recherchant la dose minimale efficace, quel qu’en soit le terme.
La dose efficace la plus faible de dipropionate de beclometasone nécessaire pour maintenir un contrôle adéquat de l’asthme devrait être utilisée.
Il semble justifié d'observer une période de surveillance clinique (poids, diurèse) et biologique du nouveau-né.
Allaitement
Les corticoïdes passent dans le lait maternel.
Fertilité
Il n’y a pas de données disponibles sur l’effet potentiel du béclométasone sur la fertilité chez l'Homme.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Des effets systémiques peuvent apparaître lors de traitement au long cours avec des doses élevées (voir rubrique 4.4).
Les effets indésirables suivants sont issus de notifications spontanées et de cas rapportés dans la littérature, après commercialisation de MIFLASONE.
Infections et infestations
Candidose oropharyngée.
Troubles psychiatriques
Hyperactivité psychomotrice, troubles du sommeil, anxiété, syndrome dépressif, agressivité, troubles du comportement (principalement observés chez l’enfant).
Troubles respiratoires, thoraciques et médiastinaux
Gêne oropharyngée, dysphonie, raucité de la voix.
Bronchospasme.
Troubles oculaires
Cataracte, glaucome (très rare).
Vision floue (voir rubrique 4.4).
Troubles cutanés et- sous cutanés
Ecchymoses, amincissements cutanés.
Troubles musculo-squelettiques
Diminution de la densité osseuse, contractures musculaires.
Troubles endocriniens.
Altération des paramètres biologiques de la fonction surrénalienne
Inhibition des fonctions surrénaliennes.
Hypercorticisme, syndrome de Cushing.
Troubles du système immunitaires
Réactions d’hypersensibilité (rash cutané, prurit, urticaire, angioedème).
Il existe un risque de pneumonie avec les glucorcorticoïdes inhalés chez les patients atteints de BPCO (voir rubrique 4.4).
Population pédiatrique
Compte-tenu du risque de ralentissement de croissance dans la population pédiatrique, la croissance des enfants et des adolescents doit être surveillée régulièrement (voir rubrique 4.4.).
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.ansm.sante.fr.
L’emploi de ce médicament à des doses très supérieures aux doses recommandées est le reflet d’une aggravation de l’affection respiratoire nécessitant une consultation rapide pour réévaluation thérapeutique.
L’effet toxique attendu, après inhalation de doses élevées de béclométasone au long court est la dépression de la fonction hypothalamo-hypophyso-surrénalienne.
Un surdosage aigu en béclométasone même à doses excessives ne devrait pas avoir d’impact clinique.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : GLUCOCORTICOIDE PAR VOIE INHALEE, ANTIASTHMATIQUE, code ATC : R03BA01.
Mécanisme d’action
Le dipropionate de béclométasone (DPB) est un glucocorticoïde. Administré par voie inhalée, il exerce une action antiinflammatoire locale. L’effet thérapeutique du dipropionate de béclométasone inhalé est principalement dû au 17-monopropionate de béclométasone (17-MPB), et notamment à la fraction retenue au niveau pulmonaire.
Les corticoïdes inhalés (CI) exercent leurs effets anti- inflammatoires en se liant aux récepteurs intracellulaires des glucocorticoïdes.
5.2. Propriétés pharmacocinétiques
Après inhalation de la poudre, une partie de la dose de DPB est déglutie et l'autre partie pénètre dans les bronches où elle exerce ses effets.
Ces deux fractions contribuent à l’exposition systémique. Le DPB est presque complètement hydrolysé en 17-monopropionate de béclométasone (17-MPB) qui passe dans la circulation systémique. Environ 70% du DPB déglutie subit un métabolisme pré-systémique. La relation entre l’augmentation de la dose administrée par voie inhalée et l’exposition systémique est quasi-linéaire. Les pics de concentration plasmatique de DPB et de 17-MBP sont observés respectivement dans les 5 min et dans les 1 à 3 heures après l’administration.
Distribution
Après administration intraveineuse, les volumes de distribution à l’état d’équilibre du DPB et du 17-MPB sont respectivement de 20L et 424L. La liaison aux protéines plasmatiques est de 87% pour le DPB. Sa valeur n'est pas connue chez l'Homme pour le 17-MPB.
Biotransformation
Le DPB est très majoritairement hydrolysé par des estérases et des enzymes de la famille des CYP3A telles que CYP3A4 et CYP3A5. Le DPB peut être totalement hydrolysé en 17- et 21-MPB dans l’intestin, les cellules épithéliales, le sang ou le foie. Le 17- et le 21-MPB peuvent aussi être hydrolysés en béclométhasone ou métabolisés par oxydo-réductions en dérivés inactifs non identifiés.
Élimination
Les demi-vies d’élimination plasmatique du DPB et du 17-MPB sont respectivement de 30 min et 2,7 h après administration intraveineuse. L’excrétion rénale du DBP et de ses métabolites est négligeable, l’excrétion dans les selles étant la principale voie d’élimination.
5.3. Données de sécurité préclinique
Aucun effet indésirable n’a été observé sur la fertilité des souris mâles et femelles à des doses inhalées allant jusqu’à 464 milligrammes de dipropionate de béclométasone par kilogramme (mg/kg), soit 11 600 fois la dose maximale recommandée en pratique clinique, qui est de 40 microgrammes de dipropionate de béclométasone par kilogramme (µg/kg).
Toxicité sur la reproduction
Le dipropionate de béclométasone s’est montré tératogène chez la Souris à des doses de 0,058 mg/kg en cas d’administration par voie inhalée et de 0,1 mg/kg en cas d’administration par voie sous-cutanée, et chez le Lapin aux doses de 0,025 mg/kg. Ces doses sont proches de la dose maximale recommandée par voie inhalée en pratique clinique, soit 40 µg/kg.
Le dipropionate de béclométasone ne s’est pas montré tératogène chez le Rat ; comme dans d’autres espèces, un retard de développement a été observé à partir de la dose de 1,6 mg/kg.
Les effets tératogènes des glucocorticoïdes chez l’animal sont connus, mais on considère que ces effets sont réduits lorsque les corticoïdes sont administrés par voie inhalée et correctement utilisés (voir rubrique 4.6).
Le dipropionate de béclométasone a été à l’origine de retards de croissance dans des portées d’animaux, lorsqu’il a été administré au cours des périodes prénatale ou postnatale ou avant le sevrage. Ces effets se sont corrigés après le sevrage.
Mutagénicité
De nombreux tests menés in vitro et in vivo n’ont pas permis de révéler d’activité mutagène ou génotoxique du dipropionate de béclométasone.
Carcinogénicité
Aucune preuve de carcinogénicité n’a été identifiée chez le Rat après 95 semaines de traitement par le dipropionate de béclométasone à des doses allant jusqu’à 2,4 mg/kg/jour en associant les voies d’administration inhalée et orale. La dose de 2,4 mg/kg/jour chez le Rat est équivalente à une dose de 17,85 mg/m2, soit 12,8 fois la dose maximale recommandée chez l’adulte (1,39 mg/m2), en considérant une exposition systémique maximale après inhalation de la dose de dipropionate de béclométasone.
Lactose monohydraté (pouvant contenir des traces de protéines de lait).
Composition de l’enveloppe de la gélule : gélatine, oxyde de fer noir (E172), oxyde de fer rouge (E172), oxyde de fer jaune (E172), dioxyde de titane (E171).
Composition de l’encre noire d’impression : laque (E904), alcool déshydraté, alcool isopropylique, alcool butylique, propylène glycol (E1520), solution d’ammoniaque concentrée (E527), oxyde de fer noir (E172), hydroxyde de potassium (E525), eau purifiée.
3 ans.
6.4. Précautions particulières de conservation
A conserver à une température ne dépassant pas 25°C.
A conserver dans l'emballage extérieur, à l'abri de l'humidité.
A conserver dans le conditionnement primaire d'origine, à l'abri de la lumière.
6.5. Nature et contenu de l'emballage extérieur
Gélules sous plaquettes (PVC/PVDC/Aluminium) avec inhalateur. Boîte de 30, 60 ou 120 gélules.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
8-10 RUE HENRI SAINTE-CLAIRE DEVILLE
92500 RUEIL-MALMAISON
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· CIP 34009 356 594 9 1 : 30 gélules sous plaquettes (PVC/PVDC/Aluminium) avec inhalateur.
· CIP 34009 356 595 5 2 : 60 gélules sous plaquettes (PVC/PVDC/Aluminium) avec inhalateur.
· CIP 34009 356 596 1 3 : 120 gélules sous plaquettes (PVC/PVDC/Aluminium) avec inhalateur.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
<{JJ mois AAAA}>
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I
ANSM - Mis à jour le : 20/09/2019
MIFLASONE 400 microgrammes, poudre pour inhalation en gélule
Dipropionate de béclométasone
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que MIFLASONE 400 microgrammes, poudre pour inhalation en gélule et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser MIFLASONE 400 microgrammes, poudre pour inhalation en gélule ?
3. Comment utiliser MIFLASONE 400 microgrammes, poudre pour inhalation en gélule ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver MIFLASONE 400 microgrammes, poudre pour inhalation en gélule ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE MIFLASONE 400 microgrammes, poudre pour inhalation en gélule ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : GLUCOCORTICOIDE PAR VOIE INHALEE, ANTIASTHMATIQUE - code ATC : R03BA01
MIFLASONE est une poudre pour inhalation contenue dans une gélule. La poudre est administrée par voie inhalée à l'aide du dispositif (Aerolizer) fourni à cet effet.
La substance active contenue dans Milflasone est le dipropionate de béclométasone,
Le dipropionate de béclométasone est un corticoïde (également appelé corticostéroïde).
Dans quels cas est-il utilisé ?
Votre médecin vous a prescrit MIFLASONE pour le traitement de fond quotidien de votre asthme.
MIFLASONE est utilisé pour diminuer l’inflammation de vos poumons réduisant ainsi les symptômes de l’asthme. Il doit être utilisé régulièrement et quotidiennement. Il ne sera efficace qu’après plusieurs jours de traitement et seulement si vous respectez bien le nombre de doses et de prises indiquées par votre médecin. Il ne doit pas être interrompu sans avis médical, même en cas d'amélioration très nette des symptômes
Attention: ce médicament n'est pas un bronchodilatateur.
Il ne permet pas le traitement de la crise d'asthme.
MIFLASONE n’apporte pas de soulagement immédiat, et est notamment sans action sur la crise d’asthme déclarée.
Si vous faites une crise d’asthme, ou si vous éprouvez une gêne respiratoire, vous devez utiliser un autre médicament contenant un bronchodilatateur (bêta-2 mimétique d’action rapide et de courte durée) qui s’administre également par inhalation, et que votre médecin vous aura prescrit pour traiter les symptômes aigus d'asthme. Le soulagement habituellement obtenu avec le bronchodilatateur bêta2 mimétique par voie inhalée doit alors être observé rapidement.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER MIFLASONE 400 microgrammes, poudre pour inhalation en gélule ?
N’utilisez jamais MIFLASONE 400 microgrammes, poudre pour inhalation en gélule :
Si vous êtes allergique à la substance active ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
Avertissements et précautions
Adressez-vous à votre médecin ou pharmacien avant d’utiliser MIFLASONE 400 microgrammes, poudre pour inhalation.
Si la dose habituellement efficace de MIFLASONE devient insuffisante, si les crises ou les épisodes de gêne respiratoire deviennent plus fréquents, il faut craindre une aggravation de l'asthme, consultez rapidement votre médecin qui réévaluera votre traitement.
Ce produit, actif en inhalation doit atteindre l'extrémité des bronches dans vos poumons. En cas d'encombrement des voies respiratoires (par des mucosités abondantes) ou d'infection, son efficacité peut être diminuée. Il convient de consulter rapidement votre médecin afin qu'il instaure un traitement adapté.
En cas de fièvre, toux, difficulté à respirer, sifflements, douleurs thoraciques en respirant qui surviendraient en cours de traitement, consultez votre médecin.
Si vous avez eu dans le passé une tuberculose pulmonaire ou une autre maladie respiratoire, parlez-en à votre médecin avant d’utiliser MIFLASONE.
En cas d'apparition d'une vision floue ou d'autres troubles visuels survenant en cours de traitement, consulter votre médecin.
Si vous recevez un traitement corticoïde par voie orale (ex : comprimés) lorsque vous débutez votre traitement par MIFLASONE, n’arrêtez pas brutalement de prendre vos comprimés. Votre médecin vous donnera les instructions nécessaires pour diminuer progressivement la dose des corticoïdes par voie orale.
Ce médicament contient du lactose. Le lactose est déconseillé chez les patients présentant une intolérance au galactose, un déficit en lactase de Lapp ou un syndrome de malabsorption du glucose ou du galactose (maladies héréditaires rares). Le lactose peut contenir des protéines de lait qui peuvent déclencher des réactions allergiques chez les personnes allergiques aux protéines de lait. Si vous êtes allergiques aux protéines de lait, n'utilisez pas ce médicament. Contactez votre médecin.
Enfants et adolescents
Le dispositif d'inhalation de MIFLASONE n'est pas adapté aux enfants de moins de 6 ans.
En cas d’utilisation prolongée et à fortes doses chez l’enfant ou l'adolescent, le médecin contrôlera régulièrement la taille de l’enfant ou l'adolescent.
Autres médicaments et MIFLASONE 400 microgrammes, poudre pour inhalation en gélule
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
Certains médicaments peuvent augmenter les effets de Miflasone et il est possible que votre médecin souhaite vous surveiller attentivement si vous prenez ces médicaments (y compris certains médicaments pour traiter l'infection à VIH : ritonavir, cobicistat).
En cas de doute demandez conseil à votre médecin ou à votre pharmacien.
MIFLASONE 400 microgrammes, poudre pour inhalation en gélule avec des aliments et boissons
Sans objet.
Ce médicament dans les conditions normales d'utilisation peut être utilisé pendant la grossesse et l’allaitement.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
Sportifs
Attention cette spécialité contient un principe actif (béclométasone) pouvant induire une réaction positive des tests pratiqués lors des contrôles antidopage.
Conduite de véhicules et utilisation de machines
MIFLASONE n'affecte pas la capacité à conduire ou à utiliser des machines.
MIFLASONE 400 microgrammes, poudre pour inhalation en gélule contient du lactose (pouvant contenir des traces de protéines de lait).
3. COMMENT UTILISER MIFLASONE 400 microgrammes, poudre pour inhalation en gélule ?
NE PAS AVALER LES GELULES DE MIFLASONE.
LA POUDRE CONTENUE DANS LES GELLULES DOIT ETRE INHALEE AVEC L’INHALATEUR (AEROLIZER) FOURNI A CET EFFET.
Voir les instructions d’utilisation de l'inhalateur détaillées ci-dessous.
Respectez toujours la posologie prescrite (nombre de doses et rythme des prises indiqués par votre médecin).
Veillez à toujours utiliser ce médicament en suivant exactement les indications de votre médecin ou pharmacien. Vérifiez auprès de votre médecin ou pharmacien en cas de doute.
Posologie
La dose est strictement individuelle et sera adaptée par votre médecin en fonction de la sévérité de votre asthme.
Il existe trois dosages pour les gélules de MIFLASONE : 100 microgrammes, 200 microgrammes et 400 microgrammes pour ajuster la posologie qui vous convient.
A titre d’information, la dose quotidienne recommandée de ce médicament est :
· Chez l’adulte : 400 à 1000 microgrammes en 2 prises par jour. Si nécessaire, votre médecin pourra augmenter la dose jusqu’à 2000 microgrammes répartis en 2 prises par jour.
· Chez l’enfant à partir de 6 ans : 200 à 500 microgrammes en 2 prises par jour. Si nécessaire, votre médecin pourra augmenter la dose jusqu’à 1000 microgrammes répartis en 2 prises par jour.
Selon les cas, votre médecin pourra vous demander de prendre votre traitement en répartissant la dose quotidienne en 3 à 4 prises par jour.
Ce dispositif d'inhalation (Aerolizer) n'est pas adapté aux enfants de moins de 6 ans.
Si vous avez l’impression que l’effet de MIFLASONE est insuffisant
Si la dose que vous prenez habituellement devient insuffisante, si les crises ou les gênes respiratoires deviennent plus fréquentes, il est possible que cela soit dû à une aggravation de votre asthme. Vous devez alors consulter rapidement votre médecin qui réévaluera votre traitement.
Mode d’administration
Voie inhalée.
Instructions pour la bonne utilisation :
· Vous ne devez pas avaler les gélules.
· La poudre contenue dans ce médicament est destinée à être inhalée. Pour cela, vous disposez d’un inhalateur avec un embout buccal prévu à cet effet : l'inhalateur Aerolizer fourni. Le médicament contenu dans la gélule se déposera dans les bronches lorsque vous inspirerez au travers de l’embout buccal de l’inhalateur.
· L'efficacité de ce médicament est en partie dépendante du bon usage de l'appareil de l’inhalateur. Il convient donc de lire très attentivement le mode d’emploi (voir ci-dessous). Au besoin, n’hésitez pas à demander à votre médecin ou votre pharmacien de vous fournir des explications détaillées.
· Si ce médicament est prescrit à votre enfant, assurez-vous qu’il utilise correctement le dispositif inhalateur. Le dispositif d'inhalation de ce médicament n'est pas adapté aux enfants de moins de 6 ans.
Comment utiliser les gélules avec l’inhalateur (Aerolizer) fourni
|
Les gélules de MIFLASONE doivent être utilisées uniquement avec l’inhalateur Aerolizer fourni avec MIFLASONE. |
|
|
|
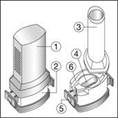
Le dispositif Aerolizer est composé des éléments suivants : 1. Un capuchon de protection 2. L'inhalateur qui permet la libération du médicament à partir de la gélule
L'inhalateur comprend :
1. Un embout buccal 2. Un logement pour la gélule 3. Des boutons poussoirs latéraux 4. Un orifice permettant le passage de l’air |
|
|
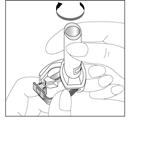
1. Retirez le capuchon de protection.
|
|
|
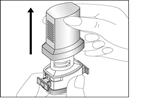
2. Ouvrez le logement de la gélule : tenez fermement le socle et faites pivoter l’embout buccal dans le sens de la flèche.
|
|
|
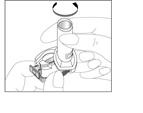
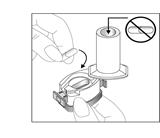
3. Avec des doigts bien secs, placez la gélule dans le logement prévu à cet effet (attention, ne mettez pas la gélule dans l’embout buccal)
Important : sortez la gélule de son emballage au dernier moment.
|
|
|
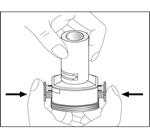
4. Refermez l’inhalateur en remettant l’embout buccal dans sa position initiale jusqu’au déclic.
|
|
|
5. Pour libérer la poudre de la gélule, appuyez à fond sur les 2 boutons poussoirs latéraux en même temps en maintenant l’inhalateur en position verticale, puis relâchez. Faire cette opération une seule fois. Cette opération a pour but de percer la gélule à ses extrémités. NB: la gélule peut se fragmenter en petits morceaux qui peuvent atteindre la bouche ou la gorge après inhalation. Ces petits fragments sont composés de gélatine comestible non nocive.
|
|
|
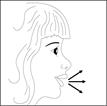
6. Expirez à fond en dehors de l'embout buccal.
|
|
|
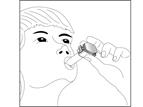
7. Placez l’embout dans la bouche et serrez les lèvres, inclinez la tête en arrière, inspirez rapidement et profondément par la bouche.
Note : un léger vrombissement continu doit être entendu lorsque la gélule tournoie dans son logement. Si ce n’est pas le cas, vérifiez que la gélule est bien en place.
|
|
|
8. Retirez l’inhalateur de la bouche en retenant sa respiration aussi longtemps que possible, puis, respirez normalement.
|
|
|
9. Ouvrez l’inhalateur pour vérifier qu’il ne reste plus de poudre dans la gélule. S’il reste de la poudre, renouvelez l’inhalation.
|
|
|
10. Rincez-vous la bouche après l’inhalation du produit. Cela permet de prévenir l’apparition d’une candidose buccale (infection à champignons microscopiques). Voir également la rubrique 4 ci-après.
|
|
|
11. Après l’utilisation : o sortez la gélule vide de son logement, o replacez l’embout buccal, o et remettez le capuchon de protection. |
|
Entretien :
|
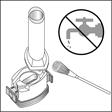
o Nettoyez l’embout buccal et le logement de la gélule avec un linge sec afin d’enlever tout résidu de poudre. o Ne lavez jamais l’inhalateur à l’eau. |
Fréquence d’administration
Les prises doivent être réparties dans la journée à intervalles réguliers.
Durée du traitement
Le traitement de l’asthme est quotidien. Ce médicament doit être utilisé très régulièrement et aussi longtemps que votre médecin vous l’aura prescrit.
Si vous avez utilisé plus de MIFLASONE 400 microgrammes, poudre pour inhalation que vous n’auriez dû
Consultez votre médecin ou votre pharmacien et montrez-leur l’emballage de MIFLASONE.
Si vous oubliez d’utiliser MIFLASONE 400 microgrammes, poudre pour inhalation
Ne prenez pas de dose double pour compenser la dose simple que vous avez oublié de prendre.
Si vous arrêtez d’utiliser MIFLASONE 400 microgrammes, poudre pour inhalation
L’arrêt de MIFLASONE peut augmenter le risque d’aggravation de votre asthme. N’arrêtez pas votre traitement sans avis médical.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
De rares cas de réactions allergiques ont été signalés. Elles se manifestent par la brusque apparition d'un gonflement du visage, de la langue et/ou gorge, de difficulté pour avaler ou pour respirer, d'éruption cutanée (urticaire) et/ou sensation de malaise après l'administration de MIFLASONE. Dans ce cas, vous devez cesser d’utiliser MIFLASONE et consulter votre médecin immédiatement.
Si vous êtes sensible à l’inhalation d’une poudre sèche, il peut apparaître une irritation de la gorge avec une toux et un enrouement ou une voix rauque. Vous pouvez éviter ces effets indésirables en vous rinçant la bouche après avoir utilisé le médicament. En cas de gêne persistante dans la bouche ou dans la gorge, avertissez votre médecin. Ne modifiez pas ou n’arrêtez pas le traitement sans son avis.
Une candidose buccale (infection à champignons microscopiques apparaissant dans la bouche) peut parfois survenir. Cette situation ne nécessite pas forcément un arrêt de MIFLASONE. Votre médecin pourra vous prescrire un traitement spécifique pour la soigner. Vous pouvez éviter cet effet indésirable en vous rinçant la bouche après avoir utilisé le médicament.
Les corticoïdes inhalés à forte dose ou administrés durant une longue durée peuvent interférer sur la fonction des glandes surrénales, pouvant se manifester par des symptômes tels que : fatigue, perte de poids, nausées et diarrhées persistantes, causés par un mauvais fonctionnement de ces glandes.
Si vous ressentez ces symptômes, consulter votre médecin.
Autres effets indésirables possibles :
· agitation, troubles du sommeil, anxiété, dépression, agressivité, troubles du comportement (principalement observés chez l’enfant)
· fragilisation osseuse (ostéoporose)
· altération des paramètres biologiques de la fonction surrénalienne
· ecchymoses (« bleus » sur la peau), amincissement de la peau
· crampes musculaires
· très rarement troubles oculaires : glaucome (augmentation de la pression à l’intérieur de l’œil), cataracte (opacification du cristallin de l’œil), vision floue
· bronchospasme (réduction du calibre des bronches) se traduisant par une gêne respiratoire et une respiration sifflante. Si ces symptômes apparaissent juste après l'inhalation de ce médicament, ne renouvelez pas la prise de MIFLASONE et contactez immédiatement votre médecin
· hypercorticisme appelé également syndrome de Cushing qui se manifeste par une augmentation du poids, un aspect lunaire du visage, une fatigue et/ou une augmentation du périmètre abdominal.
Effets indésirables supplémentaires chez les enfants et les adolescents
Un ralentissement de croissance peut être observé chez l’enfant et l’adolescent lors d’un traitement au long cours et à forte dose par Miflasone. Le médecin surveillera la croissance de l’enfant.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: www.ansm.sante.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER MIFLASONE 400 microgrammes, poudre pour inhalation en gélule ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur la boite après « EXP ». La date de péremption fait référence au dernier jour de ce mois.
A conserver à une température ne dépassant pas 25°C à l'abri de la lumière et de l'humidité.
A conserver dans l’emballage extérieur d’origine.
N’utilisez pas ce médicament si vous remarquez des signes visibles de détérioration.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient MIFLASONE 400 microgrammes, poudre pour inhalation en gélule
· La substance active est :
Dipropionate de béclométasone................................................................... 400 microgrammes
Quantité correspondant à béclométasone base : 314 microgrammes
pour une gélule.
· Les autres composants sont :
Lactose monohydraté (pouvant contenir des traces de protéines de lait).
Composition de l’enveloppe de la gélule : gélatine, oxyde de fer noir (E172), oxyde de fer rouge (E172), oxyde de fer jaune (E172), dioxyde de titane (E171).
Composition de l’encre noire d’impression : laque (E904), alcool déshydraté, alcool isopropylique, alcool butylique, propylène glycol (E1520), solution d’ammoniaque concentrée (E527), oxyde de fer noir (E172), hydroxyde de potassium (E525), eau purifiée.
Poudre pour inhalation en gélule.
Boîte de 30, 60 ou 120 gélules avec un inhalateur.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
8-10 RUE HENRI SAINTE-CLAIRE DEVILLE
92500 RUEIL-MALMAISON
Exploitant de l’autorisation de mise sur le marché
49 AVENUE GEORGES POMPIDOU
92593 LEVALLOIS-PERRET CEDEX
8-10 RUE HENRI SAINTE-CLAIRE DEVILLE
92500 RUEIL-MALMAISON
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
< {MM/AAAA}>< {mois AAAA}.>
Sans objet.
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).