Dernière mise à jour le 08/01/2026
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution
Indications thérapeutiques
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution est utilisé pour traiter une pression élevée à l’intérieur de l’œil chez les adultes, y compris les personnes âgées. Cette pression peut conduire à une maladie appelée glaucome.
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution est une solution stérile qui ne contient pas de conservateur.
Présentations
> 1 flacon(s) multidose(s) en polypropylène de 2,5 ml de collyre muni d'une pompe, d'un cylindre à pression et d'un capuchon
Code CIP : 34009 301 361 8 8
Déclaration de commercialisation : 05/06/2024
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 11,92 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 12,94 €
- Taux de remboursement :65%
> 3 flacon(s) multidose(s) en polypropylène de 2,5 ml de collyre muni d'une pompe, d'un cylindre à pression et d'un capuchon
Code CIP : 34009 301 857 0 4
Déclaration de commercialisation : 05/06/2024
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 33,78 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 34,80 €
- Taux de remboursement :65 %
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 05/12/2018 | Inscription (CT) | Le service médical rendu par KIVIZIDIALE 40 µg/ml + 5 mg/ml, collyre en solution, est important dans l’indication de l’AMM. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 05/12/2018 | Inscription (CT) | KIVIZIDIALE 40 µg/ml + 5 mg/ml, collyre en solution, n’apporte pas d’amélioration du service médical rendu (ASMR V) par rapport à DUOTRAV 40 µg/ml + 5 mg/ml, collyre en solution. |
ANSM - Mis à jour le : 13/12/2022
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chaque mL de solution contient 40 microgrammes de travoprost et 5 mg de timolol (sous forme de maléate de timolol).
Excipient à effet notoire :
Chaque mL de solution contient 2 mg d’hydroxystéarate de macrogolglycérol 40 (voir rubrique 4.4).
Pour la liste complète des excipients, voir rubrique 6.1.
Solution aqueuse, incolore, limpide, pratiquement sans particules.
pH : 5,5 - 7,5
Osmolarité : 290 mOsm/kg ± 10 % (261 - 319 mOsm/kg)
4.1. Indications thérapeutiques
4.2. Posologie et mode d'administration
Utilisation chez les adultes y compris les sujets âgés.
La posologie est d'une goutte de KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution dans le cul de sac conjonctival de l’œil ou des yeux atteint(s), une fois par jour, le matin ou le soir. Il doit être administré tous les jours à la même heure.
Si une instillation est oubliée, le traitement doit être poursuivi avec l'instillation suivante. La posologie ne doit pas dépasser une goutte par jour dans l'œil ou les yeux atteint(s).
Populations particulières
Insuffisance hépatique et rénale
Aucune étude n'a été effectuée avec Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution ou avec timolol 5 mg/mL, collyre chez les patients souffrant d’une insuffisance hépatique ou rénale.
Le travoprost a été étudié chez les patients souffrant d’une insuffisance hépatique modérée à sévère et chez les patients souffrant d’une insuffisance rénale modérée à sévère (clairance de la créatinine jusqu’à 14 mL/min). Aucun ajustement de la posologie n’est nécessaire chez ces patients.
Les patients souffrant d’insuffisance hépatique ou rénale ne nécessitent pas d’adaptation de la posologie avec KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution (voir rubrique 5.2).
Population pédiatrique
La sécurité et l’efficacité de KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution chez les enfants et adolescents de moins de 18 ans n’ont pas été établies. Aucune donnée n’est disponible.
Mode d’administration
Voie oculaire.
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution est une solution stérile qui ne contient pas de conservateur.
Les patients doivent être informés de se laver les mains avant utilisation et éviter le contact de l'embout du flacon avec l'œil ou les structures environnantes afin d’éviter tout risque de blessure.
Les patients doivent être également informés qu’une solution oculaire, utilisée de façon inappropriée, peut être contaminée par des bactéries courantes, connues pour causer des infections oculaires. L'utilisation de solutions contaminées peut causer de graves lésions oculaires et entraîner une perte de la vue.
Pour éviter la contamination de l’embout compte-gouttes et de la solution, il faut faire attention de ne pas toucher les paupières, les zones voisines ou d’autres surfaces avec l’embout compte-gouttes du flacon.
Le passage systémique peut être réduit par une occlusion nasolacrymale ou la fermeture des paupières pendant 2 minutes. Cette méthode peut contribuer à diminuer les effets indésirables systémiques et à augmenter l'efficacité locale (voir rubrique 4.4).
En cas d’utilisation concomitante de plusieurs collyres, les instillations doivent être espacées d’au moins 5 minutes (voir rubrique 4.5).
En cas de remplacement d’un autre médicament ophtalmique antiglaucomateux par KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution, interrompre l’autre médicament et commencer KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution le jour suivant.
Les patients doivent enlever leurs lentilles de contact avant l’instillation de KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution et attendre 15 minutes après l’instillation avant de les remettre (voir rubrique 4.4).
· Hypersensibilité aux substances actives, ou à l’un des excipients mentionnés à la rubrique 6.1.
· Hypersensibilité aux autres bêta-bloquants.
· Pathologies associées à une hyperréactivité bronchique notamment asthme ou antécédents d’asthme et bronchopneumopathie chronique obstructive (BPCO) sévère.
· Bradycardie sinusale, syndrome de dysfonctionnement sinusal, y compris le bloc sino-auriculaire, bloc auriculo-ventriculaire du second ou du troisième degré non contrôlé par un pacemaker.
· Insuffisance cardiaque confirmée, choc cardiogénique.
· Rhinite allergique sévère et dystrophies cornéennes.
4.4. Mises en garde spéciales et précautions d'emploi
Comme d'autres médicaments ophtalmiques à usage local, le travoprost et le timolol passent dans la circulation générale. Du fait de la présence d’un composant bêta-adrénergique, le timolol, des effets indésirables, cardiovasculaires, pulmonaires et autres, d’autres effets indésirables identiques à ceux rencontrés avec les médicaments bêta-bloquants administrés par voie systémique peuvent se produire. La fréquence des effets indésirables systémiques après administration par voie ophtalmique locale est plus faible qu’après administration par voie générale. Pour plus d’informations sur la façon de réduire l’absorption systémique, voir rubrique 4.2.
Affections cardiaques
Chez les patients atteints de maladies cardiovasculaires (par exemple : maladie coronarienne, angor de Prinzmetal et insuffisance cardiaque) et d'hypotension, le traitement par bêta-bloquants doit être soigneusement évalué et un traitement avec d'autres substances actives doit être considéré. Les patients atteints de maladies cardiovasculaires doivent être surveillés afin de détecter des signes d’aggravation de ces pathologies ou des effets indésirables.
En raison de leur effet dromotrope négatif, les bêta-bloquants ne devront être prescrits qu’avec prudence aux patients atteints d’un bloc cardiaque de premier degré.
Affections vasculaires
Les patients atteints de troubles circulatoires périphériques sévères (c'est-à-dire des formes sévères de la maladie ou du syndrome de Raynaud) doivent être traités avec prudence.
Affections respiratoires
Chez les patients asthmatiques, des manifestations respiratoires pouvant aller jusqu'au décès par bronchospasme, ont été rapportées après administration de certains bêta-bloquants ophtalmiques.
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution doit être administré avec prudence chez les patients souffrant de bronchopneumopathie chronique obstructive (BPCO) légère à modérée et seulement si le bénéfice potentiel semble supérieur au risque potentiel.
Hypoglycémie / diabète
Les bêta-bloquants doivent être administrés avec prudence chez les patients sujets à des hypoglycémies spontanées ou chez les patients présentant un diabète instable, dans la mesure où les bêta-bloquants sont susceptibles de masquer les signes et symptômes d’une hypoglycémie aiguë.
Faiblesse musculaire
Il a été rapporté que les médicaments bêta-bloquants pouvaient aggraver la faiblesse musculaire accompagnant certains symptômes de la myasthénie (par exemple : diplopie, ptosis et faiblesse générale).
Maladies cornéennes
Les bêta-bloquants ophtalmiques peuvent entrainer une sécheresse oculaire. Les patients souffrant de maladies cornéennes doivent être traités avec prudence.
Décollement choroïdien
Des décollements de la choroïde ont été observés, après chirurgie filtrante du glaucome, lors de l'administration de traitements diminuant la sécrétion d'humeur aqueuse (par exemple : timolol, acétazolamide).
Autres bêta-bloquants
L’effet sur la pression intraoculaire ou les effets connus des bêta-bloquants systémiques peuvent être majorés en cas d'administration de timolol aux patients recevant déjà un médicament bêta-bloquant par voie systémique. La réponse de ces patients doit être surveillée attentivement. L’utilisation concomitante de deux agents bloquants bêta-adrénergiques topiques n’est pas recommandée (voir rubrique 4.5).
Anesthésie chirurgicale
Les bêta-bloquants utilisés en ophtalmologie peuvent bloquer les effets des agents bêta-agonistes systémiques tels que l'adrénaline. L’anesthésiste doit être informé lorsque le patient reçoit du timolol.
Hyperthyroïdie
Les bêta-bloquants peuvent masquer les signes d'hyperthyroïdie.
Contact cutané
Les prostaglandines et les analogues de prostaglandines sont des substances biologiquement actives pouvant être absorbées par la peau. Les femmes enceintes ou souhaitant le devenir devront prendre des précautions appropriées afin d’éviter une exposition directe au contenu du flacon. En cas de contact accidentel avec le contenu du flacon, nettoyer immédiatement et soigneusement la zone concernée.
Réactions anaphylactiques
Les patients traités par des bêta-bloquants et ayant des antécédents d'atopie ou de réactions anaphylactiques graves à différents allergènes peuvent être plus réactifs à des administrations répétées de tels allergènes et ne pas répondre aux doses d'adrénaline habituellement utilisées pour traiter les réactions anaphylactiques.
Traitement concomitant
Des interactions du timolol avec d’autres médicaments ont été décrites (voir rubrique 4.5).
L'utilisation de deux prostaglandines topiques n'est pas recommandée.
Effets oculaires
Le travoprost peut modifier progressivement la couleur des yeux en augmentant le nombre de mélanosomes (granules pigmentaires) dans les mélanocytes. Avant l’instauration du traitement, les patients doivent être informés du risque de changement permanent de la couleur de l’œil. Un traitement unilatéral peut avoir pour conséquence une hétérochromie définitive. Les effets à long terme sur les mélanocytes et leurs conséquences ne sont actuellement pas connus. La modification de couleur de l’iris évolue lentement et peut passer inaperçue pendant des mois, voire des années. Le changement de la couleur des yeux a surtout été observé chez des patients ayant l’iris bicolore, c’est-à-dire bleu-marron, gris-marron, jaune-marron et vert-marron ; cependant il a également été observé chez des patients ayant des yeux marrons. Généralement, pour l’œil concerné, la pigmentation brune entourant la pupille s’étend de façon concentrique vers la périphérie, mais l’iris peut devenir, en partie ou en totalité, brun plus foncé. Après l’arrêt du traitement, aucune augmentation ultérieure de la pigmentation brune de l’iris n’a été observée.
Au cours des essais cliniques contrôlés, un assombrissement de la peau périorbitaire et/ou palpébrale associé à l’utilisation du travoprost a été rapporté.
Des modifications périorbitaires et palpébrales, incluant un approfondissement du sillon palpébral, ont été observées avec les analogues de prostaglandines.
Le travoprost peut modifier progressivement les cils de l’œil ou des yeux traité(s). Au cours des essais cliniques, ces changements, représentés par une augmentation de la longueur, de l’épaisseur, de la pigmentation et/ou du nombre de cils, ont été observés chez la moitié des patients environ. Le mécanisme de modification des cils et ses conséquences à long terme sont actuellement inconnus.
Lors des études chez le singe, le travoprost a entraîné une légère augmentation de la fente palpébrale. Cependant, cet effet n’a pas été observé au cours des essais cliniques et il est considéré comme étant spécifique à l’espèce.
Il n’y a aucune donnée concernant l’utilisation de Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution sur un œil inflammatoire, ni en cas de glaucome néovasculaire, à angle étroit ou à angle fermé ou congénital. L’expérience est encore limitée en ce qui concerne les atteintes oculaires d’origine thyroïdienne, le glaucome à angle ouvert des patients pseudophaques et les glaucomes pigmentaires ou pseudoexfoliatifs.
Des œdèmes maculaires ont été rapportés durant le traitement avec les analogues de la prostaglandine F2α. Il est recommandé d’utiliser KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution avec précaution chez des patients aphaques, pseudophaques présentant une rupture de la capsule postérieure ou porteurs d’implant de chambre antérieure ou chez des patients présentant des facteurs de risques connus d’œdème maculaire cystoïde.
Chez les patients présentant des facteurs de risques connus prédisposant aux iritis/uvéites, et chez les patients présentant une inflammation intraoculaire active, KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution devra être utilisé avec précaution.
Les patients doivent être informés d’enlever leurs lentilles de contact avant l’instillation de KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution et d’attendre 15 minutes après l’instillation avant de les remettre (voir rubrique 4.2).
Excipients
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution contient de l’hydroxystéarate de macrogolglycérol 40, qui peut entrainer des réactions cutanées.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Un effet additif, entrainant une hypotension et/ou une bradycardie marquée, peut être observé lors de l’administration concomitante de collyre bêta-bloquant avec des inhibiteurs des canaux calciques, des agents bloquants bêta-adrénergiques, des antiarythmiques (notamment l’amiodarone), des glycosides digitaliques, des parasympathomimétiques, ou de la guanéthidine, administrés par voie orale.
La poussée hypertensive réactionnelle survenant lors de l'arrêt brutal de la clonidine peut être accentuée lors de la prise de bêta-bloquants.
Une potentialisation de l’effet bêta-bloquant systémique (par exemple : diminution du rythme cardiaque, dépression) a été rapportée lors de l’association de traitements inhibiteurs du CYP2D6 (par exemple : quinidine, fluoxétine, et paroxétine) et de timolol.
Des mydriases ont été occasionnellement rapportées lorsque les bêta-bloquants ophtalmiques et l'adrénaline (épinéphrine) ont été utilisés de façon concomitante.
Les bêta-bloquants peuvent majorer l'effet hypoglycémiant des médicaments antidiabétiques.
Les bêta-bloquants peuvent masquer les signes et les symptômes de l'hypoglycémie (voir rubrique 4.4).
4.6. Fertilité, grossesse et allaitement
Femmes susceptibles d’être enceintes/contraception
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution ne doit pas être utilisé chez la femme en âge de procréer à moins qu’une contraception adéquate ne soit mise en place (voir rubrique 5.3).
Grossesse
Le travoprost a des effets pharmacologiques nocifs sur la grossesse et/ou chez le fœtus/nouveau-né.
Il n’existe pas ou peu de données sur l’utilisation de Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution ou de ses composants individuels chez la femme enceinte. Le timolol ne doit pas être utilisé au cours de la grossesse sauf en cas de nécessité absolue.
Les études épidémiologiques n'ont pas révélé d'effet malformatif mais ont montré un risque de retard de croissance intra-utérin lorsque les bêta-bloquants sont administrés par voie orale. De plus, les signes et les symptômes d’un effet bêta-bloquant (par exemple : bradycardie, hypotension, détresse respiratoire et hypoglycémie) ont été observés chez le nouveau-né lorsque les bêta-bloquants ont été administrés jusqu'à l'accouchement. Si KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution est administré jusqu’à l’accouchement, le nouveau-né doit être surveillé attentivement pendant les premiers jours de vie.
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution ne doit pas être utilisé au cours de la grossesse à moins d'une nécessité absolue. Pour plus d’informations sur la façon de réduire l’absorption systémique, voir la rubrique 4.2.
Allaitement
Il n'existe pas de données concernant l'excrétion du travoprost collyre dans le lait maternel humain. Des études chez l'animal ont mis en évidence une excrétion du travoprost et de ses métabolites dans le lait maternel. Le timolol est excrété dans le lait maternel et peut entrainer des effets indésirables graves chez les nourrissons allaités. Cependant, aux doses thérapeutiques de timolol contenues dans les collyres, il est peu probable que la quantité passant dans le lait maternel suffise à produire les symptômes cliniques des bêta-bloquants chez le nourrisson. Pour plus d’informations sur la façon de réduire l’absorption systémique, voir la rubrique 4.2.
L’utilisation de KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution n’est pas recommandée pendant l’allaitement.
Fertilité
Il n’existe pas de données sur les effets de Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution sur la fertilité humaine. Les études chez l’animal n’ont pas montré d’effet du travoprost sur la fertilité à des doses jusqu’à 75 fois supérieures aux doses oculaires maximales recommandées chez l’homme, alors qu’aucun effet significatif du timolol n’a été constaté à ce niveau de dose.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Comme avec tout collyre, une vision floue provisoire ou d’autres troubles visuels peuvent survenir. En cas de vision floue survenant lors de l’instillation, le patient doit attendre que sa vision redevienne normale avant de conduire un véhicule ou d’utiliser une machine.
Résumé du profil de sécurité
Au cours des études cliniques incluant 2170 patients, traités par Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution l’effet indésirable le plus fréquemment rapporté comme lié au traitement était l’hyperémie oculaire (12,0%).
Liste des effets indésirables
Les effets indésirables recensés dans le tableau ci-dessous ont été observés lors des essais cliniques ou après commercialisation. Ils sont présentés par classe de système d’organes et par fréquence selon la convention suivante : très fréquent (≥ 1/10), fréquent (entre ≥ 1/100 et < 1/10), peu fréquent (entre ≥ 1/1 000 et < 1/100), rare (entre ≥ 1/10 000 et < 1/1 000), très rare (< 1/10 000) ou fréquence indéterminée (la fréquence ne peut être estimée sur la base des données disponibles). Dans chaque catégorie, les effets indésirables sont présentés dans l’ordre décroissant de gravité.
|
Classe de Système d’Organes |
Fréquence |
Effets Indésirables |
|
Affections du système immunitaire |
Peu fréquent |
Hypersensibilité |
|
Affections psychiatriques |
Rare |
Nervosité |
|
Indéterminée |
Dépression, hallucination* |
|
|
Affections du système nerveux |
Peu fréquent |
Sensation vertigineuse, céphalée |
|
Indéterminée |
Accident cérébrovasculaire, syncope, paresthésie |
|
|
Affections oculaires |
Très fréquent |
Hyperhémie oculaire |
|
Fréquent |
Kératite ponctuée, douleur oculaire, défaut visuel, vision trouble, sécheresse oculaire, prurit oculaire, gêne oculaire, irritation oculaire |
|
|
Peu fréquent |
Kératite, iritis, conjonctivite, inflammation de la chambre antérieure, blépharite, photophobie, baisse de l’acuité visuelle, asthénopie, gonflement oculaire, augmentation de la sécrétion lacrymale, érythème de la paupière, croissance des cils, allergie oculaire, œdème conjonctival, œdème de la paupière |
|
|
Rare |
Erosion cornéenne, meibomite, hémorragie conjonctivale, bord de la paupière croûteux, trichiasis, distichiase |
|
|
Indéterminée |
Œdème maculaire, ptosis de la paupière, sillon palpébral approfondi, hyperpigmentation de l’iris, trouble cornéen |
|
|
Affections cardiaques |
Peu fréquent |
Bradycardie |
|
Rare |
Arythmie, fréquence cardiaque irrégulière |
|
|
Indéterminée |
Insuffisance cardiaque, tachycardie, douleur thoracique, palpitations |
|
|
Affections vasculaires |
Peu fréquent |
Hypertension, hypotension |
|
Indéterminée |
Œdème périphérique |
|
|
Affections respiratoires, thoraciques et médiastinales |
Peu fréquent |
Dyspnée, syndrome de toux d'origine des voies aériennes supérieures |
|
Rare |
Dysphonie, bronchospasme, toux, irritation de la gorge, douleur oropharyngée, gêne nasale |
|
|
Indéterminée |
Asthme |
|
|
Affections gastro-intestinales |
Indéterminée |
Dysgueusie |
|
Affections hépatobiliaires |
Rare |
Alanine-aminotransférase augmentée, aspartate-aminotransférase augmentée |
|
Affections de la peau et du tissu sous-cutané |
Peu fréquent |
Dermatite de contact, hypertrichose, hyperpigmentation cutanée (péri-oculaire) |
|
Rare |
Urticaire, altération de la couleur cutanée, alopécie |
|
|
Indéterminée |
Rash |
|
|
Affections musculo-squelettiques et du tissu conjonctif |
Rare |
Extrémités douloureuses |
|
Affections du rein et des voies urinaires |
Rare |
Chromaturie |
|
Troubles généraux et anomalies au site d’administration |
Rare |
Soif, fatigue |
*Effets indésirables observées avec le Timolol
Effets indésirables supplémentaires qui ont été observés avec l’un des principes actifs et peuvent éventuellement survenir avec KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution :
Travoprost
|
Classe de Système d’Organes |
Termes Préférentiels MedDRA |
|
Affections du système immunitaire |
Allergie saisonnière |
|
Affections psychiatriques |
Anxiété, insomnie |
|
Affections oculaires |
Uvéite, follicules conjonctivaux, sécrétions oculaires anormales, œdème périorbitaire, prurit des paupières, ectropion, cataracte, iridocyclite, herpès simplex ophtalmique, inflammation de l’œil, photopsie, eczéma des paupières, halo coloré, hypoesthésie oculaire, pigmentation de la chambre antérieure, mydriase, hyperpigmentation des cils, épaississement des cils, défaut du champ visuel |
|
Affections de l'oreille et du labyrinthe |
Vertige, acouphène |
|
Affections vasculaires |
Pression artérielle diastolique diminuée, pression artérielle systolique augmentée |
|
Affections respiratoires, thoraciques et médiastinales |
Asthme, rhinite allergique, épistaxis, trouble respiratoire, congestion nasale, sécheresse nasale |
|
Affections gastro-intestinales |
Ulcère gastroduodénal réactivé; trouble gastro- intestinal, diarrhée, constipation, bouche sèche, douleur abdominale, nausée, vomissement |
|
Affections de la peau et du tissu sous-cutané |
Exfoliation cutanée, texture anormale des cheveux ou des poils, dermatite allergique, couleur des cheveux ou des poils modifiée, madarose, prurit, pousse anormale des cheveux ou des poils, érythème |
|
Affections musculo-squelettiques et du tissu conjonctif |
Douleur musculosquelettique, arthralgie |
|
Affections du rein et des voies urinaires |
Dysurie, incontinence urinaire |
|
Troubles généraux et anomalies au site d'administration |
Asthénie |
|
Investigations |
Augmentation de l’antigène spécifique de la prostate |
Timolol
Comme d'autres médicaments ophtalmiques administrés localement, le timolol peut être absorbé dans la circulation systémique. Cela peut entrainer des effets indésirables semblables à ceux des bêta-bloquants pris par voie systémique. Les effets indésirables liés à la classe des bêta-bloquants ophtalmiques sont listés ci-dessous. L'incidence des effets indésirables systémiques après une administration par voie ophtalmique est inférieure à celle qui suit une administration systémique. Pour plus d’informations sur la façon de réduire l'absorption systémique, voir rubrique 4.2
|
Classe de Système d’Organes |
Termes Préférentiels MedDRA |
|
Affections du système immunitaire |
Réaction allergique systémique incluant angiœdème, urticaire, rash (localisé et généralisé), prurit, anaphylaxie |
|
Troubles du métabolisme et de la nutrition |
Hypoglycémie |
|
Affections psychiatriques |
Insomnie, cauchemar, perte de mémoire |
|
Affections du système nerveux |
Ischémie cérébrale, myasthénie grave (augmentation des signes et symptômes) |
|
Affections oculaires |
Signes et symptômes d’irritation oculaire (par exemple : brûlure, picotements, démangeaisons, larmoiement, rougeur), décollement choroïdien après une chirurgie filtrante (voir rubrique 4.4), hypoesthésie oculaire, diplopie |
|
Affections cardiaques |
Œdème, insuffisance cardiaque congestive, bloc auriculoventriculaire, arrêt cardiaque |
|
Affections vasculaires |
Syndrome de Raynaud, froideur des extrémités |
|
Affections gastro-intestinales |
Nausée, dyspepsie, diarrhée, bouche sèche, douleur abdominale, vomissement |
|
Affections de la peau et du tissu sous-cutané |
Dermatite psoriasiforme ou psoriasis (exacerbation) |
|
Affections musculo-squelettiques et du tissu conjonctif |
Myalgies |
|
Affections des organes de reproduction et du sein |
Dysfonction sexuelle, diminution de la libido |
|
Troubles généraux et anomalies au site d’administration |
Asthénie |
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.signalement-sante.gouv.fr.
Il est peu probable qu’un surdosage local avec KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution survienne ou soit associé à une toxicité.
En cas d’ingestion accidentelle, les symptômes d’un surdosage en bêta-bloquants systémiques peuvent inclure bradycardie, hypotension, bronchospasme et insuffisance cardiaque.
En cas de surdosage avec KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution, le traitement devra être symptomatique et de soutien. Le timolol ne dialyse pas rapidement.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Mécanisme d’action
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution contient deux substances actives : le travoprost et le maléate de timolol. Ces deux composants diminuent la pression intraoculaire par des mécanismes d'action complémentaires. L'effet combiné entraîne une diminution de la pression intraoculaire supérieure comparée à celle obtenue lors de l'administration de chaque composant seul.
Le travoprost, analogue de la prostaglandine F2α, est un agoniste complet hautement sélectif ayant une haute affinité pour le récepteur FP aux prostaglandines ; il diminue la pression intraoculaire en augmentant l’écoulement de l’humeur aqueuse par le système trabéculaire et les voies uvéosclérales. Chez l’homme, la diminution de la pression intraoculaire débute environ 2 heures après administration et l’effet maximal est atteint au bout de 12 heures. Une baisse significative de la pression intraoculaire peut être maintenue pour des périodes excédant 24 heures avec une administration unique.
Le timolol est un agent non sélectif bloquant les récepteurs adrénergiques, n'ayant ni effet sympathomimétique intrinsèque, ni effet dépresseur myocardique direct, ni effet stabilisant de membrane. Des études tonographiques et fluorophotométriques chez l'homme suggèrent que son action prédominante est liée à la réduction de production d’humeur aqueuse et une légère augmentation de l'écoulement.
Pharmacologie secondaire
Le travoprost augmente significativement le flux sanguin de la tête du nerf optique chez les lapins dans les 7 jours suivant l’instillation oculaire (1,4 microgrammes, une fois par jour).
Effets pharmacodynamiques
Effets cliniques
Dans une étude clinique contrôlée sur 12 mois, réalisée chez des patients atteints de glaucome à angle ouvert ou d'hypertension oculaire et présentant une PIO initiale moyenne de 25 à 27 mmHg, la baisse de la PIO moyenne sous Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution (1 goutte par jour, le matin) était de 8 à 10 mmHg. La non-infériorité du Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution par rapport au latanoprost 50 microgrammes/mL + timolol 5 mg/mL pour la réduction de la PIO moyenne a été démontrée à tous les temps et à toutes les visites.
Dans une étude clinique contrôlée sur 3 mois, réalisée chez des patients atteints de glaucome à angle ouvert ou d'hypertension oculaire et présentant une PIO initiale moyenne de 27 à 30 mmHg, la baisse moyenne de la PIO sous Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution (1 goutte par jour, le matin) était de 9 à 12 mmHg. Cette baisse pouvait aller jusqu’à 2 mmHg de plus qu’avec le travoprost 40 microgrammes/mL (1 goutte par jour, le soir), et jusqu’à 2 à 3 mmHg de plus qu’avec le timolol 5 mg/mL (2 fois par jour). La réduction de la PIO matinale (8h le matin, 24 heures après la dernière instillation de Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution) était statistiquement supérieure à celle obtenue avec le travoprost à toutes les visites de l’étude.
Dans deux études cliniques contrôlées sur 3 mois, réalisées chez des patients atteints de glaucome à angle ouvert ou d'hypertension oculaire et présentant une PIO initiale moyenne de 23 à 26 mmHg, la baisse moyenne de la PIO sous Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution (1 goutte par jour, le matin) était de 7 à 9 mmHg. Les réductions moyennes de la PIO étaient non inférieures, bien que numériquement plus faibles, à celles observées avec le traitement concomitant de travoprost 40 microgrammes/mL (1 fois par jour, le soir) et de timolol 5 mg/mL (1 fois par jour, le matin).
Dans une étude clinique contrôlée sur 6 semaines, réalisée chez des patients atteints de glaucome à angle ouvert ou d’hypertension oculaire et présentant une PIO initiale moyenne de 24 à 26 mmHg, la baisse moyenne de la PIO sous Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution (conservé avec du polyquaternium-1) (1 goutte par jour, le matin) était de 8 mmHg et équivalente à celle obtenue sous Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution (conservé avec du chlorure de benzalkonium).
Les critères d’inclusion étaient communs à toutes les études cliniques, à l’exception du critère de PIO initiale et de la réponse au traitement précédent pour la PIO. Le développement clinique de Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution a inclus des patients naïfs ou traités précédemment. Une réponse insuffisante à une monothérapie n’était pas un critère d’inclusion.
Des données suggèrent qu’une instillation le soir pourrait avoir quelques avantages en ce qui concerne la baisse moyenne de PIO. Le choix du moment de l’instillation (le matin ou le soir) devra prendre en compte la préférence du patient ainsi que sa capacité d’observance.
5.2. Propriétés pharmacocinétiques
Le travoprost et le timolol sont absorbés à travers la cornée. Le travoprost est une prodrogue qui subit une hydrolyse rapide par les estérases de la cornée en acide libre. Après une administration quotidienne de Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution conservé avec du polyquaternium-1 chez des volontaires sains (N = 22) pendant 5 jours, l'acide libre travoprost n'était pas quantifiable dans les échantillons de plasma pour la majorité des sujets (94,4 %) et n'était généralement pas détectable une heure après l'instillation. Les concentrations mesurables (≥ 0,01 ng/mL, limite de quantification), étaient comprises entre 0,01 et 0,03 ng/mL. A l’état d’équilibre, après l’administration du Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution, 1 fois par jour, la Cmax de timolol atteignait 1,34 ng/mL, et le Tmax approximativement 0,69 heures.
Distribution
L'acide libre travoprost peut être dosé dans l'humeur aqueuse de l’animal dans les premières heures qui suivent l’administration oculaire du Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution et dans le plasma humain seulement pendant la première heure suivant l’administration. Chez l’homme, le timolol peut être dosé dans l'humeur aqueuse après instillation de timolol et dans le plasma jusqu'à 12 heures après l’instillation de Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution.
Biotransformation
Le métabolisme est la principale voie d’élimination du travoprost et de sa forme active (acide libre). Les mécanismes métaboliques systémiques sont équivalents à ceux de la prostaglandine F2α endogène, qui sont caractérisés par la réduction de la double liaison 13-14, l’oxydation de la fonction 15-hydroxyle ainsi que la scission par β-oxydation de la partie supérieure de la chaîne.
Le timolol est métabolisé par deux voies. La première conduit à une chaîne éthanolamine sur le cycle thiadiazole et l’autre conduit à une chaîne éthanolique sur l'azote morpholine et une seconde chaîne similaire avec un groupe carbonyle adjacent à l'azote. La demi-vie plasmatique du timolol est de 4 heures après instillation de Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution.
Élimination
L'acide libre de travoprost et ses métabolites sont principalement excrétés par les reins. Moins de 2% d'une dose oculaire de travoprost ont été retrouvés dans les urines sous forme d'acide libre. Le timolol et ses métabolites sont principalement excrétés par les reins. Environ 20 % d'une dose de timolol sont excrétés dans l'urine sous forme inchangée et le reste est excrété dans l'urine sous forme métabolisée.
5.3. Données de sécurité préclinique
Chez le singe, l’administration de Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution deux fois par jour, a induit une augmentation de la fente palpébrale et une augmentation de la pigmentation de l'iris similaire à ce qui est observé avec une instillation de prostanoïdes.
Travoprost/Timolol 40 microgrammes/mL + 5 mg/mL, collyre en solution conservé avec le polyquaternium-1 a entrainé une toxicité minimale pour la surface oculaire par rapport aux collyres conservés avec du chlorure de benzalkonium, sur des cellules cornéennes humaines en culture et après administration oculaire locale chez le lapin.
Travoprost
Chez le singe, l’instillation de travoprost à des concentrations allant jusqu'à 0,012 % dans l'œil droit, deux fois par jour pendant un an, n'a conduit à aucune toxicité systémique.
Des études de toxicité pour la reproduction ont été réalisées avec le travoprost par voie systémique chez le rat, la souris et le lapin. Les résultats sont liés à l’activité agoniste du récepteur FP dans l’utérus avec létalité embryonnaire précoce, perte post implantation et fœtotoxicité.
Chez la rate gravide, l’administration systémique de travoprost à des doses plus de 200 fois supérieures à la dose thérapeutique pendant la période d’organogenèse, a conduit à une augmentation de l’incidence des malformations. Après administration de 3H-travoprost chez des rates gravides, une faible radioactivité a été mesurée dans le liquide amniotique et dans les tissus fœtaux. Les études de reproduction et de développement ont démontré un effet abortif potentiel avec un taux élevé chez le rat et la souris (respectivement 180 pg/mL et 30 pg/mL dans le plasma) avec une exposition 1,2 à 6 fois supérieure à l’exposition thérapeutique (jusqu’à 25 pg/mL).
Timolol
Les données non cliniques issues des études conventionnelles de pharmacologie de sécurité, toxicologie en administration répétée, génotoxicité, cancérogenèse avec le timolol n’ont pas révélé de risque particulier pour l’homme. Les études de toxicité pour la reproduction avec le timolol ont révélé un retard d’ossification du fœtus sans effet sur le développement post natal chez le rat (7 000 fois la dose thérapeutique) et des augmentations de résorptions fœtales chez le lapin (14 000 fois la dose thérapeutique).
2 ans
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution ne doit pas être utilisé plus de 28 jours après la première ouverture du flacon multidoses.
6.4. Précautions particulières de conservation
A conserver à une température ne dépassant pas 25°C..
6.5. Nature et contenu de l'emballage extérieur
Une boîte en carton contient un flacon multidose blanc (PP) de 5 mL avec une pompe (PP, PEHD, PEBD) et un cylindre de pression et un bouchon (PEHD) contenant 2,5 mL de la solution ophtalmique.
Boîtes de 1 ou 3 flacons.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Pas d’exigences particulières.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
416 RUE SAMUEL MORSE - CS99535
34961 MONTPELLIER
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 301 361 8 8 : 2,5 mL de collyre en flacon multidose (PP) de 5 mL, muni d’une pompe, d’un cylindre à pression et d’un capuchon. Boîte de 1.
· 34009 301 857 0 4 : 2,5 mL de collyre en flacon multidose (PP) de 5 mL, muni d’une pompe, d’un cylindre à pression et d’un capuchon. Boîte de 3.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I
ANSM - Mis à jour le : 13/12/2022
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL collyre en solution
Travoprost / Timolol
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution ?
3. Comment utiliser KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution ET DANS QUELS CAS EST-IL UTILISE ?
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution est utilisé pour traiter une pression élevée à l’intérieur de l’œil chez les adultes, y compris les personnes âgées. Cette pression peut conduire à une maladie appelée glaucome.
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution est une solution stérile qui ne contient pas de conservateur.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution ?
N’utilisez jamais KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution :
· si vous êtes allergique au travoprost, aux analogues des prostaglandines, au timolol, aux bêta-bloquants ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6 ;
· si vous souffrez ou avez souffert de troubles respiratoires tels que de l’asthme, une bronchite obstructive chronique sévère (une maladie pulmonaire sévère qui peut entraîner une respiration sifflante, une gêne respiratoire et/ou une toux persistante), ou d’autres types de troubles respiratoires ;
· si vous avez un rhume des foins sévère ;
· si vous avez un rythme cardiaque lent, une insuffisance cardiaque ou des troubles du rythme cardiaque (battements irréguliers du cœur) ;
· si vous souffrez de troubles de la surface oculaire.
Demandez l’avis de votre médecin si vous êtes atteint par l’un de ces troubles.
Avertissements et précautions
Adressez-vous à votre médecin avant d’utiliser KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution, si vous avez actuellement ou avez eu par le passé :
· une maladie coronarienne (dont les symptômes peuvent être une douleur ou une oppression thoracique, une difficulté à respirer, ou une suffocation), une insuffisance cardiaque, ou une pression artérielle basse ;
· des troubles du rythme cardiaque tels qu’un rythme cardiaque lent ;
· des problèmes respiratoires, de l’asthme ou une bronchite obstructive chronique ;
· des problèmes de circulation sanguine (tels que la maladie de Raynaud ou le syndrome de Raynaud) ;
· du diabète (parce que le timolol peut masquer les signes et symptômes d’un faible taux de sucre dans le sang) ;
· un excès d’hormones thyroïdiennes parce que le timolol peut masquer les signes et symptômes d’une maladie de la thyroïde ;
· une myasthénie grave (faiblesse neuromusculaire chronique) ;
· une chirurgie de la cataracte ;
· une inflammation oculaire.
Si vous devez subir une intervention chirurgicale, prévenez votre médecin que vous utilisez KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution car le timolol peut modifier les effets de certains médicaments utilisés pendant l’anesthésie.
Si vous avez une réaction allergique sévère (éruption cutanée, rougeur et démangeaisons de l’œil) en utilisant KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution, quelle qu'en soit la cause, le traitement par adrénaline peut ne pas s'avérer efficace. Si l'on vous prescrit un autre traitement, prévenez votre médecin que vous utilisez KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution.
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution peut modifier la couleur de votre iris (partie colorée de votre œil). Ce changement peut être permanent.
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution peut augmenter la longueur, l’épaisseur, la couleur et/ou le nombre de vos cils et peut entraîner une pilosité ciliaire anormale sur vos paupières.
Le travoprost peut être absorbé à travers la peau et il ne devra donc pas être utilisé par les femmes enceintes ou souhaitant le devenir. Si ce médicament entre en contact avec la peau, alors il doit être enlevé aussitôt par lavage.
Enfants
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution ne doit pas être utilisé chez les enfants et adolescents de moins de 18 ans.
Autres médicaments et KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament, y compris des médicaments sans prescription.
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution peut affecter ou être affecté par d'autres médicaments que vous utilisez, y compris d'autres collyres pour traiter le glaucome. Prévenez votre médecin si vous utilisez ou comptez utiliser :
· des médicaments pour diminuer votre pression artérielle,
· un traitement pour le cœur y compris la quinidine (utilisée pour traiter des maladies cardiaques et certaines formes de paludisme),
· un traitement contre le diabète ou encore des antidépresseurs connus sous le nom de fluoxétine et paroxétine.
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution avec des aliments
Sans objet.
Grossesse, allaitement et fertilité
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
N’utilisez pas KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution si vous êtes enceinte sauf si votre médecin considère que cela est nécessaire. Si vous pouvez être enceinte, utilisez un moyen de contraception adéquat pendant l’utilisation de ce médicament.
N’utilisez pas KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution si vous allaitez. Ce médicament peut passer dans votre lait.
Conduite de véhicules et utilisation de machines
Vous pouvez trouver que votre vision est trouble juste après avoir utilisé KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution. Ne conduisez pas de voiture et n’utilisez pas de machines avant que cet effet ait disparu.
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution contient de l’hydroxystéarate de macrogolglycérol 40
Ce médicament contient de l’hydroxystéarate de macrogolglycérol 40 qui peut causer des réactions cutanées.
3. COMMENT UTILISER KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution ?
La dose recommandée est d’une goutte dans l’œil ou les yeux atteint(s), une fois par jour, le matin ou le soir. Faites-le chaque jour à la même heure.
Utilisez KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution dans les deux yeux uniquement si votre médecin vous a dit de le faire. Utilisez-le aussi longtemps que votre médecin vous l’a dit.
Utilisez uniquement KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution en gouttes pour les yeux.
Si vous utilisez un autre collyre, attendez au moins 5 minutes entre l’administration de KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution et l’autre collyre.
Si vous portez des lentilles de contact souples, n’utilisez pas le collyre avec vos lentilles. Après avoir utilisé le collyre, attendez 15 minutes avant de remettre vos lentilles.
Mode d'emploi
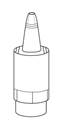
|
1a |
· Sortez le flacon (figure 1a) de la boîte en carton et inscrivez la date d'ouverture sur la boîte en carton et sur le flacon dans l'espace prévu à cet effet. · Prenez le flacon de médicament et un miroir. · Lavez-vous les mains. |
|
1b |
· Retirez le bouchon (figure 1b). |
|
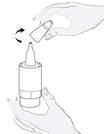
2 |
· Tenez le flacon à l'envers avec le pouce sur le rebord du flacon et les autres doigts sur le fond de la bouteille. Avant la première utilisation, pompez le flacon de façon répétée, environ 10 fois, jusqu'à ce que la première goutte sorte (figure 2). |
|
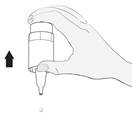
3 |
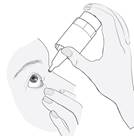
· Penchez la tête en arrière. Avec un doigt propre, tirez doucement votre paupière vers le bas pour créer une poche entre la paupière et votre œil. La goutte sera déposée à cet endroit (figure 3). · Rapprochez l’embout du flacon de l’œil. Utilisez le miroir si cela vous aide. |
|
4 |
· Ne touchez pas votre œil, vos paupières, les surfaces voisines ou d’autres surfaces avec le compte-gouttes. Cela pourrait contaminer le collyre. · Pressez doucement le bas du flacon pour libérer une goutte de médicament à la fois (figure 4). · Si une goutte tombe à côté de votre œil, recommencez. |
|
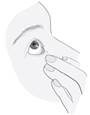
5 |
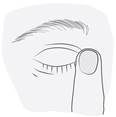
· Après avoir utilisé le médicament, appuyez avec un doigt dans le coin de votre œil, près du nez, pendant 2 minutes (figure 5). Ceci permet d’empêcher le médicament d’aller dans le reste du corps. |
|
|
· Si vous devez traiter les deux yeux, recommencez ces mêmes étapes pour l’autre œil. · Refermez bien le flacon immédiatement après utilisation. · Utilisez un seul flacon à la fois. N’ouvrez pas le bouchon tant que vous n’avez pas besoin d’utiliser le flacon. · Jetez le flacon 28 jours après la première ouverture, afin de prévenir toute contamination et utilisez un nouveau flacon. |
Si vous avez utilisé plus de KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution que vous n’auriez dû
Si vous avez utilisé plus de KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution que vous n’auriez dû, rincez avec de l’eau tiède. Ne mettez pas d’autre goutte jusqu’à ce que le moment soit venu de mettre la goutte suivante.
Si vous oubliez d’utiliser KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution
Si vous oubliez d’utiliser KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution, continuez avec la goutte suivante comme prévu. Ne prenez pas de dose double pour compenser la dose que vous avez oubliée de prendre. La posologie ne doit pas excéder une goutte par jour dans l'œil (les yeux) atteint(s).
Si vous arrêtez d’utiliser KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution
Si vous arrêtez d’utiliser KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution sans en parler à votre médecin, la pression de votre œil ne sera pas contrôlée ce qui pourrait provoquer une perte de la vue.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Vous pouvez généralement continuer à prendre le collyre, à moins que les effets soient graves. Si vous vous inquiétez, contactez un médecin ou pharmacien. N’interrompez pas l’utilisation de KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution sans en parler à votre médecin.
Effets indésirables très fréquents (peuvent affecter plus d’1 personne sur 10) :
Effets oculaires : Rougeur oculaire.
Effets indésirables fréquents (peuvent affecter jusqu’à 1 personne sur 10) :
Effets oculaires : Inflammation de la surface de l’œil avec atteinte superficielle, douleur oculaire, vision trouble, vision anormale, sècheresse oculaire, démangeaison oculaire, gêne oculaire, signes et symptômes d’irritation oculaire (par exemple : sensation de brûlure, de picotement).
Effets indésirables peu fréquents (peuvent affecter jusqu’à 1 personne sur 100) :
Effets oculaires : Inflammation de la surface de l’œil, inflammation de la paupière, conjonctive gonflée, augmentation de la pousse des cils, inflammation de l’iris, inflammation de l’œil, sensibilité à la lumière, vision réduite, fatigue oculaire, allergie oculaire, gonflement oculaire, augmentation de la production de larmes, rougeur des paupières, changement de la couleur des paupières, assombrissement de la peau (autour de l’œil).
Effets indésirables généraux : Réaction allergique à la substance active, sensation de vertige, maux de tête, augmentation ou diminution de la pression artérielle, difficultés respiratoires, croissance excessive des cheveux ou des poils, écoulement au fond de la gorge, inflammation et démangeaisons cutanées, diminution du rythme cardiaque.
Effets indésirables rares (peuvent affecter jusqu’à 1 personne sur 1 000) :
Effets oculaires : Amincissement de la surface de l’œil, inflammation des glandes de la paupière, vaisseaux sanguins rompus dans l’œil, croûte sur le bord de la paupière, positionnement anormal des cils, croissance anormale des cils.
Effets indésirables généraux : Nervosité, irrégularité du rythme cardiaque, perte de cheveux ou de poils, troubles de la voix, difficultés respiratoires, toux, irritation de la gorge, urticaire, tests sanguins hépatiques anormaux, coloration anormale de la peau, soif, fatigue, gêne à l’intérieur du nez, urines colorées, douleurs dans les mains et les pieds.
Fréquence indéterminée (la fréquence ne peut être estimée sur la base des données disponibles) :
Effets oculaires : Paupières tombantes (forçant l’œil à rester à moitié fermé), yeux enfoncés dans les orbites (les yeux apparaissent plus enfoncés), changement de la couleur de l'iris (partie colorée de l'œil).
Effets indésirables généraux : Eruption cutanée, insuffisance cardiaque, douleur thoracique, accident vasculaire cérébral, évanouissement, dépression, hallucination, asthme, augmentation du rythme cardiaque, sensation de fourmillement ou d’engourdissement, palpitations, gonflement des membres inférieurs, mauvais goût.
De plus :
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution est une association de deux substances actives, travoprost et timolol. Comme d'autres médicaments administrés dans les yeux, le travoprost et le timolol (un bêta-bloquant) sont absorbés dans le sang. Ceci peut entrainer des effets indésirables semblables à ceux observés avec des médicaments bêta-bloquants administrés par voie orale ou intraveineuse. Toutefois, l'incidence des effets indésirables après une administration ophtalmique est inférieure à celle observée, après une administration par voie orale ou intraveineuse.
Les effets indésirables cités ci-dessous incluent les réactions liées à la classe des bêta-bloquants ophtalmiques ou les réactions liées au travoprost seul :
Effets oculaires :
Inflammation de la paupière, inflammation de la cornée, décollement de la partie en dessous de la rétine qui contient les vaisseaux sanguins à la suite d’une chirurgie filtrante, ce qui peut causer des troubles de la vision, diminution de la sensibilité cornéenne, érosion cornéenne (couche supérieure du globe oculaire endommagée), vision double, écoulement de l’œil, gonflement autour de l’œil, démangeaison de la paupière, retournement externe de la paupière associé à une rougeur, irritation et larmes excessives, vision trouble (signe d’opacification du cristallin), gonflement d’une partie de l’œil (uvée), eczéma des paupières, vision avec halo, diminution de la vue, pigmentation dans l’œil, dilatation des pupilles, changement de la couleur des cils, changement de la texture des cils, champ visuel anormal.
Effets indésirables généraux :
· Affections de l'oreille et du labyrinthe : étourdissement (sensation de tête qui tourne), bourdonnement des oreilles.
· Affections cardiaques et vasculaires : ralentissement du rythme cardiaque, palpitations, œdème (accumulation de liquide), modification du rythme ou de la vitesse des battements cardiaques, insuffisance cardiaque congestive (maladie cardiaque avec essoufflement et gonflement des pieds et des jambes en raison d’une accumulation de liquide), autre type de trouble du rythme cardiaque, crise cardiaque, tension artérielle basse, syndrome de Raynaud, mains et pieds froids, diminution de l’irrigation sanguine du cerveau.
· Affections respiratoires : resserrement des voies aériennes dans les poumons (particulièrement chez les patients déjà malades), nez qui coule ou bouché, éternuements (causés par une allergie), difficulté à respirer, saignement du nez, sécheresse nasale.
· Affections du système nerveux et affections générales : difficulté à dormir (insomnie), cauchemars, perte de mémoire, perte de force et d’énergie, anxiété (détresse émotionnelle exagérée).
· Affections gastro-intestinales : altération du goût, nausée, indigestion, diarrhée, sécheresse buccale, douleur abdominale, vomissement et constipation.
· Affections du système immunitaire : augmentation des symptômes allergiques, réactions allergiques généralisées incluant des gonflements de la peau qui peuvent survenir sur le visage et les membres, pouvant obstruer les voies aériennes et provoquer des difficultés pour respirer ou avaler, éruption cutanée localisée ou généralisée, démangeaisons, réaction allergique soudaine pouvant menacer le pronostic vital.
· Affections de la peau : éruption cutanée d’apparence blanc-argenté (éruption psoriasiforme) ou aggravation d’un psoriasis, desquamation de la peau, texture anormale des cheveux ou des poils, inflammation de la peau avec éruption cutanée et rougeur, modification de la couleur des cheveux, perte des cils, démangeaison, croissance anormale des cheveux ou des poils, rougeur de la peau.
· Affections musculaires : augmentation des signes et symptômes de myasthénie gravis (trouble musculaire), sensations inhabituelles de picotements cutanés, faiblesse/fatigue musculaire, douleurs musculaires non provoquées par l'exercice, douleurs articulaires.
· Affections du rein et des voies urinaires : difficulté à uriner et douleur en urinant, fuite urinaire incontrôlée.
· Affections des organes de reproduction : troubles sexuels, diminution de la libido.
· Troubles du métabolisme : faible taux de sucre dans le sang, augmentation de l’antigène de la prostate.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.signalement-sante.gouv.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’emballage et le flacon après EXP. La date de péremption fait référence au dernier jour de ce mois.
N’utilisez pas ce médicament si vous remarquez que le flacon a été cassé ou endommagé avant sa première utilisation.
A conserver à une température ne dépassant pas 25°C.
Jetez le flacon 28 jours après la première ouverture, afin de prévenir toute contamination et utilisez un nouveau flacon. Inscrivez la date d’ouverture du flacon dans l’espace prévu à cet effet sur l’étiquette du flacon et l’emballage.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution
· Les substances actives sont :
Chaque mL de solution contient 40 microgrammes de travoprost et 5 mg de timolol (sous forme de maléate de timolol).
· Les autres composants sont :
Mannitol (E421), acide borique, hydroxyde de sodium (pour ajustement du pH), hydroxystéarate de macrogolglycérol (valeur nominale : 40), propylène glycol (E1520), chlorure de sodium, eau purifiée.
KIVIZIDIALE 40 microgrammes/mL + 5 mg/mL, collyre en solution se présente sous forme de 2,5 mL de solution aqueuse, incolore, limpide, pratiquement sans particule, dans un flacon multidoses blanc (PP) de 5 mL avec une pompe (PP, PEHD, PEBD) et un cylindre de pression et un bouchon (PEHD).
Boîte de 1 ou 3 flacons.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
416 RUE SAMUEL MORSE - CS99535
34961 MONTPELLIER
Exploitant de l’autorisation de mise sur le marché
LABORATOIRE CHAUVIN
416 RUE SAMUEL MORSE - CS99535
34961 MONTPELLIER
DERVENAKION 6
PALLINI 15351
ATTIKIS
GRECE
Ou
JADRAN - GALENSKI LABORATORIJ D.D.
SVILNO 20
RIJEKA 51000
CROATIE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[à compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).