Dernière mise à jour le 02/03/2026
THERALENE 4 POUR CENT, solution buvable
Indications thérapeutiques
Classe pharmacothérapeutique : ANTIHISTAMINIQUE A USAGE SYSTEMIQUE, code ATC : R06AD01.
Ce médicament contient un antihistaminique, l'alimémazine.
Ce médicament contient de l'alimémazine qui fait partie des substances actives appelées phénothiazines.
Il est indiqué :
· chez l’adulte, en traitement des insomnies occasionnelles (lors d'un voyage par exemple) et/ou transitoires (lors d'un événement émotionnel par exemple)
· chez l'enfant pesant plus de 20 kg, en traitement de courte durée de certaines formes insomnies et après échecs des mesures de prise en charge comportementales seules.
Vous devez vous adresser à votre médecin si vous ne ressentez aucune amélioration ou si vous vous sentez moins bien.
Présentations
> 1 flacon(s) en verre brun de 30 ml avec pipette doseuse polyéthylène polystyrène
Code CIP : 310 530-8 ou 34009 310 530 8 8
Déclaration de commercialisation : 19/02/1960
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 1,99 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 3,01 €
- Taux de remboursement :15%
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Faible | Avis du 19/10/2016 | Modification des conditions d'inscription (CT) | Le service médical rendu par les spécialités THERALENE reste faible dans les insomnies occasionnelles et les insomnies transitoires. |
| Insuffisant | Avis du 19/10/2016 | Modification des conditions d'inscription (CT) | Le service médical rendu par les spécialités THERALENE reste insuffisant dans le traitement symptomatique des manifestations allergiques diverses : rhinite (saisonnière ou perannuelle), conjonctivite, urticaire, le traitement symptomatique des toux non productives gênantes, en particulier à prédominante nocturne et dans la prémédication avant l'anesthésie générale de l'enfant (solution buvable uniquement). |
| Faible | Avis du 23/09/2015 | Renouvellement d'inscription (CT) | Le service médical rendu par THERALENE 4 %, solution buvable et THERALENE 5 mg, comprimé reste faible dans les insomnies occasionnelles et les insomnies transitoires. |
| Insuffisant | Avis du 23/09/2015 | Renouvellement d'inscription (CT) | Le service médical rendu par THERALENE 4 %, solution buvable et THERALENE 5 mg, comprimé reste insuffisant dans : • le traitement symptomatique des manifestations allergiques diverses : rhinite (saisonnière ou perannuelle), conjonctivite, urticaire, • le traitement symptomatique des toux non productives gênantes, en particulier à prédominante nocturne, • la prémédication avant l'anesthésie générale de l'enfant (solution buvable uniquement). |
Amélioration du service médical rendu (ASMR)
Pas d'ASMR disponible pour ce médicament (plus d'informations dans l'aide )
ANSM - Mis à jour le : 24/03/2023
THERALENE 4 POUR CENT, solution buvable
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Tartrate d'alimémazine................................................................................................................ 5 g
Quantité correspondante en alimémazine base............................................................................ 4 g
Pour 100 ml de solution buvable.
1 ml de solution = 40 mg d'alimémazine base.
Excipients à effet notoire : parahydroxybenzoate de propyle (E216), parahydroxybenzoate de méthyle (E218), rouge cochenille (E124), solution de saccharose, éthanol (alcool).
Le titre alcoolique volumique est de 10,7% (V/V).
Pour la liste complète des excipients, voir rubrique 6.1.
4.1. Indications thérapeutiques
· Adulte : traitement des insomnies occasionnelles ou transitoires.
· Enfant pesant plus de 20 kg : traitement de courte durée et de deuxième intention des insomnies d'endormissement liées à un état d'hyperéveil (vigilance accrue liée à des manifestations anxieuses au coucher), après échec des mesures comportementales seules.
4.2. Posologie et mode d'administration
Posologie
RESERVE A L'ADULTE ET L'ENFANT PESANT PLUS DE 20 KG.
Toujours utiliser la pipette doseuse jointe dans l'emballage
La pipette doseuse est graduée à 5 mg, 10 mg, 15 mg, 20 mg d'alimémazine base.
· Adulte : 5 à 20 mg d'alimémazine
· Enfant pesant plus de 20 kg : 0,25 à 0,5 mg d'alimémazine par kg de poids corporel, sans dépasser 10 mg. Les doses recommandées sont les suivantes :
o Enfant pesant de 20 à 40 kg (de plus de 6 à environ 10 ans) : 5 mg par jour.
o Enfant pesant de 40 à 50 kg (environ 10 à 15 ans) : 5 à 10 mg par jour.
A prendre en 1 prise par jour le soir, 15 à 30 minutes avant le coucher.
Dans tous les cas, le traitement sera initié à la dose efficace la plus faible et la dose maximale ne sera pas dépassée.
Le traitement doit être aussi bref que possible (2 à 5 jours). Si l’insomnie persiste au-delà de cette période, le traitement devra être réévalué.
Sujet âgé:
La posologie doit être diminuée chez le sujet âgé (voir rubrique 4.4. Mises en garde)
Insuffisant rénal ou hépatique :
La posologie doit être diminuée. Néanmoins, en l'absence de donnée chez l'insuffisant rénal ou hépatique, il est préférable de ne pas utiliser l'alimémazine chez les insuffisants rénaux ou hépatiques.
Population pédiatrique :
THERALENE 4 POUR CENT, solution buvable est réservé aux adultes et aux enfants pesant plus de 20 kg.
Mode d’administration
Voie orale.
Liées aux effets anticholinergiques :
· Antécédents personnels ou familiaux de glaucome aigu par fermeture de l’angle iridocornéen,
· Troubles urétroprostatiques à risque de rétention urinaire
Autres :
· Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1
· Antécédents d'agranulocytose à d'autres phénothiazines.
· Antécédents de syndrome malin des neuroleptiques
· Maladie de Parkinson ou syndrome parkinsonien
4.4. Mises en garde spéciales et précautions d'emploi
Insomnie
L’insomnie peut avoir des causes variées ne nécessitant pas obligatoirement la prise d’un médicament. La cause de l’insomnie doit si possible être identifiée, et les éventuels facteurs sous-jacents traités. La persistance de l'insomnie après 5 jours de ce traitement peut indiquer une pathologie sous-jacente, et le traitement devra être réévalué.
Syndrome malin des neuroleptiques:
Des cas de syndrome malin des neuroleptiques ont été rapportés avec l'alimémazine. Le syndrome malin des neuroleptiques se caractérise par une hyperthermie, une rigidité musculaire, une instabilité du système nerveux autonome, des troubles de la conscience et une augmentation de la créatine phosphokinase (CPK) sanguine. Des signes supplémentaires peuvent inclure une myoglobinurie témoignant d'une rhabdomyolyse et une insuffisance rénale aiguë. Tous signes évocateurs d'un syndrome malin des neuroleptiques doivent faire interrompre immédiatement le traitement par alimémazine. En cas d’hyperthermie inexpliquée, il est impératif de suspendre le traitement par alimémazine car ce signe peut être l’un des éléments du syndrome malin des neuroleptiques. Les signes de dysfonctionnement végétatif, tels que pâleur, hypersudation, et instabilité artérielle, peuvent être des signes précoces annonciateurs précédant l'apparition de l'hyperthermie. Bien que le syndrome malin des neuroleptiques puisse avoir une origine idiosyncrasique, certains facteurs de risque semblent y prédisposer, tels que la déshydratation ou des atteintes organiques cérébrales.
Agranulocytose :
Des cas d'agranulocytose ont été décrits avec l'alimémazine. L’apparition d’une fièvre, d’une angine ou d’une autre infection doit conduire à un examen médical et le contrôle de l’hémogramme. Le traitement par alimémazine doit être immédiatement interrompu en cas de neutropénie ou granulopénie.
Sujets épileptiques ou à risque de convulsions:
Les phénotiazines ainsi que les terpènes présents dans cette spécialité (levomenthol) abaissent le seuil épileptogène. La prudence est requise et la surveillance doit être renforcée chez les sujets épileptiques ou à risque de convulsions.
Sujet âgés:
L'alimémazine est déconseillée chez les sujets âgés qui, du fait de leur plus grande sensibilité, présentent un risque accru d'hypotension orthostatique, de vertiges, de chutes, de sédation, d'effets extrapyramidaux et de dépression respiratoire.
En raison des propriétés anticholinergiques de l'alimémazine, la prudence est également requise chez le sujet âgé en cas de constipation chronique (risque d'iléus paralytique), d’hypertrophie prostatique (risque de rétention urinaire) ou de traitement par les anticholinestérasiques (risque d’état confusionnel).
Si l'alimémazine est utilisée malgré tout, la posologie doit être diminuée (voir rubrique 4.2.)
Diminution du péristaltisme intestinal :
Des cas d’obstruction intestinale ont été rapportés chez des patients traités par anticholinergiques neuroleptiques. De rares cas de colite ischémique et de nécrose intestinale, d’évolution parfois fatale, ont également été rapportés. La majorité de ces patients étaient traités de façon concomitante avec un ou plusieurs médicaments induisant une diminution de la motilité intestinale (en particulier les médicaments ayant des propriétés anticholinergiques). L’apparition de douleurs abdominales avec vomissements et/ou diarrhée sous traitement doit attirer l’attention. Il est impératif que la constipation soit reconnue et traitée activement. La survenue d’un iléus/d'un syndrome occlusif intestinal nécessite une prise en charge en urgence.
Effets dépresseurs du système nerveux central :
L’alimémazine, exerce un effet dépresseur central pouvant aggraver un syndrome d’apnées du sommeil préexistant (augmentation du nombre et de la durée des apnées).
L’action sédative de l'alimémazine peut être potentialisée par l’administration de tout autre dépresseur du système nerveux central (en particulier l’alcool). La prise de boissons alcoolisées et de médicaments contenant de l'alcool est fortement déconseillée pendant la durée du traitement (voir rubrique 4.5).
Sujets polymédicamentés :
La prudence est requise chez les sujets polymédicamentés en raison du risque d'interactions médicamenteuses et de potentialisation des effets indésirables (voir rubrique 4.5).
L’association à des médicaments inhibiteurs de l’acétylcholinestérase est à éviter, les inhibiteurs de l’acétylcholinestérase peuvent interférer avec l’activité des anticholinergiques.
Troubles cardiovasculaires:
L'alimémazine doit être utilisée avec prudence chez les sujets présentant des troubles cardio-vasculaires, en raison des effets tachycardisants et hypotenseurs des phénotiazines.
Des cas d'augmentation de l'intervalle QT ont été rapportés avec l'alimémazine le plus souvent en association à d'autres médicaments susceptibles d'augmenter le QT. La prudence est requise chez les patients présentant des antécédents personnels ou familiaux de QT et en cas d'utilisation concomitante de médicaments susceptibles d'allonger l'intervalle QT.
Photosensibilisation :
Compte-tenu de l'effet photosensibilisant des phénothiazines, il est recommandé de ne pas s'exposer au soleil pendant le traitement.
Insuffisance hépatique ou rénale:
L'élimination de l'alimémazine est diminuée en cas d'insuffisances hépatique et/ou rénale sévères. Il est préférable de ne pas administrer l'alimémazine chez les patients insuffisants rénaux ou hépatiques en raison du risque d'accumulation. Si un traitement est entrepris malgré tout, les doses devront être diminuées.
Population pédiatrique
Les phénothiazines ont été considérées comme des facteurs de risque potentiels dans la survenue de mort subite du nourrisson. L'alimémazine ne doit pas être utilisée chez l'enfant de moins de 2 ans.
Surdosage
Des cas de surdosage pouvant conduire au décès ont été rapportés.
Abus
Des cas d’abus ont été rapportés en particulier chez des patients ayant des antécédents de troubles psychiatriques ou d’addiction
Liées aux excipients à effet notoire
Ce médicament contient un agent azoïque, le rouge cochenille (E124), du parahydroxybenzoate de propyle (E216), du parahydroxybenzoate de méthyle (E218), qui peuvent provoquer des réactions allergiques.
Ce médicament contient du saccharose. Son utilisation est déconseillée chez les patients présentant une intolérance au fructose, un syndrome de malabsorption du glucose et du galactose ou un déficit en sucrase/ isomaltase.
Ce médicament contient de faibles quantités d'éthanol (alcool), inférieures à 100 mg par dose.
Cette spécialité contient des dérivés terpéniques (menthol) qui à doses excessives peuvent entraîner des accidents neurologiques à type de convulsions chez le nourrisson et chez l'enfant.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Association aux médicaments connus pour allonger l'intervalle QT
La prudence est requise lorsque l'alimémazine est prescrite en association avec des médicaments susceptibles d'allonger l’intervalle QT, tels que les antiarythmiques (ex: quinidine, disopyramide, procaïnamide, propafénone, amiodarone, sotalol), les antidépresseurs tricycliques (amitriptyline), les antidépresseurs tétracycliques (maprotiline), certains antihistaminiques, les antipsychotiques, certains antipaludiques (quinine et méfloquine), et les médicaments entraînant des troubles électrolytiques (hypokaliémie, hypomagnésémie), une bradycardie. Risque d'augmentation de l'intervalle QT.
Associations déconseillées
+ ALCOOL
Majoration par l'alcool de l'effet sédatif des antihistaminiques. L'altération de la vigilance peut rendre dangereuse la conduite de véhicules et l'utilisation de machines.
Eviter la prise de boisson alcoolisées et d'autres médicaments contenant de l'alcool.
+ AUTRES MEDICAMENTS SEDATIFS
Majoration de la dépression centrale.
L'altération de la vigilance peut rendre dangereuses la conduite de véhicules et l'utilisation de machines.
Associations liées à présence d'alcool (moins de 100mg par dose)
+ Médicaments provoquant une réaction antabuse avec l'alcool (disulfirame, céfamandole, céfopérazone, latamoxef (antibactériens-céphalosporines), chloramphénicol (antibactérien-phénicolé), chlorpropamide, glibenclamide, glipizide, tolbutamide (antidiabétiques-sulfamides hypoglycémiants), griséofulvine (antifongique), nitro-5-imidazolés (métronidazole, ornidazole, secnidazole, tinidazole), kétoconazole, procarbazine (cytostatique)).
Effet antabuse : chaleur, rougeur, vomissement, tachycardie.
Eviter la prise de boisson alcoolisées et d'autres médicaments contenant de l'alcool. Tenir compte de l’élimination complète des médicaments en se référant à leur demi-vie avant la reprise de boissons alcoolisées ou du médicament contenant de l’alcool.
Associations faisant l'objet de précautions d’emploi
+ LITHIUM
Risque d’apparition de signes neuropsychiques évocateurs d’un syndrome malin des neuroleptiques ou d’une intoxication au lithium.
Surveillance clinique et biologique régulière, notamment en début d'association.
+ TOPIQUES GASTRO-INTESTINAUX, ANTIACIDES ET ADSORBANTS
Diminution de l'absorption de l’alimémazine. Prendre les topiques ou antiacides, adsorbants à distance de l’alimémazine (plus de 2 heures, si possible).
Associations à prendre en compte
+ AUTRES MEDICAMENTS SEDATIFS, HYPNOTIQUES, OU DEPRESSEURS DU SYSTEME NERVEUX CENTRAL (certains antidépresseurs sedatifs : amitriptyline, doxepine, mianserine, mirtazapine, trimipramine barbituriques, benzodiazepines et apparentes tels que zolpidem ou zopiclone, autres anxiolytiques, antihypertenseurs centraux, hypnotiques, dérivés morphiniques (analgésiques, antitussifs, traitements de substitution), autres antihistamiques sédatifs, neuroleptiques, baclofène, thalidomide)
Majoration de la dépression centrale. L'altération de la vigilance peut rendre dangereuses la conduite de véhicules et l'utilisation de machines.
+ ATROPINE ET AUTRES SUBSTANCES ANTICHOLINERGIQUES (antidepresseurs imipraminiques, antiparkinsoniens anticholinergiques, antispasmodiques atropiniques, disopyramide, neuroleptiques phenothiaziniques, antihistaminiques H1 atropiniques, clozapine)
Addition des effets indésirables anticholinergiques à type de rétention urinaire, constipation, sécheresse de la bouche.
+ DAPOXÉTINE
Risque de majoration des effets indésirables, notamment à type de vertiges ou de syncopes.
+ MÉDICAMENTS ABAISSANT LA PRESSION ARTÉRIELLE
Risque de majoration d’une hypotension, notamment orthostatique
+ AUTRES MÉDICAMENTS ABAISSANT LE SEUIL ÉPILEPTOGÈNE (antidépresseurs (imipraminiques, inhibiteurs sélectifs de la recapture de la sérotonine), neuroleptiques (phénothiazines et butyrophénones), méfloquine, chloroquine, fluoroquinolones, bupropion, tramadol)
Risque accru de convulsions.
+ BÊTA-BLOQUANTS DANS L'INSUFFISANCE CARDIAQUE
Effet vasodilatateur et risque d'hypotension, notamment orthostatique (effet additif).
+ ORLISTAT
Risque d'échec thérapeutique en cas de traitement concomitant par Orlistat.
4.6. Fertilité, grossesse et allaitement
Grossesse
Compte tenu des données disponibles, il est préférable par mesure de prudence d'éviter d'utiliser l'alimémazine au cours de la grossesse quel qu'en soit le terme.
En effet, les données animales sont insuffisantes pour conclure et les données cliniques sont rassurantes, mais encore limitées.
En cas de traitement en fin de grossesse, tenir compte des propriétés anticholinergiques et sédatives de cette molécule pour la surveillance du nouveau-né.
Allaitement
Le passage de l'alimémazine dans le lait maternel n'est pas connu. Compte tenu des possibilités de sédation ou d'excitation paradoxale du nouveau-né, et plus encore des risques d'apnée du sommeil évoqués avec les phénothiazines, ce médicament est déconseillé en cas d'allaitement.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
L'attention est appelée, notamment chez les conducteurs de véhicules et les utilisateurs de machines, sur les risques de somnolence attachés à l'emploi de ce médicament, surtout en début de traitement.
Ce phénomène est accentué par la prise de boissons alcoolisées ou de médicaments contenant de l'alcool.
Débuter le traitement le soir.
Les caractéristiques pharmacologiques de l'alimémazine sont celles des phénothiazines, à l'origine d'effets indésirables. L'intensité et la fréquence de survenue des effets indésirables sont majorés chez le sujet âgé et l'enfant.
· Affections cardiaques :
o palpitations,
o bradycardie, tachycardie
o troubles du rythme
o allongement de l'intervalle QT (pouvant potentiellement entrainer une torsade de pointe)
· Affections vasculaire :
o hypotension orthostatique
· Affections gastro-intestinales:
o constipation, diminution du péristaltisme intestinal avec possibilité de colite ischémique et de nécrose intestinale (voir rubrique 4.4.)
· Affections hématologiques et du système lymphatique:
o leucopénie, neutropénie, agranulocytose rare (voir rubrique 4.4)
o thrombocytopénie
o anémie hémolytique
· Affections hépatobiliaires:
o ictère cholestatique, hépatite à prédominance cholestatique
· Affections oculaires:
o troubles de l'accommodation
o mydriase
o syndrome de l'iris hypotonique
o glaucome aigu
o dépôts brunâtres dans les segments antérieurs de l’œil, dus à l’accumulation du produit, en général sans retentissement sur la vision
· Affections des organes de reproduction et du sein:
o hyperprolactinémie : aménorrhée, galactorrhée, gynécomastie
o troubles de l’éjaculation et de l’érection
· Affections de la peau et du tissu sous-cutané:
o photosensibilisation
o réactions cutanées allergiques : érythème, eczéma, prurit, purpura, urticaire éventuellement géante
· Affections du rein et des voies urinaires:
o rétention urinaire
· Affections respiratoires, thoraciques et médiastinales:
o hyperviscosité des sécrétions bronchiques
· Affections du système immunitaire:
o réactions allergiques systémiques, choc anaphylactique, plus rarement œdème de Quincke
· Affections psychiatriques:
o indifférence, réactions anxieuses, troubles de l'humeur
o état confusionnel (plus fréquent chez le sujet âgé)
o hallucinations
o excitation, nervosité, insomnie
· Affections du système nerveux:
o troubles de l'équilibre, vertiges
o baisse de la mémoire ou de la concentration
o sédation ou somnolence, plus marquée en début de traitement
o incoordination motrice, tremblements (plus fréquent chez le sujet âgé)
o de rares cas de crises convulsives, principalement en cas d’antécédents d’épilepsie ou en présence d’autres facteurs de risque, tels que l’association à d’autres médicaments abaissant le seuil épileptogène, ou la prise d'alcool (voir rubrique 4.4).
o syndrome malin des neuroleptiques (voir rubrique 4.4.)
o trouble de la thermorégulation (pouvant être annonciateur d'un syndrome malin des neuroleptiques - voir rubrique 4.4.)
o dyskinésies précoces (torticolis spasmodiques, crises oculogyres, trismus)
o dyskinésies tardives, survenant surtout lors de cures prolongées. Ces dyskinésies tardives surviennent parfois à l’arrêt du neuroleptique et disparaissent lors de sa réintroduction ou à l’augmentation de la posologie. Les antiparkinsoniens sont sans action ou peuvent provoquer une aggravation.
o syndrome extrapyramidal : akinétique, avec ou sans hypertonie
o akathisie
o syndrome des jambes sans repos
· Troubles généraux et anomalies au site d'administration:
o sécheresse des muqueuses
· Troubles du métabolisme et de la nutrition:
o hyperglycémie, altération de la tolérance au glucose, trouble de la glycorégulation (incluant l'hypoglycémie)
o prise de poids, augmentation de l'appétit
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
Les signes et symptômes d'un surdosage en alimémazine résultent d'une exacerbation de ses effets pharmacologiques. Ils incluent : dépression respiratoire, troubles tensionnels, convulsions (surtout chez l'enfant), troubles de la conscience, coma. Des cas d'allongement de l'intervalle QT ont été rapportés lors de surdosage en alimémazine.
Un traitement symptomatique et des mesures de réanimation adaptées seront institués en milieu hospitalier.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique :
ANTIHISTAMINIQUE A USAGE SYSTEMIQUE, code ATC : R06AD01.
Effets pharmacodynamiques
L’alimémazine est une phénothiazine à chaîne latérale aliphatique.
L'alimémazine possède des propriétés :
· neuroleptiques et sédatives aux doses usuelles,
· antihistaminiques H1,
· antidopaminergiques
· anticholinergiques (atropiniques) centrales et périphériques
· adrénolytiques (risque d'hypotension orthostatique).
Ces activités sont à l'origine des effets indésirables (voir rubrique 4.8) et elles sont exacerbées en cas de surdosage et chez les sujets polymédicamentés chez qui le risque d'interactions médicamenteuses est accru.
5.2. Propriétés pharmacocinétiques
Les données de pharmacocinétique avec l'alimémazine font défaut.
Les effets centraux de l'alimémazine témoignent du passage de la barrière hemato-méningée de l'alimémazine.
5.3. Données de sécurité préclinique
Non renseigné.
Parahydroxybenzoate de propyle (E216), parahydroxybenzoate de méthyle (E218), lévomenthol, rouge cochenille A (E 124), arôme framboise, cyclamate de sodium, solution de saccharose, alcool éthylique à 96,5°, glycérol, acide citrique monohydraté, eau purifiée.
Composition de l'arôme framboise : alcoolat de framboise, éthanol à 96 pour cent, eau distillée, jus concentré de mûre, préparations aromatisantes (oléorésine de vanille, essence de rose, de violette et d'iris).
Sans objet.
3 ans.
6.4. Précautions particulières de conservation
A conserver à l'abri de la lumière et à une température inférieure à 25°C.
Dans les conditions normales d’utilisation et de conservation le flacon peut être conservé pendant toute la durée du traitement en utilisation quotidienne et selon la posologie recommandée.
Durée de conservation après ouverture : 7 mois.
6.5. Nature et contenu de l'emballage extérieur
Flacon en verre brun de 30 ml ou 100 ml muni d'une capsule en plastique type Vistop + pipette-doseuse (polyéthylène/polystyrène).
6.6. Précautions particulières d’élimination et de manipulation
Instruction pour la prise de ce médicament
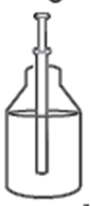
Ce médicament s’administre à l’aide d’une pipette doseuse pour administration orale fournie avec le flacon dans la boîte. L’usage de cette pipette doseuse est strictement réservé à l’administration orale de Théralène 4 pour cent, solution buvable. La pipette-doseuse doit être tenue verticalement à l’intérieur du flacon posé sur une surface plane, et l’œil positionné au niveau de la graduation de la pipette doseuse correspondant à la dose à administrer.
|
· |
· Utiliser la pipette doseuse |
|
· |
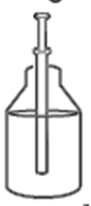
· Plonger la pipette doseuse dans le flacon posé sur une surface plane · Positionner l’œil au niveau de la graduation de la pipette doseuse correspondant à la dose à administrer · Tirer sur le piston de la pipette doseuse pour aspirer la solution buvable jusqu’au trait correspondant à la posologie (en mg) |
Après chaque utilisation, refermer le flacon de la solution buvable, bien rincer la pipette doseuse avec de l’eau et la sécher. Puis ranger immédiatement la pipette doseuse dans sa boîte dans un endroit inaccessible aux enfants. Ne jamais séparer la pipette doseuse des autres éléments de conditionnement du médicament (flacon, boîte, notice).
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur. Une fois le traitement terminé, rapportez à votre pharmacien toutes les boîtes entamées y compris la pipette doseuse ainsi que le flacon pour une destruction correcte et appropriée de ce médicament.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
170 BUREAUX DE LA COLLINE
92213 SAINT-CLOUD CEDEX
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 310 530 8 8 : Flacon de 30 ml (verre brun) + pipette-doseuse (polyéthylène/polystyrène)
· 34009 554 740 1 2 : Flacon de 100 ml (verre brun) + pipette-doseuse (polyéthylène/polystyrène)
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I
ANSM - Mis à jour le : 24/03/2023
THERALENE 4 POUR CENT, solution buvable
Alimémazine
Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations importantes pour vous.
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, qu'il soit mentionné ou non dans cette notice, parlez-en à votre médecin ou votre pharmacien. Voir rubrique 4.
· Ne laissez pas ce médicament à la portée des enfants
1. Qu'est-ce que THERALENE 4 POUR CENT, solution buvable et dans quels cas est-il utilise ?
2. Quelles sont les informations à connaitre avant de prendre THERALENE 4 POUR CENT, solution buvable?
3. Comment prendre THERALENE 4 POUR CENT, solution buvable?
4. Quels sont LES EFFETS INDESIRABLES EVENTUELS ?
5. Comment conserver THERALENE 4 POUR CENT, solution buvable?
6. Contenu de l’emballage et autres informations
1. QU’EST-CE QUE THERALENE 4 POUR CENT, solution buvable ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : ANTIHISTAMINIQUE A USAGE SYSTEMIQUE, code ATC : R06AD01.
Ce médicament contient un antihistaminique, l'alimémazine.
Ce médicament contient de l'alimémazine qui fait partie des substances actives appelées phénothiazines.
Il est indiqué :
· chez l’adulte, en traitement des insomnies occasionnelles (lors d'un voyage par exemple) et/ou transitoires (lors d'un événement émotionnel par exemple)
· chez l'enfant pesant plus de 20 kg, en traitement de courte durée de certaines formes insomnies et après échecs des mesures de prise en charge comportementales seules.
Vous devez vous adresser à votre médecin si vous ne ressentez aucune amélioration ou si vous vous sentez moins bien.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT DE PRENDRE THERALENE 4 POUR CENT, solution buvable?
Ne prenez jamais THERALENE 4 POUR CENT, solution buvable:
· Si vous êtes allergique (hypersensible) à la substance active (alimémazine) ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6 « CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS »
· Ne jamais utiliser l'alimémazine chez le nourrisson (moins de 2 ans)
· Si vous avez des antécédents d'agranulocytose (baisse importante de globules blancs dans le sang) avec d'autres phénothiazines
· Si vous avez eu un syndrome malin des neuroleptiques (trouble grave pouvant apparaitre avec la prise de médicaments neuroleptiques)
· Si vous avez une maladie de parkinson ou des symptômes qui s'y apparentent (syndrome extrapyramidal)
· Si vous avez des antécédents de retentions urinaires, ou des difficultés pour uriner d'origine prostatique ou autre
· Si vous avez un glaucome (augmentation de la pression à l'intérieur de l'œil)
Ce médicament ne doit généralement pas être utilisé, sauf avis contraire de votre médecin :
· Pendant la grossesse (voir ci-dessous rubrique Grossesse et allaitement)
· En cas d'allaitement (voir ci-dessous rubrique Grossesse et allaitement)
Faites attention avec THERALENE 4 POUR CENT, solution buvable :
Avertissements et précautions
Adressez-vous à votre médecin ou pharmacien avant de prendre THERALENE 4 POUR CENT, solution buvable.
L’insomnie peut avoir des causes variées ne nécessitant pas obligatoirement la prise d’un médicament. Un trouble du sommeil en particulier chez l'enfant, nécessite de consulter votre médecin.
La cause d'une insomnie doit être si possible identifiée. Si votre insomnie persiste au-delà de 5 jours, CONSULTEZ VOTRE MEDECIN.
Ce médicament doit être utilisé avec prudence en raison du risque de sédation. L'association avec d'autres médicaments sédatifs est déconseillée (voir rubrique « Interactions avec d'autres médicaments »). L'alcool potentialise ce risque. Ne pas prendre de boissons alcoolisées ou de médicament contenant de l'alcool pendant la durée du traitement qui peuvent accentuer l'effet sédatif.
L’alimémazine contenue dans ce médicament, comme tout produit sédatif, est susceptible d’aggraver un syndrome d’apnée du sommeil préexistant (augmentation du nombre et de la durée des apnées durant le sommeil).
En cas d'apparition de fièvre, pâleur ou sueur inexpliquées, contacter immédiatement un médecin ou un service d'urgence qui pourra décider de suspendre le traitement car ce signe peut être l’un des signes du syndrome malin décrit avec les médicaments neuroleptiques : pâleur, hyperthermie (augmentation de la température du corps). Des signes comme une augmentation de la transpiration ou l’accélération du rythme cardiaque peuvent précéder l’apparition de l'hyperthermie et constituer des signes d’appels précoces. Certains facteurs de risque peuvent prédisposer au syndrome malin des neuroleptiques : déshydratation ou atteinte du cerveau. En cas de doute, contacter rapidement votre médecin.
En cas d'apparition de fièvre accompagnée ou non de signes d'infection (angine ou autre infection), une prise de sang devra être effectuée afin de contrôle les globules blancs dans le sang (hémogramme). En cas de modification importante (augmentation ou baisse importante de certaines cellules du sang), votre médecin peut considérer qu'il est impératif d'arrêter ce traitement.
En cas de constipation persistante, de ballonnement important et de douleurs abdominales, pouvant s'accompagner de vomissements, consultez rapidement un médecin.
Ce médicament ne doit pas être administré en cas d'épilepsie ancienne ou récente, ou d'antécédent de convulsions, informez votre médecin
Ne pas s'exposer au soleil pendant le traitement en raison du risque de photosensibilisation ("coup de soleil") que peut provoquer ce médicament.
Il est préférable de ne pas utiliser ce médicament en cas d'insuffisance rénale ou insuffisance hépatique (maladie au long cours du foie ou des reins). Si ce traitement vous est prescrit malgré tout, votre médecin adaptera la posologie en fonction de votre cas.
En dehors de situations exceptionnelles, ce médicament ne doit pas être utilisé en cas de maladie de Parkinson.
La prudence est requise chez les sujets prenant plusieurs médicaments en raison des potentielles interactions médicamenteuses qui augmentent le risque de survenue d'effets indésirables.
L’association à des anticholinestératiques (médicaments utilisés dans la maladie d’Alzheimer) doit être évitée (voir rubrique « Autres médicaments et THERALENE 4 pour cent solution buvable.»).
Theralène est déconseillé chez les personnes âgées car elles sont plus sensibles aux effets indésirables de ce médicament car elles peuvent :
· être prédisposées aux constipations, à l’hypotension, à la somnolence ou aux effets extrapyramidaux (tremblements involontaires, rigidité des muscles, ralentissement des mouvements),
· présenter des troubles de la prostate
· être traitées par anticholinestératiques (médicaments utilisés dans la maladie d’Alzheimer) ou par plusieurs autres médicaments (voir ci-dessous).
Chez certains patients, il y a un risque de surdosage pouvant parfois conduire au décès.Chez certains patients, en particulier chez des patients ayant des antécédents de troubles psychiatriques ou d’addiction, un risque d’abus est possible.
Avertissements liées à la présence d'excipients à effet notoire :
Ce médicament contient du parahydroxybenzoate de propyle (E216) et du parahydroxybenzoate de méthyle (E218) qui peuvent provoquer des réactions allergiques.
Ce médicament contient un agent azoïque, le rouge cochenille (E124) qui peut provoquer des réactions allergiques.
Ce médicament contient du saccharose. Son utilisation est déconseillée chez les patients présentant une intolérance au fructose, un syndrome de malabsorption du glucose et du galactose ou un déficit en sucrase-iso maltase (maladies métaboliques héréditaires rares).
Ce médicament contient de petites quantités d'éthanol (alcool), inférieures à 100 mg par dose.
Cette spécialité contient un dérivé terpénique (levomenthol) qui peut, à doses excessives, entrainer des accidents neurologiques à type de convulsions chez le nourrisson et chez l'enfant.
EN CAS DE DOUTE N'HESITEZ PAS A DEMANDER L'AVIS DE VOTRE MEDECIN OU DE VOTRE PHARMACIEN.
Autres médicaments et THERALENE 4 POUR CENT, solution buvable.
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
· Ce médicament contient de faible quantité d'alcool (moins de 100 mg par dose). L’association avec des médicaments entraînant une réaction antabuse avec l'alcool (chaleur, rougeur, vomissement, tachycardie) est déconseillée : certains antibiotiques, antidiabétiques, antifongiques, antiinflammatoires et cytostatiques.
· Ce médicament contient de l'alimémazine qui possède, entre autres, des propriétés antihistaminiques. D'autres médicaments contiennent des substances antihistaminiques. Ne les associez pas, afin de ne pas dépasser la dose maximale d'antihistaminiques.
· L'association avec d'autres médicaments sédatifs est déconseillée en raison du risque de majoration de l'effet sédatif de ce médicament.
· Ne pas prendre de boissons alcoolisées ou de médicaments contenant de l'alcool pendant la durée du traitement car ils peuvent accentuer l'effet sédatif.
· L’association avec les médicaments contenant du lithium (le lithium est utilisé pour traiter les troubles de l’humeur) doit faire l'objet d'une surveillance particulière (risque d'interactions pouvant entrainer une intoxication au lithium ou l’apparition d’un syndrome malin des neuroleptiques (voir rubrique «Avertissements et précautions»).
· Les topiques gastro-intestinaux, les antiacides (médicaments utilisés en cas de douleurs gastriques ou de reflux gastro-intestinaux) et les adsorbants/protecteurs intestinaux (médicaments utilisés en cas de diarrhées) doivent être pris à distance de ce médicament (respectez au moins 2h entre les prises des deux médicaments).
· Prévenez votre médecin en cas de traitement par l’un des médicaments suivants :
o médicaments sédatifs, hypnotiques, ou dépresseurs du système nerveux central tels que certains antidépresseurs sedatifs : amitriptyline, doxepine, mianserine, mirtazapine, trimipramine barbituriques, benzodiazepines et apparentes tels que zolpidem ou zopiclone, autres anxiolytiques, antihypertenseurs centraux, hypnotiques, dérivés morphiniques (analgésiques, antitussifs, traitements de substitution), autres antihistamiques sédatifs, neuroleptiques, baclofène, thalidomide)
o médicaments à base de dapoxétine (risque de vertiges ou syncopes)
o les médicaments abaissant la pression artérielle
o les médicaments abaissant le seuil épileptogène (antidépresseurs (imipraminiques, inhibiteurs sélectifs de la recapture de la sérotonine), neuroleptiques (phénothiazines et butyrophénones), méfloquine, chloroquine, fluoroquinolones, bupropion, tramadol)
o certains bétabloquants utilisés dans l’insuffisance cardiaque,
o des médicaments contenant de l'orlistat (médicament utilisé pour traiter l'obésité).
THERALENE 4 POUR CENT, solution buvable avec de l’alcool
Ne pas prendre de boissons alcoolisées ou de médicament contenant de l’alcool pendant la durée du traitement.
Grossesse et allaitement
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou si vous envisagez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
Grossesse
Il est préférable de ne pas utiliser ce médicament pendant la grossesse. Si vous découvrez que vous êtes enceinte, consultez votre médecin, lui seul peut juger de la nécessité de poursuivre le traitement.
Allaitement
Ce médicament passe très vraisemblablement dans le lait maternel. Compte tenu de ses propriétés sédatives qui pourraient retentir sur votre enfant (léthargie, baisse de tonus) ou au contraire excitantes (insomnie), ce médicament est déconseillé en cas d'allaitement.
Conduite de véhicules et utilisation de machines
L'attention est appelée, notamment chez les conducteurs de véhicules et les utilisateurs de machines, sur les possibilités de somnolence attachées à l'usage de ce médicament.
Ce phénomène est accentué par la prise de boissons alcoolisées.
Le traitement doit être pris le soir avant le coucher.
THERALENE 4 POUR CENT, solution buvable contient du parahydroxybenzoate de propyle (E216), du parahydroxybenzoate de méthyle (E218), du rouge cochenille A (E124), du saccharose, de l’éthanol (alcool). (Voir avertissements ci-dessus)
3. COMMENT PRENDRE THERALENE 4 POUR CENT, solution buvable?
Veillez à toujours prendre ce médicament en suivant exactement les indications de votre médecin ou pharmacien. Vérifiez auprès de votre médecin ou pharmacien en cas de doute.
Toujours utiliser la pipette doseuse jointe dans la boite de ce médicament.
La pipette doseuse est graduée à 5 mg, 10 mg, 15 mg et 20 mg d'alimémazine base.
RESERVE A L'ADULTE ET L'ENFANT PESANT PLUS DE 20 KG.
A prendre en 1 prise par jour, le soir 15 à 30 minutes avant le coucher.
· Adulte : 5 à 20 mg d'alimémazine.
· Enfant pesant plus de 20 kg (plus de 6 ans environ) : 0,25 à 0,5 mg d'alimémazine par kg de poids corporel sans dépasser 10mg.
Les doses recommandées sont les suivantes :
o Enfant pesant de 20 à 40 kg (âgé de plus de 6 à environ 10 ans) : 5 mg par jour.
o Enfant pesant de 40 à 50 kg (environ 10 à 15 ans) : 5 à 10 mg par jour.
Ne pas dépasser la dose prescrite par votre médecin.
Mode et voie d'administration
Voie orale.
Instruction pour la prise de ce médicament
Ce médicament s’administre à l’aide d’une pipette doseuse pour administration orale fournie avec le flacon dans la boîte. L’usage de cette pipette doseuse est strictement réservé à l’administration orale de Théralène 4 pour cent solution buvable.
|
· |
· Utiliser la pipette doseuse |
|
· |
· Plonger la pipette doseuse dans le flacon posé sur une surface plane · Positionner l’œil au niveau de la graduation de la pipette doseuse correspondant à la dose à administrer · Tirer sur le piston de la pipette doseuse pour aspirer la solution buvable jusqu’au trait correspondant à la posologie (en mg) |
Après chaque utilisation, refermer le flacon de la solution buvable, bien rincer la pipette doseuse avec de l’eau et la sécher. Puis ranger immédiatement la pipette doseuse dans sa boîte dans un endroit inaccessible aux enfants. Ne jamais séparer la pipette doseuse des autres éléments de conditionnement du médicament (flacon, boîte, notice).
Durée du traitement :
Le traitement doit être aussi bref que possible (2 à 5 jours). Si l’insomnie persiste au-delà de cette période, le traitement devra être réévalué.
Si vous avez pris plus de THERALENE 4 POUR CENT, solution buvable que vous n’auriez dû :
Consultez immédiatement votre médecin ou votre pharmacien.
Si vous oubliez de prendre THERALENE 4 POUR CENT, solution buvable :
Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre.
Si vous arrêtez de prendre THERALENE 4 POUR CENT, solution buvable :
Sans objet.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Comme tous les médicaments, ce médicament peut provoquer des effets indésirables, mais ils ne surviennent pas systématiquement chez tout le monde.
Certains effets nécessitent d'ARRETER IMMEDIATEMENT LE TRAITEMENT ET D'AVERTIR UN MEDECIN.
· Syndrome malin des neuroleptiques, se manifestant par une fièvre inexpliquée (hyperthermie), une raideur musculaire, des sueurs ou une pâleur, des troubles de la conscience. Un traitement médical immédiat peut être nécessaire (voir ci-dessus rubrique 2. "Avertissements et précautions).
· Réactions allergiques:
o éruption cutanée: rougeurs, eczéma, démangeaisons de la peau, éruptions, urticaire (pouvant se généraliser à tout le corps),
o Oedème de Quincke : gonflement de la peau et/ou des muqueuses (œdème) au niveau de la tête et du cou (paupières, lèvres, langue, pharynx) pouvant entrainer des difficultés à respirer
o Choc anaphylactique (réaction allergique généralisée brutale avec chute de la tension)
· Photosensibilisation (sensibilisation au rayon de soleil entrainant coup de soleil et brulure de la peau suite à une exposition au soleil).
· Crises convulsives (rares cas), notamment en cas d’antécédents d’épilepsie ou de convulsions ou en présence d'autres facteurs de risque associés (tels que l'association à d’autres médicaments abaissant le seuil épileptogène, ou alcoolisme)
· Baisse du nombre de globules blancs du sang entrainant un risque d'infection
· Saignements de nez ou des gencives qui peuvent traduire un trouble de la coagulation en lien avec une diminution des plaquettes dans le sang
Autres effets indésirables :
Fréquence indéterminée: la fréquence de survenue ne peut être estimée sur la base des données disponibles :
· Sécheresse des muqueuses, sensation de bouche sèche, hyperviscosité des sécrétions bronchiques,
· Hypotension orthostatique (chute de la tension artérielle se traduisant par un malaise lors du passage rapide de la position allongée à la position debout)
· Palpitations, troubles du rythme cardiaque, ralentissement ou accélération du rythme cardiaque (bradycardie ou tachycardie), baisses de la tension artérielle, allongement de l'intervalle QT (anomalie détectée sur l'électrocardiogramme).
· Constipation, ralentissement du transit intestinal avec possibilité d'atteinte grave de l'intestin (colite ischémique) voir rubrique 2. "Avertissements et précautions").
· Hyperprolactinémie (augmentation du taux de prolactine dans le sang). L'augmentation de cette hormone dans le sang peut entrainer des symptômes chez la femme tels qu'une sensation de gêne au niveau des seins, un écoulement de lait au niveau du mamelon, l'absence ou des troubles des règles, ou encore des problèmes de fertilité. Chez l'homme elle peut entrainer un gonflement au niveau des seins, des dysfonctionnements sexuels avec notamment des troubles de l’éjaculation et de l’érection.
· Rétention d'urine (difficulté ou impossibilité à uriner),
· Anémie (baisse du nombre de globules rouges dans le sang pouvant donner lieu à une fatigue, une pâleur).
· Troubles visuels, trouble de l'accommodation (difficulté dans la vision de près), dilatation des pupilles, poussée aigue de glaucome,
· Dépôts brunâtres visibles lors d'un examen par l'ophtalmologue dans les segments antérieurs de l’œil, dus à l’accumulation du produit, en général sans retentissement sur la vision.
· Somnolence (plus marquée en début de traitement),
· Réaction d'anxiété ou d'indifférence inhabituelle, modification de l'humeur, hallucinations, agitation, nervosité, insomnie, état confusionnel en particulier chez les sujets âgés
· Troubles de l'équilibre, vertiges
· Trouble de la mémoire, difficultés de concentration,
· Incoordination motrice, tremblements (en particulier chez les sujets âgés)
· Dyskinésies (mouvements musculaires involontaires, qui peuvent être répétitifs, spastiques tels que torticolis, mouvements anormaux des yeux, du visage, de la bouche ou de la langue. Ces dyskinésies peuvent survenir en début de traitement ou plus tardivement lors des traitements prolongés. Les dyskinésies tardives peuvent également survenir à l'arrêt du traitement.
· Incoordination et réduction de l’activité motrice, tremblements, piétinements, raideur (syndrome extrapyramidal).
· Syndrome des "jambes sans repos"
· Trouble de la régulation de la température corporelle (une hyperthermie peut être un signe annonciateur d'un syndrome malin des neuroleptique voir ci-dessus)
· Prise de poids, augmentation de l'appétit
· Hyperglycémie (augmentation de la concentration en glucose dans le sang), altération de la tolérance au glucose pouvant également inclure des baisses de la glycémie (hypoglycémie).
· Hépatite, jaunisse (atteinte du foie).
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER THERALENE 4 POUR CENT, solution buvable?
Tenir hors de la portée et de la vue des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’emballage extérieur et l’étiquette du flacon après {EXP}. La date de péremption fait référence au dernier jour de ce mois
Ce médicament doit être conservé à l'abri de la lumière et à une température inférieure à 25°C.
Dans les conditions normales d’utilisation et de conservation le flacon peut être conservé pendant toute la durée du traitement en utilisation quotidienne et selon la posologie recommandée.
Durée de conservation après ouverture : 7 mois.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Une fois le traitement terminé, rapportez à votre pharmacien toutes les boîtes entamées y compris la pipette doseuse ainsi que le flacon pour une destruction correcte et appropriée de ce médicament.
Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient THERALENE 4 POUR CENT, solution buvable
· La substance active est :
Tartrate d'alimémazine .......................................................................................................... 5g
Quantité correspondante en alimémazine base .................................................................... 4g
Pour 100 ml de solution buvable.
1 ml de solution = 40 mg d'alimémazine base.
· Les autres composants sont :
Parahydroxybenzoate de propyle (E216), parahydroxybenzoate de méthyle (E218), lévomenthol, rouge cochenille A (E124), arôme framboise, cyclamate de sodium, solution de saccharose, alcool éthylique à 96,5°, glycérol, acide citrique monohydraté, eau purifiée.
Le titre alcoolique volumique est de 10,7% (V/V). La quantité d'alcool par unité de prise est faible (inférieure à 100 mg).
Qu’est-ce que THERALENE 4 POUR CENT, solution buvable et contenu de l’emballage extérieur
Ce médicament se présente sous forme de solution buvable. Flacon de 30 ou 100 ml.
Titulaire de l’autorisation de mise sur le marché
LABORATOIRE X.O
170 BUREAUX DE LA COLLINE
92213 SAINT-CLOUD CEDEX
Exploitant de l’autorisation de mise sur le marché
LABORATOIRE X.O
170 BUREAUX DE LA COLLINE
92213 SAINT-CLOUD CEDEX
LABORATOIRES M. RICHARD
(SIEGE SOCIAL)
583, ROUTE DE CREST
26740 SAUZET
FRANCE
Ou
NATRAPHARM LIMITED
Units 19-21
Industrial Park
WATERFORD
Irlande
Ou
LAPHAL INDUSTRIES
Avenue de Provence,
13190 ALLAUCH
France
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Sans objet.