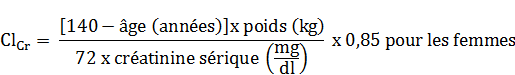Dernière mise à jour le 28/04/2026
PIRACETAM EG 800 mg, comprimé pelliculé sécable
Indications thérapeutiques
Classe pharmacothérapeutique - code ATC : N06BX03
Ce médicament est indiqué dans les situations suivantes :
Chez l'adulte :
· traitement d'appoint de troubles mineurs chroniques (cognitifs ou neurosensoriels) liés au vieillissement (à l'exclusion de la maladie d'Alzheimer et des autres démences) ;
· traitement symptomatique des vertiges.
Chez l'enfant de plus de 30 kg (soit à partir d'environ 9 ans) :
· dyslexie.
Présentations
> 1 flacon(s) en verre brun de 45 comprimé(s)
Code CIP : 349 719-4 ou 34009 349 719 4 5
Déclaration de commercialisation : 14/02/1999
Cette présentation n'est pas agréée aux collectivités
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Insuffisant | Avis du 02/11/2011 | Réévaluation suite saisine Ministères (CT) | Le service médical rendu par PIRACETAM EG 800 mg est insuffisant dans toutes les indications de l'AMM. |
Amélioration du service médical rendu (ASMR)
Ce médicament étant un générique, l'ASMR n'a pas été évalué par la commission de la transparence (CT), il est possible de se référer à la /aux spécialité(s) de référence du groupe générique auquel appartient ce médicament (cliquez ici pour aller à la rubrique des groupes génériques)
ANSM - Mis à jour le : 28/09/2020
PIRACETAM EG 800 mg, comprimé pelliculé sécable
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Piracétam....................................................................................................................... 800,00 mg
Pour un comprimé pelliculé.
Pour la liste complète des excipients, voir rubrique 6.1.
Le comprimé peut être divisé en doses égales.
4.1. Indications thérapeutiques
· traitement d'appoint à visée symptomatique du déficit pathologique cognitif et neuro-sensoriel chronique du sujet âgé (à l'exclusion de la maladie d'Alzheimer et des autres démences);
· amélioration symptomatique des vertiges.
Chez l'enfant de plus de 30 kg (soit à partir d'environ 9 ans)
· traitement d'appoint de la dyslexie.
4.2. Posologie et mode d'administration
Les posologies recommandées par indication sont :
· Traitement d'appoint à visée symptomatique du déficit pathologique cognitif et neuro-sensoriel chronique du sujet âgé et vertiges :
o 1 comprimé à 800 mg matin, midi et soir, soit 3 comprimés par jour.
Populations particulières
Sujet âgé
Un ajustement de la dose est recommandé chez les patients âgés ayant une altération de la fonction rénale (voir ci-après « Insuffisant rénal »). Pour les traitements de longue durée, une évaluation régulière de la clairance de la créatinine est nécessaire afin de permettre une adaptation posologique, le cas échéant.
Insuffisance rénale
La dose quotidienne doit être adaptée individuellement et en tenant compte de la fonction rénale. Consulter le tableau suivant et ajuster la dose comme indiqué. Pour utiliser ce tableau, il est nécessaire d'estimer la clairance de la créatinine (CLcr) du patient en ml/min. La Clcr en ml/min peut être estimée à partir de la valeur de la créatinine sérique (mg/dl) selon la formule suivante :
|
Groupe |
Clairance de la créatinine (ml/min) |
Posologie et fréquence |
|
Fonction rénale normale |
> 80 |
dose quotidienne habituelle, répartie en 2 à 4 prises |
|
Insuffisance rénale légère |
50-79 |
2/3 de la dose quotidienne habituelle, répartie en 2 ou 3 prises |
|
Insuffisance rénale modérée |
30-49 |
1/3 de la dose quotidienne habituelle, répartie en 2 prises |
|
Insuffisance rénale sévère |
< 30 |
contre-indiqué |
|
Insuffisance rénale terminale |
-- |
contre-indiqué |
Insuffisance hépatique
Aucun ajustement de la dose n'est nécessaire chez les patients atteints uniquement d'une insuffisance hépatique. L'ajustement de la posologie est recommandé chez les patients atteints d'une insuffisance hépatique et d’une insuffisance rénale (voir « Insuffisance rénale » ci-dessus).
Population pédiatrique
· Traitement de la dyslexie :
o 50 mg/kg/jour en 3 prises.
Ce dosage (800 mg en comprimé) ne convient pas pour cette posologie.
Mode d’administration
PIRACETAM EG 800 mg, comprimé pelliculé sécable doit être pris par voie orale, avec ou sans nourriture. Les comprimés doivent être avalés en entier avec une boisson. Il est recommandé de prendre la dose journalière en 2 à 4 prises.
· Insuffisance rénale sévère ou insuffisance rénale terminale.
· Hémorragie cérébrale.
· Chorée de Huntington (aggravation des symptômes).
4.4. Mises en garde spéciales et précautions d'emploi
Effets sur l'agrégation plaquettaire
En raison de l'effet du piracétam sur l'agrégation plaquettaire (voir rubrique 5.1), la prudence est recommandée chez les patients présentant une hémorragie sévère, les patients à risque de saignements comme un ulcère gastro-intestinal, les patients ayant des troubles de l'hémostase, des antécédents d'accident vasculaire cérébral (AVC) hémorragique, les patients devant subir une intervention chirurgicale (y compris chirurgie dentaire) et les patients sous anticoagulants ou antiagrégants plaquettaires, y compris l’acide acétylsalicylique à faible dose.
Insuffisance rénale
Le piracétam est éliminé par voie rénale et des précautions doivent être prises en cas d’insuffisance rénale.
En cas d'insuffisance rénale légère à modérée, les doses seront diminuées et/ou espacées si la clairance de la créatinine est inférieure à 80 ml/min (voir rubrique 4.2).
Sujet âgé
Pour les traitements de longue durée chez les sujets âgés, une évaluation régulière de la clairance de la créatinine est nécessaire pour permettre un ajustement posologique, le cas échéant (voir rubrique 4.2).
Arrêt de traitement
Tout arrêt soudain du traitement doit être évité chez les patients atteints de myoclonies, car cela peut provoquer une récidive brutale de celles-ci ou des convulsions de sevrage (voir rubrique 4.2.).
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Interactions pharmacocinétiques
Il est attendu que le risque d'interactions médicamenteuses pouvant modifier la pharmacocinétique du piracétam soit faible, car environ 90 % de la dose de piracétam est éliminée dans les urines sous forme inchangée.
In vitro, le piracétam n'inhibe pas les isoformes du cytochrome hépatique humain P450 (CYP 1A2, 2B6, 2C8, 2C9, 2C19, 2D6, 2E1 et 4A9/11) à des concentrations de 142, 426 et 1 422 µg/ml.
À une concentration de 1422 µg/ml, des effets inhibiteurs mineurs ont été observés sur les CYP 2A6 (21 %) et 3A4/5 (11 %). Toutefois, il est probable que les valeurs de Ki nécessaires à l'inhibition de ces deux isoformes CYP soient bien supérieures à 1422 µg/ml. Par conséquent, une interaction métabolique du piracétam avec d'autres médicaments est peu probable.
Hormones thyroïdiennes
Des effets à type de confusion, irritabilité et troubles du sommeil ont été rapportés lors de l’administration concomitante d’extraits thyroïdiens (T3 + T4).
Acénocoumarol
Dans une étude en simple aveugle chez des patients ayant des thromboses veineuses sévères récurrentes, le piracétam (9,6 g/j) n'a pas modifié les doses d'acénocoumarol nécessaires pour atteindre un INR compris entre 2,5 et 3,5. Toutefois, comparé aux effets de l'acénocoumarol seul, l'ajout du piracétam (9,6 g/j) a significativement diminué l'agrégation plaquettaire, la libération de β-thromboglobuline, les taux de fibrinogène et de facteurs de Willebrand (VIII : C ; VIII : vW : Ag ; VIII : vW : RCo) ainsi que la viscosité du sang total et du plasma.
Antiépileptiques
Le piracétam, administré à la dose quotidienne de 20 g pendant quatre semaines, n'a pas modifié les taux sériques maximal et résiduel des antiépileptiques (carbamazépine, phénytoïne, phénobarbital, acide valproïque), chez les patients épileptiques qui recevaient des doses stables.
Alcool
L'administration concomitante d'alcool n'a eu aucun effet sur les taux sériques de piracétam et les taux d'alcool n'ont pas été modifiés par une dose orale de 1,6 g de piracétam.
4.6. Fertilité, grossesse et allaitement
Grossesse
Il n’existe pas de données adéquates sur l'utilisation du piracétam chez la femme enceinte. Les études chez l’animal n’ont pas mis en évidence d'effets délétères directs ou indirects sur la grossesse, le développement de l'embryon/du fœtus, l'accouchement ou le développement postnatal (voir rubrique 5.3).
Le piracétam traverse la barrière placentaire. Les taux de médicament chez le nouveau-né représentent environ 70 à 90 % des taux maternels. Le piracétam n’est pas recommandé pendant la grossesse sauf en cas de réelle nécessité, lorsque le bénéfice attendu pour la mère est supérieur aux risques potentiels.
Allaitement
Le piracétam est excrété dans le lait maternel humain. Par conséquent, le piracétam ne doit pas être utilisé pendant l'allaitement ou l'allaitement doit être interrompu pendant le traitement. Une décision doit être prise soit d’interrompre l’allaitement soit d’interrompre le piracétam, en prenant en compte le bénéfice de l’allaitement pour l’enfant au regard du bénéfice du traitement pour la mère.
Fertilité
Les études effectuées chez l’animal indiquent que le piracétam n’a aucun effet sur la fertilité des rats mâles ou femelles.
Il n’existe pas de données cliniques sur les effets du piracétam sur la fertilité.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Résumé du profil de sécurité d’emploi
Les études pharmaco cliniques ou cliniques en double aveugle, contrôlées versus placebo, qui ont fourni des données de tolérance (issues de la Base de données UCB, en juin 1997), ont inclus plus de 3000 sujets ayant reçu du piracétam, sans distinction d’indication, de forme pharmaceutique, de posologie quotidienne ou de population.
Liste récapitulative des effets indésirables
Les effets indésirables rapportés au cours des études cliniques et depuis la commercialisation sont présentés par classe de systèmes d'organes et par fréquence dans le tableau ci-après. La fréquence est définie comme suit : très fréquent (≥1/10) ; fréquent (≥1/100, <1/10) ; peu fréquent (≥1/1,000, <1/100) ; rare (≥1/10,000, <1/1,000) ; très rare (<1/10,000) ; fréquence indéterminée (ne peut être estimée sur la base des données disponibles). Les données recueillies depuis la commercialisation sont insuffisantes pour déterminer leur incidence dans la population traitée.
|
Classes de Systèmes Organes |
Effet indésirable |
||
|
Fréquence |
|||
|
Fréquent |
Peu fréquent |
Indéterminée |
|
|
Affections hématologiques et du système lymphatique |
troubles hémorragiques |
||
|
Affections du système immunitaire |
réaction anaphylactoïde, hypersensibilité |
||
|
Affections psychiatriques |
nervosité |
dépression |
agitation, anxiété, confusion, hallucination |
|
Affections du système nerveux |
hyperkinésie |
nervosité |
ataxie, trouble de l'équilibre, épilepsie aggravée, céphalée, insomnie, somnolence |
|
Affections gastro-intestinales |
douleur abdominale, douleur abdominale haute, diarrhée, nausées, vomissements |
||
|
Affections de la peau et du tissu sous-cutané |
œdème angioneurotique, dermatite, prurit, urticaire |
||
|
Troubles généraux et anomalies au site d'administration |
asthénie |
||
|
Investigations |
prise de poids |
||
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.ansm.sante.fr.
Le plus important surdosage de piracétam rapporté a été une prise orale de 75 g. Un cas de diarrhée sanglante avec des douleurs abdominales a été observé, suite à la prise quotidienne de 75 g de piracétam par voie orale, mais était plus probablement dû à la dose extrême de sorbitol contenue dans la formulation utilisée.
Aucun évènement indésirable supplémentaire spécifiquement lié au surdosage n'a été rapporté avec le piracétam.
Prise en charge du surdosage
En cas de surdosage aigu et important, l'estomac peut être vidé par lavage gastrique ou induction de vomissements. Il n'existe aucun antidote spécifique du piracétam. Le traitement d'un surdosage sera symptomatique et peut inclure une hémodialyse. L’efficacité d’extraction par dialyse est de 50 à 60 % pour le piracétam.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : AUTRES PSYCHOSTIMULANTS ET NOOTROPIQUES, code ATC : N06BX03.
Mécanisme d’action
Le mécanisme d’action sous-tendant les effets thérapeutiques n’est pas connu.
Effets pharmacodynamiques
Chez l’animal, dans des conditions différentes de l’usage thérapeutique, notamment à des posologies ou concentrations souvent élevées, les effets pharmacologiques suivants ont été observés :
· amélioration des neurotransmissions GABAergiques, cholinergiques et glutamatergiques,
· facilitation de l’apprentissage et de la vitesse de traitement de l’information intra et inter-hémisphérique.
5.2. Propriétés pharmacocinétiques
Après administration orale, la résorption est complète et rapide. La concentration plasmatique maximale est atteinte en 45 minutes.
Distribution
La demi-vie plasmatique du piracétam est de 4 à 5 heures. Elle est doublée pour une clairance de créatinine inférieure à 60 ml/min.
Le piracétam traverse la barrière hémato-encéphalique.
Il franchit aisément le placenta.
Élimination
Essentiellement urinaire en 30 heures.
5.3. Données de sécurité préclinique
Les études de toxicité par administration répétée chez le chien, par voie orale, n'a révélé aucun effet délétère à la dose de 10 g/kg/jour.
Les études effectuées chez l’animal indiquent que le piracétam n’a aucun effet sur la fertilité des rats mâles ou femelles.
Flacon de verre brun: 3 ans
Plaquettes (PVC/PVDC/Aluminium): 2 ans
6.4. Précautions particulières de conservation
A conserver à l'abri de l'humidité
6.5. Nature et contenu de l'emballage extérieur
45 comprimés pelliculés sécables en flacon de verre brun (type III).
84 comprimés pelliculés sécables en flacon de verre brun (type III).
90 comprimés pelliculés sécables en flacon de verre brun (type III).
45 comprimés pelliculés sécables sous plaquettes (PVC/PVDC/Aluminium).
84 comprimés pelliculés sécables sous plaquettes (PVC/PVDC/Aluminium).
90 comprimés pelliculés sécables sous plaquettes (PVC/PVDC/Aluminium).
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Pas d’exigences particulières.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
EG LABO - LABORATOIREES EUROGENERICS
CENTRAL PARK
9-15 RUE MAURICE MALLET
92130 ISSY-LES-MOULINEAUX
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 349 719 4 5: 45 comprimés pelliculés sécables en flacon (verre brun).
· 34009 349 720 2 7: 84 comprimés pelliculés sécables en flacon (verre brun).
· 34009 349 721 9 5: 90 comprimés pelliculés sécables en flacon (verre brun).
· 34009 349 722 5 6: 45 comprimés pelliculés sécables sous plaquettes (PVC/PVDC/Aluminium).
· 34009 349 723 1 7: 84 comprimés pelliculés sécables sous plaquettes (PVC/PVDC/Aluminium).
· 34009 349 724 8 5: 90 comprimés pelliculés sécables sous plaquettes (PVC/PVDC/Aluminium).
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
<{JJ mois AAAA}>
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste II
ANSM - Mis à jour le : 28/09/2020
PIRACETAM EG 800 mg, comprimé pelliculé sécable
Piracétam
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que PIRACETAM EG 800 mg, comprimé pelliculé sécable et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant de prendre PIRACETAM EG 800 mg, comprimé pelliculé sécable ?
3. Comment prendre> PIRACETAM EG 800 mg, comprimé pelliculé sécable ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver PIRACETAM EG 800 mg, comprimé pelliculé sécable ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE PIRACETAM EG 800 mg, comprimé pelliculé sécable ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique - code ATC : N06BX03
Ce médicament est indiqué dans les situations suivantes :
Chez l'adulte :
· traitement d'appoint de troubles mineurs chroniques (cognitifs ou neurosensoriels) liés au vieillissement (à l'exclusion de la maladie d'Alzheimer et des autres démences) ;
· traitement symptomatique des vertiges.
Chez l'enfant de plus de 30 kg (soit à partir d'environ 9 ans) :
· dyslexie.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT DE PRENDRE PIRACETAM EG 800 mg, comprimé pelliculé sécable ?
Ne prenez jamais PIRACETAM EG :
· si vous êtes allergique (hypersensible) au piracétam, à un dérivé de la pyrrolidone ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
· si vous présentez une anomalie grave de la fonction des reins,
· si vous avez une hémorragie cérébrale,
· si vous avez une chorée de Huntington (aggravation des symptômes).
Avertissements et précautions
Adressez-vous à votre médecin avant de prendre PIRACETAM EG, notamment si :
· vous devez subir une intervention chirurgicale,
· vous présentez des troubles de la coagulation,
· vous présentez une insuffisance rénale car votre posologie devra être adaptée.
Enfants et adolescents
Sans objet.
Autres médicaments et PIRACETAM EG
Adressez-vous à votre médecin si vous prenez en association à PIRACETAM EG :
· des hormones thyroïdiennes
· de l’acénocoumarol (anticoagulant oral)
Si vous avez des questions, demandez plus d'informations à votre médecin.
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
PIRACETAM EG avec des aliments, boissons et de l’alcool
Sans objet.
Grossesse et allaitement
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
Les effets de PIRACETAM EG chez la femme enceinte ne sont pas connus. C'est pourquoi, l’utilisation de PIRACETAM EG n'est pas recommandée pendant la grossesse.
PIRACETAM EG passe dans le lait maternel. L’allaitement est déconseillé pendant le traitement par PIRACETAM EG. Pendant le traitement par PIRACETAM EG, vous devrez discuter avec votre médecin avant de commencer à allaiter.
Conduite de véhicules et utilisation de machines
Les vertiges, pour lesquels ce médicament peut être prescrit, peuvent rendre dangereux la conduite d'un véhicule ou l'utilisation d'une machine.
PIRACETAM EG peut avoir une influence modérée sur votre aptitude à conduire des véhicules et à utiliser des machines. Une somnolence (ou d’autres effets indésirables) peut survenir après la prise de PIRACETAM EG.
Soyez prudent. Ne pas conduire de véhicules ni utiliser de machines sans avoir lu la notice.
PIRACETAM EG contient
Sans objet.
3. COMMENT PRENDRE PIRACETAM EG 800 mg, comprimé pelliculé sécable ?
La dose est fixée par votre médecin.
A titre indicatif, la posologie habituelle dans les troubles mineurs chroniques (cognitifs ou neurosensoriels) liés au vieillissement et dans les vertiges est de 1 comprimé matin, midi et soir, soit 3 comprimés par jour.
Utilisation chez les enfants
Chez l'enfant, la solution buvable est mieux adaptée.
Mode d'administration
Voie orale.
Avaler les comprimés sans les croquer, avec un peu d'eau.
La barre de cassure n’est là que pour faciliter la prise du comprimé si vous éprouvez des difficultés à l’avaler en entier.
Fréquence d'administration
Dans tous les cas, se conformer strictement à l'ordonnance de votre médecin.
Durée du traitement
Dans tous les cas, se conformer strictement à l'ordonnance de votre médecin.
Si vous avez pris plus de PIRACETAM EG que vous n’auriez dû :
Consultez immédiatement votre médecin ou votre pharmacien.
Si vous oubliez de prendre PIRACETAM EG :
Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre.
Si vous arrêtez de prendre PIRACETAM EG :
Sans objet.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Les effets indésirables rapportés avec PIRACETAM EG sont listés ci-dessous :
Fréquents (concernent jusqu’à 1 personne sur 10) :
· nervosité,
· hyperkinésie (mouvements involontaires et anormaux)
· prise de poids
Peu fréquents (concernent jusqu’à 1 personne sur 100) :
· dépression
· somnolence
· asthénie (épuisement)
Fréquence indéterminée (ne peut être estimée sur la base des données disponibles)
· réaction anaphylactoïde (réaction d’hypersensibilité non-allergique), hypersensibilité
· agitation, anxiété, confusion, hallucination
· ataxie (mouvements incoordonnés), troubles de l’équilibre, épilepsie aggravée, maux de tête, insomnie
· douleurs abdominales, maux d’estomac, diarrhée, nausées, vomissements
· œdème angioneurotique (gonflement, difficultés respiratoires ou de déglutition), dermatite (maladie de peau), prurit, urticaire (gonflement, rougeur, démangeaisons de la peau)
· vertiges
· hémorragie
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER PIRACETAM EG 800 mg, comprimé pelliculé sécable ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’emballage et la plaquette après EXP. La date de péremption fait référence au dernier jour de ce mois.
Pas de précautions particulières de conservation.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient PIRACETAM EG 800 mg, comprimé pelliculé sécable
· La substance active est :
Piracétam...................................................................................................................... 800 mg
Pour un comprimé pelliculé
· Les autres composants sont : Povidone K 30, stéarate de magnésium, macrogol 6000, éthylcellulose, hypromellose, sébaçate de dibutyle, dioxyde de titane, talc.
Qu’est-ce que PIRACETAM EG 800 mg, comprimé pelliculé sécable et contenu de l’emballage extérieur
Titulaire de l’autorisation de mise sur le marché
EG LABO - LABORATOIREES EUROGENERICS
CENTRAL PARK
9-15 RUE MAURICE MALLET
92130 ISSY-LES-MOULINEAUX
Exploitant de l’autorisation de mise sur le marché
EG LABO - LABORATOIREES EUROGENERICS
CENTRAL PARK
9-15 RUE MAURICE MALLET
92130 ISSY-LES-MOULINEAUX
KERESZTURI UT 30-38
1106 BUDAPEST
HONGRIE
ou
EGIS LACTA FACTORY
MATYAS KIRALY UT 65
9900 KÖRMEND
HONGRIE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
< {MM/AAAA}>< {mois AAAA}.>
Sans objet.
L’ANSM réévaluera chaque année toute nouvelle information sur ce médicament et si nécessaire cette notice sera mise à jour.>