Dernière mise à jour le 28/04/2026
CELLUVISC 4 mg/0,4 ml, collyre en récipient unidose
Indications thérapeutiques
Classe pharmacothérapeutique - code ATC : S01XA20
Ce médicament est utilisé pour soulager les signes d’irritation liés à la sécheresse de l’œil (quand il existe une insuffisance de larmes).
Présentations
> 30 récipient(s) unidose(s) polyéthylène de 0,4 ml
Code CIP : 337 974-4 ou 34009 337 974 4 7
Déclaration de commercialisation : 19/06/1996
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 2,92 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 3,94 €
- Taux de remboursement :65%
> 90 récipient(s) unidose(s) polyéthylène de 0,4 ml
Code CIP : 337 975-0 ou 34009 337 975 0 8
Déclaration de commercialisation : 15/01/2010
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 7,82 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 8,84 €
- Taux de remboursement :65%
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 09/01/2019 | Renouvellement d'inscription (CT) | Le service médical rendu par CELLUVISC reste important dans l’indication de l’AMM. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 09/09/2009 | Inscription (CT) | Absence d'amélioration du service médical rendu. |
ANSM - Mis à jour le : 17/02/2026
CELLUVISC 4 mg/0,4 ml, collyre en récipient unidose
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Carmellose sodique............................................................................................................ 4,00 mg
pour un récipient unidose.
Pour la liste complète des excipients, voir rubrique 6.1.
Solution limpide et incolore.
4.1. Indications thérapeutiques
4.2. Posologie et mode d'administration
Adultes (y compris les personnes âgées)
En instillation oculaire.
La posologie est de 1 goutte dans l’œil ou les yeux à traiter, 2 à 4 fois par jour et jusqu’à 8 fois selon la gravité des symptômes.
Population pédiatrique
La sécurité et l’efficacité de CELLUVISC dans la population pédiatrique n’ont pas été établies.
Mode d’administration
Tourner le capuchon pour ouvrir l’unidose et instiller le collyre.
Instiller le collyre dans le cul de sac conjonctival en tirant légèrement la paupière inférieure vers le bas et en regardant vers le haut.
Utiliser l’unidose immédiatement après ouverture et jeter après usage.
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
4.4. Mises en garde spéciales et précautions d'emploi
Ce collyre est présenté en récipients unidoses (à usage unique) et ne contient pas de conservateur : il existe donc un risque de rapide contamination bactérienne. Pour éviter toute contamination ou un possible dommage oculaire, ne pas mettre l’embout de l’unidose en contact avec l’œil, la paupière ou toute autre surface. L’unidose doit être jetée immédiatement après usage et ne doit pas être conservée en vue d’une utilisation ultérieure.
Un trouble visuel bref peut se produire à l’instillation du produit jusqu’à ce qu’il se répartisse uniformément à la surface de l’œil.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Aucune étude d’interaction n’a été réalisée.
4.6. Fertilité, grossesse et allaitement
Grossesse et allaitement
Il n'existe pas de données sur l'utilisation de ce médicament chez la femme enceinte ou qui allaite.
CELLUVISC ne sera prescrit qu'avec prudence chez la femme enceinte ou allaitante.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Dans ce cas, il doit être recommandé au patient de ne pas conduire ni utiliser de machines jusqu’à ce que la vision normale soit rétablie.
Les effets indésirables rapportés après utilisation de CELLUVISC sont classés par classes de systèmes d’organes et listés ci-dessous comme Très fréquent (³1/10) ; Fréquent (³1/100, <1/10) ; Peu fréquent (³1/1 000, <1/100) ; Rare (³1/10 000, <1/1 000) ; Très rare (<1/10 000) et fréquence indéterminée (ne peut être estimée sur la base des données disponibles) :
Affections oculaires
Fréquent :
Irritation oculaire (incluant brûlures et gène oculaire)
Expérience après la commercialisation :
Les effets indésirables suivants ont été identifiés lors de l’utilisation de CELLUVISC en pratique clinique après sa commercialisation. Sachant que la déclaration des effets indésirables après la commercialisation est un acte volontaire et émanant d’une population de taille incertaine, il n’est pas toujours possible d’estimer la fréquence de ces effets indésirables.
Affections du système immunitaire
Hypersensibilité incluant allergie oculaire avec des symptômes de type gonflement de l’œil ou œdème de la paupière.
Affections oculaires
Vision trouble, sensation de picotement, sensation de corps étranger, œil rouge, prurit, augmentation de la sécrétion lacrymale, écoulement oculaire, douleur oculaire, formation de croûtes au bord des paupières ou de résidu du médicament, altération de la vision.
Lésions, intoxications et complications liées aux procédures
Dommage superficiel de l’œil (résultant du contact entre l’embout de l’unidose et l’œil durant l’administration) et/ou abrasion cornéenne.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
Aucun cas de surdosage n’a été rapporté.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : substitut lacrymal, code ATC : S01XA20.
Mécanisme d’action
Ce collyre est un humidificateur de la cornée.
Il ne possède pas d’activité pharmacologique mais agit par un effet mécanique (lubrification, hydratation).
Il supplée à l’insuffisance de sécrétion des larmes, en reconstituant temporairement la phase aqueuse des larmes.
La carboxyméthylcellulose sodique entrant dans la composition de ce collyre est un agent de viscosité dérivé de la cellulose. Son rôle consiste à augmenter le temps de contact cornéen du collyre.
5.2. Propriétés pharmacocinétiques
Il n’existe pas d’étude pharmacocinétique contrôlée chez l’animal ou chez l’Homme.
Une absorption ou une accumulation dans les tissus oculaires peut être vraisemblablement exclue en raison du haut poids moléculaire de la carmellose.
5.3. Données de sécurité préclinique
Chlorure de sodium, lactate de sodium, chlorure de potassium, chlorure de calcium, eau purifiée.
Avant ouverture : 24 mois
Après ouverture : utiliser immédiatement et jeter le récipient unidose après usage. Ne pas conserver le récipient unidose après ouverture.
6.4. Précautions particulières de conservation
A conserver à une température ne dépassant pas 25°C.
Conserver les récipients unidoses dans le sachet et le sachet dans la boîte, à l’abri de la lumière et de l’humidité.
6.5. Nature et contenu de l'emballage extérieur
0,4 ml en récipient unidose (PE).
Conditionnements :
Boîte contenant 5 récipients unidoses.
Boîte contenant 10, 20, 30 ou 90 récipients unidoses en sachet aluminium. Chaque sachet aluminium contient 10 récipients unidoses.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Pas d’exigences particulières.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
5/13 BOULEVARD DE LA REPUBLIQUE
92100 BOULOGNE-BILLANCOURT
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 3379715 7 : 0,4 ml en récipient unidose (PE) ; boîte de 5
· 34009 3379721 8 : 0,4 ml en récipient unidose (PE) ; boîte de 10
· 34009 3379738 6 : 0,4 ml en récipient unidose (PE) ; boîte de 20
· 34009 3379744 7 : 0,4 ml en récipient unidose (PE) ; boîte de 30
· 34009 3379750 8 : 0,4 ml en récipient unidose (PE) ; boîte de 90
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
Date de première autorisation : {JJ mois AAAA}
Date de dernier renouvellement : {JJ mois AAAA}
10. DATE DE MISE A JOUR DU TEXTE
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Médicament non soumis à prescription médicale.
ANSM - Mis à jour le : 17/02/2026
CELLUVISC 4 mg/0,4 ml, collyre en récipient unidose
Carmellose sodique
Vous devez toujours utiliser ce médicament en suivant scrupuleusement les informations fournies dans cette notice ou par votre médecin ou votre pharmacien.
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Adressez-vous à votre pharmacien pour tout conseil ou information.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
· Vous devez vous adresser à votre médecin si vous ne ressentez aucune amélioration ou si vous vous sentez moins bien.
1. Qu'est-ce que CELLUVISC 4 mg/0,4 ml, collyre en récipient unidose et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser CELLUVISC 4 mg/0,4 ml, collyre en récipient unidose ?
3. Comment utiliser CELLUVISC 4 mg/0,4 ml, collyre en récipient unidose ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver CELLUVISC 4 mg/0,4 ml, collyre en récipient unidose ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE CELLUVISC 4 mg/0,4 ml, collyre en récipient unidose ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique - code ATC : S01XA20
Ce médicament est utilisé pour soulager les signes d’irritation liés à la sécheresse de l’œil (quand il existe une insuffisance de larmes).
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER CELLUVISC 4 mg/0,4 ml, collyre en récipient unidose ?
N’utilisez jamais CELLUVISC 4 mg/0,4 ml, collyre en récipient unidose :
· si vous êtes allergique à la carmellose sodique ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
Avertissements et précautions
Adressez-vous à votre médecin ou pharmacien avant d’utiliser CELLUVISC.
En cas de persistance des symptômes, CONSULTEZ UN OPHTALMOLOGISTE afin qu’il adapte votre traitement.
Ce collyre est présenté en unidose à usage unique et ne contient pas de conservateur. Il existe donc un risque de rapide contamination bactérienne.
Afin d’éviter toute contamination ou possible dommage de l’œil, ne toucher pas l’œil ou toute autre surface avec l’embout de l’unidose.
L’unidose doit être jetée immédiatement après usage et ne doit pas être conservée en vue d’une utilisation ultérieure.
Un trouble visuel bref peut se produire à l’instillation du produit jusqu’à ce qu’il se répartisse uniformément à la surface de l’œil.
Autres médicaments et CELLUVISC 4 mg/0,4ml, collyre en récipient unidose
En cas de traitement concomitant par un autre collyre, attendre 15 minutes entre les deux instillations et terminer par le produit le plus visqueux. CELLUVISC pouvant retarder la pénétration d’autres médicaments, doit être instillé en dernier s’il est le plus visqueux.
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
CELLUVISC 4 mg/0,4ml, collyre en récipient unidose avec des aliments, boissons et de l’alcool
Sans objet.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
Conduite de véhicules et utilisation de machines
La vision peut être brouillée pendant quelques minutes après l’instillation en fonction de la viscosité du produit. Dans ce cas, il doit être recommandé au patient de ne pas conduire ni utiliser de machines jusqu’à ce que la vision normale soit rétablie.
CELLUVISC 4 mg/0,4ml, collyre en récipient unidose contient du chlorure de sodium, du lactate de sodium, du chlorure de potassium, du chlorure de calcium et de l’eau purifiée
Sans objet.
3. COMMENT UTILISER CELLUVISC 4 mg/0,4 ml, collyre en récipient unidose ?
La dose recommandée est de 1 goutte dans l’œil ou les yeux à traiter 2 à 4 fois par jour et jusqu’à 8 fois par jour si la sécheresse de l’œil persiste.
Mode d’administration
Voie locale.
EN INSTILLATION OCULAIRE.
Une unidose permet de traiter les deux yeux.
Utiliser une nouvelle unidose à chaque application de la journée.
Pour une bonne utilisation du collyre, certaines précautions doivent être prises :
· Se laver soigneusement les mains avant,
· Ne pas toucher l’œil ou toute autre surface avec l’embout de l’unidose,
· Ne pas utiliser l’unidose si le capuchon semble cassé avant usage.
Pour utiliser une unidose, procéder de la façon suivante :
|
|
|
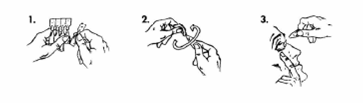
1. Détacher une unidose de la plaquette. 2. Tenir l’unidose à la verticale (capuchon tête en haut). Pour ouvrir l’unidose, tourner complètement la partie plate afin de rompre la soudure. 3. Tirer doucement la paupière inférieure vers le bas en regardant vers le haut. Renverser l’unidose et la presser légèrement pour faire tomber 1 goutte dans l’œil ou les yeux à traiter. Cligner des yeux plusieurs fois. |
Lorsque l’unidose est utilisée, la jeter immédiatement. Ne pas la conserver ni la réutiliser.
Fréquence d'administration
Répartir les instillations au cours de la journée, en fonction des besoins.
Durée du traitement
Si les troubles persistent ou s’aggravent, consulter un ophtalmologiste afin qu’il adapte votre traitement.
Si vous avez utilisé plus de CELLUVISC 4 mg/0,4 ml, collyre en récipient unidose que vous n’auriez dû
Consultez votre médecin ou votre pharmacien.
Si vous oubliez d’utiliser CELLUVISC 4 mg/0,4 ml, collyre en récipient unidose
Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre.
Si vous arrêtez d’utiliser CELLUVISC 4 mg/0,4 ml, collyre en récipient unidose
Sans objet.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Effets indésirables fréquents
Ces effets indésirables peuvent concerner 1 à 9 patients sur 100
Effets sur l’œil
· Irritation de l’œil (incluant brûlures et gêne oculaire).
Données post-commercialisation :
Les effets indésirables suivants ont été rapportés depuis la commercialisation du produit :
Effets indésirables dont la fréquence est indéterminée
· Réactions allergiques (incluant gonflement de l’œil ou des paupières).
· Ecoulement de l’œil.
· Douleur de l’œil.
· Formation de croûtes sur les paupières ou de résidus de produit.
· Troubles de la vision.
· Blessure superficielle de l’œil due au contact entre l’embout de l’unidose et l’œil lors de l’administration, et/ou traumatisme superficiel de la cornée.
· Vision trouble.
· Sensation de picotement.
· Sensation d’avoir quelque chose dans l’œil.
· Démangeaisons des yeux.
· Œil rouge.
· Augmentation des larmoiements.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER CELLUVISC 4 mg/0,4 ml, collyre en récipient unidose ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur le récipient unidose, le sachet en aluminium et l’emballage après EXP. La date de péremption fait référence au dernier jour de ce mois.
A conserver à une température ne dépassant pas 25°C.
Conserver les récipients unidoses dans le sachet et le sachet dans la boîte, à l’abri de la lumière et de l’humidité.
Après ouverture : utiliser immédiatement et jeter le récipient unidose après usage. Ne pas conserver le récipient unidose après ouverture.
N’utilisez pas ce médicament si vous remarquez que l’emballage est endommagé, que la solution a changé de couleur ou est devenue trouble.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient CELLUVISC 4 mg/0,4 ml, collyre en récipient unidose
· La substance active est :
Carmellose sodique ..................................................................................................... 4,00 mg
· Les autres composants sont : chlorure de sodium, lactate de sodium, chlorure de potassium, chlorure de calcium, eau purifiée.
Collyre.
Boîte contenant 5 récipients unidoses.
Boîte contenant 10, 20, 30 ou 90 récipients unidoses en sachet aluminium. Chaque sachet aluminium contient 10 récipients unidoses.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
5/13 BOULEVARD DE LA REPUBLIQUE
92100 BOULOGNE-BILLANCOURT
Exploitant de l’autorisation de mise sur le marché
ABBVIE
5/13 BOULEVARD DE LA REPUBLIQUE
92100 BOULOGNE-BILLANCOURT
ALLERGAN PHARMACEUTICALS IRELAND
CASTLEBAR ROAD
WESTPORT
CO. MAYO
IRLANDE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
{mois AAAA}.
Sans objet.
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).