Dernière mise à jour le 02/03/2026
TRAVOPROST EG 40 microgrammes/mL, collyre en solution
Indications thérapeutiques
Classe pharmacothérapeutique - code ATC : S01EE04
TRAVOPROST EG contient du travoprost, qui fait partie d'un groupe de médicaments appelés analogues des prostaglandines. Il agit en diminuant la pression dans l’œil. Il peut être utilisé seul ou en association avec d’autres collyres comme les bêtabloquants, qui réduisent aussi la pression oculaire.
TRAVOPROST EG est utilisé pour réduire une pression élevée à l’intérieur de l'œil chez les adultes, les adolescents et les enfants âgés de 2 mois et plus. Cette pression peut conduire à une maladie appelée glaucome.
Présentations
> 1 flacon polypropylène de 2,5 mL avec compte-gouttes polyéthylène basse densité (PEBD)
Code CIP : 278 870-7 ou 34009 278 870 7 9
Déclaration de commercialisation : 16/06/2017
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 5,56 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 6,58 €
- Taux de remboursement :65%
Service médical rendu (SMR)
Amélioration du service médical rendu (ASMR)
Ce médicament étant un générique, l'ASMR n'a pas été évalué par la commission de la transparence (CT), il est possible de se référer à la /aux spécialité(s) de référence du groupe générique auquel appartient ce médicament (cliquez ici pour aller à la rubrique des groupes génériques)
ANSM - Mis à jour le : 12/12/2022
TRAVOPROST EG 40 microgrammes/mL, collyre en solution
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chaque mL de solution contient 40 microgrammes de travoprost.
Teneur moyenne en substance active/goutte : 0,97 - 1,4 μg
Excipients à effet notoire : 150 microgrammes/mL de chlorure de benzalkonium, 5 mg/mL d’hydroxystéarate de macrogolglycérol 40.
Pour la liste complète des excipients, voir rubrique 6.1.
Solution limpide et incolore.
Osmolalité : 266 – 294 mOsm/kg.
4.1. Indications thérapeutiques
Réduction de la pression intraoculaire élevée chez les patients pédiatriques âgés de 2 mois à < 18 ans atteints d’hypertonie intraoculaire ou de glaucome pédiatrique (voir rubrique 5.1).
4.2. Posologie et mode d'administration
Utilisation chez les adultes et les sujets âgés.
La posologie est d’une goutte de TRAVOPROST EG dans le cul-de-sac conjonctival de l’œil ou des yeux atteint(s) une fois par jour. L’effet est optimal si le traitement est administré le soir.
Une occlusion nasolacrymale ou une fermeture douce des paupières après administration est recommandée. Ceci peut réduire l’absorption systémique des médicaments administrés par voie oculaire et conduire à une diminution des effets indésirables systémiques.
En cas d’utilisation de plusieurs collyres, les médicaments doivent être administrés avec au moins 5 minutes d’écart (voir rubrique 4.5).
Si une instillation est oubliée, le traitement doit être poursuivi avec l'instillation suivante comme prévu. La posologie ne doit pas dépasser une goutte par jour dans l’œil ou les yeux atteint(s).
En cas de remplacement d’un autre médicament antiglaucomateux ophtalmique par TRAVOPROST EG, l’autre médicament doit être interrompu et TRAVOPROST EG doit être commencé le jour suivant.
Population pédiatrique
Le travoprost peut être utilisé chez les patients pédiatriques âgés de 2 mois à < 18 ans à la même posologie que chez l’adulte. Cependant, les données pour le groupe d’âge 2 mois à < 3 ans (9 patients) sont limitées (voir rubrique 5.1).
La sécurité et l’efficacité de travoprost chez les enfants de moins de 2 mois n’ont pas été établies. Aucune donnée n’est disponible.
Insuffisants hépatiques et rénaux
Le travoprost a été étudié chez les insuffisants hépatiques légers à sévères et chez les insuffisants rénaux légers à sévères (clairance de la créatinine jusqu’à 14 mL/min). Aucune adaptation de la posologie n’est nécessaire chez ces patients (voir rubrique 5.2).
Mode d'administration
Voie ophtalmique.
Pour les patients qui portent des lentilles, voir la rubrique 4.4.
Le patient doit retirer le sachet protecteur juste avant la première utilisation. Pour éviter la contamination de l’embout compte-gouttes et de la solution, il faut faire attention de ne pas toucher les paupières, les surfaces voisines ou d’autres surfaces avec l’embout compte-gouttes du flacon.
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
4.4. Mises en garde spéciales et précautions d'emploi
Modification de la couleur des yeux
Le travoprost peut modifier progressivement la couleur des yeux en augmentant le nombre de mélanosomes (granules pigmentaires) dans les mélanocytes. Avant l’instauration du traitement, les patients doivent être informés du risque de changement permanent de la couleur de l’œil. Un traitement unilatéral peut avoir pour conséquence une hétérochromie définitive. Les effets à long terme sur les mélanocytes et leurs conséquences ne sont actuellement pas connus. La modification de la couleur de l’iris évolue lentement et peut passer inaperçue pendant des mois, voire des années. Le changement de la couleur des yeux a surtout été observé chez des patients ayant l’iris bicolore, c’est-à-dire bleu-marron, gris-marron, jaune-marron et vert-marron ; cependant, il a également été observé chez des patients ayant des yeux marron. Généralement, pour l’œil concerné, la pigmentation brune entourant la pupille s’étend de façon concentrique vers la périphérie, et l’iris peut devenir, en partie ou en totalité, brun plus foncé. Après l’arrêt du traitement, aucune augmentation ultérieure de la pigmentation brune de l’iris n’a été observée.
Changements périorbitaires ou palpébrales
Au cours des essais cliniques contrôlés, un assombrissement de la peau périorbitaire et/ou palpébrale associé à l’utilisation du travoprost a été rapporté chez 0,4 % des patients. Des changements périorbitaires et palpébrales, un approfondissement du pli palpébral inclus, ont aussi été observés avec les analogues des prostaglandines.
Le travoprost peut modifier progressivement les cils de l’œil ou des yeux traité(s). Au cours des essais cliniques, ces changements, représentés par une augmentation de la longueur, de l’épaisseur, de la pigmentation et/ou du nombre de cils, ont été observés chez la moitié des patients environ. Le mécanisme de modifications des cils et ses conséquences à long terme sont actuellement inconnus.
Lors des études chez le singe, le travoprost a entraîné une légère augmentation de la fente palpébrale. Cependant, cet effet n’a pas été observé au cours des essais cliniques et est considéré comme étant spécifique à l’espèce.
Il n’y a pas de données concernant l’utilisation du travoprost sur un œil inflammatoire, dans les glaucomes néovasculaires, congénitaux, à angle étroit ou à angle fermé. L’expérience est encore limitée en ce qui concerne les atteintes oculaires d’origine thyroïdienne, le glaucome à angle ouvert des patients pseudophaques et les glaucomes pigmentaires ou pseudo-exfoliatifs. Il est donc recommandé d’utiliser le travoprost avec précaution chez les patients avec une inflammation intraoculaire active.
Patients aphaques
De l’œdème maculaire a été rapporté pendant le traitement avec des analogues des prostaglandines F2α. Il est recommandé d’utiliser le travoprost avec précaution chez des patients aphaques, pseudophaques présentant une rupture capsulaire du cristallin ou porteurs d’implant de chambre antérieure ou chez des patients présentant des facteurs de risques connus d’œdème maculaire cystoïde.
Iritis/uvéite
Chez les patients présentant des facteurs de risque connus aux iritis/uvéites, le travoprost devra être utilisé avec précaution.
Contact cutané
Le contact cutané avec le travoprost doit être évité étant donné que l’absorption transdermique a été démontrée chez le lapin.
Il a été constaté que le chlorure de benzalkonium, qui est fréquemment utilisé en tant qu’agent conservateur dans les produits ophtalmiques, est à l'origine de kératopathie ponctuée et/ou de kératopathie ulcérative toxique. Étant donné que TRAVOPROST EG contient du chlorure de benzalkonium, une surveillance étroite s’impose lors d’une utilisation fréquente ou prolongée.
Les prostaglandines et les analogues de prostaglandines sont des substances biologiquement actives pouvant être absorbées par la peau. Les femmes enceintes ou souhaitant le devenir devront prendre des précautions appropriées pour éviter une exposition directe au contenu du flacon. En cas de contact accidentel avec le contenu du flacon, laver immédiatement et soigneusement la zone concernée.
Lentilles de contact :
TRAVOPROST EG contient du chlorure de benzalkonium qui peut entraîner une irritation de l’œil et est connu pour décolorer les lentilles de contact souples. Le contact avec les lentilles de contact souples doit être évité.
Les patients doivent être informés d’enlever leurs lentilles de contact avant instillation de TRAVOPROST EG et d’attendre 15 minutes après instillation de la dose avant de poser des lentilles de contact.
TRAVOPROST EG contient de l’hydroxystéarate de macrogolglycérol 40 qui peut entraîner des réactions cutanées.
Population pédiatrique
L’efficacité et la tolérance dans le groupe d’âge de 2 mois à < 3 ans (9 patients) sont limitées (voir rubrique 5.1). Aucune donnée n’est disponible pour les enfants de moins de 2 mois. Pour les enfants de moins de 3 ans qui souffrent principalement de GCP (glaucome congénital primaire), la chirurgie, (p. ex. la trabéculotomie/goniotomie) reste le traitement de première intention. Aucune donnée sur la sécurité à long terme n'est disponible dans la population pédiatrique.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Aucune étude d’interaction n’a été réalisée.
4.6. Fertilité, grossesse et allaitement
Femmes en âge de procréer/contraception
Le travoprost ne doit pas être utilisé chez les femmes en âge de procréer à moins qu’une contraception adéquate ne soit mise en place (voir rubrique 5.3).
Grossesse
Le travoprost a des effets pharmacologiques délétères sur la grossesse et/ou le fœtus/nouveau-né. Le travoprost ne doit pas être utilisé pendant la grossesse sauf en cas de nécessité absolue.
Allaitement
Il n'existe pas de données concernant l'excrétion du travoprost dans le lait maternel humain. Des études effectuées chez l'animal ont démontré que le travoprost et ses métabolites sont excrétés dans le lait maternel. L’utilisation du travoprost n’est pas recommandée pendant l'allaitement.
Fertilité
Il n'existe pas de données sur les effets du travoprost sur la fertilité humaine. Des études chez l’animal n’ont démontré aucun effet du travoprost sur la fertilité à des doses de plus de 250 fois la dose maximum oculaire recommandée chez l’homme.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Résumé du profil de sécurité
Au cours des études cliniques avec le travoprost, les effets indésirables les plus fréquents étaient l’hyperémie oculaire et une hyperpigmentation de l’iris, survenant respectivement chez environ 20 % et 6 % des patients.
Liste des effets indésirables sous forme de tableau
Les effets indésirables suivants ont été considérés comme liés au traitement (avec travoprost en monothérapie) et ont été classés de la façon suivante : très fréquent (≥ 1/10), fréquent (≥ 1/100, < 1/10), peu fréquent (≥ 1/1 000, < 1/100), rare (≥ 1/10 000, < 1/1 000), très rare (< 1/10 000) ou fréquence indéterminée (ne peut être estimée sur la base des données disponibles. Au sein de chaque groupe de fréquence, les effets indésirables sont présentés suivant un ordre décroissant de gravité. Les effets indésirables ont été obtenus des études cliniques et des données post-marketing de travoprost.
|
Classe de systèmes d’organes |
Fréquence |
Effets indésirables |
|
Affections du système immunitaire |
Peu fréquent |
hypersensibilité, allergie saisonnière |
|
Affections psychiatriques |
Fréquence indéterminée |
dépression, anxiété, insomnie |
|
Affections du système nerveux |
Peu fréquent |
Céphalées |
|
Rare |
étourdissement, anomalie du champ visuel, dysgueusie |
|
|
Affections oculaires |
Très fréquent |
hyperémie oculaire |
|
Fréquent |
hyperpigmentation de l’iris, douleur oculaire, gêne oculaire, sécheresse oculaire, prurit oculaire, irritation oculaire |
|
|
Peu fréquent |
érosion de la cornée, uvéite, iritis, inflammation de la chambre antérieure, kératite, kératite ponctuée, photophobie, sécrétions oculaires, blépharite, érythème des paupières, œdème périobitale, prurit oculaire, baisse d’acuité visuelle, vision trouble, augmentation de la sécrétion lacrymale, conjonctivite, ectropion, cataracte, bord de la paupière croûteux, croissance des cils |
|
|
Rare |
iridocyclite, herpès ophtalmique simplex, inflammation oculaire, photopsie, eczéma des paupières, œdème conjonctival, effet de halo, follicules conjonctivaux, hypo-esthésie oculaire, trichiasis, meibomite, pigmentation de la chambre antérieure, mydriase, asthénopie, hyperpigmentation des cils, épaississement des cils |
|
|
Fréquence indéterminée |
œdème maculaire, sulcus de la paupière enfoncé |
|
|
Affections de l’oreille et du labyrinthe |
Fréquence indéterminée |
sensation vertigineuse, acouphène |
|
Affections cardiaques |
Peu fréquent |
palpitations |
|
Rare |
fréquence cardiaque irrégulière, fréquence cardiaque diminuée, arythmie |
|
|
Fréquence indéterminée |
douleur thoracique, bradycardie, tachycardie |
|
|
Affections vasculaires |
Rare |
diminution de la pression artérielle diastolique, augmentation de la pression artérielle systolique, hypotension, hypertension |
|
Affections respiratoires, thoraciques et médiastinales |
Peu fréquent |
toux, congestion nasale, irritation de la gorge |
|
Rare |
dyspnée, asthme, trouble respiratoire, douleur oropharyngée, dysphonie, rhinite allergique, sècheresse nasale |
|
|
Fréquence indéterminée |
asthme aggravé, épistaxis |
|
|
Affections gastro-intestinales |
Rare |
réactivation d’un ulcère gastro-duodénal, affection gastro-intestinale, constipation |
|
Fréquence indéterminée |
diarrhées, douleurs abdominales, nausées, vomissements |
|
|
Affections de la peau et du tissu sous-cutané |
Peu fréquent |
hyperpigmentation cutanée (péri-oculaire), dépigmentation cutanée, texture anormale des cheveux, hypertrichose |
|
Rare |
dermatite allergique, dermatite de contact, érythème, éruption cutanée, modification de la couleur des cheveux, madarose |
|
|
Fréquence indéterminée |
prurit, pousse des cheveux anormale |
|
|
Affections musculo-squelettiques et systémiques |
Rare |
douleurs musculo-squelettiques, arthralgie |
|
Affections du rein et des voies urinaires |
Fréquence indéterminée |
dysurie, incontinence urinaire |
|
Troubles généraux et anomalies au site d’administration |
Rare |
asthénie |
|
Investigations |
Fréquence indéterminée |
antigènes spécifiques de la prostate augmentés |
Population pédiatrique
Lors d’un essai clinique de phase 3 d’une durée de 3 mois et d’une étude pharmacocinétique d’une durée de 7 jours impliquant 102 patients pédiatriques exposés au travoprost, les types et caractéristiques des effets indésirables rapportés ont été similaires à ce qui a été observé chez les patients adultes. Les profils de sécurité à court terme dans les différents sous-groupes pédiatriques étaient également comparables (voir rubrique 5.1). Les effets indésirables les plus fréquemment rapportés chez la population pédiatrique étaient l’hyperémie oculaire (16,9 %) et la croissance des cils (6,5 %). Dans une étude similaire de 3 mois chez des patients adultes, ces événements sont survenus avec une incidence de 11,4 % et 0,0 % respectivement.
Les effets indésirables supplémentaires rapportés chez les patients pédiatriques dans l’étude pédiatrique sur 3 mois (n=77) comparés à une étude similaire chez l’adulte (n=185) ont inclus érythème des paupières, kératite, augmentation de la sécrétion lacrymale et photophobie. Ces effets ont tous été rapportés comme des événements uniques avec une incidence de 1,3 % versus 0,0 % observé chez l’adulte.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr
Aucun cas de surdosage n’a été rapporté. Un surdosage local est peu probable et vraisemblablement pas associé à une toxicité. Un surdosage oculaire de travoprost peut être rincé avec de l’eau tiède. Le traitement d’une ingestion orale suspectée est symptomatique et de soutien.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Mécanisme d’action
Le travoprost, analogue de la prostaglandine F2α, est un agoniste complet hautement sélectif ayant une haute affinité pour le récepteur FP aux prostaglandines qui diminue la pression intraoculaire en augmentant l’écoulement de l’humeur aqueuse par le système trabéculaire et les voies uvéosclérales. Chez l’homme, la diminution de la pression intraoculaire débute environ 2 heures après l’administration et l’effet maximal est atteint au bout de 12 heures. Après une administration unique, une baisse significative de la pression intraoculaire peut être maintenue pour des périodes excédant 24 heures.
Efficacité et sécurité cliniques
Lors d’un essai clinique, une réduction de la pression intraoculaire de 8 à 9 mmHg (environ 33 %) par rapport à la pression intraoculaire de base de 24 à 26 mmHg a été obtenue chez des patients qui présentaient un glaucome à angle ouvert ou une hypertension oculaire et qui avaient été traités par travoprost (conservé avec du polyquaternium) à raison d’une fois par jour, le soir. Les données relatives à l’administration conjointe de travoprost avec du timolol 0,5 % et les données limitées de l’administration conjointe avec la brimonidine 0,2 % qui ont été rassemblées au cours des essais cliniques montrent un effet additif du travoprost avec ces médicaments antiglaucomateux. Aucune donnée clinique sur l’utilisation conjointe avec les autres médicaments oculaires hypotensifs n’est disponible.
Pharmacologie secondaire
Chez le lapin, le travoprost augmente significativement le flux sanguin à la tête du nerf optique dans les 7 jours suivant l’instillation oculaire (1,4 microgrammes, une fois par jour).
Le travoprost conservé avec le polyquaternium-1 a entrainé une toxicité minimale pour la surface oculaire par rapport aux collyres conservés avec du chlorure de benzalkonium, lors de l’application sur les cellules cornéennes humaines ou après administration locale oculaire chez le lapin.
Population pédiatrique
L’efficacité de travoprost chez la population pédiatrique âgée de 2 mois à moins de 18 ans a été démontrée lors d’une étude clinique de 12 semaines en double aveugle de travoprost comparé à timolol chez 152 patients présentant une hypertension oculaire ou un glaucome pédiatrique Les patients ont reçu soit du travoprost à 0,004 % une fois par jour, soit du timolol 0,5 % (ou 0,25 % pour les patients de moins de 3 ans) deux fois par jour. Le critère principal d’efficacité était le changement de la pression intraoculaire (PIO) par rapport à la valeur initiale à la Semaine 12 de l’étude. Les réductions moyennes de la pression intraoculaire dans les groupes travoprost et timolol ont été équivalentes (voir Tableau 1).
Dans les groupes d’âge 3 ans à ˂ 12 ans (n=36) et 12 ans à ˂ 18 ans (n=26), la réduction moyenne de la PIO à la Semaine 12 dans le groupe travoprost était similaire à celle du groupe timolol. La réduction moyenne de la PIO à la Semaine 12 dans le groupe d’âge de 2 mois à ˂ 3 ans était de 1,8 mmHg dans le groupe travoprost et de 7,3 mmHg dans le groupe timolol. Les réductions de la PIO pour ce groupe étaient observées pour 6 patients seulement dans le groupe timolol et 9 patients dans le groupe travoprost où 4 patients du groupe travoprost par rapport à 0 patients dans le groupe timolol avaient une réduction moyenne de la PIO non significative à la Semaine 12. Aucune donnée n’est disponible pour les enfants âgés de moins de 2 mois.
L’effet sur la PIO a été observé après la seconde semaine de traitement et a été constamment maintenu tout au long de la période d’étude de 12 semaines pour tous les groupes d’âge.
Table 1 – Comparaison du changement de la PIO moyenne par rapport à la valeur initiale
(mmHg) à la Semaine 12
|
Travoprost |
Timolol |
||||
|
N |
Moyenne
|
N |
Moyenne
|
Différence
|
(IC à 95 %) |
|
53 |
-6,4 |
60 |
-5,8 |
-0,5 |
(-2,1; 1,0) |
|
SE = Ecart-Type; IC = Intervalle de Confiance; a La différence moyenne est Travoprost - Timolol. Les estimations sont fondées sur les moyennes des moindres carrés dérivées d'un modèle statistique qui rend compte des mesures corrélées de la PIO parmi les patients dont le diagnostic de PIO primaire et de base sont dans le modèle. |
|||||
5.2. Propriétés pharmacocinétiques
Le travoprost est une prodrogue de type ester. Il est absorbé à travers la cornée où l’ester d’isopropyl devient actif après hydrolyse en acide. Des études chez le lapin ont montré que des pics de concentration, dans l’humeur aqueuse, de 20 ng/mL d’acide libre ont été atteints une à deux heures après instillation oculaire du travoprost. Les concentrations dans l’humeur aqueuse déclinent avec une demi-vie de 1,5 heure environ.
Distribution
A la suite de l’administration locale oculaire du travoprost chez des volontaires sains, une faible exposition systémique à la forme active (acide libre) a été démontrée. Des pics de concentrations plasmatiques de forme active (acide libre) de 25 pg/mL ou moins ont été observés entre 10 et 30 minutes après administration. Ainsi, les taux plasmatiques diminuent rapidement au-dessous de la valeur quantifiable de 10 pg/mL une heure après administration. En raison de la faible concentration plasmatique et de l’élimination rapide après administration locale, la demi-vie d’élimination de la forme active (acide libre) n’a pas pu être déterminée chez l’homme.
Biotransformation
Le métabolisme est la principale voie d’élimination du travoprost et de sa forme active (acide libre). Les mécanismes métaboliques systémiques sont équivalents à ceux de la prostaglandine F2α endogène, qui sont caractérisés par la réduction de la double liaison 13-14, l’oxydation de la fonction 15-hydroxyle ainsi que le clivage par oxydation β de la partie supérieure de la chaîne latérale.
Élimination
Le travoprost sous forme d’acide libre et ses métabolites sont principalement excrétés par les reins. Le travoprost a été étudié chez les insuffisants hépatiques légers à sévères et chez les insuffisants rénaux légers à sévères (clairance de la créatinine jusqu’à 14 mL/min). Aucune adaptation de la posologie n’est nécessaire chez ces patients.
Population pédiatrique
Une étude pharmacocinétique chez des patients pédiatriques âgés de 2 mois à < 18 ans a démontré une exposition plasmatique très faible au travoprost sous forme d’acide libre, avec des concentrations allant d’une valeur inférieure à la limite de dosage de 10 pg/mL à 54,5 pg/mL. Dans 4 études pharmacocinétiques chez des populations adultes, les concentrations plasmatiques de travoprost sous forme d'acide libre était de BLQ à 52,0 pg/mL.
Tandis que la majorité des valeurs plasmatiques dans toutes les études était non-quantifiable, rendant les comparaisons statistiques de l’exposition systémique à travers les groupes d’âge irréalisables, la tendance générale montre que l’exposition plasmatique au travoprost sous forme d’acide libre après une administration topique de travoprost est extrêmement faible à travers tous les groupes d’âge évalués.
5.3. Données de sécurité préclinique
Des études de toxicité de reproduction du travoprost par voie systémique ont été réalisées chez le rat, la souris et le lapin. Les résultats sont liés à l’activité agoniste du récepteur FP de l’utérus avec létalité embryonnaire précoce, perte post-implantation, fœtotoxicité. Chez la rate gravide, l’administration systémique de travoprost à des doses plus de 200 fois supérieures à la dose thérapeutique pendant la période d’organogenèse, a conduit à une augmentation de l’incidence des malformations. Après administration de 3H-travoprost à des rates gravides, une faible radioactivité a été mesurée dans le liquide amniotique et dans les tissus fœtaux. Les études de reproduction et de développement ont démontré un effet abortif important avec un taux élevé chez le rat et la souris (respectivement de 180 pg/mL et 30 pg/mL dans le plasma) avec une exposition 1,2 à 6 fois supérieures à l’exposition thérapeutique (jusqu’à 25 pg/mL).
Des études spécifiques d’interactions in vitro avec travoprost et des médicaments contenant du thiomersal ont été effectuées. Aucune précipitation n’a été observée.
3 ans.
Jeter 4 semaines après la première ouverture.
6.4. Précautions particulières de conservation
Avant ouverture, conserver le flacon dans son sachet d'emballage à l’abri de l'humidité.
Après la première ouverture, ce médicament ne nécessite pas de précautions particulières de conservation.
6.5. Nature et contenu de l'emballage extérieur
Flacon translucide en polypropylène (PP) de 5 mL muni d’un compte-gouttes transparent en polyéthylène basse densité (PEBD) et d’un bouchon à vis blanc inviolable en polyéthylène haute densité (PEHD), présenté dans un sachet en polyéthylène téréphtalate/aluminium/polyéthylène (PET/Alu/PE). Chaque flacon contient 2,5 mL de collyre.
Boîtes de 1, 3, 6, 9, 10 ou 12 flacons.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Pas d'exigences particulières.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
EG LABO - LABORATOIRES EUROGENERICS
CENTRAL PARK
15 RUE MAURICE MALLET
92130 ISSY LES MOULINEAUX
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 278 870 7 9 : 2,5 mL en flacon (Polypropylène); boîte de 1.
· 34009 586 747 1 6 : 2,5 mL en flacon (Polypropylène); boîte de 3.
· 34009 586 748 8 4 : 2,5 mL en flacon (Polypropylène); boîte de 6.
· 34009 586 749 4 5 : 2,5 mL en flacon (Polypropylène); boîte de 9.
· 34009 586 750 2 7 : 2,5 mL en flacon (Polypropylène); boîte de 10.
· 34009 586 751 9 5 : 2,5 mL en flacon (Polypropylène); boîte de 12.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Médicament soumis à prescription médicale.
Liste I.
ANSM - Mis à jour le : 12/12/2022
TRAVOPROST EG 40 microgrammes/mL, collyre en solution
Travoprost
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que TRAVOPROST EG 40 microgrammes/mL, collyre en solution et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser TRAVOPROST EG 40 microgrammes/mL, collyre en solution ?
3. Comment utiliser TRAVOPROST EG 40 microgrammes/mL, collyre en solution ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver TRAVOPROST EG 40 microgrammes/mL, collyre en solution ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE TRAVOPROST EG 40 microgrammes/mL, collyre en solution ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique - code ATC : S01EE04
TRAVOPROST EG contient du travoprost, qui fait partie d'un groupe de médicaments appelés analogues des prostaglandines. Il agit en diminuant la pression dans l’œil. Il peut être utilisé seul ou en association avec d’autres collyres comme les bêtabloquants, qui réduisent aussi la pression oculaire.
TRAVOPROST EG est utilisé pour réduire une pression élevée à l’intérieur de l'œil chez les adultes, les adolescents et les enfants âgés de 2 mois et plus. Cette pression peut conduire à une maladie appelée glaucome.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER TRAVOPROST EG 40 microgrammes/mL, collyre en solution ?
N’utilisez jamais TRAVOPROST EG 40 microgrammes/mL, collyre en solution
· si vous êtes allergique (hypersensible) au travoprost ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
Demandez l’avis de votre médecin si vous êtes atteint de ces troubles.
Avertissements et précautions
Adressez-vous à votre médecin ou pharmacien avant d’utiliser TRAVOPROST EG 40 microgrammes/mL, collyre en solution.
· Travoprost EG peut augmenter la longueur, l’épaisseur, la couleur et/ou le nombre de vos cils. Des changements au niveau des paupières, y compris une pilosité anormale, ou au niveau des tissus autour des yeux ont également été observés.
· Travoprost EG peut modifier la couleur de votre iris (la partie colorée de votre œil). Ce changement peut être permanent. Un changement de couleur de la peau autour de l’œil peut également survenir.
· Si vous avez eu une chirurgie de la cataracte, adressez-vous à votre médecin avant d’utiliser Travoprost EG.
· Si vous avez ou avez déjà eu une inflammation de l’œil (iritis et uvéite), adressez-vous à votre médecin avant d’utiliser Travoprost EG.
· Travoprost EG peut, à de rares occasions, provoquer des essoufflements ou une respiration sifflante, ou augmenter les symptômes de l'asthme. Si vous observez des changements dans votre manière de respirer lorsque vous utilisez TRAVOPROST EG, prévenez immédiatement votre médecin.
· Travoprost EG peut être absorbé par la peau. Si ce médicament vient en contact avec la peau, il doit être enlevé aussitôt par lavage. Ceci est particulièrement important pour les femmes enceintes ou souhaitant le devenir.
· Si vous êtes porteur de lentilles de contact souples, n’utilisez pas le collyre lorsque vous portez vos lentilles. Après avoir utilisé le collyre, attendez 15 minutes avant de remettre vos lentilles.
Enfants et adolescents
TRAVOPROST EG peut être utilisé chez les enfants de 2 mois à 18 ans à la même posologie que pour l’adulte. L’utilisation de TRAVOPROST EG n’est pas recommandée pour les enfants âgés de moins de 2 mois.
Autres médicaments et TRAVOPROST EG 40 microgrammes/mL, collyre en solution
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
TRAVOPROST EG 40 microgrammes/mL, collyre en solution avec des aliments et boissons
Sans objet.
N’utilisez pas TRAVOPROST EG si vous êtes enceinte. Si vous pensez être enceinte, parlez-en à votre médecin aussitôt. Si vous êtes susceptible de pouvoir tomber enceinte, utilisez un moyen de contraception adéquat pendant l’utilisation de Travoprost EG.
N’utilisez pas TRAVOPROST EG si vous allaitez. Travoprost EG peut passer dans votre lait.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin avant de prendre tout médicament.
Conduite de véhicules et utilisation de machines
Vous pouvez trouver que votre vision est trouble juste après avoir utilisé TRAVOPROST EG. Ne conduisez pas de voiture et n’utilisez pas de machines avant que cet effet ait disparu.
TRAVOPROST EG 40 microgrammes/mL, collyre en solution contient de l’hydroxystéarate de macrogolglycérol 40
Ce médicament contient de l’hydroxystéarate de macrogolglycérol 40 qui peut entraîner des réactions cutanées.
TRAVOPROST EG 40 microgrammes/mL, collyre en solution contient du chlorure de benzalkonium.
Ce médicament contient 0.15 mg de chlorure de benzalkonium par ml.
Le chlorure de benzalkonium peut être absorbé par des lentilles de contact souples et peut changer la couleur des lentilles. Retirer les lentilles de contact avant application et attendre au moins 15 min avant de les remettre.
Le chlorure de benzalkonium peut également causer une irritation des yeux, surtout si vous avez les yeux secs ou des troubles de la cornée (la couche claire à l'avant de l'œil). Si vous ressentez une sensation oculaire anormale, des picotements ou des douleurs dans l'œil après avoir utilisé ce médicament, parlez-en à votre médecin.
3. COMMENT UTILISER TRAVOPROST EG 40 microgrammes/mL, collyre en solution ?
La dose recommandée est de :
Une goutte dans l’œil ou les yeux malade(s), une fois par jour – le soir. Utilisez TRAVOPROST EG dans les deux yeux uniquement si votre médecin vous a dit de le faire. Utilisez-le aussi longtemps que votre médecin ou le médecin traitant de votre enfant vous l’a dit.
Utilisez TRAVOPROST EG seulement en gouttes dans votre œil/vos yeux ou celui/ceux de votre enfant.
|
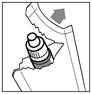
1 |
· Ouvrez le sachet d’emballage juste avant d’utiliser le flacon pour la première fois. Sortez-en le flacon (figure 1) et inscrivez la date d’ouverture sur l’étiquette dans l’espace prévu à cet effet. · Lavez-vous les mains. · Dévissez le bouchon. |
|
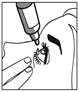
2 |
· Tenez le flacon tête en bas, entre le pouce et vos autres doigts. · Penchez la tête ou la tête de votre enfant en arrière. Avec un doigt propre, tirez doucement votre paupière vers le bas pour créer un sillon entre la paupière et l’œil. La goutte sera déposée à cet endroit (figure 2). · Rapprochez l’embout du flacon de votre œil. Utilisez le miroir pour vous aider. |
|
3 |
· Ne touchez pas l’œil, les paupières, les surfaces voisines ou d’autres surfaces avec le compte-gouttes. Cela peut infecter le collyre. · Appuyez légèrement sur le flacon pour libérer une goutte de médicament à la fois (figure 3). · Après avoir utilisé TRAVOPROST EG, gardez la paupière fermée, maintenez une légère pression en appuyant avec un doigt sur le coin de votre œil près du nez(figure 4) pendant 1 minute. Ceci permet d’empêcher TRAVOPROST EG d’aller dans le reste du corps. |
|
4 |
· Si vous devez traiter les deux yeux, recommencez ces étapes pour l’autre œil. · Refermez bien le flacon immédiatement après usage. · Utilisez un seul flacon à la fois. N’ouvrez pas le sachet tant que vous n’avez pas besoin du flacon. |
Si une goutte tombe à côté de l’œil, recommencez.
Si vous ou votre enfant utilisez d'autres préparations ophtalmiques telles que des collyres ou des pommades ophtalmiques, attendez au moins 5 minutes entre l'application de TRAVOPROST EG et les autres préparations.
Si vous ou votre enfant avez utilisé plus de TRAVOPROST EG 40 microgrammes/mL, collyre en solution que vous n’auriez dû :
Rincez l’œil avec de l’eau tiède pour éliminer tout le médicament. Ne mettez pas d’autres gouttes jusqu’à ce que le moment soit venu de mettre la goutte suivante.
Si vous oubliez d’utiliser TRAVOPROST EG 40 microgrammes/mL, collyre en solution :
Si vous arrêtez d’utiliser TRAVOPROST EG 40 microgrammes/mL, collyre en solution :
N’arrêtez pas d’utiliser TRAVOPROST EG sans en parler d’abord à votre médecin ou au médecin traitant de votre enfant, la pression de votre œil ou de l’œil de votre enfant ne serait pas contrôlée, ce qui pourrait provoquer une perte de la vue.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin, au médecin traitant votre enfant ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Vous pouvez normalement continuer à utiliser le collyre, sauf si les effets indésirables sont graves. Si vous vous inquiétez, contactez votre médecin ou votre pharmacien. N’interrompez pas l’administration de TRAVOPROST EG sans en parler à votre médecin.
Très fréquent (pouvant affecter plus de 1 personne sur 10)
Effets oculaires :
· rougeur de l’œil.
Fréquent (pouvant affecter jusqu’à 1 personne sur 10)
Effets oculaires :
· changement de la couleur de l’iris (partie colorée de l’œil) ;
· inconfort oculaire ;
· œil sec ;
· démangeaisons oculaires ;
· irritation oculaire ;
· douleur oculaire.
Peu fréquent (pouvant affecter jusqu’à 1 personne sur 100)
Effets oculaires :
· troubles de la cornée ;
· inflammation de l’œil ;
· inflammation de l’iris ;
· inflammation dans l’œil ;
· inflammation de la surface de l’œil avec ou sans lésion de surface ;
· sensibilité à la lumière ;
· écoulement de l’œil ;
· inflammation de la paupière ;
· rougeur de paupière ;
· gonflement autour de l’œil ;
· démangeaison de la paupière ;
· vision trouble ;
· augmentation de la production de larme ;
· infection ou inflammation de la conjonctive (conjonctivite) ;
· renversement externe anormal de la paupière inférieure ;
· opacification de l’œil ;
· croûte sur le bord de la paupière ;
· croissance des cils ;
Effets généraux :
· augmentation des symptômes allergiques ;
· mal de tête ;
· rythme cardiaque irrégulier ;
· toux;
· nez bouché ;
· irritation de la gorge ;
· assombrissement de la peau autour des yeux ;
· assombrissement de la peau ;
· texture de cheveux anormale ;
· croissance capillaire excessive.
Rare (pouvant affecter jusqu’à 1 personne sur 1000)
Effets oculaires :
· perception de flashs ;
· eczéma des paupières ;
· cils anormalement positionnés qui repoussent vers l'œil ;
· gonflement de l'œil ;
· vision réduite
· effet de halo ;
· sensation oculaire diminuée ;
· inflammation des glandes des paupières ;
· pigmentation dans l'œil ;
· augmentation de la taille de la pupille ;
· épaississement des cils.
· Changement de la couleur des cils
· Yeux fatigués
Effets généraux :
· infection oculaire virale ;
· vertiges
· mauvais goût ;
· rythme cardiaque diminué ou irrégulier ;
· tension artérielle diminuée ou augmentée ;
· essoufflement;
· asthme
· allergie ou inflammation nasale
· sècheresse nasale
· modifications de la voix ;
· inconfort gastro-intestinal ou ulcère ;
· constipation ;
· sécheresse buccale ;
· rougeur ou démangeaison de la peau ;
· éruption ;
· modification de la couleur des cheveux ;
· perte des cils ;
· douleurs articulaires
· douleurs musculo-squelettiques ;
· douleurs musculo-squelettiques ;
· fatigue généralisée.
Fréquence indéterminée
Effets oculaires :
· Inflammation de l’arrière de l’œil ;
· yeux apparaissent plus enfoncés.
Effets généraux :
· dépression ;
· anxiété ;
· insomnie
· sensation de faux mouvement ;
· bourdonnements d'oreilles ;
· douleur thoracique ;
· rythme cardiaque anormal
· augmentation du rythme cardiaque
· aggravation de l'asthme ;
· diarrhée ;
· saignements du nez
· douleurs abdominales ;
· nausées ;
· vomissements
· démangeaisons ;
· croissance capillaire anormale ;
· mictions involontaires ou douloureuses ;
· augmentation de l’antigène de la prostate.
Chez les enfants et les adolescents, les effets indésirables les plus fréquemment observés avec TRAVOPROST EG sont la rougeur de l'œil et la croissance des cils. Les deux effets indésirables ont été observés avec une incidence plus élevée chez les enfants et les adolescents que chez les adultes.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER TRAVOPROST EG 40 microgrammes/mL, collyre en solution ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur le flacon, le sachet et la boîte après « Exp ». La date d’expiration fait référence au dernier jour du mois.
Ne pas utiliser si vous remarquez que le système de fermeture inviolable a été cassé ou endommagé avant la première ouverture.
Avant ouverture, conserver le flacon dans son sachet d'emballage à l’abri de l'humidité.
Après ouverture, ce médicament ne nécessite pas de précautions particulières de conservation.
Vous devez jeter le flacon 4 semaines après l’avoir ouvert pour la première fois, pour prévenir les infections, et utiliser un nouveau flacon. Inscrivez la date à laquelle vous l’avez ouvert dans l’espace prévu à cet effet sur l’étiquette du flacon et sur la boîte.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient TRAVOPROST EG 40 microgrammes/mL, collyre en solution
· La substance active est : le travoprost.
Ce médicament contient 40 microgrammes/mL de travoprost.
· Les autres composants sont :
Chlorure de benzalkonium, hydroxystéarate de macrogolglycérol 40, trométamol, édétate disodique, acide borique, mannitol, hydroxyde de sodium pour l’ajustement du pH et eau pour préparations injectables.
Ce médicament se présente sous forme de solution incolore limpide fournie dans des boîtes contenant un ou plusieurs flacon(s) translucide(s) en polypropylène de 5 mL muni(s) d’un compte-gouttes transparent en polyéthylène basse densité (PEBD) et d’un bouchon à vis blanc inviolable en polyéthylène haute densité (PEHD), présenté(s) dans un sachet. Chaque flacon contient 2,5 mL de solution.
Boîtes de 1, 3, 6, 9, 10 ou 12 flacons.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
EG LABO - LABORATOIRES EUROGENERICS
CENTRAL PARK
15 RUE MAURICE MALLET
92130 ISSY LES MOULINEAUX
Exploitant de l’autorisation de mise sur le marché
EG LABO - LABORATOIRES EUROGENERICS
CENTRAL PARK
15 RUE MAURICE MALLET
92130 ISSY LES MOULINEAUX
6 DERVENAKION STR.
15351 PALLINI, ATTIKI
GRECE
OU
BALKANPHARMA-RAZGRAD AD
68 APRILSKO VASTANIE BLVD.
RAZGRAD, 7200
BULGARIE
OU
STADA ARZNEIMITTEL GMBH
MUTHGASSE 36/2
1190 VIENNE
AUTRICHE
OU
STADA ARZNEIMITTEL AG
STADASTRASSE 2-18
61118 BAD VILBEL
ALLEMAGNE
OU
CENTRAFARM SERVICES BV
VAN DE REIJSTRAAT 31-E
4814 NE BREDA
PAYS-BAS
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
[1] Indiquer le libellé détaillé qui figure dans l’application form avec le code de la modification selon les lignes directrices https://ec.europa.eu/health//sites/health/files/files/eudralex/vol-2/c_2013_2008/c_2013_2008_pdf/c_2013_2804_fr.pdf