Dernière mise à jour le 02/03/2026
PHARMATEX 18,9 mg, mini-ovule
Ce médicament n'est ou ne sera bientôt plus disponible sur le marché.
Si vous prenez actuellement ce médicament, il vous est recommandé d'en parler avec votre médecin
ou avec votre pharmacien qui pourra vous orienter vers un autre traitement.
Indications thérapeutiques
Classe pharmacothérapeutique : CONTRACEPTIF A USAGE LOCAL (G : système génito-urinaire) - code ATC : G02BB.
Ce médicament est un contraceptif local :
· il contient un spermicide (substance chimique qui détruit les spermatozoïdes) ;
· il diminue le risque de grossesse sans le supprimer totalement. L’efficacité dépend du respect du mode d’utilisation.
Quand utiliser PHARMATEX ?
Cette contraception locale s’adresse à toutes les femmes désirant une contraception et en particulier :
· Si vous ne pouvez pas utiliser une contraception hormonale (voir rubrique 6) ou un dispositif intra-utérin (DIU), aussi appelé stérilet.
· Si vous venez d’accoucher, si vous allaitez, si vous êtes en période de pré-ménopause.
· Si vous souhaitez une contraception épisodique.
· En complément de la contraception par un diaphragme, une cape cervicale ou un DIU (en particulier si vous prenez un traitement au long cours par certains médicaments, tels que les anti-inflammatoires non stéroïdiens).
· Si vous avez oublié de prendre un comprimé de votre contraception orale ou si vous l’avez pris en retard.
Dans ces cas, relisez la notice de votre contraceptif oral et associez les deux modes de contraception pendant le reste du cycle menstruel.
Présentations
> plaquette(s) PVC polyéthylène de 10 ovule(s)
Code CIP : 330 055-3 ou 34009 330 055 3 5
Déclaration d'arrêt de commercialisation : 31/12/2025
Cette présentation n'est pas agréée aux collectivités
> plaquette(s) PVC polyéthylène de 20 ovule(s)
Code CIP : 330 057-6 ou 34009 330 057 6 4
Déclaration d'arrêt de commercialisation : 31/12/2025
Cette présentation n'est pas agréée aux collectivités
Documents de bon usage du médicament
- Contraception chez la femme en post-partum
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Contraception d’urgence
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Contraception chez l’homme
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Stérilisation à visée contraceptive chez l’homme et chez la femme
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Contraception chez la femme adulte et de l'adolescente en âge de procréer (hors post-partum et post-IVG)
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Contraception chez la femme à risque cardio-vasculaire
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Contraception : prescriptions et conseils aux femmes
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Contraception hormonale orale : dispensation en officine
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Contraception d’urgence : dispensation en officine
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Contraception estroprogestative transdermique ou vaginale : dispensation en officine
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Contraception chez la femme après une interruption volontaire de grossesse (IVG)
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Méthodes contraceptives : Focus sur les méthodes les plus efficaces disponibles
Auteur : Haute autorité de santé
Type : Evaluation des technologies de santé
Date de mise à jour :Novembre 2017
Service médical rendu (SMR)
Pas de SMR disponible pour ce médicament ( plus d'informations dans l'aide )
Amélioration du service médical rendu (ASMR)
Pas d'ASMR disponible pour ce médicament (plus d'informations dans l'aide )
ANSM - Mis à jour le : 21/06/2024
PHARMATEX 18,9 mg, mini-ovule
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chlorure de benzalkonium................................................................................................... 18,9 mg
Sous forme de solution aqueuse de chlorure de benzalkonium à 50% m/v............................. 37,8 mg
Pour un mini-ovule.
Pour la liste complète des excipients, voir rubrique 6.1.
4.1. Indications thérapeutiques
Contraception locale : cette méthode diminue le risque de grossesse sans le supprimer totalement.
L’efficacité dépend du respect du mode d’utilisation.
Cette contraception locale s’adresse à toutes les femmes désirant une contraception et en particulier :
· lorsqu’il existe une contre-indication temporaire ou définitive à la contraception hormonale ou au dispositif intra-utérin (DIU) ;
· après un accouchement, lors de l’allaitement, au cours de la pré-ménopause ;
· lorsqu’est souhaitée une contraception épisodique ;
· comme adjuvant de la contraception locale par obturateur vaginal (diaphragme, cape cervicale) ou par DIU (en particulier en cas de traitement au long cours par certains médicaments, tels que les AINS) ;
· lorsqu’une méthode contraceptive complémentaire locale est recommandée dans les situations d’oubli ou de retard de prise de la contraception orale. Dans ce cas, associer les deux modes de contraception pendant le reste du cycle menstruel.
4.2. Posologie et mode d'administration
Utilisation systématique avant chaque rapport, quelle que soit la période du cycle.
Mode d’administration
Voie vaginale.
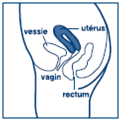
En position allongée, placer le mini-ovule au fond du vagin 5 minutes avant tout rapport sexuel.
En cas de rapports répétés, mettre en place un autre mini-ovule.
La durée de protection est de 4 heures.
Immédiatement après les rapports, seule une toilette externe, à l’eau pure est possible.
Conseils pratiques
Cette méthode contraceptive est compatible avec les diaphragmes et capes cervicales en silicone et les préservatifs masculins en latex et en polyisoprène (voir rubrique 4.5).
Ce médicament ne doit jamais être utilisé :
· en cas d’hypersensibilité au chlorure de benzalkonium ou à l’un des excipients listés dans la rubrique 6.1
· en cas d’utilisation de préservatifs masculins en polyuréthane.
4.4. Mises en garde spéciales et précautions d'emploi
L’efficacité contraceptive dépend essentiellement d’une utilisation correcte. En conséquence, il est important d’expliquer précisément le mode d’emploi à la patiente et de s’assurer de sa bonne compréhension.
Ce type de contraception sera évité chez toute personne ne pouvant ni la comprendre, ni l’accepter.
Si ce type de contraception est utilisé en cas d’oubli ou de retard à la prise d’une contraception orale, il est recommandé d’expliquer à nouveau à la patiente la nécessité de continuer sa contraception orale habituelle.
Il est nécessaire de respecter les conditions suivantes :
· placer systématiquement un mini-ovule au fond du vagin avant les rapports sexuels, quelle que soit la période du cycle ;
· ne pas utiliser de savon pour la toilette des organes génitaux 2 heures avant et 2 heures après le rapport sexuel, car l’eau savonneuse, même à l’état de traces, détruit le principe actif. Seule une toilette externe, à l’eau pure est possible pour les deux partenaires ;
· attendre 2 heures au moins si l'on veut faire une irrigation vaginale à l'eau pure, qui risque d'éliminer le produit ;
· éviter de prendre un bain, se baigner dans la mer, dans une piscine ou autre car l’action contraceptive peut être diminuée ;
· interrompre l’utilisation de PHARMATEX en cas de survenue ou d’aggravation d’une lésion génitale ;
· en cas de traitement par voie vaginale, attendre la fin de ce traitement pour utiliser PHARMATEX. Un autre mode de contraception sera alors conseillé.
Cette méthode de contraception ne protège pas contre les infections sexuellement transmissibles (IST) ni contre le Virus de l’Immunodéficience Humaine (VIH), responsable du SIDA (Syndrome d’ImmunoDéficience Acquise). Correctement utilisé lors des relations sexuelles, le préservatif (masculin ou féminin) est le seul moyen contraceptif qui protège également des IST et du VIH/SIDA
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Associations contre-indiquées
+ Préservatifs masculins en polyuréthane
Risque de rupture.
Associations déconseillées
+ Médicaments utilisés par voie vaginale
Tout traitement local vaginal est susceptible d’inactiver une contraception locale spermicide.
+ Savons
Ce spermicide est détruit par les savons : s’abstenir de tout lavage avec un savon car les savons, même à l’état de traces, détruisent le principe actif.
4.6. Fertilité, grossesse et allaitement
Grossesse
En clinique, les études épidémiologiques n’ont pas mis en évidence d’effet malformatif lié à l’utilisation fortuite de ce spermicide au début de la grossesse.
Possibilité de passage de très faibles quantités dans le lait maternel, sans conséquences néfastes connues. L’allaitement est possible.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Les effets indésirables rapportés depuis la mise sur le marché de PHARMATEX sont présentés ci-dessous selon la classe de système d’organes et par fréquence en utilisant les catégories suivantes : très fréquent (≥ 1/10), fréquent (≥ 1/100 à < 1/10), peu fréquent (≥ 1/1 000 à < 1/100), rare (≥ 1/10 000 à < 1/1 000), très rare (< 1/10 000), fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
Affection des organes de reproduction et du sein
Rare : démangeaisons, sensations de brûlures ou d’irritations locales chez l’un ou les deux partenaires.
Affections du système immunitaire
Fréquence indéterminée : possibilité d’allergie.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
Aucun cas de surdosage n’a été observé.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Le chlorure de benzalkonium est à la fois un spermicide et un antiseptique.
Le principe actif provoque la rupture de la membrane du spermatozoïde. La destruction du spermatozoïde s’effectue en deux temps : d’abord destruction du flagelle, puis éclatement de la tête.
L’efficacité de la méthode varie selon la rigueur de l’observation des recommandations et la précision du dialogue précédant la prescription. Il n’y a pas de modification de la flore saprophyte : le bacille de Döderlein est respecté.
N’étant pas de nature hormonale, PHARMATEX n’influence pas le cycle menstruel, la libido, la fertilité.
Selon des données expérimentales, le chlorure de benzalkonium possède aussi une activité antiseptique :
· in vitro, le produit est actif sur un certain nombre d’agents infectieux responsables de maladies sexuellement transmissibles notamment : Neisseria gonorrhoeae, Chlamydia spp., Herpes simplex type 2, VIH, Trichomonas vaginalis, Staphylococcus aureus. En revanche, l’activité est nulle sur Mycoplasma spp. et faible sur Gardnerella vaginalis, Candida albicans, Haemophilus ducreyi et Treponema pallidum ;
· in vivo, des éléments font état d’une possible activité dans la prévention de certaines maladies sexuellement transmissibles sans que l’on ait la preuve de cette action préventive.
5.2. Propriétés pharmacocinétiques
L’absorption du chlorure de benzalkonium par la muqueuse vaginale est très faible.
5.3. Données de sécurité préclinique
Lactose monohydraté, glycérides semi-synthétiques solides (witepsol S 51).
2 ans
6.4. Précautions particulières de conservation
A conserver à une température ne dépassant pas + 25°C.
6.5. Nature et contenu de l'emballage extérieur
Mini-ovule sous plaquette (PVC polyéthylène).
Boîtes de 5, 10 ou 20 mini-ovules.
6.6. Précautions particulières d’élimination et de manipulation
Pas d’exigences particulières.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
LABORATOIRE INNOTECH INTERNATIONAL
22 AVENUE ARISTIDE BRIAND
94110 ARCUEIL
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 330 054-7 4 : plaquette(s) PVC polyéthylène de 5 mini-ovules
· 34009 330 055-3 5 : plaquette(s) PVC polyéthylène de 10 mini-ovules
· 34009 330 057-6 4 : plaquette(s) PVC polyéthylène de 20 mini-ovules
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
Date de première autorisation : 6 avril 1988
Date de dernier renouvellement : 6 avril 2013
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Médicament non soumis à prescription médicale.
ANSM - Mis à jour le : 21/06/2024
Chlorure de benzalkonium
Vous devez toujours utiliser ce médicament en suivant scrupuleusement les informations fournies dans cette notice ou par votre médecin ou votre pharmacien.
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Adressez-vous à votre pharmacien pour tout conseil ou information.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que PHARMATEX 18,9 mg, mini-ovule et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser PHARMATEX 18,9 mg, mini-ovule ?
3. Comment utiliser PHARMATEX 18,9 mg, mini-ovule ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver PHARMATEX 18,9 mg, mini-ovule ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE PHARMATEX 18,9 mg, mini-ovule ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : CONTRACEPTIF A USAGE LOCAL (G : système génito-urinaire) - code ATC : G02BB.
Ce médicament est un contraceptif local :
· il contient un spermicide (substance chimique qui détruit les spermatozoïdes) ;
· il diminue le risque de grossesse sans le supprimer totalement. L’efficacité dépend du respect du mode d’utilisation.
Quand utiliser PHARMATEX ?
Cette contraception locale s’adresse à toutes les femmes désirant une contraception et en particulier :
· Si vous ne pouvez pas utiliser une contraception hormonale (voir rubrique 6) ou un dispositif intra-utérin (DIU), aussi appelé stérilet.
· Si vous venez d’accoucher, si vous allaitez, si vous êtes en période de pré-ménopause.
· Si vous souhaitez une contraception épisodique.
· En complément de la contraception par un diaphragme, une cape cervicale ou un DIU (en particulier si vous prenez un traitement au long cours par certains médicaments, tels que les anti-inflammatoires non stéroïdiens).
· Si vous avez oublié de prendre un comprimé de votre contraception orale ou si vous l’avez pris en retard.
Dans ces cas, relisez la notice de votre contraceptif oral et associez les deux modes de contraception pendant le reste du cycle menstruel.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER PHARMATEX 18,9 mg, mini-ovule ?
· Si vous êtes allergique à la substance active ou à l’un des autres composants contenus dans ce médicament. Vous trouverez la liste des composants à la rubrique 6.
· Si vous utilisez des préservatifs masculins en polyuréthane.
Avertissements et précautions
· Avant d’utiliser PHARMATEX, veillez à bien lire et comprendre son mode d’administration.
· Introduisez systématiquement PHARMATEX au fond du vagin avant chaque rapport sexuel, quelle que soit la période de votre cycle menstruel.
· L’eau savonneuse détruit le principe actif de ce contraceptif local. Par conséquent vous ne devez pas nettoyer vos parties génitales avec un savon 2 heures avant ou 2 heures après le rapport. Seule une toilette externe, à l’eau pure est possible pour les deux partenaires.
· Attendez 2 heures au moins si vous voulez faire une irrigation vaginale à l’eau pure.
· Evitez de prendre un bain, de vous baigner dans la mer ou dans une piscine. Cela pourrait diminuer l’efficacité de PHARMATEX.
· Si une lésion génitale survient ou s’aggrave, interrompez le traitement et consultez votre médecin.
· Si un traitement vaginal ou l’utilisation de tout autre produit par voie vaginale s’avérait nécessaire, attendez la fin du traitement pour (re)commencer la contraception avec PHARMATEX.
Attention : Ce mode de contraception ne protège pas contre les infections sexuellement transmissibles ni contre le SIDA. A ce jour, seul le préservatif permet une véritable protection.
Pourquoi est-il important que vous respectiez précisément le mode d’emploi ?
L’efficacité de cette méthode de contraception locale est inférieure à celle des autres modes de contraception tels que :
· la contraception hormonale : contraception orale, implant sous-cutané, patch contraceptif, DIU à libération hormonale, anneau vaginal,
· le DIU au cuivre,
· le diaphragme, la cape cervicale,
· le préservatif.
Par conséquent, il est très important que votre médecin ou votre pharmacien vous explique précisément le mode d’emploi.
Si vous n’avez pas compris comment ce médicament doit être utilisé, n’hésitez pas à demander à nouveau à votre pharmacien ou à votre médecin.
Pour obtenir la contraception la plus efficace possible, il est important de respecter le mode d’emploi.
Utilisez un mini-ovule systématiquement avant chaque rapport sexuel, et quel que soit le moment de votre cycle menstruel, y compris pendant les règles.
Autres médicaments et PHARMATEX 18,9 mg, mini-ovule
· Il est généralement déconseillé d’utiliser PHARMATEX en même temps que des médicaments utilisés par voie vaginale et des savons. En effet, ils peuvent faire perdre à PHARMATEX son efficacité contraceptive.
· Si votre médecin vous a prescrit un traitement vaginal, attendez la fin du traitement pour utiliser PHARMATEX.
Si vous souhaitez utiliser un préservatif avec PHARMATEX 18,9 mg, mini-ovule, veillez à vérifier au préalable la composition de votre préservatif et vous reporter aux Conseils pratiques en rubrique 3 avant utilisation.
Informez votre médecin ou pharmacien si vous utilisez, avez récemment utilisé ou pourriez utiliser tout autre médicament.
PHARMATEX avec des aliments et boissons
Sans objet.
Grossesse
L’utilisation de PHARMATEX au début d’une grossesse méconnue n’expose pas à un risque particulier pour le fœtus.
Allaitement
L’allaitement maternel est possible.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
Conduite de véhicules et utilisation de machines
Sans objet.
PHARMATEX contient
Sans objet.
3. COMMENT UTILISER PHARMATEX 18,9 mg, mini-ovule ?
· Introduisez un mini-ovule systématiquement avant chaque rapport sexuel, quel que soit le moment de votre cycle menstruel, y compris pendant les règles.
· En cas de rapports répétés, utilisez un nouveau mini-ovule avant chaque nouveau rapport.
Mode et voie d’administration
Ce médicament s’utilise par voie vaginale. Vous ne devez pas l’avaler.
Il est nécessaire de respecter les conditions d’utilisation suivantes car l’efficacité dépend du respect du mode d’utilisation :
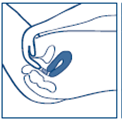
· Introduisez systématiquement un mini-ovule au fond du vagin 5 minutes avant chaque rapport sexuel, quelle que soit la période de votre cycle menstruel, y compris pendant les règles.
· Introduisez le mini-ovule de préférence en position couchée, ce qui facilite sa mise en place au fond du vagin.
· Placez un autre mini-ovule avant chaque rapport sexuel en cas de rapports répétés.
· La durée de protection est de 4 heures.
· Immédiatement avant ou après les rapports, seule une toilette externe, à l’eau pure est possible pour les deux partenaires. Ne nettoyez pas vos parties intimes avec un savon.
|
|
|
Conseils pratiques
Cette méthode contraceptive est compatible avec :
· les diaphragmes en silicone
· les capes cervicales en silicone
· les préservatifs masculins en latex et en polyisoprène.
Cette contraception est contre-indiquée avec les préservatifs masculins en polyuréthane.
Si vous avez utilisé plus de PHARMATEX que vous n’auriez dû
Consultez immédiatement votre médecin ou votre pharmacien
Si vous oubliez d’utiliser PHARMATEX
Si vous arrêtez d’utiliser PHARMATEX
Sans objet.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Effets indésirables rares (affectent 1 à 10 patients sur 10 000)
· démangeaisons, sensations de brûlures ou d’irritations locales chez l’un ou les deux partenaires.
Effets indésirables de fréquence indéterminée (ne peut être estimée sur la base des données disponibles)
· allergie à l’un des composants du médicament.
Vous reconnaitrez les signes d’une allergie par des rougeurs, des démangeaisons, et très rarement par un brusque gonflement du cou et du visage provoquant des difficultés à respirer. Si ces signes surviennent consultez immédiatement un médecin.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: https://signalement.social-sante.gouv.fr/.
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER PHARMATEX 18,9 mg, mini-ovule ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur la boîte. La date de péremption fait référence au dernier jour de ce mois.
A conserver à une température ne dépassant pas +25°C.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient PHARMATEX 18,9 mg, mini-ovule
· La substance active est :
Chlorure de benzalkonium.............................................................................................. 18,9 mg
Par mini-ovule
· Les autres composants sont :
Le lactose monohydraté et les glycérides semi synthétiques solides (type Witepsol S51).
Qu’est-ce que PHARMATEX 18,9 mg, mini-ovule et contenu de l’emballage extérieur
Ce médicament se présente sous forme d’un mini-ovule.
Chaque boîte contient 5, 10 ou 20 mini-ovules.
Titulaire de l’autorisation de mise sur le marché
LABORATOIRE INNOTECH INTERNATIONAL
22 AVENUE ARISTIDE BRIAND
94110 ARCUEIL
Exploitant de l’autorisation de mise sur le marché
LABORATOIRE INNOTECH INTERNATIONAL
22 AVENUE ARISTIDE BRIAND
94110 ARCUEIL
RUE RENE CHANTEREAU, CHOUZY-SUR-CISSE
41150 VALLOIRE-SUR-CISSE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
NOTIONS SUR LE CYCLE MENSTRUEL ET LA CONTRACEPTION
Qu’est-ce que le cycle menstruel ?
· Le cycle menstruel est la période entre le premier jour des règles et le début des règles suivantes.
· Habituellement le cycle dure 28 jours, cependant il peut varier de façon importante d’une femme à l’autre.
· Les règles surviennent quand une femme n’est pas enceinte.
Qu’est-ce que l’ovulation et quand a-t-elle lieu ?
· L’ovulation est le moment où l’ovaire expulse un ovule qui est recueilli par la trompe utérine.
· En général, l’ovulation se produit au milieu du cycle mais elle peut se produire à n’importe quel moment du cycle, même pendant les règles.
Quand commence la grossesse ?
· Si des spermatozoïdes se trouvent à proximité de l’ovule dans la trompe utérine, la « fécondation » (c’est-à-dire la rencontre de l’ovule et d’un spermatozoïde pour créer un embryon) peut avoir lieu.
· Au bout de quelques jours, l’ovule fécondé va se fixer (ou « s’implanter ») dans l’utérus, et la grossesse commence.
Quelles sont les principales méthodes de contraception ?
· La contraception hormonale : contraception orale, implant sous-cutané, patch contraceptif, dispositif intra-utérin (DIU) à libération hormonale, anneau vaginal.
· Le DIU au cuivre.
· La contraception locale : spermicides, préservatifs, diaphragmes, capes cervicales.
· La stérilisation féminine.
Quels sont les moyens pour lutter contre les infections sexuellement transmissibles (IST) y compris l’infection à VIH et le SIDA ?
Correctement utilisé lors des relations sexuelles, le préservatif (masculin ou féminin) est le seul moyen contraceptif qui protège également des IST et du Virus de l’Immunodéficience Humaine (VIH), responsable du SIDA (Syndrome d’ImmunoDéficience Acquise).
Les autres méthodes de contraception ne protègent pas contre ces infections sexuellement transmissibles ni contre le SIDA.
Que dois-je faire si j’ai eu un rapport sexuel non protégé ou si j’ai oublié d’utiliser ma méthode de contraception habituelle ?
Si vous êtes dans cette situation, demandez rapidement conseil à votre médecin ou à votre pharmacien.
· Vous pouvez utiliser la contraception d’urgence (également appelée pilule du lendemain). Elle doit être utilisée le plus rapidement possible.
· Ce type de contraception vise à empêcher la grossesse en bloquant ou en retardant l’ovulation.
Que faire si votre situation change ou si ce mode de contraception ne vous convient pas ou ne vous convient plus ?
Consultez votre médecin afin qu’il vous prescrive une autre méthode de contraception mieux adaptée à votre cas.