Dernière mise à jour le 02/03/2026
DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique
Indications thérapeutiques
Classe pharmacothérapeutique : ESTROGENES - code ATC : G03CA03.
DERMESTRIL est un traitement hormonal substitutif (THS). Il contient du 17-β estradiol. DERMESTRIL est utilisé chez les femmes ménopausées dont les dernières règles datent d’au moins 6 mois.
DERMESTRIL est utilisé pour :
Soulager les symptômes apparaissant après la ménopause.
Lors de la ménopause, la quantité d’estrogènes produits par l’organisme féminin chute. Chez certaines femmes, cette chute se traduit par des symptômes tels qu’une sensation de chaleur au niveau du visage, du cou et de la poitrine (les « bouffées de chaleur »). DERMESTRIL soulage ces symptômes après la ménopause.
DERMESTRIL vous sera prescrit uniquement si vos symptômes altèrent gravement votre vie quotidienne.
Présentations
> 8 sachet(s) aluminium P-A-M-éthylène (SURLYN) de 1 dispositif(s)
Code CIP : 340 904-3 ou 34009 340 904 3 1
Déclaration de commercialisation : 19/03/1997
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 5,87 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 6,89 €
- Taux de remboursement :65%
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 24/09/2025 | Réévaluation suite saisine Ministères (CT) | Le service médical rendu par DERMESTRIL 25 µg/24h, 50 µg/24h, 100 µg/24h (estradiol) et DERMESTRIL SEPTEM 25 µg/24h, 50 µg/24h, 75 µg/24h (estradiol) reste important dans le traitement hormonal substitutif (THS) des symptômes de déficit en estrogènes chez les femmes ménopausées |
| Important | Avis du 17/06/2015 | Renouvellement d'inscription (CT) | Le service médical rendu par les spécialités DERMESTRIL 25, 50, 100 microgrammes/24 heures et DERMESTRIL SEPTEM 25, 50, 75 microgrammes/24 heures dans le traitement hormonal substitutif (THS) des symptômes de déficit en estrogènes chez les femmes ménopausées reste important chez les patientes dont les troubles du climatère sont ressentis comme suffisamment gênant pour altérer leur qualité de vie, lorsque ces spécialités sont utilisées selon les préconisations de la Commission. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| IV (Mineur) | Avis du 24/09/2025 | Réévaluation suite saisine Ministères (CT) | DERMESTRIL (estradiol) et DERMESTRIL SEPTEM (estradiol) apportent une amélioration du service médical rendu mineure (ASMR IV) par rapport aux formes orales. |
ANSM - Mis à jour le : 11/07/2025
DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Estradiol............................................................................................................................. 4,00 mg
Pour un dispositif transdermique de 18 cm².
Pour la liste complète des excipients, voir rubrique 6.1.
4.1. Indications thérapeutiques
L'expérience de ce traitement chez les femmes âgées de plus de 65 ans est limitée.
4.2. Posologie et mode d'administration
Appliquer le dispositif transdermique 2 fois par semaine, c'est-à-dire renouveler le dispositif transdermique tous les 3 ou 4 jours.
Trois dosages de DERMESTRIL sont disponibles : DERMESTRIL 25, 50 et 100 microgrammes/24 heures, dispositif transdermique.
Pour débuter ou poursuivre un traitement dans l'indication des symptômes post-ménopausiques, la dose minimale efficace doit être utilisée pendant la plus courte durée possible (voir rubrique 4.4).
Ainsi, la posologie usuelle recommandée pour débuter le traitement est de un dispositif de DERMESTRIL 25 microgrammes/24 heures deux fois par semaine.
En fonction de l'évolution clinique, la posologie doit être adaptée aux besoins individuels :
· si la dose choisie n'a pas corrigé les signes et symptômes de déficit estrogénique, un dosage plus fort doit être administré.
· l’apparition d'une sensation de tension des seins, de métrorragies, de rétention d’eau ou ballonnements (persistant pendant plus de 6 semaines) ou d'une irritabilité indique en général que la dose est trop élevée et doit être modifiée.
DERMESTRIL 50 microgrammes/24 heures peut être utilisé selon le schéma thérapeutique :
· Cyclique (discontinu), pendant 24 à 28 jours, suivis d'un intervalle libre de 2 à 7 jours. Durant cet intervalle, des hémorragies de privation peuvent apparaître.
· Continu, sans aucune période d'arrêt du traitement.
Un traitement continu, non cyclique, peut être indiqué dans le cas où les symptômes de déficit estrogénique se manifestent à nouveau fortement au cours de l'intervalle libre.
S'il s'agit d'une prescription chez une femme ne prenant pas de THS ou d'un relais d'un THS combiné continu, le traitement peut être commencé n'importe quel jour.
Par contre, si le traitement préalable est un THS séquentiel, le cycle de traitement en cours doit être terminé avant de commencer un traitement par DERMESTRIL 50 microgrammes/24 heures.
Chez les femmes non hystérectomisées, un progestatif doit être ajouté au moins 12 jours par cycle pour s'opposer au développement d'une hyperplasie endométriale induite par l'estrogène. Le traitement séquentiel par des progestatifs doit se faire selon le schéma suivant :
· Si DERMESTRIL 50 microgrammes/24 heures est administré de façon cyclique (discontinue), le progestatif sera administré durant au moins les 12 derniers jours du traitement par l'estradiol. Ainsi, il n'y aura aucune administration hormonale pendant l'intervalle libre de chaque cycle.
· Si DERMESTRIL 50 microgrammes/24 heures est administré de façon continue, il est recommandé de prendre le progestatif pendant au moins 12 jours par mois (continu séquentiel).
Dans les deux cas, des saignements peuvent apparaître après l'arrêt du traitement par le progestatif.
Chez les femmes hystérectomisées, il n'est pas recommandé d'associer un progestatif sauf en cas d'antécédent d'endométriose.
Mode d’administration
Une fois le feuillet de protection détaché, le dispositif transdermique doit immédiatement être appliqué sur une peau propre, sèche, saine (non irritée, ni lésée), et dépourvue de crème, lait ou produit huileux. Choisir un emplacement sur l'abdomen, les fesses ou dans la région lombaire à un endroit ne présentant pas de plis importants et qui ne soit pas le siège de frottements vestimentaires.
L'estradiol étant dégradé par les rayons ultraviolets, le dispositif transdermique ne doit pas être exposé directement au soleil.
Le dispositif transdermique ne doit pas être appliqué sur les seins. Il ne doit pas non plus être appliqué 2 fois de suite au même endroit.
Il est possible de se doucher ou de prendre un bain tout en gardant le dispositif transdermique.
Dans le cas d'un décollement du dispositif transdermique (eau très chaude, hypersudation, frottement anormal de vêtements), il est recommandé de le replacer sur la peau sèche. Si cela n'est pas possible, utilisez un dispositif transdermique neuf qui sera retiré à la date initialement prévue. Reprendre ensuite le rythme de changement du dispositif transdermique conformément au schéma thérapeutique initial.
En cas d’oubli de remplacement de DERMESTRIL 50 microgrammes/24 heures, un nouveau dispositif transdermique doit être appliqué dès que possible. Reprendre ensuite le rythme de changement du dispositif transdermique conformément au schéma thérapeutique initial. L'oubli de l'application d'un patch peut favoriser la récurrence des symptômes et la survenue de saignements et de spottings.
· Cancer du sein connu ou suspecté ou antécédent de cancer du sein ;
· Tumeurs malignes estrogéno-dépendantes connues ou suspectées (exemple : cancer de l'endomètre) ;
· Hémorragie génitale non diagnostiquée ;
· Hyperplasie endométriale non traitée ;
· Antécédent d'accident thrombo-embolique veineux ou accident thrombo-embolique veineux en évolution (thrombose veineuse profonde, embolie pulmonaire) ;
· Troubles thrombophiliques connus (exemple : déficit en protéine C, en protéine S ou en antithrombine) (voir rubrique 4.4) ;
· Accident thrombo-embolique artériel récent ou en évolution (exemple : angor, infarctus du myocarde) ;
· Affection hépatique aiguë ou antécédents d'affection hépatique, jusqu'à normalisation des tests hépatiques ;
· Porphyrie.
4.4. Mises en garde spéciales et précautions d'emploi
Les preuves de l’existence de risques associés à un THS dans le traitement des femmes ménopausées prématurément sont limitées. En raison du faible niveau du risque absolu chez les femmes plus jeunes, le rapport bénéfice / risque pourrait cependant être plus favorable que chez les femmes plus âgées.
Examen clinique et surveillance
Avant de débuter ou de recommencer un traitement hormonal substitutif (THS), il est indispensable d'effectuer un examen clinique et gynécologique complet (y compris le recueil des antécédents médicaux personnels et familiaux), en tenant compte des contre-indications et des précautions particulières d'emploi. Pendant toute la durée du traitement, des examens réguliers seront effectués, leur nature et leur fréquence étant adaptées à chaque patiente.
Les femmes doivent être informées du type d'anomalies mammaires pouvant survenir sous traitement ; ces anomalies doivent être signalées au médecin traitant (voir paragraphe « cancer du sein » ci-dessous). Les examens, y compris des examens appropriés par imagerie tels qu’une mammographie, doivent être pratiqués selon les recommandations en vigueur, et adaptés à chaque patiente.
Les femmes doivent être informées que DERMESTRIL 50 microgrammes/24h n’est pas un contraceptif et ne restaure pas la fertilité.
Conditions nécessitant une surveillance
Si l'une des affections suivantes survient, est survenue précédemment, et/ou s'est aggravée au cours d'une grossesse ou d'un précédent traitement hormonal, la patiente devra être étroitement surveillée et le rapport bénéfice/risque du THS réévalué individuellement. Les affections suivantes peuvent réapparaître ou s'aggraver au cours du traitement par DERMESTRIL 50 microgrammes/24 heures, en particulier :
· léiomyome (fibrome utérin) ou endométriose ;
· présence de facteurs de risque thrombo-emboliques (voir ci-dessous) ;
· facteurs de risque de tumeurs estrogéno-dépendantes, par exemple: 1er degré d'hérédité pour le cancer du sein ;
· hypertension artérielle ;
· troubles hépatiques (par exemple: adénome hépatique) ;
· diabète avec ou sans atteinte vasculaire ;
· lithiase biliaire ;
· migraines ou céphalées sévères ;
· lupus érythémateux disséminé ;
· antécédent d'hyperplasie endométriale (voir ci-dessous) ;
· épilepsie ;
· asthme ;
· otospongiose.
Allergie de contact
Comme avec toute formulation locale, bien que cela soit extrêmement rare, une sensibilisation de contact peut survenir. Les femmes qui présentent une sensibilisation de contact à l'un des composants du patch doivent être averties qu'une réaction sévère d'hypersensibilité peut survenir si l'exposition au produit responsable est maintenue.
Arrêt immédiat du traitement
Le traitement doit être arrêté immédiatement en cas de survenue d'une contre-indication ou dans les cas suivants :
· ictère ou altération de la fonction hépatique ;
· augmentation significative de la pression artérielle ;
· céphalée de type migraine inhabituelle ;
· grossesse.
Hyperplasie endométriale et carcinome
Chez les femmes ayant un utérus intact, le risque d'hyperplasie endométriale et de cancer de l'endomètre augmente en cas d'administration prolongée d'estrogènes seuls. Le risque de cancer de l’endomètre est de 2 à 12 fois supérieur comparé aux femmes ne prenant pas d’estrogènes, selon la durée du traitement et la dose d’estrogènes utilisée (voir rubrique 4.8).
Après arrêt du traitement, le risque peut rester élevé pendant au moins 10 ans.
Chez les femmes non hystérectomisées, l'association d'un progestatif de façon cyclique pendant au moins 12 jours par mois / cycle de 28 jours ou la prise d'un traitement estro-progestatif combiné continu empêche l'augmentation du risque associée aux estrogènes seuls comme THS.
Des métrorragies et des « spottings » peuvent survenir au cours des premiers mois de traitement. La survenue de saignements irréguliers plusieurs mois après le début du traitement ou la persistance de saignements après l'arrêt du traitement doivent faire rechercher une pathologie sous-jacente. Cette démarche peut nécessiter une biopsie endométriale afin d'éliminer une pathologie maligne.
La stimulation par les estrogènes peut conduire à une transformation maligne ou prémaligne des foyers résiduels d'endométriose. L'association d'un progestatif à l'estrogène doit être envisagée en cas de foyers résiduels d'endométriose chez les femmes qui ont subi une hystérectomie suite à une endométriose.
Cancer du sein
L’ensemble des données disponibles montre un risque accru de cancer du sein chez les femmes prenant un traitement estro-progestatif, ou chez celles prenant un THS à base d’estrogènes seuls, ce risque étant dépendant de la durée du traitement.
Traitement estro-progestatif combiné
· L’essai randomisé contrôlé versus placebo Women's Health Initiative study (WHI) et une méta-analyse des études épidémiologiques prospectives montrent tous deux une augmentation du risque de survenue de cancer du sein chez les femmes traitées par un THS estro-progestatif combiné, apparaissant au bout d’environ 3 (1-4) ans de traitement (voir rubrique 4.8).
Traitement par estrogènes seuls
· L’étude WHI n’a pas montré d’augmentation du risque de survenue du cancer du sein chez les femmes hystérectomisées utilisant des estrogènes seuls comme THS. Les études observationnelles ont généralement rapporté une légère augmentation du risque de cancer du sein diagnostiqué, ce risque étant plus faible que chez les utilisatrices d’association estrogènes-progestatifs (voir rubrique 4.8).
Les résultats d’une importante méta-analyse ont montré qu’après avoir arrêté le traitement, le risque additionnel diminue dans le temps et la durée nécessaire pour qu’il revienne à la normale dépend de la durée de la prise du THS. Lorsqu’un THS a été suivi pendant plus de 5 ans, le risque peut perdurer 10 ans ou plus.
Les THS, particulièrement les traitements combinés estrogène/progestatif, augmentent la densité mammaire à la mammographie, ce qui pourrait gêner le diagnostic de cancer du sein.
Accidents thrombo-emboliques veineux
Le THS est associé à un risque 1,3 à 3 fois plus élevé d'accidents thrombo-emboliques veineux (thrombose veineuse profonde ou embolie pulmonaire). Cet événement survient plutôt au cours de la première année de traitement (voir rubrique 4.8).
Les patientes présentant une thrombophilie connue ont un risque accru d'accident thrombo-embolique veineux. Le THS pourrait majorer ce risque. Chez ces patientes, l'utilisation d'un THS est contre-indiquée (voir rubrique 4.3).
Les facteurs de risque reconnus d'accidents thrombo-emboliques veineux sont : utilisation d’estrogènes, âge, chirurgie importante, immobilisation prolongée, obésité (IMC > 30 kg/m2), grossesse / postpartum, lupus érythémateux disséminé (LED), cancer. En revanche, il n'existe aucun consensus sur le rôle possible des varices dans les accidents thrombo-emboliques veineux.
Afin de prévenir tout risque thrombo-embolique veineux post-opératoire, les mesures prophylactiques habituelles doivent être strictement appliquées. En cas d'immobilisation prolongée suite à une intervention chirurgicale programmée, une interruption provisoire du traitement 4 à 6 semaines avant l'intervention est recommandée. Le traitement ne sera réinstauré que lorsque la patiente aura repris une mobilité normale.
Chez les femmes sans antécédents de thrombose veineuse mais avec un membre de la famille proche ayant des antécédents de thrombose à un jeune âge, des examens peuvent être proposés, tout en informant de leurs limites (seuls certains types de troubles thrombophiliques sont identifiés lors de ces examens).
Si un trouble thrombophilique lié à des thromboses chez des membres de la famille est identifié ou si le trouble est sévère (par exemple déficit en antithrombine, en protéine S ou protéine C, ou combinaison de troubles), le THS est contre-indiqué.
Chez les femmes suivant déjà un traitement à long terme par anticoagulants, le rapport bénéfice/risque d'un THS doit être évalué avec précaution.
La survenue d'un accident thrombo-embolique impose l'arrêt du THS. Les patientes devront être informées de la nécessité de contacter immédiatement leur médecin en cas de survenue de signes évoquant une thrombose tels que gonflement douloureux d'une jambe, douleurs soudaines dans la poitrine ou dyspnée.
Maladie coronarienne
Les études randomisées contrôlées n'ont pas mis en évidence de protection contre l’infarctus du myocarde chez les femmes avec ou sans maladie coronarienne préexistante traitées par une association d’estro-progestatifs ou par des estrogènes seuls.
Traitement par une association estro-progestative
Le risque relatif de maladie coronarienne est légèrement augmenté lors d’un traitement par une association estro-progestative. Puisque le risque absolu de base de maladie coronarienne dépend fortement de l’âge, le nombre de cas supplémentaire de maladie coronarienne due à l’association estroprogestative est très faible chez les femmes en bonne santé proches de la ménopause, mais augmente avec l’âge.
Traitement par des estrogènes seuls
Les études randomisées contrôlées n’ont pas mis en évidence d’augmentation du risque de maladie coronarienne chez les femmes hystérectomisées utilisant les estrogènes seuls.
Accidents vasculaires cérébraux
Une augmentation jusqu’à 1,5 fois du risque d'accident vasculaire cérébral ischémique a été montré chez les femmes traitées par une association d’estro-progestatifs ou des estrogènes seuls. Le risque relatif ne change pas avec l’âge ou le temps après la ménopause. Cependant, comme le risque absolu de base d’accident vasculaire cérébral est fortement dépendant de l’âge, le risque global de survenue d’un accident vasculaire cérébral chez la femme utilisant un THS augmentera avec l’âge (voir rubrique 4.8).
Cancer des ovaires
Le cancer ovarien est beaucoup plus rare que le cancer du sein.
Les données épidémiologiques provenant d'une importante méta-analyse suggèrent une légère augmentation du risque chez les femmes prenant un THS par œstrogènes seuls ou par une combinaison d'œstrogènes et de progestatifs, qui apparaît dans les cinq ans suivant le début de l'utilisation du produit et diminue progressivement après l'arrêt du traitement.
D'autres études, y compris l'essai WHI (Women's Health Initiative), suggèrent qu'un risque similaire ou légèrement inférieur peut être associé avec une utilisation de THS combinés (voir rubrique 4.8).
Autres précautions d'emploi
· Les estrogènes pouvant provoquer une rétention hydrique, les patientes présentant une insuffisance rénale ou cardiaque doivent être étroitement surveillées.
· Les femmes avec une hypertriglycéridémie préexistante doivent être surveillées pendant le traitement hormonal substitutif. De rares cas d'augmentation importante du taux des triglycérides conduisant à une pancréatite ont été observés sous estrogénothérapie.
· La fonction thyroïdienne doit être surveillée chez les patientes recevant un traitement substitutif par hormones thyroïdiennes lors d’un traitement par estrogènes (voir rubrique 4.5).
Au cours du traitement par les estrogènes, une augmentation des taux plasmatiques de la TBG (thyroid binding globulin) est observée, elle conduit à une élévation des taux plasmatiques des hormones thyroïdiennes totales mesurés par PBI (protein-bound iodine), de la T4 totale (mesuré sur colonne ou par RIA (radioimmunoassay)) et de la T3 totale (mesuré par RIA). La fixation de la T3 sur la résine est diminuée, reflétant l'augmentation de la TBG. Les concentrations des fractions libres de T4 et de T3 restent inchangées.
· Les taux sériques d'autres protéines de liaison telles que la CBG (corticoid binding globulin) et la SHBG (sex-hormone binding globulin) peuvent être augmentés entraînant, respectivement, une augmentation des taux circulants de corticoïdes et de stéroïdes sexuels. Les concentrations des fractions libres ou actives des hormones restent inchangées.
· D'autres protéines plasmatiques peuvent également être augmentées (angiotensinogène/substrat de la rénine, alpha -1-antitrypsine, céruloplasmine).
· L’utilisation de THS n’améliore pas les fonctions cognitives. Il existe une augmentation du risque de probable démence chez les femmes débutant un traitement combiné continu ou par estrogènes seuls après 65 ans.
Au cours des essais cliniques sur le traitement de l’infection par le virus de l’hépatite C (VHC) par l’association ombitasvir/paritaprévir/ritonavir et dasabuvir avec et sans ribavirine, les élévations du taux d’ALAT au-delà de 5 fois la limite supérieure de la normale (LSN) étaient significativement plus fréquentes chez les femmes utilisant des médicaments contenant de l’éthinylestradiol, tels que des CHC. Des élévations du taux d’ALAT ont également été observées chez les patientes traitées par glécaprévir/pibrentasvir ou sofosbuvir/velpatasvir/voxilaprevir, utilisant des médicaments contenant de l’éthinylestradiol, tels que des CHC.
Chez les femmes utilisant des médicaments contenant des estrogènes autres que l’éthinylestradiol, comme l’estradiol et ombitasvir/paritaprevir/ritonavir et dasabuvir avec et sans ribavirine, la fréquence des élévations du taux d’ALAT était similaire à celle observée chez les femmes n’utilisant aucun estrogène ; cependant, étant donné le nombre limité de femmes prenant ces autres estrogènes, il convient d’être prudent en cas de co-administration avec les associations médicamenteuses suivantes : ombitasvir/paritaprévir/ritonavir et dasabuvir avec ou sans ribavirine ; glécaprévir/pibrentasvir ou sofosbuvir/ velpatasvir/voxilaprevir. Voir rubrique 4.5.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Associations faisant l'objet de précautions d’emploi
Le métabolisme des estrogènes et des progestatifs peut être augmenté par l'utilisation concomitante de médicaments inducteurs enzymatiques, en particulier des iso-enzymes du cytochrome P450, comme les anticonvulsivants (phénobarbital, phénytoïne, carbamazépine, oxcarbazépine) et les anti-infectieux (rifampicine, rifabutine, névirapine, éfavirenz).
Le ritonavir et le nelfinavir, bien que connus comme de puissants inhibiteurs enzymatiques, ont paradoxalement des propriétés inductrices quand ils sont utilisés avec des hormones stéroïdiennes.
Les préparations à base de plante contenant du millepertuis (Hypericum perforatum) pourraient modifier le métabolisme des estrogènes et des progestatifs.
L'administration transcutanée évite l’effet de premier passage hépatique, par conséquent le métabolisme des estrogènes administrés par cette voie peut être moins affecté par les inducteurs enzymatiques que par voie orale.
L'augmentation du métabolisme des estrogènes et des progestatifs peut conduire à une diminution de l'effet thérapeutique et à une modification du profil des saignements utérins.
Une surveillance clinique et une adaptation éventuelle de la posologie du THS sont recommandées pendant le traitement par inducteur enzymatique et après son arrêt.
La prise d’estrogènes peut modifier les résultats de certains examens biologiques tels que : les tests fonctionnels hépatiques, thyroïdiens, surrénaliens et rénaux, le taux plasmatique des protéines (porteuses) comme la corticosteroid-binding globulin (CBG) et des fractions lipidiques/lipoprotéiniques, les paramètres du métabolisme glucidique, les paramètres de la coagulation et de la fibrinolyse. Les modifications restent en général dans les limites de la normale.
Effet des THS œstrogéniques sur d'autres médicaments
Il a été démontré que les contraceptifs hormonaux contenant des œstrogènes diminuent significativement les concentrations plasmatiques de lamotrigine en cas d'administration concomitante, en raison de l'induction de la glucuronidation de la lamotrigine. Cela peut réduire le contrôle des crises. Bien que l'interaction potentielle entre le traitement hormonal substitutif et la lamotrigine n'ait pas été étudiée, on s'attend à ce qu'une interaction similaire existe, ce qui pourrait conduire à une réduction du contrôle des crises chez les femmes prenant les deux médicaments en même temps.
Interactions pharmacodynamiques
Agents antiviraux à action directe (AAD) et médicaments contenant de l'éthinylestradiol, tels que les CHC.
Au cours des essais cliniques sur le traitement de l’infection par le VHC par l’association médicamenteuse ombitasvir/paritaprévir/ritonavir et dasabuvir avec ou sans ribavirine, les élévations du taux d’ALAT au-delà de 5 fois la limite supérieure de la normale (LSN) étaient significativement plus fréquentes chez les femmes utilisant des médicaments contenant de l’éthinylestradiol, tels que des CHC. En outre, même chez les patients traités par glécaprevir/pibrentasvir ou sofosbuvir/velpatasvir/ voxilaprevir, des élévations du taux d'ALAT ont été observées chez les femmes utilisant des médicaments contenant de l'éthinylestradiol, tels que les CHC.
Agents antiviraux à action directe (AAD) et médicaments contenant des œstrogènes autres que l'éthinylestradiol, tels que l'estradiol.
Chez les femmes utilisant des médicaments contenant des estrogènes autres que l’éthinylestradiol, comme l’estradiol et ombitasvir/paritaprevir/ritonavir et dasabuvir avec ou sans ribavirine, la fréquence des élévations du taux d’ALAT était similaire à celle observée chez les femmes n’utilisant aucun estrogène ; cependant, étant donné le nombre limité de femmes prenant ces autres estrogènes, il convient d’être prudent en cas de co-administration avec les associations médicamenteuses suivantes : ombitasvir/paritaprévir/ritonavir et dasabuvir avec ou sans ribavirine glécaprévir/pibrentasvir ou sofosbuvir/velpatasvir/voxilaprevir (voir rubrique 4.4).
4.6. Fertilité, grossesse et allaitement
Grossesse
DERMESTRIL n'a pas d'indication au cours de la grossesse.
La découverte d'une grossesse au cours du traitement par DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique, impose l'arrêt immédiat du traitement.
A ce jour, la plupart des études épidémiologiques n'ont pas mis en évidence d'effet tératogène ou fœtotoxique chez les femmes enceintes exposées par mégarde à des doses thérapeutiques d'estrogènes.
Ce médicament n'a pas d'indication au cours de l'allaitement.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
DERMESTRIL n’a aucun effet connu sur l’aptitude à conduire des véhicules ou à utiliser des machines.
Plus de 700 patientes ont été traitées par DERMESTRIL pendant les essais cliniques.
Au cours des essais cliniques, environ 10 à 17 % des patientes traitées par DERMESTRIL ont présenté des effets indésirables systémiques légers et transitoires. Une tension mammaire a été rapportée chez 20 à 35 % des patientes. Des réactions locales au site d'application, consistant pour la plupart en un érythème léger avec ou sans prurit, sont survenues chez 10 à 25 % des patientes.
Le tableau ci-dessous présente les effets indésirables rapportés chez les utilisatrices d’un traitement hormonal substitutif (THS), classés selon la classification système-organe MedDRA, (voir également rubrique 4.4 Mises en gardes spéciales et précautions d’emploi).
|
Effets indésirables fréquents (> 1/100, < 1/10) |
Effets indésirables peu fréquents (> 1/1000, < 1/100) |
Effets indésirables rares (> 1/10 000, < 1/1000) |
Effets indésirables très rares (< 1/10000) |
Effets indésirables de fréquence indéterminée |
|
|
Infections et infestations |
Vaginite Candidose vaginale |
|
|||
|
Affections du système immunitaire |
Réaction d’hypersensibilité |
|
|||
|
Affections du métabolisme et de la nutrition |
Prise de poids ou perte de poids |
Diminution de la tolérance aux glucides |
|
||
|
Affections psychiatriques |
Nervosité, insomnies |
Humeur dépressive |
Anxiété Baisse de la libido ou augmentation de la libido |
|
|
|
Affections du système nerveux |
Céphalées |
Vertiges |
Migraine Paresthésie |
Chorée |
Epilepsie
|
|
Affections oculaires |
Troubles visuels |
Intolérance aux lentilles de contact |
|
||
|
Affections cardiaques |
Palpitations |
Angor et infarctus du myocarde |
|||
|
Affections gastro-intestinales |
Douleurs abdominales, Nausée, diarrhée |
Dyspepsie |
Ballonnement Vomissement |
Pancréatite (chez les femmes ayant des antécédents d’hypertriglycéridémie)
|
|
|
Affections hépato-biliaires |
Fonction hépatique anormale |
Affections de la vésicule biliaire, Calculs biliaires |
|
||
|
Affections de la peau et du tissu sous-cutané |
Rash Prurit Sècheresse cutanée |
Erythème nodulaires Décoloration cutanée Urticaire |
Hirsutisme Alopécie Acné |
Nécrose cutanée |
Angioedème
|
|
Affections des muscles squelettiques et des tissus conjonctifs |
Douleurs dorsales |
Crampes musculaires Myasthénie |
|
||
|
Affections des organes de reproduction et du sein |
Saignements vaginaux / utérins incluant les légers saignements (spotting) Troubles menstruels/métrorrhagies Spasmes utérins Hyperplasie de l’endomètre |
Douleur mammaire Tension mammaire |
Dysménorrhée Ecoulement vaginal Syndrome de type prémenstruel Hypertrophie mammaire Léiomyomes (aggravation) utérins, kystes paratubulaires, polypes endo-cervicaux |
Fibrose kystique du sein |
|
|
Tumeurs bénignes, malignes et non précisées (incluant kystes et polypes) |
|
|
|
|
Cancer du sein Tumeurs bénignes et malignes oestrogéno-dépendantes, c’est-à-dire, cancer de l’endomètre, cancer de l’ovaire
|
|
Affections vasculaires |
Augmentation de la pression artérielle |
Thrombo-embolie veineuse, thrombose veineuse profonde de la jambe ou pelvienne et embolie pulmonaire. |
Accident vasculaire cérébral
|
||
|
Troubles généraux et anomalies du site d’administration |
Réaction au site d’application (1) |
Œdème |
Fatigue |
Erythème au site d’application avec ou sans prurit |
|
|
Investigations |
Augmentation du taux des transaminases, |
|
(1) Les réactions cutanées au site d’application sont moins fréquentes si le dispositif transdermique est appliqué au niveau de la partie supérieure externe des fesses en changeant chaque fois de site d’application.
Le terme MedDRA le plus approprié est utilisé pour décrire une certaine réaction et son synonyme et les états apparentés.
Risque du cancer du sein
· Une augmentation jusqu’à 2 fois du risque de cancer du sein a été rapportée chez des femmes ayant pris une association estro-progestative pendant plus de 5 ans.
· L’augmentation du risque est plus faible chez les utilisatrices d’estrogènes seuls comparativement aux utilisatrices d’associations estro-progestatives.
· Le niveau de risque dépend de la durée du traitement (voir rubrique 4.4).
· Les estimations du risque absolu basées sur les résultats du plus large essai randomisé contrôlé versus placebo (étude WHI) et de la plus large méta-analyse des études épidémiologiques prospectives sont présentées ci-après.
Plus importante méta-analyse d’études épidémiologiques prospectives
Estimation du risque additionnel de cancer du sein après 5 ans de traitement chez des femmes ayant un IMC de 27 (kg/m²)
|
Age au début du THS (ans) |
Incidence pour 1000 patientes n’ayant jamais pris de THS sur une période de 5 ans (50-54 ans)* |
Risque relatif |
Nombre de cas supplémentaires pour 1000 utilisatrices de THS après 5 ans |
|
|
THS par estrogènes seuls |
||
|
50 |
13,3 |
1,2 |
2,7 |
|
|
Association estroprogestative |
||
|
50 |
13,3 |
1,6 |
8,0 |
*Issu des taux d’incidence de base en Angleterre en 2015 chez des femmes ayant un IMC de 27 (kg/m²)
Remarque : étant donné que l’incidence de base du cancer du sein diffère selon les pays de l’Union européenne (EU), le nombre de cas supplémentaires de cancer du sein variera proportionnellement.
Estimation du risque additionnel de cancer du sein après 10 ans de traitement chez des femmes ayant un IMC de 27 (kg/m²)
|
Age au début du THS (ans) |
Incidence pour 1000 patientes n’ayant jamais pris de THS sur une période de 10 ans (50-59 ans)* |
Risque relatif |
Nombre de cas supplémentaires pour 1000 utilisatrices de THS après 10 ans |
|
THS par estrogènes seuls |
|||
|
50 |
26,6 |
1,3 |
7,1 |
|
Association estroprogestative |
|||
|
50 |
26,6 |
1,8 |
20,8 |
*Issu des taux d’incidence de base en Angleterre en 2015 chez des femmes ayant un IMC de 27 (kg/m²)
Remarque : étant donné que l’incidence de base du cancer du sein diffère selon les pays de l’UE, le nombre de cas supplémentaires de cancer du sein variera proportionnellement.
Etude WHI aux Etats-Unis : risque additionnel de cancer du sein sur 5 ans de traitement
|
Age (ans) |
Incidence pour 1 000 femmes non utilisatrices de THS Sur 5 ans 2 |
Risque relatif # |
Nombre de cas supplémentaires pour 1 000 utilisatrices de THS sur 5 ans (IC 95%) |
|
Estrogènes seuls (Estrogènes conjugués équins) |
|||
|
50-79 |
21 |
0,8 (0,7-1,0) |
-4 (-6 – 0)2 |
|
Association estro-progestative CEE+ MPA § |
|||
|
50-79 |
17 |
1,2 (1,0-1,5) |
+4 (0-9) |
|
2L’étude WHI chez des femmes hystérectomisées, n’ayant pas montré d’augmentation du risque de cancer du sein § Lorsque l’analyse était limitée aux femmes n’ayant pas utilisé de THS avant l’étude, il n’était pas observé d’augmentation de risque au cours des 5 premières années de traitement : après 5 ans, le risque était plus élevé que chez les non-utilisatrices |
|||
Risque de cancer de l'endomètre
Femmes ménopausées non hystérectomisées
Le risque de cancer de l’endomètre est d’environ 5 pour 1000 femmes ayant un utérus intact et n’utilisant pas de THS.
Chez les femmes ayant un utérus intact, l’utilisation d’un THS à base d’estrogènes seuls n’est pas recommandée car cela augmente le risque de cancer de l’endomètre (voir rubrique 4.4)
Dans les études épidémiologiques, l’augmentation du risque de cancer de l’endomètre dépendait de la durée de traitement à base de d’estrogènes seuls et de la dose d’estrogènes et variait de 5 à 55 cas supplémentaires diagnostiqués pour 1 000 femmes âgées de 50 à 65 ans.
L’ajout d’un progestatif au traitement par estrogènes seuls pendant au moins 12 jours par cycle permet de prévenir cette augmentation de risque. Dans l’étude « Million Women Study », l’utilisation pendant 5 ans d’un TSH combiné (séquentiel ou continu) n’a pas augmenté le risque de cancer de l’endomètre (RR de 1,0 (0,8 – 1,2).
Risque de cancer ovarien
L'utilisation d'un THS par œstrogènes seuls ou par une combinaison d'œstrogènes et de progestatifs a été associée à une légère augmentation du risque de cancer ovarien diagnostiqué (voir rubrique 4.4). Une méta-analyse portant sur 52 études épidémiologiques a signalé un risque accru de cancer ovarien chez les femmes prenant actuellement un THS par rapport aux femmes n'en ayant jamais pris (RR 1.43, IC 95 % 1.31-1.56). Chez les femmes âgées de 50 à 54 ans, prendre un THS pendant cinq ans entraîne l'apparition d'un cas supplémentaire pour 2000 utilisatrices. Chez les femmes âgées entre 50 à 54 ans qui ne prennent pas de THS, un diagnostic de cancer ovarien sera posé chez environ 2 femmes sur 2000 sur une période de cinq ans.
Risque d’accident thromboembolique veineux
Le THS est associé à une augmentation de 1,3 à 3 fois du risque relatif de survenue d’un accident thromboembolique veineux, c’est-à-dire thrombose veineuse profonde ou embolie pulmonaire.
La probabilité de survenue d’un tel événement est plus élevée au cours de la première année d’utilisation du THS (voir rubrique 4.4). Les résultats des études WHI sont présentés ci-après :
Etudes WHI : risque additionnel d’accident thromboembolique veineux sur 5 ans de traitement
|
Age (ans) |
Incidence pour 1000 femmes dans le bras placebo sur 5 ans |
Risque relatif (IC 95%) |
Nombre de cas supplémentaires pour 1000 utilisatrices de THS |
|
Estrogènes seuls par voie orale3 |
|||
|
50-59 |
7 |
1.2 (0.6-2.4) |
1 (-3 – 10) |
|
Association estro-progestative orale |
|||
|
50-59 |
4 |
2.3 (1.2 – 4.3) |
5 (1 - 13) |
|
3 Etude chez des femmes hystérectomisées |
|||
Risque de maladie coronarienne
Le risque de maladie coronarienne est légèrement augmenté chez les utilisatrices de THS estro-progestatif au-delà de 60 ans (voir rubrique 4.4).
Risque d’accident vasculaire cérébral ischémique
L’utilisation d’un THS à base d’estrogènes seuls ou d’une association estro-progestative est associée à une augmentation jusqu’à 1,5 fois du risque relatif d’AVC ischémique. Le risque d’AVC hémorragique n’est pas augmenté lors de l’utilisation d’un THS.
Ce risque ne dépend pas de l’âge ni de la durée de traitement, mais comme le risque de base est fortement âge-dépendant, le risque global d’AVC chez les femmes utilisant un THS augmente avec l’âge (voir rubrique 4.4)
Etudes WHI combinées – risque additionnel d’AVC4 sur 5 ans de traitement
|
Age (ans) |
Incidence pour 1000 femmes dans le bras placebo sur 5 ans |
Risque relatif (IC 95%) |
Nombre de cas supplémentaires pour 1000 utilisatrices de THS sur 5 ans |
|
|
50-59 |
8 |
1.3 (1.1-1.6) |
3 (1-5) |
|
|
4 il n’a pas été fait de distinction entre les AVC ischémiques et hémorragiques |
||||
D’autres effets indésirables ont été signalés avec le traitement par estrogènes/ progestatifs :
· Pathologie de la vésicule biliaire.
· Troubles cutanés et sous-cutanés : chloasma, érythème multiforme, érythème noueux, purpura vasculaire.
· Démence probable au-delà de l’âge de 65 ans (voir rubrique 4.4).
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr.
Les effets d'un surdosage sont habituellement une sensation de tension mammaire, un gonflement abdomino-pelvien, une anxiété, une irritabilité, somnolence, sensation vertigineuse. Ces symptômes disparaissent au retrait du dispositif.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : ESTROGENES, code ATC : G03CA03.
(Système génito-urinaire et hormones sexuelles)
Le principe actif, 17-β estradiol de synthèse, est chimiquement et biologiquement identique à l'estradiol endogène humain. Il remplace l'arrêt de production des estrogènes chez les femmes ménopausées et soulage les symptômes climatériques de la ménopause.
Le dispositif transdermique libère de l'estradiol, sous forme inchangée et en quantité physiologique dans la circulation sanguine.
Le dispositif transdermique élève la concentration d'estradiol à un niveau similaire à celui obtenu dans les phases folliculaires précoce et moyenne.
Information sur les études cliniques :
Le soulagement des symptômes de la ménopause a été obtenu dès les premières semaines de traitement.
5.2. Propriétés pharmacocinétiques
Des concentrations sériques physiologiques d'estradiol proportionnelles à la quantité administrée sont atteintes dès la 8ème heure après l'application.
24 heures environ après l'application, les concentrations sériques d'estradiol atteignent des pics moyens respectivement de 37, 61 et 117 pg/ml. Les taux sériques moyens d'estradiol restent ensuite pratiquement constants pendant toute la durée de l'application (3 - 4 jours) et sont respectivement de 23, 40 et 79 pg/ml après l'application de DERMESTRIL 25 microgrammes/24 heures, 50 microgrammes/24 heures et 100 microgrammes/24 heures.
Toutefois, il convient de noter que des variations inter-individuelles importantes des taux sériques d'estradiol peuvent être observées comme lors de toute administration transcutanée (voir rubrique 4.4).
Le taux sérique d'estradiol revient à la valeur de base dans les 12 heures suivant le retrait du dispositif.
L'estradiol est principalement métabolisé dans le foie. Les métabolites les plus importants sont l'estriol, l'estrone et leurs conjugués (glucuronates, sulfates) ; ils sont beaucoup moins actifs que l'estradiol.
La plupart des métabolites sont excrétés dans l'urine sous forme de glucuronates et de sulfates.
La demi-vie d'élimination de l'estradiol dans le plasma est d'environ 1 heure. La clairance plasmatique varie de 650 à 900 l/j/m2. Les métabolites estrogéniques subissent également un cycle entéro-hépatique.
5.3. Données de sécurité préclinique
Feuillet de support : Polyéthylène téréphtalate (HOSTAPHAN RN 15).
2 ans
6.4. Précautions particulières de conservation
A conserver à une température inférieure à 25°C.
6.5. Nature et contenu de l'emballage extérieur
Dispositif transdermique en sachet (Aluminium/SURLYN) ; boîte de 8.
6.6. Précautions particulières d’élimination et de manipulation
Voir rubrique 4.2
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
AVENIDA MIRALCAMPO 7
POLIGONO IND. MIRALCAMPO
19200 AZUQUECA DE HENARES, GUADALAJARA
MADRID
ESPAGNE
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 340 904 3 1 : dispositif transdermique en sachet (Aluminium/SURLYN); boîte de 8.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste II
ANSM - Mis à jour le : 11/07/2025
DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique
Estradiol
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin, votre pharmacien ou votre infirmier/ère.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique ?
3. Comment utiliser DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : ESTROGENES - code ATC : G03CA03.
DERMESTRIL est un traitement hormonal substitutif (THS). Il contient du 17-β estradiol. DERMESTRIL est utilisé chez les femmes ménopausées dont les dernières règles datent d’au moins 6 mois.
DERMESTRIL est utilisé pour :
Soulager les symptômes apparaissant après la ménopause.
Lors de la ménopause, la quantité d’estrogènes produits par l’organisme féminin chute. Chez certaines femmes, cette chute se traduit par des symptômes tels qu’une sensation de chaleur au niveau du visage, du cou et de la poitrine (les « bouffées de chaleur »). DERMESTRIL soulage ces symptômes après la ménopause.
DERMESTRIL vous sera prescrit uniquement si vos symptômes altèrent gravement votre vie quotidienne.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique ?
N’utilisez jamais DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique :
· Si vous êtes allergique (hypersensible) à l'estradiol ou à l'un des autres composants contenus dans DERMESTRIL (listés en rubrique 6) ;
· Si vous avez ou avez eu un cancer du sein, ou s’il existe une suspicion que vous en ayez un,
· Si vous avez un cancer sensible aux estrogènes tel qu’un cancer de la paroi de l’utérus (endomètre), ou s’il existe une suspicion que vous en ayez un ;
· Si vous avez des saignements vaginaux non expliqués ;
· Si vous avez un développement exagéré de la paroi de l’utérus (hyperplasie de l’endomètre) qui n’est pas traité ;
· Si vous avez ou avez eu un caillot sanguin dans une veine (thrombose) tel que dans les jambes (thrombose veineuse profonde), ou dans les poumons (embolie pulmonaire) ;
· Si vous avez des troubles de la coagulation sanguine (tels qu’un déficit en protéine C, protéine S ou antithrombine) ;
· Si vous avez ou avez eu récemment une maladie causée par des caillots sanguins dans les artères, telle qu’une crise cardiaque, un accident vasculaire cérébral, ou de l’angine de poitrine ;
· Si vous avez ou avez eu une maladie du foie, et que vos tests de la fonction hépatique ne sont pas retournés à la normale ;
· Si vous avez une maladie héréditaire rare du sang appelée « porphyrie ».
Si l’une de ces pathologies apparaît pour la première fois lors du traitement avec DERMESTRIL, arrêtez le traitement et consultez immédiatement votre médecin.
Avertissements et précautions
Antécédents médicaux et examens réguliers.
L’utilisation d’un THS entraine des risques qui doivent être pris en considération lorsque vous décidez de commencer ce traitement ou de le continuer.
L’expérience chez les femmes avec une ménopause précoce (liée à une insuffisance ovarienne ou à une chirurgie) est limitée. Si vous avez une ménopause précoce, les risques liés à l’utilisation d’un THS peuvent être différents. Parlez-en à votre médecin.
Avant de commencer (ou recommencer) un THS, votre médecin vous interrogera sur vos antécédents médicaux personnels et familiaux. Votre médecin peut décider de pratiquer un examen physique. Cet examen peut inclure un examen de vos seins et, si nécessaire, un examen gynécologique.
Dès que vous commencez DERMESTRIL, consultez votre médecin pour des examens réguliers (au moins une fois par an). Lors de ces examens, celui-ci pourra aborder avec vous les bénéfices et les risques liés à la poursuite du traitement par DERMESTRIL.
Faites régulièrement une mammographie en suivant les recommandations de votre médecin.
Adressez-vous à votre médecin, pharmacien ou votre infirmier/ère avant d’utiliser DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique.
Mises en garde et précautions d’emploi
Signalez à votre médecin avant de débuter votre traitement, si vous avez déjà eu un des signes suivants car ils peuvent revenir ou s’aggraver pendant le traitement par DERMESTRIL. Si c’est le cas, consultez votre médecin pour des examens plus réguliers :
· fibromes dans votre utérus ;
· présence de muqueuse utérine en dehors de l'utérus (endométriose) ou antécédents de développement exagéré de votre muqueuse utérine (hyperplasie endométriale) ;
· risque augmenté de développer des caillots sanguins (voir « Caillots de sang dans une veine (thromboses) ») ;
· risque augmenté d’avoir un cancer dépendant des estrogènes (par exemple si votre mère, votre sœur ou votre grand-mère a eu un cancer du sein) ;
· hypertension artérielle ;
· maladie du foie, telle qu’une tumeur bénigne du foie ;
· diabète ;
· calcul biliaire ;
· migraine ou maux de tête sévères ;
· maladie du système immunitaire qui peut affecter plusieurs parties du corps (lupus érythémateux disséminé, LED) ;
· épilepsie ;
· asthme ;
· maladie affectant les tympans ou l’audition (otosclérose) ;
· niveau élevé de graisses dans votre sang (triglycérides) ;
· rétention d’eau liée à des troubles cardiaques ou rénaux ;
· angioœdème héréditaire ou acquis.
Arrêtez votre traitement et prévenez immédiatement votre médecin
Si vous notez l’apparition des signes suivants :
· une des pathologies signalées en rubrique « N’utilisez jamais DERMESTRIL» ;
· un jaunissement de votre peau ou du blanc de vos yeux. C’est peut-être un signe d’une maladie du foie ;
· une augmentation importante de votre pression artérielle (les symptômes peuvent être mal de tête, fatigue, sensations vertigineuses) ;
· des maux de tête tels qu’une migraine, qui apparaissent pour la première fois ;
· si vous devenez enceinte ;
· si vous remarquez des signes possibles d’un caillot sanguin, tels que :
o Gonflement douloureux dans vos jambes,
o Douleur brutale à la poitrine,
o Difficulté à respirer.
Pour plus d’informations, voir rubrique « Caillot de sang dans une veine ».
Note : DERMESTRIL n’est pas un contraceptif. S’il s’est écoulé moins d’un an depuis vos dernières règles, ou si vous avez moins de 50 ans, vous pouvez avoir besoin d’une contraception complémentaire pour éviter une grossesse. Demandez conseil à votre médecin.
THS et cancer
Développement exagéré de la muqueuse utérine (hyperplasie endométriale) et cancer de la paroi de l’utérus (cancer de l’endomètre)
La prise d’un THS à base d’estrogènes seuls augmentera le risque de développement exagéré de la muqueuse utérine (hyperplasie endométriale) et de cancer de la muqueuse utérine (cancer de l’endomètre).
La prise d’un progestatif en association à DERMESTRIL pendant au moins 12 jours sur chaque cycle de 28 jours vous protège de ce risque supplémentaire. Si vous avez toujours votre utérus, votre médecin vous prescrira donc un progestatif à prendre séparément, en plus de DERMESTRIL. Si vous n’avez plus votre utérus (si vous avez eu une hystérectomie), votre médecin vous dira si vous pouvez prendre DERMESTRIL en toute sécurité sans y associer un progestatif.
Chez les femmes qui ont toujours leur utérus et qui ne prennent pas de THS, 5 sur 1000 auront un cancer de l’endomètre diagnostiqué entre 50 et 65 ans.
Chez les femmes de 50 à 65 ans qui ont toujours leur utérus et qui prennent un THS à base d’estrogènes seuls, le nombre de cas supplémentaires peut varier de 5 à 55 sur 1000 utilisatrices selon la dose et la durée du traitement.
Saignements irréguliers
Lors d’un traitement cyclique ou continu séquentiel avec DERMESTRIL, vous aurez des saignements une fois par mois (appelés saignements de privation). Mais vous pouvez aussi avoir des saignements irréguliers ou des petites pertes sanguines (spotting), en plus des saignements mensuels. Si ces saignements irréguliers :
· persistent au-delà des 6 premiers mois
· débutent alors que vous prenez DERMESTRIL depuis plus de 6 mois
· persistent après l’arrêt du traitement par DERMESTRIL
consultez votre médecin dès que possible.
Cancer du sein
Les données disponibles montrent que la prise d’un traitement hormonal de substitution (THS) estro-progestatif combiné ou d’un THS à base d'estrogènes seuls augmente le risque de cancer du sein. Ce risque supplémentaire dépend de la durée de suivi du THS. Le risque additionnel devient évident au bout de 3 ans d’utilisation. Après avoir arrêté le THS, le risque additionnel diminuera dans le temps, mais pourra perdurer 10 ans ou plus si vous avez suivi un THS pendant plus de 5 ans.
Pour comparaison
Chez les femmes de 50 à 54 ans qui ne prennent pas de THS, un diagnostic de cancer du sein sera posé, en moyenne, chez environ 13 à 17 femmes sur 1 000 après une période de cinq ans.
Chez les femmes âgées de 50 ans qui débutent un THS à base d'estrogènes seuls pour 5 ans, on dénombrera 16 à 17 cas sur 1 000 utilisatrices (soit 0 à 3 cas supplémentaires).
Chez les femmes âgées de 50 ans qui débutent un THS estro-progestatif pour 5 ans, on dénombrera 21 cas sur 1 000 utilisatrices (soit 4 à 8 cas supplémentaires).
Chez les femmes de 50 à 59 ans qui ne prennent pas de THS, un diagnostic de cancer du sein sera posé, en moyenne, chez environ 27 femmes sur 1 000 après une période de dix ans.
Chez les femmes âgées de 50 ans qui débutent un THS à base d'estrogènes seuls pour 10 ans, on dénombrera 34 cas sur 1 000 utilisatrices (soit 7 cas supplémentaires).
Chez les femmes âgées de 50 ans qui débutent un THS estroprogestatif pour 10 ans, on dénombrera 48 cas sur 1 000 utilisatrices (soit 21 cas supplémentaires).
Ø Vérifiez régulièrement vos seins. Consultez votre médecin si vous remarquez des changements tels que :
· capitons au niveau de la peau
· modifications au niveau du mamelon
· boules éventuelles que vous pouvez voir ou sentir
De plus, il est conseillé de participer aux programmes de dépistage par mammographie, lorsqu’ils vous sont proposés. Pour la mammographie de dépistage, il est important d’informer le professionnel de santé (manipulateur en radiologie/médecin) qui vous fait la radiographie que vous utilisez un THS, car ce médicament peut augmenter la densité de vos seins, ce qui peut affecter les résultats de la mammographie. Lorsque la densité de la poitrine est augmentée, la mammographie peut ne pas détecter toutes les masses (boules).
Cancer de l’ovaire
Le cancer de l’ovaire est rare (beaucoup plus rare que le cancer du sein). L'utilisation d'un THS par œstrogènes seuls ou par une combinaison d'œstrogènes et de progestatifs a été associée à une légère augmentation du risque de cancer ovarien.
Le risque de cancer ovarien varie en fonction de l'âge. Par exemple, chez les femmes âgées de 50 à 54 ans qui ne prennent pas de THS, un diagnostic de cancer ovarien sera posé chez 2 femmes sur 2000 en moyenne sur une période de 5 ans. Chez les femmes ayant pris un THS pendant 5 ans, il y aura environ 3 cas sur 2000 utilisatrices (soit environ un cas supplémentaire).
Effets des THS sur le cœur et la circulation
Caillots de sang dans une veine (thrombose veineuse)
Le risque de caillots sanguins dans les veines est environ de 1,3 à 3 fois supérieur chez les utilisatrices de THS par rapport aux non-utilisatrices, particulièrement pendant la première année de traitement.
Ces caillots de sang peuvent être graves, et si l'un d’eux migre vers les poumons, cela peut causer des douleurs dans la poitrine, un essoufflement, un malaise, voire parfois le décès.
Vous avez plus de risque d’avoir un caillot sanguin, lorsque vous vieillissez, et si l’une des situations suivantes s’applique à vous. Signalez à votre médecin si l'une de ces situations s'applique à vous :
· vous ne pouvez pas marcher pendant une longue période en raison d’une chirurgie, blessure ou maladie grave (voir également section 3 « Si vous devez subir une opération chirurgicale »),
· vous êtes en surpoids sévère (IMC > 30 kg/m²),
· vous avez des problèmes de coagulation sanguine qui nécessitent un traitement à long terme avec un médicament utilisé pour prévenir les caillots sanguins,
· un de vos parents proches a déjà eu un caillot de sang dans la jambe, le poumon ou un autre organe,
· vous avez un lupus érythémateux disséminé (LED),
· vous avez un cancer.
Pour les signes de caillot sanguin, voir rubrique « Arrêtez votre traitement et prévenez immédiatement votre médecin ».
Chez les femmes de la cinquantaine ne prenant pas de THS, un caillot sanguin veineux survient en moyenne chez 4 à 7 femmes sur 1000 après une période de 5 ans.
Chez les femmes de la cinquantaine prenant un THS estro-progestatif après une période de 5 ans, il y aura 9 à 12 cas sur 1000 utilisatrices (c'est-à-dire 5 cas supplémentaires).
Chez les femmes de la cinquantaine qui n’ont plus leur utérus et qui ont pris un THS contenant uniquement un estrogène pendant plus de 5 ans, il y aura 5 à 8 cas sur 1000 utilisatrices (c’est-à-dire un cas supplémentaire).
Maladie cardiaque (crise cardiaque)
Il n’y a pas de preuve que le THS participe à la prévention d’une crise cardiaque.
Les femmes de plus de 60 ans utilisatrices de THS estro-progestatif ont un risque légèrement plus augmenté de développer une maladie cardiaque que celles qui ne prennent pas de THS.
Pour les femmes qui n’ont plus leur utérus et qui prennent un THS contenant uniquement un estrogène, le risque de développer une maladie cardiaque n’est pas augmenté.
Accident Vasculaire Cérébral (AVC)
Le risque d’avoir un accident vasculaire cérébral est environ 1,5 fois supérieur chez les utilisatrices de THS par rapport aux non-utilisatrices.
Le nombre de cas supplémentaires d'AVC liés à l’utilisation d’un THS augmente avec l’âge.
Comparaison
Chez les femmes de la cinquantaine ne prenant pas de THS, un AVC est attendu en moyenne chez 8 femmes sur 1000 sur une période de plus de 5 ans.
Pour les femmes de la cinquantaine prenant un THS, il y aura 11 cas sur 1000 utilisatrices sur une période de plus de 5 ans (c'est-à-dire 3 cas supplémentaires).
Autres pathologies
Le THS ne prévient pas la perte de mémoire. Le risque de perte de mémoire pourrait être toutefois plus élevé chez les femmes qui commencent à utiliser un THS après l’âge de 65 ans. Demandez conseil à votre médecin.
Enfants et adolescents
Sans objet.
Autres médicaments et DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique
Certains médicaments peuvent interférer avec les effets de DERMESTRIL. Cette interférence peut entrainer des saignements irréguliers. Cela concerne les médicaments suivants :
· les médicaments utilisés dans le traitement de l'épilepsie (par exemple phénobarbital, phénytoïne, carbamazépine)
· les médicaments utilisés dans le traitement de la tuberculose (par exemple rifampicine et rifabutine)
· les médicaments utilisés dans le traitement des infections par le VIH (par exemple névirapine, éfavirenz, ritonavir et nelfinavir)
· les préparations à base de plantes contenant du millepertuis (Hypericum perforatum)
Le THS peut modifier le mode d'action de certains autres médicaments :
· un médicament contre l'épilepsie (lamotrigine), car il pourrait augmenter la fréquence des crises
· les médicaments utilisés dans le traitement de l’infection par le virus de l’hépatite C (VHC) (l’association ombitasvir/paritaprévir/ritonavir et dasabuvir avec ou sans ribavirine; glécaprévir/pibrentasvir ou sofosbuvir/velpatasvir/ voxilaprevir), qui peuvent entraîner une augmentation de certains paramètres du fonctionnement du foie (augmentation du taux d’ALAT, une enzyme du foie) chez les femmes utilisant des contraceptifs contenant de l’éthinylestradiol. DERMESTRIL contient de l’estradiol à la place de l’éthinylestradiol. On ne sait pas si une augmentation du taux d’ALAT peut se produire lors de l’utilisation de DERMESTRIL avec cette association contre le VHC.
Veuillez informer votre médecin ou votre pharmacien si vous prenez ou avez récemment pris d’autres médicaments incluant des médicaments obtenus sans ordonnance, des médicaments à base de plantes ou d’autres produits naturels. Votre médecin vous conseillera.
Analyses en laboratoire
Si vous devez faire une prise de sang, signalez à votre médecin ou au personnel du laboratoire d’analyse que vous prenez DERMESTRIL, car ce médicament peut modifier les résultats de certaines analyses.
DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique avec des aliments et boissons
Sans objet
Grossesse, allaitement et fertilité
DERMESTRIL doit être uniquement utilisé chez les femmes ménopausées. Si vous devenez enceinte, interrompez le traitement par DERMESTRIL et parlez-en à votre médecin.
Vous ne devez pas utiliser DERMESTRIL si vous allaitez.
Demandez conseil à votre médecin ou à votre pharmacien avant de prendre tout médicament.
Conduite de véhicules et utilisation de machines
Il n'y a pas de données qui indiquent que DERMESTRIL peut avoir un effet sur l'aptitude à conduire des véhicules ou à utiliser des machines.
DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique contient
Sans objet.
3. COMMENT UTILISER DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique ?
Trois dosages de DERMESTRIL sont disponibles : DERMESTRIL 25, 50 et 100. Votre médecin choisira le dispositif DERMESTRIL le mieux adapté à votre cas, bien que la plupart des femmes commencent par le dispositif DERMESTRIL 25. Pendant le traitement, votre médecin adaptera la dose du dispositif à votre situation personnelle, c’est à dire en fonction de l’efficacité du traitement et si vous souffrez de certains effets indésirables. En traitement d’attaque et d’entretien, votre médecin choisira la plus faible dose de dispositif efficace, pendant la durée la plus courte possible.
Posologie
DESMESTRIL 50 microgrammes/24 heures, dispositif transdermique est habituellement appliqué 2 fois par semaine, c'est-à-dire renouvelé tous les 3 à 4 jours.
Vous pouvez déterminer les jours où vous devez changer le dispositif à partir du tableau ci-dessous, en commençant le premier jour d’utilisation :
|
Si vous appliquez le premier dispositif un : |
Changez-le le : |
Changez-le à nouveau le : |
|
Lundi |
Jeudi |
Lundi |
|
Mardi |
Vendredi |
Mardi |
|
Mercredi |
Samedi |
Mercredi |
|
Jeudi |
Dimanche |
Jeudi |
|
Vendredi |
Lundi |
Vendredi |
|
Samedi |
Mardi |
Samedi |
|
Dimanche |
Mercredi |
Dimanche |
Votre médecin pourra vous prescrire le traitement selon 2 modalités :
· Traitement cyclique : le dispositif transdermique doit être appliqué deux fois par semaine pendant une durée de 24 à 28 jours, suivi d'un intervalle de 2 à 7 jours sans traitement.
· Traitement continu : le dispositif transdermique doit être appliqué en traitement continu deux fois par semaine.
Si votre médecin associe à ce traitement un autre médicament hormonal (progestatif) durant au moins les 12 derniers jours de chaque cycle de traitement par DERMESTRIL, ce traitement ne devra pas être oublié.
Des saignements évoquant les règles peuvent survenir pendant la période d'interruption. Ces saignements sont normaux et peu abondants. Si des saignements abondants ou irréguliers surviennent, consultez votre médecin.
Quand faut-il démarrer le traitement ?
Vous pouvez commencer le traitement par DERMESTRIL au moment qui vous convient si vous n'êtes pas sous traitement à base d'estrogènes.
Si vous suivez actuellement un traitement estro-progestatif cyclique ou séquentiel, vous devez terminer votre cycle de traitement en cours avant de débuter le traitement par DERMESTRIL ; le moment approprié pour commencer le traitement par DERMESTRIL est le premier jour de l’hémorragie de privation (saignements évoquant les règles).
Si vous utilisez déjà un traitement estro-progestatif continu, vous pouvez passer directement au traitement par DERMESTRIL.
Comment prendre un progestatif avec DERMESTRIL ?
Si vous avez toujours votre utérus, autrement dit si vous n'avez pas subi d'hystérectomie, votre médecin vous prescrira probablement un progestatif à utiliser en même temps que le dispositif DERMESTRIL pour éviter tout problème dû à un épaississement de la paroi de l'utérus, c'est-à-dire une hyperplasie de l'endomètre (voir les mises en garde spéciales concernant le cancer de l'endomètre).
Il y a deux façons de le prendre :
1. Traitement cyclique
DERMESTRIL est généralement administré pendant 24 à 28 jours, suivis d'une période de 2 à 7 jours sans traitement. En général, le médecin prescrit le progestatif pendant au moins 12 jours de chaque cycle. Il est possible que vous présentiez une « hémorragie de privation » (saignements évoquant les règles) pendant les derniers jours du traitement par progestatif, voire après l'arrêt.
2. Traitement séquentiel continu
DERMESTRIL est administré sans interruption et il n'y a donc pas de période sans traitement. Le progestatif est généralement prescrit pendant au moins 12 jours de chaque cycle de 28 jours. Votre médecin vous recommandera cette forme de traitement si vous ressentez des symptômes de ménopause au cours de la période sans traitement. Il est possible que vous présentiez une « hémorragie de privation » (saignements évoquant les règles) pendant les derniers jours du traitement par progestatif, voire après l'arrêt.
Mode et voie d'administration
Comment appliquer DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique ?
Vous devez appliquer le dispositif sur une peau propre et sèche, à un endroit ne présentant pas de coupures, de boutons ou de taches et non recouvert de crème, d’hydratant ou de talc.
Vous ne DEVEZ PAS appliquer les dispositifs DERMESTRIL, dispositif transdermique sur ou à proximité des seins.
Votre dispositif transdermique DERMESTRIL doit être appliqué sur les hanches, les fesses ou le ventre (figure 1).
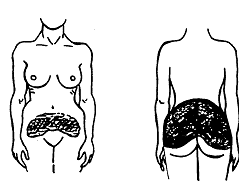
Figure 1
Les zones en noir sont celles où vous pouvez appliquer votre dispositif.
N’appliquez pas le dispositif sur une partie du corps formant des plis pendant les mouvements ou dans des zones où vos vêtements (par ex. ceintures élastiques) peuvent faire tomber le dispositif.
N’appliquez pas les dispositifs deux fois de suite au même endroit.
Dès qu’il a été retiré de son sachet, le dispositif DERMESTRIL doit être appliqué sur la peau de la manière suivante :
(i) Déchirez le sachet au niveau du bord prédécoupé pour l’ouvrir.
N’utilisez pas de ciseaux (figure 2).
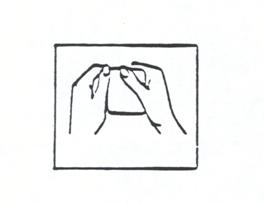
Figure 2
(ii) Tenez le dispositif entre le pouce et l’index, au niveau de la bande détachable (figure 3).
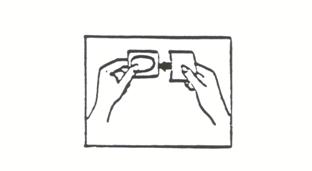
Figure 3
(iii) Retirez la partie la plus grande du film protecteur de l’autre main (voir figure 4).
Evitez de toucher la face adhésive du dispositif, car il risque ensuite de ne plus coller correctement.
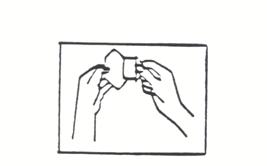
Figure 4
(iv) Appliquez la partie découverte du dispositif sur votre peau et retirez le reste du feuillet protecteur. Appuyez fermement sur toute la surface du dispositif pendant 10 secondes environ. Passez le doigt le long des bords pour vous assurer qu’il adhère fermement.
Comment enlever DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique ?
Pour enlever DERMESTRIL, dispositif transdermique, il vous suffit de détacher un bord et de tirer doucement sur le dispositif jusqu’à ce qu’il se détache.
Après emploi, le dispositif contient encore des estrogènes mais en quantité insuffisante pour être encore efficace. Les dispositifs utilisés seront repliés, coté adhésif à l'intérieur, avant d'être jetés.
Précautions particulières :
Il est possible de se doucher ou de prendre un bain tout en gardant le dispositif transdermique. En cas de décollement prématuré du dispositif, il faut tenter de le replacer sur une peau sèche.
Si cela n'est pas possible, utiliser un dispositif neuf qui sera retiré à la date initialement prévue. Reprendre ensuite le rythme de changement du dispositif conformément au schéma thérapeutique initial.
Une fois appliqué, le dispositif transdermique ne doit pas être directement exposé au soleil.
Dans tous les cas se conformer strictement à l'ordonnance de votre médecin.
Si vous devez subir une intervention chirurgicale
Si vous devez subir une intervention chirurgicale, informez votre chirurgien que vous prenez DERMESTRIL. Il sera peut-être nécessaire d’arrêter le traitement environ 4 à 6 semaines avant l’opération afin de réduire le risque de caillots sanguins (voir rubrique 2. Caillots sanguins dans une veine). Demandez à votre médecin quand vous pourrez reprendre DERMESTRIL.
Le dispositif transdermique provoque-t-il des irritations cutanées ?
Vous pouvez constater des démangeaisons pendant le port ou une certaine rougeur lors de son retrait.
Ces manifestations sont sans gravité et disparaîtront rapidement.
En cas de gêne, placez le dispositif transdermique à un autre endroit (sauf sur les seins).
Utilisation chez les enfants et les adolescents
Sans objet.
Si vous avez utilisé plus de DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique que vous n’auriez dû
Les signes de surdosage sont habituellement une sensation de douleur au niveau des seins et/ou des saignements vaginaux, une irritabilité, une anxiété, des nausées, des vomissements, une somnolence, une sensation vertigineuse, un gonflement au niveau de l’abdomen ou du bassin, des flatulences, une rétention d’eau et une sensation de lourdeur au niveau des jambes. Ces signes disparaissent lorsque le traitement est arrêté.
Si ces signes persistent, demandez l’avis de votre médecin.
Si vous oubliez d’utiliser DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique
Ne prenez pas de dose double pour compenser la dose simple que vous avez oublié de prendre.
Si vous n’avez pas de traitement pendant plusieurs jours de suite, des saignements irréguliers peuvent apparaître.
En cas de doute, consultez votre médecin.
Si vous arrêtez d’utiliser DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique
A l'arrêt du traitement, les signes de déficit en estrogènes liés à la ménopause peuvent réapparaître.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
· cancer du sein.
· épaississement anormal ou cancer de la paroi de l’utérus (hyperplasie endométriale ou cancer).
· cancer de l’ovaire.
· caillots sanguins dans les veines des jambes ou des poumons (thrombo-embolie veineuse).
· maladie cardiaque.
· accident vasculaire cérébral.
· probable perte de mémoire si le THS est commencé après l’âge de 65 ans.
Pour plus d’informations concernant ces effets indésirables, voir rubrique 2.
Les effets indésirables suivants ont été signalés lors de l'utilisation de DERMESTRIL et d’autres THS contenant du 17β-estradiol :
Très fréquents : survenant chez plus d’une patiente sur 10
Fréquents : survenant chez moins d’une patiente sur 10 mais plus d’une patiente sur 100
Peu fréquents : survenant chez moins d’une patiente sur 100 mais plus d’une patiente sur 1000
Rares : survenant chez moins d’une patiente sur 1000 mais plus d’une patiente sur 10 000
Très rares : survenant chez moins d’une patiente sur 10 000
Fréquence inconnue : ne peut pas être déterminée à partir des données disponibles
Effets indésirables fréquents (plus d'une patiente sur 100 mais moins d'une sur 10) :
· inflammation du vagin, infection vaginale due à un champignon (candidose vaginale).
· variations du poids.
· nervosité, insomnie.
· maux de tête.
· nausées, diarrhée, douleurs abdominales.
· rash (peau rouge et enflammée), prurit (démangeaisons), peau sèche.
· douleurs dorsales.
· troubles menstruels (métrorragie), saignements vaginaux / utérins incluant des légers saignements (spotting).
· spasmes de l’utérus.
· hyperplasie de l’endomètre.
· troubles menstruels.
· réactions au site d’application.
Effets indésirables peu fréquents (plus d'une patiente sur 1 000 mais moins d'une sur 100) :
· réaction allergique.
· humeur dépressive.
· vertiges.
· troubles visuels (altération de la vision).
· palpitations (rythme cardiaque irrégulier).
· dyspepsie (difficulté à digérer ou altération de la digestion).
· troubles de la vésicule biliaire, calculs biliaires.
· érythème noueux (nodules rouges douloureux sous la peau).
· urticaire, décoloration de la peau.
· tension des seins, douleur des seins.
· œdème (quantité volumineuse anormale de liquide dans le système circulatoire ou dans les tissus).
· augmentation de la pression artérielle.
· augmentation des enzymes hépatiques.
Effets indésirables rares (plus d'une patiente sur 10 000 mais moins d'une sur 1 000) :
· caillot de sang dans une veine (thrombo-embolie veineuse).
· modifications du désir sexuel (modifications de la libido).
· irritation des yeux en cas de port de lentilles de contact.
· anxiété.
· migraine.
· picotements ou engourdissement dans les mains, les pieds, les bras ou les jambes (paresthésies).
· ballonnement (plénitude ou gonflement abdominal post-prandial).
· vomissement.
· hirsutisme (croissance excessive des poils corporels ou faciaux).
· acné (boutons sur le visage, la poitrine et le dos), perte de cheveux.
· crampes musculaires, faiblesse musculaire (myasthénie).
· saignement douloureux (dysménorrhée).
· écoulement vaginal.
· syndrome de type prémenstruel (symptômes physiques présents entre l’ovulation et le début de la menstruation tels que la tension mammaire, le mal de dos, les crampes abdominales, la migraine, et les variations de l’appétit, ainsi que des symptômes psychologiques de l’anxiété, de la dépression et de l’agitation).
· hypertrophie mammaire.
· fatigue (épuisement physique et/ou moral).
Autres effets indésirables :
Les effets indésirables suivants ont été rapportés lors d’un traitement par estradiol (fréquence indéterminée) :
· augmentation du taux de sucre dans le sang (diminution de la tolérance aux glucides).
· épilepsie, soubresauts incontrôlables (chorée).
· accident vasculaire cérébral.
· caillots sanguins dans les artères (thromboembolisme artériel), angine de poitrine (angor) et infarctus.
· gonflement du visage et de la gorge pouvant entraîner des difficultés à respirer (angioœdème)
· inflammation du pancréas (pancréatite) chez les femmes présentant des taux importants de certaines graisses dans le sang (hypertriglycéridémie).
· troubles de la fonction hépatique.
· troubles cutanés et sous-cutanés :
o perte de tissu cutané (nécrose de la peau).
o décoloration brune ou brun foncé irrégulière de la peau touchant généralement le visage ou le cou, connue sous le nom de « masque de grossesse » (chloasma).
o éruption avec taches rouges-violettes ou plaies en forme de cible (érythème multiforme),
o nodules rouges douloureux sous la peau (érythème noueux).
o purpura vasculaire (inflammation des vaisseaux sanguins donnant des points ou des taches violacés sur la peau).
· démence (le THS ne prévient pas la perte de mémoire. Au cours d’une étude réalisée chez des femmes ayant débuté l’utilisation d’un THS combiné après l’âge de 65 ans, une légère augmentation du risque de démence a été observée).
· léiomyomes utérins (pouvant s’aggraver), kystes paratubulaires, polypes endo-cervicaux
· cancer du sein, tumeurs malignes ou bénignes pouvant dépendre du taux d’œstrogènes, comme le cancer de la muqueuse utérine (cancer de l’endomètre), cancer de l’ovaire.
· douleur des seins et tissus mammaire grumeleux (fibrose kystique du sein).
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou à votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur la boîte après EXP.
Ce médicament doit être conservé à une température inférieure à 25°C.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient DERMESTRIL 50 microgrammes/24 heures, dispositif transdermique
· La substance active est :
Estradiol....................................................................................................................... 4,00 mg
Pour un dispositif transdermique de 18 cm2
· Les autres composants sont :
Copolymère d'acrylates (DUROTAK 387-2353), copolymère d'acrylates et vinylacétate (DUROTAK 387-2287).
Polyéthylène téréphtalate (HOSTAPHAN RN 15).
Dispositif transdermique, boîte de 8.
Titulaire de l’autorisation de mise sur le marché
AVENIDA MIRALCAMPO 7
POLIGONO IND. MIRALCAMPO
19200 AZUQUECA DE HENARES, GUADALAJARA
MADRID
ESPAGNE
Exploitant de l’autorisation de mise sur le marché
15 RUE DE VANVES
92100 BOULOGNE BILLANCOURT
BENZSTRASSE 1
61352 BAD HOMBURG
ALLEMAGNE
ou
LTS LOHMANN THERAPIE-SYSTEME AG
LOHMANNSTR. 2
56626 ANDERNACH
ALLEMAGNE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).