Dernière mise à jour le 02/03/2026
TEGRETOL 20 mg/ml, suspension buvable
Indications thérapeutiques
Classe pharmacothérapeutique - code ATC : ANTIEPILEPTIQUE, dérivé du carboxamide - N03AF01
TEGRETOL appartient à une classe de médicaments appelés les antiépileptiques.
Il est utilisé pour traiter :
· certaines formes d’épilepsie et de convulsions
TEGRETOL est utilisé pour traiter différentes formes d’épilepsie ou de convulsions chez les adultes et les enfants. Ce médicament peut être pris seul ou en association avec un autre médicament antiépileptique.
· certains troubles de l’humeur
Dans ce cas, TEGRETOL est utilisé quand le traitement par un autre médicament (notamment le lithium) n’a pas fonctionné ou ne peut pas être utilisé.
· certains types de douleurs
o des douleurs au niveau du visage provoquées par une maladie des nerfs de la face (névralgies du trijumeau et du glossopharyngien).
o des douleurs neuropathiques périphériques chez un adulte.
Présentations
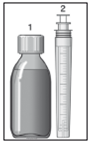
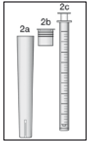
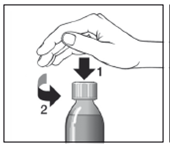
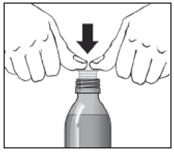
> 1 flacon(s) en verre brun de 150 ml avec seringue(s) pour administration orale
Code CIP : 329 563-9 ou 34009 329 563 9 5
Déclaration de commercialisation : 19/03/1992
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 3,47 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 4,49 €
- Taux de remboursement :65%
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 13/09/2017 | Renouvellement d'inscription (CT) | Le service médical rendu par les spécialités TEGRETOL et TEGRETOL LP reste important dans : • les épilepsies partielles avec ou sans généralisation secondaire et dans le traitement des épilepsies généralisées chez l’adulte et chez l’enfant en monothérapie ou en association à d’autres traitements antiépileptiques, • la prévention des rechutes dans le cadre des troubles bipolaires notamment chez les patients présentant une résistance relative, des contre-indications ou une intolérance au lithium et dans le traitement des états d'excitation maniaque ou hypomaniaque, • le traitement des névralgies du trijumeau et du glossopharyngien. |
| Modéré | Avis du 13/09/2017 | Renouvellement d'inscription (CT) | Le service médical rendu par TEGRETOL et TEGRETOL LP reste modéré dans le traitement des douleurs neuropathiques de l'adulte. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 19/07/2006 | Extension d'indication | Les spécialités TEGRETOL n'apportent pas d'amélioration du service médical rendu (niveau V) par rapport aux traitements médicamenteux habituellement utilisés dans la prise en charge des douleurs neuropathiques de l'adulte. |
Autres informations
- Titulaire de l'autorisation : NOVARTIS PHARMA SAS
- Conditions de prescription et de délivrance :
- à l'initiation du traitement et une fois par an
- délivrance ne pouvant se faire qu'après vérification de l'attestation co-signée
- liste II
- médicament nécessitant une surveillance particulière pendant le traitement
- pour enfants et adolescents de sexe féminin, femmes susceptibles de procréer et femmes enceintes : prescription initiale annuelle réservée à certains spécialistes
- prescription nécessitant la signature annuelle par le médecin et la patiente d'une attestation d'information
- Statut de l'autorisation : Valide
- Type de procédure : Procédure nationale
- Code CIS : 6 560 856 6
ANSM - Mis à jour le : 06/02/2026
TEGRETOL 20 mg/ml, suspension buvable
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Carbamazépine...................................................................................................................... 2,00 g
Pour 100 ml de suspension buvable.
1 ml de suspension correspond à 20 mg de carbamazépine.
Excipients à effet notoire : sorbitol (175 mg de sorbitol par ml de suspension), parahydroxybenzoate de méthyle (E218) (1,2 mg de parahydroxybenzoate de méthyle par ml de suspension), parahydroxybenzoate de propyle (0,3 mg de parahydroxybenzoate de propyle par ml de suspension) (E216), propylèneglycol (25 mg de propylèneglycol par ml de suspension).
Pour la liste complète des excipients, voir rubrique 6.1.
Suspension buvable.
4.1. Indications thérapeutiques
Epilepsies
Chez l’adulte
· soit en monothérapie ;
· soit en association à un autre traitement antiépileptique ;
· traitement des épilepsies partielles avec ou sans généralisation secondaire ;
· traitement des épilepsies généralisées : crises tonico-cloniques.
Chez l’enfant
· soit en monothérapie ;
· soit en association à un autre traitement antiépileptique ;
· traitement des épilepsies partielles avec ou sans généralisation secondaire ;
· traitement des épilepsies généralisées : crises tonico-cloniques.
Psychiatrie
· Prévention des rechutes dans le cadre des troubles bipolaires, notamment chez les patients présentant une résistance relative, des contre-indications ou une intolérance au lithium.
· Traitement des états d’excitation maniaque ou hypomaniaque.
Douleurs
· Traitement des névralgies du trijumeau et du glossopharyngien.
· Traitement des douleurs neuropathiques de l’adulte.
4.2. Posologie et mode d'administration
Enfants et adolescents de sexe féminin, femmes susceptibles de procréer
Des alternatives thérapeutiques doivent être envisagées chez les enfants et adolescents de sexe féminin et les femmes susceptibles de procréer. La nécessité du traitement par carbamazépine dans ces populations doit être réévaluée au moins une fois par an (voir rubriques 4.4 et 4.6).
Posologie
Posologie strictement individuelle selon la réponse clinique, à administrer en 2 ou 3 prises dans la journée.
La prescription de TEGRETOL suspension buvable doit être rédigée en millilitres (se reporter au tableau de conversion ci-après qui donne la posologie en milligrammes et en millilitres). La dose prescrite en mL doit être arrondie au 0,25 mL le plus proche.
|
Dose en milligrammes |
Dose en millilitres |
|
20 mg |
1,00 mL |
|
25 mg |
1,25 mL |
|
30 mg |
1,50 mL |
|
35 mg |
1,75 mL |
|
40 mg |
2,00 mL |
|
45 mg |
2,25 mL |
|
50 mg |
2,50 mL |
|
55 mg |
2,75 mL |
|
60 mg |
3,00 mL |
|
65 mg |
3,25 mL |
|
70 mg |
3,50 mL |
|
75 mg |
3,75 mL |
|
80 mg |
4,00 mL |
|
85 mg |
4,25 mL |
|
90 mg |
4,50 mL |
|
95 mg |
4,75 mL |
|
100 mg |
5,00 mL |
|
200 mg |
10,00 mL |
|
300 mg |
15,00 mL |
|
400 mg |
20,00 mL |
|
500 mg |
25,00 mL |
|
600 mg |
30,00 mL |
|
700 mg |
35,00 mL |
|
800 mg |
40,00 mL |
|
900 mg |
45,00 mL |
|
1000 mg |
50,00 mL |
|
1200 mg |
60,00 mL |
Une recherche des allèles HLA-B*1502 et HLA-A*3101 devrait être effectuée autant que possible avant instauration d’un traitement par la carbamazépine chez certains patients (voir rubrique 4.4).
Une recherche de l’allèle HLA B*1502 devrait être effectuée autant que possible avant instauration d’un traitement par carbamazépine chez les sujets d’origines Thaïlandaise ou chinoise Han car cet allèle prédit fortement le risque grave de syndromes de Steven Johnson associé à la carbamazépine (voir rubrique 4.4).
Epilepsies
La mise en place du traitement se fait de façon progressive, par paliers de 2 à 5 jours, de façon à atteindre la dose optimale en 2 semaines environ.
Chez l’adulte
10 à 15 mg/kg/jour en moyenne, en 2 ou 3 prises.
Population pédiatrique
Pour les enfants âgés de 4 ans ou moins, la dose initiale est de 20 à 60 mg/jour en augmentant la dose de 20 à 60 mg tous les 2 jours.
Pour les enfants âgés de plus de 4 ans, la dose initiale peut être de 100 mg/jour en augmentant la dose de 100 mg toutes les semaines.
Dose d’entretien : 10 à 20 mg/kg/jour en moyenne, à répartir en plusieurs prises au cours de la journée.
Dose maximale recommandée : La dose maximale recommandée est de 35 mg/kg/jour pour un enfant de moins de 6 ans, de 1000 mg/jour pour un enfant âgé de 6 à 15 ans et de 1200 mg/jour à partir de 16 ans.
Lorsque l’on substitue la carbamazépine à un autre antiépileptique, réduire graduellement la dose de ce dernier.
Une monothérapie antiépileptique est recommandée chaque fois que possible. Le traitement antiépileptique doit être administré quotidiennement et de façon prolongée parfois indéfiniment.
La prescription de carbamazépine nécessite une surveillance régulière. Toute modification posologique, toute substitution médicamenteuse doit s’effectuer très progressivement (voir rubrique 4.4).
La dose de carbamazépine doit être adaptée aux besoins de chaque patient pour atteindre un contrôle suffisant des crises épileptiques. L’établissement de la dose optimale de carbamazépine peut être rendu plus aisé par le dosage plasmatique, en particulier en cas de polythérapie antiépileptique. Dans le traitement de l’épilepsie, la dose efficace nécessite généralement d’atteindre des concentrations plasmatiques totales de carbamazépine comprises entre 4 et 12 microgrammes/mL (17 à 50 micromoles/L) (voir rubrique 5.1).
Psychiatrie
· Prévention des rechutes dans le cadre des troubles bipolaires :
400 à 800 mg/jour en 2 ou 3 prises.
· Traitement des états d’excitation maniaques ou hypomaniaques :
600 à 1200 mg/jour en 2 ou 3 prises.
Douleurs
La posologie initiale est de 200 à 400 mg/jour, en 2 ou 3 prises.
Augmenter les doses jusqu’à suppression de la douleur.
Dans la névralgie du trijumeau ou du glossopharyngien, la dose maximale recommandée est de 1200 mg/jour. Lorsque la douleur est soulagée, l’arrêt progressif du traitement doit être réalisé, jusqu’à la survenue d’un nouvel épisode douloureux.
Populations spéciales
Sujets âgés (65 ans ou plus)
En raison de possible interactions médicamenteuses et des différences de propriétés pharmacocinétiques entre les antiépileptiques, la posologie de TEGRETOL doit être choisie avec prudence chez le sujet âgé.
Chez le sujet âgé, il est recommandé d’initier le traitement à la dose de 100 mg deux fois par jour. Cette dose initiale peut être augmentée légèrement chaque jour jusqu’au soulagement de la douleur (habituellement obtenu à 200 mg 3 à 4 fois par jour). La dose doit ensuite être progressivement réduite à une dose d’entretien la plus faible possible.
Insuffisance rénale/insuffiance hépatique
Il n’existe pas de données concernant la pharmacocinétique de la carbamazépine chez les patients insuffisants rénaux ou hépatiques.
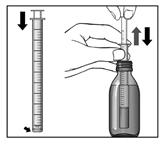
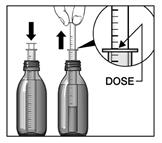
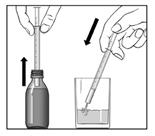
Mode d’administration
Avaler la suspension, pendant ou après le repas, avec un peu d’eau.
· Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
· Bloc auriculo-ventriculaire.
· Antécédents d’hypoplasie médullaire.
· Antécédents de porphyrie hépatique (ex : porphyrie aiguë intermittente, porphyrie variegata, porphyrie cutanée tardive).
· Traitement par le cobicistat, le dasabuvir, le délamanid, l’association grazoprevir + elbasvir, l’isavuconazole, le lédipasvir, la lurasidone, la midostaurine, l’association ombitasvir + paritaprévir, la rilpivirine, le sofosbuvir, le velpatasvir, le voriconazole (voir rubrique 4.5).
· Nouveau-nés de moins de 4 semaines nés à terme (ou les prématurés de moins de 44 semaines d'âge post-menstruel), sauf en l'absence d'alternative thérapeutique et dans le cas où le bénéfice du traitement est supérieur au risque, tout en prenant en compte les risques associés aux excipients (voir rubrique 4.4).
4.4. Mises en garde spéciales et précautions d'emploi
Mises en garde spéciales
Tout patient prenant ce médicament doit être informé que l’apparition de fièvre, d’un mal de gorge, d’autres infections, d'éruption cutanée, d'ulcérations buccales, d'apparition spontanée d'ecchymoses, de purpura ou de pétéchies, de nausées, d'ictère et d'hépatomégalie, impose d’avertir tout de suite le médecin traitant et de contrôler immédiatement l’hémogramme (voir Précautions d’emploi).
Réactions dermatologiques sévères
Des réactions dermatologiques sévères et parfois fatales incluant des Nécroses Epidermiques Toxiques (NET appelé également syndrome de Lyell) et des syndromes de Stevens Johnson (SJS) ont été rapportées très rarement avec TEGRETOL. Les patients devront être informés des signes et symptômes et devront surveiller étroitement toute réaction cutanée. Si des signes ou symptômes évocateurs d’un SJS ou d’un NET apparaissent (p.ex. éruption progressive, souvent associée à des cloques ou à des lésions des muqueuses), TEGRETOL doit être arrêté immédiatement.
Les meilleurs résultats lors de la prise en charge d’un SJS ou d’une NET sont liés à un diagnostic précoce et à un arrêt immédiat du médicament suspecté. L’arrêt précoce du médicament est associé à un meilleur pronostic.
Si le patient a développé un SJS ou une NET sous carbamazépine, aucun médicament contenant de la carbamazépine ne devra être réintroduit chez ce patient, et ce tout au long de sa vie.
La survenue, en début de traitement, d’un érythème généralisé fébrile associé à des pustules doit faire suspecter une pustulose exanthématique généralisée (voir rubrique 4.8) ; elle impose l’arrêt du traitement et contre-indique toute nouvelle administration de TEGRETOL et des spécialités contenant de la carbamazépine.
L’apparition de ces réactions est estimée à 1-6 pour 10 000 nouveaux patients exposés dans les pays où la population Caucasienne est prépondérante, mais le risque dans certains pays d’Asie est estimé comme 10 fois plus important.
Pharmacogénomique
II existe de plus en plus de données mettant en évidence le rôle des différents allèles HLA (antigène leucocytaire humain) chez les patients prédisposés aux réactions indésirables à médiation immunitaire.
Les fréquences alléliques citées ici représentent le pourcentage de chromosomes porteurs de l’allèle d’intérêt dans la population spécifiée. Ceci signifie que le pourcentage des patients porteurs d’une copie de l’allèle sur au moins un de leur deux chromosomes (c’est-à-dire la « fréquence des porteurs ») est presque deux fois plus élevé que la fréquence allélique. Ainsi, le pourcentage des patients potentiellement à risque est presque le double de la fréquence de l’allèle.
Association avec HLA-B*1502 chez les populations d’origine thaïlandaise, Chinoise Han et d’Asie du Sud-Est
Il a été observé que la présence de l’allèle HLA B*1502 chez les sujets d’origine thaïlandaise ou Chinoise Han était fortement associée au risque de réaction cutanée sévère de type SJS ou NET lors d’un traitement par la carbamazépine. La fréquence de l’allèle HLA B*1502 est autour de 8% chez les sujets d’origine thaïlandaise et est comprise entre 2 et 12% dans la population Chinoise Han.
Il est recommandé d’effectuer, dans la mesure du possible, une recherche de cet allèle chez ces sujets avant l’instauration d’un traitement par carbamazépine (voir rubrique 4.2). Si le résultat de ce test est positif, la carbamazépine ne devrait pas être instaurée chez ces patients, à l’exception des situations où aucune autre alternative thérapeutique n’est envisageable.
Les patients pour lesquels la recherche de l’allèle HLA B*1502 est négative ont un risque faible de développer une réaction de type SJS ou Lyell, mais ce risque ne doit pas être négligé car ces réactions bien que rares peuvent toujours survenir.
Il existe des données suggérant une majoration du risque de SJS ou NET associés à la carbamazépine chez les populations asiatiques. Du fait de la fréquence de cet allèle chez les autres populations asiatiques (p.ex. plus de 15% aux Philippines et dans certaines populations de Malaisie, jusqu’à 2 et 6% en Corée et en Inde, respectivement), le test génétique détectant l’allèle HLA-B*1502 doit être envisagé chez ces populations à risque.
La fréquence de l’allèle HLA-B*1502 est négligeable dans les populations échantillonnées d’origine européenne et hispanique, certaines populations africaines, les populations natives d’Amérique et chez les japonais (<1%).
Association avec HLA-A*3101 chez les populations d’origine européenne et japonaise
Il existe des données suggérant que l’allèle HLA-A*3101 est associé à une majoration du risque de réactions cutanées induites par la carbamazépine incluant SJS, NET, DRESS (syndrome d’hypersensibilité médicamenteuse avec éosinophilie et symptômes systémiques), ou PEAG (pustulose exanthématique aiguë généralisée) ou éruption maculopapulaire (voir rubrique 4.8) chez les populations d’origine européenne et japonaise. Toutefois, les données sont insuffisantes pour recommander un dépistage de l’allèle HLA-A*3101 avant l’instauration du traitement.
La fréquence de l’allèle HLA-A*3101 varie considérablement selon les populations ethniques. L’allèle HLA-A*3101 a une fréquence de 2 à 5% dans les populations européennes et environ 10% dans la population japonaise.
La présence de l’allèle HLA-A*3101 peut augmenter le risque de réactions cutanées (généralement moins sévères) de 5,0% dans la population générale à 26,0% chez les sujets originaires du Nord de l’Europe, alors que son absence peut réduire le risque de 5,0% à 3,8 %. Si les patients d’origine européenne ou japonaise sont connus pour être positifs pour l’allèle HLA-A*3101, l’utilisation de la carbamazépine peut être envisagée si le bénéfice prévaut sur le risque encouru.
Réactions d’hypersensibilité
La carbamazépine peut également entraîner un syndrome DRESS (syndrome d’hypersensibilité médicamenteuse avec éosinophilie et symptômes systémiques), hypersensibilité multi-viscérale retardée pouvant être accompagnée de fièvre, rash, vascularite, polyadénopathie, pseudo-lymphome, arthralgie, leucopénie, éosinophilie, hépatosplénomégalie, troubles de la fonction hépatique et syndrome de disparition des canaux biliaires (destruction et disparition des canaux intrahépatiques biliaires). D’autres organes peuvent également être affectés (ex : poumons, reins, pancréas, myocarde, colon) (voir rubrique 4.8).
Chez les patients présentant de telles réactions, le traitement par la carbamazépine doit être interrompu et un traitement alternatif doit être démarré.
L’existence de rares cas de réactions croisées entre la carbamazépine et les médicaments antiépileptiques aromatiques tels que la phénytoïne, la primidone et le phénobarbital doit rendre prudent le remplacement de la carbamazépine par l’une ou l’autre de ces molécules.
Des réactions d’hypersensibilité croisée sont décrites entre la carbamazépine et l’oxcarbazépine.
L’agranulocytose et l’anémie aplasique ont été associées à la carbamazépine. Cependant, compte tenu de la très faible fréquence de ces troubles, il est difficile d’obtenir une estimation significative du risque. Le risque global dans la population générale non traitée a été estimé à 4,7 personnes par million et par an pour l’agranulocytose et à 2,0 personnes par million et par an pour l’anémie aplasique.
Avant toute instauration d'un traitement par la carbamazépine, un hémogramme, une numération des plaquettes et un bilan biologique avec dosage du fer et des électrolytes doivent être pratiqués. La formule sanguine doit être pratiquée une fois par mois au cours des cinq premiers mois, puis 2 à 4 fois par an. La surveillance clinique est primordiale pendant toute la durée du traitement. L'administration de carbamazépine doit être interrompue en cas d'apparition de leucopénie ou de thrombopénie sévères.
Une diminution temporaire ou durable du nombre de leucocytes ou de thrombocytes se produit fréquemment avec l’utilisation de la carbamazépine. Ces effets sont cependant de nature passagère dans la majorité des cas, et il est peu probable qu’ils soient le signe du développement d’une anémie aplasique ou d’une agranulocytose. Le traitement par carbamazépine doit cependant être interrompu en cas de survenue d’une leucopénie sévère (principalement une neutropénie) ou d’une thrombopénie accompagnée de manifestations cliniques, par exemple une fièvre ou un mal de gorge.
La carbamazépine doit également être arrêtée en cas d’apparition de signes de dépression médullaire importante.
En présence d'affections cardiovasculaires, d'affections hépatiques ou rénales sévères et chez le sujet âgé, une surveillance rapprochée est nécessaire. La posologie doit être adaptée à chaque cas.
Crises d’épilepsie
La carbamazépine n’est pas efficace dans les absences et les crises myocloniques qui peuvent parfois être aggravées.
L’introduction d’un médicament antiépileptique peut, rarement, être suivie d’une recrudescence des crises ou de l’apparition d’un nouveau type de crise chez le patient, et ce indépendamment des fluctuations observées dans certaines maladies épileptiques. En ce qui concerne la carbamazépine, les causes de ces aggravations peuvent être : un choix de médicament mal approprié vis-à-vis des crises ou du syndrome épileptique du patient, une modification du traitement antiépileptique concomitant ou une interaction pharmacocinétique avec celui-ci, une toxicité ou un surdosage. Il peut ne pas y avoir d’autre explication qu’une réaction paradoxale.
Fonction hépatique
Un bilan hépatique sera réalisé avant le début du traitement, une fois par semaine le premier mois, puis devant tout signe clinique d’appel.
Hyponatrémie
Il est bien établi qu’une hyponatrémie peut survenir avec la carbamazépine. Chez les patients présentant une atteinte rénale prééxistante avec une natrémie basse ou chez les patients traités de façon concomitante avec des médicaments hyponatrémiants (ex : les diurétiques, les médicaments associés à une sécrétion inappropriée d’hormone anti-diurétique [ADH]), la natrémie doit être mesurée avant l’initiation d’un traitement par la carbamazépine puis renouvelée environ 2 semaines après et ensuite à intervalles d’un mois durant les trois premiers mois de traitement, ou selon l’état clinique du patient. Ces facteurs de risques concernent particulièrement les patients âgés. Lorsqu’une hyponatrémie est observée, la restriction hydrique est une mesure corrective majeure si la situation clinique l’indique.
Hypothyroïdie
Chez les patients ayant une hypothyroïdie, la carbamazépine peut réduire les concentrations plasmatiques d’hormones thyroïdiennes, via une induction enzymatique, nécessitant une augmentation de la posologie de l’hormonothérapie thyroïdienne substitutive. Un contrôle de la fonction thyroïdienne est recommandé afin d’ajuster la posologie de l’hormonothérapie thyroïdienne substitutive.
Risque suicidaire
Des idées et comportements suicidaires ont été rapportés chez des patients traités par des antiépileptiques dans plusieurs indications. Une méta-analyse d’essais randomisés, contrôlés versus placebo portant sur des antiépileptiques a également montré une légère augmentation du risque d’idées et de comportements suicidaires. Les causes de ce risque ne sont pas connues et les données disponibles n’excluent pas la possibilité d’une augmentation de ce risque pour la carbamazépine.
Par conséquent les patients doivent être étroitement surveillés pour tout signe d’idées et de comportements suicidaires et un traitement approprié doit être envisagé. Il doit être recommandé aux patients (et leur personnel soignant) de demander un avis médical en cas de survenue de signes d’idées et de comportements suicidaires.
Enfants et adolescents de sexe féminin, femmes susceptibles de procréer et femmes enceintes
La carbamazépine peut provoquer des lésions fœtales lorsqu’elle est administrée à une femme enceinte. L’exposition prénatale à la carbamazépine peut augmenter les risques de malformations congénitales majeures et d’autres effets indésirables sur le développement (voir rubrique 4.6).
Femmes susceptibles de procréer
La carbamazépine ne doit pas être utilisée chez les femmes susceptibles de procréer, à moins que le bénéfice ne soit jugé supérieur aux risques après un examen attentif des alternatives thérapeutiques disponibles.
Les femmes susceptibles de procréer doivent être pleinement informées du risque potentiel pour le fœtus de l’utilisation de la carbamazépine pendant la grossesse.
Un test de grossesse doit être réalisé avant l’instauration du traitement par carbamazépine chez une femme susceptible de procréer.
Lors de l’initiation du traitement, et une fois par an, le médecin doit s’assurer que le traitement par carbamazépine est la meilleure option pour la patiente et signer avec elle une attestation d’information partagée.
Les femmes susceptibles de procréer doivent utiliser une contraception efficace pendant le traitement et jusqu’à deux semaines après l’arrêt du traitement. En raison de l’effet inducteur enzymatique de la carbamazépine, le traitement par carbamazépine peut conduire à un échec des contraceptifs hormonaux. Par conséquent, les femmes susceptibles de procréer doivent être conseillées sur l’utilisation d’autres méthodes contraceptives efficaces (voir rubriques 4.5 et 4.6).
Les femmes susceptibles de procréer doivent être informées sur la nécessité de consulter leur médecin dès qu’elles envisagent une grossesse afin de discuter du recours à d’autres traitements antiépileptiques alternatifs avant la conception et avant l’interruption de la contraception (voir rubrique 4.6).
Il faut conseiller aux femmes susceptibles de procréer traitées par de la carbamazépine de contacter immédiatement leur médecin si elles sont enceintes ou si elles pensent l’être.
Enfants et adolescents de sexe féminin
Les prescripteurs doivent s’assurer que les parents / tuteurs des enfants et adolescents de sexe féminin traités par carbamazépine comprennent la nécessité de contacter un spécialiste aussitôt que les premières menstruations surviennent (ménarche). La patiente et ses parents / tuteurs devront alors recevoir des informations complètes sur les risques liés à l’exposition in utero à la carbamazépine et sur la nécessité d’utiliser une contraception hautement efficace dès que nécessaire. La nécessité de poursuivre le traitement par carbamazépine devra être réévaluée et des alternatives thérapeutiques devront être également envisagées.
Surveillance des taux plasmatiques
La survenue d’effets indésirables spécifiques au SNC peut être due à un surdosage relatif ou à une variation significative des taux plasmatiques. Dans de tels cas, il est conseillé de surveiller les taux plasmatiques (voir rubriques 4.8 et 4.9).
Diminution de la dose et effets du sevrage
L’arrêt brutal de la carbamazépine peut précipiter les crises, par conséquent la carbamazépine doit être arrêtée progressivement sur une période de 6 mois. Selon les cas, un traitement transitoire par un antiépileptique à effet rapide peut s’avérer nécessaire.
Interactions médicamenteuses (voir rubrique 4.5)
L’association de carbamazépine est déconseillée avec l’abiratérone, apixaban, aprémilast, aprépitant, bédaquiline, bictégravir, bosentan, clozapine, cyclophosphamide, cyprotérone, dabigatran, docétaxel, dolutégravir, dronédarone, érythromycine, estroprogestatifs et progestatifs (contraceptifs), étoposide, fentanyl, idélalisib, inhibiteurs de la 5-alpha réductase, inhibiteurs de tyrosines kinases métabolisés, irinotécan, isoniazide, itraconazole, ivacaftor, lithium, macitentan, mianserine, millepertuis, naloxégol, nimodipine, olaparib, oxycodone, paclitaxel, pamplemousse (jus et fruit), praziquantel, quétiapine, ranolazine, régorafenib, rivaroxaban, rolapitant, sertraline, simvastatine, télithromycine, ténofovir alafénamide, ticagrelor, tramadol, ulipristal, vémurafénib, vinca-alcaloides cytotoxiques, vismodégib.
Chutes
Le traitement par TEGRETOL a été associé aux effets indésirables suivants : ataxie, sensations vertigineuses, somnolence, hypotension, état confusionnel, sédation (voir rubrique 4.8), pouvant entrainer des chutes et par conséquent des fractures ou autres blessures. Chez les patients dont la maladie ou la prise de médicaments est susceptible d’exacerber ces effets, une analyse complète du risque de chute devra être régulièrement effectuée en cas de traitement au long cours par TEGRETOL.
Excipients à effet notoire
Ce médicament contient moins de 1 mmol (23 mg) de sodium par dose, c’est-à-dire qu’il est essentiellement « sans sodium ».
Ce médicament contient 175 mg de sorbitol par ml de suspension.
Le sorbitol est une source de fructose. Son utilisation est déconseillée chez les patients présentant une intolérance à certains sucres ou ayant une intolérance héréditaire au fructose (IHF), un trouble génétique rare caractérisé par l'incapacité à décomposer le fructose. Il convient de tenir compte de l'effet additif des produits contenant du sorbitol (ou du fructose) administrés de façon concomitante ainsi que l'apport alimentaire en sorbitol (ou en fructose). Le sorbitol et le propylène glycol contiennent comme solvant résiduels de l'éthylène glycol et du diéthylène glycol. Les métabolites de l'éthylène glycol peuvent provoquer une acidose métabolique et des lésions rénales.
Le sorbitol peut causer une gêne gastro-intestinale et un effet laxatif léger.
Ce médicament contient du parahydroxybenzoate de méthyle (E218) et du parahydroxybenzoate de propyle (E216) et peut provoquer des réactions allergiques (éventuellement retardées).
Ce médicament contient 25 mg de propylène glycol par ml de suspension. La suspension buvable de Tegretol ne doit pas être utilisée chez les nouveau-nés de moins de 4 semaines nés à terme (ou les prématurés de moins de 44 semaines d'âge post-menstruel), sauf en l'absence d'alternative thérapeutique (voir rubrique 4.3).
Les doses de propylène glycol ≥1mg/kg/jour augmentent le risque d'accumulation d'excipients chez les nouveau-nés en raison de l'immaturité des clairances métabolique et rénale dans cette population. Ceci peut entrainer des effets indésirables graves tels qu'une acidose métabolique, un trouble de la fonction rénale (nécrose tubulaire aiguë), une insuffisance rénale aiguë et un trouble de la fonction hépatique. Une surveillance médicale, incluant la mesure du trou osmolaire et/ou anionique, est recommandée chez les nouveau-nés âgés de moins de 4 semaines. L'administration concomitante d'autres médicaments contenant du propylène glycol ou de tout substrat de l'alcool déshydrogénase, tel que l'éthanol, augmente le risque d'accumulation et de toxicité du propylène glycol. L'éthylène glycol ainsi que le diéthylène glycol présents dans le médicament (voir ci-dessous) sont également des substrats de l'alcool désydrogénase.
L’administration concomitante avec n’importe quel substrat pour l’alcool déshydrogénase comme l’éthanol ou le propylène glycol peut induire des effets indésirables graves chez les nouveau-nés.
Précautions d’emploi
· La carbamazépine ne doit être utilisée que sous surveillance médicale stricte.
· Surveillance particulière en cas de glaucome, de rétention urinaire, d’affections hépatiques ou rénales, d’insuffisance cardiaque et chez les sujets âgés. La posologie de carbamazépine doit être adaptée à chaque cas.
· L’administration de la carbamazépine sera interrompue en cas de manifestations cutanées allergiques, d’altération de la fonction hépatique ou de modification franche de l’hémogramme faisant craindre l’apparition d’une agranulocytose ou d’une aplasie médullaire (rares).
· La prise de boissons alcoolisées est formellement déconseillée, la carbamazépine risquant d’en majorer les effets.
· Le médicament ne devra pas être administré à une dose supérieure à 200 mg par jour aux enfants de moins de 3 ans et, plus généralement, à dose élevée sans une étude préalable de la tolérance individuelle (voir rubrique 4.2).
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Étant donné que des taux plasmatiques élevés de carbamazépine-10,11-époxide peuvent entraîner des effets indésirables (par exemple, vertiges, somnolence, ataxie, diplopie), la dose de carbamazépine doit être ajustée en conséquence et/ou les taux plasmatiques doivent être surveillés en cas d’utilisation concomitante avec les substances décrites ci-dessous :
Antiépileptiques : progabide, acide valproïque, valnoctamide, valpromide, primidone, brivaracétam.
Associations contre-indiquées (voir rubrique 4.3)
+ Cobicistat
Risque de diminution de l’efficacité du cobicistat par augmentation de son métabolisme par la carbamazépine.
+ Dasabuvir
Risque de diminution des concentrations plasmatiques du dasabuvir par la carbamazépine.
+ Délamanid
Diminution des concentrations plasmatiques de délamanid par augmentation de son métabolisme hépatique par la carbamazépine.
+ Grazoprevir + Elbasvir
Risque de diminution des concentrations de grazoprévir et d’elbasvir par la carbamazépine, avec possible retentissement sur l’efficacité.
+ Isavuconazole
Diminution des concentrations plasmatiques d’isavuconazole par augmentation de son métabolisme hépatique par la carbamazépine.
+ Lédipasvir
Diminution importante des concentrations plasmatiques du lédipasvir par augmentation de son métabolisme hépatique par la carbamazépine.
+ Lurasidone
Diminution des concentrations plasmatiques de la lurasidone par augmentation de son métabolisme hépatique par la carbamazépine.
+ Midostaurine
Diminution des concentrations de midostaurine par la carbamazépine.
+ Ombitasvir + Paritaprévir
Diminution des concentrations plasmatiques de la bithérapie par augmentation de son métabolisme hépatique par la carbamazépine.
+ Rilpivirine
Diminution significative des concentrations plasmatiques de rilpivirine par augmentation de son métabolisme hépatique par la carbamazépine.
+ Sofosbuvir
Risque de diminution des concentrations plasmatiques de sofosbuvir par diminution de son absorption intestinale par la carbamazépine.
+ Velpatasvir
Diminution des concentrations plasmatiques de velpatasvir par la carbamazépine, avec possible retentissement sur l’efficacité.
+ Voriconazole
Risque de baisse de l’efficacité du voriconazole par augmentation de son métabolisme hépatique par la carbamazépine.
Associations déconseillées
+ Abiratérone
Diminution notable des concentrations plasmatiques de l’abiratérone, avec risque de moindre efficacité.
+ Apixaban
Diminution des concentrations plasmatiques de l’apixaban par la carbamazépine, avec risque de diminution de l’effet thérapeutique.
+ Aprémilast
Diminution des concentrations plasmatiques d’aprémilast par diminution de son métabolisme par la carbamazépine.
+ Aprépitant
Risque de diminution très importante des concentrations d’aprépitant.
+ Bédaquiline
Diminution des concentrations plasmatiques de bédaquiline par augmentation de son métabolisme par la carbamazépine.
+ Bictégravir
Risque de perte d’efficacité par diminution, éventuellement importante, des concentrations de bictégravir.
+ Bosentan
Risque de diminution des concentrations plasmatiques de bosentan.
+ Clozapine
Diminution des concentrations plasmatiques de clozapine avec risque de perte d’efficacité.
Risque de majoration des effets hématologiques graves.
+ Cyclophosphamide
Risque d’augmentation des concentrations plasmatiques du métabolite actif du cyclophosphamide par la carbamazépine, et donc de sa toxicité.
+ Cyprotérone (+ voir Associations faisant l’objet de précautions d’emploi)
Risque de diminution de l'efficacité de la cyprotérone.
Association déconseillée dans son utilisation comme contraceptif hormonal: utiliser de préférence une autre méthode de contraception en particulier de type mécanique, pendant la durée de l'association et un cycle suivant.
+ Dabigatran
Diminution des concentrations plasmatiques de dabigatran, avec risque de diminution de l’effet thérapeutique.
+ Docetaxel
Diminution des concentrations du cytotoxique par augmentation de son métabolisme par la carbamazépine, avec risque de moindre efficacité.
+ Dolutégravir (+ voir Associations faisant l’objet de précautions d’emploi)
Diminution des concentrations plasmatiques de dolutégravir par augmentation de son métabolisme par la carbamazépine.
Association déconseillée en cas de résistance à la classe des inhibiteurs d'intégrase.
+ Dronédarone
Diminution importante des concentrations de dronadérone par augmentation de son métabolisme, sans modification notable du métabolite actif.
+ Erythromycine
Augmentation des concentrations plasmatiques de carbamazépine avec signes de surdosage par inhibition de son métabolisme hépatique.
+ Estroprogestatifs et progestatifs (contraceptifs)
Diminution de l’efficacité contraceptive, par augmentation du métabolisme hépatique du contraceptif hormonal par la carbamazépine.
Si l’association s’avère nécessaire, utiliser une méthode additionnelle de contraception, de type mécanique (par exemple un préservatif) pendant la durée du traitement par carbamazépine, et pendant un cycle menstruel suivant l’arrêt de la carbamazépine.
+ Etoposide
Diminution des concentrations plasmatiques d’étoposide par la carbamazépine.
Si l'association s'avère nécessaire, surveillance clinique et adaptation éventuelle de la posologie d’étoposide pendant l’association, et 1 à 2 semaines après l’arrêt de la carbamazépine.
+ Fentanyl
Diminution des concentrations plasmatiques de fentanyl par augmentation de son métabolisme hépatique par la carbamazépine.
Préférer un autre morphinique.
+ Idélalisib
Diminution des concentrations plasmatiques d’idélalisib par augmentation de son métabolisme hépatique par la carbamazépine.
+ Inhibiteurs de la 5-alpha réductase
Diminution des concentrations plasmatiques de l’inhibiteur de la 5- alpha réductase par la carbamazépine.
Si l’association ne peut être évitée, surveillance clinique étroite.
+ Inhibiteurs des tyrosines kinases métabolisés
Diminution des concentrations plasmatiques et de l’efficacité de l’inhibiteur de tyrosine kinase, par augmentation de son métabolisme par la carbamazépine.
+ Irinotécan
Diminution probable des concentrations plasmatiques du métabolite actif de l'irinotécan, avec risque d'échec du traitement cytotoxique.
+ Isoniazide
Augmentation des concentrations plasmatiques de carbamazépine avec signes de surdosage par inhibition de son métabolisme hépatique.
+ Itraconazole
Diminution des concentrations plasmatiques d’itraconazole, avec risque de perte d’efficacité, par augmentation de son métabolisme hépatique par la carbamazépine.
+ Ivacaftor
Diminution importante des concentrations de l’ivacaftor, avec risque de perte d’efficacité.
+ Lithium
Risque de neurotoxicité se manifestant par des troubles cérébelleux, confusion, somnolence, ataxie. Ces troubles sont réversibles à l’arrêt du traitement par le lithium.
+ Macitentan
Diminution des concentrations plasmatiques de macitentan par augmentation de son métabolisme par la carbamazépine.
+ Miansérine
Risque d’inefficacité de la miansérine.
+ Millepertuis
Risque de diminution des concentrations plasmatiques et de l’efficacité de la carbamazépine.
+ Naloxégol
Diminution des concentrations de naloxégol par la carbamazépine.
+ Nimodipine
Diminution des concentrations plasmatiques de l’antagoniste du calcium par augmentation de son métabolisme hépatique par la carbamazépine.
Surveillance clinique et adaptation éventuelle de la posologie de l’antagoniste du calcium pendant le traitement par la carbamazépine et après son arrêt.
+ Olaparib
Diminution des concentrations plasmatiques de l’olaparib par augmentation de son métabolisme hépatique par la carbamazépine.
+ Oxycodone
Diminution des concentrations plasmatiques de l’oxycodone par augmentation de son métabolisme par la carbamazépine.
Adaptation éventuelle de la posologie d’oxycodone.
+ Paclitaxel
Diminution des concentrations du cytotoxique par augmentation de son métabolisme par la carbamazépine, avec risque de moindre efficacité.
+ Pamplemousse (jus et fruit)
Augmentation des concentrations plasmatiques de carbamazépine, avec risque de surdosage, par inhibition de son métabolisme par le pamplemousse.
+ Praziquantel
Diminution très importante des concentrations plasmatiques du praziquantel, avec risque d’échec du traitement, par augmentation de son métabolisme hépatique par la carbamazépine.
+ Quétiapine
Diminution très importante des concentrations plasmatiques de quétiapine par augmentation de son métabolisme hépatique par la carbamazépine, avec risque d’inefficacité.
+ Ranolazine
Risque de diminution importante des concentrations de ranolazine.
+ Régorafénib
Diminution des concentrations plasmatiques de régorafenib par augmentation de son métabolisme par la carbamazépine.
+ Rivaroxaban
Diminution des concentrations plasmatiques de rivaroxaban, avec risque de diminution de l'effet thérapeutique.
+ Rolapitant
Diminution très importante des concentrations de rolapitant avec risque de perte d’efficacité.
+ Sertraline
Risque d’inefficacité du traitement antidépresseur.
+ Simvastatine
Diminution importante des concentrations plasmatiques de simvastatine, par augmentation de son métabolisme hépatique.
+ Télithromycine
Diminution des concentrations plasmatiques de la télithromycine, avec risque d’échec du traitement anti-infectieux, par augmentation de son métabolisme hépatique par la carbamazépine.
+ Ténofovir alafénamide
Diminution des concentrations plasmatiques du ténofovir alafénamide par diminution de son absorption par la carbamazépine.
Si l'association ne peut être évitée, surveillance clinique pendant l’association et 1 à 2 semaines après l’arrêt de la carbamazépine.
+ Ticagrelor
Diminution importante des concentrations plasmatiques de ticagrelor par augmentation de son métabolisme hépatique par la carbamazépine, avec risque de diminution de l’effet thérapeutique.
+ Tramadol
Risque de diminution des concentrations plasmatiques du tramadol.
+ Ulipristal
Risque de diminution de l’effet de l’ulipristal, par augmentation de son métabolisme hépatique par la carbamazépine.
Préférer une alternative thérapeutique peu ou pas métabolisée.
+ Vémurafénib
Risque de diminution des concentrations du vémurafénib, avec moindre efficacité.
+ Vinca-alcaloïdes cytotoxiques
Diminution des concentrations plasmatiques du vinca-alcaloïde par la carbamazépine, avec possible retentissement sur l’efficacité.
+ Vismodégib
Risque de diminution des concentrations plasmatiques de vismodégib par augmentation de son métabolisme hépatique par la carbamazépine.
Associations faisant l'objet de précautions d’emploi
+ Acétazolamide
Augmentation des concentrations plasmatiques de carbamazépine avec signes de surdosage.
Surveillance clinique et, si besoin, contrôle des concentrations plasmatiques de carbamazépine et réduction éventuelle de sa posologie.
+ Acide valproïque et, par extrapolation, valpromide
Augmentation des concentrations plasmatiques du métabolite actif de la carbamazépine avec signes de surdosage. De plus, diminution des concentrations plasmatiques d’acide valproïque par augmentation de son métabolisme hépatique par la carbamazépine.
Surveillance clinique, dosages plasmatiques et adaptation de la posologie des deux anticonvulsivants.
+ Afatinib
Diminution des concentrations plasmatiques de l’afatinib par augmentation de son métabolisme par la carbamazépine.
Surveillance clinique pendant l’association et 1 à 2 semaines après arrêt de la carbamazépine.
+ Albendazole
Diminution importante des concentrations plasmatiques de l’albendazole et de son métabolite actif par la carbamazépine, avec risque de baisse de son efficacité.
Surveillance clinique de la réponse thérapeutique et adaptation éventuelle de la posologie de l’albendazole pendant le traitement avec la carbamazépine et après son arrêt.
+ Aminosides (en cas d’administration chronique de carbamazépine)
Potentialisation des curares lorsque l’antibiotique est administré par voie parentérale et/ou péritonéale avant, pendant ou après l’agent curarisant.
Surveiller le degré de curarisation en fin d’anesthésie.
+ Androgènes
Risque de diminution des concentrations plasmatiques de l'androgène et par conséquent de son efficacité, par augmentation de son métabolisme hépatique par la carbamazépine.
Surveillance clinique et biologique pendant l’association et 1 à 2 semaines après l’arrêt de la carbamazépine.
+ Antagonistes des canaux calciques (voir association déconseillée pour la nimodipine)
Diminution des concentrations plasmatiques de l’antagoniste du calcium par augmentation de son métabolisme hépatique.
Surveillance clinique et adaptation éventuelle de la posologie de l’antagoniste du calcium pendant le traitement par la carbamazépine et après son arrêt.
+ Antiarythmiques classe IA (disopyramide, hydroquinidine, quinidine)
Diminution des concentrations plasmatiques et de l’efficacité de l’antiarythmique, par augmentation de son métabolisme hépatique par la carbamazépine.
Surveillance clinique, ECG et contrôle des concentrations plasmatiques ; si besoin, adaptation de la posologie de l’antiarythmique pendant le traitement par la carbamazépine et après son arrêt.
+ Antivitamines K
Diminution de l’effet de l’antivitamine K par augmentation de son métabolisme hépatique par la carbamazépine.
Contrôle plus fréquent de l’INR. Adaptation éventuelle de la posologie de l’antivitamine K pendant le traitement par la carbamazépine et 8 jours après son arrêt.
+ Aripiprazole
Diminution des concentrations plasmatiques de l’aripiprazole.
Surveillance clinique et adaptation éventuelle de la posologie de l’aripiprazole pendant l’association et 1 à 2 semaines après l’arrêt de la carbamazépine.
+ Bazédoxifène
Diminution des concentrations plasmatiques de bazédoxifène par la carbamazépine.
Surveillance d’éventuels signes évocateurs d’une perte d’efficacité (saignements).
+ Caspofungine
Diminution des concentrations plasmatiques de caspofungine.
En cas de traitement par la carbamazépine, maintenir la posologie à 70 mg par jour dès le 2e jour.
+ Certains antidépresseurs inhibiteurs sélectifs de la recapture de la sérotonine (fluoxétine, fluvoxamine, paroxétine) (voir association déconseillée pour la sertraline)
Augmentation des concentrations plasmatiques de carbamazépine avec signes de surdosage.
Surveillance clinique, contrôle des concentrations plasmatiques de carbamazépine et réduction éventuelle de la posologie de la carbamazépine pendant le traitement par l’antidépresseur sérotoninergique et après son arrêt.
+ Cimétidine ≥ 800 mg/j
En début de traitement, augmentation des concentrations plasmatiques de carbamazépine par inhibition de son métabolisme hépatique par la cimétidine.
Surveillance clinique et réduction éventuelle de la posologie de la carbamazépine, spécialement pendant les premiers jours de traitement par la cimétidine.
+ Clarithromycine
Augmentation des concentrations plasmatiques de carbamazépine avec signes de surdosage, par inhibition de son métabolisme hépatique.
Surveillance clinique et réduction éventuelle de la posologie de la carbamazépine.
+ Clonazépam
Augmentation des concentrations plasmatiques du métabolite actif de la carbamazépine. De plus, diminution des concentrations plasmatiques du clonazépam par augmentation de son métabolisme hépatique par la carbamazépine.
Surveillance clinique, dosages plasmatiques et adaptation éventuelle des posologies des deux anticonvulsivants.
+ Colistine (en cas d’administration chronique de carbamazépine)
Potentialisation des curares lorsque l’antibiotique est administré par voie parentérale et/ou péritonéale avant, pendant ou après l’agent curarisant.
Surveiller le degré de curarisation en fin d’anesthésie.
+ Corticoïdes (gluco-, minéralo-) (voie générale) (sauf hydrocortisone en traitement substitutif)
Diminution des concentrations plasmatiques et de l’efficacité des corticoïdes par augmentation de leur métabolisme hépatique par la carbamazépine : les conséquences sont particulièrement importantes chez les addisoniens traités par l’hydrocortisone et en cas de transplantation.
Surveillance clinique et biologique ; adaptation de la posologie des corticoïdes pendant le traitement par la carbamazépine et après son arrêt.
+ Cyprotérone (+ voir Associations déconseillées)
Risque de diminution de l'efficacité de la cyprotérone.
Dans ses indications comme anti-androgène: surveillance clinique et adaptation éventuelle de la posologie de la cyprotérone pendant l'association et après son arrêt.
+ Danazol
Augmentation des concentrations plasmatiques de carbamazépine, avec signes de surdosage.
Surveillance clinique et réduction éventuelle de la posologie de la carbamazépine.
+ Déférasirox
Risque de diminution des concentrations plasmatiques de déférasirox.
Surveiller la ferritinémie pendant et après le traitement par la carbamazépine. Si besoin, adaptation de la posologie de déférasirox.
+ Digoxine
Augmentation des concentrations plasmatiques de carbamazépine et diminution de la digoxinémie.
Prudence dans l’interprétation des concentrations plasmatiques.
+ Disopyramide
Risque de diminution des concentrations du disopyramide par la carbamazépine.
Surveillance clinique et éventuellement adaptation de la posologie du disopyramide pendant l’association et 1 à 2 semaines après l’arrêt de la carbamazépine.
+ Diurétiques hypokaliémiants (alitizide, bendroflumethiazide, bumetanide, chlortalidone, cicletanine, clopamide, furosemide, hydrochlorothiazide, indapamide, methylclothiazide, piretanide)
Risque d’hyponatrémie symptomatique.
Surveillance clinique et biologique. Si possible, utiliser une autre classe de diurétiques.
+ Dolutégravir (+ voir Associations déconseillées)
Diminution des concentrations plasmatiques de dolutégravir par augmentation de son métabolisme par la carbamazépine.
En l'absence de résistance à la classe des inhibiteurs d'intégrase, adaptation de la posologie de dolutégravir à 50 mg 2 fois par jour pendant l’association et une semaine après son arrêt.
+ Doxycycline
Diminution des concentrations plasmatiques de la doxycycline par augmentation de son métabolisme hépatique par la carbamazépine.
Surveillance clinique et adaptation éventuelle de la posologie de la doxycycline.
+ Estrogènes non contraceptifs et progestatifs non contraceptifs, associés ou non à un estrogène
Diminution de l’efficacité de l’estrogène ou du progestatif.
Surveillance clinique et adaptation éventuelle de la posologie du traitement hormonal pendant l’administration de la carbamazépine et après son arrêt.
+ Ethosuximide
Diminution des concentrations plasmatiques d’éthosuximide.
Surveillance clinique, dosage plasmatique de l’éthosuximide et augmentation éventuelle de sa posologie.
+ Felbamate
Augmentation des concentrations plasmatiques du métabolite actif de la carbamazépine. De plus, diminution des concentrations plasmatiques de felbamate par augmentation de son métabolisme hépatique par la carbamazépine.
Surveillance clinique, dosages plasmatiques et adaptation éventuelle des posologies des deux anticonvulsivants.
+ Fluconazole ≥ 200 mg/j
Augmentation possible des effets indésirables de la carbamazépine.
Adapter la posologie de carbamazépine, pendant et après l’arrêt du traitement antifongique.
+ Halopéridol
Risque de diminution des concentrations plasmatiques de l’halopéridol et de son efficacité thérapeutique, par augmentation de son métabolisme hépatique par la carbamazépine.
Surveillance clinique et, si besoin, adaptation posologique pendant le traitement par la carbamazépine et après son arrêt.
+ Hormones thyroïdiennes
Risque d’hypothyroïdie clinique chez les patients hypothyroïdiens, par augmentation du métabolisme de la T3 et de la T4.
Surveillance des concentrations sériques de T3 et de T4 et adaptation, si besoin, de la posologie des hormones thyroïdiennes pendant le traitement par la carbamazépine et après son arrêt.
+ Hydrocortisone
Risque de diminution de l’efficacité de l’hydrocortisone (augmentation de son métabolisme) ; les conséquences sont graves lorsque l’hydrocortisone est administrée en traitement substitutif ou en cas de transplantation.
Surveillance clinique et biologique ; adaptation de la posologie de l’hydrocortisone pendant l’association et après l’arrêt de la carbamazépine.
+ Immunosuppresseurs (ciclosporine, évérolimus, sirolimus, tacrolimus, temsirolimus)
Diminution des concentrations sanguines et de l’efficacité de l’immunosuppresseur, par augmentation de son métabolisme hépatique par la carbamazépine.
Augmentation de la posologie de l’immunosuppresseur sous contrôle des concentrations sanguines. Réduction de la posologie après l’arrêt de la carbamazépine.
+ Inhibiteurs de protéases boostés par ritonavir
Risque de baisse de l’efficacité de l’inhibiteur de protéases par augmentation de son métabolisme hépatique par la carbamazépine.
Surveillance clinique et biologique régulière, notamment en début d’association.
+ Ivabradine
Risque de diminution de l’efficacité de l’ivabradine, par augmentation de son métabolisme par la carbamazépine.
Surveillance clinique et adaptation de la posologie de l’ivabradine pendant l’association et après l’arrêt de la carbamazépine.
+ Josamycine
Augmentation des concentrations plasmatiques de carbamazépine avec signes de surdosage, par inhibition de son métabolisme hépatique.
Surveillance clinique et, si besoin, dosage plasmatique et réduction éventuelle de la posologie de la carbamazépine.
+ Lamotrigine
Risque d’augmentation des effets neurologiques (vertiges, ataxie, diplopie) de la carbamazépine lors de l’introduction de la lamotrigine.
Surveillance clinique et réduction éventuelle de la posologie de la carbamazépine.
+ Levonorgestrel
Avec le lévonorgestrel utilisé dans l’indication contraception d’urgence, diminution importante des concentrations plasmatiques de lévonorgestrel, avec risque d’inefficacité.
En cas de prise de carbamazépine dans les 4 dernières semaines, l’utilisation d’une contraception d’urgence non hormonale (DIU au cuivre) devrait s’envisager.
Si ce n’est pas possible, le doublement de la dose de lévonorgestrel est une autre option.
+ Lincosanides (en cas d’administration chronique de carbamazépine)
Potentialisation des curares lorsque l’antibiotique est administré par voie parentérale et/ou péritonéale avant, pendant ou après l’agent curarisant.
Surveiller le degré de curarisation en fin d’anesthésie.
+ Maraviroc
En l’absence de co-administration avec un inhibiteur puissant du CYP3A4, diminution des concentrations de maraviroc par la carbamazépine.
La dose de maraviroc doit être augmentée à 600 mg deux fois par jour dans cette situation.
+ Méthadone
Diminution des concentrations plasmatiques de méthadone avec risque d’apparition d’un syndrome de sevrage, par augmentation de son métabolisme hépatique.
Augmenter la fréquence des prises de méthadone (2 à 3 fois par jour au lieu d’une fois par jour).
+ Métronidazole
Diminution des concentrations plasmatiques du métronidazole par augmentation de son métabolisme hépatique par la carbamazépine.
Surveillance clinique et adaptation éventuelle de la posologie du métronidazole pendant le traitement par la carbamazépine et après son arrêt.
+ Montélukast
Risque de baisse de l’efficacité du montélukast par augmentation de son métabolisme hépatique par la carbamazépine.
Surveillance clinique et adaptation éventuelle de la posologie de l’antiasthmatique pendant le traitement par la carbamazépine et après son arrêt.
+ Nintédanib
Diminution des concentrations plasmatiques du nintédanib par diminution de son absorption par la carbamazépine.
Surveillance clinique pendant l’association.
+ Olanzapine
Risque de diminution des concentrations plasmatiques de l’olanzapine et de son efficacité thérapeutique, par augmentation de son métabolisme hépatique par la carbamazépine.
Surveillance clinique, et si besoin, adaptation posologique de l’olanzapine.
+ Polymyxine B (en cas d’administration chronique de carbamazépine)
Potentialisation des curares lorsque l’antibiotique est administré par voie parentérale et/ou péritonéale avant, pendant ou après l’agent curarisant.
Surveiller le degré de curarisation en fin d’anesthésie.
+ Posaconazole
Diminution des concentrations plasmatiques et de l’efficacité du posaconazole.
Surveillance clinique. Si possible, dosages plasmatiques du posaconazole et adaptation éventuelle de sa posologie.
+ Propafénone
Diminution des concentrations plasmatiques de la propafénone par augmentation de son métabolisme hépatique par la carbamazépine.
Surveillance clinique et ECG. S’il y a lieu, adaptation de la posologie de la propafénone pendant l’association et après l’arrêt de la carbamazépine.
+ Quinine
Risque de perte de l’efficacité de la quinine par augmentation de son métabolisme hépatique par la carbamazépine.
Surveillance clinique et adaptation de la posologie de la quinine pendant le traitement par la carbamazépine et après son arrêt.
+ Rifabutine (+ voir Associations à prendre en compte)
Risque d'hypothyroïdie clinique chez les patients hypothyroïdiens, par augmentation du métabolisme de la T3 et de la T4.
Surveillance des concentrations sériques de T3 et de T4 et adaptation, si besoin, de la posologie des hormones thyroïdiennes pendant le traitement par la rifabutine et après son arrêt.
+ Rifampicine
Diminution des concentrations plasmatiques et de l’efficacité de la carbamazépine par augmentation de son métabolisme hépatique par la rifampicine.
Surveillance clinique, contrôle des concentrations plasmatiques et adaptation de la posologie de la carbamazépine pendant le traitement par la rifampicine et après son arrêt.
+ Rispéridone
Risque de diminution de la fraction active de rispéridone et de son efficacité thérapeutique par augmentation de son métabolisme hépatique par la carbamazépine.
Surveillance clinique, et si besoin, adaptation posologique de la rispéridone.
+ Stiripentol
Augmentation des concentrations plasmatiques de la carbamazépine, avec risque de surdosage, par inhibition de son métabolisme hépatique par le stiripentol.
Surveillance clinique et dosage plasmatique, lorsque cela est possible, de la carbamazépine associée au stiripentol et adaptation éventuelle de sa posologie.
+ Théophylline (et, par extrapolation, aminophylline)
Diminution des concentrations plasmatiques et de l’efficacité de la théophylline par augmentation de son métabolisme hépatique par la carbamazépine.
Surveillance clinique et, si besoin, de la théophyllinémie. Adaptation éventuelle de la posologie de la théophylline pendant le traitement par la carbamazépine et après son arrêt.
+ Tiagabine
Diminution des concentrations plasmatiques de la tiagabine par augmentation de son métabolisme hépatique par la carbamazépine.
Une augmentation de la posologie de tiagabine peut s’avérer nécessaire en cas d’association à la carbamazépine.
+ Topiramate
Diminution des concentrations du topiramate avec risque de moindre efficacité, par augmentation de son métabolisme hépatique par la carbamazépine.
Surveillance clinique, et si besoin, adaptation posologique du topiramate pendant le traitement par la carbamazépine et après son arrêt.
+ Vitamine D
Diminution des concentrations de vitamine D plus marquée qu’en l’absence de carbamazépine.
Dosage des concentrations de vitamine D et supplémentation si nécessaire.
Associations à prendre en compte
+ Atorvastatine
Risque de diminution des concentrations plasmatiques et/ou de l’efficacité de ces molécules par la carbamazépine.
Si nécessaire, adaptation de la posologie de ces molécules pendant le traitement par la carbamazépine.
+ Autres médicaments hyponatrémiants
Majoration du risque d’hyponatrémie.
+ Bortezomib
Diminution des concentrations du cytotoxique par augmentation de son métabolisme par la carbamazépine, avec risque de moindre efficacité.
+ Cabazitaxel
Diminution des concentrations du cytotoxique par augmentation de son métabolisme par la carbamazépine, avec risque de moindre efficacité.
+ Midazolam
Risque de diminution des concentrations plasmatiques du midazolam par la carbamazépine.
+ Pérampanel
Diminution importante (jusqu’aux deux-tiers) des concentrations de pérampanel.
+ Phénobarbital (et par extrapolation, primidone)
Diminution progressive des concentrations plasmatiques de carbamazépine sans modification apparente de l’efficacité anticomitiale.
Prudence quant à l’interprétation des concentrations plasmatiques.
+ Phénytoïne (et par extrapolation, fosphénytoïne)
Réduction réciproque des concentrations plasmatiques (augmentation du métabolisme sans modification apparente de l’efficacité anticomitiale).
Prudence dans l’interprétation des concentrations plasmatiques.
Afin d’éviter la survenue d’une intoxication par la phénytoïne et de concentrations infra-thérapeutiques de carbamazépine, il est recommandé d’ajuster la concentration plasmatique de phénytoïne à 13 microgrammes/mL avant d’ajouter le traitement par la carbamazépine.
+ Procarbazine
Augmentation des réactions d’hypersensibilité (hyperéosinophilie, rash), par augmentation du métabolisme de la procarbazine par la carbamazépine.
+ Rifabutine (+ voir Associations faisant l’objet de précautions d’emploi)
Risque de diminution des concentrations plasmatiques et/ou de l’efficacité de la rifabutine par la carbamazépine.
Si nécessaire, adaptation de la posologie de la rifabutine pendant le traitement par la carbamazépine.
+ Tamoxifène
Risque d’inefficacité du tamoxifène par augmentation de son métabolisme par la carbamazépine.
Interactions nécessitant une attention particulière
L’utilisation concomitante de carbamazépine avec les anticoagulants oraux d’action directe (rivaroxaban, dabigatran, apixaban, et edoxaban) peut conduire à une diminution des concentrations plasmatiques de ces derniers, et donc se traduire par un risque de thrombose. C’est pourquoi, en cas de nécessité d’administration concomitante, une surveillance étroite de l’apparition de signes et symptômes d’une thrombose est recommandée.
Interférences avec les analyses biologiques
La carbamazépine peut interférer avec les analyses de type HPLC (chromatographie liquide haute performance) résultant en des concentrations plasmatiques de perphénazine faussement positives.
La carbamazépine et son métabolite 10,11-époxyde peuvent interférer avec les méthodes de dosage immunologique par polarisation de fluorescence résultant en des concentrations plasmatiques d’antidépresseurs tricycliques faussement positives.
4.6. Fertilité, grossesse et allaitement
Grossesse
Risque lié aux médicaments antiépileptiques en général
Un avis médical spécialisé concernant les risques potentiels pour le fœtus causés à la fois par les crises d’épilepsie et par le traitement antiépileptique doit être donné à toutes les femmes susceptibles de procréer qui prennent un traitement antiépileptique, en particulier aux femmes qui planifient une grossesse et aux femmes enceintes.
L’arrêt brutal d’un traitement par un médicament antiépileptique doit être évité car il peut entraîner des crises susceptibles d’avoir des conséquences graves pour la femme et l’enfant à naître.
La monothérapie doit être privilégiée pour le traitement de l’épilepsie pendant la grossesse, dans la mesure du possible.
En effet, une polythérapie antiépileptique peut être associée à un risque plus élevé de malformations congénitales que la monothérapie ; ce risque varie selon les antiépileptiques co-administrés.
Risques liés à la carbamazépine
Dans l’espèce humaine, la carbamazépine traverse le placenta. L’exposition prénatale à la carbamazépine peut augmenter les risques de malformations congénitales et d’autres effets néfastes sur le développement. Dans l’espèce humaine, l'exposition à la carbamazépine pendant la grossesse est associée à une fréquence de malformations congénitales majeures 2 à 3 fois supérieure à celle de la population générale, qui est de 2 à 3 %. Les malformations les plus souvent rencontrées sont des anomalies du tube neural (spina bifida), des anomalies crânio-faciales (dont les fentes labiales/palatines), des malformations cardiovasculaires, des hypospadias, une hypoplasie des doigts, une microcéphalie et d’autres anomalies impliquant différents organes ont été rapportées chez les enfants de femmes traitées par carbamazépine pendant la grossesse. Les données d'une étude observationnelle basée sur des registres de population menée dans les pays nordiques suggèrent un risque accru d’enfants nés avec un petit poids pour l'âge gestationnel (PAG ; défini comme un poids de naissance inférieur au 10e percentile pour le sexe et l'âge gestationnel) après une exposition prénatale à la carbamazépine. Le risque de PAG chez les enfants de femmes épileptiques traitées par carbamazépine était de 12,8 %, contre 10,9 % chez les enfants de femmes épileptiques ne recevant pas de traitement antiépileptique. Une surveillance prénatale spécialisée de ces malformations et du retard de croissance est recommandée.
Des troubles du développement neurologique ont été rapportés chez des enfants nés de femmes épileptiques prenant de la carbamazépine seule ou en association avec d’autres antiépileptiques pendant la grossesse. Les études relatives au risque de troubles neuro-développementaux chez les enfants exposés à la carbamazépine pendant la grossesse sont contradictoires et ne permettent pas d’exclure un risque.
La carbamazépine ne doit pas être utilisée pendant la grossesse, à moins que le bénéfice ne soit jugé supérieur aux risques après un examen attentif des alternatives thérapeutiques disponibles. La femme doit être pleinement informée et comprendre les risques liés à la prise de carbamazépine pendant la grossesse.
Les données disponibles suggèrent que le risque de malformation associé à la carbamazépine peut être dose-dépendant. Si, sur la base d’une évaluation minutieuse des risques et des bénéfices, aucune alternative thérapeutique n’est appropriée, et le traitement par la carbamazépine est poursuivi, une monothérapie et la dose efficace la plus faible de carbamazépine doivent être utilisées et une surveillance des taux plasmatiques est recommandée. La concentration plasmatique pourrait être maintenue dans la partie inférieure de l’intervalle thérapeutique allant de 4 à 12 microgrammes/mL, à condition que le contrôle des crises soit maintenu.
Il a été rapporté que certains médicaments antiépileptiques, comme la carbamazépine, diminuent les taux sériques de folate. Ce déficit peut contribuer à l’incidence accrue de malformations congénitales dans la descendance des femmes épileptiques traitées. Une supplémentation en acide folique est recommandée avant et pendant la grossesse. Afin de prévenir les troubles hémorragiques dans la descendance, il a également été recommandé d’administrer de la vitamine K1 à la mère au cours des dernières semaines de grossesse, ainsi qu’au nouveau-né.
Si une femme envisage une grossesse, tous les efforts doivent être faits pour passer à un traitement alternatif approprié avant la conception et avant l’interruption de la contraception. Si une femme devient enceinte alors qu’elle prend de la carbamazépine, elle doit être orientée vers un spécialiste afin de réévaluer le traitement par la carbamazépine et d’envisager des alternatives thérapeutiques.
Enfants et adolescents de sexe féminin, femmes susceptibles de procréer
La carbamazépine ne doit pas être utilisée chez les femmes susceptibles de procréer, à moins que le bénéfice potentiel ne soit jugé supérieur aux risques après un examen attentif des alternatives thérapeutiques disponibles. La femme doit être pleinement informée et comprendre le risque d’atteinte potentielle du fœtus si la carbamazépine est prise pendant la grossesse et, par conséquent, l’importance de prévoir une grossesse. Un test de grossesse chez les femmes susceptibles de procréer doit être envisagé avant l’instauration du traitement par la carbamazépine.
Lors de l’initiation du traitement, et une fois par an, le médecin s’assure que le traitement par carbamazépine est la meilleure option pour la patiente et signe avec elle une attestation d’information partagée.
Les femmes susceptibles de procréer doivent utiliser une contraception efficace pendant le traitement et pendant deux semaines après l’arrêt du traitement. En raison de l’effet inducteur enzymatique de la carbamazépine, le traitement par TEGRETOL peut conduire à un échec des contraceptifs hormonaux (voir rubrique 4.5). Par conséquent, les femmes susceptibles de procréer doivent être conseillées sur l’utilisation d’autres méthodes contraceptives efficaces. Au moins une méthode de contraception efficace (comme un dispositif intra-utérin) ou deux formes de contraception complémentaires, y compris une méthode de contraception de type mécanique (par exemple un préservatif), doivent être utilisées. Les conditions individuelles doivent être évaluées dans chaque cas, en impliquant la patiente dans la discussion, lors du choix de la méthode de contraception.
Les prescripteurs doivent s’assurer que les parents / tuteurs des enfants et adolescents de sexe féminin traités par carbamazépine comprennent la nécessité de contacter un spécialiste aussitôt que les premières menstruations surviennent (ménarche). La patiente et ses parents / tuteurs devront alors recevoir des informations complètes sur les risques liés à l’exposition in utero à la carbamazépine et sur la nécessité d’utiliser une contraception hautement efficace dès que nécessaire. La nécessité de poursuivre le traitement par carbamazépine devra être réévaluée et des alternatives thérapeutiques devront être également envisagées.
Avant l’accouchement / Chez le nouveau-né :
Les antiépileptiques inducteurs enzymatiques peuvent parfois provoquer chez le nouveau-né de mère traitée :
· un syndrome hémorragique pouvant survenir lors de l’accouchement ou dans les premiers jours de vie. Une prévention par vitamine K1 per os chez la mère dans le mois précédant l’accouchement et l’administration de vitamine K1 par voie parentérale (IM ou IV lente) à la naissance, chez le nouveau-né semblent efficaces. Un bilan d’hémostase normal chez la mère ne permet pas d’éliminer des anomalies de l’hémostase chez le nouveau-né.
· des perturbations du métabolisme phosphocalcique et de la minéralisation osseuse, qu’une supplémentation de la mère en vitamine D au cours du 3ème trimestre semble pouvoir prévenir.
Suivi post natal / Chez l’enfant : en cas d’exposition pendant la grossesse, un suivi rapproché du développement neurocomportemental de l’enfant est à instaurer et une prise en charge adaptée doit être mise en place au plus tôt en cas de nécessité.
Allaitement
L’allaitement est déconseillé en raison du passage non négligeable de la carbamazépine dans le lait maternel et de la possibilité de survenue de troubles hépatiques chez les nouveau-nés allaités.
Fertilité
Sans objet.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
TEGRETOL 20 mg/ml, suspension buvable a une influence modérée sur l’aptitude à conduire des véhicules et à utiliser des machines.
L’attention est attirée, notamment chez les conducteurs de véhicules et les utilisateurs de machines, sur les risques liés aux crises d’épilepsie, ainsi qu’aux effets indésirables suivants : étourdissement, somnolence, sensations vertigineuses, ataxie, troubles de l’accommodation, diplopie et vision trouble, associés à l’emploi de la carbamazépine.
Résumé du profil de sécurité
Dans les situations particulières, comme l’instauration du traitement par carbamazépine, une dose initiale trop élevée ou chez les personnes âgées, certains types d’effets indésirables surviennent fréquemment ou très fréquemment tels que des effets indésirables spécifiques au SNC (sensations vertigineuses, céphalées, ataxie, somnolence, fatigue, diplopie, troubles de l’accommodation, confusion, agitation), gastro-intestinaux (nausées, vomissement, diarrhée, constipation, anorexie, sécheresse de la bouche) ainsi que des réactions allergiques cutanées.
Ces manifestations doses-dépendantes s’atténuent habituellement en quelques jours, soit spontanément, soit après une diminution posologique transitoire.
Les effets graves intéressant les systèmes hématologique, hépatique, dermatologique, cardiovasculaire (voir rubrique 4.9) ainsi que les réactions d’hypersensibilité imposent l’arrêt du traitement.
Tableau récapitulatif des effets indésirables issus des essais cliniques et de notifications spontanées
Les effets indésirables issus des essais cliniques (Tableau 1) sont listés selon la terminologie MedDRA par classes de systèmes d'organes. Dans chaque classe de systèmes d’organes, les effets indésirables sont rangés par fréquence, du plus fréquent au moins fréquent. A l’intérieur de chaque groupe de fréquence, les effets indésirables sont présentés selon un ordre décroissant de gravité.
Les catégories de fréquence sont basées sur la convention suivante (CIOMS III) : très fréquent (³1/10), fréquent (³1/100 et <1/10), peu fréquent (³1/1 000 et <1/100), rare (³1/10 000 et <1/1 000), très rare (<1/10 000).
Tableau 1. Effets indésirables issus des études cliniques et de notifications spontanées
|
Affections hématologiques et du système lymphatique |
|
|
Très fréquent : |
leucopénie. |
|
Fréquent : |
thrombocytopénie, hyperéosinophilie. |
|
Rare : |
hyperleucocytose, polyadénopathie. |
|
Très rare : |
agranulocytose, aplasie médullaire, pancytopénie, anémie aplasique, anémie, anémie mégaloblastique, anémie hémolytique. |
|
Affections respiratoires, thoraciques et médiastinales Très rare : hypersensibilité pulmonaire caractérisée par de la fièvre, une dyspnée, une pneumonie. |
|
|
Affections du système immunitaire |
|
|
Rare : |
réactions d’hypersensibilité* retardée multi-systémiques (syndrome DRESS) avec fièvre, éruption cutanée, conjonctivites, vascularite, polyadénopathies, pseudo-lymphome, arthralgie, leucopénie, hyperéosinophilie, hépatosplénomégalie, hépatite pouvant être sévère et syndrome de disparition des canaux biliaires peuvent être associées dans le cadre de ce syndrome. De façon exceptionnelle, l’atteinte multi-systémique peut concerner le rein, le pancréas, le poumon, le colon, le myocarde. L’existence de rares cas de réactions croisées entre la carbamazépine, la phénytoïne, le phénobarbital et l’oxcarbazépine doit rendre prudent le remplacement de la carbamazépine par l’une ou l’autre de ces molécules. |
|
Très rare : |
réaction anaphylactique, angio-œdème, hypogammaglobulinémie. |
|
Affections endocriniennes |
|
|
Fréquent : |
œdème, rétention liquidienne, prise de poids, hyponatrémie liée à un syndrome de sécrétion inappropriée d’hormone antidiurétique. |
|
Très rare : |
galactorrhée, gynécomastie. |
|
Troubles du métabolisme et de la nutrition |
|
|
Rare : |
carence en acide folique, appétit diminué. |
|
Très rare : |
porphyries aiguës (porphyrie aigüe intermittente et porphyrie variegata), porphyries non aiguës (porphyrie cutanée tardive). |
|
Affections psychiatriques |
|
|
Rare : |
agitation, confusion. |
|
Affections du système nerveux |
|
|
Très fréquent : |
ataxie, sensations vertigineuses, somnolence. |
|
Fréquent : |
diplopie, céphalées. |
|
Peu fréquent : |
mouvements anormaux (ex : tremblements, dystonie, dyskinésies), nystagmus. |
|
Rare : |
troubles oculomoteurs, troubles de la parole (ex : dysarthrie, troubles de l’élocution). |
|
Très rare : |
syndrome malin des neuroleptiques, méningite aseptique, dysgueusies. |
|
Affections oculaires |
|
|
Fréquent : |
troubles de l’accommodation (ex : vision trouble). |
|
Très rare : |
conjonctivite. |
|
Affections de l’oreille et du labyrinthe |
|
|
Très rare : |
troubles de l’audition (hypoacousie ou hyperacousie, acouphènes). |
|
Affections cardiaques |
|
|
Rare : |
troubles de la conduction. |
|
Très rare : |
arythmies, bloc auriculo-ventriculaire avec ou sans syncope, bradycardie, tachycardie. |
|
Affections vasculaires |
|
|
Rare : |
hypertension ou hypotension artérielle, accidents thromboemboliques. |
|
Très rare : |
embolies (ex : embolie pulmonaire). |
|
Affections gastro-intestinales |
|
|
Très fréquent : |
vomissements, nausées. |
|
Fréquent : |
sécheresse de la bouche. |
|
Peu fréquent : |
diarrhées, constipation. |
|
Rare : |
douleurs abdominales. |
|
Très rare : |
pancréatite, glossite, stomatite. |
|
Affections hépatobiliaires |
|
|
Rare : |
hépatites, exceptionnels cas de syndrome de disparition des canaux biliaires. |
|
Affections de la peau et du tissu sous-cutané |
|
|
Très fréquent : |
urticaire parfois sévère, réactions cutanées allergiques. |
|
Peu fréquent : |
dermatite exfoliatrice. |
|
Rare : |
syndrome lupique, prurit. |
|
Très rare : |
syndrome de Stevens-Johnson*, syndrome de Lyell*, photosensibilité, érythème polymorphe, érythème noueux, purpura, alopécie, pustulose exanthématique aiguë généralisée (voir rubrique 4.4). |
|
Affections musculo-squelettiques et systémiques |
|
|
Très rare : |
trouble du métabolisme osseux (diminution des concentrations de calcium plasmatique et de 25-hydroxy-cholécalciférol sanguin) pouvant être à l’origine d’une d’ostéomalacie/ostéoporose, arthralgie, myalgies, crampes. |
|
Affections du rein et des voies urinaires |
|
|
Très rare : |
néphrite tubulo-interstitielle, insuffisance rénale, trouble de la fonction rénale (protéinurie, élévation de la créatinine pouvant entrer ou non dans le cadre d’un syndrome d’hypersensibilité*), rétention urinaire. |
|
Affections des organes de reproduction et du sein |
|
|
Très rare : |
dysfonction sexuelle/dysfonction érectile. |
|
Troubles généraux et anomalies au site d’administration |
|
|
Très fréquent : |
fatigue. |
|
Investigations |
|
|
Très fréquent : |
augmentation isolée de la gammaglutamyltranpeptidase (liée au caractère inducteur enzymatique hépatique de la carbamazépine), cette augmentation est en général sans signification clinique. |
|
Fréquent : |
élévation des phosphatases alcalines. |
|
Peu fréquent : |
élévation des transaminases. |
|
Très rare : |
diminution du taux de T3 et T4. |
|
* II existe de plus en plus de preuves mettant en évidence l’association de marqueurs génétiques et l’apparition d’effets indésirables cutanés tels que SJS, NET, DRESS, PEAG et éruption maculopapulaire. Chez les patients japonais et d’Europe du Nord, ces réactions ont été rapportées comme associées à la carbamazépine et à la présence de l’allèle HLA-A*3101. Un autre marqueur, HLA-B*1502 a montré qu’il était fortement associé au SJS et NET chez les patients d’origine Chinoise Han, thaïlandaise et de l’Asie du Sud-Est (voir les rubriques 4.2 et 4.4). |
|
Effets indésirables supplémentaires issus de notifications spontanées (fréquence indéterminée)
Infections et infestations
Réactivation d’une infection au virus de l’herpès humain de type 6.
Troubles du métabolisme et de la nutrition
Hyperammoniémie.
Affections du système nerveux
Sédation, troubles mnésiques.
Affections gastro-intestinales
Colite.
Affections de la peau et du tissu sous-cutané
Kératose lichénoïde, onychomadèse.
Affections musculo-squelettiques et systémiques
Il a été rapporté des cas de diminution de la densité osseuse, d’ostéopénie, d’ostéoporose et de fractures chez les patients traités au long cours par la carbamazépine. Le mécanisme des effets osseux n’a pas été élucidé à ce jour.
Affections congénitales, familiales et génétiques :
Malformations congénitales, autres anomalies du développement (voir rubriques 4.4 et 4.6).
Lésions, intoxications et complications liées aux procédures
Chute (liée aux effets indésirables suivants pouvant être associés au traitement par TEGRETOL : ataxie, sensations vertigineuses, somnolence, hypotension, état confusionnel et sédation) (voir rubrique 4.4).
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
Le dosage plasmatique permet de confirmer l’intoxication par la carbamazépine mais les taux ne sont pas toujours corrélés à la gravité de l’intoxication.
Les signes et symptômes de surdosage sont habituellement neuromusculaires, cardiovasculaires et respiratoires, ou peuvent correspondre aux effets indésirables mentionnés en rubrique 4.8.
Effets sur le système nerveux central
Troubles de la conscience pouvant évoluer à bas bruit et conduire à un coma profond, convulsions, dyskinésies et dystonies, signes anticholinergiques. L’intoxication peut se compliquer, dans les cas sévères, par une dépression respiratoire.
Effets cardiovasculaires
Tachycardie, bradycardie, hypotension, modifications de l’électrocardiogramme (troubles de la conduction auriculo-ventriculaire et intra-ventriculaire, allongement du QT), pouvant conduire à un collapsus, une défaillance et un arrêt cardiaque.
Effets musculo-squelettiques
Des cas de rhabdomyolyse ont été rapportés lors d’une intoxication par la carbamazépine.
Anomalies biologiques
Principalement hypokaliémie, hyponatrémie, acidose métabolique.
Prise en charge
Il n’y a pas de traitement antidote spécifique. Les mesures thérapeutiques doivent être adaptées à l’état clinique du patient.
Le traitement d’une intoxication grave doit être assuré dans une unité de soins intensifs avec surveillance du niveau de conscience, des paramètres cardiovasculaires (monitoring cardiaque), des signes vitaux et correction des désordres électrolytiques.
Recommandations particulières
L’hémodialyse constitue une mesure efficace de traitement du surdosage de carbamazépine.
La durée de la surveillance doit prendre en compte la possibilité d’une apparition tardive des symptômes ou d’une ré-aggravation secondaire en raison d’une absorption retardée, ce risque étant majoré pour les formes à libération prolongée. L’évacuation digestive, qui ne sera pas conseillée de façon systématique, prendra cependant en compte, pour son délai de mise en œuvre, ce retard à l’absorption ; de même, l’utilisation de charbon activé per os, pourra être répétée, dans la limite du respect de leurs contre-indications.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : ANTIEPILEPTIQUE, dérivé du carboxamide, code ATC : N03AF01
Dérivé de la dibenzazépine.
Mécanisme d’action
La carbamazépine agit principalement sur les canaux sodiques voltage dépendant ; les autres mécanismes d’action étant partiellement élucidés.
Par ailleurs, la diminution de la libération du glutamate et la stabilisation des membranes neuronales peuvent essentiellement expliquer les effets antiépileptiques.
Les propriétés antimaniaques de la carbamazépine semblent être dues à l’effet dépressif sur la régénération de la dopamine et de la noradrénaline.
5.2. Propriétés pharmacocinétiques
Absorption
Les concentrations plasmatiques maximales sont atteintes en 2 heures après administration de la suspension buvable.
Distribution
Le taux de liaison de la carbamazépine aux protéines plasmatiques est de 70 à 80%.
L’activité est généralement observée pour des concentrations plasmatiques à l’équilibre (soit au bout d’une semaine de traitement) de 4 à 12 microgrammes/mL (soit 17 à 50 micromoles/L), et les réactions toxiques surviennent pour des concentrations supérieures à 15 microgrammes/mL.
La substance active traverse le placenta. En outre, pendant la grossesse, la fraction libre est augmentée.
La substance active passe aussi dans le lait maternel, où elle est deux fois moins concentrée.
Biotransformation
La quasi-totalité de la substance active est métabolisée par le foie. Le principal métabolite est le 10,11-époxy-carbamazépine, pharmacologiquement actif. Le cytochrome P450 3A4 a été identifié comme le principal enzyme responsable de la formation de ce métabolite.
La carbamazépine est un puissant inducteur enzymatique et donne lieu à de nombreuses interactions médicamenteuses.
Elimination
En monothérapie, la demi-vie d’élimination est de l’ordre de 16 à 24 heures en moyenne. Chez des patients recevant en même temps d’autres antiépileptiques inducteurs enzymatiques, la durée de la demi-vie de la carbamazépine peut être abaissée. 2 % de la dose de carbamazépine sont éliminés dans l’urine sous forme inchangée.
5.3. Données de sécurité préclinique
Les données non cliniques issues des études conventionnelles de toxicologie en administration unique ou répétée, génotoxicité et cancérogénèse n’ont pas révélé de risque particulier pour l’Homme. Cependant les résultats des études chez l’animal sont insuffisants pour exclure un effet tératogène de la carbamazépine.
Toxicité de la reproduction
D’après les preuves cumulées issues des différentes études réalisées chez la Souris, le Rat et le Lapin, le potentiel tératogène de la carbamazépine est faible ou nul aux posologies utilisées chez l’Homme. Toutefois, les résultats des études chez l’animal ne permettent pas d’exclure totalement un effet tératogène de la carbamazépine. Dans une étude de la reproduction chez le Rat, il a été observé une diminution de la prise de poids chez les petits des mères traitées à la dose de 192 mg/kg/j.
Stéarate de macrogol 400, cellulose microcristalline, sorbitol à 70 pour cent, parahydroxybenzoate de méthyle, parahydroxybenzoate de propyle, saccharine sodique, hydroxyéthylcellulose, acide sorbique, propylèneglycol, arôme caramel 52 929 A*, eau purifiée.
* Composition de l’arôme caramel n° 52 929 A : extrait naturel de cacao, alcool benzylique, vanilline, furfural, acétylméthylcarbinol, acide lactique, furoate de méthyle, delta decalactone.
Sans objet.
3 ans.
6.4. Précautions particulières de conservation
A conserver à une température ne dépassant pas 30°C.
Conserver le flacon dans l’emballage extérieur, à l’abri de la lumière.
6.5. Nature et contenu de l'emballage extérieur
Flacon (verre brun) de 100 mL, 150 mL, ou 200 mL avec seringue pour administration orale (polyéthylène) de 10 mL.
6.6. Précautions particulières d’élimination et de manipulation
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
NOVARTIS PHARMA S.A.S.
8-10 RUE HENRI SAINTE-CLAIRE DEVILLE
92500 RUEIL-MALMAISON
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· CIP 34009 315 244 3 4 :100 ml en flacon (verre brun) + seringue pour administration orale
· CIP 34009 329 563 9 5 :150 ml en flacon (verre brun) + seringue pour administration orale
· CIP 34009 329 564 5 6 :200 ml en flacon (verre brun) + seringue pour administration orale
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Sans objet.
Liste II
Enfants et adolescents de sexe féminin, femmes susceptibles de procréer et femmes enceintes : Médicament nécessitant une surveillance particulière pendant le traitement : à l’initiation du traitement et une fois par an, la prescription est précédée de la signature par le médecin et la patiente de l'attestation d'information partagée. La délivrance nécessite la présentation de l'attestation annuelle co-signée.
Informations importantes
Les informations importantes disponibles pour ce médicament sont les suivantes :
- Tegretol 20 mg/ml suspension buvable : restriction d'utilisation chez les nouveau-nés, en raison de la concentration de l'excipient propylène glycol dépassant le seuil recommandé
- Antiépileptiques pendant la grossesse entre 2013 et 2021 : une étude du GIS EPI-PHARE met en évidence une baisse importante de l'exposition au valproate et dérivés, mais moindre pour le topiramate et la carbamazépine
- Carbamazépine et grossesse : renforcement de l'information des femmes pour les sensibiliser aux risques encourus par les enfants à naître
- Antiépileptiques et grossesse : mieux connaître les risques pour l'enfant à naître
- Encore trop de grossesses sous carbamazépine : nous souhaitons renforcer l'information pour limiter l'exposition
ANSM - Mis à jour le : 06/02/2026
TEGRETOL® 20 mg/ml, suspension buvable
Carbamazépine
Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations importantes pour vous.
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin, votre pharmacien ou votre infirmier/ère.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que TEGRETOL 20 mg/ml, suspension buvable et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant de prendre TEGRETOL 20 mg/ml, suspension buvable ?
3. Comment prendre TEGRETOL 20 mg/ml, suspension buvable ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver TEGRETOL 20 mg/ml, suspension buvable ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE TEGRETOL 20 mg/ml, suspension buvable ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique - code ATC : ANTIEPILEPTIQUE, dérivé du carboxamide - N03AF01
TEGRETOL appartient à une classe de médicaments appelés les antiépileptiques.
Il est utilisé pour traiter :
· certaines formes d’épilepsie et de convulsions
TEGRETOL est utilisé pour traiter différentes formes d’épilepsie ou de convulsions chez les adultes et les enfants. Ce médicament peut être pris seul ou en association avec un autre médicament antiépileptique.
· certains troubles de l’humeur
Dans ce cas, TEGRETOL est utilisé quand le traitement par un autre médicament (notamment le lithium) n’a pas fonctionné ou ne peut pas être utilisé.
· certains types de douleurs
o des douleurs au niveau du visage provoquées par une maladie des nerfs de la face (névralgies du trijumeau et du glossopharyngien).
o des douleurs neuropathiques périphériques chez un adulte.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT DE PRENDRE TEGRETOL 20 mg/ml, suspension buvable ?
Si votre médecin vous a informé d’une intolérance à certains sucres, contactez-le avant de prendre ce médicament.
Ne prenez jamais TEGRETOL 20 mg/mL, suspension buvable :
· Si vous êtes allergique à la carbamazépine ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
· Si vous avez certains troubles du rythme cardiaque comme un ralentissement du cœur (bloc auriculo-ventriculaire).
· Si vous avez eu dans le passé une diminution de vos globules rouges, de vos globules blancs et/ou de vos plaquettes, provoquée par un problème de moelle osseuse (hypoplasie médullaire).
· Si vous avez eu dans le passé une maladie provoquant l’accumulation dans le foie de certains composés (porphyrie hépatique).
· Ce médicament ne doit pas être administré à votre bébé s'il a moins de 4 semaines (voir "Avertissements et précautions")
· En même temps que certains médicaments contenant une ou plusieurs substances actives suivantes :
o le cobicistat (utilisé dans le traitement de l’infection par le VIH (virus de l’immunodéficience humaine)),
o le dasabuvir (utilisé pour traiter le virus de l’hépatite C),
o le délamanid (antibiotique destiné au traitement de la tuberculose localisée au niveau du poumon),
o l’association grazoprevir et elbasvir (utilisée pour traiter le virus de l’hépatite C),
o l’isavuconazole (utilisé chez l’adulte pour traiter certaines infections à champignons),
o le lédipasvir (utilisé avec le sofosbuvir pour traiter le virus de l’hépatite C),
o la lurasidone (utilisée pour traiter les symptômes de la schizophrénie),
o la midostaurine (utilisée dans le traitement des leucémies aiguës myéloïdes et des mastocytoses),
o l’association ombitasvir + paritaprévir (utilisée avec le ritonavir pour traiter le virus de l’hépatite C),
o la rilpivirine (utilisée dans le traitement de l’infection par le VIH (virus de l’immunodéficience humaine)),
o le sofosbuvir (utilisé pour traiter le virus de l’hépatite C),
o le velpatasvir (utilisé pour traiter le virus de l’hépatite C),
o le voriconazole (utilisé pour traiter certaines infections à champignons).
Avertissements et précautions
Adressez-vous à votre médecin ou pharmacien avant de prendre TEGRETOL 20 mg/mL, suspension buvable.
TEGRETOL peut provoquer des anomalies chez l’enfant à naître lorsqu’il est administré pendant la grossesse. Si vous êtes une femme susceptible d’avoir des enfants, vous devez utiliser une contraception efficace pendant le traitement par TEGRETOL et pendant les deux semaines suivant l’administration de la dernière dose (voir «Grossesse et allaitement»).
Enfants (âgés de 4 semaines ou plus), adolescents (moins de 18 ans) et personnes âgées (65 ans et plus)
Tegretol peut être utilisé en toute sécurité chez les enfants âgés de 4 semaines ou plus et chez les personnes âgées, conformément aux instructions du médecin. Si nécessaire, des informations spécifiques seront fournies, notamment concernant l'ajustement de la dose et la nécessité d'une surveillance étroite (voir rubriques 3 et 4).
Avant de prendre ce médicament, prévenez votre médecin :
· Si vous avez ou avez eu une maladie du cœur, du foie ou des reins.
· Si vous avez déjà eu dans le passé une allergie avec un autre médicament antiépileptique.
· Si vous ressentez une gêne quand vous urinez.
· Si vous avez une maladie de l’œil provoquant une augmentation de la pression à l’intérieur de l’œil (glaucome).
· Si vous prenez des médicaments pouvant diminuer le taux de sodium (sel) sanguin, par exemple des médicaments diurétiques (médicaments utilisés pour aider les reins à éliminer les sels et l’eau en augmentant la quantité d’urine produite).
· Si vous savez que votre taux sanguin de sodium est bas (voir la rubrique 4).
· Si vous prenez des hormones thyroïdiennes (en cas d’hypothyroïdie).
· Si vous êtes une femme et prenez la pilule contraceptive, TEGRETOL peut rendre inefficace ce moyen de contraception. Si l’association s’avère nécessaire, utiliser une méthode contraceptive additionnelle de type mécanique (par exemple un préservatif) et poursuivre un cycle après l’arrêt de la carbamazépine.
· Si vous avez des origines thaïlandaise ou chinoise Han. Si vous êtes dans ce cas, votre risque d’avoir une réaction grave de la peau est plus important. Prévenez votre médecin avant de prendre ce médicament.
Pendant le traitement, consultez immédiatement votre médecin ou présentez-vous au service des urgences de l’hôpital le plus proche :
· En cas d’apparition de lésions cutanées (rougeur, pustules), de fièvre inexpliquée, d’angine, ou autre signe d’infection, de manifestations allergiques cutanées ou de jaunisse.
Des éruptions cutanées potentiellement mortelles (Syndrome de Stevens-Johnson et Nécrolyses Epidermiques Toxiques) ont été rapportées sous carbamazépine. Les signes précoces peuvent être des boutons au centre rougeâtre ou des plaques circulaires souvent avec des vésicules (cloques) au centre sur le corps. Les autres signes à rechercher sont des ulcères dans la bouche, la gorge, le nez, les organes génitaux et des conjonctivites (yeux rouges et gonflés). Ces éruptions cutanées potentiellement mortelles sont souvent accompagnées de symptômes pseudo-grippaux. L’éruption peut évoluer vers une formation de cloques généralisée ou desquamation de la peau. Le plus grand risque pour la survenue de réactions cutanées graves survient dans les premières semaines de traitement.
Des réactions allergiques (hypersensibilité), telles que éruptions cutanées, démangeaisons, urticaire, œdème de Quincke avec gonflement des lèvres, des paupières, du visage, de la gorge et une difficulté soudaine à respirer ont également été rapportées sous carbamazépine, tout comme des cas d’hypersensibilité médicamenteuse (syndrome DRESS) pouvant être accompagnée de fièvre, éruption cutanée, inflammation des vaisseaux, atteinte des ganglions (augmentation du volume, pseudo-lymphome), douleur au niveau des articulations, modification des bilans sanguins, troubles au niveau du foie avec d’autres organes pouvant également être affectés (ex : poumons, reins, pancréas, myocarde, colon).
Si vous avez développé un Syndrome de Stevens-Johnson ou une Nécrolyse Epidermique Toxique ou une réaction allergique, y compris un syndrome DRESS, avec la carbamazépine, vous ne devrez jamais reprendre ce traitement ou un autre médicament contenant de la carbamazépine.
· Si la fréquence de vos crises d’épilepsie augmente ou si des crises d’un type différent apparaissent.
· Si vous avez des pensées autodestructrices ou suicidaires. Des pensées autodestructrices ou suicidaires ont été observées chez un petit nombre de personnes traitées par des antiépileptiques tels que la carbamazépine.
· En cas de sensations vertigineuses, somnolence, baisse de la tension artérielle, confusion lors du traitement par TEGRETOL et pouvant entrainer des chutes.
Analyses de sang
Votre médecin vous demandera de réaliser des prises de sang :
· avant le début du traitement,
· durant le premier mois de traitement,
· et pendant le traitement si des symptômes inhabituels apparaissent.
Autres mises en gardes
· Ce médicament contient moins de 1 mmol (23 mg) de sodium par dose, c’est-à-dire qu’il est essentiellement « sans sodium ».
· Ce médicament contient 175 mg de sorbitol par ml de suspension. Le sorbitol est une source de fructose. Si votre médecin vous a informé(e) que vous (ou votre enfant) présentez une intolérance à certains sucres ou si vous avez été diagnostiqué(e) avec une intolérance héréditaire au fructose (IHF), un trouble génétique rare caractérisé par l'incapacité à décomposer le fructose, parlez-en à votre médecin avant que vous (ou votre enfant) ne preniez ou ne receviez ce médicament.
Le sorbitol peut causer une gêne gastro-intestinale et un effet laxatif léger.
· Ce médicament contient du parahydroxybenzoate de méthyle et du parahydroxybenzoate de propyle et peut provoquer des réactions allergiques (éventuellement retardées).
· Ce médicament contient 25 mg de propylène glycol par ml de suspension. Si votre bébé a moins de 4 semaines, demandez à votre médecin ou à votre pharmacien avant de lui administrer ce médicament, en particulier si le bébé reçoit d’autres médicaments contenant du propylène glycol ou de l’alcool. Si votre bébé a moins de 4 semaines, il ne doit pas recevoir ce médicament, sauf en l'absence d'alternative thérapeutique disponible et après une évaluation approfondie par votre médecin. A cet âge, votre bébé pourrait ne pas être en mesure de métaboliser le propylène glycol, ce qui peut entrainer des effets indésirables graves, notamment des troubles de la fonction rénale et du foie. Le risque est augmenté si le bébé reçoit d'autres médicaments contenant du propylène glycol ou d'autres alcools. Si le traitement est néanmoins nécessaire, votre bébé sera surveillé afin de détecter ces effets indésirables. Consultez votre médecin si votre bébé est né prématurément (né avant terme).
Enfants
Si vous êtes un des parents ou tuteurs d’une fille ou adolescente traitée par carbamazépine, vous devez contacter immédiatement son médecin dès que votre enfant a ses premières règles (ménarche). Le médecin vous informera des risques pour un enfant à naître dus à l’exposition à la carbamazépine pendant la grossesse et de la nécessité d’utiliser une contraception hautement efficace (voir rubrique
« Grossesse et allaitement »).
Autres médicaments et TEGRETOL 20 mg/ml, suspension buvable
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
Vous ne devez jamais utiliser TEGRETOL 20 mg/ml, suspension buvable en même temps que :
· le cobicistat (utilisé dans le traitement de l’infection par le VIH (virus de l’immunodéficience humaine)),
· le dasabuvir (utilisé pour traiter le virus de l’hépatite C),
· le délamanid (antibiotique destiné au traitement de la tuberculose localisée au niveau du poumon),
· l’association grazoprevir et elbasvir (utilisée pour traiter le virus de l’hépatite C),
· l’isavuconazole (utilisé chez l’adulte pour traiter certaines infections à champignons),
· le lédipasvir (utilisé avec le sofosbuvir pour traiter le virus de l’hépatite C),
· la lurasidone (utilisée pour traiter les symptômes de la schizophrénie),
· la midostaurine (utilisée dans le traitement des leucémies aiguës myéloïdes et des mastocytoses),
· l’association ombitasvir + paritaprévir (utilisée avec le ritonavir pour traiter le virus de l’hépatite C),
· la rilpivirine (utilisée dans le traitement de l’infection par le VIH (virus de l’immunodéficience humaine)),
· le sofosbuvir (utilisé pour traiter le virus de l’hépatite C),
· le velpatasvir (utilisé pour traiter le virus de l’hépatite C),
· le voriconazole (utilisé pour traiter certaines infections à champignons).
Il est déconseillé d’utiliser TEGRETOL 20 mg/ml, suspension buvable en même temps que :
· l’abiratérone (utilisé chez les hommes adultes pour traiter le cancer de la prostate qui s’est disséminé dans d’autres parties du corps),
· l’apixaban (médicament anticoagulant),
· l’aprémilast (utilisé dans le traitement du psoriasis),
· l’aprépitant (utilisé dans la prévention des nausées et vomissements),
· la bédaquiline (antibiotique utilisé pour traiter la tuberculose),
· le bictégravir (utilisé dans le traitement de l’infection par le VIH (virus de l’immunodéficience humaine)),
· le bosentan (médicament utilisé pour traiter l’hypertension artérielle pulmonaire),
· la clozapine (médicament utilisé pour traiter certains troubles mentaux),
· le cyclophosphamide (médicament immunodépresseur),
· la cyprotérone (médicament hormonal qui s'oppose aux effets des hormones sexuelles mâles (androgènes), produites également en faible quantité par l'organisme féminin),
· le dabigatran (médicament anti-coagulant),
· le docétaxel (utilisé pour traiter certains cancers),
· le dolutégravir (utilisé dans le traitement de l’infection par le VIH (virus de l’immunodéficience humaine)),
· la dronédarone (médicament utilisé pour traiter des troubles des battements du coeur),
· l’érythromycine (antibiotique),
· les estroprogestatifs et progestatifs (médicaments contraceptifs utilisés pour éviter une grossesse ou pour traiter la ménopause),
· l’étoposide (utilisé pour traiter certains cancers),
· le fentanyl (médicament utilisé pour traiter la douleur),
· l’idélalisib (utilisé pour le traitement de deux cancers différents, la leucémie lymphoïde chronique et le lymphome folliculaire),
· les inhibiteurs de la 5-alpha réductase (utilisés dans la prise en charge des symptômes de l’hypertrophie bénigne de la prostate),
· les inhibiteurs des tyrosines kinases métabolisés (médicaments utilisés pour traiter certains cancers),
· l’irinotécan (utilisé dans le traitement de certains cancers du côlon ou du rectum),
· l’isoniazide (antibiotique),
· l’itraconazole (utilisé dans le traitement de certaines mycoses (infections dues à des champignons microscopiques)),
· l’ivacaftor (médicament utilisé pour traiter la mucoviscidose),
· le lithium (médicament utilisé pour traiter certains troubles mentaux),
· le macitentan (utilisé pour traiter l’hypertension artérielle pulmonaire),
· la miansérine (médicament utilisé dans la dépression),
· le millepertuis (plante naturelle utilisée pour traiter la dépression),
· le naloxégol (utilisé pour traiter les constipations induites par les opioïdes),
· la nimodipine (médicament utilisé pour traiter l’hypertension artérielle),
· l’olaparib (utilisé pour le traitement d’un certain type de cancer de l'ovaire),
· l’oxycodone (puissant traitement de la douleur à action centrale, du groupe des opioïdes),
· le paclitaxel (utilisé pour traiter certains types de cancers),
· le praziquantel (médicaments utilisés pour traiter une infection par un parasite ou un champignon),
· la quétiapine (utilisé pour traiter diverses maladies psychiatriques),
· la ranolazine (médicament utilisé pour traiter l’angor),
· le régorafenib (utilisé pour traiter certains types de cancers du côlon, du rectum, de l’estomac et de l’intestin),
· le rivaroxaban (médicament anticoagulant),
· le rolapitant (utilisé dans la prévention des nausées et vomissements),
· la sertraline (médicament utilisé dans la dépression),
· la simvastatine (médicament principalement utilisé pour traiter un excès de cholestérol),
· la télithromycine (médicament antibiotique),
· le ténofovir alafénamide (utilisé dans le traitement de l’infection par le VIH (virus de l’immunodéficience humaine)),
· le ticagrélor (agit en empêchant l'agrégation de certaines cellules sanguines (les plaquettes) pour diminuer le risque de formation d’un caillot sanguin),
· le tramadol et le dextropropoxyphène (médicaments utilisés pour traiter la douleur),
· l’ulipristal (médicament utilisé dans la contraception d’urgence et appelé « pilule du lendemain »),
· le vémurafénib (médicament utilisé pour traiter les mélanomes).
· les vinca-alcaloïdes cytotoxiques (utilisés pour traiter certains cancers),
· le vismodegib (utilisé pour traiter les patients adultes atteints d’un type de cancer de la peau).
Des précautions sont nécessaires avec d’autres médicaments pris en même temps que TEGRETOL.
Médicaments antiépileptiques : brivaracétam, progabide, acide valproïque, valnoctamide, valpromide, primidone.
Contraceptifs hormonaux, tels que pilules, patchs, injections ou implants.
TEGRETOL peut affecter le fonctionnement des contraceptifs hormonaux et les rendre moins efficaces dans la prévention de la grossesse. Adressez-vous à votre médecin, qui discutera avec vous du type de contraception le plus approprié à utiliser pendant que vous prenez TEGRETOL.
TEGRETOL 20 mg/ml, suspension buvable avec des aliments, boissons et de l’alcool
Si vous prenez ce médicament, il est déconseillé de consommer :
· du pamplemousse (jus et fruit),
· de l’alcool ou des boissons alcoolisées.
Grossesse et allaitement
Conseils importants destinés aux adolescentes et femmes susceptibles d’avoir des enfants et femmes enceintes
TEGRETOL peut provoquer des malformations congénitales et autres anomalies du développement. Si vous prenez TEGRETOL pendant la grossesse, votre bébé présente jusqu'à 3 fois plus de risques d'avoir une anomalie congénitale que ceux de femmes ne prenant pas de médicament antiépileptique. Des anomalies congénitales majeures, notamment une anomalie du tube neural (ouverture de la colonne vertébrale), une malformation du visage, telle que la fente de la lèvre supérieure et du palais, une malformation du crâne, une tête de plus petite taille (microcéphalie), des anomalies du cœur, une malformation du pénis impliquant l’orifice urinaire (hypospadias) et des anomalies au niveau des doigts ont été signalées. Si vous prenez de la carbamazépine pendant votre grossesse, votre enfant risque d'être plus petit et de peser moins que prévu à la naissance [né avec un petit poids pour l'âge gestationnel (PAG)]. Dans une étude menée auprès de femmes épileptiques, environ 13 enfants sur 100 nés de mères ayant pris de la carbamazépine pendant leur grossesse étaient plus petits et pesaient moins que prévu à la naissance, contre environ 11 enfants sur 100 nés de mères n'ayant pas pris de traitement antiépileptique pendant leur grossesse. Votre bébé doit être étroitement surveillé si vous avez pris TEGRETOL pendant la grossesse.
Des problèmes neuro-développementaux ont été rapportés chez des bébés nés de mères traitées par TEGRETOL pendant la grossesse. Certaines études ont montré que la carbamazépine affecte le développement neurologique des enfants exposés à la carbamazépine au cours de la grossesse, tandis que d’autres études n’ont pas retrouvé un tel effet. La possibilité d’un effet sur le développement neurologique ne peut être exclue.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
Avant le début du traitement par TEGRETOL, un test de grossesse doit être réalisé chez une femme susceptible d’avoir des enfants.
Si vous êtes une fille, adolescente ou femme susceptible d’avoir des enfants, avant l’initiation du traitement et une fois par an, votre médecin vérifiera que le traitement par TEGRETOL est la meilleure option pour vous et vous signerez avec lui une attestation d’information partagée.
Vous devez utiliser une contraception efficace pendant le traitement par TEGRETOL. TEGRETOL peut affecter la manière dont les contraceptifs hormonaux, tels que la pilule contraceptive, fonctionnent et les rendre moins efficaces pour éviter une grossesse. Adressez-vous à votre médecin qui discutera avec vous du type de contraception le plus approprié à utiliser pendant que vous prenez TEGRETOL. Si le traitement par TEGRETOL est interrompu, vous devez continuer à utiliser une contraception efficace pendant deux semaines supplémentaires après l’arrêt du traitement.
Si vous êtes une femme susceptible d’avoir des enfants et que vous planifiez une grossesse, n’interrompez pas votre contraception ou votre traitement antiépileptique avant d’en avoir parlé à votre médecin. Il prendra les mesures appropriées pour éviter d’exposer le bébé à la carbamazépine.
Si vous êtes ou pensez être enceinte, contactez immédiatement votre médecin. Vous ne devez pas interrompre brutalement votre traitement avant d’en avoir discuté avec votre médecin. L’arrêt de TEGRETOL sans avis médical risquerait de provoquer des crises d’épilepsie qui pourraient être dangereuses pour vous et votre enfant. Votre médecin pourrait décider de changer votre traitement.
Si vous prenez TEGRETOL pendant la grossesse, votre bébé risque également de présenter des saignements après l’accouchement. Votre médecin peut vous donner, à vous et à votre bébé, un médicament pour éviter cela.
TEGRETOL passe dans le lait maternel. Des troubles du foie pourraient survenir chez les nouveau-nés allaités. Il est déconseillé d’allaiter votre enfant durant le traitement.
Conduite de véhicules et utilisation de machines
Ce médicament peut provoquer des étourdissements, une somnolence, des sensations vertigineuses, un trouble de la coordination des mouvements, des troubles de la vue. Il est déconseillé de conduire si vous ressentez ces effets.
TEGRETOL 20 mg/ml, suspension buvable contient du sorbitol, du parahydroxybenzoate de méthyle, du parahydroxybenzoate de propyle et du propylèneglycol
3. COMMENT PRENDRE TEGRETOL 20 mg/ml, suspension buvable ?
Veillez à toujours prendre ce médicament en suivant exactement les indications de votre médecin. Vérifiez auprès de votre médecin ou pharmacien en cas de doute.
Posologie
· Respectez l’ordonnance de votre médecin. La dose à utiliser est déterminée par votre médecin. Elle est strictement individuelle.
· La seringue pour administration orale utilisée pour prélever la dose correcte de suspension est graduée en millilitres. La dose que votre médecin vous a prescrite doit être indiquée en millilitres (ml). Si votre prescription a été rédigée en milligrammes (mg), contactez votre médecin ou votre pharmacien.
· Suivez régulièrement le traitement. Ne le modifiez pas et ne l’arrêtez pas brutalement sans prévenir votre médecin auparavant.
Mode d’administration
Lisez attentivement les instructions suivantes afin de prélever et administrer la suspension buvable de TEGRETOL correctement.
SE CONFORMER STRICTEMENT A LA PRESCRIPTION MEDICALE.
A propos du système d’administration
|
|
Le système d’administration de TEGRETOL 20 mg/ml, suspension buvable se compose de cinq éléments : 1. Un flacon contenant le médicament avec un bouchon de sécurité enfant. Remettez toujours le bouchon en place après utilisation. |
|
|
2. Une seringue pour administration orale de 10 ml pour l’administration orale composée de 3 éléments : · 2a. Un étui protecteur, · 2b. Un adaptateur que vous devez enfoncer dans le col du flacon. L’adaptateur doit toujours rester en place. Il permet d’insérer la seringue pour administration orale dans le flacon et d’essuyer la partie externe de la seringue pour administration orale quand vous l’enlevez du flacon, · 2c. Une seringue pour administration orale de 10 ml à introduire dans l’adaptateur pour prélever dans le flacon la dose prescrite de médicament. |
Insertion de l’adaptateur dans le flacon
|
|
3. Retirez le bouchon de sécurité enfant en appuyant fermement et en le tournant dans le sens inverse des aiguilles d’une montre (comme indiqué sur le dessus du bouchon). 4. Retirez la seringue pour administration orale et l’adaptateur de l’étui protecteur. |
|
|
5. Placez le flacon ouvert sur une table et enfoncez fortement l’adaptateur dans le col du flacon aussi loin que possible. Note : Il se peut que vous n’arriviez pas à enfoncer complètement l’adaptateur mais celui-ci se trouvera définitivement enfoncé dans le flacon lorsque vous revisserez le bouchon. |
6. Refermez le flacon à l’aide du bouchon.
Pour délivrer une dose, veuillez suivre les instructions mentionnées dans « Préparation d’une dose de TEGRETOL 20 mg/ml suspension buvable ».
Préparation d’une dose de TEGRETOL 20 mg/ml suspension buvable
|
|
7. Secouez le flacon pendant au moins 10 secondes. Préparez la dose immédiatement après. 8. Ouvrez le flacon en enfonçant et tournant le bouchon de sécurité enfant dans le sens inverse des aiguilles d’une montre (remarque : remettez toujours le bouchon en place après utilisation). 9. Vérifiez que le piston est complètement enfoncé dans le corps de la seringue pour administration orale. 10. Insérez la seringue pour administration orale dans le flacon de façon légèrement inclinée et enfoncez-la jusqu’au fond. 11. Remontez le piston jusqu’à mi-hauteur de la seringue pour administration orale puis repoussez-le rapidement afin d’éliminer les grosses bulles d’air qui auraient pu se trouver aspirées. Note : En cas de difficultés à faire glisser le piston, évitez de positionner la seringue pour administration orale de façon trop verticale dans le flacon.
12. Prélevez la dose prescrite : tirez lentement le piston jusqu’à ce que la graduation indiquant le volume à prélever arrive au niveau du bord supérieur du corps de la seringue pour administration orale. Note : Si la dose prescrite est supérieure à 10 ml, vous devrez recharger la seringue pour administration orale jusqu’à obtention de la dose totale prescrite.
13. Retirez doucement la seringue pour administration orale du flacon sans toucher le piston. 14. La dose de TEGRETOL 20 mg/ml suspension buvable doit être mélangée dans un petit verre d’eau juste avant son administration. Videz le contenu de la seringue pour administration orale en poussant fermement le piston vers le bas. Agitez le mélange et buvez-le immédiatement. 15. Remettez le bouchon de sécurité en place après utilisation. 16. Nettoyage : après utilisation, essuyez l’extérieur de la seringue pour administration orale avec un tissu propre et humide. 17. Replacez la seringue pour administration orale dans l’étui protecteur. 18. Protégez la seringue pour administration orale de la lumière directe du soleil. |
Note : Un nouvel adaptateur et une nouvelle seringue pour administration orale doivent être utilisés chaque fois que vous commencez un nouveau flacon.
Fréquence d’administration
La dose est à répartir en plusieurs prises (2-3 prises) par jour, pendant ou après les repas.
SE CONFORMER STRICTEMENT A LA PRESCRIPTION MEDICALE.
Durée du traitement
Vous devez impérativement respecter la dose et la durée du traitement prescrite, en particulier vous ne devez pas interrompre le traitement sans demander l’avis de votre médecin.
Si vous avez pris plus de TEGRETOL 20 mg/ml, suspension buvable que vous n’auriez dû
Consultez immédiatement un médecin.
Si vous oubliez de prendre TEGRETOL 20 mg/ml, suspension buvable
Si vous vous en apercevez peu de temps après l’heure prévue, prenez la dose habituelle.
Si vous vous en apercevez peu de temps avant la prise suivante, ne doublez pas la dose. Ensuite, continuez comme précédemment. Si vous avez oublié de prendre plusieurs doses, consultez immédiatement votre médecin.
Si vous arrêtez de prendre TEGRETOL 20 mg/ml, suspension buvable
L’arrêt du traitement doit se faire de manière progressive. En effet, l’arrêt brutal du traitement (ou la diminution importante des doses) peut entraîner la réapparition des crises.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Comme tous les médicaments, ce médicament peut provoquer des effets indésirables, mais ils ne surviennent pas systématiquement chez tout le monde.
Effets très fréquents ou fréquents survenant dans des situations particulières :
Ces effets surviennent surtout au début du traitement, avec une dose initiale trop élevée ou lorsque le médicament est utilisé chez une personne âgée de plus de 65 ans.
· des sensations vertigineuses, des maux de tête, une difficulté pour coordonner ses mouvements, une somnolence, de la fatigue, des troubles de la vue (vision double, vision floue), une confusion (conscience perturbée, idées ralenties, désorientation), une agitation.
· des nausées, des vomissements, des diarrhées, une constipation, une perte de l’appétit (anorexie), une sécheresse de la bouche.
· des réactions allergiques sur la peau (boutons, démangeaisons, rougeurs ).
Les effets indésirables suivants sont très fréquents (plus de 1 personne sur 10) :
· sensations vertigineuses, difficulté pour coordonner ses mouvements, somnolence, fatigue.
· réactions allergiques (démangeaisons, rougeurs, boutons, gonflement du visage et du cou, difficulté à respirer ) et éruptions sur la peau, urticaire.
· diminution du nombre des globules blancs.
· augmentation de gammaglutamyltranspeptidase ou gamma-GT (enzyme du foie).
· nausées, vomissements.
Les effets indésirables suivants sont fréquents (de 1 à 10 personnes sur 100) :
· maux de tête, vision double, vision floue.
· diminution du nombre des plaquettes, augmentation du nombre de certains globules blancs (les éosinophiles).
· augmentation des phosphatases alcalines (enzymes du foie).
· sécheresse de la bouche.
· prise de poids.
· diminution du sodium sanguin.
· œdème.
· rétention d’eau.
Les effets indésirables suivants sont peu fréquents (de 1 à 10 personnes sur 1 000) :
· tremblements (contraction anormalement prolongée d’un groupe de muscles et mouvements involontaires des membres), mouvements anormaux (des membres, de la face et de la bouche), nystagmus (mouvements anormaux des yeux).
· peau qui pèle (dermatite exfoliatrice).
· augmentation des transaminases (enzymes du foie).
· diarrhées, constipation.
Les effets indésirables suivants sont rares (de 1 à 10 personnes sur 10 000) :
· troubles des mouvements des yeux, troubles de la parole, agitation, confusion (conscience perturbée, idées ralenties, désorientation)
· des démangeaisons, syndrome lupique (maladie auto-immune chronique fréquemment caractérisée par une rougeur du visage et des douleurs articulaires).
· inflammation du foie (hépatite).
· douleurs au ventre.
· augmentation du nombre des globules blancs, augmentation de la taille des ganglions, diminution du taux de vitamine B (carence en acide folique).
· diminution de l’appétit.
· troubles du rythme cardiaque, augmentation ou diminution importante de la tension artérielle, formation de caillots dans le sang.
· réactions allergiques (hypersensibilité) parfois graves qui peuvent associer principalement une fièvre, une éruption cutanée, une rougeur au niveau des yeux (conjonctivite), une inflammation des vaisseaux sanguins (vascularite), une augmentation de taille de plusieurs ganglions, des douleurs des articulations, une baisse des globules blancs, une augmentation de certains globules blancs, une augmentation de taille du foie et de la rate et une inflammation du foie (hépatite). De façon exceptionnelle, l'atteinte peut concerner le rein, le pancréas, le poumon, le colon, le myocarde.
Les effets indésirables suivants sont très rares (moins de 1 personne sur 10 000) :
· réactions allergiques graves de la peau (par exemple, syndrome de Lyell), réactions de la peau à la lumière, bleus, chute des cheveux
· réaction allergique au niveau des poumons caractérisée par de la fièvre, une difficulté à respirer (essoufflement) et une infection pulmonaire.
· diminution du nombre de globules rouges (anémie), diminution voire disparition des globules rouges, des globules blancs et/ou des plaquettes (aplasie médullaire ou pancytopénie), diminution importante du nombre d’un certain type de globules blancs (agranulocytose), augmentation dans le sang de certains composants nocifs (porphyrie) pouvant provoquer des réactions sur la peau
· inflammation de la bouche et de la langue.
· inflammation du pancréas (pancréatite).
· inflammation de l’enveloppe entourant le cerveau (méningite aseptique), ensemble d’effets appelés syndrome malin des neuroleptiques (caractérisé par la présence de certains ou l'ensemble des symptômes suivants: fièvre, rigidité, douleurs musculaires, secousses musculaires, urines foncées, confusion).
· réactions allergiques (démangeaisons, rougeurs, boutons, œdème de Quincke avec gonflement du visage et du cou et difficulté à respirer ).
· ralentissement ou accélération du rythme cardiaque, troubles du rythme cardiaque pouvant provoquer parfois un malaise avec perte de connaissance, formation de caillots dans les vaisseaux sanguins pouvant être localisés au niveau des poumons (embolie pulmonaire).
· diminution du taux des hormones thyroïdiennes (T3– T4).
· difficulté pour aller uriner, inflammation des reins, mauvais fonctionnement des reins (insuffisance rénale, protéinurie, élévation de l’urée et de la créatinine).
· troubles du goût, troubles de l’audition.
· rougeurs au niveau des yeux (conjonctivites).
· douleurs articulaires et musculaires, crampes, troubles de la formation des os pouvant provoquer une fragilisation des os.
· diminution du taux d’un certain type d’anticorps (hypogammaglobulinémie).
· écoulement de lait par le mamelon en dehors de l'allaitement, développement de la poitrine chez l’homme.
· diminution des concentrations de calcium et de dérivés de la vitamine D dans le sang.
· trouble sexuel (y compris des troubles de l’érection).
Les effets indésirables suivants ont été rapportés (fréquence indéterminée) :
· infection causée par la réactivation d’un virus de type herpès.
· taux élevés d’ammoniaque dans le sang (hyperammoniémie). Les symptômes de l’hyperammoniémie peuvent être les suivants : irritabilité, confusion, vomissements, perte d’appétit et somnolence.
· effet tranquillisant, troubles de la mémoire.
· inflammation du colon.
· chute d’ongles.
· fractures osseuses, diminution de la densité osseuse.
· malformations et autres anomalies du développement de l’enfant à naître.
· chute provoquée par des sensations vertigineuses, une somnolence, une baisse de la tension artérielle, une confusion.
L’apparition d’effets indésirables au niveau du sang, du foie, de la peau, du cœur et des vaisseaux, ainsi que des réactions allergiques graves nécessite la CONSULTATION IMMEDIATE DE VOTRE MEDECIN qui pourra juger de l’arrêt du traitement et envisager un autre traitement.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: https://signalement.social-sante.gouv.fr/
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER TEGRETOL 20 mg/ml, suspension buvable ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur la boîte. La date de péremption fait référence au dernier jour de ce mois.
A conserver à une température ne dépassant pas 30°C.
Conserver le flacon dans l’emballage extérieur, à l’abri de la lumière.
N’utilisez pas ce médicament si vous remarquez des signes visibles de détérioration.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient TEGRETOL 20 mg/mL, suspension buvable
· La substance active est :
Carbamazépine...................................................................................................................... 2,00 g
pour 100 ml de suspension buvable.
1 ml de suspension correspond à 20 mg de carbamazépine.
· Les autres composants sont :
Stéarate de macrogol 400, cellulose microcristalline, sorbitol à 70 pour cent, parahydroxybenzoate de méthyle, parahydroxybenzoate de propyle, saccharine sodique, hydroxyéthylcellulose, acide sorbique, propylèneglycol, arôme caramel 52 929 A, eau purifiée.
Qu’est-ce que TEGRETOL 20 mg/ml, suspension buvable et contenu de l’emballage extérieur
Ce médicament se présente sous forme de suspension buvable en flacon de 150 ml avec une seringue pour administration orale.
Titulaire de l’autorisation de mise sur le marché
Novartis Pharma S.A.S.
8-10 RUE HENRI SAINTE-CLAIRE DEVILLE
92500 RueiL-Malmaison
Exploitant de l’autorisation de mise sur le marché
Novartis Pharma S.A.S.
8-10 RUE HENRI SAINTE-CLAIRE DEVILLE
92500 RueiL-Malmaison
Novartis farmaceutica, S.A.
gran via de les corts catalanes, 764
08013 BARCELONE
ESPAGNE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
Attestation d’information partagée
Une attestation d’information partagée est signée par le médecin et la patiente susceptible d’avoir des enfants, lors de l’initiation du traitement et une fois par an.