Dernière mise à jour le 30/03/2026
PROPIONATE DE FLUTICASONE/SALMETEROL BGR 125 microgrammes/25 microgrammes/dose, suspension pour inhalation en flacon pressurisé
Indications thérapeutiques
PROPIONATE DE FLUTICASONE/SALMETEROL BGR est un médicament contenant deux principes actifs, le salmétérol et le propionate de fluticasone :
· Le salmétérol est un bronchodilatateur de longue durée d’action. Les bronchodilatateurs aident à garder les bronches ouvertes. Cela permet de faciliter l’entrée et la sortie de l’air dans les poumons. L’effet dure au moins 12 heures.
· Le propionate de fluticasone est un corticoïde qui diminue l’inflammation et l’irritation dans les poumons.
Votre médecin vous a prescrit ce médicament pour aider à prévenir certains troubles respiratoires tels que l’asthme.
Vous devez utiliser PROPIONATE DE FLUTICASONE/SALMETEROL BGR tous les jours comme indiqué par votre médecin. Cela permettra de contrôler correctement votre asthme.
PROPIONATE DE FLUTICASONE/SALMETEROL BGR permet d’éviter la survenue d’essoufflement et de sifflement. Cependant, PROPIONATE DE FLUTICASONE/SALMETEROL BGR ne doit pas être utilisé lorsque vous avez une crise soudaine d’essoufflement ou de sifflement. Dans ces cas, vous devez utiliser votre médicament bronchodilatateur dit « de secours » d’action rapide et de courte durée, comme le salbutamol. Vous devez toujours avoir sur vous votre inhalateur dit « de secours » d’action rapide et de courte durée.
Présentations
> 1 flacon(s) pressurisé(s) aluminium de 120 doses avec valve(s) doseuse(s) avec embout(s) buccal(aux)
Code CIP : 34009 301 915 4 5
Déclaration de commercialisation : 05/03/2020
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 17,64 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 18,66 €
- Taux de remboursement :65 %
Service médical rendu (SMR)
Amélioration du service médical rendu (ASMR)
Ce médicament étant un générique, l'ASMR n'a pas été évalué par la commission de la transparence (CT), il est possible de se référer à la /aux spécialité(s) de référence du groupe générique auquel appartient ce médicament (cliquez ici pour aller à la rubrique des groupes génériques)
ANSM - Mis à jour le : 25/02/2025
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Salmétérol............................................................................................................ 25 microgrammes
Sous forme de xinafoate de salmétérol
Propionate de fluticasone.................................................................................... 125 microgrammes
Par dose émise par la valve doseuse.
Ce qui correspond à une dose délivrée de 21 microgrammes de salmétérol et 110 microgrammes de propionate de fluticasone.
Pour la liste complète des excipients, voir rubrique 6.1.
Suspension pour inhalation en flacon pressurisé.
La cartouche contient une suspension blanche à blanchâtre.
Les cartouches sont placées dans un applicateur en plastique violet comprenant un embout buccal et un capuchon de protection.
4.1. Indications thérapeutiques
· chez des patients insuffisamment contrôlés par une corticothérapie inhalée et la prise d’un bronchodilatateur β2 agoniste de courte durée d’action par voie inhalée « à la demande » ;
ou
· chez des patients contrôlés par l’administration d’une corticothérapie inhalée associée à un traitement continu par β2 agoniste de longue durée d’action par voie inhalée.
4.2. Posologie et mode d'administration
Voie d’administration : voie inhalée.
Il conviendra d’informer le patient que pour observer un effet optimal du traitement, PROPIONATE DE FLUTICASONE/SALMETEROL BGR doit être administré quotidiennement même lorsque les symptômes sont améliorés.
Le médecin devra vérifier régulièrement que le dosage prescrit de PROPIONATE DE FLUTICASONE/SALMETEROL BGR est bien adapté à l’état clinique du patient. Il ne sera modifié que sur avis médical. Il convient de toujours rechercher la posologie minimale efficace. Lorsque les symptômes sont contrôlés par la plus faible posologie recommandée en deux prises par jour, l’administration d’un corticoïde inhalé seul sera alors envisagée. Il pourra être également envisagé de réduire la posologie de PROPIONATE DE FLUTICASONE/SALMETEROL BGR à une prise par jour, si le médecin estime nécessaire de maintenir un traitement par β2 mimétique de longue durée d’action pour le contrôle des symptômes. L’horaire de la prise de PROPIONATE DE FLUTICASONE/SALMETEROL BGR sera alors fonction de la fréquence d’apparition des symptômes. Si la prédominance des symptômes est nocturne, PROPIONATE DE FLUTICASONE/SALMETEROL BGR sera administré le soir ; si elle est diurne, PROPIONATE DE FLUTICASONE/SALMETEROL BGR sera administré le matin.
Le dosage de PROPIONATE DE FLUTICASONE/SALMETEROL BGR qui sera prescrit au patient devra correspondre à la dose de propionate de fluticasone adaptée à la sévérité de son asthme. Il convient de souligner que le dosage propionate de fluticasone/salmétérol 50 microgrammes/25 microgrammes/dose, n’est pas adapté au traitement de l’asthme sévère de l’adulte et de l’enfant. Si les dosages disponibles de cette association fixe ne répondent pas aux nécessités pour ajuster les posologies en fonction de l’état du patient, les β2 agonistes et/ou corticoïdes devront être prescrits individuellement.
Posologie préconisée
Adultes et adolescents de 12 ans et plus :
Deux inhalations de 50 microgrammes de propionate de fluticasone et 25 microgrammes de salmétérol 2 fois par jour ;
ou
Deux inhalations de 125 microgrammes de propionate de fluticasone et 25 microgrammes de salmétérol 2 fois par jour ;
ou
Deux inhalations de 250 microgrammes de propionate de fluticasone et 25 microgrammes de salmétérol 2 fois par jour.
PROPIONATE DE FLUTICASONE/SALMETEROL BGR peut être envisagé en traitement d’initiation pendant une courte période d’essai chez des adultes et adolescents ayant un asthme persistant modéré (défini par l’existence d’une symptomatologie diurne, l’utilisation quotidienne d’un bronchodilatateur de courte durée d’action en traitement symptomatique de secours et une obstruction bronchique modérée à sévère) et chez qui il apparaît essentiel d’obtenir un contrôle rapide de l’asthme. Dans ces cas, la dose initiale recommandée est de deux inhalations de 25 microgrammes de salmétérol et 50 microgrammes de propionate de fluticasone, deux fois par jour. Lorsque le contrôle de l’asthme est obtenu, le traitement doit être réévalué afin d’envisager la réduction du traitement à un corticoïde inhalé seul. Il est important que les patients soient suivis régulièrement lors de la période de réduction du traitement.
Il n’a pas été établi de bénéfice évident de PROPIONATE DE FLUTICASONE/SALMETEROL BGR utilisé en traitement d’initiation par rapport à un traitement inhalé par propionate de fluticasone seul, lorsque 1 à 2 des critères de sévérité évoqués ci-dessus ne sont pas présents. Dans la majorité des cas, le traitement de première intention demeure l’administration de corticoïdes inhalés seuls. PROPIONATE DE FLUTICASONE/SALMETEROL BGR n’est pas destiné au traitement de première intention de l’asthme léger. Le dosage 50 microgrammes/25 microgrammes de propionate de fluticasone/salmétérol ne convient pas aux adultes et aux enfants atteints d’asthme sévère ; la dose appropriée de corticoïdes inhalés devra être ajustée individuellement avant d’instaurer un traitement par une association fixe chez des patients atteints d’asthme sévère.
Population pédiatrique
Enfants de 4 ans et plus
Deux inhalations de 50 microgrammes de propionate de fluticasone et 25 microgrammes de salmétérol 2 fois par jour.
Chez l’enfant, la dose maximale de propionate de fluticasone par voie inhalée qui est préconisée est de 100 microgrammes, 2 fois par jour.
La sécurité et l’efficacité de PROPIONATE DE FLUTICASONE/SALMETEROL BGR chez l’enfant de moins de 4 ans n’ont pas été établies (voir rubrique 5.1).
Les enfants de moins de 12 ans peuvent avoir des difficultés à coordonner le déclenchement du dispositif d’inhalation avec leur inspiration. L’utilisation d’une chambre d’inhalation avec PROPIONATE DE FLUTICASONE/SALMETEROL BGR suspension pour inhalation en flacon pressurisé est recommandée chez les patients ayant ou susceptible d’avoir des difficultés à coordonner leur inspiration avec le déclenchement du dispositif d’inhalation. Une étude clinique récente a montré que les patients pédiatriques ayant utilisé une chambre d’inhalation ont obtenu une exposition similaire à celle d’adultes n’ayant pas utilisé de chambre d’inhalation et à celle de patients pédiatriques ayant utilisé un dispositif pour poudre pour inhalation, ce qui confirme que les chambres $d’inhalation compensent une mauvaise technique d’inhalation (voir rubrique 5.2).
Il est possible d’utiliser une chambre d’inhalation Volumatic (selon les recommandations nationales).
Les patients devront être informés des modalités d’utilisation et d’entretien de leur dispositif d’inhalation et de leur chambre d’inhalation. Il conviendra également de vérifier que le patient utilise convenablement la chambre d’inhalation afin que le produit soit délivré de façon optimale jusqu’au poumon. Dans la mesure du possible, les patients doivent continuer à utiliser le même type de chambre d’inhalation, le passage d’une chambre d’inhalation à une autre pouvant faire varier la dose de produit inhalé (voir rubrique 4.4).
Lors de l’introduction ou du changement de chambre d’inhalation, il convient de toujours rechercher la dose minimale efficace.
Populations à risque
Il n’y a pas lieu d’ajuster les doses chez les sujets âgés ou atteints d’insuffisance rénale. Aucune donnée n’est disponible concernant l’utilisation de PROPIONATE DE FLUTICASONE/SALMETEROL BGR chez les patients atteints d’insuffisance hépatique.
Mode d’administration
Instructions pour l’utilisation
Il convient d’informer les patients sur les modalités de fonctionnement de l’aérosol doseur (voir notice).
Durant l’inhalation, le patient doit, de préférence, se tenir assis ou debout. L’aérosol a été conçu pour un usage en position verticale.
Vérification du fonctionnement du dispositif
Avant la première utilisation, afin de vérifier le bon fonctionnement du dispositif, libérer des bouffées de produit dans l’air jusqu’à ce que le compteur indique 120 doses. Pour cela, après avoir retiré le capuchon de l’embout buccal en exerçant une pression de chaque côté, bien agiter l’inhalateur, tenir le dispositif entre les doigts en positionnant le pouce à la base du dispositif sous l’embout buccal, puis presser sur la cartouche. Bien agiter le dispositif juste avant de l’activer pour libérer chaque bouffée. Si le dispositif n’a pas été utilisé depuis une semaine ou plus, le patient doit bien agiter l’inhalateur après avoir retiré le capuchon de l’embout buccal et doit libérer deux bouffées de produit dans l’air. Le compteur de doses est décompté d’une unité à chaque fois que le dispositif est déclenché.
Utilisation de l’aérosol :
1. Le patient doit retirer le capuchon de l’embout buccal en exerçant une pression de chaque coté.
2. Le patient devra vérifier qu’il n’existe pas de corps étranger à l’intérieur ou à l’extérieur du dispositif et notamment de l’embout buccal, pour s’assurer qu’il est propre.
3. Le patient doit bien agiter l’aérosol pour éliminer tout corps étranger et assurer le mélange des composants de la suspension dans le flacon.
4. Le patient doit tenir l’aérosol bien droit entre les doigts et le pouce avec son pouce à la base, sous l’embout buccal.
5. Le patient doit expirer autant que possible puis placer l’embout buccal dans sa bouche entre les dents et fermer les lèvres autour. Signaler au patient qu’il ne doit pas mordre l’embout buccal.
6. Juste après avoir commencé à inspirer par la bouche à travers le dispositif, le patient doit fermement appuyer vers le bas sur le haut de l’aérosol doseur pour libérer le produit, tout en inspirant régulièrement et profondément.
7. Pendant qu’il retient sa respiration, le patient retirera l’inhalateur de sa bouche. Le patient retiendra sa respiration autant que cela lui est possible.
8. Si le patient doit prendre une seconde inhalation, il devra garder l’aérosol-doseur bien droit et attendre environ 30 secondes avant de répéter les étapes 3 à 7.
9. Le patient devra replacer le capuchon sur l’embout buccal immédiatement après en appuyant fermement sur le capuchon en veillant à ce qu’il soit placé dans la position correcte. Il n’y a pas besoin d’exercer une force importante pour replacer le capuchon sur l’embout buccal, un simple « clic » suffit à s’assurer de la fermeture de l’embout buccal par le capuchon.
IMPORTANT
Les étapes 5, 6 et 7 ne devront pas être réalisées dans la précipitation. Il est important que le patient débute une respiration aussi lente que possible avant de déclencher son dispositif. Le patient devra s’entraîner les premières fois devant un miroir. S’il voit un peu de « fumée » sortir du haut de l’aérosol doseur ou à la commissure des lèvres, il doit alors recommencer à partir de l’étape 3.
Les patients devront se rincer la bouche avec de l’eau en la recrachant et/ou se brosser les dents après chaque utilisation de PROPIONATE DE FLUTICASONE/SALMETEROL BGR afin de réduire les risques de candidose buccale et pharyngée ainsi que l’apparition d’une raucité de la voix.
Les patients doivent penser au remplacement de l’aérosol doseur lorsque le compteur de doses affiche le nombre 020. Lorsque toutes les doses disponibles dans le dispositif auront été délivrées, le compteur affiche 000. L’aérosol doseur devra être remplacé lorsque le compteur affiche 000.
Les patients ne doivent jamais essayer de modifier les chiffres sur le compteur ou de détacher celui-ci de la cartouche métallique. Le compteur ne peut pas être remis à zéro et reste en permanence attaché à la cartouche.
Nettoyage (également détaillé dans la notice d’information à l’utilisateur) :
Le dispositif doit être nettoyé au moins une fois par semaine.
1. Retirer le capuchon de l’embout buccal.
2. Ne pas retirer la cartouche de son adaptateur en plastique.
3. Essuyer l’intérieur et l’extérieur de l’embout buccal et de l’adaptateur en plastique avec un tissu ou un mouchoir propre et sec.
4. Remettre le capuchon de l’embout buccal en veillant à ce qu’il soit placé correctement dans le bon sens. Il n’y a pas besoin d’exercer une force importante pour replacer le capuchon sur l’embout buccal, un simple « clic » suffit à s’assurer de la fermeture de l’embout buccal par le capuchon.
NE PAS METTRE LA CARTOUCHE EN METAL DANS L’EAU.
Hypersensibilité aux substances actives ou à l’un des excipients mentionnés à la rubrique 6.1.
4.4. Mises en garde spéciales et précautions d'emploi
PROPIONATE DE FLUTICASONE/SALMETEROL BGR n'est pas adapté au traitement des crises d'asthme et des épisodes de dyspnée paroxystique. Dans ces situations, le patient devra avoir recours à un bronchodilatateur à action rapide et de courte durée pour traiter les symptômes aigus. Le patient sera informé qu'il doit ainsi avoir en permanence à sa disposition un médicament bronchodilatateur à action rapide et de courte durée destiné à être utilisé en cas de crise d'asthme.
Le traitement par PROPIONATE DE FLUTICASONE/SALMETEROL BGR ne doit pas être initié pendant une phase d’exacerbation, ni en cas d’aggravation significative ou de détérioration aiguë de l’asthme.
Des évènements indésirables graves liés à l’asthme et des exacerbations peuvent survenir lors du traitement par PROPIONATE DE FLUTICASONE/SALMETEROL BGR. Il convient d’informer les patients que si les symptômes de l’asthme persistent ou s’aggravent au cours du traitement par PROPIONATE DE FLUTICASONE/SALMETEROL BGR, ils doivent continuer leur traitement mais prendre avis auprès de leur médecin.
Une augmentation de la consommation de médicaments bronchodilatateurs à action rapide et de courte durée (dit « médicaments de secours ») ou une diminution de la réponse à ceux-ci est le signe d'une déstabilisation de la maladie. Dans ce cas, le patient devra consulter son médecin.
Une détérioration plus ou moins rapide du contrôle des symptômes doit faire craindre une évolution vers un asthme aigu grave pouvant mettre en jeu le pronostic vital et, par conséquent, nécessite une consultation médicale urgente. Il conviendra alors d'envisager une augmentation de la corticothérapie.
Dès que les symptômes de l’asthme sont contrôlés, une diminution progressive de la dose de propionate de fluticasone/salmétérol doit être envisagée. Il est important que les patients soient suivis régulièrement lors de la période de réduction du traitement. La dose minimale efficace de propionate de fluticasone/salmétérol doit être utilisée (voir rubrique 4.2).
Le traitement par PROPIONATE DE FLUTICASONE/SALMETEROL BGR ne devra pas être interrompu brusquement en raison du risque d'exacerbation. Le traitement ne devra être diminué que sous la supervision d'un médecin.
Comme les autres corticoïdes destinés à être administrés par voie inhalée, PROPIONATE DE FLUTICASONE/SALMETEROL BGR doit être utilisé avec précaution chez les patients atteints de tuberculose pulmonaire active ou quiescente, d’infections fongiques et virales ou d'autres infections des voies respiratoires. Un traitement approprié doit être instauré rapidement si nécessaire.
Rarement, PROPIONATE DE FLUTICASONE/SALMETEROL BGR peut entraîner des troubles du rythme cardiaque tels que tachycardie supraventriculaire, extrasystoles et fibrillation auriculaire, ainsi qu’une baisse modérée et transitoire de la kaliémie à des doses thérapeutiques élevées. PROPIONATE DE FLUTICASONE/SALMETEROL BGR doit être utilisé avec prudence en cas de pathologies cardiovasculaires sévères, de troubles du rythme cardiaque et chez les patients présentant un diabète, une hyperthyroïdie, une hypokaliémie non corrigée ou à risque d’hypokaliémie.
Des augmentations de la glycémie ont été très rarement rapportées (voir rubrique 4.8). Ceci doit être pris en compte lors de la prescription à des patients diabétiques.
Comme avec d’autres traitements inhalés, un bronchospasme paradoxal peut survenir, caractérisé par une augmentation des sifflements et un essoufflement survenant immédiatement après l’administration. Le bronchospasme paradoxal doit être traité immédiatement avec un bronchodilatateur d’action rapide et de courte durée. Il convient alors de cesser toute administration de PROPIONATE DE FLUTICASONE/SALMETEROL BGR, d'évaluer l'état du patient et au besoin, d’instaurer un traitement alternatif.
Les effets indésirables pharmacologiques des traitements β2 agonistes, tels que tremblements, palpitations et maux de tête ont été rapportés, mais ces manifestations sont généralement transitoires, passagères et s'atténuent au cours d'un traitement régulier.
La corticothérapie inhalée peut entraîner des effets systémiques, en particulier lors de traitements à fortes doses au long cours. La survenue de ces effets reste cependant moins probable qu'au cours d'une corticothérapie orale. Il peut être observé un syndrome de Cushing, un tableau cushingoïde, une inhibition de la fonction surrénalienne, une diminution de la densité minérale osseuse, une cataracte et un glaucome et, plus rarement, divers effets psychologiques ou comportementaux incluant hyperactivité psychomotrice, troubles du sommeil, anxiété, dépression ou agressivité (en particulier chez l’enfant) (voir la sous-rubrique « Population pédiatrique » ci-dessous pour plus d’informations sur les effets systémiques des corticoïdes inhalés chez les enfants et les adolescents). En conséquence, le patient sera suivi régulièrement et la posologie minimale efficace devra toujours être recherchée.
L’administration prolongée de doses élevées de corticoïdes par voie inhalée peut provoquer une inhibition de la fonction surrénalienne et une insuffisance surrénalienne aiguë. Des cas d’inhibition de la fonction surrénalienne et d’insuffisance surrénale aiguë ont également été très rarement décrits avec des doses de propionate de fluticasone comprises entre 500 et 1000 microgrammes. Les crises d’insuffisance surrénalienne peuvent être déclenchées par un traumatisme, une intervention chirurgicale, une infection ou toute diminution rapide de la posologie. Le tableau clinique est généralement atypique pouvant comprendre anorexie, douleur abdominale, perte de poids, fatigue, maux de tête, nausées, vomissements, hypotension, troubles de la conscience, hypoglycémie et convulsions. En cas de stress ou lorsqu'une intervention chirurgicale est prévue, une corticothérapie de supplémentation par voie générale peut être nécessaire.
Le propionate de fluticasone et le salmétérol sont essentiellement absorbés par voie pulmonaire. L’utilisation d’une chambre d’inhalation associée à l’aérosol-doseur peut augmenter la dose de produit délivrée au poumon pouvant ainsi augmenter le risque de survenue d’effets indésirables systémiques.
L'administration de propionate de fluticasone par voie inhalée favorise la diminution du recours aux corticoïdes oraux pour traiter l'asthme, mais elle ne prévient pas le risque d'apparition d'une insuffisance surrénalienne lors du sevrage des patients traités au long cours par une corticothérapie orale. Par conséquent, ces patients doivent être traités avec précaution et leur fonction cortico-surrénalienne régulièrement surveillée. Ce risque existe également chez les patients ayant reçu de fortes doses de corticoïdes en urgence. Le risque de persistance d'une inhibition des fonctions surrénaliennes doit rester présent à l'esprit dans les situations d'urgence et/ou susceptibles de déclencher un état de stress. Une corticothérapie substitutive adaptée devra être envisagée. Un avis spécialisé peut être requis.
Le ritonavir peut augmenter considérablement les concentrations plasmatiques de propionate de fluticasone. Par conséquent, à moins que le bénéfice attendu pour le patient ne l’emporte sur le risque d’effets systémiques de la corticothérapie, il convient d’éviter de les administrer de façon concomitante. Le risque d’effets indésirables systémiques de la corticothérapie est également augmenté en cas d’administration concomitante de propionate de fluticasone avec d’autres inhibiteurs puissants du cytochrome P450 3A4 (voir rubrique 4.5).
Une augmentation des cas d’infections respiratoires basses (en particulier pneumonie et bronchite) a été observée dans une étude menée sur 3 ans (étude TORCH) chez des patients atteints de Broncho-Pneumopathie Chronique Obstructive (BPCO) traités par l’association fixe salmétérol et propionate de fluticasone administrée via le dispositif pour poudre pour inhalation, par rapport à ceux recevant du placebo (voir rubrique 4.8). Dans cette étude, le risque de développer une pneumonie, indépendamment du traitement, était le plus élevé chez les patients âgés, les patients ayant un faible indice de masse corporelle (< 25 kg/m2) et ceux ayant une maladie très sévère (VEMS < 30 % de la valeur théorique). Les médecins doivent rester vigilants sur la survenue possible d’une pneumonie ou d’autres infections respiratoires basses chez les patients atteints de BPCO car les manifestations cliniques de ce type d’infection et d’une simple exacerbation sont souvent confondues. La survenue d’une pneumonie chez un sujet atteint de BPCO à un stade sévère doit conduire à réévaluer le traitement par PROPIONATE DE FLUTICASONE/SALMETEROL BGR. La sécurité et l’efficacité de propionate de fluticasone/salmétérol en flacon pressurisé n’a pas été établie pour les patients atteints de BPCO, par conséquent PROPIONATE DE FLUTICASONE/SALMETEROL BGR en flacon pressurisé n’est pas indiqué dans le traitement des patients atteints de BPCO.
L’administration concomitante de kétoconazole par voie systémique augmente de manière significative l’exposition systémique au salmétérol pouvant entraîner une augmentation du risque de survenue d’effets systémiques (par exemple : prolongation de l’intervalle QTc et palpitations). Par conséquent, il convient d’éviter l’administration concomitante de kétoconazole ou d’autres inhibiteurs puissants du cytochrome P450 3A4 sauf si les bénéfices attendus l’emportent sur le risque potentiel de survenue d’effets systémiques du salmétérol (voir rubrique 4.5).
L’attention des sportifs sera attirée sur le fait que cette spécialité contient deux principes actifs pouvant induire une réaction positive des tests pratiqués lors des contrôles antidopage.
Troubles visuels
Des troubles visuels peuvent apparaître lors d'une corticothérapie par voie systémique ou locale. En cas de vision floue ou d'apparition de tout autre symptôme visuel apparaissant au cours d'une corticothérapie, un examen ophtalmologique est requis à la recherche notamment d'une cataracte, d'un glaucome, ou d'une lésion plus rare telle qu'une choriorétinopathie séreuse centrale, décrits avec l'administration de corticostéroïdes par voie systémique ou locale.
Population pédiatrique
Les enfants et les adolescents de moins de 16 ans recevant de fortes doses de propionate de fluticasone (généralement ≥ 1000 microgrammes par jour) sont particulièrement à risque. Des effets systémiques peuvent survenir, en particulier lors de traitements à fortes doses au long cours. Il peut être observé un syndrome de Cushing, un tableau cushingoïde, une inhibition de la fonction surrénalienne, une insuffisance surrénalienne aiguë et un retard de croissance chez l'enfant et l'adolescent et, plus rarement, divers effets psychologiques ou comportementaux incluant hyperactivité psychomotrice, troubles du sommeil, anxiété, dépression ou agressivité. Il convient alors d’adresser l’enfant ou l’adolescent à un pédiatre spécialisé en pneumologie.
La croissance des enfants recevant une corticothérapie inhalée à long terme devra être régulièrement surveillée. La corticothérapie inhalée devra être réduite à la plus faible dose assurant un contrôle efficace de l’asthme.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Les β-bloquants adrénergiques peuvent diminuer ou antagoniser l’effet du salmétérol. Les β-bloquants, sélectifs ou non, doivent être évités chez les patients atteints d’asthme, sauf nécessité absolue. Une hypokaliémie potentiellement grave peut survenir suite à un traitement par β2 agoniste. Une attention particulière est recommandée en cas d’asthme aigu sévère en raison du risque d’aggravation de cette hypokaliémie par l’administration d’un traitement concomitant à base de dérivés de la xanthine, de stéroïdes et de diurétiques.
L’administration concomitante d’autres b-adrénergiques peut potentialiser les effets b2 mimétiques.
Propionate de fluticasone
Dans les conditions normales d’emploi, les concentrations plasmatiques de propionate de fluticasone atteintes après administration par voie inhalée sont faibles du fait d’un effet de premier passage présystémique important (hépatique et intestinal) et d’une forte clairance plasmatique par une importante métabolisation médiée par le cytochrome CYP3A4. Par conséquent, le risque d’interactions cliniquement significatives avec le propionate de fluticasone semble faible.
Néanmoins, une étude d’interaction chez des volontaires sains recevant du propionate de fluticasone par voie nasale a montré que le ritonavir (un inhibiteur très puissant du cytochrome CYP3A4) à la dose de 100 mg deux fois par jour augmentait de plusieurs centaines de fois les concentrations plasmatiques de propionate de fluticasone, entraînant une diminution marquée des concentrations en cortisol plasmatique. Il n’y a pas de donnée documentant l’interaction avec le propionate de fluticasone administré par voie inhalée, mais une augmentation importante des concentrations plasmatiques est attendue ; des cas de syndrome de Cushing et d’inhibition de la fonction surrénalienne ont été rapportés. Il convient donc d’éviter l’administration concomitante de propionate de fluticasone et de ritonavir, à moins que le bénéfice ne l’emporte sur le risque accru d’effets systémiques de la corticothérapie.
Une étude de faible effectif menée chez des volontaires sains a montré que le kétoconazole, inhibiteur un peu moins puissant du cytochrome P450 3A4 augmentait de 150 % l’exposition systémique d’une dose de propionate de fluticasone par voie inhalée. La réduction du cortisol plasmatique était plus importante que celle observée après l’administration de propionate de fluticasone seul. Une augmentation de l’exposition systémique et du risque d’effets indésirables systémiques est attendue en cas d’administration concomitante d’autres inhibiteurs puissants du cytochrome P450 3A4 (ex : itraconazole et médicaments contenant du cobicistat) et d’inhibiteurs modérés du CYP3A4 (ex : érythromycine). L'administration concomitante doit être évitée sauf si les bénéfices attendus sont supérieurs au risque accru d'effets secondaires systémiques des corticostéroïdes. Dans ce cas, les patients doivent être surveillés en vue de détecter les éventuels effets secondaires systémiques des corticostéroïdes.
Salmétérol
Inhibiteurs puissants du cytochrome P450 3A4
L’administration concomitante de kétoconazole (400 mg par voie orale une fois par jour) et de salmétérol (50 microgrammes par voie inhalée deux fois par jour) chez 15 volontaires sains pendant 7 jours a entraîné une augmentation significative des concentrations plasmatiques de salmétérol (Concentration maximale (Cmax) augmentée d’un facteur 1,4 et aire sous la courbe (ASC) augmentée d’un facteur 15). Cette observation suggère donc une augmentation du risque de survenue des effets systémiques du salmétérol, tels que prolongation de l’intervalle QT et palpitations, par rapport à l’administration de salmétérol ou de kétoconazole seuls (voir rubrique 4.4).
Il n’a pas été observé d’effet cliniquement significatif sur la pression artérielle, la fréquence cardiaque, la glycémie et la kaliémie. L’administration concomitante de kétoconazole n’a pas entraîné de prolongation de la demi-vie d’élimination du salmétérol ni son accumulation après administrations répétées.
Il convient d’éviter l’association de kétoconazole avec un traitement par salmétérol sauf si les bénéfices attendus l’emportent sur le risque potentiel de survenue d’effets systémiques du salmétérol. Un risque d’interaction du même ordre est attendu avec d’autres inhibiteurs puissants du cytochrome P450 3A4 (par exemple avec l’itraconazole, la télithromycine, le ritonavir).
Inhibiteurs modérés du cytochrome P450 3A4
L’administration concomitante d’érythromycine (500 mg par voie orale trois fois par jour) et de salmétérol (50 microgrammes par voie inhalée deux fois par jour) chez 15 volontaires sains pendant 6 jours a entraîné une légère augmentation, mais non statistiquement significative, des concentrations plasmatiques du salmétérol (Cmax augmentée d’un facteur 1,4 et ASC augmentée d’un facteur 1,2). Aucun effet indésirable grave n’a été associé à l’administration concomitante avec l’érythromycine.
4.6. Fertilité, grossesse et allaitement
Fertilité
Il n’existe pas de donnée chez l’Homme. Cependant, les études menées chez l’animal n’ont montré aucun effet du salmétérol ou du propionate de fluticasone sur la fécondité.
Grossesse
Une quantité importante de données obtenues chez la femme enceinte (plus de 1000 cas de grossesses documentées) ne rapportent pas de toxicité malformative ou fœto-néonale en relation avec propionate de fluticasone/salmétérol. Les études menées chez l’animal sur les fonctions de reproduction ont mis en évidence une toxicité des β2 mimétiques et des glucocorticoïdes (voir rubrique 5.3).
L’utilisation de PROPIONATE DE FLUTICASONE/SALMETEROL BGR au cours de la grossesse ne devra être envisagée que si le bénéfice attendu pour la mère l’emporte sur tout risque éventuel pour le fœtus.
Chez la femme enceinte, il conviendra de toujours rechercher la dose minimale efficace de propionate de fluticasone assurant un contrôle satisfaisant des symptômes de l’asthme.
Le passage dans le lait maternel du salmétérol et du propionate de fluticasone et de leurs métabolites n’est pas connu.
Des études ont mis en évidence que le salmétérol et le propionate de fluticasone, et leurs métabolites, sont excrétés dans le lait des rates allaitantes.
Un risque pour les nouveau-nés/nourrissons nourris au sein ne peut être exclu. La décision d’interruption de l’allaitement ou du traitement par PROPIONATE DE FLUTICASONE/SALMETEROL BGR sera établie en fonction du bénéfice attendu de l'allaitement maternel pour l'enfant face à celui du traitement pour la femme qui allaite.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
PROPIONATE DE FLUTICASONE/SALMETEROL BGR n’a aucun effet ou un effet négligeable sur l’aptitude à conduire des véhicules et à utiliser des machines.
PROPIONATE DE FLUTICASONE/SALMETEROL BGR contient du salmétérol et du propionate de fluticasone, dont les effets indésirables sont connus. Aucun effet indésirable nouveau n’est apparu lors de l’administration conjointe des deux principes actifs dans la même formulation.
Les effets secondaires associés au salmétérol et au propionate de fluticasone sont cités ci-dessous, listés par classe de systèmes d’organes et par fréquence. Les fréquences sont définies en : très fréquent (³ 1/10), fréquent (³ 1/100 à < 1/10), peu fréquent (³ 1/1000 à < 1/100), rare (³ 1/10 000 à < 1/1000) et fréquence indéterminée (ne peut être estimée sur la base des données disponibles). Les fréquences ont été définies sur la base des essais cliniques. L’incidence correspondante dans le bras placebo n’a pas été prise en considération.
|
Classe de systèmes d’organes |
Effets indésirables |
Fréquence |
|
Infections et Infestations |
Candidose buccale et pharyngée |
Fréquent |
|
Pneumonie |
Fréquent1,3 |
|
|
Bronchite |
Fréquent1,3 |
|
|
Candidose œsophagienne |
Rare |
|
|
Troubles du système immunitaire |
Réactions d’hypersensibilité à type de : - Réactions cutanées d’hypersensibilité |
Peu fréquent |
|
- Angiœdème (principalement œdème facial et oropharyngé) |
Rare |
|
|
- Symptômes respiratoires (dyspnée) |
Peu fréquent |
|
|
- Symptômes respiratoires (bronchospasme) |
Rare |
|
|
- Réactions anaphylactiques incluant le choc anaphylactique |
Rare |
|
|
Troubles endocriniens |
Syndrome de Cushing, tableau cushingoïde, inhibition de la fonction surrénalienne, ralentissement de la croissance chez l’enfant et l’adolescent, diminution de la densité minérale osseuse |
Rare4 |
|
Troubles du métabolisme et de la nutrition |
Hypokaliémie |
Fréquent3 |
|
Hyperglycémie |
Peu fréquent4 |
|
|
Troubles psychiatriques |
Anxiété |
Peu fréquent |
|
Troubles du sommeil |
Peu fréquent |
|
|
Modifications du comportement incluant hyperactivité psychomotrice et irritabilité (principalement chez les enfants) |
Rare
|
|
|
Dépression, agressivité (principalement chez les enfants) |
Fréquence indéterminée |
|
|
Troubles du système nerveux |
Maux de tête |
Très fréquent1 |
|
Tremblements |
Peu fréquent |
|
|
Troubles oculaires |
Cataracte |
Peu fréquent |
|
Glaucome |
Rare4 |
|
|
Vision floue |
Fréquence indéterminée 4 |
|
|
Troubles cardiaques |
Palpitations |
Peu fréquent |
|
Tachycardie |
Peu fréquent |
|
|
Arythmies cardiaques (y compris tachycardie supraventriculaire et extrasystoles) |
Rare |
|
|
Fibrillation auriculaire |
Peu fréquent |
|
|
Angine de poitrine |
Peu fréquent |
|
|
Troubles respiratoires, thoraciques et médiastinaux |
Rhino-pharyngite |
Très fréquent2,3 |
|
Gêne pharyngée |
Fréquent |
|
|
Raucité de la voix/dysphonie |
Fréquent |
|
|
Sinusite |
Fréquent1,3 |
|
|
Bronchospasme paradoxal |
Rare4 |
|
|
Troubles cutanés et sous cutanés |
Contusions |
Fréquent1,3 |
|
Troubles musculo-squelettiques et systémiques
|
Crampes musculaires |
Fréquent |
|
Fractures traumatiques |
Fréquent1,3 |
|
|
Arthralgies |
Fréquent |
|
|
Myalgies |
Fréquent |
1. Rapportés fréquemment dans les groupes placebo.
2. Rapportés très fréquemment dans les groupes placebo.
3. Rapportés sur une période de 3 ans dans une étude dans la BPCO.
4. Voir rubrique 4.4.
Description de certains effets indésirables
Des effets secondaires liés aux propriétés pharmacologiques β2 mimétiques du salmétérol, tels que tremblements, palpitations et maux de tête, ont été rapportés. Ils sont le plus souvent transitoires et diminuent avec la poursuite du traitement.
Comme avec d’autres traitements inhalés, un bronchospasme paradoxal peut survenir, caractérisé par une augmentation des sifflements et un essoufflement survenant immédiatement après l’administration. Le bronchospasme paradoxal doit être traité immédiatement avec un bronchodilatateur d’action rapide et de courte durée. Il convient alors de cesser toute administration de PROPIONATE DE FLUTICASONE/SALMETEROL BGR, d'évaluer l'état du patient et au besoin, d’instaurer un traitement alternatif.
Des effets indésirables associés au propionate de fluticasone comme une raucité de la voix et une candidose (muguet) buccale et pharyngée, et rarement œsophagienne, peuvent survenir chez certains patients. Les candidoses buccales et pharyngées peuvent être réduites par le rinçage de la bouche à l’eau et/ou le brossage de dents après utilisation de PROPIONATE DE FLUTICASONE/SALMETEROL BGR. Les candidoses buccales et pharyngées symptomatiques peuvent être traitées par des antifongiques locaux tout en continuant le traitement par PROPIONATE DE FLUTICASONE/SALMETEROL BGR.
Population pédiatrique
Les effets systémiques, tels que Syndrome de Cushing, tableau cushingoïde, inhibition de la fonction surrénalienne et ralentissement de la croissance chez l’enfant et chez l’adolescent, sont possibles (voir rubrique 4.4). Anxiété, troubles du sommeil et modifications du comportement, incluant hyperactivité et irritabilité, peuvent également survenir chez les enfants.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr
Les symptômes d’un surdosage en salmétérol sont des vertiges, une augmentation de la pression artérielle systolique, des tremblements, des céphalées et une tachycardie. Si le traitement par PROPIONATE DE FLUTICASONE/SALMETEROL BGR doit être interrompu en raison d’une exposition excessive aux β2 mimétiques, il sera remplacé par un corticoïde seul. Si une hypokaliémie apparaît, elle devra être corrigée par un apport adapté de potassium et la kaliémie devra être surveillée.
Surdosage aigu : l'administration de propionate de fluticasone à des doses supérieures à celles recommandées par voie inhalée peut entraîner une inhibition temporaire de la fonction surrénalienne. Il n’y a pas lieu d’adopter une mesure d’urgence car la fonction surrénalienne se rétablit en quelques jours comme en témoignent les mesures du cortisol plasmatique.
Surdosage chronique en propionate de fluticasone inhalé : La fonction surrénalienne doit être surveillée et un traitement à base de corticoïde systémique peut alors être nécessaire. Une fois stabilisé, le traitement doit être poursuivi avec un corticoïde inhalé à la dose recommandée. Se reporter à la rubrique 4.4 : Risque d’inhibition surrénalienne.
En cas de surdosage aigu ou chronique en propionate de fluticasone, le traitement par PROPIONATE DE FLUTICASONE/SALMETEROL BGR doit être poursuivi en ajustant la posologie aux doses suffisantes pour un contrôle optimal des symptômes de l’asthme.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Mécanisme d'action et effets pharmacodynamiques
PROPIONATE DE FLUTICASONE/SALMETEROL BGR contient du salmétérol et du propionate de fluticasone qui ont des modes d’action différents.
Les mécanismes d’action respectifs de ces 2 principes actifs sont présentés ci-après.
Salmétérol
Le salmétérol est un agoniste sélectif de longue durée d'action (12 heures) des récepteurs β2 adrénergiques. Il possède une longue chaîne latérale qui le lie à l'exo-site du récepteur.
Le salmétérol produit une bronchodilatation qui persiste pendant environ 12 heures. Cette durée est supérieure à celle observée généralement avec les β2 mimétiques de courte durée d'action administrés aux posologies usuelles.
Propionate de fluticasone
Le propionate de fluticasone administré par voie inhalée aux doses préconisées exerce une activité glucocorticoïde entraînant un effet anti-inflammatoire local au niveau de la muqueuse bronchique. En conséquence, les symptômes et les exacerbations d'asthme sont diminués alors que les effets systémiques sont limités comparativement à l'administration de corticoïdes par voie générale.
Efficacité clinique et sécurité
Etudes cliniques conduites avec propionate de fluticasone/salmétérol dans l’asthme
Une étude de 12 mois (Gaining Optimal Asthma controL, GOAL) réalisée chez 3416 patients adultes et adolescents atteints d’asthme persistant, a comparé la tolérance et l’efficacité de propionate de fluticasone/salmétérol à une corticothérapie inhalée seule (propionate de fluticasone) afin d’évaluer la possibilité d’atteindre les objectifs de la prise en charge de l’asthme. La posologie du traitement était augmentée toutes les 12 semaines jusqu’à ce que le contrôle total** ait été obtenu ou que la posologie la plus forte de l’étude ait été atteinte. GOAL a montré qu’il y avait plus de patients qui atteignaient le contrôle de l’asthme lorsqu’ils étaient traités par propionate de fluticasone/salmétérol que lors d’un traitement par corticoïdes inhalés seuls, ce contrôle étant obtenu avec une moindre dose de corticoïdes.
Un bon contrôle* de l’asthme a été obtenu plus rapidement chez les patients traités par propionate de fluticasone/salmétérol que chez les patients traités par un corticoïde inhalé seul. Le temps nécessaire pour que 50 % des sujets inclus dans l’étude atteignent leur première semaine de bon contrôle* a été de 16 jours pour les sujets traités par propionate de fluticasone/salmétérol et de 37 jours pour ceux traités par corticostéroïdes inhalés (CSI). Dans le sous-groupe des patients asthmatiques non traités préalablement par des corticoïdes inhalés, ce temps était respectivement de 16 jours (propionate de fluticasone/salmétérol) et de 23 jours (CSI).
Les résultats globaux de l’étude étaient les suivants :
|
Pourcentage de patients atteignant le Bon Contrôle* (BC) et le Contrôle Total** (CT) de l’asthme sur 12 mois |
|||||
|
Traitement avant inclusion dans l’étude |
FP4/Salmétérol |
FP4 |
|
||
|
BC |
CT |
BC |
CT |
|
|
|
Aucun CSI1 (ß2 CDA2 seul) |
78% |
50% |
70% |
40% |
|
|
CSI à faible dose (≤ 500 microgrammes de BDP3 ou équivalent par jour) |
75% |
44% |
60% |
28% |
|
|
CSI à dose moyenne (> 500 à 1000 microgrammes de BDP3 ou équivalent par jour) |
62% |
29% |
47% |
16% |
|
|
Résultats globaux (quel que soit le traitement antérieur) |
71% |
41% |
59% |
28% |
|
1 CSI : corticostéroïdes par voie inhalée
2 ß2 CDA : Bêta-2 agoniste de courte durée d’action
3 BDP : Dipropionate de béclométasone
4 FP : Propionate de fluticasone
* Bon contrôle de l’asthme : 2 jours par semaine maximum avec un score des symptômes supérieur à 1 (un score des symptômes de 1 est défini comme « présence de symptômes pendant une courte période pendant la journée »), utilisation d’un bronchodilatateur bêta-2 agoniste de courte durée d’action : 2 jours par semaine maximum et 4 fois maximum par semaine, valeur du débit expiratoire de pointe mesuré le matin ≥ à 80 % de la valeur théorique, pas de réveil nocturne, ni exacerbation, ni effet indésirable entraînant une modification de traitement.
** Contrôle total de l’asthme : pas de symptômes, pas d’utilisation d’un bronchodilatateur bêta-2 agoniste de courte durée d’action, valeur du débit expiratoire de pointe mesuré le matin ≥ à 80 % de la valeur théorique, sans réveil nocturne, ni exacerbation, ni effet indésirable entraînant une modification de traitement.
Les résultats de cette étude suggèrent que propionate de fluticasone/salmétérol 100/50 microgrammes/dose, deux fois par jour, peut être envisagé en initiation d’un traitement de fond chez des patients ayant un asthme persistant modéré chez qui il apparaît essentiel d’obtenir un contrôle rapide de l’asthme (voir rubrique 4.2).
Une étude en double aveugle, randomisée en groupes parallèles, conduite chez 318 patients d’au moins 18 ans, atteints d’asthme persistant, a évalué la sécurité et la tolérance de l’administration de deux inhalations deux fois par jour (double dose) de propionate de fluticasone/salmétérol pendant deux semaines. Cette étude a montré que le doublement de la dose de propionate de fluticasone/salmétérol (quel que soit le dosage), sur une durée allant jusqu’à 14 jours, entraîne par rapport à l’administration d’une inhalation deux fois par jour, une légère augmentation des effets indésirables liés à l’activité β-mimétique (tremblements : 1 patient [1 %] vs 0, palpitations : 6 [3 %] vs 1 [<1 %], crampes musculaires : 6 [3 %] vs 1 [<1 %]) et une incidence similaire des effets indésirables liés au corticoïde inhalé (candidose orale : 6 [6 %] vs 16 [8 %], raucité de la voix : 2 [2 %] vs 4 [2 %]). La faible augmentation des effets indésirables liés à l’activité β-mimétique doit être prise en considération, s’il est envisagé de doubler la dose prescrite de propionate de fluticasone/salmétérol chez des patients adultes qui nécessiteraient une augmentation de la corticothérapie inhalée pendant une courte période (jusqu’à 14 jours).
Asthme
Essai multicentrique dans l’asthme avec le salmétérol (« Salmeterol Multi-Center Asthma Research Trial, SMART »)
L’étude SMART (Salmeterol Multi-center Asthma Research Trial) était une étude de 28 semaines réalisée aux Etats-Unis chez des patients adultes et adolescents afin d’évaluer la sécurité du salmétérol comparé au placebo ajouté au traitement habituel. Bien qu’aucune différence significative n’ait été observée pour le critère principal d’évaluation, critère combiné associant le nombre de décès liés à une cause respiratoire et le nombre de détresses respiratoires mettant en jeu le pronostic vital, l’étude a montré une augmentation significative du nombre de décès liés à l’asthme chez les patients recevant du salmétérol (13 décès chez les 13 176 patients traités par salmétérol comparé à 3 décès chez les 13 179 patients recevant le placebo). L’étude n’était pas conçue pour évaluer l’impact des corticostéroïdes inhalés administrés en parallèle ; à l’inclusion, l’utilisation de CSI n’a été rapportée que chez 47 % des patients.
Sécurité et efficacité de l’association propionate de fluticasone/salmétérol versus propionate de fluticasone en monothérapie dans l’asthme
Deux études multi-centriques de 26 semaines ont été réalisées afin de comparer la sécurité et l’efficacité de l’association propionate de fluticasone/salmétérol versus propionate de fluticasone en monothérapie : une chez des patients adultes et adolescents (étude AUSTRI) et l’autre chez des patients pédiatriques âgés de 4 à 11 ans (étude VESTRI). Pour les deux études, les patients inclus présentaient un asthme persistant modéré à sévère, associé à des antécédents d’hospitalisations liées à l’asthme ou à des épisodes d’exacerbation au cours de l’année précédente. Le critère principal d’évaluation de chaque étude consistait à déterminer si l’ajout de LABA au traitement par CSI (propionate de fluticasone/salmétérol) était non-inférieur au CSI administré seul en termes de risque d’évènements indésirables graves liés à l’asthme (hospitalisation due à l’asthme, intubation endotrachéale et décès). L’objectif secondaire de ces études consistait à évaluer si l’association CSI/LABA (propionate de fluticasone/salmétérol) était supérieure au traitement par CSI seuls (propionate de fluticasone) en termes d’exacerbation sévère de l’asthme (définie comme une détérioration de l’asthme nécessitant l’utilisation de corticostéroïdes par voie systémique pendant au moins 3 jours ou bien une hospitalisation ou une consultation dans un service d’urgences pour un asthme qui requière l’utilisation de corticostéroïdes par voie systémique).
Un total de respectivement 11 679 et 6208 patients ont été randomisés afin de recevoir le traitement défini dans le cadre des études AUSTRI et VESTRI. En ce qui concerne le critère principal d’évaluation, une non-infériorité a été démontrée dans les deux études (voir tableau ci-dessous).
Effets indésirables graves liés à l’asthme rapportés dans les études de 26 semaines AUSTRI et VESTRI
|
|
AUSTRI |
VESTRI |
||
|
PF-Salmétérol (n = 5834) |
PF en monothérapie (n = 5845) |
PF-Salmétérol (n = 3107) |
PF en monothérapie (n = 3101) |
|
|
Critère d’évaluation composite (hospitalisation liée à l’asthme, intubation endotrachéale ou décès) |
34 (0,6%) |
33 (0,6%) |
27 (0,9%) |
21 (0,7%) |
|
PF-Salmétérol/PF Hazard ratio (IC 95%) |
1,029 (0,638-1,662)a |
|
1,285 (0,726-2,272)b |
|
|
Décès |
0
|
0 |
0 |
0 |
|
Hospitalisation liée à l’asthme |
34 |
33 |
27 |
21 |
|
Intubation endotrachéale |
0 |
2 |
0 |
0 |
a L’obtention d’une estimation supérieure de l’IC 95% du risque relatif inférieure à 2,0 a permis de conclure à une non-infériorité.
b L’obtention d’une estimation supérieure de l’IC 95% du risque relatif inférieure à 2,675 a permis de conclure à une non-infériorité.
Pour le critère d’évaluation secondaire, une réduction du délai de survenue de la première exacerbation de l’asthme avec l’association PF-salmétérol par rapport au PF seul a été observée dans les deux études, cependant cette réduction n’a été statistiquement significative que dans l’étude AUSTRI.
|
|
AUSTRI |
VESTRI |
||
|
PF-Salmétérol (n = 5834) |
PF en monothérapie (n = 5845) |
PF-Salmétérol (n = 3107) |
PF en monothérapie (n = 3101) |
|
|
Nombre de sujets présentant une exacerbation de leur asthme |
480 (8%) |
597 (10%) |
265 (9%) |
309 (10%) |
|
PF-Salmétérol/PF Hazard ratio (IC 95%) |
0,787 (0,698 ; 0,888) |
0,859 (0,729 ; 1,012) |
||
Population pédiatrique
Dans l'étude SAM101667, conduite chez 158 enfants âgés de 6 à 16 ans présentant un asthme symptomatique, l'association propionate de fluticasone/salmétérol était aussi efficace qu’une double dose de propionate de fluticasone, sur le contrôle des symptômes et sur la fonction pulmonaire. Cette étude n'était pas conçue pour l’étude de l'effet sur les exacerbations.
Dans une étude de 12 semaines conduite chez des enfants âgés de 4 à 11 ans [n = 428], un traitement par propionate de fluticasone/salmétérol poudre pour inhalation en récipient unidose (100/50 microgrammes, une inhalation deux fois par jour) a été comparé à un traitement par propionate de fluticasone/salmétérol en flacon pressurisé avec valve doseuse (50/25 microgrammes, 2 inhalations deux fois par jour). La moyenne ajustée du débit expiratoire de pointe (DEP ou Peak Expiratory Flow) mesurée le matin à l’inclusion par rapport à sa valeur après 12 semaines de traitement était de 37,7 L/min pour le groupe poudre pour inhalation en récipient unidose et de 38,6 L/min pour le groupe en flacon pressurisé avec valve doseuse.
Dans les 2 groupes de traitement, des améliorations ont également été observées sur les symptômes et sur la diminution de la consommation de traitement dit « de secours » aussi bien nocturne que diurne.
Une étude multicentrique de 8 semaines, en double aveugle, a été réalisée afin d’évaluer la sécurité et l’efficacité de l’association propionate de fluticasone/salmétérol (dose de 50/25 microgrammes administrée par un aérosol doseur en 1 ou 2 inhalations deux fois par jour) par rapport au propionate de fluticasone seul (dose de 50 microgrammes administrée en 1 ou 2 inhalations deux fois par jour) chez des enfants japonais (âgés de 6 mois à 4 ans) atteints d’asthme bronchitique infantile. Quatre-vingt-dix-neuf pour cent (148/150) et quatre-vingt-quinze pour cent (142/150) des patients randomisés traités respectivement par l’association propionate de fluticasone/salmétérol ou par propionate de fluticasone seul, ont terminé la période de l’étude en double aveugle. La sécurité d’un traitement au long cours par l’association propionate de fluticasone/salmétérol (dose de 50/25 microgrammes administrée par un aérosol doseur en 1 ou 2 inhalations deux fois par jour) a été évaluée au cours d’une étude d’extension de 16 semaines, en ouvert. Quatre-vingt-treize pour cent des patients (268/288) ont terminé la période d’extension de l’étude.
Le critère principal d’évaluation de l’efficacité n’a pas été atteint en ce qui concerne l’évolution moyenne du score total des symptômes de l’asthme par rapport aux valeurs à l’inclusion (période en double aveugle). Aucune supériorité statistiquement significative en faveur de l’association propionate de fluticasone/salmétérol par rapport au propionate de fluticasone seul n’a été démontrée (IC 95%
[-2,47 ; 0,54], p=0,206). Il n’y avait pas de différences évidentes au niveau du profil de sécurité entre l’association propionate de fluticasone/salmétérol et le propionate de fluticasone seul (période de 8 semaines en double aveugle) ; de plus, aucun nouveau signal de sécurité n’a été identifié suite à l’administration de l’association propionate de fluticasone/salmétérol au cours de la période d’extension en ouvert de 16 semaines. Cependant les données sur l’efficacité et la sécurité du salmétérol sont insuffisantes pour établir une balance bénéfice/risque de l’association propionate de fluticasone/salmétérol chez l’enfant de moins de 4 ans.
Médicaments anti-asthmatiques contenant du propionate de fluticasone utilisés pendant la grossesse
Une étude de cohorte épidémiologique rétrospective observationnelle a été réalisée sur la base de dossiers médicaux électroniques émanant du Royaume-Uni afin d’évaluer le risque de MCM (Malformations congénitales majeures) suite à l’exposition au propionate de fluticasone inhalé seul et à l’association PF/salmétérol comparativement à un traitement par CSI ne contenant pas de propionate de fluticasone, pendant le premier trimestre de la grossesse. Aucun comparateur par placebo n’a été inclus dans cette étude.
Au sein de la cohorte « asthme » de 5362 grossesses exposées aux CSI au cours du premier trimestre, 131 MCM diagnostiquées ont été identifiées ; 1612 (30%) grossesses ont été exposées au propionate de fluticasone ou à l’association propionate de fluticasone/salmétérol, parmi lesquelles 42 MCM diagnostiquées ont été identifiées. Les « odds ratio » ajustés pour les MCMs diagnostiquées en un an étaient de 1,1 (IC 95 % ; 0,5 – 2,3) pour les femmes présentant un asthme modéré et exposées au propionate de fluticasone par rapport à un traitement par CSI sans propionate de fluticasone et de 1,2 (IC 95 % ; 0,7– 2,0) pour les femmes présentant un asthme important à sévère. Aucune différence dans le risque de MCM n’a été identifiée suite à l’exposition au propionate de fluticasone en monothérapie pendant le premier trimestre de la grossesse par rapport à l’association salmétérol/propionate de fluticasone. Les risques absolus de MCM quel que soit le degré de sévérité de l’asthme se situaient entre 2,0 et 2,9 pour 100 grossesses exposées au propionate de fluticasone, ce qui est comparable aux résultats d’une étude portant sur 15 840 grossesses non exposées à un traitement de l’asthme d’après la « General Practice Research Database » (2,8 MCMs pour 100 grossesses).
5.2. Propriétés pharmacocinétiques
Salmétérol
Le salmétérol agissant localement au niveau pulmonaire, les taux plasmatiques ne sont pas corrélés à l’effet thérapeutique. De plus, peu de données sont disponibles sur la pharmacocinétique du salmétérol après administration par voie inhalée car les concentrations plasmatiques observées aux doses thérapeutiques sont très faibles (au maximum 200 picogrammes/mL), et difficilement mesurables.
Propionate de fluticasone
La biodisponibilité absolue après administration d’une dose unique de propionate de fluticasone inhalé chez les volontaires sains varie approximativement de 5 à 11% de la dose nominale selon le dispositif d’inhalation utilisé. Une moindre exposition systémique au propionate de fluticasone a été observée chez les patients asthmatiques.
L’absorption est essentiellement pulmonaire. Elle est rapide dans un premier temps puis se poursuit plus lentement. Le reste de la dose peut être dégluti mais ne contribue qu’en faible partie à l’exposition systémique du fait d’une faible solubilité aqueuse et d’un important métabolisme de premier passage. La biodisponibilité orale est ainsi inférieure à 1%. L’exposition systémique augmente de façon linéaire avec l’augmentation de la dose inhalée.
L’élimination du propionate de fluticasone est caractérisée par une forte clairance plasmatique (1150 mL/min), un important volume de distribution à l’état d’équilibre (environ 300 L) et une demi-vie terminale d’environ 8 heures.
La liaison aux protéines plasmatiques est de 91 %.
Le propionate de fluticasone est éliminé très rapidement de la circulation systémique. Le produit est essentiellement métabolisé en un dérivé acide carboxylique inactif, par l’isoenzyme CYP3A4 du cytochrome P450. D’autres métabolites non identifiés sont également trouvés dans les fécès.
La clairance rénale du propionate de fluticasone est négligeable. Moins de 5% de la dose est excrétée dans les urines, principalement sous forme de métabolites. La majorité de la dose est éliminée dans les fécès sous forme de métabolites et sous forme inchangée.
Population pédiatrique
L’effet de 21 jours de traitement par propionate de fluticasone/salmétérol suspension pour inhalation en flacon pressurisé 50/25 microgrammes/dose (2 inhalations deux fois par jour avec ou sans chambre d’inhalation) ou par propionate de fluticasone/salmétérol poudre pour inhalation en récipient unidose 100/50 microgrammes/dose (1 inhalation deux fois par jour) a été évalué chez 31 enfants âgés de 4 à 11 ans ayant un asthme léger. L’exposition systémique au propionate de fluticasone était similaire pour propionate de fluticasone/salmétérol suspension pour inhalation en flacon pressurisé avec chambre d’inhalation (107 picogrammes*heure/mL [IC à 95% : 45,7 - 252,2]) et pour propionate de fluticasone/salmétérol poudre pour inhalation en récipient unidose (138 picogrammes*heure/mL [IC à 95% : 69,3 - 273,2]), mais plus faible pour propionate de fluticasone/salmétérol suspension pour inhalation en flacon pressurisé (24 picogrammes*heure/mL [IC à 95% : 9,6 - 60,2]). L’exposition systémique au salmétérol était similaire pour propionate de fluticasone/salmétérol suspension pour inhalation en flacon pressurisé, propionate de fluticasone/salmétérol suspension pour inhalation en flacon pressurisé avec chambre d’inhalation et propionate de fluticasone/salmétérol poudre pour inhalation en récipient unidose (126 picogrammes*heure/mL [IC à 95% : 70 - 225], 103 picogrammes*heure/mL [IC à 95% : 54 - 200], et 110 picogrammes*heure/mL [IC à 95% : 55 - 219], respectivement).
5.3. Données de sécurité préclinique
Au cours des études de reproduction menées chez l’animal, des malformations ont été observées après administration de glucocorticoïdes (fentes palatines, malformations osseuses). Cependant, ces résultats expérimentaux observés chez l’animal, ne semblent pas prédictifs d’un effet malformatif chez l’homme aux doses recommandées. Les études menées chez l’animal avec le salmétérol ont montré une toxicité embryofoetale seulement après exposition à de fortes doses. Après administration concomitante des deux principes actifs, il a été observé chez des rats recevant des doses de glucocorticoïdes connues pour induire des anomalies, une augmentation de la fréquence d’apparition de transposition de l’artère ombilicale et d’ossifications incomplètes au niveau de l’occipital. Ni le xinafoate de salmétérol ni le propionate de fluticasone n’ont montré d’effet potentiel en termes de toxicité génétique.
L’expérimentation animale, menée en administration quotidienne pendant deux ans, n’a pas mis en évidence d’effet toxique du gaz propulseur, le norflurane, lorsqu’il était administré à des doses nettement supérieures à celles qui peuvent être utilisées en thérapeutique.
Gaz propulseur : norflurane (HFA 134a).
2 ans.
6.4. Précautions particulières de conservation
À conserver à une température ne dépassant pas 25°C. Ne pas réfrigérer ou congeler.
La cartouche contient un liquide pressurisé. Ne pas exposer à des températures supérieures à 50°C, protéger des rayons du soleil.
La cartouche ne doit pas être perforée, ni percée, ni brûlée même si elle semble vide.
Comme pour la plupart des produits en cartouche pressurisée, l’effet thérapeutique peut être diminué quand la cartouche est froide.
6.5. Nature et contenu de l'emballage extérieur
La suspension est contenue dans une cartouche pressurisée de 8 mL en aluminium, vernie intérieurement et munie d’une valve doseuse. La cartouche est insérée dans un applicateur en plastique violet muni d’un embout buccal fermé par un capuchon. Un compteur de doses indique le nombre de doses restantes. Ce nombre est visible au travers d’une fenêtre située à l’arrière du dispositif en plastique. Une cartouche pressurisée délivre 120 doses.
Les dispositifs sont présentés dans des boîtes contenant :
1 flacon de 120 doses.
ou 2 flacons de 120 doses
ou 3 flacons de 120 doses.
ou 10 flacons de 120 doses - destinés à l’usage hospitalier uniquement.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
15, BOULEVARD CHARLES DE GAULLE
92700 COLOMBES
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 301 915 4 5 : 120 doses en flacon pressurisé (Aluminium) muni d’un compteur de doses.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I
ANSM - Mis à jour le : 25/02/2025
Propionate de fluticasone/Salmétérol
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que PROPIONATE DE FLUTICASONE/SALMETEROL BGR 125 microgrammes/25 microgrammes/dose, suspension pour inhalation en flacon pressurisé et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser PROPIONATE DE FLUTICASONE/SALMETEROL BGR 125 microgrammes/25 microgrammes/dose, suspension pour inhalation en flacon pressurisé ?
3. Comment utiliser PROPIONATE DE FLUTICASONE/SALMETEROL BGR 125 microgrammes/25 microgrammes/dose, suspension pour inhalation en flacon pressurisé ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver PROPIONATE DE FLUTICASONE/SALMETEROL BGR 125 microgrammes/25 microgrammes/dose, suspension pour inhalation en flacon pressurisé ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE PROPIONATE DE FLUTICASONE/SALMETEROL BGR 125 microgrammes/25 microgrammes/dose, suspension pour inhalation en flacon pressurisé ET DANS QUELS CAS EST-IL UTILISE ?
PROPIONATE DE FLUTICASONE/SALMETEROL BGR est un médicament contenant deux principes actifs, le salmétérol et le propionate de fluticasone :
· Le salmétérol est un bronchodilatateur de longue durée d’action. Les bronchodilatateurs aident à garder les bronches ouvertes. Cela permet de faciliter l’entrée et la sortie de l’air dans les poumons. L’effet dure au moins 12 heures.
· Le propionate de fluticasone est un corticoïde qui diminue l’inflammation et l’irritation dans les poumons.
Votre médecin vous a prescrit ce médicament pour aider à prévenir certains troubles respiratoires tels que l’asthme.
Vous devez utiliser PROPIONATE DE FLUTICASONE/SALMETEROL BGR tous les jours comme indiqué par votre médecin. Cela permettra de contrôler correctement votre asthme.
PROPIONATE DE FLUTICASONE/SALMETEROL BGR permet d’éviter la survenue d’essoufflement et de sifflement. Cependant, PROPIONATE DE FLUTICASONE/SALMETEROL BGR ne doit pas être utilisé lorsque vous avez une crise soudaine d’essoufflement ou de sifflement. Dans ces cas, vous devez utiliser votre médicament bronchodilatateur dit « de secours » d’action rapide et de courte durée, comme le salbutamol. Vous devez toujours avoir sur vous votre inhalateur dit « de secours » d’action rapide et de courte durée.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER PROPIONATE DE FLUTICASONE/SALMETEROL BGR 125 microgrammes/25 microgrammes/dose, suspension pour inhalation en flacon pressurisé ?
· Si vous êtes allergique au salmétérol, au propionate de fluticasone ou à l’autre composant contenu dans ce médicament, le norflurane (HFA 134a), mentionnés dans la rubrique 6.
Avertissements et précautions
Adressez-vous à votre médecin avant d’utiliser PROPIONATE DE FLUTICASONE/SALMETEROL BGR si vous avez :
· une maladie du cœur, y compris un rythme cardiaque irrégulier ou trop rapide,
· une hyperactivité de la thyroïde,
· une pression artérielle élevée,
· du diabète (PROPIONATE DE FLUTICASONE/SALMETEROL BGR peut augmenter le taux de sucre dans votre sang),
· un faible taux de potassium dans votre sang,
· une tuberculose actuellement en cours d’évolution ou survenue dans le passé, ou toute autre infection pulmonaire.
Contactez votre médecin en cas de vision floue ou d’autres troubles visuels.
Enfants et adolescents
Sans objet.
Autres médicaments et PROPIONATE DE FLUTICASONE/SALMETEROL BGR 125 microgrammes/25 microgrammes/dose, suspension pour inhalation en flacon pressurisé
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament. Cela concerne les médicaments pour l’asthme et tout autre médicament y compris ceux obtenus sans ordonnance. Ceci est dû au fait que PROPIONATE DE FLUTICASONE/SALMETEROL BGR peut ne pas être adapté à la prise simultanée d’autres médicaments.
Avant de commencer à utiliser PROPIONATE DE FLUTICASONE/SALMETEROL BGR, informez votre médecin si vous prenez les médicaments suivants :
· b-bloquants (tels que aténolol, propranolol et sotalol). Les b-bloquants sont surtout utilisés dans le traitement de l’hypertension artérielle ou pour d’autres maladies cardiaques.
· Médicaments utilisés pour traiter les infections (tels que le kétoconazole, l’itraconazole et l’érythromycine), y compris certains médicaments utilisés dans le traitement du VIH (tels que le ritonavir, les médicaments contenant du cobicistat). Certains de ces médicaments peuvent augmenter le taux de propionate de fluticasone ou de salmétérol dans votre organisme. Cela peut augmenter le risque d’avoir des effets indésirables avec PROPIONATE DE FLUTICASONE/SALMETEROL BGR, notamment des battements cardiaques irréguliers, ou rendre plus graves des effets indésirables. Il se peut que votre médecin souhaite instaurer une surveillance particulière si vous prenez ces médicaments.
· Corticoïdes (par voie orale ou injectable). Si vous avez pris ces médicaments récemment, il existe un risque que ce médicament exerce également un effet sur les glandes surrénales de votre organisme.
· Diurétiques, utilisés pour traiter l’hypertension artérielle.
· D’autres bronchodilatateurs (comme le salbutamol).
· Médicaments contenant de la xanthine. Ils sont souvent utilisés pour traiter l'asthme.
PROPIONATE DE FLUTICASONE/SALMETEROL BGR 125 microgrammes/25 microgrammes/dose, suspension pour inhalation en flacon pressurisé avec des aliments et boissons
Sans objet.
Grossesse, allaitement et fertilité
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant d’utiliser ce médicament.
Conduite de véhicules et utilisation de machines
PROPIONATE DE FLUTICASONE/SALMETEROL BGR n’a pas de raison d’affecter la capacité à conduire un véhicule ou à utiliser une machine.
PROPIONATE DE FLUTICASONE/SALMETEROL BGR 125 microgrammes/25 microgrammes/dose, suspension pour inhalation en flacon pressurisé contient
Sans objet.
3. COMMENT UTILISER PROPIONATE DE FLUTICASONE/SALMETEROL BGR 125 microgrammes/25 microgrammes/dose, suspension pour inhalation en flacon pressurisé ?
· Utilisez PROPIONATE DE FLUTICASONE/SALMETEROL BGR tous les jours, jusqu’à avis contraire de votre médecin. Ne prenez pas plus que la dose recommandée.
· N’arrêtez pas votre traitement ou ne réduisez pas vous-même vos doses de traitement sans en avoir préalablement parlé à votre médecin.
· PROPIONATE DE FLUTICASONE/SALMETEROL BGR doit être inhalé par la bouche pour aller dans les poumons.
Adultes et adolescents âgés de 12 ans et plus
Deux inhalations deux fois par jour (matin et soir).
Vos symptômes doivent être bien contrôlés en utilisant PROPIONATE DE FLUTICASONE/SALMETEROL BGR deux fois par jour. Si c’est le cas, votre médecin peut alors décider de réduire votre dose à une prise par jour. Votre dose pourrait donc être réduite à :
· une prise le soir si vous avez des symptômes pendant la nuit,
ou
· une prise le matin si vous avez des symptômes pendant la journée.
Il est très important de suivre les indications données par votre médecin sur le nombre de bouffées à inhaler ou l’intervalle de temps entre chaque prise de votre médicament.
Si vous utilisez PROPIONATE DE FLUTICASONE/SALMETEROL BGR pour le traitement de votre asthme, votre médecin souhaitera vérifier régulièrement votre état clinique. Si votre asthme ou votre essoufflement s’aggrave, consultez votre médecin immédiatement. Si vous entendez des sifflements bronchiques plus importants, si vous vous sentez plus souvent oppressé au niveau de la poitrine ou si vous avez plus souvent besoin d’utiliser votre traitement bronchodilatateur de secours, continuez à utiliser PROPIONATE DE FLUTICASONE/SALMETEROL BGR sans augmenter le nombre de bouffées de PROPIONATE DE FLUTICASONE/SALMETEROL BGR. Votre état respiratoire pourrait s’aggraver et vous pourriez alors être davantage malade. Dans ce cas, consultez votre médecin, car il se peut que vous ayez besoin d’un traitement supplémentaire.
Instructions d’utilisation
· Votre médecin, votre infirmier(ère) ou votre pharmacien devront vous montrer comment utiliser votre dispositif d’inhalation. Ils vérifieront comment vous l’utilisez à chaque visite. Ne pas utiliser PROPIONATE DE FLUTICASONE/SALMETEROL BGR correctement ou comme vous l’a prescrit votre médecin pourrait limiter son efficacité pour traiter votre asthme.
· Le médicament est contenu dans une cartouche pressurisée insérée dans un applicateur en plastique muni d’un embout buccal.
· Un compteur de doses positionné au dos du dispositif vous indique le nombre de doses restantes dans le dispositif. Chaque fois que vous pressez sur la cartouche, une dose de médicament est libérée et le nombre de doses indiqué au compteur est décompté d’une unité.
· Faites attention à ne pas laisser tomber le dispositif, car cela pourrait déclencher un décompte sur le compteur.
Vérification du fonctionnement du dispositif :
1. Lorsque vous utilisez le dispositif pour la première fois, testez son bon fonctionnement. Retirez le capuchon de l’embout buccal en pressant doucement les côtés, entre le pouce et l’index et tirez-le.
2. Afin de s’assurer qu’il fonctionne, agitez-le bien, éloignez l’embout buccal de vous et appuyez sur la cartouche pour libérer une bouffée dans l’air. Répétez ces étapes, en agitant bien le dispositif avant de libérer chaque bouffée, jusqu’à ce que le compteur indique 120. Si vous n’avez pas utilisé votre dispositif depuis une semaine ou plus, libérez deux bouffées de produit dans l’air.
Utilisation du dispositif :
Il est important de commencer à respirer le plus lentement possible juste avant d’utiliser le dispositif :
1. Tenez-vous debout ou assis quand vous utilisez votre dispositif.
2. Retirez le capuchon de l’embout buccal (selon le 1er schéma). Vérifiez l’intérieur et l’extérieur de l’embout buccal afin de vous assurer que celui-ci est propre et ne contient pas de corps étranger.
3. Agitez l’appareil 4 à 5 fois afin d’éliminer tout corps étranger et d’assurer le mélange des composants de la suspension contenue dans le flacon.
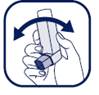
4. Tenez l’appareil bien à la verticale en plaçant le pouce à la base, sous l’embout buccal. Expirez autant que vous le pouvez.
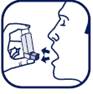
5. Placez l’embout buccal dans votre bouche entre les dents. Fermez les lèvres autour. Ne mordez pas l’embout buccal.
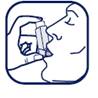
6. Inspirez par la bouche doucement et profondément. Juste après avoir commencé à inspirer à travers le dispositif, appuyez fermement vers le bas sur le haut de l’appareil pour libérer une bouffée de médicament, tout en inspirant régulièrement et profondément.
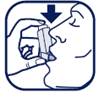
7. Pendant que vous retenez votre respiration, retirez le dispositif de votre bouche et vos doigts du haut de l’appareil. Continuez à retenir votre respiration durant quelques secondes, autant que vous le pouvez.

8. Attendez environ 30 secondes avant une nouvelle inhalation puis répétez les étapes 3 à 7.
9. Ensuite, rincez votre bouche à l’eau en la recrachant et/ou brossez-vous les dents. Ceci permettra d’éviter l’apparition d’une candidose ou d’une voix rauque.
10. Après utilisation, remettez toujours immédiatement le capuchon en place pour protéger l’embout buccal de la poussière. Quand le capuchon est fixé convenablement on peut entendre un « clic ». Si vous n’entendez pas de « clic », tournez le capuchon dans l’autre sens et réessayez sans forcer.
Ne pas précipiter les étapes 4, 5, 6 et 7. Il est important de respirer le plus lentement possible juste avant une inhalation. Vous devez utiliser votre inhalateur debout face à un miroir les premières fois. Si vous voyez du "brouillard" provenant du haut de l’inhalateur ou des coins de votre bouche, vous devez recommencer à l'étape 3.
Comme avec tous les inhalateurs, les soignants doivent s'assurer que les enfants qui se voient prescrire l’association propionate de fluticasone/salmétérol utilisent une technique d'inhalation correcte, telle que décrite ci-dessus.
Si vous ou votre enfant avez des difficultés à utiliser votre dispositif, votre médecin, votre infirmier/ère ou tout autre professionnel de santé peut vous recommander d'utiliser une chambre d’inhalation Volumatic avec votre inhalateur : votre médecin, votre infirmier/ère, votre pharmacien ou tout autre professionnel de santé doit vous montrer comment utiliser une chambre d’inhalation avec votre inhalateur, comment en prendre soin. Ils devront également répondre à toutes les questions que vous pourriez vous poser. Il est important de ne pas cesser d’utiliser votre chambre d’inhalation avec votre inhalateur sans en parler à votre médecin ou votre infirmier/ère au préalable. Il est également important que vous ne changiez pas vous même de type de chambre d’inhalation sans en avoir parlé à votre médecin. Si vous cessez d'utiliser une chambre d’inhalation ou si vous changez le type de chambre d’inhalation, votre médecin devra peut-être modifier la dose de médicament nécessaire pour contrôler votre asthme.
Consultez toujours votre médecin avant de faire tout changement dans votre traitement de l'asthme Les enfants plus âgés ou des personnes ayant peu de force dans les mains peuvent trouver plus facile de tenir l'inhalateur avec les deux mains. Pour cela, mettez les deux index sur le dessus de l'inhalateur et les deux pouces sur le fond sous l'embout buccal.
Vous devez envisager le renouvellement de votre médicament lorsque le compteur affiche le nombre 020. Arrêtez d’utiliser l’appareil quand le compteur affiche 000 car la quantité du médicament délivrée dans les bouffées éventuellement restantes risque d’être insuffisante pour être efficace. N’essayez jamais de modifier les chiffres sur le compteur de doses ou de détacher le compteur de la cartouche métallique.
Nettoyage du dispositif :
Pour son bon fonctionnement, le dispositif doit être nettoyé au moins une fois par semaine.
Pour nettoyer le dispositif :
· Retirez le capuchon de l’embout buccal.
· Ne séparez la cartouche de l’applicateur en plastique à aucun moment.
· Essuyez l’intérieur et l’extérieur de l’embout buccal et l’applicateur plastique avec un tissu ou un mouchoir propre et sec.
· Remettez le capuchon sur l’embout buccal jusqu’à entendre un « clic » indiquant que celui-ci est fixé convenablement. Si vous n’entendez pas de « clic », tournez le capuchon dans l’autre sens et réessayez sans forcer.
Ne pas plonger la cartouche métallique dans l’eau.
Si vous avez utilisé plus de PROPIONATE DE FLUTICASONE/SALMETEROL BGR 125 microgrammes/25 microgrammes/dose, suspension pour inhalation en flacon pressurisé que vous n’auriez dû
Il est important d’utiliser le dispositif comme votre médecin vous l’a montré. Si vous avez pris accidentellement une dose plus élevée que la dose recommandée, parlez-en à votre médecin ou à votre pharmacien. Vous pouvez remarquer une accélération du rythme cardiaque et des tremblements. Vous pouvez également ressentir des vertiges, des maux de tête, une faiblesse musculaire et des douleurs articulaires.
Si vous avez pris des doses importantes pendant une longue période, vous devez en parler à votre médecin ou à votre pharmacien. Des doses élevées administrées au long cours peuvent entraîner une diminution des hormones stéroïdiennes sécrétées par les glandes surrénales.
Si vous oubliez d’utiliser PROPIONATE DE FLUTICASONE/SALMETEROL BGR 125 microgrammes/25 microgrammes/dose, suspension pour inhalation en flacon pressurisé
Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre. Prenez juste la dose suivante à l’heure habituelle.
Si vous arrêtez d’utiliser PROPIONATE DE FLUTICASONE/SALMETEROL BGR 125 microgrammes/25 microgrammes/dose, suspension pour inhalation en flacon pressurisé
Il est très important que vous preniez PROPIONATE DE FLUTICASONE/SALMETEROL BGR tous les jours comme indiqué par votre médecin. Continuez votre traitement jusqu’à l’avis contraire de votre médecin. N’arrêtez pas ou ne réduisez pas les doses de PROPIONATE DE FLUTICASONE/SALMETEROL BGR subitement. Cela pourrait rendre votre respiration plus difficile.
De plus, si vous arrêtez brusquement de prendre PROPIONATE DE FLUTICASONE/SALMETEROL BGR ou si vous réduisez votre dose de PROPIONATE DE FLUTICASONE/SALMETEROL BGR cela peut (très rarement) conduire à des problèmes de glande surrénale (insuffisance surrénalienne) qui provoquent parfois des effets indésirables.
Ces effets indésirables peuvent inclure :
· Douleurs d’estomac,
· Fatigue et perte d’appétit, nausée,
· Vomissement et diarrhée,
· Perte de poids,
· Maux de tête ou somnolence,
· Diminution du taux de sucre dans votre sang,
· Baisse de tension artérielle et survenue de convulsions (crises d’épilepsie).
L’insuffisance surrénalienne peut s’aggraver et vous pouvez présenter un des effets indésirables mentionnés ci-dessus lorsque votre corps est soumis à des facteurs de stress tels que de l’apparition de fièvre ou un traumatisme (comme un accident de voiture), une infection ou une intervention chirurgicale.
Si vous présentez un de ces effets indésirables, parlez-en à votre médecin ou votre pharmacien. Pour éviter l’apparition de ces symptômes, votre médecin peut vous prescrire un traitement supplémentaire par corticoïdes sous forme de comprimé (tel que la prednisolone).
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin, à votre pharmacien ou à votre infirmier/ère.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Afin de prévenir l’apparition d’effets indésirables, votre médecin vous prescrira la dose la plus faible possible contrôlant votre asthme.
Réactions allergiques : vous pouvez constater que votre essoufflement s’aggrave subitement, immédiatement après avoir utilisé PROPIONATE DE FLUTICASONE/SALMETEROL BGR. Vous pouvez percevoir des sifflements bronchiques et tousser ou être essoufflé. Vous pouvez également ressentir des démangeaisons, remarquer une éruption cutanée (urticaire) ou un gonflement (généralement au niveau du visage, des lèvres, de la langue ou de la gorge), sentir que votre cœur se met soudainement à battre très rapidement ou vous sentir mal et avoir la tête qui tourne (malaise pouvant aller jusqu’à un évanouissement ou une perte de connaissance). Si vous ressentez l’un de ces symptômes ou s’ils apparaissent subitement après avoir utilisé PROPIONATE DE FLUTICASONE/SALMETEROL BGR, arrêtez de prendre PROPIONATE DE FLUTICASONE/SALMETEROL BGR et parlez-en à votre médecin immédiatement. Les réactions allergiques à l’association propionate de fluticasone/salmétérol sont peu fréquentes (elles affectent moins de 1 personne sur 100).
Les autres effets indésirables sont décrits ci-dessous :
Effets très fréquents (affectent plus d’1 personne sur 10) :
· Maux de tête diminuant généralement à la poursuite du traitement.
· Une augmentation du nombre de rhumes a été rapportée chez les patients atteints de Broncho-Pneumopathie Chronique Obstructive (BPCO) traitée par l’association propionate de fluticasone/salmétérol.
Effets fréquents (affectent moins d’1 personne sur 10) :
· Candidose de la bouche et de la gorge (parfois douloureuse). Egalement langue irritée, voix rauque et irritation de la gorge. Rincer votre bouche avec de l’eau et la cracher et/ou se brosser les dents immédiatement après chaque prise de votre médicament peut permettre d’éviter ces effets. Votre médecin peut vous prescrire un traitement antifongique pour soigner la candidose.
· Douleurs et inflammations des articulations, douleurs musculaires.
· Crampes musculaires.
Les effets indésirables suivants ont également été rapportés avec l’association propionate de fluticasone/salmétérol chez des patients atteints de Broncho-Pneumopathie Chronique Obstructive (BPCO) :
· Pneumonie et bronchite (infection respiratoire). Informez votre médecin si vous ressentez l’un des symptômes suivants : quantité des crachats augmentée, modification de la coloration des crachats, fièvre, frissons, augmentation de la toux, augmentation de la gêne respiratoire.
· Ecchymoses (bleus sur la peau) et fractures.
· Inflammation des sinus (sensation de tension ou de pesanteur au niveau du nez, des joues et derrière les yeux, parfois accompagnée d’une douleur pulsatile).
· Diminution de la quantité de potassium dans votre sang (qui peut se manifester par des palpitations, une faiblesse musculaire, des crampes).
Effets peu fréquents (affectent moins d’1 personne sur 100) :
· Augmentation du taux de sucre (glucose) dans votre sang (hyperglycémie). Si vous avez du diabète, des contrôles plus fréquents de votre taux de sucre dans le sang et un ajustement possible de votre traitement antidiabétique peuvent être nécessaires.
· Cataracte (opacification du cristallin de l'œil provoquant généralement une gêne visuelle).
· Accélération rapide du rythme cardiaque (tachycardie).
· Tremblements et rythme cardiaque rapide ou irrégulier (palpitations). Cela est généralement sans gravité et diminue à la poursuite du traitement.
· Douleur thoracique.
· Sentiment d'inquiétude (cet effet survient principalement chez les enfants).
· Troubles du sommeil.
· Eruption cutanée allergique.
Effets rares (affectent moins d’1 personne sur 1000) :
· Survenue brutale d’une difficulté à respirer ou de sifflements bronchiques juste après la prise de l’association propionate de fluticasone/salmétérol. Dans ce cas, arrêtez d’utiliser PROPIONATE DE FLUTICASONE/SALMETEROL BGR. Utilisez votre médicament bronchodilatateur dit « de secours » pour vous aider à respirer et prévenez votre médecin immédiatement.
· L’association propionate de fluticasone/salmétérol peut affecter la production normale d’hormones stéroïdiennes par l’organisme, particulièrement si vous l’avez pris à des doses élevées et sur de longues périodes. Les effets incluent :
o un ralentissement de la croissance de l’enfant et de l’adolescent,
o un amincissement de la trame osseuse,
o un glaucome (affection de l'œil liée à une augmentation de la pression intraoculaire),
o une prise de poids,
o un arrondissement (aspect en forme de lune) du visage (Syndrome de Cushing).
Votre médecin s’assurera régulièrement que vous ne présentez pas ces effets indésirables et que vous utilisez l’association propionate de fluticasone/salmétérol à la plus faible dose permettant de contrôler votre asthme.
· Modifications du comportement, telles qu’activité et irritabilité inhabituelles (ces effets surviennent principalement chez les enfants).
· Irrégularité du rythme cardiaque (arythmies). Prévenez votre médecin, mais n'interrompez pas votre traitement par PROPIONATE DE FLUTICASONE/SALMETEROL BGR, sauf si votre médecin vous demande de l’arrêter.
· Une infection fongique de l’œsophage (arrière-gorge) qui peut causer des difficultés pour avaler.
Effets de fréquence indéterminée, mais pouvant également survenir :
· Dépression ou agressivité. Ces effets sont davantage susceptibles de survenir chez les enfants.
· Vision floue.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER PROPIONATE DE FLUTICASONE/SALMETEROL BGR 125 microgrammes/25 microgrammes/dose, suspension pour inhalation en flacon pressurisé ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’emballage. La date de péremption fait référence au dernier jour de ce mois.
A conserver à une température ne dépassant pas 25°C. Ne pas réfrigérer ou congeler.
La cartouche métallique contient un liquide pressurisé. Ne pas exposer à une température supérieure à 50°C, protéger des rayons du soleil. Ne pas perforer, ni percer ou brûler la cartouche même si elle semble vide.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
· Les substances actives sont :
Salmétérol (sous forme de xinafoate de salmétérol)......................................... 25 microgrammes
Propionate de fluticasone............................................................................. 125 microgrammes
Pour une dose pré-mesurée.
L’autre composant est un gaz propulseur : le norflurane (HFA 134a).
Ce médicament contient des gaz à effet de serre fluorés. Chaque inhalateur contient 12 g de HFC-134a (aussi appelé norflurane ou HFA 134a) correspondant à 0,0172 tonne équivalent CO2 (potentiel de réchauffement global (PRG) = 1 430).
· PROPIONATE DE FLUTICASONE/SALMETEROL BGR, suspension pour inhalation en flacon pressurisé est conditionnée dans un aérosol-doseur qui délivre des doses prémesurées sous forme de suspension pressurisée à inhaler par la bouche pour atteindre les poumons.
· La cartouche pressurisée contient une suspension pour inhalation blanche à blanchâtre.
· Les cartouches sont insérées dans un applicateur en plastique muni d’un embout buccal fermé par un capuchon.
· Les dispositifs sont conditionnés dans des boîtes contenant 1, 2, 3 ou 10 flacons.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
15, BOULEVARD CHARLES DE GAULLE
92700 COLOMBES
Exploitant de l’autorisation de mise sur le marché
BIOGARAN
15, BOULEVARD CHARLES DE GAULLE
92700 COLOMBES
ZONE INDUSTRIELLE N°2
23 RUE LAVOISIER
27000 EVREUX
ou
GLAXO WELLCOME S.A.
AVENIDA DE EXTREMADURA, 3
09400, ARANDA DE DUERO
BURGOS
ESPAGNE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Sans objet.
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).