
ANSM - Mis à jour le : 24/12/2024
FLAGYL 125 mg/5 ml, suspension buvable
2. COMPOSITION QUALITATIVE ET QUANTITATIVE 
Métronidazole......................................................................................................................... 2,5 g
(sous forme de benzoate de métronidazole ............................................................................. 4,0 g)
Pour 100 ml.
1 cuillère-mesure (5 ml) contient 125 mg de métronidazole.
Excipients à effet notoire : éthanol 31,4 mg par 5 ml, saccharose, parahydroxybenzoate de méthyle (E218), parahydroxybenzoate de propyle (E216).
Pour la liste complète des excipients, voir rubrique 6.1.
4.1. Indications thérapeutiques 
Elles sont limitées aux infections dues aux germes définis comme sensibles :
· Amibiases,
· Trichomonases urogénitales,
· Vaginites non spécifiques,
· Lambliases,
· Traitement curatif des infections médico-chirurgicales à germes anaérobies sensibles,
· Relais des traitements curatifs par voie injectable des infections à germes anaérobies sensibles.
Il convient de tenir compte des recommandations officielles concernant l'utilisation appropriée des antibactériens.
4.2. Posologie et mode d'administration 
· Amibiase
o Adultes
1,50 g par jour en trois prises.
o Enfants
30 à 40 mg/kg/jour en trois prises.
Dans l'amibiase hépatique, au stade abcédaire, l'évacuation de l'abcès doit être effectuée conjointement au traitement par le métronidazole.
La durée de traitement est de sept jours consécutifs.
· Trichomonase
o Chez la femme (urétrites et vaginites à Trichomonas), de préférence, traitement mixte de dix jours comportant :
§ 0,50 g par jour par voie orale en deux prises.
§ 1 ovule par jour.
Que le partenaire présente ou non des signes cliniques d'infestation à Trichomonas vaginalis, il importe qu'il soit traité concurremment, même en l'absence d'une réponse positive du laboratoire.
o Chez l'homme (uréthrites à Trichomonas) :
0,50 g par voie orale en deux prises pendant dix jours.
Très exceptionnellement, il peut être nécessaire d'élever à 0,750 g ou à 1 g la dose journalière.
· Lambliase
o Adultes
0,750 g à 1 g par jour pendant cinq jours consécutifs.
o Enfants de :
2 à 5 ans : 250 mg/jour.
5 à 10 ans : 375 mg/jour.
10 à 15 ans : 500 mg/jour.
· Vaginites non spécifiques
500 mg 2 fois par jour pendant sept jours.
Un traitement simultané du partenaire doit être pratiqué.
· Traitement des infections à germes anaérobies
(en première intention ou en traitement de relais).
o Adultes :
1 à 1,5 g/jour.
o Enfants :
20 à 30 mg/kg/jour.
Mode d’administration
Voie orale.
Utilisez la cuillère-mesure pour administration orale fournie avec le flacon dans la boîte (voir rubrique 6.6).
4.4. Mises en garde spéciales et précautions d'emploi 
Hypersensibilité/peau et annexes
Des réactions d’allergie, y compris des chocs anaphylactiques, peuvent survenir et mettre en jeu le pronostic vital (voir rubrique 4.8). Dans ce cas, le métronidazole doit être interrompu et un traitement médical adapté doit être mis en place.
La survenue, en début de traitement, d’un érythème généralisé fébrile associé à des pustules, doit faire suspecter une pustulose exanthématique aiguë généralisée (voir rubrique 4.8) ; elle impose l’arrêt du traitement et contre-indique toute nouvelle administration de métronidazole seul ou associé.
Des cas de réactions cutanées sévères incluant syndrome de Stevens-Johnson, syndrome de Lyell, Pustulose Exanthématique Aiguë Généralisée (PEAG) ont été rapportés avec le métronidazole. Les patients doivent être informés des signes et symptômes et une surveillance cutanée rapprochée doit être pratiquée.
La survenue de signes ou symptômes du Syndrome de Stevens-Jonhson, Syndrome de Lyell (par exemple : éruption progressive souvent accompagnée de bulles ou de lésions des muqueuses) ou AGEP (érythème généralisé fébrile associé à des pustules) (voir rubrique 4.8) impose l’arrêt du traitement et contre-indique toute nouvelle administration de métronidazole seul ou associée.
Système nerveux central
Si des symptômes évocateurs d’encéphalopathie ou de syndrome cérébelleux (par exemple : ataxie, dysarthrie, troubles de la démarche, nystagmus, tremblements, vertiges, confusions, convulsions, neuropathies sensitives périphériques, céphalées (voir rubrique 4.8)) apparaissent, la prise en charge du patient doit être immédiatement réévaluée et le traitement par le métronidazole doit être arrêté.
Des cas d’encéphalopathie ont été rapportés lors de la surveillance de ce médicament post-commercialisation. Des cas de modifications de l’IRM associées à une encéphalopathie ont également été observés (voir rubrique 4.8). Les lésions observées sont localisées le plus fréquemment dans le cervelet (particulièrement dans le noyau dentelé) et dans le splenium du corps calleux. La plupart des cas d’encéphalopathie et de modifications de l’IRM sont réversibles à l’arrêt du traitement. D’exceptionnels cas d’évolution fatale ont été rapportés.
Surveiller l’apparition de signes évocateurs d’encéphalopathie ou en cas d’aggravation chez des malades atteints d’affection neurologique centrale.
En cas de méningite aseptique sous métronidazole, la réintroduction du traitement est déconseillée ou doit faire l’objet d’une appréciation du rapport bénéfice-risque en cas d’infection grave.
Système nerveux périphérique
Surveiller l’apparition de signes évocateurs de neuropathies périphériques, en particulier en cas de traitement prolongé ou chez les malades atteints d’affections neurologiques périphériques sévères, chroniques ou évolutives.
Troubles psychiatriques
Des réactions psychotiques avec possible comportement à risque pour le patient, peuvent survenir dès les premières prises du traitement, notamment en cas d’antécédents psychiatriques (voir rubrique 4.8). Le métronidazole doit alors être arrêté, le médecin informé et les mesures thérapeutiques nécessaires prises immédiatement.
En cas d’antécédents de troubles hématologiques, de traitement à forte dose et/ou de traitement prolongé, il est recommandé de pratiquer régulièrement des examens sanguins, particulièrement le contrôle de la formule leucocytaire.
En cas de leucopénie, l’opportunité de la poursuite du traitement dépend de la gravité de l’infection.
Hépatotoxicité chez les patients atteints du syndrome de Cockayne
Des cas d'hépatotoxicité sévère/d'insuffisance hépatique aiguë, y compris des cas entraînant une issue fatale avec une survenue très rapide après l'initiation du traitement chez des patients atteints du syndrome de Cockayne, ont été rapportés avec des produits contenant du métronidazole destinés à une utilisation systémique. Dans cette population, le métronidazole ne doit pas être utilisé sauf si le bénéfice est considéré comme supérieur au risque et si aucun traitement alternatif n'est disponible. Des tests de la fonction hépatique doivent être réalisés juste avant le début du traitement, tout au long de celui-ci et après la fin du traitement, jusqu'à ce que la fonction hépatique se situe dans les limites des valeurs normales, ou jusqu'à ce que les valeurs initiales soient obtenues. Si les tests de la fonction hépatique deviennent nettement élevés pendant le traitement, la prise du médicament doit être interrompue.
Il faut informer les patients atteints du syndrome de Cockayne de rapporter immédiatement tous les symptômes de lésions hépatiques potentielles à leur médecin et d'arrêter la prise de métronidazole (voir rubrique 4.8).
Excipients à effet notoire
Ce médicament contient du saccharose. Son utilisation est déconseillée chez les patients présentant une intolérance au fructose, un syndrome de malabsorption du glucose et du galactose ou de déficit en sucrase/isomaltase.
Ce médicament contient 3 g de saccharose par cuillère-mesure dont il faut tenir compte dans la ration journalière en cas de régime pauvre en sucre ou de diabète.
Ce médicament contient 31,4 mg d’éthanol par cuillère-mesure de 5 ml ce qui est équivalent à 6,28 mg par ml (0,628 % p/v). La quantité d’éthanol pour 5 ml de ce médicament équivaut à moins de 1 ml de bière ou moins de 1 ml de vin.
La faible quantité d'éthanol contenue dans ce médicament n'est pas susceptible d'entraîner d'effet notable.
Ce médicament contient moins de 1 mmol (23 mg) de sodium par dose c’est-à-dire qu’il est essentiellement « sans sodium ».
Ce médicament contient du « parahydroxybenzoate » et peut provoquer des réactions allergiques (éventuellement retardées).
Interactions médicamenteuses
L’utilisation concomitante de métronidazole et d’alcool est déconseillée (voir rubrique 4.5).
L’utilisation concomitante de métronidazole et de busulfan est déconseillée (voir rubrique 4.5).
L’utilisation concomitante de métronidazole et de disulfirame est déconseillée (voir rubrique 4.5).
Interférence avec les examens paracliniques et les tests de laboratoire
Le métronidazole peut immobiliser les tréponèmes et donc faussement positiver un test de Nelson.
Le métronidazole peut interférer avec certains types de tests sanguins (alanine aminotransférase [ALAT], aspartate aminotransférase [ASAT], lactate déshydrogénase [LDH], triglycérides, glucose), ce qui peut conduire à un faux négatif ou à un résultat anormalement bas. Ces méthodes analytiques sont basées sur une diminution de l’absorbance dans l’ultraviolet, ce qui se produit lorsque le nicotinamide adénine dinucléotide hydrogéné (NADH) est oxydé en nicotinamide adénine dinucléotide (NAD). Cette interférence est due à la similarité des pics d’absorption du NADH (340 nm) et du métronidazole (322 nm) à pH 7.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions 
Les médicaments provoquant une réaction antabuse avec l’alcool sont nombreux, et leur association avec l’alcool est déconseillée.
Associations déconseillées
+ Alcool (boisson ou excipient)
Effet antabuse (chaleur, rougeurs, vomissements, tachycardie). Eviter la prise de boissons alcoolisées et de médicaments contenant de l’alcool. Tenir compte de l’élimination complète des médicaments en se référant à leur demi-vie avant la reprise de boissons alcoolisées ou du médicament contenant de l’alcool.
+ Busulfan
Avec le busulfan à fortes doses : doublement des concentrations de busulfan par le métronidazole.
+ Disulfirame
Risque d’épisodes de psychose aiguë ou d’état confusionnel, réversibles à l’arrêt de l’association.
+ Médicaments provoquant un allongement de l’intervalle QT
Des cas d’allongements de l’intervalle QT ont été rapportés, en particulier lorsque le métronidazole est administré avec des médicaments susceptibles d’allonger l’intervalle QT.
Associations faisant l'objet de précautions d’emploi
+ Anticonvulsivants inducteurs enzymatiques
Diminution des concentrations plasmatiques du métronidazole par augmentation de son métabolisme hépatique par l’inducteur.
Surveillance clinique et adaptation éventuelle de la posologie de métronidazole pendant le traitement par l’inducteur et après son arrêt.
+ Rifampicine
Diminution des concentrations plasmatiques du métronidazole par augmentation de son métabolisme hépatique par la rifampicine.
Surveillance clinique et adaptation éventuelle de la posologie de métronidazole pendant le traitement par la rifampicine et après son arrêt.
+ Lithium
Augmentation de la lithémie pouvant atteindre des valeurs toxiques, avec signes de surdosage en lithium.
Surveillance stricte de la lithémie et adaptation éventuelle de la posologie du lithium.
Associations à prendre en compte
+ Fluoro-uracile (et par extrapolation, tegafur et capécitabine)
Augmentation de la toxicité du fluoro-uracile par diminution de sa clairance.
Problèmes particuliers du déséquilibre de l'INR:
De nombreux cas d'augmentation de l'activité des anticoagulants oraux ont été rapportés chez des patients recevant des antibiotiques. Le contexte infectieux ou inflammatoire marqué, l'âge et l'état général du patient apparaissent comme des facteurs de risque. Dans ces circonstances, il apparaît difficile de faire la part entre la pathologie infectieuse et son traitement dans la survenue du déséquilibre de l'INR. Cependant, certaines classes d'antibiotiques sont davantage impliquées : il s'agit notamment des fluoroquinolones, des macrolides, des cyclines, du cotrimoxazole et de certaines céphalosporines.
4.6. Fertilité, grossesse et allaitement 
Grossesse
Les études chez l'animal n'ont pas mis en évidence d'effet tératogène. En l'absence d'effet tératogène chez l'animal, un effet malformatif dans l'espèce humaine n'est pas attendu. En effet, à ce jour, les substances responsables de malformations dans l'espèce humaine se sont révélées tératogènes chez l'animal au cours d'études bien conduites sur deux espèces.
En clinique, l'analyse d'un nombre élevé de grossesses exposées n'a apparemment révélé aucun effet malformatif ou fœtotoxique particulier du métronidazole. Toutefois, seules des études épidémiologiques permettraient de vérifier l'absence de risque. En conséquence, le métronidazole peut être prescrit pendant la grossesse si besoin.
Le métronidazole passant dans le lait maternel, éviter l'administration de ce médicament pendant l'allaitement.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines 
Affections hématologiques et du système lymphatique
· Neutropénie, agranulocytose, thrombopénie.
Affections cardiaques
· Fréquence indéterminée : des cas d’allongements de l’intervalle QT ont été rapportés, en particulier lorsque le métronidazole est administré avec des médicaments susceptibles d’allonger l’intervalle QT.
Affections psychiatriques
· Hallucinations,
· Réactions psychotiques avec paranoïa et/ou délire pouvant s’accompagner de manière isolée d’idées ou d’actes suicidaires (voir rubrique 4.4),
· Humeur dépressive.
Affections du système nerveux
· Neuropathies sensitives périphériques,
· Céphalées,
· Vertiges,
· Confusion,
· Convulsions,
· Encéphalopathie pouvant être associés à des modifications de l’IRM généralement réversibles à l’arrêt du traitement. D’exceptionnels cas d’évolution fatale ont été rapportés (voir rubrique 4.4),
· Syndrome cérébelleux subaigu (ataxie, dysarthrie, troubles de la démarche, nystagmus, tremblements) (voir rubrique 4.4),
· Méningite aseptique (voir rubrique 4.4).
Affections oculaires
· Troubles visuels transitoires tels que vision trouble, diplopie, myopie, diminution de l’acuité visuelle, changement dans la vision des couleurs,
· Neuropathies/névrites optiques.
Affections gastro-intestinales
· Troubles digestifs bénins (douleurs épigastriques, nausées, vomissements, diarrhée),
· Glossites avec sensation de sécheresse de la bouche, stomatites, troubles du goût, anorexie,
· Pancréatites réversibles à l'arrêt du traitement,
· Décoloration ou modification de l’aspect de la langue (mycose).
Affections hépatobiliaires
· Elévations des enzymes hépatiques (ALAT, ASAT, phosphatases alcalines), très rares cas d’atteinte hépatique aiguë de nature cytolytique (parfois ictérique), cholestatique ou mixte. Des cas isolés d’insuffisance hépatocellulaire pouvant nécessiter une transplantation hépatique ont été rapportés.
· Des cas d'hépatotoxicité sévère irréversible/insuffisance hépatique aiguë, y compris des cas d'issue fatale avec une apparition très rapide après l'initiation de l'utilisation systémique du métronidazole, ont été rapportés chez des patients atteints du syndrome de Cockayne (voir rubrique 4.4).
Affections de la peau et du tissu sous-cutané
· Bouffées congestives, prurit, éruption cutanée parfois fébrile,
· Urticaire, œdème de Quincke, choc anaphylactique (voir rubrique 4.4),
· Très rares cas de pustulose exanthématique aiguë généralisée (voir rubrique 4.4),
· Syndrome de Lyell,
· Syndrome de Stevens Johnson,
· Erythème pigmenté fixe.
Divers
· Apparition d’une coloration brun-rougeâtre des urines due à la présence de pigments hydrosolubles provenant du métabolisme du produit.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr.
Des cas d'administration d'une dose unique jusqu'à 12 g ont été rapportés lors de tentatives de suicide et de surdosage accidentel.
Les symptômes se sont limités à des vomissements, ataxie et légère désorientation. Il n'y a pas d'antidote spécifique pour les surdosages de métronidazole. En cas de surdosage massif, le traitement est symptomatique.
5. PROPRIETES PHARMACOLOGIQUES 
5.1. Propriétés pharmacodynamiques 
Les concentrations critiques séparent les souches sensibles des souches de sensibilité intermédiaire et ces dernières, des résistantes : S ≤ 4 mg/l et R > 4 mg/l.
La prévalence de la résistance acquise peut varier en fonction de la géographie et du temps pour certaines espèces. Il est donc utile de disposer d'informations sur la prévalence de la résistance locale, surtout pour le traitement d'infections sévères. Ces données ne peuvent apporter qu'une orientation sur les probabilités de la sensibilité d'une souche bactérienne à cet antibiotique.
Lorsque la variabilité de la prévalence de la résistance en France est connue pour une espèce bactérienne, elle est indiquée dans le tableau ci-dessous :
|
Catégories |
Fréquence de résistance acquise en France (> 10 %) (valeurs extrêmes) |
|
Espèces sensibles |
|
|
Aérobies à Gram négatif |
|
|
Helicobacter pylori |
30 % |
|
Anaérobies |
|
|
Bacteroides fragilis |
|
|
Bifidobacterium |
60 – 70 % |
|
Bilophila |
|
|
Clostridium |
|
|
Clostridium difficile |
|
|
Clostridium perfringens |
|
|
Eubacterium |
20 – 30 % |
|
Fusobacterium |
|
|
Peptostreptococcus |
|
|
Porphyromonas |
|
|
Prevotella |
|
|
Veillonella |
|
|
Espèces résistantes |
|
|
Aérobies à Gram positif |
|
|
Actinomyces |
|
|
Anaérobies |
|
|
Mobiluncus |
|
|
Propionibacterium acnes |
|
|
Activité antiparasitaire |
|
|
Entamoeba histolytica |
|
|
Giardia intestinalis |
|
|
Trichomonas vaginalis |
|
5.2. Propriétés pharmacocinétiques 
L'hydrolyse du benzoate de métronidazole est réalisée progressivement au cours de son cheminement dans le tube digestif. L'absorption du benzoate de métronidazole est inférieure de 30 % (aire sous la courbe) à celle du métronidazole.
Le pic plasmatique apparaît à la 4ème heure suivant l'administration per os du produit.
A posologie identique, métronidazole et benzoate de métronidazole ne présentent pas de résultats thérapeutiques significativement différents.
La demi-vie plasmatique est de 6.9 h par H.P.L.C.
Diffusion
· La liaison aux protéines sanguines est inférieure à 10 %.
· La diffusion est rapide et importante dans : les poumons, les reins, le foie, la peau, la bile, le LCR, la salive, le liquide séminal, les sécrétions vaginales.
Le métronidazole traverse la barrière placentaire et passe dans le lait maternel.
Biotransformation
Il donne deux métabolites non conjugués ayant une activité anti-bactérienne (10 %).
Elimination
Forte concentration hépatique et biliaire. Faible concentration colique. Faible élimination fécale. Excrétion surtout urinaire (40 à 70% dont 20% environ sous forme inchangée) entraînant une coloration des urines en brun ou rougeâtre.
5.3. Données de sécurité préclinique 
2 ans.
Après ouverture du flacon, ce médicament doit être conservé au maximum 8 jours.
6.4. Précautions particulières de conservation 
A conserver à une température ne dépassant pas 30 °C.
6.5. Nature et contenu de l'emballage extérieur 
120 ml en flacon (verre) et bouchon sécurité enfant en polypropylène/polyéthylène avec film en polyéthylène, avec cuillère-mesure de 5 ml.
6.6. Précautions particulières d’élimination et de manipulation 
1.Pour ouvrir le flacon, il faut tourner le bouchon de sécurité-enfant en appuyant dessus, comme indiqué sur le schéma ci-après :

2. Ce médicament s’administre à l’aide d’une cuillère-mesure pour administration orale fournie avec le flacon dans la boîte. L’usage de cette cuillère-mesure est strictement réservé à l’administration orale de FLAGYL 125 mg/5 ml, suspension buvable.
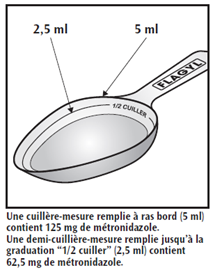
Le volume total de la cuillère-mesure remplie à ras bord correspond à un volume de 5 ml, soit une dose de 125 mg de métronidazole.
Il est possible d’administrer un volume de 2,5 ml, équivalent à une dose de 62,5 mg de métronidazole, à l’aide de la cuillère-mesure remplie au niveau de la graduation « ½ cuiller ».
3. Après chaque utilisation, refermer le flacon de la suspension buvable, bien rincer la cuillère-mesure pour administration orale avec de l’eau et la sécher. Puis ranger immédiatement la cuillère-mesure pour administration orale dans sa boîte dans un endroit inaccessible aux enfants. Ne jamais séparer la cuillère-mesure pour administration orale des autres éléments de conditionnement du médicament (flacon, boîte, notice).
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur. Une fois le traitement terminé, il doit être rapporté au pharmacien (boîtes entamées y compris la cuillère-mesure ainsi que le flacon) pour une destruction correcte et appropriée de ce médicament.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE 
1 PARVIS DE LA DEFENSE
IMMEUBLE PAROI NORD DE LA GRANDE ARCHE
92800 PUTEAUX
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE 
· 313 169-4 : 120 ml en flacon (verre) et bouchon sécurité-enfant en polypropylène/polyéthylène avec film en polyéthylène, avec cuillère-mesure de 5 ml ; boîte de 1.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION 
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE 
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES 
Liste I.
|
| Plan du site | Accessibilité | Contact | Téléchargement | Declaration de confidentialité | Service-Public.fr | Legifrance | Gouvernement.fr |