Dernière mise à jour le 02/03/2026
COLOFOAM, mousse rectale
Indications thérapeutiques
Classe pharmacothérapeutique : corticoïde à usage local - code ATC : A07EA02.
Ce médicament est un anti-inflammatoire intestinal. Il est indiqué dans les cas de :
· Rectocolite hémorragique : maladie inflammatoire chronique de la muqueuse du rectum et du côlon responsable d’ulcération et se manifestant par des rectorragies (saignement d’origine rectale).
· Maladie de Crohn : maladie inflammatoire de tout ou partie de l’intestin et se manifestant principalement par des douleurs abdominales, des troubles du transit (diarrhée), de la fièvre et un amaigrissement.
· Rectite post-radique : inflammation rectale secondaire à un traitement par radiothérapie.
· Rectite après colectomie : inflammation du rectum après ablation de la totalité ou d’une partie du côlon.
Présentations
> 1 flacon(s) pressurisé(e)(s) aluminium de 20 g - avec applicateur - avec valve doseuse -
Code CIP : 326 061-2 ou 34009 326 061 2 2
Déclaration de commercialisation : 19/08/1983
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 15,46 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 16,48 €
- Taux de remboursement :65%
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 07/02/2018 | Renouvellement d'inscription (CT) | Le service médical rendu par COLOFOAM reste important dans les indications de l’AMM. |
Amélioration du service médical rendu (ASMR)
Pas d'ASMR disponible pour ce médicament (plus d'informations dans l'aide )
ANSM - Mis à jour le : 01/04/2024
COLOFOAM, mousse rectale
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Acétate d’hydrocortisone ..................................................................................................... 2,000 g
Pour un flacon de 20 g de mousse (14 doses)
Une dose contient environ 100 mg d’acétate d’hydrocortisone.
Excipients à effet notoire : propylène glycol (4,000 g/20 g), alcool cétylique (0,036 g/20 g), parahydroxybenzoate de méthyle (0,020g/20g), parahydroxybenzoate de propyle (0,002 g/20 g).
Pour la liste complète des excipients, voir rubrique 6.1.
Mousse rectale
4.1. Indications thérapeutiques
Les indications thérapeutiques sont limitées à :
· rectocolite hémorragique
· rectite post-radique
· rectite après colectomie
· maladie de Crohn colique
4.2. Posologie et mode d'administration
Posologie
· En général, une application par jour, pendant deux à trois semaines, puis éventuellement une application un jour sur deux.
Mode d’administration
· Pour l'administration, le malade sera couché sur le côté.
· Ne jamais introduire directement le poussoir du boîtier dans l'anus.
· Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
· Contre-indications de la corticothérapie générale, en particulier :
o ulcère gastro-duodénal en évolution
o tout état infectieux ou mycosique non contrôlé par un traitement spécifique.
· Contre-indications locales : obstruction, abcès, perforation, péritonite, anastomose intestinale récente, fistule extensive.
4.4. Mises en garde spéciales et précautions d'emploi
· Bien que dans le cadre des études cliniques disponibles, peu de complications d'hypercorticisme aient été observées, ce risque potentiel doit être envisagé et mis en balance avec les effets bénéfiques attendus de l'utilisation de ce produit.
· Les précautions d'emploi communes à toute thérapeutique corticostéroïde doivent être observées en cas de traitement prolongé ou de posologies élevées.
· Une attention particulière doit être portée chez les enfants lors d’un traitement par corticoïde en raison du risque de retard de croissance.
· Lors d’un traitement des patients diabétiques par corticoïde, il faut prendre en considération que ces patients peuvent nécessiter de davantage d'insuline ou d'antidiabétiques oraux.
· Les corticostéroïdes peuvent provoquer une élévation de la pression artérielle, une rétention de sel et d'eau dans le sang et une augmentation de l'excrétion urinaire de potassium. Par conséquent, une attention particulière devra être portée aux patients souffrant d'insuffisance cardiaque, rénale ou d'hypertension.
· Ce médicament ne devrait pas être utilisé chez les patients atteints de glaucome aigu ou de glaucome à angle ouvert.
· Perturbation visuelle : Une perturbation visuelle peut être signalée lors d’une utilisation systémique et topique de corticoïdes. Si un patient présente des symptômes tels qu’une vision trouble ou d'autres troubles visuels, le patient doit être dirigé vers un ophtalmologiste afin d'évaluer les causes possibles, ce qui peut inclure la cataracte, le glaucome ou des maladies rares telles que la Choriorétinopathie Séreuse Centrale (CRSC), qui ont été rapportés après utilisation de corticoïdes systémiques et topiques.
· Des effets indésirables psychiatriques potentiellement graves peuvent survenir avec des stéroïdes systémiques. Une attention particulière doit être portée chez les patients ayant des antécédents de troubles affectifs sévères.
· Les patients ne devraient pas être vaccinés avec des vaccins vivants pendant un traitement par corticostéroïde.
· Les patients sous traitement prolongé devraient être surveillés pour des effets systémiques. Le traitement devrait être interrompu progressivement. L’arrêt brutal du traitement devrait être évité.
· L'administration sera prudente chez les patients atteints de rectocolites ulcéreuses sévères, en raison du risque de perforation de la paroi intestinale.
· Ce médicament contient du parahydroxybenzoate de méthyle (E218) et du parahydroxybenzoate de propyle (E216) et peut provoquer des réactions allergiques (éventuellement retardées).
· Ce médicament contient du propylène glycol et peut causer une irritation cutanée.
· Ce médicament contient de l’alcool cétylique et peut provoquer des réactions cutanées locales (par exemple dermatite de contact).
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
A ce jour, aucune interaction n'a été rapportée avec COLOFOAM. Toutefois, du fait de l’absorption systémique de la substance active (hydrocortisone) jusqu'à 5% dans le tractus gastro-intestinal, il convient de tenir compte des interactions médicamenteuses habituelles des corticoïdes.
Médicaments hypokaliémiants
L’hypokaliémie est un facteur favorisant l’apparition de troubles du rythme cardiaque (torsades de pointes, notamment) et augmentant la toxicité de certains médicaments, par exemple la digoxine. De ce fait, les médicaments qui peuvent entrainer une hypokaliémie sont impliqués dans un grand nombre d’interactions. Il s’agit des diurétiques hypokaliémiants, seuls ou associés, des laxatifs stimulants, des glucocorticoïdes, du tétracosactide et de l’amphotéricine B (voie IV).
Il est prévu que l’administration concomitante d’inhibiteurs du CYP3A, y compris de produits contenant du cobicistat, augmente le risque d’effets secondaires systémiques. L’association doit être évitée, sauf si les bénéfices sont supérieurs au risque accru d’effets secondaires systémiques des corticostéroïdes ; dans ce cas, les patients doivent être surveillés en vue de détecter les éventuels effets secondaires systémiques des corticostéroïdes.
Associations déconseillées
+ Acide acétylsalicylique à des doses anti-inflammatoires (≥ 1g par prise et/ou ≥ 3g par jour)
Majoration du risque hémorragique.
+ Vaccins vivants atténués
Glucocorticoïdes (voies générale et rectale) : risque de maladie vaccinale généralisée, potentiellement mortelle.
Associations faisant l'objet de précautions d’emploi
+ Anticoagulants oraux
Glucocorticoïdes (voies générale et rectale) : impact éventuel de la corticothérapie sur le métabolisme de l’antivitamine K et sur celui des facteurs de la coagulation. Risque hémorragique propre à la corticothérapie (muqueuse digestive, fragilité vasculaire) à fortes doses ou en traitement prolongé supérieur à 10 jours.
Lorsque l’association est justifiée, renforcer la surveillance : le cas échéant, contrôle biologique au 8ème jour, puis tous les 15 jours pendant la corticothérapie et après son arrêt.
+ Inducteurs enzymatiques (carbamazepine, efavirenz, fosphenytoine, nevirapine, oxcarbazepine, phenobarbital, phenytoine, primidone, rifabutine, rifampicine)
Risque de diminution de l’efficacité de l’hydrocortisone (augmentation de son métabolisme) ; les conséquences sont graves lorsque l’hydrocortisone est administrée en traitement substitutif ou en cas de transplantation. Surveillance clinique et biologique ; adaptation de la posologie de l’hydrocortisone pendant l’association et après l’arrêt de l’inducteur enzymatique.
+ Autres hypokaliémiants
Risque majoré d’hypokaliémie. Surveillance de la kaliémie avec si besoin correction.
+ Digitaliques (deslanoside, digitoxine, digoxine)
Hypokaliémie favorisant les effets toxiques des digitaliques. Corriger auparavant toute hypokaliémie et réaliser une surveillance clinique, électrolytique et électrocardiographique.
+ Isoniazide (décrit pour la prednisolone)
Diminution des concentrations plasmatiques de l’isoniazide. Mécanisme invoqué : augmentation du métabolisme hépatique de l’isoniazide et diminution de celui des glucocorticoïdes. Surveillance clinique et biologique.
+ Médicaments susceptibles de donner des torsades de pointes (amiodarone, amisulpride, arsenieux, bepridil, chlorpromazine, cisapride, cyamemazine, diphemanil, disopyramide, dofetilide, dolasetron, droperidol, erythromycine, flupentixol, fluphenazine, halofantrine, haloperidol, hydroquinidine, ibutilide, levomepromazine, lumefantrine, methadone, mizolastine, moxifloxacine, pentamidine, pimozide, pipamperone, pipotiazine, quinidine, sertindole, sotalol, spiramycine, sulpiride, sultopride, tiapride, toremifene, vincamine, zuclopenthixol).
Risque majoré de troubles du rythme ventriculaire, notamment de torsades de pointes. Corriger toute hypokaliémie avant d’administrer le produit et réaliser une surveillance clinique, électrolytique et électrocardiographique.
+ Rifampicine
Diminution des concentrations plasmatiques et de l’efficacité des corticoïdes par augmentation de leur métabolisme hépatique par la rifampicine ; les conséquences sont particulièrement importantes chez les addisoniens traités par l’hydrocortisone et en cas de transplantation.
Surveillance clinique et biologique : adaptation de la posologie des corticoïdes pendant le traitement par la rifampicine et après son arrêt.
+ Topiques gastro-intestinaux, antiacides et adsorbants
Décrit pour la prednisolone, la dexaméthasone. Diminution de l’absorption digestive des glucocorticoïdes.
Prendre les topiques gastro-intestinaux et antiacides à distance des glucocorticoïdes (plus de 2 heures, si possible).
+ Macrolides et kétoconazole
Diminution de la clairance des corticostéroïdes.
+ Agents antidiabétiques
Diminution de l'effet de réduction du sucre dans le sang
+ Agents antirétroviraux
Risque de suppression surrénalienne.
Associations à prendre en compte
+ Acide acétylsalicylique à des doses antalgiques ou antipyrétiques (≥ 500 mg par prise et/ou <3 g par jour).
Majoration du risque hémorragique.
+ Anti-inflammatoires non stéroïdiens
Augmentation du risque d’ulcération et d’hémorragie gastro-intestinale.
+ Curares non dépolarisants
Avec les glucocorticoïdes par voie IV : risque de myopathie sévère, réversible après un délai éventuellement long (plusieurs mois).
+ Fluoroquinolones
Possible majoration du risque de tendinopathie, voire de rupture tendineuse (exceptionnelle), particulièrement chez les patients recevant une corticothérapie prolongée.
4.6. Fertilité, grossesse et allaitement
Grossesse
Chez l'animal, l'expérimentation met en évidence un effet tératogène, variable selon les espèces.
Dans l'espèce humaine, les études épidémiologiques n'ont décelé aucun risque malformatif lié à la prise de corticoïdes per os et notamment de l'hydrocortisone lors du premier trimestre.
Lors de maladies chroniques nécessitant un traitement tout au long de la grossesse, un léger retard de croissance intra-utérin est possible. Une insuffisance surrénale néonatale a été exceptionnellement observée après corticothérapie à doses élevées. Il semble justifié d'observer une période de surveillance clinique (poids, diurèse) et biologique (glycémie) du nouveau-né.
En conséquence, ce médicament peut être prescrit pendant la grossesse si besoin.
Allaitement
L'hydrocortisone est excrétée dans le lait maternel. Le retentissement biologique ou clinique pour l’enfant allaité, notamment en termes de retard de croissance, ne peut être exclu. Par conséquent ce médicament ne doit pas être utilisé pendant l'allaitement. Sinon, l'allaitement maternel devrait être interrompu.
Fertilité
L’effet de l’hydrocortisone sur la fertilité chez l’homme ou la femme traité par COLOFOAM n’est pas connu.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
COLOFOAM n’a aucun effet ou un effet négligeable sur l’aptitude à conduire des véhicules et à utiliser des machines. Cependant, des troubles visuels peuvent se produire sous corticothérapie (voir rubriques 4.4 et 4.8). Si cela est le cas, il convient de ne pas conduire de véhicules ou d’utiliser des machines.
Dans le tableau ci-dessous, les effets indésirables sont classés par ordre de fréquence selon la convention suivante : très fréquent (≥1/10) ; fréquent (≥1/100, <1/10) ; peu fréquent (≥1/1 000, <1/100) ; rare (≥1/10 000, <1/1 000) ; très rare (<1/10 000) et fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
|
Classe de systèmes d’organes |
Fréquence |
Effet indésirable |
|
Infections et infestations |
Fréquence indéterminée |
Diminution de la résistance aux infections |
|
Affections du système immunitaire |
Fréquence indéterminée |
Réaction d’hypersensibilité incluant les réactions anaphylactiques, angiœdème. |
|
Troubles oculaires |
Fréquence indéterminée |
Vision trouble (voir rubrique 4.4) |
|
Affections gastro-intestinales |
Fréquence indéterminée |
Proctalgie, gène anorectale |
|
Affections de la peau et du tissu sous-cutané |
Fréquence indéterminée |
Dermatite allergique, urticaire, prurit, rash |
|
Troubles généraux et anomalies au site d’administration |
Fréquence indéterminée |
Réactions au site d’application telles qu’érythème, irritation, brûlure, sécheresse |
Les corticoïdes peuvent entraîner des effets indésirables systémiques (comme le syndrome de Cushing, une diminution de la résistance aux infections), en particulier lors d'une utilisation à long terme, et si le médicament n'est pas utilisé comme indiqué.
Le risque d'effets indésirables systémiques lorsqu'il est utilisé à la dose correcte par la voie d'administration locale est beaucoup plus faible qu'en cas d’utilisation par voie générale.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.signalement-sante.gouv.fr.
Aucun cas de surdosage n’a été rapporté, cependant une utilisation excessive pourra entrainer une exacerbation des effets indésirables.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : corticoïde à usage local, code ATC : A07EA02
Mécanisme d’action
L'acétate d'hydrocortisone a une activité anti-inflammatoire résultant, au moins en partie, de la liaison avec un récepteur aux glucocorticoïdes.
Ils agissent en diminuant la perméabilité capillaire, en inhibant la production de facteurs chimiotactiques et en réduisant la migration des cellules inflammatoires dans le tissu.
5.2. Propriétés pharmacocinétiques
Les stéroïdes appliqués topiquement agissent principalement localement. Après administration rectale, la biodisponibilité de l'acétate d'hydrocortisone varie entre 2% et 3% chez les sujets sains, et entre 4% et 5% chez les patients traités.
5.3. Données de sécurité préclinique
Les études chez l’animal ont montré qu’une exposition prénatale à de très fortes doses de glucocorticoïdes peut entraîner des malformations (fente palatine, anomalies du squelette). Les études chez l’animal ont également montré qu’une exposition prénatale à de fortes doses de glucocorticoïdes (inférieures toutefois aux doses tératogènes) peut être associée à une augmentation du risque de retard de croissance intra-utérin, de maladie cardiovasculaire à l’âge adulte et de modification permanente de la densité des récepteurs aux glucocorticoïdes, du renouvellement des neurotransmetteurs et du comportement.
Propylène glycol, monoéther stéarylique de polyoxyéthylène glycol, alcool cétylique, éther stéarylique de macrogol 500, parahydroxybenzoate de méthyle, parahydroxybenzoate de propyle, solution aqueuse de trolamine à 2,5 pour cent, eau purifiée.
Gaz de pressurisation
Propellant HP-70 (Propane/Isobutane dans la proportion de 43/57).
Sans objet.
3 ans.
6.4. Précautions particulières de conservation
Flacon pressurisé :
A protéger des rayons du soleil, ne pas exposer à des températures supérieures à 50°C.
Ne pas percer, ne pas jeter au feu même vide.
Ne pas vaporiser vers une flamme ou un objet incandescent
Ne pas mettre au réfrigérateur.
6.5. Nature et contenu de l'emballage extérieur
20 g de mousse dans un flacon pressurisé (aluminium) avec applicateur doseur (14 doses au minimum).
6.6. Précautions particulières d’élimination et de manipulation
Pas d’exigences particulières.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
VIATRIS MEDICAL
1 BIS PLACE DE LA DEFENSE – TOUR TRINITY
92400 COURBEVOIE
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 326 061 2 2 : flacon pressurisé (aluminium) de 20 g + un applicateur doseur
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Sans objet.
Liste I
ANSM - Mis à jour le : 01/04/2024
COLOFOAM, mousse rectale
Acétate d’hydrocortisone
Veuillez lire attentivement cette notice avant d’utiliser ce médicament car elle contient des informations importantes pour vous.
- Gardez cette notice. Vous pourriez avoir besoin de la relire.
- Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
- Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
- Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que COLOFOAM, mousse rectale et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser COLOFOAM, mousse rectale ?
3. Comment utiliser COLOFOAM, mousse rectale ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver COLOFOAM, mousse rectale ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE COLOFOAM, mousse rectale ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : corticoïde à usage local - code ATC : A07EA02.
Ce médicament est un anti-inflammatoire intestinal. Il est indiqué dans les cas de :
· Rectocolite hémorragique : maladie inflammatoire chronique de la muqueuse du rectum et du côlon responsable d’ulcération et se manifestant par des rectorragies (saignement d’origine rectale).
· Maladie de Crohn : maladie inflammatoire de tout ou partie de l’intestin et se manifestant principalement par des douleurs abdominales, des troubles du transit (diarrhée), de la fièvre et un amaigrissement.
· Rectite post-radique : inflammation rectale secondaire à un traitement par radiothérapie.
· Rectite après colectomie : inflammation du rectum après ablation de la totalité ou d’une partie du côlon.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER COLOFOAM, mousse rectale ?
N’utilisez jamais COLOFOAM, mousse rectale dans les cas suivants :
· contre-indications de la corticothérapie générale, en particulier :
o ulcère gastro-duodénal en évolution,
o tout état infectieux ou mycosique (affections dues à des champignons microscopiques) non contrôlé par un traitement spécifique.
· contre-indications locales : obstruction, abcès, perforation, péritonite, anastomose intestinale récente, fistule extensive.
EN CAS DE DOUTE, IL EST INDISPENSABLE DE DEMANDER L'AVIS DE VOTRE MEDECIN OU DE VOTRE PHARMACIEN.
Adressez-vous à votre médecin ou pharmacien avant d’utiliser COLOFOAM, mousse rectale.
L’administration sera prudente chez les patients atteints de rectocolite ulcéreuse sévère, en raison du risque de perforation de la paroi intestinale.
Si vous êtes diabétique, une adaptation du traitement peut être nécessaire. Parlez-en à votre médecin.
Les corticostéroïdes peuvent provoquer une élévation de la pression artérielle, une rétention de sel et d'eau dans le sang et une augmentation de l'excrétion urinaire de potassium. Par conséquent, si vous souffrez d'insuffisance cardiaque, rénale ou si vous souffrez d’hypertension une surveillance adéquate doit être considérée.
Si vous êtes atteint de glaucome aigu ou de glaucome à angle ouvert, ce médicament ne devrait pas être utilisé.
Si vous souffrez ou avez des antécédents de troubles psychiques sévères, parlez-en à votre médecin.
En cas de traitement prolongé, l’arrêt du traitement devrait être progressif.
Contactez votre médecin en cas de vision trouble ou d’autres troubles visuels.
Ce médicament contient du parahydroxybenzoate de méthyle (E218) et du parahydroxybenzoate de propyle (E216) et peut provoquer des réactions allergiques (éventuellement retardées).
Ce médicament contient 200 mg de propylène glycol par gramme peut causer une irritation cutanée.
Ce médicament contient de l’alcool cétylique et peut provoquer des réactions cutanées locales (par exemple dermatite de contact).
Enfants
Une attention particulière doit être portée chez les enfants lors du traitement en raison du risque de retard de croissance.
Autres médicaments et COLOFOAM, mousse rectale
Informez votre médecin ou pharmacien si vous utilisez, avez récemment utilisé ou pourriez utiliser tout autre médicament.
A ce jour, aucune interaction n’a été rapportée avec COLOFOAM. Cependant, il convient de tenir compte des interactions médicamenteuses habituelles des corticoïdes.
Prévenir votre médecin en cas de vaccination récente (notamment par un vaccin vivant atténué).
Ce médicament DOIT ETRE EVITE en association à de l’aspirine à des doses anti-inflammatoires (≥ 1 g par prise et/ou ≥ 3 g par jour).
Si vous prenez ou avez pris récemment un autre médicament comme : un anticoagulant, un anti-épileptique, un hypokaliémiant (diminuant le taux de potassium comme un diurétique ou des laxatifs stimulants), des digitaliques (utilisés en cardiologie), des médicaments susceptibles de donner des troubles du rythme ventriculaire, l’isoniazide (anti-tuberculeux), la rifampicine (antibiotique), des topiques gastro-intestinaux, des antiacides, des antibiotiques de la famille des macrolides (érythromycine, spiramycine, clarithromycine, roxithromycine, azithromycine, midécamycine, josamycine, télithromycine), des médicaments antidiabétiques, du kétoconazole (utilisé lors du traitement de la maladie de Cushing), ou des antirétroviraux, y compris un médicament obtenu sans ordonnance, parlez-en à votre médecin ou à votre pharmacien.
Certains médicaments peuvent augmenter les effets de COLOFOAM et il est possible que votre médecin souhaite vous surveiller attentivement si vous prenez ces médicaments (y compris certains médicaments pour traiter l’infection à VIH : ritonavir, cobicistat).
COLOFOAM, mousse rectale avec des aliments
Sans objet.
Grossesse et allaitement
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
Ce médicament, dans les conditions normales d'utilisation, peut être utilisé pendant la grossesse si besoin. En raison du passage dans le lait maternel et d’effets potentiels chez le nouveau-né allaité, ce médicament ne doit pas être utilisé pendant l'allaitement. En cas de prescription, l'allaitement maternel devrait être interrompu.
Conduite de véhicules et utilisation de machines
COLOFOAM n’a aucun effet ou un effet négligeable sur l’aptitude à conduire des véhicules et à utiliser des machines. Cependant, des troubles visuels peuvent se produire sous corticothérapie. Si cela est le cas, il convient de ne pas conduire de véhicules ou d’utiliser des machines.
COLOFOAM, mousse rectale contient du propylène glycol, de l’alcool cétylique, du parahydroxybenzoate de propyle et du parahydroxybenzoate de méthyle.
3. COMMENT UTILISER COLOFOAM, mousse rectale ?
Posologie
Respectez toujours la posologie indiquée par votre médecin. En cas de doute, consultez votre médecin ou votre pharmacien.
En général, la dose recommandée est de :
· une application par jour pendant deux à trois semaines
· puis, dans certains cas une application un jour sur deux.
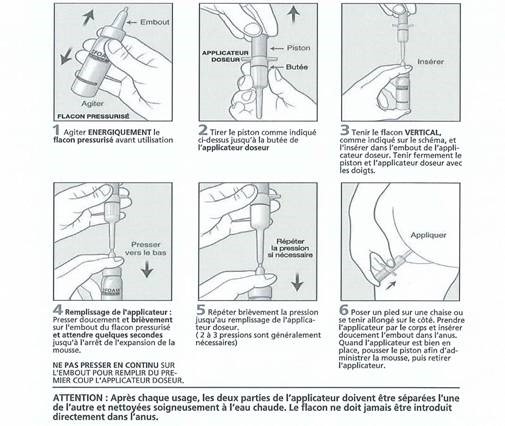
Mode et voie d’administration :
Voie rectale. Voir schéma
|
|
Si vous avez utilisé plus de COLOFOAM, mousse rectale que vous n’auriez dû
Sans objet.
Si vous oubliez d’utiliser COLOFOAM, mousse rectale
Sans objet.
Si vous arrêtez d’utiliser COLOFOAM, mousse rectale
Sans objet.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Comme tous les médicaments, ce médicament peut provoquer des effets indésirables, mais ils ne surviennent pas systématiquement chez tout le monde.
Fréquence indéterminée (fréquence ne pouvant être estimée sur la base des données disponibles) :
- vision trouble,
- diminution de la résistance aux infections,
- réactions d’hypersensibilité y compris les réactions anaphylactiques, angiœdème,
- proctalgie, gène anorectale,
- dermatite allergique, urticaire, démangeaisons, rash,
- réactions au site d’injection : érythème, irritation, brulure, sécheresse.
Comme tout produit à base de corticoïdes, en cas de traitement prolongé :
· Risque d’effets à type d’hypercorticisme (ensemble de troubles provoqués par une sécrétion trop abondante de la glande corticosurrénale).
· Risques locaux infectieux et trophiques (qui concernent la nutrition des tissus).
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.signalement-sante.gouv.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER COLOFOAM, mousse rectale ?
Tenir hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur le conditionnement extérieur. La date de péremption fait référence au dernier jour de ce mois.
Flacon pressurisé : INFLAMMABLE
A protéger des rayons du soleil, ne pas exposer à des températures supérieures à 50°C.
Ne pas percer, ne pas jeter au feu même vide.
Ne pas vaporiser vers une flamme ou un objet incandescent
Ne pas mettre au réfrigérateur.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient COLOFOAM, mousse rectale
· La substance active est :
Acétate d’hydrocortisone..................................................................................................... 2,000 g
Pour un flacon de 20 g de mousse (14 doses)
Une dose contient environ 100 mg d’acétate d’hydrocortisone.
· Les autres composants sont :
Propylène glycol, monoéther stéarylique de polyoxyéthylène glycol, alcool cétylique, éther stéarylique de macrogol 500, parahydroxybenzoate de méthyle, parahydroxybenzoate de propyle, solution aqueuse de trolamine à 2,5 pour cent, eau purifiée.
Gaz propulseur : Propellant HP-70 (Propane/Isobutane dans la proportion de 43/57)
Qu’est-ce que COLOFOAM, mousse rectale et contenu de l’emballage extérieur
Ce médicament se présente sous forme de mousse rectale ; flacon pressurisé avec applicateur doseur.
Un flacon contient 20 g de mousse (14 doses minimum).
Titulaire de l’autorisation de mise sur le marché
VIATRIS MEDICAL
1 BIS PLACE DE LA DEFENSE – TOUR TRINITY
92400 COURBEVOIE
Exploitant de l’autorisation de mise sur le marché
VIATRIS SANTE
1 BIS PLACE DE LA DEFENSE – TOUR TRINITY
92400 COURBEVOIE
PHARMASOL LIMITED
NORTH WAY
WALWORTH INDUSTRIAL ESTATE
ANDOVER
HAMPSHIRE
SP10 5AZ
ROYAUME-UNI
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).