Dernière mise à jour le 02/03/2026
EPIDUO 0,3 %/2,5 %, gel
Indications thérapeutiques
EPIDUO 0,3 %/2,5 %, gel appartient à un groupe de médicaments appelés « préparation anti-acnéique pour usage topique ». Il est utilisé pour le traitement de l'acné vulgaire, en présence de comédons (points noirs ou blancs), de nombreuses papules et pustules (boutons inflammatoires).
Ce gel est une association de 2 principes actifs, l’adapalène et le peroxyde de benzoyle qui agissent ensemble mais avec des mécanismes d’action différents :
· L’adapalène appartient à un groupe de produits appelés « rétinoïdes » et agit spécifiquement sur le mécanisme de l’acné ;
· Le peroxyde de benzoyle, agit comme un anti-microbien et a une action assouplissante et exfoliante de la couche supérieure cutanée.
EPIDUO 0,3 %/2,5 %, gel ne doit être utilisé que chez les adultes et les adolescents âgés de 12 ans et plus.
Présentations
> 1 récipient multidose polypropylène de 30 g avec système de fermeture sans entrée d'air muni d'un capuchon protecteur
Code CIP : 34009 300 811 3 6
Déclaration de commercialisation : 24/08/2017
Cette présentation n'est pas agréée aux collectivités
> 1 récipient multidose polypropylène de 45 g avec système de fermeture sans entrée d'air muni d'un capuchon protecteur
Code CIP : 34009 300 811 5 0
Déclaration de commercialisation : 25/02/2021
Cette présentation n'est pas agréée aux collectivités
Service médical rendu (SMR)
Pas de SMR disponible pour ce médicament ( plus d'informations dans l'aide )
Amélioration du service médical rendu (ASMR)
Pas d'ASMR disponible pour ce médicament (plus d'informations dans l'aide )
ANSM - Mis à jour le : 29/09/2025
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Adapalène 3 mg (0,3 % p/p)
Peroxyde de benzoyle hydraté, équivalent à 25 mg (2,5 % p/p) de peroxyde de benzoyle anhydre.
Excipient à effet notoire : propylène glycol (E1520) 40 mg/g (4,0%), polysorbate 80 (E433) ≤4 mg/g.
Pour la liste complète des excipients, voir rubrique 6.1.
Gel opaque de couleur blanche à jaune très pâle.
4.1. Indications thérapeutiques
EPIDUO 0,3 %/2,5 %, gel est indiqué chez les adultes et adolescents âgés de 12 ans et plus.
4.2. Posologie et mode d'administration
EPIDUO 0,3 %/2,5 %, gel doit être appliqué une fois par jour, le soir, sur l’ensemble des zones affectées par l’acné du visage et du tronc, sur une peau nettoyée et séchée.
La durée du traitement doit être déterminée par le prescripteur en fonction de l'état clinique global et de la réponse thérapeutique au traitement. Les premiers signes d'amélioration clinique apparaissent généralement après 1 à 4 semaines de traitement. Si aucune amélioration n’est observée après 4 à 8 semaines de traitement, l’intérêt de la poursuite du traitement doit être réévalué.
Un dosage plus faible d’EPIDUO est disponible (EPIDUO 0,1 %/2,5 % gel) et ce dosage doit être envisagé chez les patients atteint d'acné vulgaire modérée (voir rubrique 5.1).
Lorsque l'ensemble du visage est atteint par de nombreuses papulopustules, un bénéfice clinique plus élevé a été observé chez les patients traités avec EPIDUO 0,3 %/2,5 %, gel par rapport au traitement de référence (EPIDUO 0,1 %/2,5% gel). Le prescripteur peut choisir entre les deux dosages en fonction de l’atteinte et de la gravité clinique du patient.
Populations particulières
Personnes âgées
La sécurité et l'efficacité d'EPIDUO 0,3 %/2,5 %, gel chez les patients âgés de 65 ans et plus n'ont pas été établies.
Personnes souffrant d’insuffisance rénale ou hépatique
EPIDUO 0,3 %/2,5 %, gel n'a pas été étudié chez les patients présentant une insuffisance rénale et hépatique.
Population pédiatrique
La sécurité et l'efficacité d'EPIDUO 0,3 %/2,5 %, gel chez les enfants de moins de 12 ans n'ont pas été étudiées.
Mode d’administration
Voie cutanée uniquement.
Appliquer une fine couche d’EPIDUO 0,3 %/2,5 %, gel sur les zones atteintes du visage et / ou du tronc une fois par jour sur une peau nettoyée. Une quantité de la taille d’un petit pois doit être appliquée sur chaque zone du visage (par exemple le front, le menton, chaque joue), en évitant les yeux et les lèvres (voir rubrique 4.4).
Les patients doivent être informés de se laver les mains après l'application du médicament.
Des cosmétiques peuvent être appliqués une fois que le gel EPIDUO 0,3 %/2,5 %, gel ait séché.
En cas d’irritation, il doit être recommandé au patient d’appliquer un produit hydratant non comédogène, d'utiliser le médicament moins fréquemment (par exemple tous les 2 jours), de suspendre temporairement le traitement ou de l’arrêter définitivement.
· Grossesse (voir rubrique 4.6)
· Femmes planifiant une grossesse (voir rubrique 4.6)
· Hypersensibilité aux substances actives ou à l’un des excipients listés dans la rubrique 6.1.
4.4. Mises en garde spéciales et précautions d'emploi
Le médicament ne doit pas entrer en contact avec les yeux, les lèvres, la bouche, les narines ou les muqueuses. En cas de contact avec les yeux, rincer immédiatement avec de l’eau tiède.
Si une réaction suggérant une sensibilité à l’un des composants apparaît, l’utilisation d’EPIDUO 0,3%/ 2,5%, gel doit être interrompue.
L’exposition excessive au soleil ou aux lampes à ultraviolets doit être évitée.
EPIDUO 0,3 %/2,5 %, gel ne doit pas entrer en contact avec des matières colorées dont les cheveux et les fibres textiles teintées, en raison du risque de blanchiment et de décoloration.
Ce médicament contient 40 mg de propylène glycol (E1520) dans chaque gramme de gel, ce qui équivaut à 4% p/p.
Ce médicament contient du polysorbate 80 (E433) qui peut provoquer des réactions allergiques.
L'efficacité et la sécurité d'EPIDUO 0,3 %/2,5 %, gel chez les patients atteints d’acné nodulaire sévère ou d’acné nodulo-kystique n'ont pas été étudiées. Comme les patients souffrant d'acné nodulaire sévère ou nodulo-kystique sont à risque accru de cicatrices permanentes secondaires aux lésions d'acné, l'utilisation d’EPIDUO 0,3 %/2,5 %, gel chez ces patients n’est pas recommandée en raison du risque de réponse thérapeutique insuffisante.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Aucune étude d’interaction n’a été réalisée avec EPIDUO 0,3 %/2,5 %, gel.
D’après l’expérience précédente avec l’adapalène et le peroxyde de benzoyle, il n’existe pas d’interactions connues avec d’autres médicaments qui pourraient être utilisés par voie cutanée et simultanément avec EPIDUO 0,3 %/2,5 %, gel.
Cependant, d'autres médicaments contenant des rétinoïdes, du peroxyde de benzoyle ou ayant un mode d'action similaire ne doivent pas être utilisés de manière concomitante. L’utilisation de produits cosmétiques desquamant, irritants ou desséchants doit être faite avec précaution, car elle peut entrainer une irritation supplémentaire avec EPIDUO 0,3 %/2,5 %, gel.
L'absorption de l'adapalène à travers la peau humaine est faible (voir rubrique 5.2), et donc l'interaction avec un médicament pris par voie systémique est peu probable.
La pénétration percutanée du peroxyde de benzoyle dans la peau est faible, et la substance active est complètement métabolisée en acide benzoïque qui est rapidement éliminé. Par conséquent, l'interaction potentielle de l'acide benzoïque avec des médicaments systémiques est peu probable.
4.6. Fertilité, grossesse et allaitement
Les rétinoïdes administrés par voie orale sont associés à des anomalies congénitales. Dans le cadre d’une utilisation conforme aux informations de prescription, il est généralement considéré que les rétinoïdes topiques induisent une faible exposition systémique en raison d'une absorption dermique minimale. Cependant, des facteurs individuels (par exemple : lésion cutanée, usage excessif) peuvent contribuer à augmenter l’exposition systémique.
Grossesse
EPIDUO 0,3 %/2,5 %, gel est contre-indiqué (voir rubrique 4.3) chez les femmes enceintes ou planifiant une grossesse.
Il n'existe pas de données ou il existe des données limitées sur l'utilisation de l'adapalène topique chez la femme enceinte.
Les études chez l’animal par voie orale ont montré une toxicité sur la reproduction à des doses systémiques élevées (voir rubrique 5.3).
L’expérience clinique avec l’adapalène et le peroxyde de benzoyle appliqués localement pendant la grossesse est limitée.
En cas d’utilisation chez une patiente enceinte ou si une patiente traitée par ce médicament débute une grossesse, le traitement doit être interrompu.
Aucune étude sur le passage dans le lait chez l’animal ou chez l’Homme n’a été conduite après application cutanée d’EPIDUO 0,3 %/2,5 %, gel.
Les données pharmacocinétiques disponibles chez le rat ont mis en évidence l’excrétion de l'adapalène dans le lait après administration par voie orale ou intraveineuse d'adapalène. Un risque pour les enfants allaités ne peut être exclu. Une décision doit être prise soit d'interrompre l'allaitement soit d'interrompre / de s’abstenir du traitement par EPIDUO 0,3 %/2,5 %, gel en tenant compte du bénéfice de l’allaitement pour l'enfant et de celui du traitement pour la mère.
Afin d’éviter une exposition du bébé, l’application d’EPIDUO 0,3 %/2,5 %, gel sur la poitrine de la mère doit être évitée durant l’allaitement.
Fertilité
Aucune étude de fertilité humaine n’a été menée avec EPIDUO 0,3 %/2,5 %, gel.
Cependant, aucun effet de l'adapalène ou du peroxyde de benzoyle sur la fertilité n’a été trouvé chez les rats dans les études de reproduction (voir rubrique 5.3).
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
EPIDUO 0,3 %/2,5 %, gel n’a aucun effet ou qu’un effet négligeable sur l’aptitude à conduire des véhicules et à utiliser des machines.
Résumé du profil de sécurité
Environ 10% des patients sont susceptibles de présenter des effets cutanés indésirables.
Les effets indésirables liés au traitement habituellement associés à l'utilisation d'EPIDUO 0,3 %/2,5 %, gel sont des réactions légères à modérées au site d’application telles qu’irritation cutanée caractérisée principalement par desquamation, sécheresse, érythème, brûlure/picotements. Il est recommandé d'utiliser un produit hydratant, de réduire temporairement la fréquence d'application quotidienne à un jour sur 2, ou de cesser temporairement l’utilisation jusqu'à ce que l’application quotidienne puisse être reprise.
Ces réactions se produisent généralement au début du traitement, et ont tendance à diminuer graduellement au cours du temps.
Liste des effets indésirables sous forme de tableau
Les effets indésirables sont répertoriés par classe de systèmes d'organes et par fréquence en utilisant la convention suivante : très fréquent (≥ 1/10), fréquent (≥ 1/100, < 1/10), peu fréquent (≥ 1/1 000, < 1/100), rare (≥ 1/10 000, < 1/1 000), très rare (< 1/10 000), fréquence indéterminée (ne peut être estimée sur la base des données disponibles). Ces effets indésirables ont été rapportés avec EPIDUO 0,3 %/2,5 %, gel lors d’une étude clinique de phase 3 contrôlée versus véhicule (voir Tableau 1).
Tableau 1 : Effets indésirables
|
Système Organe Classe |
Fréquence |
Effets indésirables |
|
Affection oculaire |
Peu fréquent |
Erythème palpébral |
|
Fréquence indéterminée* |
Œdème palpébral |
|
|
Affections du système immunitaire |
Fréquence indéterminée * (Ne peut être estimée sur la base des données disponibles) |
Réaction anaphylactique |
|
Affections du système nerveux |
Peu fréquent |
Paresthésie (picotements au site d’application) |
|
Affections respiratoires, thoraciques et médiastinales |
Fréquence indéterminée* |
Sensation de gorge serrée, dyspnée |
|
Affections de la peau et du tissu sous-cutané |
Fréquent |
Dermatite atopique, eczéma, sensation de brûlure de la peau, irritation cutanée, érythème, exfoliation de la peau (desquamation) |
|
Peu fréquent |
Sécheresse cutanée, prurit, rash |
|
|
Fréquence indéterminée* |
Dermite de contact allergique, gonflement du visage, douleur de la peau (sensation de picotement), vésicules cutanées, décoloration de la peau (hyperpigmentation et hypopigmentation), urticaire, brûlure au site d’application ** |
*Données de surveillance recueillies après la mise sur le marché d’EPIDUO 0,1% / 2,5%, gel à partir d’une population de taille inconnue.
** La plupart des cas de « brûlure au site d’application » étaient des brûlures superficielles, mais des cas de brûlures au deuxième degré ou de brûlures sévères ont été rapportés.
Les effets indésirables cutanés étaient plus fréquents avec EPIDUO 0,3 %/2,5 %, gel qu’avec EPIDUO 0,1% / 2,5%, gel par rapport au véhicule. Dans l'étude pivot (voir rubrique 5.1), 9,2% des patients dans la population combinée traitée avec EPIDUO 0,3 %/2,5 %, gel avaient des effets indésirables cutanés liés au traitement et 3,7% dans la population traitée avec EPIDUO 0,1% / 2,5% gel par rapport au groupe véhicule (2,9 %).
En plus de ceux cités ci-dessus, d’autres effets indésirables ont été rapportés avec EPIDUO 0,1% / 2,5%, gel, l’association fixe précédemment approuvée d'adapalène et de peroxyde de benzoyle:
· Essais cliniques :
D'autres effets indésirables rapportés lors des essais cliniques avec EPIDUO 0,1% / 2,5%, gel sont la dermite irritante de contact (fréquent) et brûlure à type coup de soleil (peu fréquent).
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.signalement.social-sante.gouv.fr.
En cas d’ingestion accidentelle, les mesures symptomatiques appropriées doivent être prises.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : préparations anti-acnéiques à usage topique, code ATC : D10AD53.
Mécanisme d’action et Effets pharmacodynamiques
EPIDUO 0,3 %/2,5 %, gel associe deux substances actives, dont les mécanismes d’action sont différents mais complémentaires.
· Adapalène : l’adapalène est un dérivé de l’acide naphtoïque, chimiquement stable, d’activité type rétinoïde. Les études de son profil biochimique et pharmacologique ont démontré que l’adapalène a une action sur la pathologie de l’acné vulgaire : c’est un modulateur puissant de la différenciation cellulaire et de la kératinisation, et il a des propriétés anti-inflammatoires. Sur le plan du mécanisme d’action, l’adapalène se lie aux récepteurs nucléaires spécifiques de l’acide rétinoïde. Les preuves actuelles suggèrent que l’adapalène topique normalise la différenciation des cellules épithéliales folliculaires, entrainant une diminution de la formation de microcomédons. L’adapalène inhibe les réponses chimiotactiques (ciblées) et chimiocinétiques (non spécifiques) des leucocytes polymorphonucléaires humains, au cours de tests in vitro ; il inhibe aussi le métabolisme de l’acide arachidonique en médiateurs inflammatoires. Les études in vitro ont montré une inhibition des facteurs AP-1 et une inhibition de l’expression des récepteurs Toll-like 2. Ce profil suggère que la composante inflammatoire cellulaire dans l’acné est réduite par adapalène.
· Peroxyde de benzoyle : le peroxyde de benzoyle a montré une activité antimicrobienne, en particulier contre Cutibacterium acnes, qui est anormalement présent dans le follicule pilo-sébacé acnéique. Sur le plan du mécanisme d'action, le peroxyde de benzoyle a une activité fortement lipophile lui permettant de pénétrer à travers l'épiderme dans les membranes de cellules bactériennes et des kératinocytes du follicule pilo-sébacée. Le peroxyde de benzoyle est reconnu pour être un agent antibactérien à large spectre très efficace dans le traitement de l'acné vulgaire. Il a été démontré qu’il exerçait un effet bactéricide en générant des radicaux libres qui oxydent les protéines et les autres constituants cellulaires essentiels dans la paroi de la bactérie. La concentration minimale inhibitrice du peroxyde de benzoyle est bactéricide et a démontré son efficacité sur des souches de C. acnes sensibles et résistantes aux antibiotiques. En outre, le peroxyde de benzoyle a démontré des activités exfoliative et kératolytique.
Efficacité et sécurité clinique
La sécurité et l'efficacité d’EPIDUO 0,3 %/2,5 %, gel appliqué une fois par jour dans le traitement de l'acné vulgaire ont été évaluées pendant 12 semaines, dans une étude clinique contrôlée, multicentrique, randomisée, en double aveugle comparant EPIDUO 0,3 %/2,5 %, gel au véhicule chez 503 patients atteints d'acné. Dans cette étude, 217 patients ont été traités avec EPIDUO 0,3 %/2,5 %, gel, 217 patients avec adapalène 0,1% / peroxyde de benzoyle 2,5% gel et 69 patients avec le véhicule.
Les critères d’efficacité étaient :
· Le taux de succès, défini comme le pourcentage de patients évalués comme « guéri » ou « presque guéri » à la 12ème semaine avec une amélioration d’au moins 2 grades sur l’échelle IGA (Investigator Global Assessment/Evaluation Globale par l’Investigateur). Un grade IGA « guéri » correspond à une peau guérie sans lésion inflammatoire ou non-inflammatoire. Un grade IGA « presque guéri » correspond à quelques comédons dispersés et quelques petites papules.
· La différence absolue moyenne du nombre de lésions inflammatoires et non-inflammatoires à la 12ème semaine par rapport à l’inclusion.
A l’inclusion, 50 % des patients avaient une sévérité d’acné évaluée comme « modérée » (IGA=3) et 50 % «sévère» (IGA=4). Dans la population globale de l'étude, un maximum de deux nodules était autorisé. Concernant le nombre de lésions, les patients avaient une moyenne de 98 lésions au totale (intervalle : 51-226), dont le nombre moyen de lésions inflammatoires était de 38 (intervalle: 20-99) et le nombre moyen de lésions non-inflammatoires était de 60 (intervalle: 30-149). L'âge des patients variait de 12 à 57 ans (âge moyen : 19,6 ans), avec 273 (54,3 %) des patients âgés de 12 à 17 ans. Un nombre similaire d'hommes (47,7 %) et les femmes (52,3 %) étaient inclus.
Dans cette étude pivot, 55,2 % des patients évalués « sévère » avaient de l'acné sur le tronc. Les patients ont traité une fois par jour le soir le visage et les autres zones atteintes d'acné sur le tronc.
· Les analyses statistiques ont été réalisées pour comparer et interpréter les résultats de l'étude en deux étapes EPIDUO 0,3 %/2,5 %, gel vs véhicule dans la population globale de patients atteints d'acné modérée et sévère (IGA = 3 et IGA = 4).
· EPIDUO 0,3 %/2,5 %, gel vs véhicule dans le sous-groupe de patients atteints d'acné sévère (IGA = 4).
Les résultats d'efficacité sont présentés dans le tableau 2 pour les populations combinées d'acné modérée et sévère.
Tableau 2 : Efficacité clinique à la semaine 12 dans la population globale : patients atteints d’acné vulgaire modérée et sévère (IGA combiné = 3 et 4, IM, population ITT)
|
Paramètres d’efficacité |
EPIDUO 0,3 %/2,5 %, gel (N = 217) |
Adapalène 0,1% / peroxyde de benzoyle 2,5%, gel (N = 217)a |
Véhicule du gel (N = 69) |
|
Taux de succès (Amélioration minimum de 2 grades et IGA «guéri» ou «presque guéri») |
33,7%b |
27,3% |
11,0 % |
|
Différence de lésions inflammatoires, Réduction absolue moyenne (pourcentage) |
27,8b (68,7 %) |
26,5 (69,3%) |
13,2 (39,2 %) |
|
Différence de lésions non-inflammatoires, Réduction absolue moyenne (pourcentage) |
40,5b (68,3 %) |
40,0 (68,0%) |
19,7 (37,4 %) |
IM = Imputation multiple; ITT = intention de traiter
a) Cette étude n’était pas conçue ou pas assez puissante pour comparer formellement l'efficacité d’EPIDUO 0,3 %/2,5 %, gel au plus faible dosage d’Adapalène 0,1 % / peroxyde de benzoyle 2,5%, ni pour comparer le plus faible dosage d’Adapalène 0,1 % / peroxyde de benzoyle 2,5% au véhicule.
b) p < 0,001 vs véhicule
Les résultats des critères principaux d’efficacité dans la population d'acné sévère sont présentés dans le Tableau 3.
Tableau 3: Efficacité clinique chez les patients atteints d'acné vulgaire sévère (IGA = 4, IM, population ITT)
|
Paramètres d’efficacité |
EPIDUO 0,3 %/2,5 %, gel (N = 106) |
Adapalène 0,1% / peroxyde de benzoyle 2,5% Gel (N = 112) |
Véhicule du gel (N = 34) |
|
Taux de succès (Amélioration minimum de 2 grades et IGA «guéri» ou «presque guéri») |
31,9 %a |
20,5% |
11,8 % |
|
Différence de lésions inflammatoires, Réduction absolue moyenne (pourcentage) |
37,3b (74,4 %) |
30,2 (68%) |
14,3 (33,0 %) |
|
Différence de lésions non-inflammatoires, Réduction absolue moyenne (pourcentage) |
46,3b (72,1 %) |
43,9 (68,4%) |
17,8 (30,8 %) |
IM = Imputation multiple; ITT = intention de traiter
a) p = 0,029 vs véhicule
b) p <0,001 vs véhicule
Le gel adapalène 0,1% / peroxyde de benzoyle 2,5 % était inclus dans cet essai comme traitement de référence. Chez les patients évalués comme «modéré» (IGA=3), EPIDUO 0,3 %/2,5 %, gel n’a pas montré d’avantage en termes d’efficacité vs le traitement de référence. Dans l’analyse des patients évalués comme « sévère » (IGA=4), EPIDUO 0,3 %/2,5 %, gel a eu une plus grande efficacité versus véhicule avec une différence de traitement de 20,1 % (31,9% vs 11,8% ; IC à 95% : [6,0%, 34,2%)], p = 0,029), contrairement au traitement de référence (différence de traitement vs véhicule de 8,8 %).
L'efficacité d’EPIDUO 0,3 % / 2,5 %, gel sur les cicatrices d'acné a été étudié dans l'étude OSCAR. Il s'agissait d'une étude contrôlée versus véhicule, multicentrique, randomisée, investigateur aveugle, basée sur une comparaison intra-individuelle (la moitié droite du visage versus la moitié gauche du visage), chez des sujets masculins et féminins âgés de 16 à 35 ans (n=67) souffrant d'acné vulgaire faciale modérée à sévère, avec un nombre moyen de 40 lésions d'acné (18 lésions inflammatoires, 22 lésions non inflammatoires) sur chaque moitié de visage. La grande majorité des sujets présentaient une acné de sévérité globale évaluée comme modérée (93 %). Les 2 hémifaces étaient bien équilibrées en ce qui concerne les lésions d’acné, la sévérité des cicatrices d’acné était de 12 cicatrices de chaque côté avec une majorité de cicatrices de 2 à 4 mm.
La majorité des patients (63%) présentaient des cicatrices de sévérité globalement légère et environ 30 % présentaient des cicatrices de sévérité modérée.
Des sujets masculins ou féminins, âgés de 16 à 35 ans, et présentant un phototype de peau de type I à IV sur l'échelle de Fitzpatrick ont été inclus dans cette étude.
La population recrutée était majoritairement féminine (65,7 %), et la plupart des sujets ont été classés comme étant principalement caucasien (86,6 %) et le reste de la population était asiatique (13,4 %), l'ethnicité n'a pas été prise en compte. Les phototypes de peau les plus fréquents étaient les types II (47,8%) et III (34,3%) et le reste présentait un phototype IV (13,4%) et I (4,5%).
Tous les sujets éligibles ont été randomisés pour recevoir EPIDUO 0,3 % / 2,5 % sur une moitié du visage et le véhicule sur l'autre moitié du visage, une fois par jour, le soir, pendant 24 semaines. Le critère principal d'efficacité était le nombre de cicatrices atrophiques d'acné par hémiface à la 24ème semaine.
L'analyse du critère principal a montré que la thérapie médicamenteuse réduisait le nombre total de cicatrices d'acné (voir tableau 4).
Tableau 4 : Nombre total de cicatrices d’acné (ITT/LOCF)
|
Nombre total de cicatrices d’acné ITT/LOCF) |
EPIDUO 0,3 %/2,5 %, gel |
Véhicule |
Différence de traitement |
Résultat statistique |
|
Moyenne ± ET Médiane (Q1, Q3) (Min, Max) |
9,5 ± 5,5 8,0 (6,0 ; 12,0) (0 ; 27) |
13,3 ± 7,4 13,0 (8,0 ; 19,0) (0 ; 36) |
-3,7 ± 4,4 -3,0 (-7,0 ; 0,0) (-16 ; 3) |
p<0,0001 |
ITT = intention de traiter ; LOCF = dernières observations rapportées ; ET = écart type
EPIDUO 0,3 %/2,5 %, gel a principalement réduit les cicatrices de 2 à 4 mm (moyenne avec EPIDUO 0,3 %/2,5%, gel de 9,0 ± 5,4 ; moyenne avec le véhicule de 12,1 ± 7,0 ; différence moyenne de traitement vs véhicule de -3,1 ± 4,1), tandis que la réduction des cicatrices de > 4 mm était plus faible (moyenne avec EPIDUO 0,3 % / 2,5 % gel de 0,6 ± 0,8 ; moyenne avec le véhicule de 1,2 ± 1,9 ; différence de traitement moyenne vs véhicule de -0,6 ± 1,5)
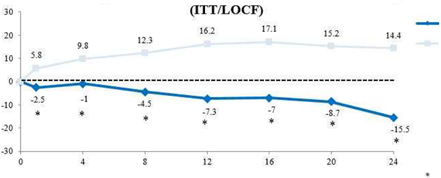
La figure 1 montre l'évolution en pourcentage du nombre total de cicatrices atrophiques par visite pour chaque moitié de visage ayant reçu respectivement Epiduo 0,3 % / 2,5 % gel et le véhicule.
Figure 1 :
![]()
![]()

![]()
![]()
* valeur-p nominale non ajustée pour les tests multiples
5.2. Propriétés pharmacocinétiques
Une étude pharmacocinétique a été conduite avec EPIDUO 0,3 %/2,5 %, gel chez 26 sujets adultes et adolescents (12 à 33 ans) atteints d’acné vulgaire sévère. Pendant 4 semaines, les sujets étaient traités par 1 application quotidienne d’EPIDUO 0,3 %/2,5 %, gel en couche mince sur toutes les zones potentiellement atteintes (visage, épaules, poitrine et haut du dos) soit, en moyenne, 2,3 grammes / jour (intervalle : 1,6 -3,1 grammes / jour). Après 4 semaines de traitement, 16 sujets (62 %) présentaient des concentrations plasmatiques d’adapalène quantifiables supérieures à la limite de quantification (LoQ de 0,1 ng / ml), avec une Cmax moyenne de 0,16 ± 0,08 ng / ml et une ASC0-24h moyenne de 2,49 ± 1,21 ng.h / ml. Le sujet le plus exposé avait une Cmax et une ASC0-24h d’adapalène de 0,35 ng / ml et 6,41 ng.h / ml, respectivement
Les études pharmacocinétiques effectuées avec EPIDUO 0,1% / 2,5%, gel et EPIDUO 0,3 %/2,5 %, gel ont mis en évidence que l'absorption transdermique de l'adapalène n'est pas affectée par le peroxyde de benzoyle.
La pénétration percutanée du peroxyde de benzoyle est faible. Lors d’une application cutanée, le peroxyde de benzoyle est complètement transformé en acide benzoïque qui est rapidement éliminé.
5.3. Données de sécurité préclinique
Des études de toxicologie sur la reproduction ont été conduites avec l’adapalène par voie orale et cutanée chez le rat et le lapin. Un effet tératogène a été démontré à des doses systémiques élevées (doses orales de 25 mg/kg/jour). A des expositions inférieures (dose cutanée de 6 mg/kg/jour), il a été observé une modification du nombre de côtes ou de vertèbres.
Des études chez l’animal conduites avec EPIDUO 0,1% / 2,5%, gel ou EPIDUO 0,3 %/2,5 %, gel comprenant des études de tolérance locale et des études de toxicologie en administrations cutanées répétées chez le rat, le chien et/ou le mini-porc jusqu’à 13 semaines, ont démontré une irritation locale et un potentiel sensibilisant, attendues pour une association contenant du peroxyde de benzoyle. L’exposition systémique à l’adapalène à la suite d’applications cutanées répétées de l’association fixe chez l’animal est très faible, ceci étant cohérent avec les données de pharmacocinétique clinique. Le peroxyde de benzoyle est rapidement et complètement transformé en acide benzoïque dans la peau, et après absorption est éliminé dans les urines, avec une exposition systémique limitée.
La toxicité de l'adapalène sur la reproduction a été testée par voie orale chez le rat pour la fertilité.
Il n'y a eu aucun effet indésirable sur les performances de reproduction et sur la fertilité, sur la survie de la portée F1, la croissance et le développement jusqu'au sevrage et sur les performances de reproduction ultérieures après un traitement avec l'adapalène par voie orale à des doses allant jusqu'à 20 mg/kg/jour.
Une étude de toxicité sur la reproduction et le développement a été conduite chez des rats exposés à des doses orales de peroxyde de benzoyle allant jusqu'à 1 000 mg/kg/jour (5 mL / kg). Cette étude a montré que le peroxyde de benzoyle n'induit ni tératogénicité ni effet sur la fonction reproductrice à des doses allant jusqu'à 500 mg/kg/jour.
Évaluation du risque environnemental :
Les études d'évaluation du risque environnemental ont montré que l'adapalène peut être très persistant et toxique pour l'environnement (voir rubrique 6.6).
Les études d'évaluation du risque environnemental ont montré que l'adapalène peut présenter un risque pour le milieu aquatique.
Edétate disodique, docusate sodique, glycérol, poloxamère, propylèneglycol (E1520), SIMULGEL 600PHA (copolymère d'acrylamide et d'acryloyldiméthyltaurate de sodium, isohexadécane, polysorbate 80 (E433), oléate de sorbitan), eau purifiée.
Après première ouverture pour la pompe : 6 mois.
Après première ouverture pour le tube : 7 jours.
6.4. Précautions particulières de conservation
A conserver à une température ne dépassant pas 25°C.
6.5. Nature et contenu de l'emballage extérieur
EPIDUO 0,3 %/2,5 %, gel existe sous 2 types de présentation :
Tube :
· 2 g et 5 g en tube de plastique avec une structure interne en polyéthylène haute densité, à tête en polyéthylène haute densité, fermé par un bouchon à vis en polypropylène.
Récipient multidose (pompe) avec système de fermeture sans entrée d'air :
· 15 g, 30 g, 45 g et 60 g en récipient multi-dose avec système de fermeture sans entrée d'air et capuchon protecteur ; en polypropylène et polyéthylène haute densité ou en polypropylène, polyéthylène haute densité et polyéthylène très basse densité.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Ce médicament peut présenter un risque pour l'environnement (voir rubrique 5.3).
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
TOUR EUROPLAZA
20, AVENUE ANDRE PROTHIN
LA DEFENSE 4
92927 LA DEFENSE CEDEX
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 300 811 0 5 : 2 g en tube (plastique blanc). Boîte de 1.
· 34009 300 811 1 2 : 5 g en tube (plastique blanc). Boîte de 1.
· 34009 300 811 2 9 : 15 g en récipient multidose avec système de fermeture sans entrée d'air muni d'un capuchon protecteur. Boîte de 1.
· 34009 300 811 3 6 : 30 g en récipient multidose avec système de fermeture sans entrée d'air muni d'un capuchon protecteur. Boîte de 1.
· 34009 300 811 5 0 : 45 g en récipient multidose avec système de fermeture sans entrée d'air muni d'un capuchon protecteur. Boîte de 1.
· 34009 300 811 6 7 : 60 g en récipient multidose avec système de fermeture sans entrée d'air muni d'un capuchon protecteur. Boîte de 1.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I.
ANSM - Mis à jour le : 29/09/2025
Adapalène/Peroxyde de benzoyle
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que EPIDUO 0,3 %/2,5 %, gel et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser EPIDUO 0,3 %/2,5 %, gel ?
3. Comment utiliser EPIDUO 0,3 %/2,5 %, gel ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver EPIDUO 0,3 %/2,5 %, gel ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE EPIDUO 0,3 %/2,5 %, gel ET DANS QUELS CAS EST-IL UTILISE ?
EPIDUO 0,3 %/2,5 %, gel appartient à un groupe de médicaments appelés « préparation anti-acnéique pour usage topique ». Il est utilisé pour le traitement de l'acné vulgaire, en présence de comédons (points noirs ou blancs), de nombreuses papules et pustules (boutons inflammatoires).
Ce gel est une association de 2 principes actifs, l’adapalène et le peroxyde de benzoyle qui agissent ensemble mais avec des mécanismes d’action différents :
· L’adapalène appartient à un groupe de produits appelés « rétinoïdes » et agit spécifiquement sur le mécanisme de l’acné ;
· Le peroxyde de benzoyle, agit comme un anti-microbien et a une action assouplissante et exfoliante de la couche supérieure cutanée.
EPIDUO 0,3 %/2,5 %, gel ne doit être utilisé que chez les adultes et les adolescents âgés de 12 ans et plus.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER EPIDUO 0,3 %/2,5 %, gel ?
N’utilisez jamais EPIDUO 0,3 %/2,5 %, gel :
· Si vous êtes enceinte
· Si vous planifiez une grossesse
· Si vous êtes allergique (hypersensible) à l’adapalène ou au peroxyde de benzoyle ou à l’un des autres composants contenus dans ce médicament (mentionnés dans la rubrique 6).
Avertissements et précautions
Adressez-vous à votre médecin ou pharmacien avant d’utiliser EPIDUO 0,3 %/2,5 %, gel.
· Ne pas appliquer EPIDUO 0,3 %/2,5 %, gel sur les zones ou vous avez des coupures, des éraflures, un coup de soleil ou de l’eczéma.
· Assurer vous qu’EPIDUO 0,3 %/2,5 %, gel n’entre pas en contact avec vos yeux, votre bouche, vos narines ou vos muqueuses ou tout autre zone très sensible du corps. En cas de contact accidentel, rincer immédiatement et abondamment à l’eau tiède.
· Eviter une exposition excessive au soleil et aux lampes à ultraviolets.
· Eviter l’application d’EPIDUO 0,3 %/2,5 %, gel sur les cheveux et sur les fibres textiles teintées en raison du risque de décoloration. Se laver les mains soigneusement après avoir appliqué le produit.
Adressez-vous à votre médecin, si vous ressentez une irritation persistante de la peau au début de votre traitement par EPIDUO 0,3 %/2,5 %, gel (voir rubrique « 3. Comment utiliser EPIDUO 0,3 %/ 2,5 %, gel ? »).
Enfants Sans objet.Autres médicaments et EPIDUO 0,3 %/2,5 %, gel
· Ne pas appliquer d’autres produits contre l’acné (contenant du peroxyde de benzoyle et/ou des rétinoïdes) en même temps qu’EPIDUO 0,3 %/2,5 %, gel.
· Eviter l’utilisation concomitante de produits cosmétiques qui irritent, dessèchent ou exfolient la peau.
Informez votre médecin ou pharmacien si vous utilisez, avez récemment utilisé ou pourriez utiliser tout autre médicament.
EPIDUO 0,3 %/2,5 %, gel avec des aliments
Sans objet.
Grossesse
N’utilisez PAS EPIDUO 0,3 %/2,5 %, GEL si vous êtes enceinte ou envisagez une grossesse. Votre médecin pourra vous fournir plus d’informations.
Si vous découvrez que vous êtes enceinte pendant le traitement avec EPIDUO 0,3 %/2,5 %, gel, le traitement devrait être interrompu et vous devez informer votre médecin aussi vite que possible pour un suivi adapté.
Allaitement
Si vous allaitez demandez conseil à votre médecin avant de prendre ce médicament. Votre médecin vous conseillera soit d'interrompre l'allaitement soit d’arrêter le traitement par EPIDUO 0,3%/ 2,5%, gel.
Si votre médecin vous conseille de poursuivre le traitement, l’application du gel sur la poitrine doit être évitée afin d’éviter un contact accidentel avec l’enfant.
Conduite de véhicules et utilisation de machines
EPIDUO 0,3 %/2,5 %, gel n’a aucun effet ou qu’un effet négligeable sur l’aptitude à conduire des véhicules et à utiliser des machines.
EPIDUO 0,3 %/2,5 %, gel contient du propylène glycol.
Ce médicament contient 40 mg de propylèneglycol (E1520) dans chaque gramme de gel, ce qui équivaut à 4% p/p.
EPIDUO 0,3%/2,5 %, gel contient des polysorbates.
Les polysorbates peuvent provoquer des réactions allergiques.
3. COMMENT UTILISER EPIDUO 0,3 %/2,5 %, gel ?
EPIDUO 0,3 %/2,5 %, gel est réservé aux adultes et adolescents âgés de 12 ans et plus.
EPIDUO 0,3 %/2,5 %, gel est un gel, pour une utilisation sur la peau.
Le médecin décidera du dosage du gel d’EPIDUO dont vous avez besoin, en fonction de la sévérité et de l'aspect de votre acné. Le médecin devra également décider si vous avez besoin d'un traitement complémentaire.
· La peau doit être nettoyée et séchée avant l’application.
· Appliquez une fine couche de gel de façon homogène sur l’ensemble des zones affectées par l’acné du visage et/ou du tronc, une fois par jour avant le coucher. Eviter le contact avec les yeux, les lèvres, les narines et les muqueuses.
· Si vous l’appliquez sur le visage : lavez et séchez-vous le visage, puis appliquer une quantité de la taille d’un petit pois pour couvrir chaque partie du visage (front, menton, chaque joue).
· Lavez-vous les mains soigneusement après avoir appliqué EPIDUO 0,3 %/2,5 %, gel.
Votre médecin vous indiquera combien de temps vous devez appliquer EPIDUO 0,3 %/2,5 %, gel. En cas d'absence d'amélioration après 4 à 8 semaines, consultez votre médecin afin d’évaluer le bénéfice de la poursuite du traitement.
Si vous ressentez une irritation persistante de la peau durant les premières semaines d’utilisation d’EPIDUO 0,3 %/2,5 %, gel, contacter votre médecin. Celui-ci pourra vous demander d’appliquer un produit hydratant, de diminuer la fréquence des applications, d’arrêter le traitement pendant une courte période, ou d’arrêter l’utilisation du gel définitivement.
N’appliquez pas de produits cosmétiques (tels que d’autres crèmes pour le visage ou du maquillage) avant l'application quotidienne d’EPIDUO 0,3 %/2,5 %, gel. Ces produits peuvent être utilisés après qu’EPIDUO 0,3 %/2,5 %, gel ait séché.
Utilisation chez les enfants
EPIDUO 0,3 %/2,5 %, gel ne doit pas être utilisé chez les enfants de moins de 12 ans.
Si vous avez utilisé plus d’EPIDUO 0,3 %/2,5 %, gel que vous n’auriez dû :
Si vous appliquez plus d’EPIDUO 0,3 %/2,5 %, gel que vous ne devez sur votre peau, votre acné ne disparaitra pas plus rapidement, mais cela pourrait provoquer irritation et rougeur cutanées.
Contacter votre médecin ou les services d’urgence :
· Si vous avez utilisé plus d’EPIDUO 0,3 %/2,5 %, gel que vous n’auriez dû,
· Si un enfant a pris accidentellement ce médicament,
· Si vous ou quelqu’un d’autre avez avalé accidentellement ce médicament.
Votre médecin vous conseillera sur les mesures à prendre.
Si vous oubliez d’utiliser EPIDUO 0,3 %/2,5 %, gel :
Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre.
Si vous arrêtez d’utiliser EPIDUO 0,3 %/2,5 %, gel :
Les boutons (comédons, papules et pustules) seront réduits seulement après plusieurs applications de ce médicament. Continuer EPIDUO 0,3 %/2,5 %, gel aussi longtemps que votre médecin l’aura prescrit.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Environ 1 personne sur 10 utilisant EPIDUO 0,3 %/2,5 %, gel peut présenter des réactions cutanées indésirables.
Cessez d'utiliser le produit et consultez immédiatement un médecin si vous avez une sensation de gorge ou un gonflement des yeux, du visage, des lèvres ou de la langue, si vous vous sentez faible ou si vous avez des difficultés à respirer. Cessez d’utiliser le produit si vous développez de l’urticaire ou des démangeaisons du visage ou du corps. La fréquence avec laquelle ces effets secondaires se produisent n’est pas connue.
Fréquents (touchant moins de 1 personne sur 10)
· Irritation de la peau
· Eczéma
· Sensation de brûlure cutanée
· Rougeur de la peau
· Desquamation
Peu fréquents (touchant moins de 1 personne sur 100)
· Rougeur de la paupière
· Picotements ou sensation d’épingles et d’aiguilles au site d’application
· Démangeaison de la peau, réaction cutanée allergique
· Eruption
· Peau sèche
En plus des effets indésirables décrits ci-dessus, les effets indésirables suivants ont été rapportés avec un plus faible dosage d’EPIDUO (adapalène 0,1 % de peroxyde / benzoyle 2,5%) :
· Peu fréquent (touchant moins de 1 personne sur 100) : Brûlure de type de coup de soleil
Fréquence d’apparition non connue (ne peut être déterminée avec les données disponibles) :
· Gonflement de la paupière
· Sensation de gorge serrée
· Réactions allergiques de contact
· Gonflement du visage
· Douleur de la peau (sensation de picotement)
· Vésicules cutanées
· Difficultés à respirer
· Décoloration de la peau (modification de la couleur de la peau)
· Brûlure au site d’application.
Les effets indésirables habituellement associés à l'utilisation d'EPIDUO incluent des réactions légères à modérées au site d'application, tels qu'irritation de la peau avec rougeur, sécheresse, desquamation, picotement et/ou brûlure de la peau.
Des brûlures au site d’application étaient principalement des cas superficiels, mais des cas plus sévères impliquant des cloques ont aussi été rapportés.
Si vous ressentez une irritation persistante de la peau pendant les premières semaines d’utilisation d’EPIDUO 0,3 %/2,5 %, gel, consultez avec votre médecin. Les effets indésirables cutanées, comme irritation de la peau, sont plus fréquents avec EPIDUO 0,3 %/2,5 %, gel qu’avec le dosage inférieur EPIDUO 0,1 % / 2,5% gel. Vous pouvez être conseillé d’appliquer un produit hydratant, d'utiliser le gel moins souvent, d'arrêter pour une courte période, ou de cesser d'utiliser le gel. Ces réactions se produisent généralement au début du traitement, et ont tendance à diminuer progressivement au cours du temps.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: www.signalement.social-sante.gouv.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER EPIDUO 0,3 %/2,5 %, gel ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’emballage et le tube / flacon après EXP. La date de péremption fait référence au dernier jour de ce mois.
A conserver à une température ne dépassant pas 25°C.
Durée de conservation après première ouverture pour le tube : 7 jours.
Durée de conservation après première ouverture pour la pompe : 6 mois.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient EPIDUO 0,3 %/2,5 %, gel
· Les substances actives sont l’adapalène et le peroxyde de benzoyle.
1 gramme de gel contient 3 mg (0.3 % p/p) d’adapalène et 25 mg de peroxyde de benzoyle hydraté, équivalent à 25 mg (2.5% p/p) de peroxyde de benzoyle anhydre.
· Les autres ingrédients sont :
Edétate disodique, docusate sodique, glycérol, poloxamère, propylèneglycol (E1520), SIMULGEL 600 PHA (copolymère d'acrylamide et d'acryloyldiméthyl taurate de sodium, isohexadécane, polysorbate 80 (E433), oléate de sorbitan), eau purifiée. Voir en fin de la rubrique 2 pour plus d’information.
Qu’est-ce que EPIDUO 0,3 %/2,5 %, gel et contenu de l’emballage extérieur
· Un tube plastique contenant 2 g ou 5 g de gel ;
· Un flacon-pompe contenant 15 g, 30 g, 45 g ou 60 g.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
TOUR EUROPLAZA
20, AVENUE ANDRE PROTHIN
LA DEFENSE 4
92927 LA DEFENSE CEDEX
Exploitant de l’autorisation de mise sur le marché
GALDERMA INTERNATIONAL
TOUR EUROPLAZA
20, AVENUE ANDRE PROTHIN
LA DEFENSE 4
92927 LA DEFENSE CEDEX
Z.I. MONTDESIR
74540 ALBY SUR CHERAN
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
< {MM/AAAA}>< {mois AAAA}.>
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).