Dernière mise à jour le 30/03/2026
BELARA 0,03 mg/2 mg, comprimé pelliculé
Indications thérapeutiques
Classe pharmacothérapeutique - code ATC : G03AA15
BELARA est un CONTRACEPTIF HORMONAL ORAL. Lorsque les contraceptifs hormonaux contiennent 2 hormones comme dans BELARA, ils sont appelés Contraceptif Hormonal Combiné (CHC). Les 21 comprimés de la plaquette contiennent les mêmes quantités d'hormones, c'est pourquoi BELARA est une contraception monophasique.
Les contraceptifs hormonaux comme BELARA ne vous protègent pas du Sida ou des autres affections sexuellement transmissibles. Seuls les préservatifs vous en protègent.
Présentations
> 1 plaquette(s) thermoformée(s) PVC PVDC aluminium de 21 comprimé(s)
Code CIP : 369 500-8 ou 34009 369 500 8 5
Déclaration d'arrêt de commercialisation : 15/12/2024
Cette présentation n'est pas agréée aux collectivités
> 3 plaquette(s) thermoformée(s) PVC PVDC aluminium de 21 comprimé(s)
Code CIP : 369 501-4 ou 34009 369 501 4 6
Déclaration de commercialisation : 05/12/2005
Cette présentation n'est pas agréée aux collectivités
Documents de bon usage du médicament
- Contraception chez la femme en post-partum
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Contraception d’urgence
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Contraception chez l’homme
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Stérilisation à visée contraceptive chez l’homme et chez la femme
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Contraception chez la femme adulte et de l'adolescente en âge de procréer (hors post-partum et post-IVG)
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Contraception chez la femme à risque cardio-vasculaire
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Contraception : prescriptions et conseils aux femmes
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Contraception hormonale orale : dispensation en officine
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Contraception d’urgence : dispensation en officine
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Contraception estroprogestative transdermique ou vaginale : dispensation en officine
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Contraception chez la femme après une interruption volontaire de grossesse (IVG)
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Septembre 2019
- Méthodes contraceptives : Focus sur les méthodes les plus efficaces disponibles
Auteur : Haute autorité de santé
Type : Evaluation des technologies de santé
Date de mise à jour :Novembre 2017
- Contraceptifs oraux estroprogestatifs : préférez les «pilules» de 1re ou 2e génération
Auteur : Haute autorité de santé
Type : Fiche Bon Usage du Médicament
Date de mise à jour :Janvier 2013
Service médical rendu (SMR)
Pas de SMR disponible pour ce médicament ( plus d'informations dans l'aide )
Amélioration du service médical rendu (ASMR)
Pas d'ASMR disponible pour ce médicament (plus d'informations dans l'aide )
ANSM - Mis à jour le : 24/07/2024
BELARA 0,03 mg/2 mg, comprimé pelliculé
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Acétate de chlormadinone ................................................................................................ 2,000 mg
Ethinylestradiol ................................................................................................................ 0,030 mg
Pour un comprimé pelliculé.
Excipient à effet notoire : lactose monohydraté 69,5 mg.
Pour la liste complète des excipients, voir rubrique 6.1.
Comprimé pelliculé rond, de couleur rose clair.
4.1. Indications thérapeutiques
Contraception hormonale orale.
La décision de prescrire BELARA doit être prise en tenant compte des facteurs de risque de la patiente, notamment ses facteurs de risque de thrombo-embolie veineuse (TEV), ainsi que du risque de TEV associé à BELARA en comparaison aux autres Contraceptifs Hormonaux Combinés (CHC) (voir rubriques 4.3 et 4.4).
4.2. Posologie et mode d'administration
Un comprimé doit être pris chaque jour à peu près au même moment, (de préférence le soir) pendant 21 jours consécutifs, suivi d'un arrêt de 7 jours entre chaque plaquette. Les règles apparaissent dans les 2 à 4 jours suivant la prise du dernier comprimé. Après l'arrêt de 7 jours, le traitement est poursuivi en entamant la plaquette suivante de BELARA, que les règles soient ou non terminées.
Mode d'administration
Les comprimés doivent être sortis du blister en face du jour de la semaine indiqué sur la plaquette correspondant à la prise et doivent être avalés, éventuellement avec un peu d'eau. Les comprimés sont pris quotidiennement en suivant le sens des flèches.
Modalités d'instauration du traitement :
Absence de contraception hormonale antérieure (au cours du mois précédent) :
La prise du premier comprimé doit commencer le premier jour du cycle naturel de la femme, c'est à dire le premier jour des règles. Si le comprimé est bien pris le premier jour des règles, l'efficacité contraceptive commence dès le premier jour de prise et est maintenue pendant l'arrêt de 7 jours.
La prise du premier comprimé peut également commencer entre le 2ème et le 5ème jour des règles, que les règles aient cessé ou non. Dans ce cas, une méthode contraceptive mécanique complémentaire est nécessaire pendant les 7 premiers jours.
Au-delà du 5ème jour du cycle, la femme doit attendre les prochaines règles pour démarrer la contraception sous BELARA.
Relais d'une autre contraception hormonale :
Relais d'un contraceptif hormonal combiné :
La femme doit prendre le premier comprimé de BELARA le premier jour qui suit l'intervalle habituel sans comprimé, ou la prise des comprimés placebos du précédent contraceptif COC.
Relais d'un contraceptif par progestatif seul :
Le premier comprimé de BELARA doit être pris le lendemain de l'arrêt de la pilule progestative. Durant les 7 premiers jours, une méthode de contraception mécanique complémentaire doit être utilisée.
Relais d'un contraceptif hormonal injectable ou un implant :
L'administration de BELARA peut commencer le jour du retrait de l'implant, ou le jour prévu pour l'injection suivante s'il s'agit d'une forme injectable.
Cependant, durant les 7 premiers jours, il est recommandé d'utiliser une méthode de contraception mécanique complémentaire.
Après une interruption de grossesse (fausse couche ou avortement) au cours du premier trimestre de grossesse :
Après une interruption de grossesse au cours du premier trimestre de grossesse, la prise de BELARA peut commencer immédiatement. Dans ce cas, aucune méthode contraceptive complémentaire n'est nécessaire.
Après une interruption de grossesse au cours du 2ème trimestre de grossesse :
Les femmes qui n'allaitent pas peuvent commencer la contraception entre 21 et 28 jours après l'accouchement. Dans ce cas, aucune méthode contraceptive mécanique complémentaire n'est nécessaire.
Si la contraception débute au-delà de 28 jours après l'accouchement, une contraception mécanique complémentaire pendant les 7 premiers jours est nécessaire.
Si des rapports sexuels ont déjà eu lieu, il convient de s'assurer de l'absence d'une grossesse ou d'attendre les premières règles avant de commencer la contraception.
Allaitement (voir rubrique 4.6.) :
BELARA ne doit pas être pris au cours de l'allaitement.
Après l'arrêt de BELARA :
Après l'arrêt de BELARA, le premier cycle peut être allongé d'environ 1 semaine.
Conduite à tenir en cas d'oubli d'un ou de plusieurs comprimés
Si l'oubli d'un comprimé est constaté dans les 12 heures, aucune autre méthode contraceptive n'est nécessaire. La femme doit prendre le comprimé oublié dès qu'elle constate cet oubli et prendre les comprimés suivants comme d'habitude.
Si l'oubli est supérieur à 12 heures, l'efficacité de la contraception peut être réduite. Vous devez dans ce cas tenir compte des 2 règles de base suivantes pour choisir la conduite à tenir:
1/ la prise de comprimés ne doit jamais être interrompue pendant plus de 7 jours,
2/ 7 jours de prises ininterrompues sont nécessaires pour obtenir une inhibition correcte de l'axe hypothalamo-hypophyso-ovarien.
Le dernier comprimé oublié devra être pris immédiatement, même si cela implique la prise de 2 comprimés en même temps. Les comprimés suivants devront être pris à l'heure habituelle. Une contraception mécanique complémentaire (par exemple, préservatifs) est cependant nécessaire pendant les 7 jours suivants.
Si les comprimés oubliés correspondent à la première semaine du cycle et si un rapport sexuel a eu lieu dans les 7 jours qui précèdent l'oubli des comprimés (incluant l'intervalle libre), il existe un risque de grossesse. Le risque de grossesse est d'autant plus élevé que le nombre de comprimés oubliés est important ou que la date de l'oubli est proche de la fin de la plaquette.
S'il reste sur la plaquette de BELARA moins de 7 comprimés, la plaquette suivante doit être commencée dès la fin de la plaquette en cours, c'est à dire sans interruption de prise entre les plaquettes. Dans ce cas, les règles n'apparaîtront probablement que lors du cycle suivant; cependant quelques saignements pourront survenir pendant la prise de comprimés. Si, après la fin de la seconde plaquette, les règles n'apparaissent pas, un test de grossesse doit être effectué.
Conduite à tenir en cas de vomissement ou de diarrhées
Si des vomissements ou diarrhées se produisent dans les 4 heures qui suivent la prise d'un comprimé, il est possible que son absorption ne soit pas complète et que l'effet contraceptif ne soit plus assuré. Dans ce cas, se reporter au paragraphe ci-dessus « Conduite à tenir en cas d'oubli d'un ou de plusieurs comprimés ». La prise de BELARA devra continuer.
Comment retarder les hémorragies de privation ?
Pour retarder l'hémorragie de privation, la femme doit commencer une nouvelle plaquette de BELARA sans intervalle libre de 7 jours. Ce décalage des règles peut être maintenu aussi longtemps que la femme le souhaite, jusqu'à la fin de la seconde plaquette. Pendant cette période, des spottings ou des saignements irréguliers peuvent survenir.
La prise régulière de BELARA est alors reprise après un intervalle libre de 7 jours.
Pour décaler les hémorragies de privation à un autre jour de la semaine, la femme peut raccourcir l'intervalle libre du nombre de jours qu'elle souhaite. Plus l'intervalle est court, plus le risque d'absence d'hémorragie de privation est important, avec l'éventualité de spottings et de saignements irréguliers.
Population pédiatrique
BELARA est indiqué uniquement après la ménarche. La sécurité et l'efficacité de l'acétate de chlormadinone et de l'éthinylestradiol chez les adolescents de moins de 16 ans n'ont pas été établies. Aucune donnée n'est disponible.
Personnes âgées
BELARA n'est pas indiqué après la ménopause.
Les contraceptifs hormonaux combinés (CHC) ne doivent pas être utilisés dans les situations suivantes.
BELARA devra être interrompu immédiatement si l'un de ces troubles apparaît au cours de son utilisation :
· Diabète déséquilibré ;
· Hypertension artérielle non contrôlée ou augmentation significative et constante de la pression (valeurs constamment > 90/140 mm Hg) ;
· Présence ou risque de thrombo-embolie veineuse (TEV)
· Thrombo-embolie veineuse - présence de TEV (patient traité par des anticoagulants) ou antécédents de TEV (p. ex. thrombose veineuse profonde [TVP] ou embolie pulmonaire [EP])
· Prédisposition connue, héréditaire ou acquise, à la thrombo-embolie veineuse, telle qu’une résistance à la protéine C activée (PCa) (y compris une mutation du facteur V de Leiden), un déficit en antithrombine III, un déficit en protéine C, un déficit en protéine S
· Intervention chirurgicale majeure avec immobilisation prolongée (voir rubrique 4.4)
· Risque élevé de thrombo-embolie veineuse dû à la présence de multiples facteurs de risque (voir rubrique 4.4)
Présence ou risque de thrombo-embolie artérielle (TEA)
· Thrombo-embolie artérielle - présence ou antécédents de thrombo-embolie artérielle (p. ex. infarctus du myocarde [IM]) ou de prodromes (p. ex. angine de poitrine)
· Affection cérébrovasculaire - présence ou antécédents d’accident vasculaire cérébral (AVC) ou de prodromes (p. ex. accident ischémique transitoire [AIT])
· Prédisposition connue, héréditaire ou acquise, à la thrombo-embolie artérielle, telle qu’une hyperhomocystéinémie ou la présence d’anticorps anti-phospholipides (anticorps anti-cardiolipine, anticoagulant lupique).
· Antécédents de migraine avec signes neurologiques focaux
· Risque élevé de thrombo-embolie artérielle dû à la présence de multiples facteurs de risque (voir rubrique 4.4) ou d’un facteur de risque sévère tel que :
o diabète avec symptômes vasculaires
o hypertension artérielle sévère
o dyslipoprotéinémie sévère
· Hépatite, ictère, anomalies de la fonction hépatique, tant que les tests fonctionnels hépatiques ne se sont pas normalisés ;
· Prurit généralisé, cholestase, en particulier lors d'une précédente grossesse ou d'un traitement antérieur par œstrogènes ;
· Maladie de Dubin-Johnson, maladie de Rotor, troubles du flux biliaire ;
· Existence ou antécédents de méningiomes ;
· Tumeurs hépatiques ou antécédents ;
· Douleur épigastrique aiguë, hypertrophie du foie ou symptômes d'hémorragie intra-abdominale (voir rubrique 4.8) ;
· Première apparition ou réapparition de porphyrie (les trois formes, en particulier la porphyrie acquise) ;
· Tumeurs malignes hormono-dépendantes connues ou présumées (de l'utérus ou des seins) ;
· Troubles graves du métabolisme lipidique ;
· Pancréatite ou antécédent de pancréatite, si associée à une hypertriglycéridémie sévère ;
· Symptômes primaires de maux de tête migraineux ou apparition plus fréquente de maux de tête exceptionnellement aigus ;
· Troubles sensoriels aigus, notamment troubles de la vue ou de l'audition ;
· Troubles moteurs (en particulier, parésie) ;
· Crises d'épilepsie répétées ;
· Dépression sévère ;
· Antécédents d'otospongiose survenue au cours de grossesses précédentes ;
· Aménorrhées inexpliquées ;
· Hyperplasie endométriale ;
· Saignements vaginaux d'origine inconnue ;
· Hypersensibilité à l'un des composants actifs ou des excipients mentionnés à la rubrique 6.1.
L'existence d'un ou de plusieurs facteurs de risque de thrombose veineuse ou artérielle constitue une contre-indication (voir rubrique 4.4)
BELARA est contre-indiqué en administration concomitante avec les des médicaments contenant l’association ombitasvir/paritaprévir/ritonavir, et le dasabuvir, ou médicament contenant glécaprévir/pibrentasvir ou sofosbuvir/velpatasvir/voxilaprévir (voir rubriques 4.5).
4.4. Mises en garde spéciales et précautions d'emploi
Mises en garde spéciales
Le tabagisme augmente le risque d'effets secondaires cardio-vasculaires sévères au cours de la contraception hormonale combinée (CHC). Le risque augmente avec l'âge et la consommation de tabac de façon plus prononcée chez les femmes âgées de plus de 35 ans. Chez ces dernières, une autre méthode contraceptive est recommandée.
L'utilisation de CHC est associée à une augmentation du risque de survenue de maladies graves telles que infarctus du myocarde, maladies thrombo-emboliques, AVC ou néoplasies hépatiques. D'autres facteurs de risques tels que l'hypertension, l'hyperlipidémie, l'obésité, le diabète augmentent les risques de morbidité et de mortalité.
Si la patiente présente l’un des troubles ou l’un des facteurs de risque mentionnés ci-dessous, la pertinence du traitement par BELARA doit être discutée avec elle.
En cas d’aggravation ou de survenue de l’un de ces troubles ou facteurs de risque, la nécessité d’interrompre l’utilisation de BELARA doit être discutée entre le médecin et la patiente.
Maladies thrombo-emboliques et autres maladies vasculaires :
Les études épidémiologiques ont établi un lien entre l'utilisation d'un contraceptif hormonal et un risque accru de maladies thromboemboliques veineuse ou artérielle (infarctus du myocarde, apoplexie, thromboses veineuses profondes, embolie pulmonaire). Ces évènements demeurent rares. De façon extrêmement rare, des cas de thrombose ont été signalés chez des utilisatrices de CHC dans d’autres vaisseaux sanguins, p. ex. les veines et artères hépatiques, mésentériques, rénales ou rétiniennes.
Risque de thrombo-embolie veineuse (TEV)
Le risque de TEV est augmenté chez les femmes qui utilisent un contraceptif hormonal combiné (CHC) en comparaison aux femmes qui n’en utilisent pas. Les CHC contenant du lévonorgestrel, du norgestimate ou de la noréthistérone sont associés au risque de TEV le plus faible. D’autres CHCs à base de chlormadinone/éthinylestradiol tels que BELARA peuvent avoir un risque multiplié par 1,25 par rapport à celui associé aux CHCs contenant du lévonorgestrel. La décision d’utiliser tout autre CHC que ceux associés au risque de TEV le plus faible doit être prise uniquement après concertation avec la patiente afin de s’assurer qu’elle comprend le risque de TEV associé aux CHC, l’influence de ses facteurs de risque actuels sur ce risque et le fait que le risque de TEV est maximal pendant la première année d’utilisation. Certaines données indiquent également une augmentation du risque lors de la reprise d’un CHC après une interruption de 4 semaines ou plus.
Parmi les femmes qui n’utilisent pas de CHC et qui ne sont pas enceintes, environ 2 sur 10 000 développeront une TEV sur une période d’un an. Cependant, chez une femme donnée, le risque peut être considérablement plus élevé, selon les facteurs de risque qu’elle présente (voir ci-dessous).
Les études épidémiologiques concernant les femmes qui utilisent des contraceptifs oraux combinés faiblement dosés (< 50 μg d’éthinylestradiol) ont montré que, sur 10 000 femmes, environ 6 à 12 développeront une TEV sur une période d’un an.
On estime que sur 10 000 femmes qui utilisent un CHC contenant de la chlormadinone, 6 à 9 développeront une TEV sur une période d’un an, contre 61 environ chez les utilisatrices de CHC contenant du lévonorgestrel.
Nombre d’événements de TEV pour 10 000 femmes sur un an
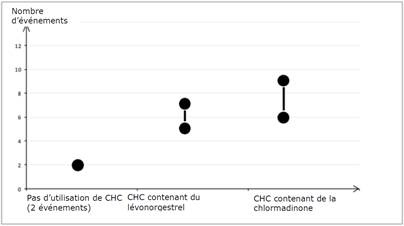
Le nombre de TEV par année associé aux CHC faiblement dosés (< 50 µg d’éthinylestradiol) est inférieur à celui attendu pendant la grossesse ou en période post-partum.
La TEV peut être fatale dans 1 à 2 % des cas.
1 Point central de l’intervalle de 5-7 pour 10 000 années-femmes sur la base d’un risque relatif, pour les CHC contenant du lévonorgestrel par rapport à la non-utilisation d’un CHC, d’environ 2,3 à 3,6
Facteurs de risque de TEV
Le risque de complications thrombo-emboliques veineuses chez les utilisatrices de CHC peut être considérablement accru si d’autres facteurs de risque sont présents, en particulier si ceux-ci sont multiples (voir le tableau ci-dessous).
BELARA est contre-indiqué chez les femmes présentant de multiples facteurs de risque, ceux-ci les exposant à un risque élevé de thrombose veineuse (voir rubrique 4.3). Lorsqu’une femme présente plus d’un facteur de risque, il est possible que l’augmentation du risque soit supérieure à la somme des risques associés à chaque facteur pris individuellement – dans ce cas, le risque global de TEV doit être pris en compte. Si le rapport bénéfice/risque est jugé défavorable, le CHC ne doit pas être prescrit (voir rubrique 4.3).
Tableau : Facteurs de risque de TEV
|
Facteur de risque |
Commentaire |
|
Obésité (indice de masse corporelle supérieur à 30 kg/m²) |
L’élévation de l’IMC augmente considérablement le risque. Ceci est particulièrement important à prendre en compte si d’autres facteurs de risque sont présents. |
|
Immobilisation prolongée, intervention chirurgicale majeure, toute intervention chirurgicale sur les jambes ou le bassin, neurochirurgie ou traumatisme majeur
Remarque : l’immobilisation temporaire, y compris les trajets aériens > 4 heures, peut également constituer un facteur de risque de TEV, en particulier chez les femmes présentant d’autres facteurs de risque |
Dans ces situations, il est conseillé de suspendre l’utilisation du dispositif transdermique/de la pilule/de l’anneau (au moins quatre semaines à l’avance en cas de chirurgie programmée) et de ne reprendre le CHC que deux semaines au moins après la complète remobilisation. Une autre méthode de contraception doit être utilisée afin d’éviter une grossesse non désirée. Un traitement anti-thrombotique devra être envisagé si BELARA n’a pas été interrompu à l’avance. |
|
Antécédents familiaux (thrombo-embolie veineuse survenue dans la fratrie ou chez un parent, en particulier à un âge relativement jeune, c.-à-d. avant 50 ans) |
En cas de prédisposition héréditaire suspectée, la femme devra être adressée à un spécialiste pour avis avant toute décision concernant l’utilisation de CHC |
|
Autres affections médicales associées à la TEV |
Cancer, lupus érythémateux disséminé, syndrome hémolytique et urémique, maladies inflammatoires chroniques intestinales (maladie de Crohn ou rectocolite hémorragique) et drépanocytose |
|
Âge |
En particulier au-delà de 35 ans |
Il n’existe aucun consensus quant au rôle éventuel joué par les varices et les thrombophlébites superficielles dans l’apparition ou la progression d’une thrombose veineuse.
L’augmentation du risque de thrombo-embolie pendant la grossesse, et en particulier pendant les 6 semaines de la période puerpérale, doit être prise en compte (pour des informations concernant « Grossesse et allaitement », voir rubrique 4.6).
Symptômes de TEV (thrombose veineuse profonde et embolie pulmonaire)
Les femmes doivent être informées qu’en cas d’apparition de ces symptômes, elles doivent consulter un médecin en urgence et lui indiquer qu’elles utilisent un CHC.
Les symptômes de la thrombose veineuse profonde (TVP) peuvent inclure :
· gonflement unilatéral d’une jambe et/ou d’un pied ou le long d’une veine de la jambe ;
· douleur ou sensibilité dans une jambe, pouvant n’être ressentie qu’en position debout ou lors de la marche ;
· sensation de chaleur, rougeur ou changement de la coloration cutanée de la jambe affectée.
Les symptômes de l’embolie pulmonaire (EP) peuvent inclure :
· apparition soudaine et inexpliquée d’un essoufflement ou d’une accélération de la respiration ;
· toux soudaine, pouvant être associée à une hémoptysie ;
· douleur thoracique aiguë ;
· étourdissements ou sensations vertigineuses sévères ;
· battements cardiaques rapides ou irréguliers.
Certains de ces symptômes (p. ex. « essoufflement », « toux ») ne sont pas spécifiques et peuvent être interprétés à tort comme des signes d’événements plus fréquents ou moins sévères (infections respiratoires, p. ex.).
Les autres signes d’une occlusion vasculaire peuvent inclure : douleur soudaine, gonflement et coloration légèrement bleutée d’une extrémité.
Si l’occlusion se produit dans l’œil, les symptômes peuvent débuter sous la forme d’une vision trouble indolore pouvant évoluer vers une perte de la vision. Dans certains cas, la perte de la vision peut survenir presque immédiatement.
Risque de thrombo-embolie artérielle (TEA)
Des études épidémiologiques ont montré une association entre l’utilisation de CHC et l’augmentation du risque de thrombo-embolie artérielle (infarctus du myocarde) ou d’accident cérébrovasculaire (p. ex. accident ischémique transitoire, AVC). Les événements thrombo-emboliques artériels peuvent être fatals.
Facteurs de risque de TEA
Le risque de complications thrombo-emboliques artérielles ou d’accident cérébrovasculaire chez les utilisatrices de CHC augmente avec la présence de facteurs de risque (voir le tableau). BELARA est contre-indiqué chez les femmes présentant un facteur de risque sévère ou de multiples facteurs de risque de TEA qui les exposent à un risque élevé de thrombose artérielle (voir rubrique 4.3). Lorsqu’une femme présente plus d’un facteur de risque, il est possible que l’augmentation du risque soit supérieure à la somme des risques associés à chaque facteur pris individuellement – dans ce cas, le risque global doit être pris en compte. Si le rapport bénéfice/risque est jugé défavorable, le CHC ne doit pas être prescrit (voir rubrique 4.3).
Tableau : Facteurs de risque de TEA
|
Facteur de risque |
Commentaire |
|
Âge |
En particulier au-delà de 35 ans |
|
Tabagisme |
Il doit être conseillé aux femmes de ne pas fumer si elles souhaitent utiliser un CHC. Il doit être fortement conseillé aux femmes de plus de 35 ans qui continuent de fumer d’utiliser une méthode de contraception différente. |
|
Hypertension artérielle |
|
|
Obésité (indice de masse corporelle supérieur à 30 kg/m2) |
L’élévation de l’IMC augmente considérablement le risque. Ceci est particulièrement important à prendre en compte chez les femmes présentant d’autres facteurs de risque. |
|
Antécédents familiaux (thrombo-embolie artérielle survenue dans la fratrie ou chez un parent, en particulier à un âge relativement jeune, c.-à-d. avant 50 ans) |
En cas de prédisposition héréditaire suspectée, la femme devra être adressée à un spécialiste pour avis avant toute décision concernant l’utilisation de CHC. |
|
Migraine |
L’accroissement de la fréquence ou de la sévérité des migraines lors de l’utilisation d’un CHC (qui peut être le prodrome d’un événement cérébrovasculaire) peut constituer un motif d’arrêt immédiat du CHC. |
|
Autres affections médicales associées à des événements indésirables vasculaires |
Diabète, hyperhomocystéinémie, valvulopathie cardiaque et fibrillation auriculaire, dyslipoprotéinémie et lupus érythémateux disséminé |
Symptômes de TEA
Les femmes doivent être informées qu’en cas d’apparition de ces symptômes, elles doivent consulter un médecin en urgence et lui indiquer qu’elles utilisent un CHC.
Les symptômes d’un accident cérébrovasculaire peuvent inclure :
· apparition soudaine d’un engourdissement ou d’une faiblesse du visage, d’un bras ou d’une jambe, en particulier d’un côté du corps ;
· apparition soudaine de difficultés à marcher, de sensations vertigineuses, d’une perte d’équilibre ou de coordination ;
· apparition soudaine d’une confusion, de difficultés à parler ou à comprendre ;
· apparition soudaine de difficultés à voir d’un œil ou des deux yeux ;
· céphalée soudaine, sévère ou prolongée, sans cause connue ;
· perte de conscience ou évanouissement avec ou sans crise convulsive.
Des symptômes temporaires suggèrent qu’il s’agit d’un accident ischémique transitoire (AIT).
Les symptômes de l’infarctus du myocarde (IM) peuvent inclure :
· douleur, gêne, pression, lourdeur, sensation d’oppression ou d’encombrement dans la poitrine, le bras ou sous le sternum ;
· sensation de gêne irradiant vers le dos, la mâchoire, la gorge, le bras, l’estomac ;
· sensation d’encombrement, d’indigestion ou de suffocation ;
· transpiration, nausées, vomissements ou sensations vertigineuses ;
· faiblesse, anxiété ou essoufflement extrêmes ;
· battements cardiaques rapides ou irréguliers.
Les utilisatrices de CHC doivent consulter leur médecin dès les premiers signes de thromboses. BELARA doit être arrêté sur suspicion ou confirmation de thrombose.
Tumeurs
Certaines études épidémiologiques ont rapporté une augmentation de l'incidence du cancer du col de l'utérus chez les utilisatrices de CHC à long terme (plus particulièrement en cas d'infections par le papillomavirus Humain HPV). Cependant, il n'existe aucun consensus quant à l'influence d'autres facteurs, tels que le comportement sexuel ou l'utilisation de méthodes contraceptives mécaniques (voir Examen médical).
Une méta-analyse de 54 études épidémiologiques a rapporté qu'il existe une légère augmentation du risque relatif de cancer du sein chez les femmes sous CHC (RR = 1,24). Cette majoration du risque disparaît progressivement au cours des 10 ans qui suivent l'arrêt des CHC. Ces études ne donnent aucune information quant à la cause.
Le cancer du sein étant rare chez les femmes de moins de 40 ans, le nombre plus élevé de diagnostic de cancers du sein chez les utilisatrices habituelles ou nouvelles utilisatrices est faible par rapport au risque global de cancer du sein.
Dans de rares cas, des tumeurs hépatiques bénignes, et encore plus rarement malignes, ont été rapportées chez des femmes sous contraceptifs oraux. Dans de rares cas isolés, ces tumeurs ont conduit à une hémorragie intra-abdominale pouvant compromettre le pronostic vital. En cas de douleurs abdominales sévères accompagnées d'hépatomégalie ou de signes d'hémorragies intra abdominales, une tumeur hépatique doit être suspectée et le traitement par BELARA doit être arrêté.
Méningiome
Des cas de méningiomes (simples et multiples) ont été rapportés lors de l'utilisation d’acétate de chlormadinone, en particulier à des doses élevées et pendant une durée prolongée (plusieurs années). Les patientes doivent faire l’objet d’une surveillance pour détecter les signes et symptômes de méningiomes conformément à la pratique clinique. Si un méningiome est diagnostiqué chez une patiente, tout traitement contenant de l’acétate de chlormadinone doit être arrêté, par mesure de précaution.
Certaines données montrent que le risque de méningiome peut diminuer après l’arrêt du traitement par l’acétate de chlormadinone.
Autres pathologies
Trouble psychiatrique
L'état dépressif et la dépression sont des effets indésirables bien connus liés à l'utilisation de contraceptif hormonal (voir rubrique 4.8). La dépression peut être grave et constitue un facteur de risque bien connu de comportement suicidaire et de suicide. Il convient de conseiller aux femmes de contacter leur médecin en cas de changement d'humeur et de symptômes dépressifs, y compris peu de temps après le début du traitement.
Bien qu'une légère augmentation de la pression artérielle ait été rapportée chez de nombreuses femmes sous contraception hormonale, les élévations cliniquement significatives sont rares. Aucune relation systématique n'a été établie entre l'utilisation de CHC et une hypertension artérielle clinique. Si, au cours d'une CHC, chez une femme présentant une hypertension artérielle, les valeurs tensionnelles restent constamment élevées de façon significative, le traitement par BELARA devra être interrompu et un traitement de l'hypertension artérielle sera instauré. La reprise de BELARA pourra être envisagée après normalisation des valeurs tensionnelles sous anti-hypertenseur.
Les estrogènes exogènes peuvent provoquer ou aggraver des symptômes d’angiœdème acquis ou héréditaire.Une récidive d'herpès gestationnel peut survenir au cours d'une CHC.
Le risque de pancréatite augmente chez les femmes sous CHC ayant des antécédents d'hyperlipidémies. Des altérations aiguës ou chroniques du foie nécessitent l'arrêt de prise de la CHC jusqu'au retour à la normale des paramètres biologiques hépatiques. La récurrence d'un ictère cholostatique précédemment apparu au cours d'une première grossesse ou sous hormones sexuelles impose l'arrêt de la prise de CHC.
L'administration de CHC peut exercer un effet sur la résistance périphérique à l'insuline et la tolérance au glucose. Par conséquent, les femmes diabétiques doivent être attentivement surveillées, en particulier lors de l'instauration d'une contraception hormonale.
Un chloasma peut parfois se produire, en particulier chez les femmes ayant des antécédents de chloasma gravidique. Les femmes ayant une prédisposition au chloasma doivent éviter de s'exposer au soleil ou aux ultra-violets lorsqu'elles prennent une contraception hormonale.
Précautions d'emploi
L'administration d'estrogènes ou d'associations estrogène/progestatifs peut avoir des effets négatifs sur certaines maladies. Une surveillance médicale est nécessaire dans les situations pathologiques suivantes:
· Epilepsie ;
· sclérose en plaques ;
· tétanie ;
· migraine (voir rubrique 4.3.) ;
· asthme ;
· insuffisance cardiaque ou rénale ;
· chorée mineure ;
· diabète sucré (voir rubrique 4.3.) ;
· troubles hépatiques (voir rubrique 4.3.) ;
· dyslipoprotéinémie (voir rubrique 4.3.) ;
· maladies auto-immune (notamment, lupus érythémateux disséminé) ;
· obésité ;
· hypertension artérielle (voir rubrique 4.3.) ;
· endométriose ;
· varices ;
· phlébite (voir rubrique 4.3.) ;
· troubles de la coagulation (voir rubrique 4.3.) ;
· mastopathie ;
· myome utérin ;
· herpès gestationnel ;
· dépression ;
· maladie inflammatoire chronique intestinale (maladie de Crohn, colite ulcérative, voir rubrique 4.8).
Consultation/examen médical
Avant l’instauration ou la reprise d’un traitement par BELARA, une recherche complète des antécédents médicaux (y compris les antécédents familiaux) doit être effectuée et la présence d’une grossesse doit être exclue. La pression artérielle doit être mesurée et un examen physique doit être réalisé, en ayant à l’esprit les contre-indications (voir rubrique 4.3) et les mises en garde (voir rubrique 4.4).
Il est important d’attirer l’attention des patientes sur les informations relatives à la thrombose veineuse et artérielle, y compris le risque associé à BELARA comparé à celui associé aux autres CHC, les symptômes de la TEV et de la TEA, les facteurs de risque connus et la conduite à tenir en cas de suspicion de thrombose.
Il doit également être indiqué aux patientes de lire attentivement la notice et de suivre les conseils fournis. La fréquence et la nature des examens doivent être définies sur la base des recommandations en vigueur et adaptées à chaque patiente.
Les patientes doivent être averties que les contraceptifs hormonaux ne protègent pas contre l’infection par le VIH (SIDA) et les autres maladies sexuellement transmissibles.
Diminution de l'efficacité
L'efficacité contraceptive peut être diminuée en cas d'oubli de comprimé (voir rubrique ' Conduite à tenir en cas d'oubli d'un ou de plusieurs comprimés'), de vomissements, de troubles intestinaux y compris diarrhées (voir rubrique 4.2), de prise concomitante de certains médicaments (voir rubrique 4.5) ou, très rarement, de troubles métaboliques.
Altération du contrôle du cycle
Saignements irréguliers (spottings).
Tous les contraceptifs hormonaux peuvent entraîner des saignements irréguliers (métrorragies/ spottings) en particulier au cours des premiers mois. Les saignements irréguliers ne sont donc significatifs qu'après un certain temps d'adaptation, d'environ 3 cycles. Si pendant la prise de BELARA, les saignements irréguliers persistent ou se produisent après des cycles jusque là réguliers, des examens supplémentaires appropriés devront être pratiqués afin d'exclure une grossesse ou un dysfonctionnement organique. Une fois exclus, la prise de BELARA pourra alors être poursuivie ou un switch pourra se faire vers un autre produit.
L'hémorragie inter-menstruelle peut être un signe d'une baisse de l'efficacité contraceptive (voir les rubriques 4.2 "Conduite à tenir en cas d'oubli d'un ou de plusieurs comprimés", "Conduite à tenir en cas de vomissements ou de diarrhées" et voir rubrique 4.5).
Absence de saignements de privation
Après 21 jours de prise de pilule, les hémorragies de privation peuvent survenir normalement. Très rarement et en particulier pendant les premiers mois, les hémorragies de privation peuvent ne pas survenir au cours de l'intervalle libre. Cependant cela n'entraîne pas de diminution de l'effet contraceptif. Si la prise de CHC a été suivie correctement, sans oubli de comprimé, sans prolongation de l'intervalle libre, sans traitement concomitant, sans vomissement ni diarrhée, la conception est peu probable et BELARA peut être continué.
Cependant, si la prise de BELARA n'a pas été suivie correctement avant l'absence de la première hémorragie de privation ou si deux hémorragies de privations successives ne se produisent pas, il convient d'éliminer une grossesse avant de poursuivre la prise de CHC.
Les produits à base de millepertuis (hypericum perforatum) ne doivent pas être administrés pendant la prise de BELARA (voir rubrique 4.5).
Excipients
Ce médicament contient du lactose (lactose monohydraté). Les patients présentant une intolérance au galactose, un déficit total en lactase ou un syndrome de malabsorption du glucose ou du galactose (maladies héréditaires rares) ne doivent pas prendre ce médicament.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Note : l'information relative à la prescription de médicaments associés doit être consultée pour identifier les interactions potentielles.
Interactions pharmacodynamiques
Au cours des essais cliniques menés chez des patients traités pour une infection par le virus de l'hépatite C (VHC) et recevant des médicaments contenant ombitasvir/paritaprevir/ritonavir et dasabuvir, avec ou sans ribavirine, il a été observé des augmentations de transaminase (ALAT) supérieures à 5 fois la limite supérieure de la normale (LSN), significativement plus fréquentes chez les femmes utilisant des médicaments contenant de l'éthinylestradiol, tel que les contraceptifs hormonaux combinés (CHC). De plus, chez des patients traités par le glecaprevir/pibrentasvir ou sofosbuvir/velpatasvir/voxilaprevir, des augmentations des ALAT ont été observées chez les femmes utilisant des médicaments contenant de l'éthinylestradiol tels que les CHC (voir la rubrique 4.3).
Par conséquent, les femmes prenant BELARA doivent passer à une autre méthode de contraception (par exemple, une contraception uniquement progestative ou une contraception non hormonale) avant de commencer un traitement avec ces associations de médicaments. BELARA peut être repris 2 semaines après la fin du traitement avec ces associations de médicaments.
Interactions pharmacocinétiques
Effets d'autres médicaments sur BELARA
Des interactions peuvent se produire avec les médicaments inducteurs des enzymes microsomales avec pour conséquence une augmentation de la clairance des hormones sexuelles qui peut conduire à une hémorragie de privation et/ou un échec de la contraception orale.
Prise en compte de l'effet inducteur enzymatique
L'induction enzymatique peut déjà être observée après quelques jours de traitement. L'induction enzymatique maximale est généralement atteinte en quelques semaines. Après l'arrêt de la prise du médicament inducteur enzymatique, l'induction enzymatique peut être maintenue pendant environ 4 semaines.
Traitement de courte durée
Les femmes prenant un médicament inducteur enzymatique doivent utiliser temporairement une contraception mécanique ou autre contraception supplémentaire en plus du COC. La contraception mécanique doit être utilisée pendant toute la durée du traitement et pendant 28 jours après l'arrêt du traitement.
Si la prise du médicament se poursuit au-delà du dernier comprimé, il conviendra de commencer immédiatement la plaquette suivante sans intervalle libre.
Traitement de longue durée
Il est recommandé aux femmes qui prennent un médicament inducteur enzymatique pendant une période longue de choisir une autre méthode fiable de contraception non hormonale.
Les interactions suivantes ont été rapportées dans la littérature.
Substances augmentant la clairance des COC (diminution de l’efficacité des COC par induction enzymatique), ex. :
Les barbituriques, le bosentan, la carbamazépine, la barbexaclone, la phenytoïne, la primidone, le modafinil, la rifampicine, la rifabutine, les médicaments utilisés pour traiter les infections par le HIV le ritonavir, la névirapine et l'éfavirenz et aussi éventuellement le felbamate, la griséofulvine, l’oxcarbazépine, le topiramate, et les préparations contenant du millepertuis (Hypericum perforatum).
Médicaments/substances actives qui peuvent réduire les concentrations sériques d'éthinylestradiol en augmentant la motilité gastro-intestinale ou en altérant l'absorption :
Le métoclopramide, le charbon actif.
Substances ayant des effets variables sur la clairance des COC :
La prise concomitante de COC en association avec des inhibiteurs de la protéase du VIH et des inhibiteurs non nucléosidiques de la transcriptase inverse, dont les inhibiteurs du VHC, peut augmenter ou diminuer les concentrations plasmatiques de l’estrogène ou des progestatifs. L'effet de ces changements peut avoir une incidence clinique dans certains cas.
Par conséquent, une attention particulière devra être portée aux co-prescriptions de médicaments utilisés pour traiter les infections par VIH/VHC afin d'identifier les interactions potentielles et de faire les recommandations nécessaires. En cas de doute, une méthode contraceptive mécanique supplémentaire doit être utilisée par les femmes qui suivent une thérapie composée d'inhibiteur de protéase ou d'inhibiteur non nucléosidique de la transcriptase inverse.
Les substances suivantes peuvent augmenter les concentrations sériques d'éthinylestradiol :
· les substances inhibant la sulfatation de l'éthinylestradiol au niveau intestinal (par ex. acide ascorbique ou paracétamol) ;
· atorvastatine (augmentation de 20% de l'aire sous la courbe (ASC) de l'éthinylestradiol) ;
· les substances inhibitrices enzymatiques hépatiques telles que les antimycosiques imidazolés (par ex. fluconazole), indinavir, troléandomycine.
Effets de BELARA sur d'autres médicaments.
Les contraceptifs oraux peuvent affecter le métabolisme de certaines autres substances actives. Ainsi, les concentrations tissulaires ou plasmatiques peuvent soit augmenter soit diminuer.
· par inhibition enzymatique hépatique entraînant une augmentation des concentrations sériques tel que diazépam (et autres benzodiazépines métabolisées par hydroxylation), ciclosporine, théophylline, prednisolone;
· par induction enzymatique hépatique (glucuroconjugaison) entraînant une diminution des concentrations sériques : lamotrigine, clofibrate, paracétamol, morphine et lorazépam.
Le besoin en insuline ou en anti diabétique oral peut être modifié en raison des effets sur les niveaux de quantité de glucose tolérée (voir rubrique 4.4).
Ceci peut s'appliquer aux médicaments pris récemment.
Le Résumé des Caractéristiques du Produit (RCP) du médicament prescrit devra être contrôlé en vue des interactions éventuelles avec BELARA.
Tests biologiques :
L'utilisation de contraceptifs stéroïdiens peut modifier les résultats de certains examens biologiques tels que : les tests fonctionnels hépatiques, thyroïdiens, surrénaliens et rénaux, le taux plasmatique des protéines (porteuses) comme la corticosteroid-binding globulin (CBG) et des fractions lipidiques/lipoprotéiniques, les paramètres du métabolisme glucidique, les paramètres de la coagulation et de la fibrinolyse. Les modifications restent en général dans les limites de la normale.
4.6. Fertilité, grossesse et allaitement
Grossesse
BELARA n'est pas indiqué au cours de la grossesse. Toute grossesse potentielle doit être écartée avant le début de l'administration du médicament. Si une grossesse survient au cours de la prise de BELARA, le traitement doit être immédiatement interrompu. De nombreuses études épidémiologiques n'ont montré aucune preuve clinique d'effets tératogènes ou de toxicité fœtale lors de la prise accidentelle d'œstrogènes pendant la grossesse en association avec d'autres progestatifs dans des doses similaires à celles présentes dans BELARA. Bien que les expériences sur les animaux aient identifié une toxicité reproductive (voir rubrique 5.3), les données cliniques sur plus de 330 femmes enceintes exposées à l'acétate de chlormadinone n'ont identifié aucun effet embryotoxique.
L’augmentation du risque de TEV en période post-partum doit être prise en compte lors de la reprise de BELARA (voir rubriques 4.2 et 4.4).
Allaitement
L'allaitement peut être affecté par les œstrogènes, ces derniers pouvant influer sur la quantité et la composition du lait maternel. De petites quantités de stéroïdes contraceptifs et/ou de leurs métabolites peuvent être excrétées dans le lait maternel et affecter l'enfant. Par conséquent, BELARA ne doit pas être utilisé pendant l'allaitement.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Il n'a pas été observé d'effet sur l'aptitude à conduire ou à utiliser des machines.
a/ Les effets indésirables les plus fréquemment observés au cours des études cliniques (> 20%) sont: saignements irréguliers au cours du cycle, spottings, céphalées et douleurs mammaires. Les saignements irréguliers diminuent habituellement avec la durée de la prise de BELARA.
b/ Les effets indésirables suivants ont été rapportés au cours de l'utilisation de BELARA dans une étude clinique chez 1629 femmes.
|
Fréquence des effets secondaires/ classification système-organes (MedDRA 17.1) |
Très fréquent ≥ 1/10 |
Fréquent (≥ 1/100 á < 1/10) |
Peu fréquent (≥ 1/1 000 á < 1/100) |
Rare (≥ 1/10 000 á < 1/1 000) |
Très rare (< 1/10 000) |
Fréquence indéterminée (ne peut être estimée sur la base des données disponibles) |
|
Infections et infestations |
|
|
Candidose vaginale |
Vulvovaginite |
|
|
|
Tumeurs bénignes, malignes et non précisées (incl kystes et polypes) |
|
|
Adénofibrome du sein |
|
|
|
|
Affections du système immunitaire |
|
|
Hypersensibilité médicamenteuse (y compris réactions allergiques cutanées) |
|
|
Exacerbation des symptômes de l'angio-œdème héréditaire et acquis |
|
Troubles du métabolisme et de la nutrition |
|
|
Dyslipidémie incluant hyper-triglycéridémie |
Augmentation de l'appétit |
|
|
|
Affections psychiatriques |
|
Etat dépressif, nervosité, irritabilité |
Diminution de la libido |
|
|
|
|
Affections du système nerveux |
|
Vertige migraine (avec ou sans aggravation) |
|
|
|
|
|
Affections oculaires |
|
Troubles visuels |
|
Conjonctivite, intolérance aux lentilles de contact. |
|
|
|
Affections auditives et du labyrinthe |
|
|
|
Perte brutale de l'audition, acouphènes, |
|
|
|
Affections vasculaires |
|
|
|
Hypertension, hypotension, collapsus circulatoire, varices, thrombo-embolie veineuse (TEV) ou artérielle (TEA)* |
|
|
|
Affections gastro-intestinales |
Nausées |
Vomissements |
Douleur abdominale, ballonnements et diarhées. |
|
|
|
|
Affections de la peau et du tissu sous -cutané |
|
Acné |
Troubles de la pigmentation anormale, chloasma, alopécie, sécheresse cutanée, hyperhydrose. |
Urticaire, eczéma, érythème, prurit, aggravation de psoriasis, hypertrichose |
Erythème noueux |
|
|
Affections musculo-squelettiques et du tissu conjonctif |
|
Sensation de lourdeur |
Douleur dorsale, troubles musculaires |
|
|
|
|
Affections des organes de reproduction et du sein |
Ecoulement vaginal, dysménorrhée, aménorrhée |
Douleurs abdominales basses |
Galactorrhée |
Hypertrophie mammaire, ménorragie, syndrome prémenstruel |
|
|
|
Troubles généraux et du site d'administration |
|
Fatigue, œdème, prise de poids |
|
|
|
|
|
Investigations |
|
Augmentation de la pression artérielle |
|
|
|
|
*voir paragraphe « Description d’effets indésirables sélectionnés »
Des effets indésirables suivants ont aussi été rapportés associés aux substances actives éthinylestradiol et acétate de chlormadinone dans l’utilisation post marketing : asthénie et réactions allergiques, y compris œdème de Quincke.
« Description d’effets indésirables sélectionnés »
Les effets indésirables suivants ont aussi été rapportés chez des femmes utilisant des contraceptifs hormonaux combinés (CHC) contenant 0,03 mg d'éthinylestradiol et 2 mg d'acétate de chlormadinone :
· une augmentation du risque d'événement thrombotique et thrombo-embolique artériel et veineux, incluant l’infarctus du myocarde, l’AVC, les accidents ischémiques transitoires, la thrombose veineuse et l’embolie pulmonaire, a été observée chez les femmes utilisant des CHC ; ceci est abordé plus en détails en rubrique 4.4 ;
· une augmentation du risque de troubles de la voie biliaire principale a été rapportés dans plusieurs études lors de l'utilisation de CHC au long cours ;
· de rares cas de tumeurs hépatiques bénignes, et très rarement, malignes, ont été rapportés lors de l'utilisation de contraceptifs hormonaux et dans des cas isolés une hémorragie intra-abdominale menaçant le pronostic vital a été observée (voir rubrique 4.4) ;
· aggravation de maladie inflammatoire chronique intestinale (maladie de Crohn, colite ulcérative (voir rubrique 4.4).
Pour les autres effets secondaires tels que cancer du col de l'utérus ou du sein, voir rubrique 4.4.
Interactions
Des interactions entre les contraceptifs oraux et d’autres médicaments (inducteurs enzymatiques) peuvent entraîner des métrorragies et/ou un échec de la contraception (voir rubrique 4.5).
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr.
Aucune information sur les effets indésirables graves n'a été rapportée en cas de surdosage. Les symptômes suivants sont susceptibles d'apparaître : nausées, vomissements et, chez les jeunes filles, petits saignements vaginaux. Il n'existe pas d'antidote et le traitement doit être symptomatique. Un monitoring des électrolytes et des paramètres hépatiques peut être nécessaire dans de rares cas.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : Hormones sexuelles et modulateurs de la fonction génitale ; Progestatifs et estrogènes, associations fixes, code ATC: G03AA15.
Mécanisme d’action
La prise continue de BELARA sur 21 jours provoque la suppression de la sécrétion hypophysaire de FSH et de LH et donc une suppression de l'ovulation. L'endomètre prolifère et est à l'origine de la transformation sécrétoire. De même, la consistance de la glaire cervicale change, ce qui réduit la migration du sperme dans le canal cervical et modifie la motilité du sperme.
La dose journalière minimale d'acétate de chlormadinone nécessaire pour une suppression complète de l'ovulation est de 1,7 mg, celle pour une transformation complète de l'endomètre est de 25 mg par cycle.
L'acétate de chlormadinone est un progestatif de synthèse anti-androgène.
Son effet est basé sur sa capacité à déplacer les androgènes de leurs récepteurs.
Efficacité et sécurité clinique
Lors de l'administration de BELARA dans les essais cliniques effectués sur 1 655 femmes et sur une durée allant jusqu'à 2 ans (soit 22 000 cycles menstruels), 12 grossesses ont été observées. Parmi ces grossesses, 7 sont dues à des erreurs d'administration ou des maladies associées entraînant nausées et vomissements, ou des prises de médicaments concomitants connus pour réduire l'effet contraceptif.
|
Type d'utilisation |
Nombre de grossesses |
Indice de Pearl |
Intervalle de confiance à 95 % |
|
Utilisation type |
12 |
0,698 |
[0,389 ; 1,183] |
|
Utilisation parfaite |
5 |
0,291 |
[0,115 ; 0,650] |
5.2. Propriétés pharmacocinétiques
Acétate de chlormadinone (ACM)
Absorption
Après l'administration orale, l'acétate de chlormadinone est rapidement et presque totalement absorbé. Sa biodisponibilité est élevée car non soumis à l'effet de premier passage hépatique. La concentration plasmatique maximale est atteinte au bout de 1,0 à 2,0 heures.
Distribution
La fraction de l'ACM liée aux protéines plasmatiques humaines, principalement l'albumine, représente plus de 95 %. L'ACM n'a pas d'affinité de liaison avec la SHBG. L'ACM est principalement stocké dans les tissus adipeux.
Biotransformation
Après réactions de réduction, d'oxydation, de conjugaison (par le glucuronide et le sulfate), l'acétate de chlormadinone est métabolisé en plusieurs métabolites. Les principaux métabolites chez l'Homme sont le 3 α -et le 3β-hydroxy-ACM dont les demi- vies ne sont pas sensiblement différentes de celles de l'ACM non métabolisé. Les métabolites 3α- et 3β- hydroxy présentent une activité anti androgène similaire à celle de la molécule mère. Dans l'urine, les métabolites se trouvent principalement sous forme conjuguée. Après clivage enzymatique, les autres métabolites sont le 2a-hydroxy- ACM et les métabolites dihydroxy et 3-hydroxy.
Élimination
La demi-vie moyenne d'élimination plasmatique est d'environ 34 heures (après dose unique) et d'environ 36 à 39 heures (après doses multiples). L'ACM et ses métabolites sont excrétés par voie rénale et dans les fèces en quantités équivalentes après administration orale.
Ethinylestradiol (EE)
Absorption
L'EE est rapidement et presque totalement absorbé après administration orale; le pic plasmatique est atteint au bout de 1 heure et demie. Après effet de premier passage hépatique, la biodisponibilité absolue est d'environ 40 % mais peut varier en fonction des individus (20 à 65 %).
Distribution
Les concentrations plasmatiques en éthinylestradiol rapportées dans la littérature varient considérablement. La fixation aux protéines plasmatiques est d'environ 98 % (essentiellement l'albumine).
Biotransformation
Comme les estrogènes naturels, l'EE est biotransformé par hydroxylation (cytochrome P- 450) et aboutit à la formation du métabolite principal, le 2-hydroxy-EE, métabolisé en plusieurs métabolites et conjugués. L'EE est métabolisé au niveau du foie et de l'intestin grêle. Dans l'urine, sont éliminés principalement des métabolites glucuroconjugués et dans la bile et le plasma, principalement des métabolites sulfates.
Elimination
La demi-vie moyenne d'élimination plasmatique de l'EE est d'environ 12 à 14 heures. L'EE est excrété dans les urines et dans les fèces avec un rapport d'excrétion urine/fèces de 2/3. Après hydrolyse par les bactéries intestinales et passage dans la circulation entéro-hépatique, l'EE est excrété dans la bile sous forme de sulfate.
5.3. Données de sécurité préclinique
La toxicité aiguë des estrogènes est faible. En raison des différences marquées entre les espèces animale et humaine, le résultat des expériences sur les animaux avec des estrogènes n'ont qu'une valeur prédictive limitée pour l'utilisation chez l'homme. Chez l'animal, des doses faibles d'éthinylestradiol, produit de synthèse fréquemment utilisé dans les contraceptifs hormonaux, ont montré un effet embryolétal, avec des anomalies des voies urogénitales et féminisation des fœtus mâles. Ces effets sont spécifiques aux espèces.
L'acétate de chlormadinone a présenté des effets embryoléthaux chez le lapin, le rat et la souris. De plus, un effet tératogène a été observé à des doses embryotoxiques chez le lapin et à la plus faible dose testée (1 mg/kg/jour) chez la souris. L'extrapolation de ces données à l'espèce humaine reste incertaine.
D'après les études conventionnelles, les données précliniques sur la toxicité chronique, la génotoxicité et la carcinogénèse n'ont pas mis en évidence de risque particulier pour l'homme à part ceux qui sont déjà décrits dans d'autres rubriques du RCP.
Noyau : lactose monohydraté, amidon de maïs, povidone K30, stéarate de magnésium
Pelliculage: hypromellose, lactose monohydraté, macrogol 6000, propylène glycol, talc, dioxyde de titane (E171), oxyde de fer rouge (E172).
3 ans
6.4. Précautions particulières de conservation
A conserver à une température ne dépassant pas 30°C.
6.5. Nature et contenu de l'emballage extérieur
21 comprimés sous plaquettes en PVC/PVDC/Aluminium. Boîte de 1, 3, 6 ou 13 plaquettes.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
GEDEON RICHTER PLC.
GYÖMRŐI ÚT 19-21
1103 BUDAPEST
HONGRIE
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 369 500 8 5 : 21 comprimés sous plaquettes (PVC/PVDC/Aluminium). Boîte de 1.
· 34009 369 501 4 6 : 21 comprimés sous plaquettes (PVC/PVDC/Aluminium). Boîte de 3.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I
Informations importantes
Les informations importantes disponibles pour ce médicament sont les suivantes :
- Acétate de nomégestrol et de chlormadinone et méningiome : des mesures dans l'ensemble de l'Europe pour limiter le risque
- Retour d'information sur le PRAC de juillet 2022 (4 - 7 juillet)
- Médicaments à base de nomégestrol et de chlormadinone (dont Lutényl/Luteran et génériques) : l'ANSM a exprimé sa réserve lors du vote des conclusions du PRAC sur la réévaluation de leur bénéfice/risque
- Lutényl/Lutéran et risque de méningiome
ANSM - Mis à jour le : 24/07/2024
BELARA 0,03 mg/2 mg, comprimé pelliculé
Ethinylestradiol / Acétate de chlormadinone
Points importants à connaître concernant les contraceptifs hormonaux combinés (CHC) :
· Ils comptent parmi les méthodes de contraception réversibles les plus fiables lorsqu’ils sont utilisés correctement.
· Ils augmentent légèrement le risque de formation d’un caillot sanguin dans les veines et les artères, en particulier pendant la première année de leur utilisation ou lorsque le contraceptif hormonal combiné est repris après une interruption de 4 semaines ou plus.
· Soyez vigilante et consultez votre médecin si vous pensez présenter les symptômes évocateurs d’un caillot sanguin (voir rubrique 2 « Caillots sanguins »).
Veuillez lire attentivement cette notice avant de prendre ce médicament car elle contient des informations importantes pour vous.
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que BELARA 0,03 mg/2 mg, comprimé pelliculé et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant de prendre BELARA 0,03 mg/2 mg, comprimé pelliculé ?
3. Comment prendre BELARA 0,03 mg/2 mg, comprimé pelliculé ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver BELARA 0,03 mg/2 mg, comprimé pelliculé ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE BELARA 0,03 mg/2 mg comprimé pelliculé ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique - code ATC : G03AA15
BELARA est un CONTRACEPTIF HORMONAL ORAL. Lorsque les contraceptifs hormonaux contiennent 2 hormones comme dans BELARA, ils sont appelés Contraceptif Hormonal Combiné (CHC). Les 21 comprimés de la plaquette contiennent les mêmes quantités d'hormones, c'est pourquoi BELARA est une contraception monophasique.
Les contraceptifs hormonaux comme BELARA ne vous protègent pas du Sida ou des autres affections sexuellement transmissibles. Seuls les préservatifs vous en protègent.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT DE PRENDRE BELARA 0,03 mg/2 mg comprimé pelliculé ?
Avant de commencer à utiliser BELARA, vous devez lire les informations concernant les caillots sanguins (thrombose) en rubrique 2. Il est particulièrement important de lire la description des symptômes d’un caillot sanguin – voir rubrique 2, « Caillots sanguins »).
Avant de commencer la prise de BELARA, votre médecin vous fera un examen général et gynécologique approfondi, éliminera la présence d’une grossesse, tiendra compte des contre-indications et précautions d’emploi, et décidera si BELARA vous convient. Cet examen devrait être effectué chaque année tout au long de la prise de BELARA.
Ne prenez jamais BELARA 0,03 mg/2 mg, comprimé pelliculé :
Vous ne devez pas utiliser BELARA si vous êtes dans l’une des situations listées ci-dessous. Si tel est le cas, vous devez en informer votre médecin. Votre médecin discutera avec vous d’autres méthodes de contraception qui seraient plus adaptées.
· Si vous êtes allergique à l'éthinylestradiol, l'acétate de chlormadinone ou à l'un des autres composants contenus dans ce médicament mentionnés dans la rubrique 6 ;
· si vous avez (ou avez déjà eu) un caillot dans un vaisseau sanguin d’une jambe (thrombose veineuse profonde [TVP]), d’un poumon (embolie pulmonaire [EP]) ou d’autres organes ;
· si vous notez des signes précurseurs d'un caillot sanguin ou d'une inflammation des veines ou d'une embolie comme une douleur lancinante fugace ou une douleur à la poitrine ou une sensation d'oppression dans la poitrine ;
· si vous vous savez atteinte d’un trouble affectant la coagulation sanguine - par exemple, un déficit en protéine C, un déficit en protéine S, un déficit en antithrombine III, une mutation du facteur V de Leiden ou la présence d’anticorps anti-phospholipides ;
· si vous devez être opérée ou si vous êtes alitée pendant une durée prolongée (voir la rubrique « Caillots sanguins ») ;
· si vous avez un diabète ou une glycémie mal contrôlé ;
· si vous avez une hypertension artérielle non contrôlée (valeur constamment supérieure à 140/ 90 mm Hg) ;
· si vous avez déjà eu une crise cardiaque ou un accident vasculaire cérébral (AVC) ;
· si vous avez (ou avez déjà eu) une angine de poitrine (une maladie provoquant des douleurs intenses dans la poitrine et pouvant être le signe précurseur d’une crise cardiaque) ou un accident ischémique transitoire (AIT - symptômes temporaires d’AVC) ;
· si vous avez l’une des maladies suivantes pouvant augmenter le risque de caillot dans les artères :
· diabète sévère avec atteinte des vaisseaux sanguins,
· pression artérielle très élevée,
· taux très élevé de graisses dans le sang (cholestérol ou triglycérides),
· maladie appelée hyperhomocystéinémie.
· si vous avez (ou avez déjà eu) un type de migraine appelé « migraine avec aura » ;
· si vous souffrez d'une atteinte du foie (par exemple, d'origine virale) ou une jaunisse ou tant que les valeurs de la fonction hépatique ne sont pas normalisées ;
· si vous ressentez des démangeaisons sur tout le corps ou avez une maladie des voies biliaires, particulièrement en cas de survenue d'une précédente grossesse ou d'un traitement par estrogènes ;
· en cas d'augmentation du taux sanguin de bilirubine (produit de dégradation des globules rouges) par exemple due à une maladie de naissance (syndrome Dubin-Johnson ou maladie de Rotor) ;
· Si vous avez un méningiome ou si l'on vous a déjà diagnostiqué un méningiome (une tumeur généralement bénigne de la couche de tissu située entre le cerveau et le crâne) ;
· si vous avez une tumeur du foie (ou antécédent) ;
· si vous souffrez de maux d'estomac aigus, si vous présentez un grossissement du foie ou des signes d'hémorragie abdominale ;
· si une porphyrie (affection des pigments sanguins) apparaît pour la première fois ou réapparaît ;
· si vous avez ou avez eu ou si vous suspectez une tumeur maligne hormono-dépendante (par exemple, cancer du sein, des trompes) ;
· si vous avez des troubles graves du métabolisme lipidique ;
· si vous souffrez ou avez souffert d'une maladie inflammatoire du pancréas, accompagnée d'une augmentation importante des triglycérides ;
· si vous souffrez de céphalées anormalement sévères, fréquentes ou prolongées ;
· si vous souffrez soudainement de troubles de la perception (vue ou ouïe) ;
· si vous observez des troubles du mouvement (en particulier, des signes de paralysie) ;
· si vous notez une aggravation d'une épilepsie ;
· si vous souffrez de dépression sévère ;
· si vous souffrez d'un certain type de surdité (otospongiose) qui s'est aggravé lors de grossesses précédentes ;
· si vous observez une absence de règle inexpliquée ;
· si vous observez une croissance anormale de la muqueuse utérine (hyperplasie endométriale) ;
· si vous observez des saignements vaginaux d'origine non déterminée.
N’utilisez pas BELARA si vous souffrez d’hépatite C et que vous prenez des médicaments contenant l’association ombitasvir/paritaprévir/ritonavir, dasabuvir, glécaprévir/pibrentasvir ou sofosbuvir/velpatasvir/voxilaprévir (voir aussi rubrique « Autres médicaments et BELARA »).Si l'un des points ci-dessus vous concerne, stoppez immédiatement BELARA.
Vous ne devez pas prendre BELARA ou l'arrêter immédiatement si vous avez des risques sérieux de troubles de la coagulation.
Avertissements et précautions
Adressez-vous à votre médecin ou pharmacien avant de prendre BELARA 0,03 mg/2 mg comprimé pelliculé.
|
Dans quels cas devez-vous contacter votre médecin ? Consultez un médecin de toute urgence · si vous remarquez de possibles signes d’un caillot sanguin, qui pourraient indiquer que vous avez un caillot sanguin dans une jambe (thrombose veineuse profonde), que vous avez un caillot sanguin dans un poumon (embolie pulmonaire) ou que vous faites une crise cardiaque ou un AVC (voir la rubrique « Caillots sanguins » ci-dessous). Pour la description des symptômes de ces effets indésirables graves, reportez-vous à la rubrique « Comment reconnaître un caillot sanguin ». |
Si vous êtes dans l’une des situations suivantes, informez-en votre médecin.
· Si vous fumez : le tabac augmente le risque d'effets secondaires cardiovasculaires sévères au cours de l'utilisation de contraceptifs hormonaux combinés. Ce risque s'accentue avec l'âge (notamment à partir de 35 ans) et avec l'usage du tabac. Il est vivement recommandé aux fumeuses de plus de 35 ans d'utiliser un autre mode de contraception.
Si le problème apparaît ou s’aggrave pendant l’utilisation de BELARA, vous devez également en informer votre médecin.
· Si vous présentez des symptômes d'angioœdème tels qu'un gonflement du visage, de la langue et/ou de la gorge et/ou des difficultés à avaler ou de l'urticaire pouvant entraîner des difficultés respiratoires, contactez immédiatement un médecin. Les produits contenant des œstrogènes peuvent provoquer ou aggraver les symptômes d’un angioœdème héréditaire et acquis.
· Si vous avez une hypertension artérielle, une hyperlipidémie, un surpoids ou un diabète (voir rubrique Contre-indications et Autres maladies), le risque d'effets indésirables graves (tels que crise cardiaque, embolie, accident vasculaire cérébral, ou tumeurs hépatiques) augmente ;
· si vous êtes atteinte de la maladie de Crohn ou de rectocolite hémorragique (maladies inflammatoires chroniques des intestins) ;
· si vous avez un lupus érythémateux disséminé (LED) (une maladie qui affecte votre système de défenses naturelles) ;
· si vous avez un syndrome hémolytique et urémique (SHU) (un trouble de la coagulation sanguine qui entraîne une défaillance des reins) ;
· si vous avez une drépanocytose (une maladie héréditaire touchant les globules rouges) ;
· si vous avez des taux élevés de graisses dans le sang (hypertriglycéridémie) ou des antécédents familiaux de ce trouble. L’hypertriglycéridémie a été associée à une augmentation du risque de pancréatite (inflammation du pancréas) ;
· si vous devez être opérée ou si vous êtes alitée pendant une durée prolongée (reportez-vous à la rubrique 2, « Caillots sanguins ») ;
· si vous venez juste d’accoucher, vous êtes exposée à un risque augmenté de caillots sanguins. Vous devez demander à votre médecin combien de temps après l’accouchement vous pouvez commencer à prendre BELARA ;
· si vous avez une inflammation des veines situées sous la peau (thrombophlébite superficielle) ;
· si vous avez des varices.
CAILLOTS SANGUINS
L’utilisation d’un contraceptif hormonal combiné tel que BELARA augmente le risque d’apparition d’un caillot sanguin en comparaison à une non-utilisation. Dans de rares cas, un caillot sanguin peut bloquer des vaisseaux sanguins et provoquer de graves problèmes.
Les caillots sanguins peuvent se former :
· dans les veines (on parle alors de « thrombose veineuse » ou de « thrombo-embolie veineuse » [TEV]) ;
· dans les artères (on parle alors de « thrombose artérielle » ou de « thrombo-embolie artérielle » [TEA]).
Le rétablissement, suite à des caillots sanguins, n’est pas toujours complet. Dans de rares cas, ils peuvent entraîner des séquelles graves et durables et, dans de très rares cas, ils peuvent être fatals.
Il est important de garder à l’esprit que le risque global de caillot sanguin dû à BELARA est faible.
COMMENT RECONNAÎTRE UN CAILLOT SANGUIN
Consultez un médecin de toute urgence si vous remarquez l’un des signes ou symptômes suivants.
|
Présentez-vous l’un de ces signes ? |
Il peut éventuellement s’agir de : |
|
· gonflement d’une jambe ou le long d’une veine de la jambe ou du pied, en particulier s’il s’accompagne de :
|
Thrombose veineuse profonde |
|
· apparition soudaine et inexpliquée d’un essoufflement ou d’une respiration rapide, · toux soudaine sans cause apparente, avec parfois des crachats de sang, · douleur aiguë dans la poitrine, qui peut s’accentuer en cas de respiration profonde, · étourdissements ou sensations vertigineuses sévères, · battements de cœur rapides ou irréguliers, · douleur intense dans l’estomac. En cas de doute, consultez un médecin car certains de ces symptômes, comme la toux ou l’essoufflement, peuvent être pris à tort pour les signes d’une maladie moins sévère telle qu’une infection respiratoire (p.ex. un simple rhume). |
Embolie pulmonaire |
|
Symptômes apparaissant le plus souvent dans un seul œil : · perte immédiate de la vision ou vision trouble sans douleur pouvant évoluer vers une perte de la vision. |
Thrombose veineuse rétinienne (caillot sanguin dans l’œil) |
|
· douleur, gêne, pression, lourdeur dans la poitrine ; · sensation d’oppression ou d’encombrement dans la poitrine, le bras ou sous le sternum ; · sensation d’encombrement, d’indigestion ou de suffocation ; · sensation de gêne dans le haut du corps irradiant vers le dos, la mâchoire, la gorge, le bras et l’estomac ; · transpiration, nausées, vomissements ou sensations vertigineuses ; · faiblesse, anxiété ou essoufflement extrêmes ; · battements de cœur rapides ou irréguliers ; |
Crise cardiaque |
|
· apparition soudaine d’une faiblesse ou d’un engourdissement au niveau du visage, d’un bras ou d’une jambe, en particulier d’un côté du corps ; · apparition soudaine d’une confusion, de difficultés à parler ou à comprendre ; · apparition soudaine de difficultés à voir d’un œil ou des deux yeux ; · apparition soudaine de difficultés à marcher, de sensations vertigineuses, d’une perte d’équilibre ou de coordination ; · maux de tête soudains, sévères ou prolongés, sans cause connue ; · perte de conscience ou évanouissement avec ou sans crise convulsive. Parfois, les symptômes de l’AVC peuvent être de courte durée, avec un rétablissement presque immédiat et complet, mais vous devez tout de même consulter un médecin de toute urgence car vous pourriez être exposée au risque d’un nouvel AVC. |
Accident vasculaire cérébral (AVC) |
|
· gonflement et coloration légèrement bleutée d’une extrémité ; · douleur intense dans l’estomac (« abdomen aigu ») |
Caillots sanguins bloquant d’autres vaisseaux sanguins. |
CAILLOTS SANGUINS DANS UNE VEINE
Que peut-il se passer si un caillot sanguin se forme dans une veine ?
· Un lien a été établi entre l’utilisation de contraceptifs hormonaux combinés et l’augmentation du risque de caillots sanguins dans les veines (thrombose veineuse). Cependant, ces effets indésirables sont rares. Le plus souvent, ils surviennent pendant la première année d’utilisation d’un contraceptif hormonal combiné.
· Lorsqu’un caillot sanguin se forme dans une veine d’une jambe ou d’un pied, il peut provoquer une thrombose veineuse profonde (TVP).
· Si le caillot sanguin migre de la jambe vers le poumon, il peut provoquer une embolie pulmonaire.
· Dans de très rares cas, un caillot peut se former dans une veine d’un autre organe, comme l’œil (thrombose veineuse rétinienne).
À quel moment le risque d’apparition d’un caillot sanguin dans une veine est-il le plus élevé ?
Le risque d’apparition d’un caillot sanguin dans une veine est maximal pendant la première année d’utilisation d’un contraceptif hormonal combiné pris pour la première fois. Le risque peut également être augmenté lorsque vous recommencez à prendre un contraceptif hormonal combiné (le même produit ou un produit différent) après une interruption de 4 semaines ou plus.
Après la première année, le risque diminue mais reste toujours légèrement plus élevé que si vous n’utilisiez pas de contraceptif hormonal combiné.
Lorsque vous arrêtez de prendre BELARA, le risque d’apparition de caillot sanguin revient à la normale en quelques semaines.
Quel est le risque d’apparition d’un caillot sanguin ?
Le risque dépend de votre risque de base de TEV et du type de contraceptif hormonal combiné que vous prenez.
Le risque global de caillot sanguin dans une jambe ou un poumon (TVP ou EP) associé à BELARA est faible.
· Sur 10 000 femmes qui n’utilisent aucun contraceptif hormonal combiné et qui ne sont pas enceintes, environ 2 développeront un caillot sanguin sur une période d’un an.
· Sur 10 000 femmes qui utilisent un contraceptif hormonal combiné contenant du lévonorgestrel, de la noréthistérone ou du norgestimate, environ 5 à 7 développeront un caillot sanguin sur une période d’un an.
· Sur 10 000 femmes qui utilisent un contraceptif hormonal combiné contenant de la chlormadinone tel que BELARA, environ 6 à 9 développeront un caillot sanguin sur une période d’un an.
· Le risque d’apparition d’un caillot sanguin variera selon vos antécédents médicaux personnels (voir « Facteurs augmentant le risque de caillot sanguin » ci-dessous).
|
|
Risque d’apparition d’un caillot sanguin sur une période d’un an |
|
Femmes qui n’utilisent pas de contraceptif hormonal combiné (pilule/patch/anneau) et qui ne sont pas enceintes |
Environ 2 femmes sur 10 000 |
|
Femmes qui utilisent une pilule contraceptive hormonale combinée contenant du lévonorgestrel, de la noréthistérone ou du norgestimate |
Environ 5 à 7 femmes sur 10 000 |
|
Femmes qui utilisent BELARA |
Environ 6 à 9 femmes sur 10 000 |
Si vous notez des maux de tête, importants et inhabituels, qui peuvent faire craindre la survenue de troubles circulatoires cérébraux, consultez votre médecin dès que possible. Il pourra vous conseiller d'interrompre BELARA immédiatement.
Facteurs augmentant le risque de caillot sanguin dans une veine
Le risque de caillot sanguin associé à BELARA est faible mais certaines situations peuvent augmenter ce risque. Le risque sera plus élevé :
· si vous avez un surpoids important (indice de masse corporelle [IMC] supérieur à 30 kg/m2) ;
· si l’un des membres de votre famille proche a eu un caillot sanguin dans une jambe, un poumon ou un autre organe à un âge relativement jeune (p. ex. avant l’âge de 50 ans). Si tel est le cas, vous pourriez être atteinte d’un trouble héréditaire de la coagulation sanguine ;
· si vous devez être opérée ou si vous êtes alitée pendant une période prolongée en raison d’une blessure ou d’une maladie, ou si votre jambe est immobilisée (p. ex. plâtre). Il pourra être nécessaire d’interrompre l’utilisation de BELARA plusieurs semaines avant l’opération chirurgicale et/ou tant que votre mobilité est réduite. Si vous devez arrêter d’utiliser BELARA, demandez à votre médecin à quel moment vous pourrez recommencer à l’utiliser.
· avec l’âge (en particulier au-delà de 35 ans) ;
· si vous avez accouché dans les semaines précédentes.
Plus vous cumulez ces situations, plus le risque d’apparition d’un caillot sanguin augmente.
Les voyages en avion (de plus de 4 heures) peuvent augmenter temporairement le risque de caillot sanguin, en particulier si vous présentez déjà certains des autres facteurs listés.
Il est important de prévenir votre médecin si vous êtes concernée par l’une de ces situations, même si vous n’en êtes pas certaine. Votre médecin pourra décider qu’il est nécessaire d’arrêter le traitement par BELARA.
Si l’une des situations ci-dessus évolue pendant la période où vous utilisez BELARA, par exemple si un membre de votre famille proche développe une thrombose sans raison connue ou si vous prenez beaucoup de poids, parlez-en à votre médecin.
CAILLOTS SANGUINS DANS UNE ARTÈRE
Que peut-il se passer si un caillot sanguin se forme dans une artère ?
Comme un caillot sanguin dans une veine, un caillot dans une artère peut provoquer de graves problèmes. Par exemple, il peut provoquer une crise cardiaque ou un accident vasculaire cérébral (AVC).
Facteurs augmentant le risque de caillot sanguin dans une artère
Il est important de noter que le risque de crise cardiaque ou d’AVC lié à l’utilisation de BELARA est très faible mais peut augmenter :
· avec l’âge (au-delà de 35 ans) ;
· si vous fumez. Lors de l’utilisation d’un contraceptif hormonal combiné tel que BELARA, il est conseillé d’arrêter de fumer. Si vous ne parvenez pas à arrêter de fumer et si vous êtes âgée de plus de 35 ans, votre médecin pourra vous conseiller d’utiliser une méthode de contraception différente ;
· si vous êtes en surpoids ;
· si vous avez une pression artérielle élevée ;
· si un membre de votre famille proche a déjà eu une crise cardiaque ou un AVC à un âge relativement jeune (avant l’âge de 50 ans). Si tel est le cas, le risque que vous ayez une crise cardiaque ou un AVC pourrait également être plus élevé ;
· si vous, ou un membre de votre famille proche, avez un taux de graisses élevé dans le sang (cholestérol ou triglycérides) ;
· si vous avez des migraines, en particulier des migraines avec aura ;
· si vous avez des problèmes cardiaques (maladie de la valve cardiaque, trouble du rythme appelé fibrillation auriculaire) ;
· si vous êtes diabétique.
Si vous cumulez plusieurs de ces situations ou si l’une d’entre elles est particulièrement sévère, le risque d’apparition d’un caillot sanguin peut être encore plus élevé.
Si l’une des situations ci-dessus évolue pendant la période où vous utilisez BELARA, par exemple si vous commencez à fumer, si un membre de votre famille proche développe une thrombose sans raison connue ou si vous prenez beaucoup de poids, parlez-en à votre médecin.
Tumeurs
Certaines études suggèrent qu'il existe un facteur de risque de cancer du col de l'utérus chez les utilisatrices de contraceptifs hormonaux combinés(CHC) à long terme qui ont présenté une infection du col de l'utérus par un virus sexuellement transmissible (papillomavirus). Cependant, d'autres facteurs pourraient intervenir (par exemple, le nombre de partenaires, une contraception mécanique).
Des études ont rapporté une légère augmentation du risque de cancer du sein chez les femmes sous CHC. Cette majoration du risque disparaît progressivement au cours des 10 ans qui suivent l'arrêt des CHC pour revenir au risque lié à l'âge. Le cancer du sein étant rare chez la femme de moins de 40 ans, le nombre plus élevé de cancers du sein diagnostiqués chez les utilisatrices habituelles ou nouvelles utilisatrices de CHC est faible par rapport au risque global de cancer du sein.
Dans de rares cas, des tumeurs bénignes du foie, et dans de plus rares cas encore, des tumeurs malignes du foie ont été rapportées. Dans de rares cas isolés, ces tumeurs ont conduit à une hémorragie intra abdominale mettant en jeu le pronostic vital. En cas de douleurs abdominales sévères qui ne disparaissent pas spontanément, consultez votre médecin.
L'utilisation de l'acétate de chlormadinone a été associée au développement d'une tumeur généralement bénigne de la couche de tissu située entre le cerveau et le crâne (méningiome). Le risque augmente en particulier lorsque vous l'utilisez à des doses élevées pendant une longue durée (plusieurs années). Si un méningiome vous est diagnostiqué, votre médecin arrêtera votre traitement par BELARA (voir rubrique " Ne prenez jamais BELARA"). Si vous remarquez des symptômes tels que des modifications de la vision (par exemple, vision double ou floue), une perte d'audition ou des bourdonnements d'oreilles, une perte d'odorat, des maux de tête qui s'aggravent avec le temps, des pertes de mémoire, des crises convulsives, une faiblesse dans les bras ou les jambes, vous devez en informer immédiatement votre médecin.
Troubles psychiatriques
Certaines femmes qui utilisent des contraceptifs hormonaux, dont BELARA, ont fait état d'une dépression ou d'un état dépressif. La dépression peut être grave et peut parfois donner lieu à des idées suicidaires. Si vous présentez des changements d'humeur et des symptômes dépressifs, sollicitez les conseils de votre médecin dès que possible.
Autres maladies
Un certain nombre de femmes présente une légère augmentation de la pression artérielle sous contraception hormonale. Si votre pression artérielle augmente de façon importante sous BELARA, votre médecin vous proposera d'arrêter BELARA et vous prescrira un traitement pour abaisser la pression artérielle. Dès que votre pression artérielle reviendra à la normale, vous pourrez reprendre BELARA.
Si vous avez souffert d'herpès apparu lors d'une grossesse antérieure, celui-ci peut réapparaître lors de la prise d'un contraceptif hormonal.
Si vous avez des troubles lipidiques ou des antécédents familiaux de ces troubles (de type hypertriglycéridémie), vous avez un risque accru d'inflammation du pancréas. Si vous avez des troubles de la fonction hépatique, votre médecin vous conseillera d'arrêter BELARA jusqu'à ce que les paramètres hépatiques redeviennent normaux. Si vous avez souffert de jaunisse lors d'une grossesse antérieure ou d'une prise antérieure de contraceptif hormonal et que celle-ci réapparait, le médecin vous conseillera d'arrêter BELARA.
Votre médecin vous suivra régulièrement si vous êtes diabétique avec un bon contrôle de la glycémie. Il pourrait être nécessaire d'adapter votre traitement anti-diabétique.
Des taches brunes anormales peuvent apparaître sur votre peau (chloasma) notamment si elles étaient déjà apparues lors d'une grossesse. Si vous avez cette prédisposition, vous devez éviter l'exposition au soleil et aux ultra-violets sous BELARA.
Maladies pouvant s'aggraver
Un suivi médical particulier est également nécessaire dans les cas suivants :
· épilepsie ;
· sclérose en plaque ;
· crampes sévères (tétanie) ;
· migraine (voir rubrique Contre-indications) ;
· asthme ;
· insuffisance cardiaque ou rénale (voir rubrique Contre- indications) ;
· chorée mineure ;
· diabète (voir rubrique Contre-indications et Autres maladies) ;
· maladie du foie (voir rubrique Contre-indications) ;
· désordres lipidiques (voir rubrique Contre-indications) ;
· maladies auto-immunes (y compris lupus érythémateux disséminé) ;
· obésité ;
· hypertension artérielle (voir rubrique Contre-indications) ;
· endométriose (il s'agit du tissu qui tapisse la cavité utérine (appelé endomètre), et qui se fixe en dehors de la cavité utérine (voir rubrique Contre-indications) ;
· inflammation des veines, varices (voir rubrique Contre- indications) ;
· troubles de la coagulation (voir rubrique Contre-indications) ;
· maladie du sein (mastopathie) ;
· antécédent de tumeur bénigne de l'utérus (fibrome) ;
· herpès lors d'une précédente grossesse ;
· dépression ;
· maladies inflammatoires chroniques intestinales (maladie de Crohn, colite ulcérative).
Consultez votre médecin si vous avez ou avez eu l'une de ces maladies ou si celle-ci apparaît sous BELARA.
Efficacité
En cas d'oubli du contraceptif, ou de vomissements ou de diarrhées ( voir rubrique 3. « Comment prendre BELARA », ou lors de la prise concomitante de médicaments, l'efficacité contraceptive peut être modifiée (voir rubrique « Interactions médicamenteuses »). Dans de rares cas, des désordres métaboliques peuvent modifier l'efficacité contraceptive.
Même si vous prenez correctement un contraceptif hormonal, son efficacité n'est pas de 100%.
Saignements irréguliers
Des saignements irréguliers (« spottings » ou métrorragies) peuvent survenir sous contraceptifs hormonaux, en particulier au cours des premiers mois. Si ces saignements persistent ou apparaissent pour la première fois après une utilisation prolongée, consultez votre médecin.
Les saignements peuvent être aussi un signe de réduction de l'effet contraceptif. Dans certains cas, les saignements peuvent être absents après la prise de BELARA pendant 21 jours. Si vous avez pris BELARA selon les recommandations de la rubrique « Comment prendre BELARA », il est peu probable que vous soyez enceinte. Si vous n'avez pas pris BELARA selon les recommandations de la rubrique « comment prendre BELARA », il convient de s'assurer de l'absence de grossesse avant de poursuivre la contraception.
Enfants et adolescents
BELARA est indiqué seulement après l’apparition des premières menstruations. La sécurité et l'efficacité de BELARA chez les adolescentes de moins de 16 ans n'ont pas été établies.
Patientes âgées
BELARA n’est pas indiqué après la ménopause.
Autres médicaments et BELARA 0,03 mg/2 mg comprimé pelliculé
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
N’utilisez pas BELARA si vous souffrez d’hépatite C et que vous prenez des médicaments contenant l’association ombitasvir/paritaprévir/ritonavir, dasabuvir, glécaprévir/pibrentasvir ou sofosbuvir/ velpatasvir/voxilaprévir, car cela ces produits pourraient entraîner des élévations aux tests sanguins de la fonction hépatique (élévation de l’enzyme hépatique ALAT). Votre médecin voues prescrira une autre méthode contraceptive à prendre avant de commencer de prendre ces médicaments.
BELARA peut être repris 2 semaines après la fin de ce traitement. Voir rubrique "Ne prenez pas BELARA".
Certains médicaments peuvent avoir une influence sur les concentrations sanguines de BELARA et peuvent réduire son efficacité à prévenir une grossesse ou peuvent provoquer des saignements entre les règles. Ceux-ci incluent les médicaments pour le traitement de :
· L'épilepsie (par exemple, les barbituriques, la carbamazépine, la phénytoïne, le topiramate, le felbamate, l'oxcarbazépine, le barbexaclone, la primidone),
· La tuberculose (par exemple, la rifampicine, la rifabutine),
· Les troubles du sommeil (le modafinil),
· du VIH et de l'hépatite C (appelés inhibiteurs de la protéase et inhibiteurs non nucléosidiques de la transcriptase inverse tel que le ritonavir, le névirapine, l'efavirenz),
· d'infections dus à des champignons (la griséofulvine),
· L'hypertension artérielle pulmonaire (le bosentan),
· les médicaments à base de Millepertuis (hypericum perforatum). Si vous voulez prendre une préparation à base de Millepertuis alors que vous prenez déjà BELARA, vous devez d'abord commercer par consulter votre médecin.
Les médicaments qui stimulent la motricité intestinale (par ex. métoclopramide) et le charbon actif peuvent modifier l'absorption des substances actives de BELARA et en réduire ses effets
Si vous prenez l'un de ces médicaments, vous devez ajouter une autre méthode contraceptive mécanique (par exemple, préservatifs) pendant toute la durée du traitement concomitant et 28 jours après la fin de ce traitement. Si le traitement concomitant continue après la fin de la plaquette de contraceptif, vous devez commencer la nouvelle plaquette dès la fin de la plaquette, sans arrêt de 7 jours.
Si un traitement au long cours est nécessaire, vous devez utiliser des méthodes contraceptives non hormonales. Demandez conseil à votre médecin ou votre pharmacien.
Des interactions entre BELARA et d'autres médicaments peuvent augmenter ou accentuer les effets indésirables de BELARA. Les médicaments suivants peuvent avoir un effet défavorable sur la tolérance de BELARA :
· acide ascorbique (un conservateur aussi connu sous le nom de vitamine C),
· paracétamol (soulage la douleur et combat la fièvre),
· atorvastatine (diminue les taux de cholestérol élevés),
· troléandomycine (antibiotique),
· antifongiques imidazolés (par exemple : le fluconazole utilisé dans le traitement des infection fongiques),
· indinavir (utilisé dans le traitement du VIH).
BELARA peut modifier l'effet d'autres médicaments. L’efficacité ou la tolérance des médicaments suivants peut être diminuée par BELARA :
· certaines benzodiazépines, par exemple le diazépam (pour le traitement des troubles du sommeil),
· la ciclosporine (un médicament qui inhibe le système immunitaire),
· la théophylline (traitement des symptômes de l'asthme),
· les corticostéroïdes, par exemple la prednisolone (connu sous le nom d'anti-inflammatoire stéroïdien utilisés dans le traitement du lupus, de l'arthrite, du psoriasis),
· la lamotrigine (traitement de l'épilepsie),
· le clofibrate (abaissement du taux de cholestérol élevé),
· le paracétamol (soulageant la douleur et combat la fièvre),
· la morphine (un analgésique puissant - soulageant la douleur),
· le lorazépam (utilisé pour traiter l'anxiété).
Veuillez également lire les notices des autres préparations prescrites.
Prévenez votre médecin si vous prenez de l'insuline ou d'autres médicaments destinés à abaisser votre glycémie. Il peut être nécessaire de modifier le dosage de ces médicaments.
Il en est de même si vous avez pris une de ces substances actives avant de commencer à prendre BELARA.
Les modifications demeurent généralement dans les limites de la normale. Avant d’effectuer une prise de sang, prévenez votre médecin que vous prenez BELARA.
Grossesse et allaitement
En cas de grossesse, BELARA n'a pas lieu de vous être prescrit.
En cas de survenue d'une grossesse BELARA arrêtez immédiatement le traitement. La découverte d'une grossesse sous BELARA ne nécessite pas une interruption de la grossesse.
En cas d'allaitement, l'utilisation de BELARA est déconseillée, en raison d'un très faible passage des substances actives dans le lait maternel. Les contraceptifs hormonaux tels que BELARA doivent être démarrés après arrêt de l’allaitement. BELARA peut influer sur la quantité et la composition du lait maternel.
Conduite de véhicules et utilisation de machines
Les CHC ne sont pas connus pour avoir d'effet négatif sur l'aptitude à conduire des véhicules ou à utiliser des machines.
BELARA 0,03 mg/2 mg comprimé pelliculé contient du lactose.
Si votre médecin vous a informée d'une intolérance à certains sucres, contactez-le avant de prendre ce médicament.
3. COMMENT PRENDRE BELARA 0,03 mg/2 mg comprimé pelliculé ?
Mode d'administration
Voie orale.
Comment et quand prendre BELARA 0,03 mg/2 mg, comprimé pelliculé ?
1 comprimé par jour au même moment de la journée, pendant 21 jours consécutifs, sans oubli, avec un arrêt de 7 jours entre deux plaquettes.
Sortez le comprimé correspondant au jour de la semaine (par ex. Dim. pour dimanche) et avalez-le sans le mâcher. Prenez ensuite un autre comprimé chaque jour en suivant la flèche si possible à la même heure, de préférence le soir. Respectez toujours un intervalle de 24 heures entre 2 prises. Les jours imprimés sur la plaquette vous permettent de savoir chaque jour si vous avez bien pris le comprimé ce jour-là.
Prenez un comprimé chaque jour, pendant 21 jours consécutifs. Pendant les 7 jours suivants, ne prenez pas de comprimé. En général, les hémorragies de privation (règles) commenceront 2 à 4 jours après la prise du dernier comprimé de la plaquette.
Après cette interruption libre de 7 jours, commencez à prendre les comprimés de la nouvelle plaquette, même si les règles ne sont pas terminées.
Quand démarrer BELARA 0,03 mg/2 mg comprimé pelliculé ?
Si vous n'avez pas pris de contraception hormonale durant le mois précédent :
Prendre le 1er comprimé de BELARA le premier jour du cycle.
La contraception commence le premier jour d'administration et continue pendant l'interruption des sept jours.
Si vos règles ont déjà commencé, prendre le premier comprimé entre le 2ème et 5ème jour des règles, qu'elles soient finies ou non. Cependant, dans ce cas, vous devez utiliser une méthode contraceptive mécanique complémentaire pendant les 7 premiers jours (règle des 7 jours).
Au-delà de 5 jours de règles, vous devez attendre votre prochain cycle avant de commencer à prendre BELARA.
Si vous changez de contraceptif hormonal combiné :
Le 1er comprimé de BELARA est à prendre le jour suivant la fin de la période sans prise de comprimé ou la fin de la prise des comprimés placebos de votre précédente contraception hormonale combinée.
Si vous utilisiez une contraception progestative :
Si vous utilisez une contraception progestative orale, les hémorragies de privation (règles) peuvent être absentes. Commencez BELARA le lendemain de l'arrêt de la pilule progestative. Dans ce cas, vous devez utiliser une méthode contraceptive mécanique complémentaire pendant les 7 premiers jours.
Si vous utilisiez une méthode par injection ou par implant :
Débutez BELARA le jour prévu du retrait de l'implant ou le jour prévu pour la nouvelle injection. Dans ce cas, il est nécessaire d'utiliser une méthode contraceptive mécanique complémentaire pendant les 7 premiers jours.
Après une fausse couche, un avortement dans les 3 premiers mois de la grossesse :
Vous pouvez commencer BELARA immédiatement. Dans ce cas, aucune méthode contraceptive mécanique complémentaire n'est nécessaire.
Après un accouchement ou un avortement dans les 3 à 6 mois de la grossesse:
Si vous n'allaitez pas, vous pouvez commencer BELARA dans les 21 à 28 jours après la naissance. Il n'est pas nécessaire d'utiliser une méthode contraceptive complémentaire.
Si plus de 28 jours se sont écoulés depuis l'accouchement, une contraception mécanique complémentaire pendant les 7 premiers jours est nécessaire.
Si des rapports sexuels ont déjà eu lieu, il convient d'éliminer la présence d'une grossesse ou d'attendre les premières règles avant de commencer BELARA.
Vous ne devez pas prendre BELARA si vous allaitez (voir rubrique grossesse et allaitement).
Combien de temps pouvez-vous prendre BELARA ?
Vous pouvez prendre BELARA aussi longtemps que vous le souhaitez si votre santé vous le permet (voir rubrique « Contre-indications » et « Précautions d’emploi »). A l'arrêt de BELARA, le début des hémorragies de privation pourra être retardé d'environ 1 semaine.
Que devez-vous faire en cas de vomissements ou de diarrhée pendant la prise de BELARA 0,03 mg/2 mg comprimé pelliculé ?
En cas de vomissement ou de diarrhée dans les 4 heures suivant la prise de BELARA, il est possible que les substances actives de BELARA ne soient pas complètement absorbées. Cette situation est comparable à l’oubli d’un comprimé, et vous devez prendre un nouveau comprimé d’une nouvelle plaquette immédiatement. Si possible il faut prendre le nouveau comprimé dans les 12 heures qui suivent la prise du dernier comprimé, puis poursuivre la prise de BELARA, ou si plus de 12 heures se sont écoulées voir rubrique 3 « si vous avez oublié de prendre BELARA » ou contacter votre médecin.
Si vous avez pris plus de BELARA 0,03 mg/2 mg comprimé pelliculé que vous n’auriez dû :
Il n'y a pas de signe caractéristique d'intoxication après la prise de plusieurs comprimés en une seule fois.
Nausées, vomissements et, chez les jeunes filles, de petits saignements vaginaux peuvent apparaître. Dans de tels cas, consultez un médecin. Si nécessaire, il vérifiera les paramètres sanguins et la fonction hépatique.
Si vous oubliez de prendre BELARA 0,03 mg/2 mg comprimé pelliculé :
· Si l'oubli d'un comprimé est constaté dans les 12 heures qui suivent l'heure habituelle de la prise, prenez immédiatement le comprimé oublié, et poursuivez la prise normalement en prenant le comprimé suivant à l'heure habituelle. Aucun autre moyen contraceptif n'est nécessaire.
· Si l'oubli d'un comprimé est constaté plus de 12 heures après l'heure normale de la prise, l'efficacité de BELARA n'est plus assurée. Dans ce cas, prendre immédiatement le comprimé oublié et poursuivre la plaquette normalement même si cela entraîne la prise de 2 comprimés le même jour. Cependant, vous devez utiliser un autre moyen de contraception (type préservatif) pendant les 7 jours suivants. Si pendant ces sept jours vous terminez la plaquette commencée, commencez immédiatement une nouvelle plaquette de BELARA, c'est à dire que vous ne devez pas faire d'arrêt entre les deux plaquettes (règle des sept jours). Vous n'aurez probablement pas d'hémorragie de privation jusqu'à la fin de la plaquette. Mais quelques saignements ou spottings pourront survenir pendant la prise de la nouvelle plaquette.
Le risque de grossesse augmente avec le nombre de comprimés oubliés. Si un ou les comprimés oubliés correspondent à la première semaine du cycle et si un rapport a eu lieu dans la semaine qui précède l'oubli des comprimés, la probabilité d'une grossesse doit être envisagée. Ceci est également le cas si vous oubliez un ou plusieurs comprimés et que vous n'avez pas vos règles durant l'intervalle libre qui suit. Dans tous les cas, consultez votre médecin.
Si vous voulez retarder les hémorragies de privation
Même si cela n'est pas recommandé, vous pouvez retarder les hémorragies de privation (règles) en commençant de suite une nouvelle plaquette sans intervalle libre de 7 jours. Il peut y avoir des spottings et des saignements irréguliers pendant la prise de la seconde plaquette. A la fin de la seconde plaquette, observez l'intervalle libre de 7 jours puis enchaînez avec une nouvelle plaquette de BELARA.
Demandez conseil à votre médecin avant de décaler les hémorragies de privation.
Si vous voulez décaler le premier jour des hémorragies de privation
Si vous prenez les comprimés selon la notice, la période d'hémorragies de privation commencera pendant l'intervalle libre des 7 jours. Vous pouvez décaler ce jour en raccourcissant l'intervalle libre (ne jamais l'augmentez). Par exemple, si l'intervalle libre démarre un vendredi et que vous le modifier au mardi (soit 3 jours plus tôt), vous devrez commencer la nouvelle plaquette 3 jours plus tôt que prévu.
Si vous réduisez l'intervalle libre (par exemple, de 3 jours ou moins), il se peut que vous n'ayez pas d'hémorragie de privation pendant l'intervalle libre mais des spottings (gouttelettes ou taches de sang) et des saignements irréguliers éventuels.
Si vous n'êtes pas sûre de la manière de procéder, demandez conseil à votre médecin.
Si vous arrêtez de prendre BELARA 0,03 mg/2 mg comprimé pelliculé :
Si vous arrêtez de prendre BELARA, vos ovaires reprendront leur activité normale et vous pourrez démarrer une grossesse.
Si vous avez d'autres questions sur l'utilisation de ce médicament, demandez plus d'informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Comme tous les médicaments, ce médicament peut provoquer des effets indésirables, mais ils ne surviennent pas systématiquement chez tout le monde. Si vous ressentez un quelconque effet indésirable, en particulier si l’effet est sévère et persistant, ou si vous remarquez une modification de votre état de santé qui pourrait selon vous être due à BELARA, informez-en votre médecin.
Contactez immédiatement un médecin si vous présentez l'un des symptômes suivants d’angioœdème : gonflement du visage, de la langue et/ou de la gorge et/ou difficulté à avaler ou urticaire potentiellement accompagnée de difficultés à respirer (voir également la rubrique "Mises en garde et précautions").
Il existe une augmentation du risque de caillots sanguins dans les veines (thrombo-embolie veineuse [TEV]) ou dans les artères (thrombo-embolie artérielle [TEA]) chez toutes les femmes qui prennent des contraceptifs hormonaux combinés. Pour plus de précisions sur les différents risques associés à la prise de contraceptifs hormonaux combinés, reportez-vous à la rubrique 2, « Quelles sont les informations à connaître avant de prendre BELARA ».
Les effets indésirables et leur fréquence sont rapportés ci-dessous :
Très fréquent (pouvant concerner plus de 1 personne sur 10) : nausées, écoulements vaginaux, douleurs lors des règles, ou absence de règles.
Fréquent (pouvant concerner jusqu’à 1 personne sur 10) : dépression, nervosité, irritabilité, vertiges, migraines (et/ou aggravation), troubles visuels, vomissements, acné, sensation de lourdeur, douleurs abdominales basses, fatigue, œdème, prise de poids, augmentation de la tension artérielle.
Peu fréquent (pouvant concerner entre 1 personne sur 100 et 1 sur 1 000) : mycoses vaginales, changements bénins des tissus conjonctifs des seins , hypersensibilité médicamenteuse notamment réactions allergiques cutanées, modification du taux lipidique incluant hypertriglycéridémie, diminution de la libido, maux d'estomac, ballonnements, diarrhées, problèmes de pigmentation de la peau, apparition de taches brunes sur le visage, perte de cheveux, sécheresse cutanée, tendance à la sudation, mal de dos, problèmes musculaires, écoulement mammaire.
Rares (pouvant concerner entre 1 personne sur 1 000 et 1 sur 10 000) : inflammation vaginale, augmentation de l'appétit, conjonctivite, irritation des yeux par les lentilles de contact, troubles de l'audition, acouphène, hypertension, hypotension, collapsus, varices, urticaire, eczéma, érythème, prurit, aggravation de psoriasis, hirsutisme, hypertrophie mammaire, règles plus longues et plus abondantes, syndrome prémenstruel (troubles physiques et émotionnels avant les règles), caillots sanguins dans une veine ou une artère, par exemple :
· dans une jambe ou un pied (thrombose veineuse profonde, TVP),
· dans un poumon (embolie pulmonaire, EP),
· crise cardiaque,
· accident vasculaire cérébral (AVC),
· mini-AVC ou symptômes temporaires de type AVC, connus sous le nom d’accident ischémique transitoire (AIT),
· caillots sanguins dans le foie, l’estomac/l’intestin, les reins ou un œil.
Le risque d’apparition d’un caillot sanguin peut être plus élevé si vous présentez certains autres facteurs qui augmentent ce risque (voir rubrique 2 pour plus d’informations sur les facteurs augmentant le risque de caillots sanguins et les symptômes d’un caillot sanguin).
Très rares (pouvant concerner moins de 1 personne sur 10 000) : érythème noueux.
Des effets indésirables suivants ont aussi été rapportés associés aux substances actives éthinylestradiol et acétate de chlormadinone dans l’utilisation post marketing : faiblesse et réactions allergiques, y compris le gonflement des couches plus profondes de la peau (œdème de Quincke).
Les contraceptifs hormonaux combinés dont BELARA, sont aussi associés à une augmentation du risque de maladies graves et d'effets indésirables :
· Risque d'obstruction des veines ou des artères (voir rubrique Précautions d'emploi) ;
· Risque de maladies des voies biliaires (voir rubrique Précautions d’emploi) ;
· Risque de tumeurs (par exemple, tumeurs du foie qui peuvent être dans des cas isolés des saignements dans la cavité abdominale menaçant le pronostic vital, cancer du col de l'utérus et du sein) (voir rubrique Précautions d’emploi) ;
· Aggravation des maladies inflammatoires de l'intestin, maladie de Crohn, colite ulcérative (voir rubrique Précautions d’emploi").
Lire attentivement la rubrique « Précautions d’emploi » et si nécessaire, veuillez en informer votre médecin ou votre pharmacien immédiatement.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance. Site internet : https://signalement.social-sante.gouv.fr.
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER BELARA 0,03 mg/2 mg comprimé pelliculé ?
Tenir ce médicament hors de la vue et de la portée des enfants.
A conserver à une température ne dépassant pas 30°C.
N’utilisez pas ce médicament après la date de péremption indiquée sur la boite et la plaquette. La date de péremption fait référence au dernier jour de ce mois.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d'éliminer les médicaments les médicaments que vous n'utilisez plus. Ces mesures contribueront à protéger l'environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient BELARA 0,03 mg/2 mg comprimé pelliculé
· Les substances actives sont :
Acétate de chlormadinone .......................................................................................... 2,000 mg
Ethinylestradiol .......................................................................................................... 0,030 mg
· Les autres composants sont :
Noyau : lactose monohydraté, amidon de maïs, povidone K30, stéarate de magnésium.
Pelliculage : hypromellose, lactose monohydraté, macrogol 6000, propylène glycol, talc, dioxyde de titane (E171), oxyde de fer rouge (E172).
Qu’est-ce que BELARA 0,03 mg/2 mg comprimé pelliculé et contenu de l’emballage extérieur
Ce médicament se présente sous forme de comprimé pelliculé. Boîte de 1, 3, 6 ou 13 plaquettes de 21 comprimés.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
GYÖMRŐI ÚT 19-21.
1103 BUDAPEST
HONGRIE
Exploitant de l’autorisation de mise sur le marché
103 BOULEVARD HAUSSMANN,
75008 PARIS
GYÖMRŐI ÚT 19-21.
1103 BUDAPEST
HONGRIE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
< {MM/AAAA}>< {mois AAAA}.>
Sans objet.