Dernière mise à jour le 02/03/2026
SUMATRIPTAN SUN 3 mg/0,5 ml, solution injectable en seringue préremplie (voie SC)
Indications thérapeutiques
Classe pharmacothérapeutique : Analgésique; Antimigraineux; Agonistes sélectifs des récepteurs 5-HT1, Code ATC: N02CC01.
La substance active contenue dans SUMATRIPTAN SUN est le sumatriptan. Il appartient à un groupe de médicaments appelés agonistes des récepteurs 5-HT1.
Ce médicament est indiqué dans le traitement de la crise de migraine. Les symptômes de la migraine peuvent être dus à une dilatation temporaire des vaisseaux sanguins crâniens. Ce médicament agit en réduisant la taille de ces vaisseaux sanguins.
Présentations
> 2 seringue(s) préremplie(s) en verre de 0,5 ml avec injecteur(s) automatique(s)
Code CIP : 34009 302 035 0 7
Déclaration de commercialisation : 03/12/2021
Cette présentation est agréée aux collectivités
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 05/10/2022 | Inscription (CT) | Le service médical rendu par SUMATRIPTAN SUN 3mg/0,5ml, solution injectable en seringue préremplie (sumatriptan) est important uniquement dans le traitement de la crise de migraine épisodique sévère avec une composante digestive majeure et installation rapidement progressive, lors-que les autres traitements oraux et nasaux de la crise de migraine ne peuvent être utilisés. |
| Insuffisant | Avis du 05/10/2022 | Inscription (CT) | Le service médical rendu par SUMATRIPTAN SUN 3mg/0,5ml, solution injectable en seringue préremplie (sumatriptan) est insuffisant pour justifier d’une prise en charge par la solidarité nationale dans les autres situations de l’AMM. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 05/10/2022 | Inscription (CT) | Compte-tenu : • de la démonstration de la supériorité du sumatriptan 3 mg injectable uniquement par rapport au placebo en traitement des crises de migraine épisodique modérées à sévères, • de l’absence de donnée d’efficacité et de tolérance versus un comparateur cliniquement perti-nent, • et prenant en compte le profil de tolérance connu du sumatriptan injectable, la spécialité SUMATRIPTAN SUN 3mg/0,5ml, solution injectable en seringue préremplie (sumatrip-tan) n’apporte pas d’amélioration du service médical rendu (ASMR V) dans le traitement de la crise de migraine épisodique sévère avec une composante digestive majeure et installation rapidement pro-gressive, lorsque les autres traitements oraux et nasaux de la crise de migraine ne peuvent être utili-sés. |
ANSM - Mis à jour le : 09/10/2025
SUMATRIPTAN SUN 3 mg/0,5 ml, solution injectable en seringue préremplie (voie SC)
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Sumatriptan............................................................................................................................. 3 mg
Sous forme de succinate de sumatriptan
Pour une seringue préremplie de 0,5 ml.
Excipient à effet notoire: sodium 1,63 mg.
Pour la liste complète des excipients, voir rubrique 6.1.
Solution injectable en seringue préremplie.
La solution est claire, incolore à jaune pâle sans particules visibles.
Le pH est compris entre 4,2 et 5,3. L’osmolalité est comprise entre 260 à 340 mOsmol.
4.1. Indications thérapeutiques
SUMATRIPTAN SUN doit être utilisé uniquement quand le diagnostic de migraine est bien établi.
4.2. Posologie et mode d'administration
Le sumatriptan ne doit pas être utilisé en prophylaxie.
L'efficacité du sumatriptan est indépendante de la durée de la crise lors de l'initiation du traitement. L'administration durant l'aura migraineuse, avant la survenue de tous les autres symptômes, peut ne pas prévenir le développement de la céphalée.
Posologie
Adultes
Il est conseillé de prendre le traitement dès les premiers signes de crise de migraine, ou dès l’apparition des symptômes associés tels que les nausées, les vomissements ou la photophobie. Le traitement est aussi efficace quel que soit le stade de la crise auquel il est administré.
La posologie recommandée de SUMATRIPTAN SUN chez l’adulte est une seule injection sous-cutanée de 6 mg (qui peut être administrée avec une seringue préremplie de SUMATRIPTAN SUN 6 mg/0,5 ml). Toutefois, en raison de la variabilité entre les patients et chez un même patient des crises de migraine et de la tolérance, certains patients pourraient bénéficier d'une dose plus faible de 3 mg, qui peut être administrée avec SUMATRIPTAN SUN 3 mg/0,5 ml.
Les patients qui ne sont pas soulagés après la première injection ne doivent pas prendre une deuxième dose de SUMATRIPTAN SUN au cours de la même crise. Une seconde injection pourra être utilisée pour une crise ultérieure dans les 24 heures suivantes à condition de respecter un intervalle d'au moins 1 heure entre les 2 injections.
Si un patient n’a pas été soulagé par une seule injection de ce médicament, il n’y a aucune raison, que ce soit pour des raisons théoriques ou de l’expérience clinique limitée, de ne pas utiliser des médicaments à base d’aspirine, d’anti-inflammatoires non-stéroïdiens ou de paracétamol pour le traitement ultérieur de cette crise.
Si le patient a été soulagé après la première dose mais que les symptômes réapparaissent, une seconde injection peut être utilisée dans les 24 heures suivantes, à condition de respecter un intervalle d’au moins 1 heure entre les 2 injections.
Il est recommandé d'utiliser sumatriptan en monothérapie dans le traitement de la crise de migraine et de ne pas le donner de façon concomitante avec de l'ergotamine ou des dérivés de l'ergotamine (y compris le méthysergide) (voir rubrique 4.3).
Population pédiatrique (de moins de 18 ans)
L’utilisation du sumatriptan n’est pas recommandée chez les enfants et les adolescents compte-tenu de l’absence de données d’utilisation sumatriptan injectable dans ces catégories d’âges.
Patient âgé (de plus de 65 ans)
L’expérience de l’utilisation de sumatriptan chez les patients âgés de plus de 65 ans est limitée. La pharmacocinétique n’est pas significativement différente de celle d’une population plus jeune. Cependant, tant que des données cliniques complémentaires ne seront pas disponibles, l'utilisation du sumatriptan chez les patients âgés de plus de 65 ans n'est pas recommandée.
Mode d’administration
Le sumatriptan doit être administré par voie sous-cutanée à l’aide d’une seringue préremplie. Après avoir retiré le capuchon protecteur de l’aiguille, la partie ouverte de l’injecteur automatique doit être placée sur le site d’injection (par exemple sur le haut du bras ou la cuisse), à la verticale avec un angle droit (90°). Le sumatriptan ne doit pas être injecté dans les zones où la peau est sensible, contusionnée, rouge ou dure. En pressant et en relâchant immédiatement le bouton bleu un premier clic est entendu, indiquant que l’injection a commencé. L’injecteur automatique doit être maintenu appuyé sur la peau jusqu’à ce qu’un second clic soit entendu. Ceci indique que l’injection est terminée. L’injecteur automatique peut alors être retiré de la peau. La gaine blanche protectrice de l’aiguille de l’injecteur automatique se déploiera automatiquement pour recouvrir l'aiguille. La fenêtre d’inspection sera bleue confirmant que l’injection est terminée. Les patients doivent être avertis qu’il faut strictement respecter la notice d’utilisation de ce médicament et notamment la partie concernant l’utilisation de la seringue préremplie.
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
Le sumatriptan ne doit pas être utilisé chez les patients ayant des antécédents d'infarctus du myocarde ou une pathologie cardiaque ischémique, un vasospasme coronarien (Angor de Prinzmetal), une pathologie vasculaire périphérique ou chez les patients présentant des symptômes ou des signes compatibles avec une pathologie cardiaque ischémique.
Le sumatriptan ne doit pas être administré aux patients présentant des antécédents d'accident vasculaire cérébral (AVC) ou d'accident ischémique transitoire (AIT).
Le sumatriptan ne doit pas être administré aux patients ayant une insuffisance hépatique sévère.
L'utilisation du sumatriptan est contre-indiquée chez les patients ayant une hypertension modérée ou sévère et chez les patients ayant une hypertension légère non contrôlée.
L’administration concomitante avec l'ergotamine ou les dérivés de l'ergotamine (y compris le méthysergide), un autre triptan/agoniste des récepteurs de la 5-hydroxytriptamine1 (5-HT1) est contre-indiquée (voir rubrique 4.5).
L'association du sumatriptan avec les inhibiteurs de la monoamine-oxydase est contre-indiquée. Le sumatriptan ne doit pas être utilisé dans les 2 semaines suivant l'arrêt d'un traitement par les inhibiteurs de la monoamine-oxydase (voir rubrique 4.5).
4.4. Mises en garde spéciales et précautions d'emploi
Le sumatriptan ne doit être utilisé qu’après avoir clairement établi le diagnostic de migraine.
Le sumatriptan n'est pas indiqué dans le traitement des migraines hémiplégiques, basilaires ou ophtalmoplégiques.
Les doses recommandées de ce médicament ne doivent pas être dépassées.
Le sumatriptan ne doit pas être administré par voie intraveineuse en raison de risque de spasme coronaire. Le spasme coronaire peut se traduire par des arythmies, des modifications de l’ECG de type ischémique ou un infarctus du myocarde.
Avant de traiter les céphalées des patients sans diagnostic antérieur de migraine, et des patients migraineux présentant des symptômes atypiques, il est nécessaire d'exclure d'autres pathologies neurologiques potentiellement graves. Il faut noter que les migraineux peuvent présenter un risque accru de survenue d’événements vasculaires cérébraux (par exemple, accidents cérébro-vasculaires, accident ischémique transitoire)
Après administration, la prise de sumatriptan peut être associée à des symptômes transitoires comprenant des douleurs thoraciques ou une sensation d'oppression pouvant être intense et pouvant s'étendre au niveau de la gorge. Si la symptomatologie évoque une ischémie cardiaque, des doses supplémentaires de sumatriptan ne doivent pas être administrées et des explorations appropriées devront être réalisées.
Le sumatriptan ne doit pas être administré aux patients ayant des facteurs de risque de maladie cardiaque ischémique, y compris les gros fumeurs ou les patients utilisant des thérapies de substitution à base de nicotine, sans un bilan cardiovasculaire préalable (voir rubrique 4.3). Une attention particulière doit être portée aux femmes ménopausées et aux hommes de plus de 40 ans présentant ces facteurs de risque. Cependant, ce bilan peut ne pas identifier tous les patients qui ont une maladie cardiovasculaire et, dans de très rares cas, des événements cardiaques graves sont survenus chez des patients sans maladie cardiovasculaire sous-jacente (voir section 4.8).
Si le patient présente des symptômes qui sont graves ou persistants ou compatibles avec l'angine de poitrine, des doses supplémentaires ne doivent pas être prises jusqu'à ce que des examens appropriés aient été effectués pour vérifier la possibilité de changements ischémiques.
Le sumatriptan doit être administré avec prudence chez les patients présentant une hypertension légère contrôlée, en raison de l’augmentation transitoire de la pression artérielle et des résistances vasculaires périphériques observée chez une petite proportion de patients (rubrique section 4.3).
Après commercialisation, de rares cas de syndrome sérotoninergique (incluant une modification de de la conscience, des manifestations neurovégétatives et des troubles neuromusculaires) ont été décrits après utilisation concomitante d'un inhibiteur sélectif de la recapture de la sérotonine (ISRS) et du sumatriptan. Des cas de syndrome sérotoninergique ont également été rapportés après administration concomitante de triptans et d'inhibiteurs de la recapture de la sérotonine et de la noradrénaline (IRSN). Si l'association du sumatriptan et d'un ISRS/IRSN est cliniquement justifiée, une surveillance appropriée du patient est recommandée (voir rubrique 4.5).
Le sumatriptan doit être administré avec précaution chez les patients présentant des facteurs pouvant modifier l'absorption, le métabolisme ou l'élimination du médicament, par exemple chez l'insuffisant hépatique ou rénal.
Le sumatriptan doit être utilisé avec précaution chez les patients ayant des antécédents de convulsions ou présentant d'autres facteurs de risque susceptibles d'abaisser le seuil épileptogène, car des cas de convulsions ont été rapportés en association avec le sumatriptan (voir rubrique 4.8).
Chez les patients ayant une hypersensibilité connue aux sulfamides, des réactions allergiques peuvent être observées après administration de sumatriptan. Ces réactions vont de l'allergie cutanée aux réactions anaphylactiques.
La démonstration d'une allergie croisée est limitée, cependant la prudence est recommandée avant d'utiliser le sumatriptan chez ces patients.
La fréquence des effets indésirables peut être augmentée par l'association de triptans à des préparations contenant du millepertuis (Hypericum perforatum).
L'utilisation prolongée d'un traitement antalgique pour traiter les céphalées peut entraîner une aggravation de celles-ci. Dans ces cas ou en cas de suspicion, un avis médical est nécessaire et le traitement doit être interrompu. Le diagnostic de céphalée par abus médicamenteux (CAM) doit être suspecté chez les patients présentant des céphalées fréquentes ou quotidiennes malgré (ou à cause) de l’utilisation régulière d’un traitement antimigraineux.
Ce médicament contient moins de 1 mmol de sodium (23mg) par dose (3mg) c’est-à-dire pratiquement « sans sodium ».
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
L'intervalle nécessaire entre l'utilisation du sumatriptan et des médicaments contenant de l'ergotamine ou un autre triptan/agoniste des récepteurs 5-HT1 n'est pas connu. Il dépendra aussi des doses et du type de produits utilisés. Les effets peuvent être additifs. Il est conseillé d'attendre au moins 24 heures après l'utilisation de médicaments contenant de l'ergotamine ou un autre triptan/agoniste des récepteurs 5-HT1, avant l'administration du sumatriptan. Inversement, il est conseillé d'attendre au moins 6 heures après l'utilisation du sumatriptan avant l'administration d'un médicament contenant de l'ergotamine et au moins 24 heures avant l'administration d’un autre triptan/agoniste des récepteurs 5-HT1.
Une interaction peut se produire entre le sumatriptan et les IMAO. L'administration concomitante de ces deux produits est donc contre-indiquée (voir rubrique 4.3).
Après commercialisation, de rares cas de syndrome sérotoninergique (incluant une modification de la conscience, des manifestations neurovégétatives et des troubles neuromusculaires) ont été décrits après utilisation concomitante d'un inhibiteur sélectif de la recapture de la sérotonine (ISRS) et du sumatriptan. Des cas de syndrome sérotoninergique ont également été rapportés après administration concomitante de triptans et d’IRSN (voir section 4.4). Il existe aussi un risque de syndrome sérotoninergique en cas d’utilisation concomitante du lithium et du sumatriptan.
4.6. Fertilité, grossesse et allaitement
Grossesse
Des données d'après commercialisation, provenant de l'utilisation du sumatriptan au cours du premier trimestre de la grossesse chez plus de 1 000 femmes, sont disponibles. Bien que ces données soient insuffisantes pour tirer des conclusions définitives, elles ne montrent pas une augmentation du risque tératogène. L'expérience de l'utilisation du sumatriptan au cours des deuxième et troisième trimestres de la grossesse est limitée.
Les études chez l'animal n'indiquent pas d'effets tératogènes directs ou des effets nuisibles sur le développement péri et postnatal. Toutefois, la viabilité embryofœtale peut être altérée chez le lapin (voir rubrique 5.3).
En conséquence, l'administration de sumatriptan ne doit être envisagée que si le bénéfice attendu pour la mère est supérieur aux risques possibles pour le fœtus.
Allaitement
Le sumatriptan est excrété dans le lait maternel, avec des doses relatives moyennes pour le nourrisson de < 4 % après administration d'une dose unique de sumatriptan. L'exposition du nourrisson peut être minimisée en évitant l'alimentation au lait maternel dans les 12 heures suivant le traitement, période pendant laquelle le lait maternel exprimé doit être jeté..
Des cas de douleur mammaire et/ou du mamelon ont été rapportés après l’utilisation du sumatriptan chez des femmes qui allaitent (voir rubrique 4.8). La douleur était généralement transitoire et disparaissait en 3 à 12 heures.
Fertilité
Il n'existe pas de données sur les effets du sumatriptan dans la fertilité chez l'Homme.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Une somnolence due à la migraine ou à son traitement par le sumatriptan peut survenir. Ceci peut influer sur l'aptitude à conduire des véhicules et à utiliser des machines.
Aucune étude sur les effets sur la capacité à conduire et à utiliser des machines n'a été réalisée.
Les effets indésirables sont classés ci-dessous par système-organe et par fréquence.
La classification selon la fréquence utilise la convention suivante: très fréquent (≥ 1/10), fréquent (≥ 1/100 et < 1/10), peu fréquent (≥ 1/1000 et< 1/100), rare (≥ 1/10000 et < 1/1000), très rare (< 1/10000), inconnu (ne pouvant pas être estimé sur la base des données disponibles). Certains symptômes rapportés comme effets indésirables peuvent être considérés comme des symptômes associés à la migraine.
Affections du système immunitaire
Inconnu : réactions d'hypersensibilité allant d'une allergie cutanée à une réaction anaphylactique.
Affections psychiatriques
Inconnu : anxiété.
Affections du système nerveux
Fréquent : vertiges, somnolence, troubles de la sensibilité dont paresthésie et hypoesthésie.
Inconnu : convulsions, bien que certaines de ces convulsions soient survenues chez des patients présentant soit des antécédents de convulsions soit des facteurs de risque. Quelques cas ont été rapportés chez des patients en l'absence de tels facteurs de risque. Tremblements, dystonie, nystagmus, scotome.
Affections oculaires
Inconnu : papillotements, diplopie, baisse de la vision. Perte de la vision, dont certains cas peuvent être permanents. Toutefois, des troubles visuels peuvent également survenir au cours de la crise de migraine.
Affections cardiaques
Inconnu : bradycardie, tachycardie, palpitations, arythmies cardiaques, signes ischémiques transitoires à l'ECG, vasospasme des artères coronaires, angor, infarctus du myocarde (voir rubriques 4.3 et 4.4).
Affections vasculaires
Fréquent : augmentations transitoires de la pression artérielle survenant juste après le traitement, flush.
Inconnu : hypotension, syndrome de Raynaud.
Affections respiratoires, thoraciques et médiastinales
Fréquent : dyspnée
Affections gastro-intestinales
Fréquent : des nausées et vomissements sont survenus chez certains patients, sans que l'on puisse déterminer si ces symptômes sont liés au sumatriptan ou à la pathologie sous-jacente.
Inconnu : colites ischémiques, diarrhées.
Affections de la peau et du tissu sous-cutané
Inconnu : hyperhidrose.
Affections musculo-squelettiques et systémiques
Fréquent : sensation de lourdeur (habituellement transitoire, mais pouvant être intense et intéresser n'importe quelle partie du corps, y compris la poitrine et la gorge). Myalgies.
Inconnu : raideur de la nuque, arthralgies.
Troubles du système reproducteur et des seins
Rare : Douleurs mammaires
Troubles généraux et anomalies au site d'administration
Très fréquents : douleur transitoire au site d’injection. piqûre/brûlure, gonflement, érythème, hématome et saignements au site d’injection, ont aussi été rapportés.
Fréquent: douleur, sensation de chaleur ou de froid, de pression ou d'oppression (ces effets sont habituellement transitoires, mais ils peuvent être intenses et intéresser n'importe quelle partie du corps, y compris la poitrine et la gorge). Sensation de faiblesse, fatigue (ces deux effets sont le plus souvent d'intensité faible à modérée et transitoires).
Bien qu'il n'y ait eu aucune comparaison directe, les bouffées de chaleurs, paresthésies et sensations de chaleur, de pression et de lourdeur peuvent être plus fréquentes après injection de sumatriptan.
Inversement, les nausées, vomissements et la fatigue apparaissent moins fréquemment lors de l’administration sous-cutanée en comparaison avec les comprimés.
Investigations
Très rare : des perturbations mineures des tests de la fonction hépatique ont parfois été observées.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/
Des cas de surdosage avec le sumatriptan injectable ont été rapportés.
Des patients ont reçu des injections uniques allant jusqu'à 12 mg par voie sous-cutanées sans entraîner d'effets indésirables significatifs. Des doses allant jusqu'à 16 mg par voie sous-cutanée n'ont pas entraîné d'effets indésirables autres que ceux mentionnés.
En cas de surdosage avec sumatriptan, le patient doit être mis sous surveillance pendant au moins 10 heures et un traitement symptomatique standard doit être administré, si nécessaire. L'effet de l'hémodialyse ou de la dialyse péritonéale sur les concentrations plasmatiques de sumatriptan n'est pas connu.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Le sumatriptan est un agoniste sélectif des récepteurs vasculaires à la 5-hydroxy-tryptamine-1 (5HT1d) sans effet sur les autres sous-types de récepteurs 5HT (5HT2 à 5HT7). Les récepteurs vasculaires 5HT1d sont localisés principalement au niveau des vaisseaux sanguins crâniens et induisent une vasoconstriction. Chez l'animal, le sumatriptan est responsable d'une vasoconstriction sélective de la circulation artérielle carotidienne. La circulation artérielle carotidienne vascularise les tissus extracrâniens et intracrâniens tels que les méninges et on pense que la dilatation et/ou la formation d'œdèmes au niveau de ces vaisseaux pourraient correspondre au mécanisme de la migraine chez l'homme. De plus, les résultats des études chez l'animal indiquent que le sumatriptan inhibe l'activité du nerf trijumeau. Ces deux actions (vasoconstriction crânienne et inhibition de l'activité du nerf trijumeau) pourraient contribuer à l'action anti-migraineuse du sumatriptan chez l'homme.
Le sumatriptan est également efficace dans le traitement de la crise de migraine périmenstruelle, c'est-à-dire la migraine sans aura qui survient entre 3 jours avant et jusqu’à 5 jours après le début des menstruations. Le sumatriptan doit être administré le plus tôt possible lors d’une crise.
En raison de sa voie d’administration, le sumatriptan peut être particulièrement adapté aux patients souffrant de nausées et vomissements au cours d’une crise.
5.2. Propriétés pharmacocinétiques
Absorption
Distribution
La liaison aux protéines plasmatiques est faible (14 à 21 %).
La clairance non rénale représente environ 80 % de la clairance totale. Le sumatriptan présente une augmentation de Cmax et de l'AUC proportionnelle à la dose dans la gamme posologique de 1 à 16 mg lors de l'administration sous-cutanée. Le volume moyen de distribution est de 177,5 litres. La clairance plasmatique moyenne est d'environ 1197 ml/min et la clairance rénale est d'environ 264 ml/min.
Elimination
Le sumatriptan est éliminé tout d'abord par métabolisme oxydatif dû à la monoamine oxydase A.
Le principal métabolite, l'analogue acide indolacétique du sumatriptan, est principalement excrété dans les urines, où il est retrouvé sous forme d'acide libre ou de glucuroconjugué. Il n'a pas d'activité 5HT1 ou 5HT2 connue. Les métabolites mineurs n'ont pas été identifiés.
Dans une étude pilote, aucune différence significative n'a été observée dans les paramètres pharmacocinétiques entre les personnes âgées et les jeunes volontaires sains.
5.3. Données de sécurité préclinique
Lors d'une étude de fertilité chez le rat, des doses orales de sumatriptan entraînant des concentrations plasmatiques d'environ 150 fois supérieures à celles observées chez l'homme après une dose de 6mg par voie sous-cutanée ont été associées à une réduction du succès de l'insémination. Lors d’une étude de fertilité chez le rat, une réduction du succès de l'insémination a été observée à des concentrations plasmatiques largement supérieures aux concentrations maximales obtenues chez l’Homme.
Chez le lapin, une embryolétalité sans anomalies tératogènes marquées a été observée. La pertinence de ces résultats chez l'homme n'est pas connue.
Chlorure de sodium, eau pour préparations injectables.
3 ans.
6.4. Précautions particulières de conservation
Ce médicament ne nécessite pas de précautions température particulières de conservation. A conserver dans l'emballage d'origine afin de protéger de la lumière.
6.5. Nature et contenu de l'emballage extérieur
Seringue préremplie composée d'un cylindre en verre de type I (Ph.Eur) de 1 ml avec aiguille 27 gauge de 1/2 pouce de longueur et butée de piston noire en chlorobutyle, emballé dans un blister en PVC (polychlorure de vinyle) recouvert d’un film pelable en PET (polyéthyléne téréphtalate).
Boîte de 1 seringue préremplie avec injecteur automatique.
Boîte de 2 seringues préremplies avec injecteurs automatiques.
Boîte de 6 seringues préremplies avec injecteurs automatiques.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
SUN PHARMACEUTICAL INDUSTRIES EUROPE B.V.
POLARISAVENUE 87
2132 JH HOOFDDORP
PAYS-BAS
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 302 034 9 1: 0,5 mL en seringue préremplie (verre) avec injecteur automatique. Boîte de 1.
· 34009 302 035 0 7: 0,5 mL en seringue préremplie (verre) avec injecteur automatique. Boîte de 2.
· 34009 302 035 2 1: 0,5 mL en seringue préremplie (verre) avec injecteur automatique. Boîte de 6.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
Date de première autorisation:{JJ mois AAAA}
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
{JJ mois AAAA}
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I.
ANSM - Mis à jour le : 09/10/2025
SUMATRIPTAN SUN 3 mg/0,5 ml, solution injectable en seringue préremplie (voie SC)
Sumatriptan
Veuillez lire attentivement cette notice avant d’utiliser ce médicament car elle contient des informations importantes pour vous.
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que SUMATRIPTAN SUN 3 mg/0,5 ml, solution injectable en seringue préremplie (voie SC) et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d’utiliser SUMATRIPTAN SUN 3 mg/0,5 ml, solution injectable en seringue préremplie (voie SC) ?
3. Comment utiliser SUMATRIPTAN SUN 3 mg/0,5 ml, solution injectable en seringue préremplie (voie SC) ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver SUMATRIPTAN SUN 3 mg/0,5 ml, solution injectable en seringue préremplie (voie SC) ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE SUMATRIPTAN SUN 3 mg/0,5 ml, solution injectable en seringue préremplie (voie SC) ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : Analgésique; Antimigraineux; Agonistes sélectifs des récepteurs 5-HT1, Code ATC: N02CC01.
La substance active contenue dans SUMATRIPTAN SUN est le sumatriptan. Il appartient à un groupe de médicaments appelés agonistes des récepteurs 5-HT1.
Ce médicament est indiqué dans le traitement de la crise de migraine. Les symptômes de la migraine peuvent être dus à une dilatation temporaire des vaisseaux sanguins crâniens. Ce médicament agit en réduisant la taille de ces vaisseaux sanguins.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER SUMATRIPTAN SUN 3 mg/0,5 ml, solution injectable en seringue préremplie (voie SC) ?
· si vous êtes allergique au sumatriptan ou à l'un des autres composants contenus dans ce médicament (mentionnés dans la rubrique 6).
· si vous avez des troubles cardiaques ou des antécédents d'infarctus.
· si vous avez des troubles circulatoires au niveau des bras et des jambes.
· si vous avez des antécédents d'accident vasculaire cérébral ou de mini-AVC (aussi appelé accident ischémique transitoire ou AIT).
· si vous avez une maladie grave du foie.
· si vous avez une hypertension artérielle modérée à sévère ou non contrôlée par un traitement.
· En association à certains autres médicaments utilisés également dans le traitement de la migraine contenant de l’ergotamine et dérivés de l'ergotamine, y compris le méthysergide, un autre triptan ou un agoniste 5-HT.
· En association aux IMAO (inhibiteur de la monoamine oxydase) ou si vous avez pris un IMAO dans les deux dernières semaines.
Avertissements et précautions
Adressez-vous à votre d’utiliser SUMATRIPTAN SUN 3 mg/0,5 ml, solution injectable en seringue préremplie (voie SC) si :
· vous avez l'une des maladies suivantes : maladie cardiaque telle que : insuffisance cardiaque, angine de poitrine ou infarctus du myocarde (crise cardiaque), hypertension artérielle, maladie du foie ou des reins, épilepsie ou une maladie du cerveau. Les femmes ménopausées et les hommes de plus de 40 ans en particulier doivent avoir un examen cardiaque et des vaisseaux sanguins avant d'utiliser ce médicament;
· vous avez des facteurs de risque de maladies cardiaques, tels que, si vous êtes un grand fumeur ou si vous utilisez des thérapies de substitution de la nicotine, et surtout si vous être un homme de plus de 40 ans ou une femme ménopausée. Dans de très rares cas, des personnes ont développé de graves problèmes cardiaques après avoir utilisé du sumatriptan, alors qu’elles ne présentaient aucun signe de maladie cardiaque auparavant. Si l’un des facteurs de risque mentionnés s’applique à vous, cela pourrait signifier que vous avez un plus grand risque de développer une maladie cardiaque et votre fonction cardiaque devrait être vérifiée avant d’utiliser ce médicament.;
· vous êtes allergique à certains antibiotiques (sulfamides) : les personnes allergiques aux sulfamides peuvent présenter une réaction allergique au sumatriptan ;
· vous utilisez certains médicaments pour traiter une dépression (appelés ISRS ou IRSN) ou du lithium (un médicament utilisé pour le traitement les troubles maniaco-dépressifs (troubles bipolaires)). Après avoir discuté de ce qui précède, votre médecin peut encore vous conseiller d'utiliser ce médicament et vous donnera des directives sur l'utilisation de l'injection.
Comme avec d'autres traitements de la migraine, l’abus peut aggraver votre migraine et rendre les crises plus fréquentes.
Vous devez utiliser ce médicament seulement lorsque votre médecin est certain que vous souffrez de crises de migraine.
Faites immédiatement recours à une aide médicale si vous ressentez des symptômes tels que la confusion mentale, l’accélération du rythme cardiaque, des frissons, des sueurs et des contractions musculaires. Il peut s’agir de signes d’une affection très grave appelée « syndrome sérotoninergique ».
Autres médicaments et SUMATRIPTAN SUN 3 mg/0,5 ml, solution injectable en seringue préremplie (voie SC)
Avant d'utiliser SUMATRIPTAN SUN informez votre médecin si :
· vous prenez d’autres médicaments pour votre migraine qui contiennent des dérivés de l'ergotamine ou de l'ergotamine, tels que le tartrate d'ergotamine ou de maléate méthysergide (si c’est le cas, vous devez arrêter de les prendre au moins 24 heures avant de prendre du sumatriptan) ;
· vous prenez des médicaments sur ordonnance d'un médecin pour le traitement de la dépression tels que les IMAO ou les ISRS (y compris le citalopram, la fluoxétine, la fluvoxamine, la paroxétine et la sertraline), ou si vous avez pris un IMAO dans les 2 dernières semaines ;
· vous prenez du lithium (un médicament utilisé pour le traitement des troubles maniaco-dépressifs (troubles bipolaires)) ;
· vous prenez des médicaments sur ordonnance d'un médecin afin de vous aider à perdre du poids, ou pour le traitement de l'épilepsie ;
· vous prenez un produit qui contient la plante médicinale millepertuis (Hypericum perforatum). Le prendre avec sumatriptan peut augmenter les possibilités de présenter d'effets indésirables.
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
Demandez conseil à votre médecin ou votre pharmacien avant de prendre ce médicament :
· Si vous êtes enceinte, si vous pensez être enceinte ou planifiez une grossesse.
· Si vous allaitez. Votre médecin peut vous conseiller de prendre du sumatriptan, mais l'allaitement doit être suspendu pendant 12 heures après une dose de sumatriptan et pendant ce temps tout le lait maternel collecté doit être éliminé.
Certaines femmes qui allaitent signalent de la douleur mammaire et/ou au mamelon après l’utilisation du sumatriptan. La douleur est généralement temporaire et disparaît en 3 à 12 heures.
Conduite de véhicules et utilisation de machines
Ce médicament peut entraîner une somnolence. Si vous êtes concerné, ne conduisez pas et n’utilisez pas de machines.
SUMATRIPTAN SUN 3 mg/0,5 ml, solution injectable en seringue préremplie (voie SC) contient du sodium
Ce médicament contient moins de 1 mmol de sodium (23 mg) par dose (3 mg), c'est à dire pratiquement «sans sodium».
3. COMMENT UTILISER SUMATRIPTAN SUN 3 mg/0,5 ml, solution injectable en seringue préremplie (voie SC) ?
Vérifiez auprès de votre médecin ou pharmacien en cas de doute
SUMATRIPTAN SUN est habituellement injecté dans la cuisse ou le haut du bras.
Lisez attentivement la section « Comment utiliser l'injecteur automatique», à la fin de la notice. La seringue préremplie avec injecteur automatique injectera une dose de ce médicament juste sous la peau, rapidement et sans douleur. L'injection ne doit PAS être réalisée par une autre voie que la voie indiquée.
NE PAS injecter SUMATRIPTAN SUN dans une veine.
NE PAS utiliser de SUMATRIPTAN SUN pour prévenir une crise.
Utilisez une seringue préremplie avec injecteur automatique dès le premier signe d'une crise de migraine (bien qu'il soit tout aussi efficace s'il est utilisé plus tard au cours d'une crise).
Si votre migraine disparaît mais revient :
En cas de soulagement de votre crise de migraine après la première dose mais que la douleur réapparait, vous pouvez utiliser une deuxième seringue préremplie avec injecteur automatique, à tout moment dans les prochaines 24 heures, à condition de respecter un intervalle d'au moins une heure entre les 2 injections.
NE PAS utiliser plus de DEUX seringues préremplies par 24 heures.
Si votre migraine ne disparaît pas
N'utilisez pas une deuxième dose pour la même crise. Ce médicament peut toutefois être utilisé pour votre prochaine crise à tout moment dans les 24 heures suivantes, à condition de respecter un intervalle d'au moins une heure entre les 2 injections.
. N'utilisez pas plus de deux seringues préremplies par 24 heures.
Si l'injection ne soulage pas votre migraine, vous pouvez prendre vos antalgiques habituels, à condition qu'ils ne contiennent pas d'ergotamine ou ses dérivés. Attendez au moins six heures après l'utilisation de ce médicament avant de prendre un médicament contenant de l'ergotamine ou ses dérivés.
Utilisation chez les enfants et les adolescents de moins de 18 ans
Le sumatriptan injectable ne doit pas être utilisé chez les enfants et les adolescents de moins de 18 ans.
Personnes âgées de plus de 65 ans
Il y a peu d'expérience du sumatriptan injectable chez les personnes âgées de plus de 65 ans, il n'est donc pas indiqué pour ce groupe d'âge.
Si vous avez utilisé plus de SUMATRIPTAN SUN 3 mg/0,5 ml, solution injectable en seringue préremplie (voie SC) que vous n’auriez dû :
Utiliser une quantité supérieure à celle prescrite vous rendra malade. En cas de surdosage, N’ATTENDEZ PAS, demandez à votre médecin ce qu'il faut faire ou contactez le service des urgences le plus proche.
Si vous avez d'autres questions sur l'utilisation de ce médicament, demandez plus d'informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Effets secondaires graves
Les effets secondaires suivants ont été signalés (fréquence inconnue).
Si vous présentez les effets secondaires suivants, vous devez contacter votre médecin immédiatement et ne plus utiliser ce médicament, sauf sur indication contraire de votre médecin
· une respiration sifflante, un battement ou un serrement soudain de la poitrine, un gonflement des paupières, du visage ou des lèvres, une éruption cutanée - des taches rouges ou de l'urticaire (masses de peau), qui peuvent être des signes d'une réaction allergique
· les crises (généralement chez les personnes ayant des antécédents d'épilepsie)
· inflammation du côlon (partie de l'intestin), qui peut se présenter sous forme de douleurs abdominales du côté gauche inférieur et/ou de diarrhée sanglante, avec de la fièvre (colite ischémique)
· le phénomène de Raynaud, qui peut se traduire par une pâleur ou une teinte bleue de la peau et/ou une douleur des doigts, des orteils, des oreilles, du nez ou de la mâchoire en réponse au froid ou au stress
· douleurs thoraciques (angine)
· crise cardiaque
Autres effets indésirables
Très fréquents (pouvant affecter plus de 1 personne sur 10)
· douleur temporaire au site d'injection ;
· picotements/brûlure, rougeur, gonflement, ecchymoses et des saignements au site d'injection.
Fréquents (pouvant affecter jusqu’à 1 personne sur 10)
· bouffées vasomotrices (rougeur de la face durant quelques minutes), vertiges, sensation de faiblesse, fatigue et somnolence ;
· augmentation de la pression artérielle de courte durée, peu après l’utilisation de ce médicament ;
· nausées et vomissements, lorsqu'ils ne font pas partie de la crise de migraine ;
· douleur, des sensations inhabituelles, comme des picotements, d’engourdissement, de chaleur ou de froid, de lourdeur et de pression ou d'oppression. Ces symptômes disparaissent généralement rapidement, mais peuvent être intenses et affecter n'importe quelle partie du corps, notamment la poitrine et la gorge. Si ces symptômes persistent ou sont particulièrement graves, en particulier si vous avez une douleur au niveau de la poitrine ou du cœur qui se propage dans les bras, parlez-en immédiatement à votre médecin car il y a eu de rares cas pour lesquels ces problèmes ont été causés par une crise cardiaque ;
· essoufflement ;
· douleurs musculaires (myalgies).
Rares
· Douleur mammaire
Très rares (pouvant affecter jusqu’à 1 personne sur 10 000)
· modifications de la fonction hépatique: si vous avez un test sanguin afin de vérifier comment votre foie fonctionne et que vous avez utilisé du sumatriptan, parlez-en à votre médecin car cela peut affecter les résultats.
Fréquence inconnue (ne peut être estimée à partir des données disponibles)
· tremblements, contractions musculaires, mouvements involontaires des yeux ;
· troubles visuels, y compris le scintillement, une vision double et une vision réduite. Il y a eu des cas où les défauts de vision permanents se sont produits ;
· abaissement de la pression artérielle qui peut entraîner une sensation de malaise en particulier en se relevant ;
· le ralentissement ou accélération de votre fréquence cardiaque, des palpitations (sensation de battements cardiaques rapides), des changements du rythme cardiaque ;
· diarrhée ;
· raideur de la nuque ;
· douleurs articulaires ;
· anxiété, transpiration.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: https://signalement.social-sante.gouv.fr/
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER SUMATRIPTAN SUN 3 mg/0,5 ml, solution injectable en seringue préremplie (voie SC) ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur la boîte après « EXP ». La date de péremption fait référence au dernier jour de ce mois.
Ce médicament ne nécessite pas de précautions de température particulières de conservation. A conserver dans l'emballage d'origine afin de protéger de la lumière.
N’utilisez pas ce médicament si vous remarquez des particules dans la solution.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient SUMATRIPTAN SUN 3 mg/0,5 ml, solution injectable en seringue préremplie (voie SC)
· La substance active est le sumatriptan.
Chaque seringue préremplie contient 3 mg de sumatriptan sous forme de succinate de sumatriptan équivalent à 3 mg de sumatriptan.
· Les autres composants sont : chlorure de sodium et eau pour préparations injectables.
Seringue préremplie avec injecteur automatique, contenant une solution pour injection claire, incolore ou jaune pâle sans particules visibles. Chaque boîte contient 1, 2 ou 6 seringue préremplies.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
SUN PHARMACEUTICAL INDUSTRIES EUROPE B.V.
POLARISAVENUE 87
2132 JH HOOFDDORP
PAYS-BAS
Exploitant de l’autorisation de mise sur le marché
SUN PHARMA FRANCE
31 RUE DES POISSONNIERS
92200 NEUILLY-SUR-SEINE
SUN PHARMACEUTICAL INDUSTRIES EUROPE B.V.
POLARISAVENUE 87
2132 JH HOOFDDORP
PAYS-BAS
OU
TERAPIA S.A.
STR. FABRICII NR 124
CLUJ-NAPOCA,
JUDETUL CLUJ 400632
ROUMANIE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
{mois AAAA}.
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
Comment utiliser Sumatriptan sun 3 mg/0,5 ml, solution injectable en seringue préremplie (voie sc)
Cette notice explique comme utiliser l'injecteur automatique SUMATRIPTAN SUN.
Lisez cette notice DEUX FOIS avant la première étape. Si vous avez des questions, demandez plus d'informations à votre médecin ou votre pharmacien.
Ne doit être utilisé que chez les patients pour lesquels une dose de 3 mg a été prescrite.
Vue de face de l’injecteur automatique
Figure 1
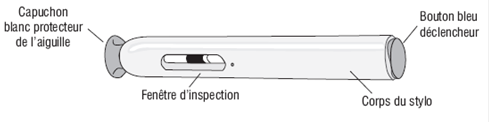
Attention :
· VERIFIEZ l'apparence de la solution de SUMATRIPTAN SUN à travers la fenêtre d'inspection. La solution doit être claire, incolore à jaune pâle. Ne pas injecter la solution si elle semble décolorée ou trouble ou si elle contient des grumeaux, des flocons, ou des particules.
· NE PAS retirer le capuchon blanc protecteur de l'aiguille avant que vous soyez prêt à effectuer l'injection.
· NE JAMAIS enfoncer le capuchon blanc protecteur de l'aiguille dans l'injecteur automatique.
· NE JAMAIS mettre ou appuyer le pouce, les doigts ou la main sur la gaine blanche protectrice de l'aiguille.
Comment utiliser l'injecteur automatique
a) Lavez-vous soigneusement les mains.
b) Trouvez un endroit confortable et bien éclairé et mettez tout ce dont vous avez besoin à portée de main (injecteur automatique, alcool ou des compresses stériles).
c) Identifiez une zone d'application avec une couche suffisante de tissu adipeux, par exemple sur la partie supérieure du bras ou sur la cuisse (Figure 2).
Ne pas injecter dans les zones où la peau est sensible, blessée, rouge ou dure.
Figure 2
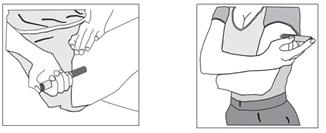
d) Nettoyez le site d'injection avec de l'alcool ou une compresse stérile neuve et laisser sécher votre peau. Ne touchez cette zone avant de faire l'injection.
e) Sortez l'injecteur automatique de sa boîte.
f) Prenez l'injecteur automatique dans une main et enlevez doucement le capuchon blanc protecteur de l'aiguille en tirant dessus avec l’autre main (Figure 3). Ne le tournez pas et ne remettez pas le capuchon blanc protecteur de l'aiguille, car ces manipulations pourraient endommager l'aiguille qui se trouve à l'intérieur de l'injecteur automatique
Figure 3
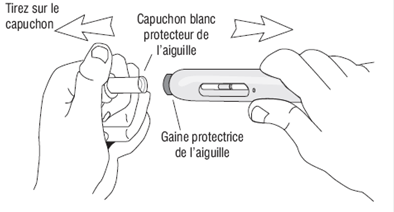
Comment commencer l'injection:
1) Sans appuyer sur le bouton bleu déclencheur, placez l'extrémité ouverte de l'injecteur automatique sur le site d'injection avec un angle droit (90°) et poussez la gaine blanche protectrice de l'aiguille fermement sur la peau pour déverrouiller le système. L’injecteur automatique ne fonctionne que si la gaine protectrice de l’aiguille est complètement rétractée (Figure 4).
Continuez à tenir l'injecteur automatique fermement sur la peau.
Figure 4
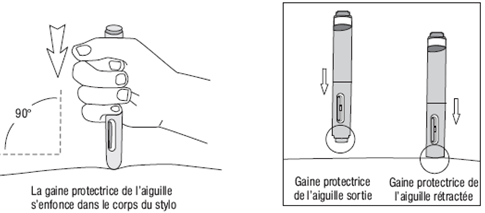
2) Appuyez et relâchez le bouton bleu déclencheur (un premier « clic » sonore se fait entendre). Cela déclenche l'injection (Figure 5a).
Figure 5a
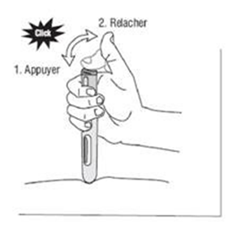
3) Ne pas retirer l'injecteur automatique de la peau.
4) Attendez jusqu'à ce que vous entendiez un deuxième « clic ».La fenêtre d’inspection deviendra bleue, confirmant que l’injection est finie (Figure 5b).
5) Levez l'injecteur automatique directement vers le haut. L'injection est terminée.
Figure 5b
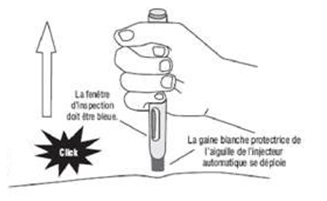
Si la fenêtre d'inspection n'est pas bleue, n'essayez pas d'utiliser une seconde fois l'injecteur automatique.
6) La gaine blanche protectrice de l'aiguille du l'injecteur automatique se déploiera automatiquement pour recouvrir l'aiguille et se verrouillera. L'aiguille ne sera plus visible.
Il n'est pas nécessaire de remettre le capuchon blanc (Figure 6).
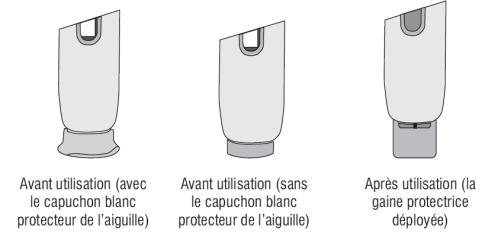
NE JAMAIS ESSAYER DE REUTILISER UN INJECTEUR AUTOMATIQUE.
Si vous pensez que vous n'avez pas reçu la totalité de la dose, ne répétez pas l'injection en utilisant un nouvel injecteur automatique.
7) Si vous remarquez une goutte de sang au site d'injection, essuyez la avec du coton ou un mouchoir. Ne frottez pas le site d'injection. Si besoin, vous pouvez couvrir le site d'injection avec un bandage.