Dernière mise à jour le 30/03/2026
TRUE TEST 36, patch pour test épicutané
Indications thérapeutiques
Classe pharmacothérapeutique : AUTRES MEDICAMENTS POUR DIAGNOSTIC, code ATC : V04CL
TRUE TEST 36, patch pour test épicutané est indiqué comme aide au diagnostic de la dermatite allergique de contact. La dermatite de contact est une réaction inflammatoire qui survient en cas de contact cutané avec une substance à laquelle vous être allergique.
TRUE TEST 36, patch pour test épicutané est un patch prêt à l’emploi permettant de déterminer la cause d’une dermatite allergique de contact.
TRUE TEST 36 est destiné aux adultes.
Le test se compose de trois bandes adhésives chirurgicales. Chaque bande contient 12 patchs. Chaque patch est recouvert d’un film contenant la substance qui peut provoquer une réaction cutanée chez les personnes sensibles. Ces substances sont appelées allergènes. Chaque patch contient différents allergènes, ainsi qu’un patch vierge. TRUE TEST 36, patch pour test épicutané contient 35 des allergènes ou mélanges d’allergènes les plus répandus, ainsi qu’un patch vierge.
TRUE TEST 36, patch pour test épicutané sert à déterminer si vous être allergique à une des substances (allergènes) des patchs. Si une substance à laquelle vous êtes allergique est en contact avec votre peau, cela peut provoquer une réaction inflammatoire appelée dermatite de contact.
On trouve de telles substances dans certains parfums, lotions après rasage, crèmes ou pommades, gants en caoutchouc, produits chimiques, etc. Les substances contenues dans TRUE TEST 36, patch pour test épicutané sont des allergènes bien connus. Si vous être allergique à une substance d’un patch en particulier, la peau en contact avec le patch réagira à la substance, elle deviendra rouge et inflammée. Si vous n’êtes pas allergique à un patch en particulier, la peau en contact avec le patch ne réagira pas. Vous pouvez être allergique à plus d’un patch.
Composition en substances actives
-
Patch n°1 bande 1 ( Composition pour un patch )
- > sulfate de nickel hexahydraté 162 microgrammes
-
Patch n°10 bande 1 ( Composition pour un patch )
- > baume du Pérou 648 microgrammes
-
Patch n°11 bande 1 ( Composition pour un patch )
- > dichlorhydrate d'éthylènediamine 41 microgrammes
-
Patch n°12 bande 1 ( Composition pour un patch )
- > chlorure de cobalt hexahydraté 16 microgrammes
-
Patch n°13 bande 2 ( Composition pour un patch )
- > résine p-tert-butylphénolformaldéhyde 36 microgrammes
-
Patch n°14 bande 2 ( Composition pour un patch )
- > résine époxy 41 microgrammes
-
Patch n°15 bande 2 ( Composition )
- > diphénylguanidine
- > diéthyldithiocarbamate de zinc
- > dibutyldithiocarbamate de zinc
-
Patch n°16 bande 2 ( Composition )
- > isopropylphénylparaphénylènediamine
- > cyclohexylphénylparaphénylènediamine
- > diphénylparaphénylènediamine
-
Patch n°17 bande 2 ( Composition pour un patch )
- > Cl+Me-isothiazolinone 3 microgrammes
-
Patch n°18 bande 2 ( Composition pour un patch )
- > quaternium 15 81 microgrammes
-
Patch n°19 bande 2 ( Composition pour un patch )
- > méthyldibromoglutaronitrile 4,1 microgrammes
-
Patch n°2 bande 1 ( Composition pour un patch )
- > alcools de graisse de laine 810 microgrammes
-
Patch n°20 bande 2 ( Composition pour un patch )
- > p-phénylènediamine 65 microgrammes
-
Patch n°21 bande 2 ( Composition pour un patch )
- formaldéhyde146 microgrammes
- sous forme de : N-hydroxyméthylsuccinimide
- formaldéhyde146 microgrammes
- > morpholinylmercaptobenzothiazole
- > cyclohexylbenzothiazolesulfenamide
- > disulfure de dibenzothiazole
- > thiomersal 6 microgrammes
- > disulfirame
- > disulfure de dipentaméthylènethiurame
- > disulfure de tétraméthylthiurame
- > monosulfure de tétraméthylthiurame
- > diazolidinyl urée 450 microgrammes
- > clioquinol
- > chlorquinaldol
- > pivalate de tixocortol 2,4 microgrammes
- > thiosulfate de sodium d'or 61 microgrammes
- > imidazolidinylurée 490 microgrammes
- > sulfate de néomycine 486 microgrammes
- > budésonide 0,81 microgrammes
- > butyrate d'hydrocortisone 16 microgrammes
- > mercaptobenzothiazole 61 microgrammes
- > bacitracine 490 microgrammes
- > parthénolide 2,4 microgrammes
- > disperse blue 106 41 microgrammes
- > bronopol 200 microgrammes
- > dichromate de potassium 44 microgrammes
- > benzocaïne
- > chlorhydrate de tétracaïne
- > chlorhydrate de cinchocaïne
- > géraniol
- > mousse de chêne
- > hydroxycitronellal
- > alcool cinnamique
- > cinnamaldéhyde
- > eugénol
- > isoeugénol
- > alpha-amylcinnamaldéhyde
- > colophane 972 microgrammes
- > parahydroxybenzoate de méthyle
- > parahydroxybenzoate d'éthyle
- > parahydroxybenzoate de propyle
- > parahydroxybenzoate de butyle
- > parahydroxybenzoate de benzyle
- > Pas de substance active.
Présentations
> 10 x 1 Test de 3 bandes sous sachets (aluminium) de 12 patchs
Code CIP : 34009 302 053 3 4
Déclaration de commercialisation : 05/07/2021
Cette présentation n'est pas agréée aux collectivités
Service médical rendu (SMR)
Pas de SMR disponible pour ce médicament ( plus d'informations dans l'aide )
Amélioration du service médical rendu (ASMR)
Pas d'ASMR disponible pour ce médicament (plus d'informations dans l'aide )
ANSM - Mis à jour le : 06/05/2021
TRUE TEST 36, patch pour test épicutané
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
|
|
|
|
|
|
microgrammes/cm² |
microgrammes/patch |
|
1. Sulfate de nickel |
200 |
162 |
|
2. Alcools de graisse de laine |
1000 |
810 |
|
3. Sulfate de néomycine |
600 |
486 |
|
4. Dichromate de potassium |
54 |
44 |
|
5. Mélange Cainea) |
630 |
510 |
|
6. Mélange de parfumsb) |
430 |
348 |
|
7. Colophane |
1200 |
972 |
|
8. Mélange de parabensc) |
1000 |
810 |
|
9. Patch vierge |
- |
- |
|
10. Baume du Pérou |
800 |
648 |
|
11. Dichlorhydrate d’éthylènediamine |
50 |
41 |
|
12. Chlorure de cobalt hexahydraté |
20 |
16 |
|
Bande 2 : |
|
|
|
|
microgrammes/cm² |
microgrammes/patch |
|
13. Résine de p-tert-butyl phénol formaldéhyde |
45 |
36 |
|
14. Résine époxy |
50 |
41 |
|
15. Mélange Carbad) |
250 |
203 |
|
16. Mélange de caoutchouc noir e) |
75 |
61 |
|
17. Chlorométhylisothiazolinone |
4 |
3 |
|
18. Quaternium-15 |
100 |
81 |
|
19. Méthyldibromoglutaronitrile |
5 |
4,1 |
|
20. p-Phénylènediamine |
80 |
65 |
|
21. Formaldéhydef) |
180 |
146 |
|
22. Mélange Mercaptog) |
75 |
61 |
|
23. Thiomersal |
7 |
6 |
|
24. Mélange Thiuramh) |
27 |
22 |
|
Bande 3 : |
|
|
|
|
microgrammes/cm² |
microgrammes/patch |
|
25. Diazolidinyl urée |
550 |
450 |
|
26. Mélange de quinolinei) |
190 |
154 |
|
27. Tixocortol-21-pivalate |
3,0 |
2,4 |
|
28. Thiosulfate de sodium d’or |
75 |
61 |
|
29. Imidazolidinyl urée |
600 |
490 |
|
30. Budésonide |
1,0 |
0,81 |
|
31. Hydrocortisone-17-butyrate |
20 |
16 |
|
32. Mercaptobenzothiazole |
75 |
61 |
|
33. Bacitracine |
600 |
490 |
|
34. Parthénolide |
3,0 |
2,4 |
|
35. Disperse blue 106 |
50 |
41 |
|
36. 2-bromo-2-nitropropane-1,3-diol |
250 |
200 |
|
a) Cinq portions de benzocaïne, une portion de chlorhydrate de tétracaïne et de chlorhydrate de cinchocaïne. b) Cinq portions de géraniol et de mousse de chêne, quatre portions d’hydroxycitronellal et d’alcool cinnamique, deux portions de cinnamaldéhyde et d’eugénol, et une portion d’isoeugénol et d’alpha-amylcinnamaldéhyde. c) Poids égal de parahydroxybenzoate de méthyle, de parahydroxybenzoate d’éthyle, de parahyroxybenzoate de propyle, de parahydroxybenzoate de butyle et de parahydroxybenzoate de benzyle. d) Poids égal de diphénylguanidine, de diéthyldithiocarbamate de zinc et de dibutyldithiocarbamate de zinc. e) Deux portions de N-isopropyl-N’-phényl paraphénylènediamine, cinq portions de N-cyclohexyl-N’-phényl paraphénylènediamine et cinq portions de N,N’-diphényl paraphénylènediamine. f) Contient du N-hydroxyméthylsuccinimide. g) Poids égal de morpholinylmercaptobenzothiazole, de sulfénamide de N-cyclohexylbenzothiazole et de disulfure de dibenzothiazole. h) Poids égal de disulfirame, de disulfure de dipentaméthylènethiuame, de disulfure de tétraméthylthiurame et de monosulfure de tétraméthylthiurame. i) Poids égal de clioquinol et de chlorquinaldol. |
||
Pour la liste complète des excipients, voir rubrique 6.1.
TRUE TEST 36 se compose de trois bandes adhésives chirurgicales à raison de 12 patchs par bande, soit un total de 36 patchs. 35 de ces patchs sont recouverts d’un film contenant la substance à tester. L’un des patches (patch n° 9) est un patch vierge.
4.1. Indications thérapeutiques
Ce médicament est à usage diagnostique chez l’adulte uniquement.
Diagnostic de la dermatite allergique de contact.
4.2. Posologie et mode d'administration
1) Ouvrir l’étui et sortir la bande de test.
2) Retirer le plastique de protection recouvrant la surface de test de la bande, en veillant à ne pas toucher les substances à tester.
3) Appliquer la bande sur la partie haute du dos du patient, la partie extérieure du haut du bras peut également être recouverte. Lisser la bande à partir du centre vers les bords, en s’assurant que chaque allergène est bien en contact avec la peau. Les deux premières bandes doivent être placées de chaque côté de la colonne vertébrale, à quelques centimètres de la ligne médiane. La troisième bande doit être placée près de l’une des deux autres bandes.
4) Marquer à l’aide d’un crayon médical la position des encoches de chaque bande.
Les bandes doivent être appliquées sur une peau saine, sans cicatrice, acné, dermatite ou tout autre état pouvant interférer avec l’interprétation des réactions au test (voir section 4.4).
Posologie
Le patient doit conserver TRUE TEST 36 pendant 48 heures, sans le retirer et en prenant garde de ne pas le mouiller (eau, transpiration).
Passé ce délai, la bande est retirée. La réaction doit être lue une demie heure après le retrait de la bande, et à nouveau un à deux jours après, c’est-à-dire lorsque les réactions allergiques sont complètement développées et que les éventuelles réactions d’irritation bénignes se sont atténuées.
Certains allergènes (sulfate de néomycine, p-phénylènediamine, alcool de laine, mélange Caine, thiosulfate de sodium d’or, parthénolide, disperse blue 106, bacitracine, imidazolidinyl urée, diazolidinyl urée, budésonide, hydrocortisone-17-butyrate et tixocortol-21-pivalate) peuvent provoquer des réactions qui ne devraient pas apparaître avant 4 à 5 jours après l’application. Les patients doivent être informés qu’ils doivent signaler l’apparition de ce type de réaction. Le cas échéant, une consultation supplémentaire avec une autre lecture 5 à 7 jours plus tard est nécessaire pour surveiller cette réaction tardive.
La réaction au test doit être lue par le médecin.
Interprétation
Toutes les réactions positives doivent être évaluées avec attention, en considérant les antécédents cliniques et les symptômes de chaque patient, en particulier en cas de réaction positive à des allergènes spécifiques présentant des taux de sensibilisation pertinents plus faibles (par ex. thiosulfate de sodium d’or).
Un modèle d’identification est fourni avec chaque boîte de TRUE TEST 36 pour l’identification rapide d’un allergène causant une réaction. Pour assurer un positionnement correct, les marques sur la peau doivent correspondre aux encoches du modèle. Les différences entre la page 1 et 2 du modèle correspondent à la bande 1 et 2.
La méthode d’interprétation recommandée par le Groupe de Recherche International contre la Dermatite de Contact est la suivante :
- Réaction négative
? Réaction douteuse : érythème maculaire faible, peu ou pas d’infiltration
+ Réaction positive faible non vésiculaire) : érythème, infiltration faible, papules possibles
++ Réaction positive forte (vésiculaire) : érythème, infiltration, papules, vésicules
+++ Réaction positive intense : érythème intense, infiltration, vésicules coalescentes
IR Réaction irritante de différents types
NT Non testé
Remarque
· Les patients présentant une réaction négative peuvent être sensibles à d’autres substances non incluses dans ce test. De plus, des faux-négatifs peuvent survenir. Renouveler le test ou effectuer un test avec des substances complémentaires est conseillé.
· Une réaction positive doit correspondre aux caractéristiques d’une réaction allergique (érythème papulaire ou vésiculaire et infiltration).
· Des pustules, tout comme un érythème folliculaire irrégulier ou homogène sans infiltration sont souvent le signe d’une irritation et n’indiquent pas d’allergie.
Le but de l’évaluation d’une réponse positive au test n’est pas de déterminer le nombre de points positifs, mais de déterminer si la réponse est réellement une réaction positive (causée par une allergie) ou une réaction d’irritation non spécifique.
Population pédiatrique
La sécurité et l’efficacité de TRUE TEST 36 chez les enfants n’ont pas encore été établies. TRUE TEST 36 est indiqué uniquement chez l’adulte.
Hypersensibilité à l’un des excipients, outre les substances actives, mentionnés à la rubrique 6.1.
4.4. Mises en garde spéciales et précautions d'emploi
Une sensibilisation à une substance de TRUE TEST 36 ne se produit que rarement. Une réaction qui n’apparaît qu’au bout de 10 jours ou plus peut traduire une sensibilisation de contact (voir rubrique 4.8).
Le syndrome de la peau excitée (syndrome du « dos en colère » ou « angry back ») est un état d’hyperréactivité induit par une dermatite sur une autre partie du corps ou par une forte réaction cutanée positive. De ce fait, les résultats du test doivent être évalués avec attention chez les patients présentant des résultats positifs multiples concomitants. Les réactions faussement positives pourront être décelées en procédant à de nouveaux tests ultérieurement.
L’utilisation de TRUE TEST 36 chez les patients ayant des antécédents de réactions anaphylactoïdes doit être évaluée avec précaution avant l’application.
Il convient d’éviter toute transpiration excessive ou exposition au soleil de la zone d’application de la bande. Le bronzage peut diminuer la réactivité au test et causer des résultats faux-négatifs.
Eviter d’appliquer la bande sur une peau présentant de l’acné, des cicatrices, des zones de dermatite ou tout autre état pouvant interférer avec les résultats du test.
Si une réaction cutanée grave se développe, le patient pourra être traité avec un corticostéroïde local, ou, dans de rares cas, avec un corticostéroïde systémique.
L’hydroxyanisole butylé (BHA) (E320) et l’hydroxytoluène butylé (BHT) (E312) sont présents en tant qu’antioxydants dans la colophane, soit l’allergène n° 7 (bande 1). Le BHA et BHT peuvent causer des réactions cutanées locales (par exemple : dermatite de contact), une réaction faux-positif à la colophane peut donc se produire.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
L’utilisation d’immunosuppresseurs (dont les stéroïdes) peut empêcher une réaction positive au test.
L’usage de stéroïdes topiques sur la zone d'application des bandes ou l'usage de stéroïdes oraux (en quantité équivalente à 20 mg de prednisolone ou plus par jour) devra être interrompu au moins deux semaines avant l’utilisation de TRUE TEST 36.
Aucune étude d’interaction n’a été réalisée.
4.6. Fertilité, grossesse et allaitement
Il n’existe aucune donnée sur l’utilisation de TRUE TEST 36 chez la femme enceinte. Les études chez l’animal sont insuffisantes en ce qui concerne la toxicité sur la reproduction. TRUE TEST 36 n’est pas recommandée pendant la grossesse, sauf s’il est indispensable, et ne doit pas être utilisé pendant l’allaitement.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Les effets indésirables suivants ont été rapportés lors des études cliniques et sont classés selon la convention de fréquences suivante : très fréquent (≥ 1/10) ; fréquent (≥ 1/100 à < 1/10) ; peu fréquent (≥ 1/1 000 à < 1/100) ; rare (≥ 1/10 000 à < 1/1 000) ; très rare (< 1/10 000) ; fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
|
Classes système organe |
Fréquence |
Effets indésirables |
|
Troubles cutanés et des tissus sous-cutanés |
Très fréquent (≥ 1/10) |
Réaction de longue durée, sensation de brûlure |
|
Fréquent (³ 1/100 à < 1/10) |
Hypopigmentation/hyperpigmentation temporaire, érythème |
|
|
Peu fréquent (³ 1/1 000 à < 1/100) |
Poussée de dermatite |
|
|
Rare (³ 1/10 000 à < 1/1 000) |
Sensibilisation |
|
|
Troubles généraux et anomalies au site d’administration |
Très fréquent (≥ 1/10) |
Irritation causée par la bande adhésive chirurgicale |
|
Affections du système immunitaire |
Rare (³ 1/10 000 à < 1/1 000) |
Sensibilisation |
|
Fréquence indéterminée |
Réactions anaphylactiques*, hypersensibilité* |
* d’après les données post-commercialisation.
Dans de très rares cas et seulement avec certaines substances, des réactions anaphylactiques (réaction systémique, éventuellement accompagnée d’une chute de la pression artérielle pouvant être mortelle) se sont produites. Le service traitant les allergies est, pour d’autres raisons, préparé à traiter de tels événements. Les réactions de type anaphylactiques liées à l’application de TRUE TEST 36 n’ont pas été documentées.
L’irritation causée par la bande adhésive chirurgicale disparaît rapidement.
Une réaction positive à TRUE TEST 36 disparaît généralement en 1 à 2 semaines. Les réactions de longue durée sont des réactions positives, qui persistent pendant quelques semaines ou mois.
Une réaction positive à TRUE TEST 36 peut laisser une zone d’hypopigmentation ou d’hyperpigmentation transitoire sur la zone d’application.
Une poussée de dermatite peut être observée si on réalise le test au cours d’une phase active de dermatite.
Sensibilisation (voir rubrique 4.4).
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.signalement-sante.gouv.fr.
Sans objet.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : AUTRES MEDICAMENTS POUR DIAGNOSTIC, Code ATC : V04CL.
Une réaction positive au test est une réaction classique d'hypersensibilité retardée (type IV), qui peut apparaître entre 6 et 96 heures après l'exposition.
La réponse à médiation cellulaire implique les cellules de Langerhans et les lymphocytes T, qui interagissent et produisent des lymphokines. Ces lymphokines forment ensuite des clones de lymphocytes, stimulent les macrophages et déclenchent une inflammation cutanée.
Les signes cliniques d'une réaction de dermatite de contact sont : l'érythème, l'œdème, les papules, les vésicules ainsi qu’un infiltrat inflammatoire dermique palpable au niveau de la zone d'application.
5.2. Propriétés pharmacocinétiques
Sans objet.
5.3. Données de sécurité préclinique
Les données non cliniques n’ont pas révélé de risque de toxicité aiguë. Un potentiel cancérigène a été montré pour certaines substances dans les études chez l’animal. Toutefois, ces résultats ne représentent pas de risque significatif supplémentaire concernant l’utilisation clinique de TRUE TEST 36 étant donné la dose, le temps d’exposition et/ou les autres modes d’exposition aux mêmes substances.
2 ans.
6.4. Précautions particulières de conservation
A conserver au réfrigérateur (entre 2°C et 8°C).
6.5. Nature et contenu de l'emballage extérieur
Chaque bande est recouverte d’une feuille protectrice de polyéthylène traité à la silicone, puis emballée dans des sachets hermétiques d’emballage stratifié.
Pour des raisons de stabilité, la bande 2 contient un dessiccatif.
Boîte contenant 10 tests.
Un test = une bande 1, une bande 2, une bande 3 et un modèle d’interprétation.
De plus, le conditionnement contient une notice d’utilisation pour le patient.
6.6. Précautions particulières d’élimination et de manipulation
Pas d’exigences particulières pour l’élimination.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
HERREDSVEJEN 2
3400 HILLEROED
DANEMARK
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 302 053 3 4 : Test de 3 bandes sous sachets (aluminium) de 12 patchs. Boîte de 10.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
Date de première autorisation:{JJ mois AAAA}
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
{JJ mois AAAA}
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste II
ANSM - Mis à jour le : 06/05/2021
TRUE TEST 36, patch pour test épicutané
TRUE TEST 36, patch pour test épicutané se compose de trois bandes adhésives chirurgicales à raison de 12 patchs par bande. 35 de ces patchs sont recouverts d’un film contenant la substance à tester.
|
Bande 1 : |
|
|
|
|
microgrammes/cm² |
microgrammes/patch |
|
1. Sulfate de nickel |
200 |
162 |
|
2. Alcools de graisse de laine |
1000 |
810 |
|
3. Sulfate de néomycine |
600 |
486 |
|
4. Dichromate de potassium |
54 |
44 |
|
5. Mélange Cainea) |
630 |
510 |
|
6. Mélange de parfumsb) |
430 |
348 |
|
7. Colophane |
1200 |
972 |
|
8. Mélange de parabensc) |
1000 |
810 |
|
9. Patch vierge |
- |
- |
|
10. Baume du Pérou |
800 |
648 |
|
11. Dichlorhydrate d’éthylènediamine |
50 |
41 |
|
12. Chlorure de cobalt hexahydraté |
20 |
16 |
|
Bande 2 : |
|
|
|
|
microgrammes/cm² |
microgrammes/patch |
|
13. Résine de p-tert-butyl phénol formaldéhyde |
45 |
36 |
|
14. Résine époxy |
50 |
41 |
|
15. Mélange Carbad) |
250 |
203 |
|
16. Mélange de caoutchouc noir e) |
75 |
61 |
|
17. Chlorométhylisothiazolinone |
4 |
3 |
|
18. Quaternium-15 |
100 |
81 |
|
19. Méthyldibromoglutaronitrile |
5 |
4,1 |
|
20. p-Phénylènediamine |
80 |
65 |
|
21. Formaldéhydef) |
180 |
146 |
|
22. Mélange Mercaptog) |
75 |
61 |
|
23. Thiomersal |
7 |
6 |
|
24. Mélange Thiuramh) |
27 |
22 |
|
Bande 3 : |
|
|
|
|
microgrammes/cm² |
microgrammes/patch |
|
25. Diazolidinyl urée |
550 |
450 |
|
26. Mélange de quinolinei) |
190 |
154 |
|
27. Tixocortol-21-pivalate |
3,0 |
2,4 |
|
28. Thiosulfate de sodium d’or |
75 |
61 |
|
29. Imidazolidinyl urée |
600 |
490 |
|
30. Budésonide |
1,0 |
0,81 |
|
31. Hydrocortisone-17-butyrate |
20 |
16 |
|
32. Mercaptobenzothiazole |
75 |
61 |
|
33. Bacitracine |
600 |
490 |
|
34. Parthénolide |
3,0 |
2,4 |
|
35. Disperse blue 106 |
50 |
41 |
|
36. 2-bromo-2-nitropropane-1,3-diol |
250 |
200 |
|
a) Cinq portions de benzocaïne, une portion de chlorhydrate de cinchocaïne et de chlorhydrate de tétracaïne. b) Cinq portions de géraniol et de mousse de chêne, quatre portions d’hydroxycitronellal et d’alcool cinnamique, deux portions de cinnamaldéhyde et d’eugénol, et une portion d’isoeugénol et d’alpha-amylcinnamaldéhyde. c) Poids égal de parahydroxybenzoate de méthyle, de parahydroxybenzoate d’éthyle, de parahyroxybenzoate de propyle, de parahydroxybenzoate de butyle et de parahydroxybenzoate de benzyle. d) Poids égal de diphénylguanidine, de diéthyldithiocarbamate de zinc et de dibutyldithiocarbamate de zinc. e) Deux portions de N-isopropyl-N’-phényl paraphénylènediamine, cinq portions de N-cyclohexyl-N’-phényl paraphénylènediamine et cinq portions de N,N’-diphényl paraphénylènediamine. f) Contient du N-hydroxyméthylsuccinimide. g) Poids égal de morpholinylmercaptobenzothiazole, de sulfénamide de N-cyclohexylbenzothiazole et de disulfure de dibenzothiazole. h) Poids égal de disulfirame, de disulfure de dipentaméthylènethiuame, de disulfure de tétraméthylthiurame et de monosulfure de tétraméthylthiurame. i) Poids égal de clioquinol et de chlorquinaldol. |
||
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin, votre pharmacien ou votre infirmier/ère.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin votre pharmacien ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que TRUE TEST 36, patch pour test épicutané et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d’utiliser TRUE TEST 36, patch pour test épicutané ?
3. Comment utiliser TRUE TEST 36, patch pour test épicutané ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver TRUE TEST 36, patch pour test épicutané ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE TRUE TEST 36, patch pour test épicutané ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : AUTRES MEDICAMENTS POUR DIAGNOSTIC, code ATC : V04CL
TRUE TEST 36, patch pour test épicutané est indiqué comme aide au diagnostic de la dermatite allergique de contact. La dermatite de contact est une réaction inflammatoire qui survient en cas de contact cutané avec une substance à laquelle vous être allergique.
TRUE TEST 36, patch pour test épicutané est un patch prêt à l’emploi permettant de déterminer la cause d’une dermatite allergique de contact.
TRUE TEST 36 est destiné aux adultes.
Le test se compose de trois bandes adhésives chirurgicales. Chaque bande contient 12 patchs. Chaque patch est recouvert d’un film contenant la substance qui peut provoquer une réaction cutanée chez les personnes sensibles. Ces substances sont appelées allergènes. Chaque patch contient différents allergènes, ainsi qu’un patch vierge. TRUE TEST 36, patch pour test épicutané contient 35 des allergènes ou mélanges d’allergènes les plus répandus, ainsi qu’un patch vierge.
TRUE TEST 36, patch pour test épicutané sert à déterminer si vous être allergique à une des substances (allergènes) des patchs. Si une substance à laquelle vous êtes allergique est en contact avec votre peau, cela peut provoquer une réaction inflammatoire appelée dermatite de contact.
On trouve de telles substances dans certains parfums, lotions après rasage, crèmes ou pommades, gants en caoutchouc, produits chimiques, etc. Les substances contenues dans TRUE TEST 36, patch pour test épicutané sont des allergènes bien connus. Si vous être allergique à une substance d’un patch en particulier, la peau en contact avec le patch réagira à la substance, elle deviendra rouge et inflammée. Si vous n’êtes pas allergique à un patch en particulier, la peau en contact avec le patch ne réagira pas. Vous pouvez être allergique à plus d’un patch.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER TRUE TEST 36, patch pour test épicutané ?
N’utilisez jamais TRUE TEST 36, patch pour test épicutané :
· si vous souffrez de dermatite grave ou généralisée, le test devra être repoussé jusqu’à la fin de la phase aigüe de la dermatite.
· si vous êtes allergique à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
Avertissements et précautions
· Eviter toute exposition au soleil au niveau de la zone d’application. Le bronzage pourrait empêcher la détection de réactions positives aux allergènes auxquels vous êtes allergique ;
· Eviter toute transpiration excessive lorsque la bande est appliquée ;
· Si vous prenez des médicaments qui affaiblissent votre système immunitaire comme les stéroïdes (prednisolone) ou utilisez des crèmes contenant des stéroïdes (hydrocortisone). Leur utilisation doit être interrompue au moins 2 semaines avant l’application du test ;
· Si vous souffrez de syndrome de la peau excitable (syndrome du « dos en colère » ou « angry back »), un état d’hyperréactivité causé par une réaction sur une autre partie du corps. Si votre peau réagit à tous les patchs, il peut être utile de renouveler le test ultérieurement ;
· Si vous avez des antécédents de réactions anaphylactoïdes, l’utilisation de TRUE TEST 36, patch pour test épicutané doit être évaluée avec précaution.
Adressez-vous à votre médecin avant d’utiliser TRUE TEST 36, patch pour test épicutané si vous êtes dans l’un des cas ci-dessus. Votre médecin vous indiquera si vous pouvez l’utiliser.
Sensibilisation
Dans de rares cas, vous pouvez développer une sensibilité à l’une des substances contenues dans les patchs lors de l’application de TRUE TEST 36, patch pour test épicutané. Une réaction qui n’apparaît qu’au bout de 10 jours ou plus peut traduire une sensibilisation de contact.
TRUE TEST 36, patch pour test épicutané doit être appliqué uniquement sur une peau :
· Sans acné
· Sans cicatrices
· Sans dermatite
· Exempte de tout autre état pouvant interférer avec les résultats du test. Vous pouvez consulter votre médecin en cas de doute.
Les bandes adhésives doivent être tenues à l’écart de l’humidité, vous devez donc veiller à ne pas les mouiller lors du bain ou de la douche. Si elles prennent l’humidité, elles risquent de se décoller, provoquant l’élimination des substances à tester.
Eviter toute exposition au soleil ou activité physique, car les bandes pourraient se décoller.
L’hydroxyanisole butylé (BHA) (E320) et l’hydroxytoluène butylé (BHT) (E312) sont présents en tant qu’antioxydants dans la colophane, soit l’allergène n° 7 (bande 1) pour des raisons de stabilité. Le BHA et BHT peuvent causer des réactions cutanées locales (par exemple : dermatite de contact), une réaction faux-positif à la colophane peut donc se produire.
Enfants
L’utilisation de TRUE TEST 36, patch pour test épicutané n’est pas conseillée chez les enfants, sa sécurité et son efficacité n’ayant pas été démontrées dans cette population.
Autres médicaments et TRUE TEST 36, patch pour test épicutané
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament, y compris les médicaments pouvant être obtenus sans ordonnance, avant l’utilisation de TRUE TEST 36, patch pour test épicutané. Notez que votre dermatologue n’a pas connaissance des autres médicaments que vous prenez.
Les stéroïdes peuvent empêcher une réaction cutanée positive, leur usage sur la zone d'application des bandes ou l'usage de stéroïdes oraux (en quantité équivalente à 20 mg de prednisolone ou plus par jour) devra être interrompu au moins deux semaines avant l’utilisation de TRUE TEST 36, patch pour test épicutané.
TRUE TEST 36, patch pour test épicutané avec des aliments et boissons
Sans objet.
Grossesse, allaitement et fertilité
TRUE TEST 36, patch pour test épicutané n’est pas indiqué chez la femme enceinte. Informez votre médecin si vous être enceinte ou si vous pensez l’être.
Ne pas allaiter pendant l’utilisation de TRUE TEST 36, patch pour test épicutané.
Conduite de véhicules et utilisation de machines
TRUE TEST 36, patch pour test épicutané n’affecte pas la conduite de véhicule ni l’utilisation de machines. Parlez-en à votre médecin si vous avez le moindre doute.
3. COMMENT UTILISER TRUE TEST 36, patch pour test épicutané ?
TRUE TEST 36 est appliqué par votre médecin.
|
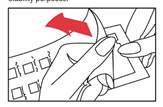
1) Ouvrir l’étui de la bande TRUE TEST 36, patch pour test épicutané et sortir celle-ci. |
|
|
|
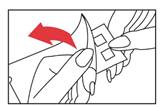
2) Retirer le plastique de protection recouvrant la surface de la bande, en veillant à ne pas toucher les patchs. Un dessiccatif est ajouté à l’emballage de la bande 2 pour des raisons de stabilité. |
|
|
|
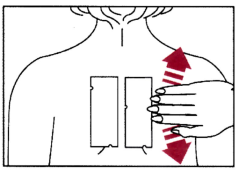
3) Appliquer la bande sur le dos du patient, la partie extérieure du haut du bras peut également être recouverte. Lisser la bande à partir du centre vers les bords, en s’assurant que chaque allergène est bien en contact avec la peau. Les deux bandes doivent être placées de chaque côté à quelques centimètres de la ligne médiane. La bande 3 est placée juste à côté de l’une des deux autres bandes. |
|
|
|
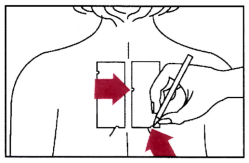
4) Marquer à l’aide d’un crayon médical la position des encoches de chaque bande (en haut à gauche et sur le bord inférieur).
|
Vous devez conserver la bande pendant 48 heures sans la retirer, en veillant à ne pas la mouiller (eau, transpiration).
Si les bandes sont retirées ou décollées trop tôt, il est possible qu’une réaction positive à une substance à laquelle vous êtes allergique ne soit pas mise en évidence lors du test. Contactez votre médecin si les bandes ont été retirées ou décollées au cours des 48 heures d’application.
Après 48 heures, vous ou votre médecin pouvez retirer la bande.
A quel moment doivent être lus les résultats ?
Votre médecin pourra lire les résultats 30 minutes après avoir retiré la bande, et une nouvelle fois 1 à 2 jours après, lorsque les réactions allergiques sont complètement développées et que les éventuelles réactions d’irritation bénignes se sont atténuées. Certains allergènes peuvent parfois causer une réaction n’apparaissant que 4 à 5 jours après avoir retiré la bande. Informez votre médecin si cela se produit.
Comment votre médecin va-t-il interpréter les résultats ?
Le médecin examinera la zone d’application du test à la recherche de signes indiquant une réaction allergique. Cette réaction se présente de manière générale par une éruption cutanée avec un gonflement, des rougeurs et de minuscules cloques. Les rougeurs seules ne traduisent pas nécessairement une réaction allergique. Si vous êtes allergique, votre médecin vous donnera des informations concernant :
· Les conditions dans lesquelles vous pouvez être amené à vous trouver quotidiennement au contact des substances incriminées ;
· Le meilleur moyen pour éviter ces substances. Votre médecin peut vous proposer des alternatives aux substances à éviter.
Vérifiez auprès de votre médecin ou pharmacien en cas de doute.
Consulter votre médecin si vous ressentez une gêne importante sur la zone d’application du test. Votre médecin pourra décider du retrait des bandes si nécessaire.
Si vous oubliez d’utiliser TRUE TEST 36, patch pour test épicutané
Si vous arrêtez d’utiliser TRUE TEST 36, patch pour test épicutané
Sans objet.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Effets indésirables très fréquents (peuvent affecter plus d’une personne sur 10) :
· Irritation causée par la bande adhésive chirurgicale, mais qui disparaît rapidement ;
· Sensation de brûlure ;
· Réactions de longue durée. Une réaction positive disparaît généralement en 1 à 2 semaines, tandis qu’une réaction de longue durée peut durer plusieurs semaines ou mois.
Effets indésirables fréquents (peuvent affecter jusqu’à 1 personne sur 10) :
· Les réactions au test peuvent provoquer une hypopigmentation ou hyperpigmentation de la peau temporaire ;
· Rougeur de la peau causée par une irritation ou une inflammation (érythème).
Effets indésirables peu fréquents (peuvent affecter jusqu’à 1 personne sur 100) :
· Poussée de dermatite.
Effets indésirables rares (peuvent affecter jusqu’à 1 personne sur 1 000) :
· Sensibilisation à une substance de TRUE TEST 36 après utilisation du test.
Fréquence indéterminée (ne peut être estimée sur la base des données disponibles) :
· Réaction anaphylactique (réaction systémique, éventuellement accompagnée d’une chute de la pression artérielle pouvant être mortelle) ;
· Hypersensibilité (réaction allergique).
Dans de très rares cas et seulement avec certaines substances, des réactions anaphylactiques (réaction systémique, éventuellement accompagnée d’une chute de la pression artérielle pouvant être mortelle) se sont produites. Le service traitant les allergies est, pour d’autres raisons, préparé à traiter de tels événements. Les réactions de type anaphylactiques liées à l’application de TRUE TEST 36 n’ont pas été documentées.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: www.signalement-sante.gouv.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER TRUE TEST 36, patch pour test épicutané ?
A conserver au réfrigérateur (2°C à 8°C).
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur la boîte. La date de péremption fait référence au dernier jour de ce mois.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient TRUE TEST 36, patch pour test épicutané
· En plus des substances actives listées en première page, le test contient les excipients suivants :
Bande de fibres de polyester avec liant (copolymère d’éthylène-acétate de vinyle) et adhésif acrylique, film de polyester, povidone 90, hydroxypropyle cellulose, méthylcellulose, β-cyclodextrine, carbonate de sodium, bicarbonate de sodium, butylhydroxyanisole, butylhydroxytoluène.
Qu’est-ce que TRUE TEST 36, patch pour test épicutané et contenu de l’emballage extérieur
Chaque bande est recouverte d’une feuille protectrice de polyéthylène traité à la silicone, puis emballée dans des sachets hermétiques d’emballage stratifié.
L’emballage de la bande 2 contient également un dessiccatif pour conserver les allergènes.
Contenu de la boîte : 10 tests (un test = une bande 1, une bande 2 et une bande 3).
Titulaire de l’autorisation de mise sur le marché
HERREDSVEJEN 2
3400 HILLERØD
DANEMARK
Exploitant de l’autorisation de mise sur le marché
6 RUE ALEXIS DE TOCQUEVILLE
92160 ANTONY
FRANCE
HERREDSVEJEN 2
3400 HILLERØD
DANEMARK
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
{mois AAAA}.
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
A découper -----------------------------------------------------------------------------------------------------------------------
Les informations suivantes sont destinées exclusivement aux professionnels de santé :
Un modèle d’identification est fourni avec chaque boîte de TRUE TEST 36 pour l’identification rapide d’un allergène causant une réaction. Pour assurer un positionnement correct, les marques sur la peau doivent correspondre aux encoches du modèle. Les différences entre la page 1 et 2 du modèle correspondent à la bande 1 et 2.
La méthode d’interprétation recommandée par le Groupe de Recherche International contre la Dermatite de Contact est la suivante :
- Réaction négative
? Réaction douteuse : érythème maculaire faible, peu ou pas d’infiltration
+ Réaction positive faible (non vésiculaire) : érythème, infiltration faible, papules possibles
++ Réaction positive forte (vésiculaire) : érythème, infiltration, papules, vésicules
+++ Réaction positive intense : érythème intense, infiltration, vésicules coalescentes
IR Réaction irritante de différents types
NT Non testé
Remarque
· Les patients présentant une réaction négative peuvent être sensibles à d’autres substances non incluses dans ce test. De plus, des faux-négatifs peuvent survenir. Renouveler le test ou effectuer un test avec des substances complémentaires est conseillé.
· Une réaction positive doit correspondre aux caractéristiques d’une réaction allergique (érythème papulaire ou vésiculaire et infiltration).
· Des pustules, tout comme un érythème folliculaire irrégulier ou homogène sans infiltration sont souvent le signe d’une irritation et n’indiquent pas d’allergie.
Le but de l’évaluation d’une réponse positive au test n’est pas de déterminer le nombre de points positifs, mais de déterminer si la réponse est réellement une réaction positive (causée par une allergie) ou une réaction d’irritation non spécifique.
Certains allergènes (sulfate de néomycine, p-phénylènediamine, alcool de laine, mélange Caine, thiosulfate de sodium d’or, parthénolide, disperse blue 106, bacitracine, imidazolidinyl urée, diazolidinyl urée, budésonide, hydrocortisone-17-butyrate et tixocortol-21-pivalate) peuvent provoquer des réactions qui ne devraient pas apparaître avant 4 à 5 jours après l’application. Les patients doivent être informés qu’ils doivent signaler l’apparition de ce type de réaction. Le cas échéant, une consultation supplémentaire avec une autre lecture 5 à 7 jours plus tard est nécessaire pour surveiller cette réaction tardive.
Toutes les réactions positives doivent être évaluées avec attention, en considérant les antécédents cliniques et les symptômes de chaque patient, en particulier en cas de réaction positive à des allergènes spécifiques présentant des taux de sensibilisations pertinents plus faibles (par ex. thiosulfate de sodium d’or).
Contre-indications
Dermatite grave ou généralisée. Ce test devra être repoussé jusqu’à la fin de la phase aigüe de la dermatite de contact.
Hypersensibilité à l’un des excipients, outre les substances actives, contenus dans ce test.
Mises en garde spéciales et précautions d’emploi
Une sensibilisation à une substance des bandes du test ne se produit que rarement. Une réaction au test qui n’apparaît qu’au bout de 10 jours ou plus peut traduire une sensibilisation de contact.
Le syndrome de la peau excitable (syndrome du « dos en colère » ou « angry back ») est un état d’hyperréactivité induit par une dermatite sur une autre partie du corps ou par une forte réaction cutanée positive. De ce fait, les résultats du test doivent être évalués avec attention chez les patients présentant des résultats positifs multiples concomitants. Les réactions faussement positives pourront être décelées en procédant à de nouveaux tests ultérieurement.
L’utilisation de TRUE TEST 36 chez les patients ayant des antécédents de réactions anaphylactoïdes doit être évaluée avec précaution avant l’application.
Il convient d’éviter toute transpiration excessive ou exposition au soleil de la zone d’application de la bande. Le bronzage peut diminuer la réactivité au test et causer des résultats faux-négatifs.
Eviter d’appliquer la bande sur une peau présentant de l’acné, des cicatrices, des zones de dermatite ou tout autre état pouvant interférer avec les résultats du test.
Si une réaction cutanée grave se développe, le patient pourra être traité avec un corticostéroïde local, ou, dans de rares cas, avec un corticostéroïde systémique.
L’hydroxyanisole butylé (BHA) (E320) et l’hydroxytoluène butylé (BHT) (E312) sont présents en tant qu’antioxydants dans la colophane, soit l’allergène n° 7 (bande 1). Le BHA et BHT peuvent causer des réactions cutanées locales (par exemple : dermatite de contact), une réaction faux-positif à la colophane peut donc se produire.