Dernière mise à jour le 28/04/2026
FIXAPOST 50 microgrammes/ml + 5 mg/ml, collyre en solution
Indications thérapeutiques
FIXAPOST est indiqué pour faire baisser la pression intraoculaire chez les patients atteints de glaucome à angle ouvert ou d’hypertonie intraoculaire. Ces deux pathologies sont liées à une augmentation de la pression interne de l’œil qui risque éventuellement d’endommager votre vue. Votre médecin prescrira FIXAPOST quand d’autres médicaments n’auront pas agi de manière adéquate.
FIXAPOST est un collyre en solution sans conservateur.
Présentations
> 1 flacon(s) multidose(s) polyéthylène haute densité (PEHD) de 6 ml avec fermeture de sécurité avec pompe
Code CIP : 34009 302 186 0 0
Déclaration de commercialisation : 12/10/2023
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 23,89 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 24,91 €
- Taux de remboursement :65 %
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 07/04/2021 | Inscription (CT) | Le service médical rendu par FIXAPOST (latanoprost, timolol) est important dans l’indication de l’AMM. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 07/04/2021 | Inscription (CT) | Cette spécialité est un complément de gamme qui n’apporte pas d’amélioration du service médical rendu (ASMR V) par rapport à la présentation déjà inscrite. |
ANSM - Mis à jour le : 28/10/2025
FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Latanoprost.......................................................................................................... 50 microgrammes
Timolol (sous forme de maléate de timolol)............................................................................... 5 mg
Pour 1 ml de solution.
Une goutte contient environ 1,5 microgrammes de latanoprost et 0,15 mg de timolol.
Excipient à effet notoire : 1 ml de collyre en solution contient 50 mg d’hydroxystéarate de macrogolglycérol (huile de ricin hydrogénée polyoxyéthylénée).
Pour la liste complète des excipients, voir rubrique 6.1.
La solution est légèrement jaune et opalescente, pratiquement exempte de particules.
pH : 5,7 – 6,2.
Osmolalité : 300 - 340 mosmol/kg.
4.1. Indications thérapeutiques
4.2. Posologie et mode d'administration
Adultes (y compris le sujet âgé)
La posologie recommandée est d'une goutte dans l'œil (les yeux) atteint(s) une fois par jour.
En cas d'oubli, le traitement doit être poursuivi normalement par l'instillation suivante. La dose ne doit pas dépasser une goutte par jour dans l'œil (les yeux) atteint(s).
Population pédiatrique
Chez les enfants et les adolescents, l'efficacité et la tolérance de FIXAPOST n'ont pas été établies.
Mode d’administration
Voie ophtalmique.
Comme pour tout collyre, afin de réduire une possible absorption systémique, une pression du sac lacrymal (occlusion ponctuelle) au niveau du canthus interne, pendant deux minutes, est recommandée après chaque instillation.
Les lentilles de contact doivent être retirées avant l'instillation du collyre et peuvent être remises 15 minutes après.
En cas d'utilisation concomitante de plusieurs collyres, les instillations de chacun des collyres doivent être espacées d'au moins cinq minutes.
Les patients doivent être informés qu’il faut éviter de mettre en contact l’extrémité du flacon avec l'œil ou les parties avoisinantes de l’œil.
Ce médicament est une solution stérile qui ne contient pas de conservateur. Les patients doivent aussi être informés que les solutions ophtalmiques, incorrectement manipulées, peuvent être contaminées par des bactéries communes, connues pour entraîner des infections oculaires. L’usage de solutions contaminées peut provoquer des lésions graves de l’œil et une perte de vision.
Précautions à prendre avant la manipulation ou l’administration du médicament
Avant la première utilisation :
- Veuillez vérifier que le bouchon d’inviolabilité est intact. Dévissez ensuite fermement le bouchon d’inviolabilité pour ouvrir le flacon.
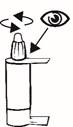
- Lavez-vous soigneusement les mains et enlevez le bouchon de l’embout du flacon. Appuyez plusieurs fois avec le flacon à l'envers, pour activer le mécanisme de pompe jusqu'à ce que la première goutte apparaisse. Ce processus est à effectuer seulement lors de la toute première utilisation et ne sera pas nécessaire lors des administrations suivantes.
1. Avant chaque utilisation, se laver soigneusement les mains et enlever le bouchon de l'embout du flacon. Évitez tout contact entre l'embout du flacon et les doigts.
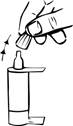
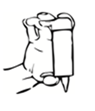
2. Placer le pouce sur la languette située en haut du flacon et l’index sur la base du flacon. Ensuite, placer le majeur sur la seconde languette située à la base du flacon. Tenir le flacon à l’envers.
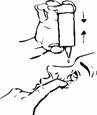
3. Pour l’utiliser, inclinez votre tête légèrement vers l’arrière et maintenez le compte-goutte du flacon à la verticale au-dessus de l’œil. Avec l’index de l’autre main, tirez légèrement la paupière inférieure vers le bas. L'espace créé est appelé le sac conjonctival inférieur. Eviter tout contact entre l’embout du flacon et vos doigts ou vos yeux.
Afin d’instiller une goutte dans le sac conjonctival inférieur de l’œil ou les yeux atteint(s), appuyer brièvement et fermement sur le flacon. Grâce au système automatique, une goutte est libérée précisemment à chaque pompage.
Si la goutte ne tombe pas, secouez doucement le flacon afin de libérer la goutte restée sur l’embout. Dans ce cas, répétez l’étape 3.
4. Une compression du canal lacrymal ou une fermeture des paupières pendant 2 minutes réduit l'absorption systémique. Cela peut entrainer une diminution des effets secondaires systémiques et une augmentation de l'activité locale.
5. Fermez l’extrémité du flacon avec le bouchon immédiatement après l’utilisation.
FIXAPOST est contre-indiqué chez les patients présentant :
· Une hypersensibilité à l’une des substances actives ou à l’un des excipients mentionnés à la rubrique 6.1.
· Des pathologies associées à une hyperréactivité bronchique notamment asthme ou antécédents d’asthme et bronchopneumopathie chronique obstructive sévère.
· Une bradycardie sinusale, une maladie du sinus coronarien, un bloc sino-auriculaire, un bloc auriculo-ventriculaire du second ou du troisième degré non contrôlé par un pace-maker, une insuffisance cardiaque confirmée, un choc cardiogénique.
4.4. Mises en garde spéciales et précautions d'emploi
Comme tout agent ophtalmique appliqué localement, FIXAPOST a un passage systémique. Du fait de la présence de timolol, composant bêta-adrénergique, des effets indésirables cardiovasculaires, pulmonaires et d’autres effets indésirables identiques à ceux rencontrés avec les agents bloquants bêta-adrénergiques administrés par voie systémique, peuvent se produire.
La fréquence des effets indésirables systémiques après administration par voie ophtalmique locale est plus faible qu’après administration par voie générale. Pour réduire l’absorption systémique, voir rubrique 4.2.
Troubles cardiaques
Chez les patients souffrant de maladies cardiovasculaires (maladie coronarienne, angor de Prinzmetal, et insuffisance cardiaque), et d’hypotension, le traitement par bêta-bloquants doit être soigneusement évalué et un traitement par d’autres substances actives doit être considéré. Chez ces patients une surveillance doit être effectuée afin de rechercher des signes d’aggravation de ces pathologies ou des effets indésirables.
En raison de leur effet dromotrope négatif, les bêta-bloquants ne devront être prescrits qu’avec prudence aux patients atteints d’un bloc cardiaque de premier degré.
Après administration de timolol, des effets cardiaques et rarement, des décès en association avec des insuffisances cardiaques ont été rapportés.
Troubles vasculaires
Les patients souffrant de troubles sévères de la circulation périphérique (c'est-à-dire la forme sévère de la maladie ou du syndrome de Raynaud) doivent être traités avec prudence.
Troubles respiratoires
Chez les patients asthmatiques, des manifestations respiratoires pouvant aller jusqu'au décès par bronchospasme ont été rapportées après administration de certains bêta-bloquants ophtalmiques. FIXAPOST doit être administré avec prudence chez les patients souffrant de bronchopneumopathie chronique obstructive (BPCO) modérée à sévère et seulement si le bénéfice potentiel semble supérieur au risque potentiel.
Hypoglycémie/Diabète
Les bêta-bloquants doivent être administrés avec prudence chez les patients sujets à des hypoglycémies spontanées ou chez les patients présentant un diabète instable dans la mesure où les bêta-bloquants sont susceptibles de masquer les signes d’une hypoglycémie aiguë.
Hyperthyroïdie
Les bêta-bloquants peuvent également masquer les signes d'hyperthyroïdie.
Maladies cornéennes
Les bêta-bloquants ophtalmiques peuvent entrainer une sécheresse oculaire. Les patients souffrant de maladies cornéennes doivent être traités avec prudence.
Autres agents bêta-bloquants
L’effet sur la pression intra-oculaire ou les effets connus des bêta-bloquants systémiques peuvent être majorés en cas d'administration de timolol à des patients recevant déjà un bêta-bloquant par voie orale. La réponse de ces patients doit être surveillée attentivement.
L’utilisation concomitante de deux agents bloquants bêta-adrénergiques n’est pas recommandée (voir la rubrique 4.5).
Traitement concomitant
Le timolol peut interagir avec d'autres médicaments (voir rubrique 4.5).
Autres analogues de prostaglandines
L’utilisation concomitante de deux ou plusieurs prostaglandines, analogues de prostaglandine, ou des dérivés de prostaglandine n’est pas recommandée (voir rubrique 4.5).
Réactions anaphylactiques
Les patients traités par bêta-bloquants et ayant des antécédents d’atopie ou de réaction anaphylactique grave à différents allergènes, peuvent être plus réactifs à des administrations répétées de tels allergènes et ne pas répondre aux doses d’adrénaline habituellement utilisées dans le traitement des réactions anaphylactiques.
Décollement choroïdien
Des décollements de la choroïde ont été observés après chirurgie filtrante du glaucome lors de l'administration de traitements diminuant la sécrétion d'humeur aqueuse (ex: timolol, acétazolamide).
Anesthésie chirurgicale
Les bêta-bloquants utilisés en ophtalmologie peuvent bloquer les effets des agents bêta-agonistes systémiques tels que l'adrénaline. L'anesthésiste doit être informé lorsque le patient reçoit du timolol.
Modifications de la pigmentation de l’iris
Le latanoprost peut modifier progressivement la couleur des yeux, en augmentant la quantité de pigments bruns dans l’iris. Tout comme le latanoprost seul en collyre, cette pigmentation a été observée (avec contrôle photographique) chez 16 à 20 % des patients traités pendant un an avec le produit de référence à base de latanoprost/timolol avec conservateur; en particulier chez les patients ayant l’iris de plusieurs couleurs : vert-marron, jaune-marron ou bleu/gris-marron. Elle est due à une augmentation de la teneur en mélanine des mélanocytes du stroma de l’iris. Généralement, dans les yeux concernés, la pigmentation brune entourant la pupille s’étend de façon concentrique vers la périphérie, l’iris pouvant devenir partiellement ou totalement, plus brun. Les études cliniques montrent qu’après deux ans de traitement, ces modifications de couleur n’ont été que rarement observées chez des patients ayant des yeux de couleur uniforme, bleus, gris, verts ou marron. La modification de couleur de l’iris évolue lentement et peut passer inaperçue pendant des mois, voire des années. Cet effet n’a été associé à aucun symptôme, ni modification pathologique.
Après arrêt du traitement, aucune progression ultérieure de la pigmentation brune de l’iris n’a été observée, mais la modification de couleur peut être définitive.
Ni les naevi ni les éphélides de l’iris n’ont été affectés par le traitement.
Aucune accumulation de pigments dans le trabeculum ou en d’autres points de la chambre antérieure n’a été observée. Cependant les patients devront être examinés régulièrement, et, en fonction du contexte clinique du patient, le traitement pourra être interrompu en cas d’augmentation de la pigmentation irienne.
Avant l’instauration du traitement, les patients doivent être informés du risque de modification de la couleur de l’œil. Un traitement unilatéral peut entraîner une hétérochromie définitive.
Modifications des paupières et des cils
Une coloration plus foncée de la peau palpébrale, qui peut être réversible, a été rapporté en association avec l'utilisation de latanoprost.
Le latanoprost peut modifier progressivement les cils et le duvet palpébral de l'œil traité ; ces modifications incluent une augmentation de la longueur, de l'épaisseur, de la pigmentation et du nombre de cils ou de poils, et une orientation inadéquate des cils. Les modifications des cils sont réversibles à l'arrêt du traitement.
Glaucome
Il n'y a actuellement aucune expérience documentée portant sur l’efficacité du latanoprost dans le glaucome inflammatoire, néovasculaire ou dans le glaucome chronique à angle fermé, dans le glaucome à angle ouvert de patients pseudophaques et dans le glaucome pigmentaire.
Le latanoprost a peu ou pas d'effet sur la pupille. Cependant il n’y a pas actuellement d’expérience documentée dans les crises de glaucome aigu par fermeture de l’angle. Par conséquent, en l’absence de données complémentaires, il est recommandé d’utiliser FIXAPOST avec précaution dans ces situations.
Kératite herpétique
Le latanoprost doit être utilisé avec précaution chez les patients ayant des antécédents de kératite herpétique et son utilisation doit être évitée en cas de kératite à herpès simplex active et chez les patients ayant des antécédents de kératite herpétique récurrente spécifiquement associée aux analogues des prostaglandines.
Œdème maculaire
Des cas d'œdème maculaire, notamment d’œdème maculaire cystoïde, ont été rapportés au cours du traitement par le latanoprost. Il s'agissait principalement de patients aphaques ou pseudophaques présentant une rupture capsulaire postérieure ou de patients ayant des facteurs de risque connus d'œdème maculaire. De ce fait, FIXAPOST doit être utilisé avec précaution chez ces patients.
Excipients
FIXAPOST contient de l’hydroxystéarate de macrogolglycérol (huile de ricin hydrogénée polyoxyéthylénée) et peut provoquer des réactions cutanées. Aucune donnée de sécurité à long terme n’est disponible actuellement pour cet excipient.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Aucune étude d’interaction médicamenteuse spécifique n’a été menée avec FIXAPOST.
Des élévations paradoxales de la pression intraoculaire ont été rapportées suite à l’administration ophtalmique concomitante de deux analogues de prostaglandines. Par conséquent, l’utilisation de deux ou plus de deux prostaglandines, analogues de prostaglandine, ou dérivés de prostaglandine n’est pas recommandée.
Un effet additif, entrainant une hypotension et/ou une bradycardie, peut être observé lors de l’administration simultanée de solution ophtalmique de bêta-bloquants et d’inhibiteurs des canaux calciques, d’agents bloquants bêta-adrénergiques, d’antiarythmiques (notamment l’amiodarone), de glycosides digitaliques, de parasympathomimétiques, de guanéthidine administrés par voie générale.
Une potentialisation de l’effet bêta-bloquant systémique (par exemple : diminution du rythme cardiaque, dépression) a été rapportée lors de l’association de traitements inhibiteurs du CYP2D6 (par exemple : quinidine, fluoxétine, et paroxétine) et de timolol.
L’effet sur la pression intraoculaire ou les effets connus des bêta-bloquants par voie systémique peuvent être potentialisés quand FIXAPOST est administré aux patients recevant déjà un bêta-bloquant par voie orale, et l’utilisation de deux ou plus de deux agents bêta-bloquants locaux n’est pas recommandée.
Une mydriase a été occasionnellement rapportée lorsque les bêta-bloquants ophtalmiques et l'adrénaline (épinéphrine) ont été utilisés de façon concomitante.
La poussée hypertensive réactionnelle survenant lors de l’arrêt brutal de la clonidine peut être majorée en cas d’administration de bêta-bloquants.
Les bêta-bloquants peuvent majorer l’effet hypoglycémiant des antidiabétiques. Ils peuvent masquer les signes et les symptômes de l’hypoglycémie (voir rubrique 4.4).
4.6. Fertilité, grossesse et allaitement
Grossesse
Latanoprost :
Il n’y a pas de données relatives à l’utilisation du latanoprost chez la femme enceinte. Chez l'animal, les études ont montré une toxicité sur les fonctions de reproduction (voir rubrique 5.3). Le risque potentiel chez l'Homme n'est pas connu.
Timolol :
Il n'y a aucune donnée adéquate sur l'utilisation de timolol chez la femme enceinte. Le timolol ne doit pas être utilisé pendant la grossesse sauf en cas de nécessité absolue. Pour réduire l'absorption systémique, voir la rubrique 4.2.
Les études épidémiologiques n'ont pas révélé d'effet malformatif mais démontrent un risque de retard de croissance intra-utérin lorsque les bêta-bloquants sont administrés par voie orale. De plus, les signes et les symptômes d’un effet bêta-bloquant (par exemple : bradycardie, hypotension, détresse respiratoire et hypoglycémie) ont été observés chez le nouveau-né lorsque les bêta-bloquants ont été administrés jusqu'à l'accouchement. Si FIXAPOST est administré jusqu'à l'accouchement, le nouveau-né devrait être surveillé attentivement pendant les premiers jours de vie.
Par conséquent, FIXAPOST ne doit pas être utilisé au cours de la grossesse.
Les bêta-bloquants sont excrétés dans le lait maternel. Cependant, aux doses thérapeutiques de timolol contenues dans les collyres, il est peu probable que la quantité passant dans le lait maternel suffise à produire les symptômes cliniques des bêta-bloquants chez le nourrisson. Pour réduire l'absorption systémique voir la rubrique 4.2.
Le latanoprost et ses métabolites peuvent passer dans le lait maternel.
Par conséquent, FIXAPOST ne doit pas être utilisé chez la femme qui allaite.
Fertilité
Ni le latanoprost ni le timolol n’a révélé avoir un impact sur la fertilité masculine ou féminine dans les études animales (voir rubrique 5.3).
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Pour le latanoprost, la majorité des effets indésirables se rapporte au système oculaire. Lors de la phase d’extension des études pivots sur le produit de référence à base de latanoprost/timolol avec conservateur, 16 à 20% des patients ont développé une augmentation de la pigmentation irienne, qui peut être permanente. Dans un essai clinique en ouvert étudiant la tolérance du latanoprost sur 5 ans, 33% des patients ont développé une augmentation de la pigmentation irienne (voir rubrique 4.4). D’autres effets indésirables oculaires sont généralement passagers et surviennent à l’administration de la dose. Pour le timolol, les effets indésirables les plus graves sont de nature systémique, incluant bradycardie, arythmie, insuffisance cardiaque congestive, bronchospasme et réactions allergiques.
Comme d'autres médicaments ophtalmiques utilisés par voie locale, le timolol est absorbé dans la circulation générale. Cela peut entraîner des effets indésirables semblables à ceux des bêta-bloquants systémiques. L'incidence des effets indésirables systémiques après une administration ophtalmique est inférieure par rapport à une administration systémique. Les effets indésirables attendus incluent les effets observés avec la classe des bêta-bloquants ophtalmiques.
Les effets indésirables liés au traitement et observés dans les essais cliniques avec le produit de référence à base de latanoprost/timolol avec conservateur sont listés ci-dessous.
Les effets indésirables sont classés selon leur fréquence d’apparition, comme suit : très fréquent (≥ 1/10), fréquent (≥ 1/100 à < 1/10), peu fréquent (≥ 1/1 000 à < 1/100), rare (≥ 1/10 000 à < 1/1 000) et très rare (< 1/10 000), fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
Tableau 1 : Effets indésirables observées au cours d’essais
|
Classe de systèmes d’organes |
Très fréquent (≥ 1/10) |
Fréquent ≥ 1/100 à < 1/10 |
Peu fréquent ≥ 1/1 000 à < 1/100 |
|
Affections du système nerveux |
Céphalées |
||
|
Affections oculaires |
Hyperpigmentation de l’iris |
Douleur oculaire, irritation oculaire (notamment picotements, sensation de brûlure, démangeaison, sensation de corps étrangers) |
Atteinte cornéenne, conjonctivite, blépharite, hyperhémie oculaire, vision trouble, augmentation de la sécrétion lacrymale |
|
Affections de la peau et du tissu sous-cutané |
Eruption cutanée, prurit |
D’autres effets indésirables liés à l’utilisation de l’un des deux composants de FIXAPOST ont été rapportés dans le cadre d’études cliniques, de notifications spontanées ou issus de la littérature.
Pour le latanoprost :
|
Tableau 2 répertoriant les effets indésirables : latanoprost |
|
|
Classe de systèmes d’organes |
Effets indésirables |
|
Infections et infestations |
Kératite herpétique |
|
Affections du système nerveux |
Etourdissement |
|
Affections oculaires |
Modifications des cils et du duvet palpébral (augmentation de la longueur, de l'épaisseur, de la pigmentation et du nombre de cils) ; kératite ponctuée, œdème périorbitaire, iritis ; uvéite ; œdème maculaire, y compris un œdème cystoïde maculaire ; sécheresse oculaire ; kératite ; œdème cornéen ; ulcération cornéenne ; trichiasis ; kyste irien ; photophobie ; modifications périorbitaires et palpébrales suite au creusement du sillon de la paupière ; œdème palpébral ; réaction cutanée localisée au niveau des paupières ; pseudo-pemphigoïde de la conjonctive oculaire ; coloration plus foncée de la peau palpébrale |
|
Affections cardiaques |
Angor ; angor instable ; palpitations |
|
Affections respiratoires, thoraciques et médiastinales |
Asthme ; aggravation de l'asthme ; dyspnée |
|
Affections gastro-intestinales |
Nausées ; vomissements |
|
Affections musculo-squelettiques et du tissu conjonctif |
Myalgie ; arthralgie |
|
Troubles généraux et anomalies au site d’administration |
Douleurs thoraciques |
Pour le timolol :
|
Tableau 3 répertoriant les effets indésirables : maléate de timolol (instillation oculaire) |
|
|
Classe de systèmes d’organes |
Effets indésirables |
|
Affections du système immunitaire |
Réactions allergiques systémiques notamment réaction anaphylactique, angio-œdème, urticaire, rash localisé ou généralisé, prurit |
|
Troubles du métabolisme et de la nutrition |
Hypoglycémie |
|
Affections psychiatriques |
Perte de mémoire, insomnie, dépression, cauchemars, hallucination |
|
Affections du système nerveux |
Accident vasculaire cérébral, ischémie cérébrale, étourdissement, augmentation des signes et symptômes de myasthénie grave, paresthésie, céphalées, syncope |
|
Affections oculaires |
Décollement de la choroïde après chirurgie filtrante (voir rubrique 4.4), érosion cornéenne, kératite, diplopie, baisse de la sensibilité cornéenne, signes et symptômes d'irritation oculaire (par exemple : brûlure, picotement, démangeaison, larmoiement et rougeur), sécheresse oculaire, ptose, blépharite, vision floue |
|
Affections de l'oreille et du labyrinthe |
Acouphènes |
|
Affections cardiaques |
Arrêt cardiaque, insuffisance cardiaque, bloc auriculo-ventriculaire, insuffisance cardiaque congestive, douleur thoracique, arythmie, bradycardie, œdème, palpitations |
|
Affections vasculaires |
Refroidissement des extrémités, hypotension, phénomène de Raynaud |
|
Affections respiratoires, thoraciques et médiastinales |
Bronchospasme (principalement chez les patients présentant une pathologie bronchospastique pré-existante), toux, dyspnée |
|
Affections gastro-intestinales |
Douleurs abdominales, vomissements, diarrhée, bouche sèche, dysgueusie, dyspepsie, nausées |
|
Affections de la peau et du tissu sous-cutané |
Rash cutané, rash psoriasiforme, exacerbation du psoriasis, alopécie |
|
Affections musculo-squelettiques et du tissu conjonctif |
Myalgie |
|
Affections des organes de reproduction et du sein |
Trouble sexuel, baisse de la libido |
|
Troubles généraux et anomalies au site d'administration |
Asthénie, fatigue |
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/
Il n’existe aucune expérience clinique de surdosage de FIXAPOST.
Symptômes
Les symptômes d’un surdosage de timolol par voie systémique sont : bradycardie, hypotension, bronchospasme et arrêt cardiaque.
En dehors d'une irritation oculaire et d'une hyperhémie conjonctivale, aucun effet indésirable oculaire n'est connu pour être dû à un surdosage en latanoprost.
Traitement
Si les symptômes d’un surdosage apparaissaient, le traitement devrait être symptomatique et d’appoint.
En cas d’ingestion accidentelle, les informations suivantes peuvent être utiles :
Des études ont montré que le timolol n’est pas facilement dialysable.
Un lavage gastrique si nécessaire.
Le latanoprost est largement métabolisé lors du premier passage hépatique. Une perfusion intraveineuse de 3 microgrammes/kg chez le volontaire sain n’a entraîné aucun symptôme, par contre, une dose de 5,5– 10 microgrammes/kg a entraîné des nausées, des douleurs abdominales, des vertiges, une fatigue, des bouffées de chaleur et des sueurs. Ces effets étaient légers et modérés et ont disparu sans traitement, dans les 4 heures suivant la fin de la perfusion.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Mécanisme d’action
FIXAPOST associe deux composants : le latanoprost et le maléate de timolol. Ces deux composants diminuent la pression intraoculaire (PIO) élevée par différents mécanismes d’action. L’effet combiné entraîne une diminution supplémentaire de la pression intraoculaire comparée à celle obtenue lors de l’administration de chaque composant seul.
Le latanoprost, analogue de la prostaglandine F2α, est un agoniste sélectif des récepteurs FP des prostanoïdes qui diminue la pression intraoculaire en augmentant l’écoulement de l’humeur aqueuse. Le principal mécanisme d’action est l’augmentation de l’écoulement par la voie uvéo-sclérale. De plus, une augmentation de la facilité d’écoulement (diminution de la résistance à l’écoulement par la voie trabéculaire) a été notée chez l’Homme. Le latanoprost n’a pas d’effet significatif sur la production de l’humeur aqueuse, sur la barrière hémato-aqueuse ou sur la circulation sanguine intraoculaire. Après un traitement chronique par le latanoprost chez le singe ayant auparavant subi une chirurgie extracapsulaire du cristallin, aucune lésion des vaisseaux sanguins rétiniens n'a été mise en évidence par angiographie à la fluorescéine. Un traitement à court terme par le latanoprost n'a pas induit de fuite de la fluorescéine dans le segment postérieur de l’œil de patients pseudophaques.
Le timolol est un agent bloquant les récepteurs adrénergiques bêta-1 et bêta-2 (non-sélectif), n’ayant ni effet sympathomimétique intrinsèque significatif, ni effet dépresseur cardiaque direct, ni effet de stabilisant de membrane. Le timolol abaisse la pression intraoculaire en diminuant la formation de l’humeur aqueuse dans l’épithélium ciliaire.
Le mécanisme d’action précis n’est pas clairement établi mais l’inhibition de l'augmentation de la synthèse d’AMP cyclique engendrée par la stimulation bêta-adrénergique endogène est probable. Il n’a pas été prouvé que le timolol affecte de façon significative la perméabilité de la barrière hémato-aqueuse aux protéines plasmatiques. Chez le lapin, le timolol est resté sans effet sur le flux sanguin oculaire local après un traitement chronique.
FIXAPOST est un collyre en solution sans conservateur, fourni dans un flacon multidose incluant une pompe.
Effets pharmacodynamiques
Effets cliniques
Dans les études de recherche de doses, le produit de référence à base de latanoprost/timolol avec conservateur a entraîné une diminution significativement plus importante de la pression intraoculaire moyenne diurne comparé au latanoprost et au timolol administrés une fois par jour en monothérapie.
Dans deux études cliniques contrôlées, en double insu et d’une durée de six mois, l’effet du produit de référence à base de latanoprost/timolol avec conservateur sur la pression intraoculaire a été comparé à celui d’une monothérapie de latanoprost et de timolol, chez les patients ayant une pression intraoculaire d'au moins 25 mm Hg. Après une période de 2 à 4 semaines de traitement par timolol (entraînant une diminution moyenne de la pression intraoculaire de 5 mm Hg par rapport à l'inclusion), des baisses supplémentaires de la pression intraoculaire moyenne diurne de 3,1; 2,0 et 0,6 mm Hg, ont été respectivement observées après 6 mois de traitement par le produit de référence à base de latanoprost/timolol avec conservateur, latanoprost et timolol (deux fois par jour). L’effet s’est maintenu pendant la phase ouverte d’extension à 6 mois de ces études.
Les données existantes suggèrent qu’une administration le soir pourrait être plus efficace pour baisser la PIO qu’une administration le matin. Toutefois, pour décider d’une administration le matin ou le soir, il convient de prendre suffisamment en considération le mode de vie des patients et leur possibilité d’adhésion au traitement.
On doit garder à l’esprit qu’en cas d’efficacité insuffisante avec l’association fixe, les résultats d’études montrent que l’utilisation de l’association concomitante de timolol deux fois par jour et de latanoprost une fois par jour peut être encore efficace.
L’effet du produit de référence à base de latanoprost/timolol avec conservateur débute dans l’heure qui suit l'administration, et un effet maximal est observé au bout de 6 à 8 heures. Lors d'administrations répétées, la diminution de la pression intraoculaire se maintient jusqu’à 24 heures après l’instillation.
Efficacité et sécurité clinique
FIXAPOST sans conservateur a été évalué lors d’une étude de trois mois, randomisée, investigateur en insu en comparaison avec le produit de référence à base de latanoprost/timolol 50 microgrammes/5 mg par ml avec conservateur chez 242 patients présentant une hypertension oculaire ou un glaucome à angle ouvert, confirmé comme insuffisamment contrôlé en monothérapie. Avant le début de l'étude, les patients ont été traités et contrôlés par le produit de référence ou des génériques (association fixe latanoprost/timolol 50 microgrammes / 5 mg par ml de collyre conservé) pendant au moins 2 mois.
Le critère primaire d'efficacité était la variation de la pression intraoculaire entre la valeur de base et celle du jour 84.
Au jour 84, la diminution de la pression intraoculaire induite par FIXAPOST était de – 0,49 mmHg. Et cette diminution était semblable à celle observée avec le produit de référence latanoprost/timolol 50 microgrammes/5 mg par ml avec conservateur.
|
Oeil le plus sévèrement atteint (population en ITM) |
|
FIXAPOST |
Produit de référence |
|
Valeur de référence (J0) |
n Moyenne ± Ecart type |
124 15,6 ± 2,1 |
112 15,7 ± 2,1 |
|
J84 |
n Moyenne ± Ecart type |
122 15,1 ± 2,4 |
110 15,2 ± 2,2 |
|
Variation moyenne (J0 – J84) |
n Moyenne ± Ecart type [95% IC] |
122 -0,49 ± 1,80 [-0,81 ; -0,17] |
110 -0,49 ± 2,25 [-0,92 ; -0,07] |
|
Analyse statistique |
Différence moyenne ajustée ± Ecart type [95%IC] |
0,01 ± 0.25 [-0,48; 0,50] |
|
n = nombre de patients ; IC = intervalle de confiance ; ITM = intention de traiter modifiée
Cette étude de 3 mois a montré qu'aucun événement indésirable ophtalmique n'a été identifié pour FIXAPOST en dehors de ceux déjà bien documentés avec le produit de référence à base de latanoprost/timolol avec conservateur chlorure de benzalkonium (BAK).
Par rapport au produit de référence, FIXAPOST a été associé à moins de symptômes subjectifs lors de l'instillation à J84 (irritation / brûlure / picotements: 20,5% vs 41,8%, p <0,001, démangeaisons : 4,9% vs 13,9%, p = 0,010) ainsi qu’à moins de symptômes subjectifs tout au long de la journée indépendamment de l'instillation (irritation / brûlure / picotement : 7,4% vs 12,7%, p = 0,094; démangeaisons: 1,6% vs 13,6%, p <0,001).
Quelques effets indésirables systémiques, déjà bien connus pour le timolol, mais non observés dans les essais cliniques avec le produit de référence à base de latanoprost/timolol avec conservateur (voir rubrique 4.8), ont été observés à une fréquence peu fréquente : dysgueusie, arythmie et fatigue.
5.2. Propriétés pharmacocinétiques
Latanoprost
Absorption
Le latanoprost est une prodrogue de type ester isopropylique, inactive en elle-même, qui devient biologiquement active après hydrolyse par les estérases de la cornée en acide de latanoprost. La prodrogue est bien absorbée par la cornée et la totalité de la substance pénétrant dans l’humeur aqueuse est hydrolysée au cours du passage à travers la cornée.
Distribution
Les études cliniques chez l'Homme montrent que la concentration maximale dans l’humeur aqueuse, approximativement de 15-30 ng/ml, est atteinte environ 2 heures après une administration locale de latanoprost seul. Après une administration locale chez le singe, le latanoprost est distribué principalement dans le segment antérieur, la conjonctive et les paupières.
L’acide de latanoprost a une clairance plasmatique de 0,40 l/h/kg et un faible volume de distribution de 0,16 l/kg, résultant en une demi-vie plasmatique courte de 17 minutes.
Après une administration oculaire, la biodisponibilité systémique de l’acide de latanoprost est de 45 %. L’acide de latanoprost a une fixation aux protéines plasmatiques de 87 %.
Biotransformation et élimination
L'acide de latanoprost n'est pratiquement pas métabolisé dans l'œil. Le métabolisme est principalement hépatique. Les études animales ont montré une activité faible, voire nulle, des principaux métabolites, le 1, 2-dinor et le 1, 2, 3, 4-tétranor, qui sont principalement éliminés dans l'urine.
Timolol
Absorption et distribution
La concentration maximale de timolol dans l’humeur aqueuse est atteinte environ 1 heure après une administration locale du collyre. Une partie de la dose est absorbée par voie systémique et la concentration plasmatique maximale de 1 ng/ml est atteinte 10-20 minutes après administration locale quotidienne d’une goutte dans chaque œil (300 microgrammes/jour).
Biotransformation
La demi-vie plasmatique du timolol est d'environ 6 heures. Il est largement métabolisé dans le foie.
Elimination
Les métabolites sont excrétés dans l’urine en même temps que du timolol inchangé.
Produit de référence à base de latanoprost/timolol avec conservateur
Interaction Pharmacocinétique / Pharmacodynamique
Aucune interaction pharmacocinétique entre le latanoprost et le timolol n’a été observée malgré une concentration en acide de latanoprost dans l’humeur aqueuse 1-4 heures après administration du produit de référence à base de latanoprost/timolol avec conservateur, deux fois supérieure à celle observée en monothérapie
5.3. Données de sécurité préclinique
Pour le latanoprost, aucun effet sur la fertilité chez le rat mâle et femelle n'a été observé. Aucun pouvoir tératogène n'a été détecté chez le rat et le lapin. Aucun effet embryotoxique n'a été observé chez le rat après administration intraveineuse de doses allant jusqu’à 250 microgrammes/kg/jour. Toutefois, le latanoprost induit une toxicité embryo-fœtale, caractérisée par une incidence accrue des résorptions tardives, des avortements ainsi qu’une diminution du poids fœtal chez le lapin à des doses intraveineuses supérieures ou égales à 5 microgrammes/kg/jour (environ 100 fois la dose thérapeutique). Le timolol n’entraîne pas d’effet sur la fertilité du rat mâle ou femelle. Aucun pouvoir tératogène n’a été observé chez la souris, le rat et le lapin.
Toxicité oculaire
L'administration oculaire de FIXAPOST collyre chez l’animal deux fois par jour pendant 28 jours n'a pas montré de toxicité locale ou systémique.
2 ans.
Après la première ouverture : 4 semaines pour le flacon de 2,5 ml ; 3 mois pour le flacon de 6 ml.
Ce médicament ne nécessite pas de précautions particulières de conservation.
6.4. Précautions particulières de conservation
Après la première ouverture : pour les conditions de conservation après la première ouverture du médicament, voir la rubrique 6.3.
6.5. Nature et contenu de l'emballage extérieur
Flacon multidose (PEHD) équipé d'une pompe munie d'un système d’aide à l’utilisation Easygrip et d’un bouchon inviolable (PEHD).
1 flacon de 2,5 ml (au moins 80 gouttes sans conservateur - pour 4 semaines de traitement).
1 flacon de 6 ml (au moins 190 gouttes sans conservateur - pour 3 mois de traitement).
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Pas d’exigences particulières.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
12 RUE LOUIS BLERIOT
63017 CLERMONT-FERRAND CEDEX 2
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 302 185 9 4 : 2,5 mL en flacon (PEHD) avec une fermeture sécurité (PEHD).
· 34009 302 186 0 0 : 6 mL en flacon (PEHD) avec une fermeture sécurité (PEHD).
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
Date de première autorisation:{JJ mois AAAA}
Date de dernier renouvellement:{JJ mois AAAA}
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
{JJ mois AAAA}
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I
ANSM - Mis à jour le : 28/10/2025
FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution
Latanoprost / Timolol
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin, votre pharmacien ou votre infirmier/ère.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution ?
3. Comment utiliser FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution ET DANS QUELS CAS EST-IL UTILISE ?
FIXAPOST est indiqué pour faire baisser la pression intraoculaire chez les patients atteints de glaucome à angle ouvert ou d’hypertonie intraoculaire. Ces deux pathologies sont liées à une augmentation de la pression interne de l’œil qui risque éventuellement d’endommager votre vue. Votre médecin prescrira FIXAPOST quand d’autres médicaments n’auront pas agi de manière adéquate.
FIXAPOST est un collyre en solution sans conservateur.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution ?
N’utilisez jamais FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution :
· si vous êtes allergique (hypersensible) au latanoprost, timolol, bêta-bloquant ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
· si vous avez souffert ou souffrez actuellement de troubles respiratoires graves tels que de l’asthme, une bronchite chronique obstructive sévère (trouble pulmonaire sévère pouvant entraîner une respiration sifflante, une difficulté à respirer et/ou une toux de longue date),
· si vous présentez des troubles cardiaques graves ou des troubles du rythme cardiaque.
Avertissements et précautions
Adressez-vous à votre médecin, pharmacien ou votre infirmier/ère avant d’utiliser FIXAPOST si vous avez ou si vous avez eu dans le passé :
· Une maladie coronarienne (dont les symptômes peuvent être une douleur ou une oppression de la poitrine, une difficulté à respirer, ou une suffocation), une insuffisance cardiaque, ou une tension artérielle basse.
· des troubles de la fréquence cardiaque tels que les pulsations cardiaques lentes.
· des problèmes respiratoires, de l’asthme ou une bronchite chronique obstructive.
· des problèmes de circulation sanguine (tels que la maladie ou le syndrome de Raynaud).
· du diabète puisque le timolol peut masquer les signes et les symptômes de glycémie basse.
· un excès d’hormones thyroïdiennes (hyperthyroïdie) puisque le timolol peut en masquer les signes et les symptômes.
· si vous devez subir ou si vous avez subi une intervention au niveau de l’œil (y compris une opération de la cataracte).
· si vous souffrez d’une autre maladie oculaire (douleur au niveau de l’œil, irritation ou inflammation oculaire, vision trouble).
· si vous souffrez d’une sécheresse oculaire.
· si vous portez des lentilles de contact. Vous pouvez utiliser FIXAPOST, à condition de suivre les instructions mentionnées en rubrique 3.
· si vous souffrez d’angine de poitrine (en particulier d’angor de Prinzmetal).
· si vous souffrez de réactions allergiques sévères nécessitant une prise en charge hospitalière.
· si vous avez souffert ou souffrez actuellement d’une infection virale de l’œil due au virus herpès simplex (VHS).
Prévenez votre médecin que vous utilisez FIXAPOST avant une intervention chirurgicale car le timolol peut modifier les effets de certains médicaments utilisés durant l’anesthésie.
Enfants
Sans objet.
Autres médicaments et FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution
Informez votre médecin ou pharmacien si vous utilisez, avez récemment utilisé ou pourriez utiliser tout autre médicament y compris les médicaments obtenus sans ordonnance.
L’effet de FIXAPOST peut être affecté par les autres thérapeutiques que vous prenez y compris d’autres collyres pour le traitement du glaucome, de même FIXAPOST peut en modifier l’effet. Prévenez votre médecin si vous utilisez ou avez l’intention d’utiliser des médicaments visant à diminuer la pression artérielle, des traitements pour le cœur ou pour le diabète. Informez en particulier votre médecin ou votre pharmacien si vous prenez un des médicaments suivants :
· prostaglandines, analogues des prostaglandines, ou dérivés des prostaglandines ;
· bêta-bloquants ;
· adrénaline ;
· médicaments utilisés dans le traitement de l’hypertension artérielle, tels que des inhibiteurs calciques, la guanethidine, les antiarythmiques, les glycosides digitaliques ou parasympathomimétiques ;
· quinidine (utilisée pour le cœur et pour certaines formes de paludisme) ;
· antidépresseurs connus comme la fluoxétine et la paroxétine.
FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution avec des aliments et boissons
Une alimentation normale (boisson et nourriture) n’influence pas les modalités d’utilisation de FIXAPOST.
Grossesse, allaitement et fertilité
N'utilisez pas FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution si vous êtes enceinte ou si vous allaitez.
FIXAPOST peut être excrété dans le lait.
Ni le latanoprost ni le timolol n’a révélé avoir un impact sur la fertilité masculine ou féminine dans les études animales.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
Conduite de véhicules et utilisation de machines
Lorsque vous utilisez FIXAPOST vous pouvez avoir une vision trouble pendant un court instant. Si cela vous arrive, vous ne devez pas conduire, utiliser des outils ou des machines jusqu’à ce que votre vision redevienne normale.
FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution contient de l’hydroxystéarate de macrogolglycérol (dérivé de l’huile de ricin) qui peut provoquer des réactions cutanées.
3. COMMENT UTILISER FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution ?
La dose recommandée chez l’adulte (y compris chez le sujet âgé) est d’une goutte dans l’œil (les yeux) à traiter, une fois par jour.
N’utilisez pas FIXAPOST plus d’une fois par jour, votre traitement pourrait être moins efficace si vous l’utilisez plus souvent.
Utilisez FIXAPOST tel que vous l’a indiqué votre médecin jusqu’à ce que votre médecin vous demande d’arrêter.
Si vous utilisez FIXAPOST, votre médecin pourra vous demander d’effectuer des examens complémentaires pour évaluer le fonctionnement de votre cœur et de votre circulation sanguine.
Ce médicament est un collyre en solution sans conservateur. Ne touchez pas l’œil ou les surfaces avoisinantes avec l’embout du flacon. Une bactérie pourrait le contaminer et causer une infection de l’œil qui pourrait entraîner des lésions de l’œil, et même une perte de vision. Afin d’éviter toute contamination du flacon, maintenir l’embout du flacon éloigné de tout contact.
Porteurs de lentilles de contact
Si vous portez des lentilles de contact, retirez-les avant d’utiliser FIXAPOST et ne les remettez que 15 minutes après l’instillation.
Mode d’administration
Ce médicament doit être administré dans l’œil.
Veuillez suivre les instructions suivantes lors de l’utilisation de ce collyre :
|
|
Avant d’utiliser ce médicament pour la première fois : - Veuillez vérifier que le bouchon inviolable est intact. Dévissez ensuite fermement le bouchon d’inviolabilité pour ouvrir le flacon. - Lavez-vous soigneusement les mains et enlever le bouchon de l'embout du flacon. Pressez plusieurs fois avec le flacon à l'envers, pour activer le mécanisme de pompage jusqu'à ce que la première goutte apparaisse. Ce processus est à effectuer seulement pour la toute première utilisation et ne sera pas nécessaire pour les administrations suivantes.
|
|
|
1. Avant chaque utilisation, se laver soigneusement les mains et enlever le bouchon de l'embout du flacon. Évitez tout contact entre l'embout du flacon et les doigts. |
|
|
2. Placer le pouce sur la languette située en haut du flacon et l’index sur la base du flacon. Ensuite, placer le majeur sur la seconde languette située à la base du flacon. Tenir le flacon à l’envers. |
|
|
3. Pour l’utiliser, incliner votre tête légèrement vers l’arrière et maintenez le flacon compte-goutte à la verticale au-dessus de l’œil. Avec l’index de l’autre main, tirez légèrement la paupière inférieure vers le bas. L'espace créé est appelé le sac conjonctival inférieur. Eviter tout contact entre l’embout du flacon et vos doigts ou vos yeux. Afin d’instiller une goutte dans le sac conjonctival inférieur de l’œil ou les yeux atteint(s), appuyer brièvement et fermement sur le flacon. Grâce au dosage automatique, une goutte est libérée précisément à chaque pompage. |
|
Si la goutte ne tombe pas, secouez doucement le flacon afin de libérer la goutte restée sur l’embout. Dans ce cas, répétez l’étape 3. |
|
|
|
4. Fermez les paupières et appuyez avec votre doigt sur le coin interne (proche de votre nez) de l’œil pendant 2 minutes. Ceci aide à empêcher le collyre de passer dans le reste de votre organisme. |
|
|
5. Fermez l’extrémité du flacon avec le bouchon immédiatement après l’utilisation. |
Si vous utilisez FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution avec un autre collyre
Attendez au moins 5 minutes entre l’administration de FIXAPOST et celle de l’autre collyre.
Si vous avez utilisé plus de FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution que vous n’auriez dû
Si vous avez mis trop de gouttes dans votre œil, une sensation d'irritation peut apparaître et vos yeux peuvent larmoyer et devenir rouges. Ceci doit disparaître mais si vous êtes inquiet, demandez conseils à votre médecin.
Si vous avalez FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution
En cas d’ingestion accidentelle de FIXAPOST, contactez immédiatement votre médecin. Si vous ingérez une grande quantité de FIXAPOST, vous pouvez vous sentir mal, avoir des maux d’estomac, vous sentir fatigué, présenter des rougeurs et avoir une sensation d’étourdissement, ou commencer à transpirer.
Si vous oubliez d’utiliser FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution
En cas de doute, parlez-en à votre médecin ou à votre pharmacien.
Si vous arrêtez d’utiliser FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution
Utiliser FIXAPOST tel que vous l’a indiqué votre médecin jusqu’à ce que votre médecin vous demande d’arrêter. Ne pas interrompre ou arrêter votre traitement avec FIXAPOST sans en parler avec votre médecin.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin, à votre pharmacien ou à votre infirmier/ère
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
De manière générale, vous pouvez continuer à utiliser les gouttes comme d'habitude à moins que les effets ne soient graves. Si vous êtes inquiet, parlez-en à votre médecin ou à votre pharmacien. N'arrêtez pas d'utiliser FIXAPOST sans en parler à votre médecin.
Sont listés ci-dessous les effets indésirables connus liés à l’utilisation de FIXAPOST. L’effet indésirable le plus important est une modification progressive et définitive de la couleur des yeux. Il est aussi possible que FIXAPOST entraîne des modifications importantes du fonctionnement de votre cœur. Si vous remarquez des troubles affectant votre cœur, parlez-en à votre médecin en mentionnant que vous avez utilisé FIXAPOST.
Les effets indésirables suivants ont été rapportés lors de l’utilisation de FIXAPOST :
Très fréquent (peut affecter plus de 1 patient sur 10) :
Une modification de la couleur des yeux par augmentation de la quantité de pigments bruns dans la partie colorée de l’œil appelée l’iris. Si vous avez des yeux de plusieurs couleurs (c'est-à-dire bleu-marron, gris-marron, jaune-marron ou vert-marron) vous avez une plus grande probabilité d’observer ces changements que si vos yeux sont d’une seule couleur (bleu, gris, vert ou brun). Cette modification de la couleur des yeux peut évoluer pendant des années. Cette modification de couleur peut être définitive et peut être plus visible si votre traitement par FIXAPOST ne concerne qu’un seul œil. Il ne semble pas y avoir d’autre problème associé au changement de couleur de l’œil. Le changement de la couleur de l’œil ne se poursuit pas après l’arrêt du traitement par FIXAPOST.
Fréquent (peut affecter jusqu’à 1 patient sur 10) :
Une irritation oculaire (sensation de brûlure, grain de sable, démangeaison, picotement ou sensation de corps étranger) et douleur oculaire.
Peu fréquent (peut affecter jusqu’à 1 patient sur 100) :
· Maux de tête.
· Une rougeur au niveau de l’œil, une infection de l’œil (conjonctivite), une vision trouble, des yeux larmoyants, inflammation de la paupière, une irritation ou une érosion de la surface oculaire.
· Une éruption cutanée ou des démangeaisons (prurit).
· Des nausées, des vomissements.
Autres effets indésirables :
Comme d'autres médicaments appliqués dans les yeux, FIXAPOST (latanoprost et timolol) est absorbé dans le sang. L'incidence des effets indésirables après utilisation du collyre est inférieure à celle observée après une administration de médicaments par voie orale ou par voie injectable.
Bien que n’ayant pas été observés avec FIXAPOST, les effets indésirables suivants ont été observés lors de l’utilisation séparée des deux principes actifs de FIXAPOST (latanoprost et timolol) et pourraient être rapportés lors de l’utilisation de FIXAPOST. Les effets indésirables répertoriés incluent des réactions observées au sein de la classe des bêta-bloquants (par ex., timolol) lorsqu’ils sont utilisés dans le traitement des maladies oculaires :
· Développement d’une infection virale de l’œil due au virus herpès simplex (VHS).
· Réactions allergiques généralisées, y compris gonflement sous la peau pouvant se manifester dans des parties du corps comme le visage ou les membres et pouvant obstruer les voies respiratoires et ainsi provoquer des difficultés à avaler ou à respirer, urticaire ou éruption avec démangeaisons, éruption cutanée localisée ou généralisée, démangeaisons, brusque réaction allergique grave pouvant engager le pronostic vital.
· Taux bas de glucose dans le sang.
· Vertiges.
· Difficulté à dormir (insomnie), dépression, cauchemars, perte de mémoire, hallucination.
· Évanouissement, accident vasculaire cérébral, baisse de l'apport de sang au cerveau, aggravation des signes et symptômes de myasthénie grave (affection musculaire), sensations anormales comme fourmillements, et maux de tête.
· Gonflement au fond de l’œil (œdème maculaire), kyste dans la partie colorée de l’œil (kyste irien), sensibilité à la lumière (photophobie), des yeux d’apparence creuse (creusement du sillon de la paupière).
· Signes et symptômes d'irritation de l'œil (par ex., sensations de brûlure, picotements, démangeaisons, larmoiement, rougeur), inflammation de la paupière, inflammation de la cornée, vision floue et décollement de la couche qui contient les vaisseaux sanguins située sous la rétine, suite à une chirurgie filtrante qui peut entraîner des anomalies de la vision, diminution de la sensibilité de la cornée, sécheresse des yeux, érosion de la cornée (lésion de la couche superficielle du globe oculaire), abaissement de la paupière supérieure (à cause duquel l'œil reste à moitié fermé), vision double.
· Coloration plus foncée de la peau autour des yeux, modifications des cils et du duvet au niveau de la paupière (plus foncés, plus épais, plus longs et en nombre plus important), croissance des cils mal orientée, gonflement péri-orbitaire, inflammation de la partie colorée de l’œil (iritis/uvéite), lésions cicatricielles de la surface de l’œil.
· Sifflements ou bourdonnements d’oreille (tinnitus).
· Angine de poitrine, aggravation de l’angine de poitrine chez les patients ayant déjà une maladie cardiaque.
· Rythme cardiaque ralenti, douleur dans la poitrine, palpitations (perception du rythme cardiaque), œdème (accumulation de liquide), changements du rythme et de la vitesse des battements cardiaques, insuffisance cardiaque congestive (maladie cardiaque avec essoufflement et gonflement des pieds et des jambes en raison d’une accumulation de liquide), un type de trouble du rythme cardiaque, crise cardiaque, insuffisance cardiaque.
· Tension artérielle basse, mauvaise circulation sanguine qui entraîne un engourdissement et une pâleur des doigts et des orteils, mains et pieds froids.
· Essoufflement, rétrécissement des voies respiratoires dans les poumons (surtout chez les patients souffrant d'une maladie préexistante), difficultés à respirer, toux, asthme, aggravation de l'asthme.
· Modification du goût, nausées, indigestion, diarrhée, sécheresse de la bouche, douleur abdominale, vomissements.
· Chute des cheveux, éruption cutanée ayant une apparence de couleur blanche argentée (éruption psoriasiforme) ou aggravation d’un psoriasis, éruption cutanée.
· Douleurs articulaires, douleurs musculaires non causées par l’exercice physique, faiblesse/fatigue musculaire.
· Trouble sexuel, libido diminuée.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: https://signalement.social-sante.gouv.fr/
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur la boîte et le flacon. La date de péremption fait référence au dernier jour de ce mois.
Avant la première ouverture : ce médicament ne nécessite pas de précautions particulières de conservation.
Après la première ouverture : FIXAPOST peut être utilisé jusqu’à 4 semaines pour le flacon de 2,5 ml et jusqu’à 3 mois pour le flacon de 6 ml, sans précautions particulières de conservation.
Notez la date de la première ouverture sur la boîte.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient FIXAPOST 50 microgrammes/mL + 5 mg/mL, collyre en solution
· Les substances actives sont :
Le latanoprost (50 microgrammes/ml) et le timolol (5,00 mg/ml) sous forme de maléate de timolol.
· Les autres composants sont :
Hydroxystéarate de macrogolglycérol, sorbitol, macrogol, carbomère, édétate disodique, hydroxyde de sodium (pour ajustement du pH) et eau.
FIXAPOST est une solution légèrement jaune et opalescente, pratiquement exempte de particules.
FIXAPOST est disponible dans les présentations suivantes :
· 1 flacon de 2,5 ml (au moins 80 gouttes sans conservateur), pour 4 semaines de traitement, incluant une pompe équipée d'un système Easygrip avec supports ergonomiques.
· 1 flacon de 6 ml (au moins 190 gouttes sans conservateur), pour 3 mois de traitement, incluant une pompe équipée d'un système Easygrip avec supports ergonomiques.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
12 RUE LOUIS BLERIOT
63017 CLERMONT-FERRAND CEDEX 2
Exploitant de l’autorisation de mise sur le marché
THEA PHARMA
37 rue georges besse
63100 CLERMONT-FERRAND
RUE PAUL LANGEVIN
37170 CHAMBRAY LES TOURS
OU
LABORATOIRES THEA
12 RUE LOUIS BLERIOT
63017 CLERMONT-FERRAND CEDEX 2
OU
FARMILA-THEA Farmaceutici S.p.A.
VIA ENRICO FERMI, 50
20019 settimo milanese
italy
Noms du médicament dans les Etats membres de l'Espace Economique Européen
[dans le cas des MRP et DCP]
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
{mois AAAA}.
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).