
ANSM - Mis à jour le : 28/07/2020
MILRINONE STRAGEN 1mg/ml, solution injectable
Milrinone
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre infirmier/ère.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que MILRINONE STRAGEN 1 mg/mL, solution injectable et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser MILRINONE STRAGEN 1 mg/mL, solution injectable ?
3. Comment utiliser MILRINONE STRAGEN 1 mg/mL, solution injectable ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver MILRINONE STRAGEN 1 mg/mL, solution injectable ?
6. Contenu de l’emballage et autres informations.

Classe pharmacothérapeutique - code ATC : STIMULANTS CARDIAQUES - C01CE02
MILRINONE STRAGEN 1 mg/mL, solution injectable est un stimulant cardiaque, utilisé seulement chez les patients hospitalisés dans une unité de soins intensifs :
· chez l’adulte pour traiter l’insuffisance cardiaque aiguë congestive (quand le cœur ne peut pas pomper assez de sang du reste du corps) ;
· chez l’enfant pour traiter sur une courte période (jusqu’à 35 heures) l’insuffisance cardiaque congestive sévère (quand le cœur a des difficultés pour pomper le sang du corps), si d’autres médicaments n’ont pas été efficaces ;
· chez l’enfant après une opération du cœur, pour traiter sur une courte période (jusqu’à 35 heures) l’insuffisance cardiaque, c’est-à-dire quand son cœur a des difficultés pour pomper le sang de son corps.

N’utilisez jamais MILRINONE STRAGEN 1 mg/mL, solution injectable :
· si vous êtes allergique (hypersensible) à la milrinone ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
· si votre volume sanguin a diminué de façon importante (hypovolémie sévère). Cela peut engendrer des symptômes plus ou moins graves tels qu’une pâleur de la peau, notamment des lèvres, une baisse de la pression artérielle, une accélération du rythme cardiaque, ou une perte de connaissance.
Avertissements et précautions
Adressez-vous à votre médecin ou votre infirmier/ère avant d’utiliser MILRINONE STRAGEN.
· Si vous souffrez d’insuffisance rénale sévère (défaillance des fonctions des reins), prévenez votre médecin ou votre infirmier/ère.
· Il est possible que surviennent une hypotension et des troubles du rythme cardiaque (tachycardie, arythmie supraventriculaire et ventriculaire). C’est pourquoi votre médecin
· ou votre infirmier/ère contrôlera tout au long du traitement votre pression artérielle, votre fréquence cardiaque et votre électrocardiogramme.
Il sera particulièrement vigilant :
o Si vous présentez une diminution importante de la pression artérielle pendant le traitement. La perfusion devra être arrêtée jusqu’au retour à la normale, puis reprise à un débit plus faible si nécessaire.
o Vous ne pourrez pas prendre MILRINONE STRAGEN si vous avez une hypotension avant de commencer ce traitement.
o Si vous présentez un risque élevé de troubles du rythme cardiaque.
o Si vous souffrez d’insuffisance cardiaque (défaillance des fonctions du muscle cardiaque), car le risque de trouble du rythme cardiaque peut être augmenté par l'association à d'autres médicaments.
o Si vous présentez un trouble du rythme cardiaque (flutter ou fibrillation), un traitement préalable pourra vous être administré.
o Si vous avez reçu précédemment un traitement diurétique intensif (traitement qui augmente la sécrétion d’urine et qui est utilisé notamment pour traiter l’hypertension artérielle).
· Avant et pendant le traitement, votre médecin ou votre infirmier/ère devra surveiller également :
o Votre équilibre hydro-électrolytique (eau et sels minéraux de l’organisme).
o Votre bilan sanguin.
o Votre créatininémie (test sanguin qui permet de vérifier le bon fonctionnement des reins).
o Le point d’injection. En effet, des cas de réactions au point d’injection ont été constatés.
· Ce médicament étant administré par injection intraveineuse, il peut être utilisé si vous êtes intolérant au glucose.
Enfants
Utilisation chez les enfants :
Les informations suivantes doivent être aussi considérées.
· Avant de faire une perfusion de MILRINONE STRAGEN à votre enfant, votre médecin ou votre infirmier/ère devra vérifier de nombreux paramètres tels que le rythme cardiaque et la pression sanguine. Des tests sanguins seront aussi réalisés.
· La perfusion ne commencera que si le rythme cardiaque et la pression sanguine de votre enfant sont stables.
· Vous devez prévenir votre médecin ou votre infirmier/ère si :
o Votre enfant a des problèmes rénaux,
o Votre enfant est un prématuré ou a un faible poids de naissance,
o Votre enfant a un problème cardiaque appelé « persistance du canal artériel » c’est-à-dire une communication entre 2 vaisseaux sanguins majeurs (l’aorte et l’artère pulmonaire) qui persiste alors qu’elle devrait être fermée.
Dans ces cas, votre médecin décidera si votre enfant sera traité avec MILRINONE STRAGEN.
Autres médicaments et MILRINONE STRAGEN 1 mg/mL, solution injectable
Informez votre médecin ou votre infirmier/ère si vous utilisez, avez récemment utilisé ou pourriez utiliser tout autre médicament.
MILRINONE STRAGEN 1 mg/mL, solution injectable avec des aliments, boissons et de l’alcool
Sans objet.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin avant de prendre ce médicament.
D’une façon générale, il convient de demander conseil à votre médecin, pharmacien ou votre infirmier/ère avant de prendre tout médicament.
Conduite de véhicules et utilisation de machines
Sans objet.
MILRINONE STRAGEN 1 mg/mL, solution injectable contient : du sodium.
Ce médicament contient moins de 1 mmol (23 mg) de sodium par ampoule, c.-à-d. qu’il est essentiellement « sans sodium ».

MILRINONE STRAGEN ne peut être utilisé qu’en milieu hospitalier dans une unité de soins intensifs.
Il vous sera donc administré par un professionnel de santé.
Posologie
Dans tous les cas, l’ordonnance devra être strictement respectée et la posologie ne devra pas être modifiée sans avis médical.
Utilisation chez les adultes :
Le traitement débutera par une injection intraveineuse rapide et se poursuivra par une perfusion continue.
Si vous souffrez d’une maladie des reins (insuffisance rénale), votre médecin ou infirmier/ère peut être amené à diminuer les quantités administrées.
Utilisation chez les enfants :
Votre médecin ou infirmier/ère devra donner à votre enfant une 1ère dose sur une période de 30 à 60 minutes.
Cette dose sera alors suivie par une perfusion continue.
MILRINONE STRAGEN peut être donné sur une période de temps allant jusqu’à 35 heures.
Pendant la perfusion, votre enfant sera surveillé de près (voir aussi la rubrique « Avertissements et précautions »).
Mode d'administration
MILRINONE STRAGEN sera administré par voie intraveineuse (injecté dans une veine).
Si vous avez utilisé plus de MILRINONE STRAGEN 1 mg/mL, solution injectable que vous n’auriez dû :
Consultez immédiatement votre médecin ou votre pharmacien.
Pour plus d’informations, voir Informations réservées aux professionnels de santé.
Si vous oubliez d’utiliser MILRINONE STRAGEN 1 mg/mL, solution injectable:
Si vous arrêtez d’utiliser MILRINONE STRAGEN 1 mg/mL, solution injectable:
Sans objet.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre infirmier/ère.

Les plus fréquemment rapportés sont :
· troubles du rythme cardiaque (arythmies supraventriculaires, extrasystoles ventriculaires, tachycardie ventriculaire) ;
· baisse de la pression sanguine (hypotension) ;
· maux de tête.
Peu fréquemment :
· baisse du taux de plaquettes dans le sang (thrombopénie) ;
· tremblements ;
· fibrillation ventriculaire (trouble du rythme cardiaque, pouvant causer un arrêt cardiaque) ;
· baisse du taux de potassium dans le sang (hypokaliémie) ;
· anomalies des tests évaluant l'état et le fonctionnement du foie ;
· angine de poitrine, douleur dans la poitrine.
Très rarement :
· réaction allergique grave mettant le patient en danger avec malaise brutal et baisse importante de la tension artérielle, pouvant être précédée d’une éruption de boutons, de démangeaisons, de rougeurs sur la peau, d’une difficulté à respirer, d’un gonflement du visage et/ou du cou (choc anaphylactique) ;
· troubles du rythme cardiaque graves (torsades de pointes) ;
· difficulté à respirer (bronchospasme) ;
· éruptions cutanées (rougeurs sur la peau...) ;
· réactions au point d’injection.
Fréquence inconnue :
· diminution des globules rouges et/ou des concentrations de l’hémoglobine.
· maladie des reins (insuffisance rénale), suite à une hypotension.
Effets indésirables supplémentaires chez les enfants (fréquence inconnue) :
· saignement dans le cerveau (hémorragie intraventriculaire) ;
· problème cardiaque appelé persistance du canal artériel : communication entre 2 vaisseaux sanguins majeurs (l’aorte et l’artère pulmonaire) qui persiste alors qu’elle devrait être fermée. Ceci peut causer des excès de fluides dans les poumons, des saignements, une destruction des intestins ou d’une partie des intestins et peut être fatal.
De plus, chez les enfants, comparativement aux adultes :
· la diminution du nombre de plaquettes dans le sang (thrombocytopénie) semble se produire plus souvent ;
· le risque de survenue d’effets indésirables augmente en fonction du temps de perfusion de MILRINONE STRAGEN ;
· les troubles du rythme cardiaque semblent survenir moins souvent.
Si vous remarquez des effets indésirables non mentionnés dans cette notice, ou si certains effets indésirables deviennent graves, veuillez en informer votre médecin ou à votre infirmier/ère.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou à votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: www.signalement-sante.gouv.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.

Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’étiquette après EXP. La date de péremption fait référence au dernier jour de ce mois.
N’utilisez pas ce médicament si vous remarquez la présence de particules en suspension ou d’anomalies de coloration.
Durée de conservation après dilution : après dilution dans une solution de NaCl 0,45%, de NaCl 0,9%, de glucose à 5% ou de Ringer lactate, la stabilité physico-chimique de la solution diluée a été démontrée pendant 72 heures à une température ne dépassant pas 25°C ou au réfrigérateur (entre 2°C et 8°C).
Toutefois, du point de vue microbiologique, le produit doit être utilisé immédiatement. En cas d’utilisation non immédiate, les durées et conditions d’utilisation relèvent de la seule responsabilité de l’utilisateur et ne devraient pas dépasser 24 heures à une température comprise entre 2°C et 8°C.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.

Ce que contient MILRINONE STRAGEN 1 mg/mL, solution injectable 
· La substance active est :
Milrinone............................................................................................................................ 1 mg
Pour 1 ml de solution
· Les autres composants sont : Acide lactique, glucose anhydre, hydroxyde de sodium, eau pour préparations injectables.
Qu’est-ce que MILRINONE STRAGEN 1 mg/mL, solution injectable et contenu de l’emballage extérieur 
Ce médicament se présente sous forme de solution injectable, transparente, incolore à jaune pâle.
Boîte de 10 ampoules de 10 ml.
Boîte de 10 ampoules de 20 ml.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché 
30 RUE EDOUARD NIEUPORT
69008 LYON
Exploitant de l’autorisation de mise sur le marché 
STRAGEN FRANCE
30 RUE EDOUARD NIEUPORT
69008 LYON
52 RUE MARCEL ET JACQUES GAUCHER
94120 FONTENAY SOUS BOIS
Noms du médicament dans les Etats membres de l'Espace Economique Européen 
Sans objet.
La dernière date à laquelle cette notice a été révisée est : 
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
Les informations suivantes sont destinées exclusivement aux professionnels de santé:
L’utilisation de la milrinone injectable ne pourra être envisagée que chez des patients hospitalisés dans une unité de soins intensifs et soumis à un contrôle continu hémodynamique.
Posologie
Le traitement par la milrinone intraveineuse débutera d’abord par une dose de charge de 50 μg/kg en 10 min environ, suivie d’une perfusion continue de 0,375 à 0,750 μg/kg/min.
La posologie sera ajustée de façon à obtenir un effet hémodynamique maximum sans toutefois dépasser une dose totale de 1,13 mg/kg/jour.
La durée du traitement réalisée au cours des essais a été de 48 heures.
Population pédiatrique :
Dans les études publiées, les doses choisies pour les nourrissons et les enfants étaient :
· Dose de charge intraveineuse : 50 à 75 μg/kg administrée sur 30 à 60 minutes.
· Perfusion continue intraveineuse : à initier sur la base de la réponse hémodynamique et la survenue possible d’effets indésirables entre 0,25 à 0,75 μg/kg/min sur une période de temps allant jusqu’à 35 heures.
Dans les études cliniques du syndrome de bas débit cardiaque chez les nourrissons et les enfants de moins de 6 ans après une chirurgie correctrice d’une maladie cardiaque congénitale, une dose de charge de 75 μg/kg sur 60 minutes suive par une perfusion de 0,75 μg/kg/min pendant 35 heures réduisent significativement le risque de développement de syndrome de bas débit cardiaque.
Les résultats des études de pharmacocinétiques (voir rubrique 5.2 du RCP) ont été pris en considération.
Insuffisance rénale :
Du fait du manque de données, l’utilisation de MILRINONE STRAGEN n’est pas recommandée dans la population pédiatrique souffrant d’insuffisance rénale (voir rubrique 4.4 du RCP pour plus d’informations).
Persistance du canal artériel :
Si l’utilisation de MILRINONE STRAGEN est souhaitable chez les prématurés et les enfants à terme à risque de/ou souffrant de persistance du canal artériel, la nécessité du traitement doit être évaluée en fonction des risques potentiels (voir rubriques 4.4, 4.8, 5.2 et 5.3 du RCP).
Ajustement posologique chez les insuffisants rénaux :
Un ajustement posologique est nécessaire. L’ajustement posologique chez les insuffisants rénaux est basé sur des données obtenues avec des patients souffrant fréquemment d’insuffisance rénale mais sans insuffisance cardiaque congestive, qui montrent une augmentation significative de la demi-vie d’élimination terminale de la milrinone. La dose de charge n’est pas affectée, mais une diminution de la dose d’entretien peut être nécessaire en fonction de la sévérité de l’insuffisance rénale (fonction de la clairance de la créatinine) (voir tableau ci-dessous).
|
Clairance de la créatinine (ml/min/1,73 m2) |
Débit de perfusion (μg/kg/min) |
|
5 |
0,20 |
|
10 |
0,23 |
|
20 |
0,28 |
|
30 |
0,33 |
|
40 |
0,38 |
|
50 |
0,43 |
Mode et voie d’administration
Voie intraveineuse.
La milrinone intraveineuse peut être administrée pure ou diluée. La solution pour perfusion diluée de la manière recommandée dans une solution de NaCI 0,45%, de NaCI 0,9%, du glucose à 5% ou de Ringer lactate doit être fraîchement préparée juste avant utilisation.
La perfusion de milrinone sera établie à l’aide d’une pompe à débit constant reliée à une aiguille ou à un cathéter placé dans une veine aussi grosse que possible.
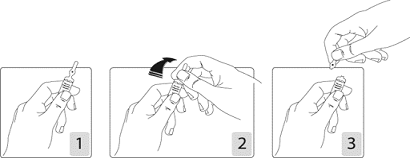
Pour ouvrir l’ampoule :
Tenez fermement l’ampoule, le point coloré face à vous (schéma 1).
Saisissez la tête de l’ampoule entre le pouce et l’index (le pouce sur le point coloré), puis exercez une pression vers l’arrière (schémas 2 et 3).
Si vous avez injecté plus de MILRINONE STRAGEN que vous n’auriez dû
De fortes doses de milrinone peuvent provoquer une hypotension et une arythmie cardiaque. Dans de telles circonstances, l’administration de la milrinone devra être interrompue jusqu’à stabilisation de l’état du patient.
Il n’existe pas d’antidote connu de la milrinone. Des mesures générales d’assistance circulatoire devront être mises en place, si nécessaire.
|
| Plan du site | Accessibilité | Contact | Téléchargement | Declaration de confidentialité | Service-Public.fr | Legifrance | Gouvernement.fr |