Dernière mise à jour le 28/04/2026
ACTIQ 200 microgrammes, comprimé avec applicateur buccal
Indications thérapeutiques
La substance active contenue dans ACTIQ, le fentanyl, est un antalgique puissant, également connu sous le nom d’opioïde.
L'unité d'ACTIQ se présente sous forme d'un comprimé sur un applicateur buccal.
· Il est utilisé pour traiter l’accès douloureux paroxystique chez les adultes et adolescents âgés de 16 ans et plus atteints d’un cancer et prenant déjà d’autres antalgiques de type morphinique pour le traitement des douleurs chroniques (permanentes) d’origine cancéreuse. L’accès douloureux paroxystique est une douleur supplémentaire qui survient brutalement en dépit de la prise des autres antalgiques habituels de type opioïde.
Présentations
> plaquette(s) papier aluminium PVC (ACLAR RX) polytrifluorochloroéthylène de 3 comprimé(s) avec applicateur(s) buccal(aux) en plastique
Code CIP : 358 063-0 ou 34009 358 063 0 7
Déclaration de commercialisation : 02/09/2002
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 18,17 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 19,19 €
- Taux de remboursement :65%
Documents de bon usage du médicament
- Prévenir le risque de surdose d’opioïdes
Auteur : Haute autorité de santé
Type : Fiche Bon Usage du Médicament
Date de mise à jour :Avril 2023
- Les médicaments des accès douloureux paroxystiques du cancer
Auteur : Haute autorité de santé
Type : Fiche Bon Usage du Médicament
Date de mise à jour :Juin 2014
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 16/09/2015 | Renouvellement d'inscription (CT) | Le service médical rendu par les spécialités ACTIQ et EFFENTORA reste important dans l’indication de leur AMM. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| III (Modéré) | Avis du 11/02/2004 | Inscription (CT) | L’amélioration du service médical rendu est de niveau III versus la prise en charge habituelle des accès douloureux paroxystiques chez des patients souffrant de douleurs chroniques d’origine cancéreuse. |
Autres informations
- Titulaire de l'autorisation : PHOENIX LABS UNLIMITED COMPANY
- Conditions de prescription et de délivrance :
- délivrance fractionnée de 7 jours
- prescription en toutes lettres sur ordonnance sécurisée
- prescription limitée à 4 semaines
- stupéfiants
- Statut de l'autorisation : Valide
- Type de procédure : Procédure de reconnaissance mutuelle
- Code CIS : 6 422 630 0
ANSM - Mis à jour le : 20/11/2025
ACTIQ 200 microgrammes, comprimé avec applicateur buccal
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Fentanyl (sous forme de citrate)........................................................................... 200 microgrammes
Pour un comprimé.
Excipients à effet notoire :
Un comprimé contient environ 1,89 g de glucose et 20-36 mg de saccharose.
Pour la liste complète des excipients, voir rubrique 6.1.
Comprimé avec applicateur buccal.
ACTIQ se présente sous la forme d’une matrice de poudre comprimée, blanche à blanc cassé, fixée à l’aide de colle alimentaire à un applicateur en plastique radio-opaque incassable. Le dosage est inscrit sur le comprimé et l’applicateur en plastique.
4.1. Indications thérapeutiques
Un accès douloureux paroxystique est une exacerbation passagère d’une douleur chronique par ailleurs contrôlée par un traitement de fond.
Les patients recevant un traitement de fond morphinique sont ceux prenant au moins 60 mg de morphine par voie orale par jour, au moins 25 microgrammes de fentanyl transdermique par heure, au moins 30 mg d’oxycodone par jour, au moins 8 mg d’hydromorphone par voie orale par jour ou une dose équianalgésique d’un autre opioïde pendant une durée d’au moins une semaine.
4.2. Posologie et mode d'administration
Afin de réduire au minimum les risques d’effets indésirables liés aux morphiniques et de déterminer la dose la plus "efficace" adaptée à un patient, il est indispensable que les patients soient étroitement surveillés par des professionnels de santé durant la période de titration.
ACTIQ n’est pas interchangeable sur la base d'une équivalence de dose avec d’autres fentanyl à action rapide prescrits pour les accès douloureux paroxystiques d'origine cancéreuse, étant donné que les profils pharmacocinétiques et/ou les schémas posologiques de ces produits sont significativement différents. Les patients traités pour des accès douloureux paroxystiques d'origine cancéreuse doivent être informés de ne pas utiliser simultanément plusieurs fentanyl à action rapide, et d’éliminer tout autre produit contenant du fentanyl antérieurement prescrit pour les accès douloureux paroxystiques (ADP) lors du passage à ACTIQ. Le nombre de dosages différents d’ACTIQ mis à disposition du patient, à tout moment, doit être réduit au minimum pour éviter les erreurs et un surdosage potentiel.
Toute unité d’ACTIQ non utilisée et dont le patient n’a plus l’utilité doit être dûment éliminée.
Il faut rappeler aux patients qu'ACTIQ doit impérativement être conservé hors de la portée des enfants.
Chez l’adulte
Adaptation posologique et traitement d’entretien
Il convient de déterminer la posologie optimale d'ACTIQ pour chaque patient, c'est-à-dire la dose produisant l'effet antalgique recherché avec un minimum d'effets indésirables. Lors des études cliniques, il n’a pas été établi de relation entre la dose efficace d'ACTIQ dans les accès douloureux paroxystiques et la dose du traitement morphinique de fond.
a) Titration
Avant de déterminer la posologie d'ACTIQ chez un patient, il est nécessaire de s’assurer que ses douleurs chroniques sont contrôlées par un traitement morphinique de fond et qu’il ne présente pas plus de 4 accès douloureux paroxystiques par jour.
La dose initiale d'ACTIQ doit être de 200 microgrammes, avec augmentation de la posologie, si nécessaire, conformément à la gamme de dosages disponibles (200, 400, 600, 800, 1200 et 1600 microgrammes). Les patients doivent être surveillés avec attention jusqu’à l'obtention de la dose procurant une analgésie efficace et des effets indésirables acceptables, avec une seule unité d'ACTIQ par accès douloureux paroxystique. Cette dose est définie comme étant la dose efficace.
Durant la titration, si une analgésie satisfaisante n’est pas obtenue dans les 30 minutes suivant l’administration d'une première unité d’ACTIQ (c’est-à-dire 15 minutes suivant la fin de la dissolution d’une unité d'ACTIQ), une seconde unité d'ACTIQ du même dosage pourra être utilisée. En aucun cas il ne faudra utiliser plus de deux unités d'ACTIQ pour traiter un même accès douloureux paroxystique. Avec le dosage de 1600 microgrammes, il ne sera vraisemblablement nécessaire d'administrer une seconde dose que chez une minorité de patients.
Si le traitement de plusieurs accès douloureux paroxystiques consécutifs requiert plus d’une unité d'ACTIQ par accès, il convient d’envisager de passer au dosage immédiatement supérieur.
SCHEMA PRATIQUE DE TITRATION
Commencer par une unité dosée à 200 microgrammes
¯
1. Laisser fondre dans la bouche 1 unité d’ACTIQ jusqu’à dissolution complète (15 minutes)
2. Attendre encore 15 minutes supplémentaires. Si nécessaire, en cas d’analgésie insuffisante, prendre une seconde unité à laisser fondre en 15 minutes
3. Tester la même dose d’ACTIQ lors de plusieurs accès douloureux paroxystiques consécutifs.
¯
Soulagement satisfaisant avec 1 unité ?
|
¯ OUI |
|
¯ NON |
|
Dose efficace déterminée |
|
utiliser le dosage d'ACTIQ immédiatement supérieur (dosages disponibles : 200, 400, 600, 800, 1200, 1600 microgrammes) |
b) Traitement d'entretien
Une fois la dose efficace établie (c'est-à-dire un accès douloureux paroxystique est efficacement traité par une seule unité, en moyenne), les patients doivent utiliser cette dose et limiter leur consommation à un maximum de quatre unités d'ACTIQ par jour.
Les patients doivent être surveillés par un professionnel de santé afin de veiller à ce que la consommation maximale de quatre unités d'ACTIQ par jour ne soit pas dépassée.
Réajustement de la dose
La dose d’entretien d’ACTIQ doit être augmentée si le traitement de plusieurs accès douloureux paroxystiques consécutifs requiert plus d’un comprimé par accès. Pour l'ajustement de la dose, les mêmes principes que ceux décrits pour la titration s'appliquent (voir ci-dessus).
Si les patients présentent plus de 4 accès douloureux paroxystiques par jour, il peut être nécessaire de réévaluer la posologie du traitement morphinique de fond. Si celle-ci est augmentée, il peut être nécessaire de réajuster la dose d'ACTIQ utilisée pour traiter les accès douloureux paroxystiques.
En l’absence de contrôle adéquat de la douleur, la possibilité d’hyperalgésie, de tolérance et de progression de la maladie sous-jacente doit être envisagée (voir rubrique 4.4).
Tout réajustement de la posologie du traitement analgésique doit impérativement être surveillé par un professionnel de santé.
Durée et objectifs du traitement
Avant l’instauration du traitement par ACTIQ, une stratégie thérapeutique comprenant la durée et les objectifs du traitement, doivent être convenus avec le patient, conformément aux lignes directrices relatives à la prise en charge de la douleur. Pendant le traitement, des contacts fréquents doivent avoir lieu entre le médecin et le patient afin d’évaluer la nécessité de poursuivre le traitement, d’envisager l’arrêt du traitement et d’ajuster les doses si nécessaire. En l’absence d’un contrôle adéquat de la douleur, la possibilité d’hyperalgésie, de tolérance et de progression de la maladie sous-jacente doit être envisagée (voir rubrique 4.4). ACTIQ ne doit pas être utilisé plus longtemps que nécessaire.
Arrêt du traitement
Le traitement par ACTIQ doit être immédiatement arrêté si le patient ne présente plus d’accès douloureux paroxystiques. Le traitement de la douleur chronique de fond doit être poursuivi conformément à la prescription. Si l’arrêt de tout traitement opioïde est nécessaire, le patient doit être étroitement surveillé par le médecin car un protocole d’arrêt progressif des morphiniques est nécessaire afin d’éviter le risque d’apparition de symptômes liés à un sevrage brutal.
Utilisation chez le sujet âgé
Les sujets âgés se sont avérés plus sensibles aux effets du fentanyl administré par voie intraveineuse. Par conséquent, la titration impose des précautions particulières chez ces patients. Le fentanyl est éliminé plus lentement chez le sujet âgé et sa demi-vie terminale d'élimination est plus longue, ce qui peut entraîner une accumulation de la substance active et majorer les risques d'effets indésirables.
Aucune étude clinique spécifique n'a été menée avec ACTIQ chez le sujet âgé. Néanmoins, au cours des études cliniques, les doses d'ACTIQ permettant un soulagement efficace des accès douloureux paroxystiques ont été plus basses chez les patients âgés de plus de 65 ans.
Utilisation chez les patients présentant une insuffisance hépatique ou rénale
Il convient d’être particulièrement prudent durant la phase de titration chez les patients présentant une insuffisance rénale ou hépatique (voir rubrique 4.4).
Population pédiatrique
Chez les adolescents âgés de 16 ans et plus : suivre la posologie adulte.
Chez les enfants et adolescents de moins de 16 ans : la sécurité et l’efficacité chez les enfants et adolescents de moins de 16 ans n’ont pas été établies. L’expérience clinique concernant l’utilisation d’ACTIQ en pédiatrie, chez des patients recevant déjà un traitement morphinique de fond est limitée (voir rubriques 5.1 et 5.2). L’utilisation dans cette population de patients n’est donc pas recommandée.
Mode d’administration
ACTIQ est destiné à l’administration par voie buccale transmuqueuse. Par conséquent, le comprimé doit être placé contre la face interne de la joue. A l’aide de l'applicateur, il faut ensuite déplacer le comprimé contre la muqueuse des joues et tourner l’applicateur, afin d'optimiser le degré d’exposition de la muqueuse au produit. Il faut laisser fondre le comprimé d'ACTIQ au contact de la muqueuse, en le suçant, sans le mâcher, car l’absorption du fentanyl par la muqueuse buccale est plus rapide que l’absorption systémique par voie gastro-intestinale.
Les patients souffrant de sécheresse buccale peuvent humidifier leur muqueuse buccale en buvant un peu d'eau avant la prise du médicament.
L'unité d’ACTIQ doit être consommée en 15 minutes. Si des effets morphiniques excessifs apparaissent avant que le comprimé d'ACTIQ soit entièrement dissout, celui-ci devra être immédiatement retiré de la bouche et il devra être envisagé de réduire les doses ultérieures.
· Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
· Patients ne recevant pas de traitement de fond morphinique, en raison d’un risque accru de dépression respiratoire.
· Traitement de la douleur aiguë autre que les accès douloureux paroxystiques.
· Administration concomitante ou interrompue depuis moins de 2 semaines, d'inhibiteurs de la monoamine-oxydase (IMAO) (voir rubriques 4.4 et 4.5).
· Patients traités avec des médicaments contenant de l’oxybate de sodium.
· Dépression respiratoire sévère ou obstruction sévère des voies aériennes.
4.4. Mises en garde spéciales et précautions d'emploi
Utilisation accidentelle chez les enfants
Les patients et leurs soignants doivent être informés de la nécessité de conserver toutes les unités hors de la vue et de la portée des enfants et d’éliminer soigneusement toutes les unités, utilisées ou non. Chez tout patient ambulatoire, il est recommandé d'évaluer les éventuels risques d'exposition accidentelle d'enfants au médicament.
Traitement de fond morphinique
ACTIQ ne doit en aucun cas être administré à des patients ne recevant pas un traitement de fond par des morphiniques, en raison d'un risque accru de dépression respiratoire et de décès. Avant de commencer un traitement par ACTIQ, le traitement morphinique de fond doit être stabilisé et le patient doit continuer le traitement par les morphiniques pendant la prise d’ACTIQ.
Tolérance et troubles liés à l’usage d’opioïdes (abus et dépendance)
Une accoutumance, une dépendance physique et une dépendance psychologique sont susceptibles d’apparaître lors de l’administration répétée de morphiniques. Le risque d’une utilisation abusive peut apparaître avec le fentanyl, de la même manière qu’avec d’autres morphiniques, et tous les patients traités par morphiniques doivent faire l’objet d’une surveillance dans le but de mettre en évidence tout signe d’utilisation abusive et d’addiction. Les patients ayant un risque accru d’utilisation abusive des morphiniques peuvent, malgré tout, être traités par morphiniques, mais l’apparition de tout signe de mésusage, d’utilisation abusive ou d’addiction doit être étroitement surveillé.
L’utilisation répétée d’ACTIQ peut conduire à un trouble lié à l’usage d’opioïdes (TUO). Une dose plus élevée et une durée plus longue du traitement par opioïdes peuvent augmenter le risque de développer un TUO. Une utilisation abusive ou un mésusage intentionnel d’ACTIQ peut entraîner un surdosage et/ou le décès. Le risque de survenue d’un TUO est accru chez les patients ayant des antécédents personnels ou familiaux (parents ou fratrie) de troubles liés à la consommation de substances (y compris d’alcoolisme), en cas de tabagisme actif ou chez les patients ayant des antécédents personnels d’autres troubles de la santé mentale (dépression caractérisée, troubles anxieux et troubles de la personnalité, par exemple).
Avant l’instauration du traitement par ACTIQ et pendant le traitement, les objectifs du traitement et un plan d’arrêt doivent être convenus en accord avec le patient (voir rubrique 4.2). Avant et pendant le traitement, le patient doit également être informé des risques et des signes de TUO. En cas d’apparition de ces signes, les patients doivent être invités à contacter leur médecin.
Les patients doivent être surveillés afin de détecter tout signe de comportements de recherche compulsive du produit (demande de renouvellement trop précoce de la prescription, par exemple). Dans ce cadre, les opioïdes et médicaments psychoactifs (tels que les benzodiazépines) utilisés en concomitance devront être passés en revue. Pour les patients présentant des signes et symptômes de TUO, une consultation auprès d’un addictologue devra être envisagée.
Hyperalgésie
Comme avec les autres opioïdes, en cas de contrôle insuffisant de la douleur en réponse à une dose plus élevée de fentanyl, la possibilité d’hyperalgésie induite par les opioïdes doit être envisagée. Une réduction de la dose de fentanyl, l’arrêt du traitement par le fentanyl ou une réévaluation du traitement peuvent être indiqués.
Effets endocriniens
Les morphiniques peuvent avoir une action pharmacologique sur l’axe hypothalamo-hypophyso-surrénalien ou sur l’axe hypothalamo-hypophyso-gonadique. Une augmentation de la prolactine sérique et une diminution du cortisol plasmatique et de la testostérone peuvent être observés. Des signes et des symptômes cliniques peuvent apparaître suite à ces modifications hormonales.
Des cas d'insuffisance surrénale ont plus souvent été rapportés avec l'utilisation des opioïdes incluant les comprimés de fentanyl, après plus d’un mois d'utilisation. Le patient doit progressivement arrêter l'opioïde pour permettre la récupération de la fonction surrénale et doit continuer le traitement corticoïde jusqu'à ce que la fonction surrénale soit rétablie (voir rubrique 4.8).
Dépression respiratoire
Comme pour tous les morphiniques, l’utilisation d'ACTIQ expose à un risque de dépression respiratoire cliniquement significative, par conséquence les patients devront être surveillés. Une prudence particulière est recommandée lors de la titration d'ACTIQ chez des patients présentant une bronchopneumopathie chronique obstructive non sévère ou toute autre pathologie pré-existante les prédisposant à une dépression respiratoire car, même administré aux doses thérapeutiques normales, ACTIQ peut aggraver les troubles respiratoires jusqu'à provoquer une insuffisance respiratoire.
Troubles respiratoires liés au sommeil
Les opioïdes peuvent provoquer des troubles respiratoires liés au sommeil, notamment une apnée centrale du sommeil (ACS) et une hypoxémie liée au sommeil. L’utilisation d’opioïdes augmente le risque d’ACS de façon dose-dépendante. Chez les patients présentant une ACS, une réduction de la dose totale des opioïdes doit être envisagée.
Alcool
L’utilisation concomitante d’alcool et de fentanyl peut induire une augmentation des effets dépresseurs pouvant entraîner une issue fatale (voir rubrique 4.5).
Risques en cas d’administration concomitante de benzodiazépines
L’utilisation concomitante d’opioïdes, dont ACTIQ, et de benzodiazépines peut entraîner une sédation profonde, une dépression respiratoire, un coma et le décès. Compte tenu de ces risques, la prescription concomitante d’opioïdes et de benzodiazépines ne doit se faire que chez les patients pour lesquels il n’existe pas d’autres options thérapeutiques adéquates.
Si la décision est prise de prescrire ACTIQ conjointement à des benzodiazépines, il conviendra de choisir la plus faible dose efficace et la durée minimale d’utilisation concomitante. Les patients doivent être étroitement surveillés pour déceler tout signe et symptôme éventuel de dépression respiratoire et de sédation (voir rubrique 4.5).
Effets cérébraux de l'hypercapnie, troubles de la conscience, traumatisme crânien
ACTIQ doit être administré avec une extrême prudence chez les patients qui pourraient être particulièrement sensibles aux effets cérébraux de l'hypercapnie, par exemple chez les patients présentant des signes d'hypertension intracrânienne ou des troubles de la conscience. Les morphiniques pouvant masquer l’évolution clinique en cas de traumatisme crânien, ils ne doivent être utilisés dans ce cadre qu'en cas de nécessité clinique absolue.
Bradyarythmies
Le fentanyl peut provoquer une bradycardie. Par conséquent, le fentanyl doit être utilisé avec prudence chez les patients présentant des antécédents de bradyarythmie ou une bradyarythmie préexistante.
Insuffisance rénale ou hépatique
En outre, ACTIQ doit être administré avec prudence chez les patients présentant une insuffisance hépatique ou rénale, car on ne connaît pas l'influence d'un dysfonctionnement hépatique et rénal sur la pharmacocinétique du fentanyl. Toutefois, en cas d'administration intraveineuse, la clairance du fentanyl est altérée par l'insuffisance hépatique ou rénale, en raison d'une détérioration de la clairance métabolique et des effets sur les protéines plasmatiques. L'insuffisance hépatique ou rénale peut augmenter la biodisponibilité du fentanyl absorbé par voie buccale et diminuer sa clairance systémique, entraînant ainsi des effets morphiniques accrus et prolongés. Une prudence particulière est donc de rigueur lors de la phase de titration chez des patients présentant une insuffisance hépatique ou rénale modérée à sévère.
Hypovolémie, hypotension
Le traitement par ACTIQ doit être envisagé avec prudence en présence d'hypovolémie ou d'hypotension.
Caries dentaires
Une hygiène buccale normale est recommandée pour réduire tout effet nocif pour les dents. ACTIQ contenant environ 2 grammes de glucose, une consommation fréquente augmente le risque de caries dentaires. La sécheresse buccale associée au traitement par morphiniques peut augmenter ce risque. Pendant le traitement par ACTIQ, il est conseillé de se rendre régulièrement chez le dentiste pour des visites de contrôle.
Syndrome sérotoninergique
Il est conseillé de faire preuve de prudence lorsqu’ACTIQ est administré en association avec des médicaments qui affectent les systèmes de neurotransmission sérotoninergique.
Un syndrome sérotoninergique, susceptible de mettre en jeu le pronostic vital, peut se développer lors de l'utilisation concomitante de médicaments sérotoninergiques tels que des inhibiteurs sélectifs de la recapture de la sérotonine (ISRS) et des inhibiteurs de la recapture de la sérotonine et de la noradrénaline (IRSN), ainsi qu’avec des médicaments qui altèrent le métabolisme de la sérotonine (y compris les inhibiteurs de la monoamine oxydase [inhibiteurs MAO]) (voir rubrique 4.3). Cela peut se produire aux doses recommandées.
Le syndrome sérotoninergique peut s’accompagner d’altérations de l'état mental (p. ex. agitation, hallucinations, coma), d’une instabilité du système nerveux autonome (p. ex. tachycardie, pression artérielle labile, hyperthermie), de troubles neuromusculaires (p. ex. hyperréflexie, incoordination, rigidité) et/ou de symptômes gastro-intestinaux (p. ex. nausées, vomissements, diarrhée).
En cas de suspicion de syndrome sérotoninergique, il convient d’arrêter le traitement par ACTIQ.
Anaphylaxie et hypersensibilité
Des cas d’anaphylaxie et d’hypersensibilité ont été rapportés avec l’utilisation de médicaments à base de fentanyl administrés par voie buccale transmuqueuse (voir rubrique 4.8).
Population pédiatrique
L’utilisation d’ACTIQ chez les enfants et les adolescents de moins de 16 ans n’est pas recommandé en raison d’un manque de données sur la sécurité et l’efficacité (voir rubriques 5.1 et 5.2).
Excipients
Glucose
Contient 1,89 g de glucose par dose. Ceci est à prendre en compte pour les patients atteints de diabète sucré.
Les patients présentant un syndrome de malabsorption du glucose et du galactose (maladie héréditaire rare) ne doivent pas prendre ce médicament.
Peut être nocif pour les dents.
Saccharose
Les patients présentant une intolérance au fructose, un syndrome de malabsorption du glucose et du galactose ou un déficit en sucrase/isomaltase (maladies héréditaires rares) ne doivent pas prendre ce médicament.
Peut être nocif pour les dents.
Sodium
Ce médicament contient moins de 1 mmol (23 mg) de sodium par comprimé, c.-à-d. qu’il est essentiellement « sans sodium ».
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Agents ayant un effet sur l’activité du CYP3A4
Inhibiteurs du CYP3A4
Le fentanyl est métabolisé par l'isoenzyme CYP3A4 dans le foie et la muqueuse intestinale.
Les inhibiteurs puissants de l’isoenzyme CYP3A4, comme les macrolides (tels que l’érythromycine), les antifongiques azolés (tels que le kétoconazole, l’itraconazole et le fluconazole) et certains inhibiteurs de protéases (tels que le ritonavir) sont susceptibles d'augmenter la biodisponibilité du fentanyl absorbé par voie buccale et de diminuer également sa clairance systémique, provoquant ainsi des effets morphiniques accrus et prolongés.
Des effets similaires pourraient être observés après ingestion concomitante de jus de pamplemousse, connu pour inhiber le CYP3A4. La prudence est donc de rigueur lors de l'administration concomitante de fentanyl avec des inhibiteurs du CYP3A4.
Inducteurs du CYP3A4
La co-administration d’inducteurs du CYP3A4 peut réduire l’efficacité d’ACTIQ.
Agents pouvant augmenter les effets dépresseurs sur le SNC
La co-administration de fentanyl avec d’autres dépresseurs du SNC (autres morphiniques, sédatifs ou hypnotiques [dont les benzodiazépines], anesthésiques généraux, phénothiazines, tranquillisants, myorelaxants, antihistaminiques sédatifs, gabapentinoïdes [gabapentine et prégabaline] ou alcool) peut potentialiser les effets dépresseurs de chaque produit, ce qui peut conduire à une dépression respiratoire, une hypotension, une sédation profonde, un coma ou une issue fatale (voir rubrique 4.4).
Sédatifs tels que les benzodiazépines ou les médicaments apparentés
L’utilisation concomitante d’opioïdes et de sédatifs tels que les benzodiazépines ou les médicaments apparentés augmente le risque de sédation, de dépression respiratoire, de coma et de décès en raison de l’effet dépresseur additif exercé sur le SNC. La dose et la durée de l’utilisation concomitante doivent être limitées (voir rubrique 4.4).
Antalgiques morphiniques agonistes/antagonistes partiels
L’utilisation concomitante d'antalgiques agonistes/antagonistes partiels (p. ex. buprénorphine, nalbuphine, pentazocine) n'est pas recommandée. En effet, ils possèdent une forte affinité pour les récepteurs opioïdes avec une activité intrinsèque relativement faible et donc antagonisent partiellement l’effet analgésique du fentanyl pouvant ainsi induire un syndrome de sevrage chez les patients dépendants aux opioïdes.
Agents sérotoninergiques
La co-administration de fentanyl et d’un agent sérotoninergique, tel qu’un inhibiteur sélectif de la recapture de la sérotonine (ISRS), un inhibiteur de la recapture de la sérotonine et de la noradrénaline (IRSN) ou un inhibiteur de la monoamine oxydase (IMAO), peut augmenter le risque de syndrome sérotoninergique, une pathologie pouvant mettre en jeu le pronostic vital (voir rubrique 4.3).
Oxybate de sodium
L’administration concomitante de fentanyl avec des médicaments contenant de l’oxybate de sodium est contre-indiquée (voir rubrique 4.3). Le traitement par l’oxybate de sodium doit être interrompu avant le début du traitement par ACTIQ.
4.6. Fertilité, grossesse et allaitement
Grossesse
Il n'existe pas de données ou des données limitées sur l’utilisation du fentanyl durant la grossesse. Les études animales ont montré une toxicité sur la reproduction (voir rubrique 5.3). Les analgésiques morphiniques peuvent entraîner une dépression respiratoire chez le nouveau-né. En cas d’utilisation prolongée de fentanyl pendant la grossesse, il existe un risque de syndrome de sevrage des opioïdes chez le nouveau-né, pouvant engager le pronostic vital s’il n’est pas identifié et traité, et nécessitant une prise en charge conformément aux protocoles développés par les experts en néonatalogie. ACTIQ ne doit être utilisé chez la femme enceinte que s'il s'avère manifestement nécessaire.
Si l’utilisation d’opioïdes est nécessaire sur une durée prolongée chez une femme enceinte, la patiente doit être informée du risque de syndrome de sevrage néonatal des opioïdes et un traitement approprié doit être tenu à disposition (voir rubrique 4.8).
Il est recommandé de ne pas utiliser ACTIQ pendant le travail et l'accouchement (y compris en cas de césarienne), car le fentanyl franchit la barrière placentaire et peut entraîner une dépression respiratoire chez le fœtus. Le taux de passage transplacentaire est de 0,44 (rapport fœto-maternel : 1,00/2,27).
Allaitement
Le fentanyl est excrété dans le lait maternel, et peut entraîner une sédation et une dépression respiratoire chez le nourrisson allaité. Le fentanyl ne doit pas être utilisé pendant l’allaitement. L'allaitement ne doit pas être repris avant au moins 5 jours après la dernière administration de fentanyl.
Fertilité
Il n'existe pas de données sur la fertilité chez l’être humain. Dans les études animales, la fertilité des mâles était altérée (voir rubrique 5.3).
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Les effets indésirables typiques des morphiniques peuvent être observés lors de la prise d’ACTIQ. Le plus souvent, ils disparaissent ou diminuent d'intensité avec la poursuite du traitement et l'obtention de la posologie adéquate.
Cependant, les effets indésirables les plus graves sont la dépression respiratoire (pouvant aboutir à l’apnée ou l’arrêt respiratoire), la dépression circulatoire, l’hypotension et le choc, et tous les patients doivent être attentivement suivis afin de détecter ces effets indésirables
Des réactions au niveau du site d’administration telles que des saignements des gencives, des irritations, des douleurs et des ulcères ont été rapportées depuis la commercialisation d’ACTIQ.
Les études cliniques menées avec ACTIQ avaient pour but d’évaluer l’efficacité et la tolérance du produit dans le traitement des accès douloureux paroxystiques, les patients inclus ont reçu en même temps d’autres morphiniques (morphine à libération prolongée ou fentanyl par voie transdermique) pour traiter leurs douleurs chroniques. Par conséquent, il n’est pas possible d’isoler avec certitude les effets indésirables dus au seul traitement par ACTIQ.
Les effets indésirables suivants ont été rapportés au cours des études cliniques avec ACTIQ et/ou d’autres médicaments contenant du fentanyl, durant les essais cliniques ou au cours de la période post-commercialisation. Les effets indésirables sont répertoriés ci-dessous selon la classification MedDRA par classe de systèmes d’organes et par fréquence (les fréquences sont définies comme suit : très fréquent ≥ 1/10, fréquent ≥ 1/100 à < 1/10, peu fréquent ≥ 1/1 000 à < 1/100, fréquence indéterminée (ne peut être estimée sur la base des données disponibles) :
|
Classe de systèmes d’organes |
Très fréquent |
Fréquent |
Peu fréquent |
Fréquence indéterminée |
|
Affections du système immunitaire |
|
|
|
réaction anaphylactique, œdème de la langue, œdème des lèvres |
|
Affections endocriniennes |
|
|
|
Insuffisance surrénale, déficit androgénique |
|
Troubles du métabolisme et de la nutrition |
|
anorexie |
|
|
|
Affections psychiatriques |
|
confusion, anxiété, hallucinations, dépression, labilité émotionnelle |
rêves anormaux, dépersonnalisation, troubles de la pensée, euphorie |
Insomnie, pharmacodépendance (addiction), utilisation abusive (voir rubrique 4.4), délire |
|
Affections du système nerveux |
somnolence, sensations vertigineuses, céphalées |
perte de conscience, convulsions, vertiges, myoclonie, sédation, paresthésies (incluant hyperesthésies/paresthésies péribuccales), démarche anormale/incoordination, perversion du goût |
coma, dysarthrie |
|
|
Affections oculaires |
|
Vision anormale (vision trouble, vision double) |
|
|
|
Affections vasculaires |
|
|
vasodilatation |
bouffée congestive, bouffée de chaleur |
|
Affections respiratoires, thoraciques et médiastinales |
dyspnée |
|
|
œdème pharyngé, dépression respiratoire, syndrome d’apnée du sommeil |
|
Affections gastro-intestinales |
nausées, vomissements, constipation, douleurs abdominales |
bouche sèche, dyspepsie, stomatite, trouble de la langue (par exemple : sensation de brûlure, ulcères), flatulence, distension abdominale |
iléus, ulcérations de la bouche, caries dentaires, saignement gingival |
chute de dent, rétraction gingivale, gingivites, diarrhée, dysphagie |
|
Affections de la peau et du tissu sous-cutané |
|
prurit, sécrétion de sueur, rash |
urticaire |
|
|
Affections du rein et des voies urinaires |
|
rétention urinaire |
|
|
|
Troubles généraux et anomalies au site d’administration |
asthénie |
réactions au site d’administration y compris irritation, douleur et ulcère, malaise |
|
fatigue, œdème périphérique, fièvre, syndrome de sevrage, syndrome de sevrage néonatal (voir rubrique 4.6), tolérance au médicament, saignement au site d’application |
|
Investigations |
|
poids diminué |
|
|
|
Lésions, intoxications et complications liées aux procédures |
|
blessures accidentelles (par exemple : chutes) |
|
|
* des symptômes de sevrage des opioïdes tels que nausées, vomissements, diarrhée, anxiété, frissons, tremblements et sécrétion de sueur ont été observés avec le fentanyl administré par voie transmuqueuse.
Description de certains effets indésirables
Tolérance
La tolérance peut se développer lors d’une utilisation répétée.
Pharmacodépendance
L’utilisation répétée d’ACTIQ peut entraîner une dépendance aux médicaments (pharmacodépendance), même à des doses thérapeutiques. Le risque de pharmacodépendance peut varier selon les facteurs de risque propres au patient, de la posologie et de la durée du traitement par opioïdes (voir rubrique 4.4).
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr.
Symptômes
Les symptômes à attendre en cas de surdosage par fentanyl sont de même nature que ceux observés après l'administration intraveineuse de fentanyl ou d'autres morphiniques, et résultent de son action pharmacologique. Les effets indésirables les plus graves sont l’altération des facultés mentales, la perte de conscience, le coma, l’arrêt cardio-respiratoire, la dépression respiratoire, la détresse respiratoire et l’insuffisance respiratoire ayant entraîné le décès.
Des cas de respiration de Cheyne Stokes ont été observés en cas de surdosage en fentanyl, en particulier chez les patients ayant des antécédents d’insuffisance cardiaque.
Une leucoencéphalopathie toxique a également été observée lors d’un surdosage en fentanyl.
Prise en charge
Les mesures à prendre immédiatement en présence d'un surdosage morphinique consistent à retirer immédiatement l'unité d'ACTIQ de la bouche du patient si elle s'y trouve encore, à l'aide de l'applicateur, assurer la perméabilité des voies respiratoires, effectuer des stimulations physiques et verbales du patient et déterminer son niveau de conscience ainsi que son état ventilatoire et circulatoire. Instaurer si nécessaire une ventilation assistée.
Surdosage (ingestion accidentelle) chez une personne n’ayant jamais reçu de traitement morphinique
Le traitement du surdosage chez une personne qui n'a jamais reçu de traitement morphinique (ingestion accidentelle), nécessite de mettre en place une voie d'abord veineux et d’administrer de la naloxone ou un autre antagoniste des morphiniques, selon l'état clinique. La durée de la dépression respiratoire due au surdosage peut être plus longue que les effets de l'antagoniste morphinique (par exemple, la demi-vie de la naloxone est comprise entre 30 et 81 minutes) et il peut donc être nécessaire de répéter l'administration de l'antidote.
Pour plus de détails sur le mode d'emploi de l'antagoniste morphinique utilisé, se référer au Résumé des Caractéristiques du Produit en question.
Surdosage chez les patients recevant un traitement d’entretien morphinique
Chez les patients recevant un traitement morphinique bien toléré, mettre en place une voie d'abord intraveineux. Dans certains cas, l'utilisation judicieuse de naloxone ou d'autres antagonistes des morphiniques peut être justifiée, mais elle expose au risque de déclenchement d'un syndrome de sevrage aigu.
Bien qu'il n'ait jamais été décrit de rigidité musculaire associée à la dépression respiratoire après administration d'ACTIQ, un tel phénomène est possible avec le fentanyl ou d'autres morphiniques. Si une telle rigidité musculaire apparaît, il faudra instaurer une ventilation assistée, administrer un antagoniste des morphiniques et, en dernier recours, un curarisant.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Le fentanyl, agoniste morphinomimétique pur, agit essentiellement sur les récepteurs morphiniques μ du cerveau, de la moelle épinière et des muscles lisses. L'effet thérapeutique s'exerce essentiellement au niveau du SNC. L'analgésie représente l'effet pharmacologique clinique le plus utile résultant de l'interaction du fentanyl sur les récepteurs μ. Cet effet est corrélé aux taux sanguins circulants du fentanyl, à condition de tenir compte du délai de pénétration dans le SNC et du délai de disparition du SNC (phénomène dont la demi-vie est de 3 à 5 minutes).
Chez les sujets n'ayant jamais reçu de traitement morphinique, l'effet analgésique apparaît à des concentrations sanguines de 1 à 2 ng/mL, alors que l'effet anesthésique chirurgical associé à une profonde dépression respiratoire se produit à des concentrations de 10 à 20 ng/mL.
Chez des patients cancéreux dont les douleurs chroniques étaient contrôlées par des administrations régulières de doses stables de morphiniques, le soulagement des accès douloureux paroxystiques induit par ACTIQ a été significativement supérieur à celui d'un placebo, 15, 30, 45 et 60 minutes après le début de l'administration.
Les effets indésirables des morphiniques incluent une augmentation du tonus et une diminution des contractions des muscles lisses du tractus gastro-intestinal. Ces deux phénomènes allongent la durée du transit intestinal et peuvent être responsables de la constipation liée aux morphiniques.
Bien que les morphiniques augmentent généralement le tonus des muscles lisses des voies urinaires, l'effet global est variable : dans certains cas, ils provoquent un besoin impérieux d'uriner et dans d'autres cas une dysurie.
Tous les agonistes des récepteurs μ, y compris le fentanyl, induisent une dépression respiratoire dose-dépendante. Le risque de dépression respiratoire est moindre chez les patients présentant des douleurs et chez ceux qui reçoivent un traitement morphinique de fond, car il apparaît une tolérance à la dépression respiratoire et aux autres effets morphiniques. Chez les patients non traités par les morphiniques, la dépression respiratoire maximale est généralement observée 15 à 30 minutes après le début de l'administration d'ACTIQ et peut se prolonger plusieurs heures.
Les opioïdes peuvent influer sur l’axe hypothalamo-hypophyso-surrénalien ou sur l’axe hypothalamo-hypophyso-gonadique. Les modifications pouvant être observées comprennent notamment une augmentation de la prolactine sérique et des diminutions du cortisol plasmatique et de la testostérone. Ces modifications hormonales peuvent se manifester par des signes et symptômes cliniques (voir également rubrique 4.8). Les effets pharmacologiques secondaires supplémentaires incluent le myosis.
Population pédiatrique
L’expérience de l’utilisation d’ACTIQ en pédiatrie, chez des patients âgés de moins de 16 ans, est limitée. Dans une étude clinique, 15 patients (sur 38) âgés de 5 à 15 ans, recevant déjà un traitement morphinique de fond et présentant des accès douloureux paroxystiques ont été traités avec ACTIQ. L’effectif de l’étude était trop faible pour permettre des conclusions sur la sécurité et l’efficacité d’ACTIQ dans cette population de patients.
5.2. Propriétés pharmacocinétiques
Le fentanyl est une substance très lipophile. Il est absorbé très rapidement par la muqueuse buccale et plus lentement par le tractus gastro-intestinal. Il subit un métabolisme par effet de premier passage hépatique et intestinal, mais ses métabolites ne contribuent pas à ses effets thérapeutiques.
Absorption
La pharmacocinétique de l'absorption du fentanyl après l'utilisation d'ACTIQ comprend une absorption initiale rapide à partir de la muqueuse buccale et une absorption plus lente du fentanyl dégluti, à partir du tractus gastro-intestinal.
Environ 25 % de la dose totale d'ACTIQ sont rapidement absorbés par la muqueuse buccale. Le reste de la dose totale (soit 75 %) est dégluti avec la salive et ensuite lentement absorbé au niveau du tractus gastro-intestinal. Environ un tiers de cette fraction (soit 25 % de la dose totale) échappe à l'élimination lors du premier passage hépatique et intestinal et devient disponible sur le plan systémique.
Autrement dit, la biodisponibilité d'ACTIQ généralement observée (50 %) se répartit en parts égales entre l'absorption transmuqueuse rapide et l'absorption gastro-intestinale plus lente.
La valeur de Cmax est comprise entre 0,39 et 2,51 ng/mL (200 microgrammes à 1600 microgrammes). La concentration plasmatique maximale est atteinte en médiane en 20 à 40 minutes (Tmax) (valeurs extrêmes : 20 et 480 minutes) après le début de la consommation d'ACTIQ.
Distribution
Les expérimentations animales montrent que le fentanyl se répartit rapidement dans le cerveau, le cœur, les poumons, les reins et la rate, puis est redistribué de façon plus lente vers les muscles et le tissu adipeux. Le taux de liaison du fentanyl aux protéines plasmatiques est de 80-85 %, cette liaison impliquant essentiellement l'alpha-1 glycoprotéine acide mais également, dans une certaine mesure, l'albumine et les lipoprotéines. L'acidose augmente la fraction libre de fentanyl. Le volume moyen de distribution à l'état d'équilibre (Vss) est de 4 L/kg.
Biotransformation
Le fentanyl est métabolisé en norfentanyl dans le foie et la muqueuse intestinale sous l'effet de l'isoenzyme 3A4 du cytochrome P450. Lors des expérimentations animales, le norfentanyl n'a pas montré d'effet pharmacologique. Plus de 90 % de la dose de fentanyl administrée sont éliminés par biotransformation en métabolites N-désalkylés et hydroxylés inactifs.
Elimination
Moins de 7 % de la dose sont excrétés sous forme inchangée dans les urines et seul environ 1 % est excrété sous forme inchangée dans les selles. Les métabolites sont essentiellement excrétés par voie urinaire, l'excrétion fécale étant moins importante. La clairance plasmatique totale du fentanyl est de 0,5 L/h/kg (extrêmes : 0,3 - 0,7 L/h/kg). Après administration d'ACTIQ, la demi-vie d'élimination terminale est d'environ 7 heures.
Linéarité/non linéarité
Pour la gamme de dosages disponibles (200 à 1600 microgrammes), les paramètres pharmacocinétiques d’ACTIQ sont dose-dépendants.
Population pédiatrique
Dans une étude clinique, 15 patients âgés de 5 à 15 ans, recevant déjà un traitement morphinique de fond et présentant des accès douloureux paroxystiques ont été traités avec ACTIQ à des doses de 200 microgrammes à 600 microgrammes. Les valeurs de l’air sous la courbe basées sur les concentrations observées étaient 2 fois plus élevées chez les jeunes enfants que chez les adolescents (respectivement, 5,25 versus 2,65 ng.h/mL) et 4 fois plus élevées chez les jeunes enfants par rapport aux adultes (5,25 versus 1,20 ng.h/mL). Sur une base ajustée au poids, les valeurs de la clairance et du volume de distribution étaient similaires dans la tranche d’âge.
5.3. Données de sécurité préclinique
Les études de toxicité sur le développement embryo-fœtal conduites chez le rat et le lapin n’ont révélé aucune malformation ou modification du développement lors de l’administration pendant la période d'organogenèse.
Dans une étude de fertilité et de développement embryonnaire précoce chez le rat, un effet médié par les mâles a été observé à forte dose (300 µg/kg/jour, voie sous-cutanée), concordant avec les effets sédatifs du fentanyl.
Dans les études de développement pré et post-natal chez le rat, le taux de survie de la descendance était significativement réduit à des doses entraînant une toxicité maternelle sévère. Les effets des doses toxiques maternelles sur la première génération sont : un retard du développement physique, des fonctions sensorielles, du réflexe et du comportement. Ces effets peuvent être des effets indirects de négligence maternelle et/ ou de diminution de l’allaitement ou un effet direct du fentanyl.
Les études de cancérogénicité (test alternatif par voie cutanée chez la souris transgénique Tg AC durant 26 semaines, étude de cancérogénèse par voie sous-cutanée chez le rat durant deux ans) avec le fentanyl ne montrent pas de résultats suggérant un potentiel oncogène. L’analyse de coupes de cerveau provenant de l’étude de cancérogenèse réalisée chez le rat a montré des lésions cérébrales chez les animaux ayant reçu des doses élevées de citrate de fentanyl. La pertinence clinique de ces résultats n’est pas connue.
Dextrates hydratés (contenant du glucose), acide citrique, phosphate disodique, arôme artificiel de baies (maltodextrine (contenant du glucose), propylène glycol, arômes artificiels, citrate de triéthyle), stéarate de magnésium.
Colle alimentaire liant le comprimé à l'applicateur :
Amidon de maïs modifié (E 1450), sucre à confiserie (contenant du saccharose et de l’amidon de maïs), eau purifiée.
Encre pour le marquage des comprimés :
Eau désionisée, gomme laque décirée blanche, colorant bleu synthétique à base de goudron (E 133) et hydroxyde d’ammonium (E 527) pour ajustement du pH.
3 ans.
6.4. Précautions particulières de conservation
A conserver à une température ne dépassant pas 30°C.
A conserver dans le blister protecteur jusqu’à utilisation.
6.5. Nature et contenu de l'emballage extérieur
Comprimé avec applicateur buccal sous plaquettes (Papier/Aluminium/PVC/ACLAR). Boîtes de 3, 6, 15 ou 30.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Toutes les unités, utilisées ou non, doivent être conservées hors de portée des enfants et éliminées soigneusement, comme indiqué ci-dessous. Les unités partiellement utilisées sont particulièrement dangereuses pour les enfants.
Après la consommation totale d'ACTIQ, l'applicateur doit être immédiatement stocké dans le container prévu à cet effet qui sera placé hors de portée des enfants.
Si le médicament n'a été que partiellement consommé, le reste du comprimé doit être dissous sous un robinet d'eau chaude, puis l'applicateur doit être immédiatement stocké dans le container prévu à cet effet qui sera placé hors de portée des enfants.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
PHOENIX LABS UNLIMITED COMPANY
SUITE 12 BUNKILLA PLAZA
BRACETOWN BUSINESS PARK
CLONEE, COUNTY MEATH
IRLANDE
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 358 063 0 7 : 3 comprimés avec applicateur buccal sous plaquettes (Papier/Aluminium/PVC/ACLAR)
· 34009 358 064 7 5 : 6 comprimés avec applicateur buccal sous plaquettes (Papier/Aluminium/PVC/ACLAR)
· 34009 358 065 3 6 : 15 comprimés avec applicateur buccal sous plaquettes (Papier/Aluminium/PVC/ACLAR)
· 34009 358 067 6 5 : 30 comprimés avec applicateur buccal sous plaquettes (Papier/Aluminium/PVC/ACLAR)
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Stupéfiant :
· Prescription limitée à 28 jours.
· Délivrance limitée à 7 jours.
Prescription sur ordonnance répondant aux spécifications fixées par l’arrêté du 31 mars 1999.
ANSM - Mis à jour le : 20/11/2025
ACTIQ 200 microgrammes, comprimé avec applicateur buccal
fentanyl
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s'applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que ACTIQ 200 microgrammes, comprimé avec applicateur buccal et dans quel cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d’utiliser ACTIQ 200 microgrammes, comprimé avec applicateur buccal ?
3. Comment utiliser ACTIQ 200 microgrammes, comprimé avec applicateur buccal ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver ACTIQ 200 microgrammes, comprimé avec applicateur buccal ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE ACTIQ 200 microgrammes, comprimé avec applicateur buccal ET DANS QUELS CAS EST-IL UTILISE ?
La substance active contenue dans ACTIQ, le fentanyl, est un antalgique puissant, également connu sous le nom d’opioïde.
L'unité d'ACTIQ se présente sous forme d'un comprimé sur un applicateur buccal.
· Il est utilisé pour traiter l’accès douloureux paroxystique chez les adultes et adolescents âgés de 16 ans et plus atteints d’un cancer et prenant déjà d’autres antalgiques de type morphinique pour le traitement des douleurs chroniques (permanentes) d’origine cancéreuse. L’accès douloureux paroxystique est une douleur supplémentaire qui survient brutalement en dépit de la prise des autres antalgiques habituels de type opioïde.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER ACTIQ 200 microgrammes, comprimé avec applicateur buccal ?
N’utilisez jamais ACTIQ 200 microgrammes, comprimé avec applicateur buccal :
· si vous ne prenez pas régulièrement des médicaments de type opioïde sous ordonnance (p.ex. codéine, fentanyl, hydromorphone, morphine, oxycodone, péthidine) tous les jours à intervalles réguliers depuis au moins une semaine pour contrôler votre douleur persistante. Si vous ne prenez pas ces médicaments, vous ne devez pas utiliser ACTIQ, car cela peut augmenter le risque que votre respiration devienne dangereusement lente et/ou superficielle, voire qu’elle s’arrête ;
· si vous êtes allergique au fentanyl ou à l'un des autres composants contenus dans ce médicament (mentionnés dans la rubrique 6) ;
· si vous prenez actuellement des inhibiteurs de la monoamine oxydase (MAO) (médicaments utilisés dans la dépression sévère) ou si vous en avez pris au cours des deux dernières semaines (voir rubrique 2 sous « Adressez-vous à votre médecin ou pharmacien AVANT d’utiliser ACTIQ si ») ;
· si vous prenez un médicament qui contient de l’oxybate de sodium ;
· si vous avez de graves problèmes respiratoires ou de graves problèmes pulmonaires avec obstruction ;
· si vous souffrez de douleurs de courte durée (par ex. douleurs liées à des blessures, une chirurgie, des maux de tête ou des migraines) autres que des accès douloureux paroxystiques.
N’utilisez PAS ACTIQ si vous êtes concerné(e) par l’un des cas cités ci-dessus. Si vous avez un doute, veuillez en informer votre médecin ou votre pharmacien AVANT d’utiliser ACTIQ.
Avertissements et précautions
Au cours de votre traitement par ACTIQ, continuez d’utiliser l'antalgique opioïde que vous prenez pour vos douleurs chroniques (permanentes) dues au cancer.
Adressez-vous à votre médecin ou pharmacien AVANT d’utiliser ACTIQ si :
· votre traitement avec un antalgique de type opioïde pour traiter vos douleurs chroniques (permanentes) d’origine cancéreuse n’est pas encore stabilisé ;
· vous avez une maladie qui affecte votre respiration (par ex. asthme, respiration sifflante, ou essoufflement) ;
· vous présentez un traumatisme crânien ou si vous avez eu des pertes de conscience ;
· vous avez des problèmes cardiaques, notamment une fréquence cardiaque lente ;
· vous avez des problèmes au foie ou aux reins, le processus de dégradation du médicament dans votre organisme peut être affecté ;
· vous avez une tension artérielle basse due à un volume sanguin bas ;
· vous avez du diabète ;
· vous avez plus de 65 ans - vous avez besoin d’une dose plus faible. Toute augmentation de dose sera revue avec attention par votre médecin ;
· vous prenez des benzodiazépines (voir rubrique 2 « Autres médicaments et ACTIQ »). L’utilisation de benzodiazépines peut augmenter le risque d’effets indésirables graves, y compris le décès.
· vous prenez des antidépresseurs ou des neuroleptiques (inhibiteurs sélectifs de la recapture de la sérotonine [ISRS], inhibiteurs de la recapture de la sérotonine et de la noradrénaline [IRSN], inhibiteurs de la monoamine oxydase [IMAO], voir rubrique 2 sous « Ne prenez PAS ACTIQ » et « Autres médicaments et ACTIQ »). L’utilisation de ces médicaments avec ACTIQ peut entraîner un syndrome sérotoninergique, une affection potentiellement mortelle (voir rubrique 2 sous « Autres médicaments et ACTIQ, comprimé avec applicateur buccal ») ;
· vous avez déjà utilisé de manière abusive ou été dépendant(e) d’opioïdes ou de tout autre médicament, alcool ou drogue illicite ;
· vous avez déjà développé une insuffisance surrénalienne, une affection au cours de laquelle les glandes surrénales ne produisent pas suffisamment d’hormones, ou un manque d’hormones sexuelles (carence en androgènes) avec l'utilisation d’un opioïde (voir rubrique 4 sous « Effets indésirables graves ») ;
· vous consommez de l’alcool ; veuillez consulter la rubrique « ACTIQ, comprimé avec applicateur buccal avec des aliments, boissons et de l’alcool ».
Consultez votre médecin PENDANT votre traitement par ACTIQ si :
· vous ressentez une douleur ou une sensibilité accrue à la douleur (hyperalgésie) qui ne répond pas à une augmentation de la dose du médicament prescrite par votre médecin.
· vous présentez des signes de carie dentaire. ACTIQ contenant environ 2 grammes de sucre, une consommation fréquente vous expose à un risque accru de caries dentaires qui peuvent être graves. Il est important de prendre bien soin de vos dents pendant le traitement par ACTIQ. Allez régulièrement chez le dentiste pour faire contrôler vos dents pendant le traitement.
· vous présentez une association des symptômes suivants : nausées, vomissements, anorexie, fatigue, faiblesse, sensations vertigineuses et pression artérielle basse. Ensemble, ces symptômes peuvent être le signe d’une maladie pouvant engager le pronostic vital appelée insuffisance surrénalienne, dans laquelle les glandes surrénaliennes ne produisent pas suffisamment d’hormones.
· Troubles respiratoires liés au sommeil : ACTIQ peut provoquer des troubles respiratoires liés au sommeil tels que des apnées du sommeil (interruption de la respiration pendant le sommeil) et une hypoxémie liée au sommeil (faible taux d’oxygène dans le sang). Les symptômes associés comprennent des arrêts de la respiration pendant le sommeil, des réveils nocturnes dus à un essoufflement, des difficultés à rester endormi(e) ou d’une somnolence excessive durant la journée. Si vous ou une personne de votre entourage remarquez ces symptômes, contactez votre médecin. Une réduction de la dose pourra être envisagée par votre médecin.
Utilisation au long cours et tolérance
Ce médicament contient du fentanyl, qui est un médicament opioïde. L’utilisation répétée d’analgésiques opioïdes peut entraîner une diminution de l’efficacité du médicament (vous vous y habituez, ce que l’on appelle la tolérance aux médicaments). Vous pouvez également devenir plus sensible à la douleur lors de l’utilisation d’ACTIQ. C’est ce que l’on appelle l’hyperalgésie. L’augmentation de la dose d’ACTIQ peut vous aider à réduire davantage vos douleurs pendant un certain temps, mais elle peut également être nocive. Si vous remarquez que votre médicament devient moins efficace, parlez-en à votre médecin. Votre médecin décidera s’il est préférable pour vous d’augmenter la dose ou de diminuer progressivement votre utilisation d’ACTIQ.
Dépendance et addiction
L’utilisation répétée d’ACTIQ peut également entraîner une dépendance, un abus et une addiction, qui peuvent aboutir à un surdosage mettant la vie en danger. Le risque de ces effets indésirables peut augmenter avec une dose plus élevée et une durée d’utilisation plus longue. La dépendance ou l’addiction peut vous donner l’impression que vous ne contrôlez plus la quantité de médicament que vous devez utiliser ou la fréquence à laquelle vous devez l’utiliser. Vous pouvez avoir l’impression que vous devez continuer à prendre votre médicament, même s’il ne vous aide pas à soulager votre douleur.
Le risque de développer une dépendance ou une addiction varie d’une personne à l’autre. Vous pouvez présenter un risque plus élevé de développer une dépendance ou une addiction à ACTIQ si :
· vous ou un membre de votre famille avez déjà consommé de façon abusive ou été dépendant(e) de l’alcool, à des médicaments prescrits sur ordonnance ou à des substances illicites (« addiction ») ;
· vous fumez ;
· vous avez déjà présenté des troubles de l’humeur (dépression, anxiété ou trouble de la personnalité) ou avez été traité(e) par un psychiatre pour d’autres maladies mentales.
Si vous remarquez l’un des signes suivants lors de l’utilisation d’ACTIQ, il pourrait s’agir d’un signe que vous avez développé une dépendance ou une addiction :
· vous avez besoin d’utiliser le médicament pendant une durée plus longue que celle indiquée par votre médecin ;
· vous avez besoin d’utiliser une dose supérieure à la dose recommandée ;
· vous utilisez le médicament pour des raisons autres que celles qui vous ont été prescrites, par exemple « pour rester calme » ou « pour vous aider à dormir » ;
· vous avez tenté à plusieurs reprises et sans succès d’arrêter d’utiliser le médicament ou de contrôler son utilisation
· Lorsque vous arrêtez de prendre le médicament, vous vous sentez mal (par exemple, nausées, vomissements, diarrhées, anxiété, frissons, tremblements et transpiration), et vous vous sentez mieux lorsque vous reprenez le médicament (« effets de sevrage »).
Si vous remarquez l’un de ces signes, parlez-en à votre médecin pour discuter de la meilleure voie de traitement pour vous, y compris le moment opportun pour arrêter et la façon d’arrêter en toute sécurité.
Consultez IMMEDIATEMENT un médecin si :
· vous présentez des symptômes tels que des difficultés respiratoires ou des sensations vertigineuses, un gonflement de la langue, des lèvres ou de la gorge pendant votre traitement par ACTIQ. Il pourrait s’agir des premiers symptômes d’une grave réaction allergique (anaphylaxie, hypersensibilité ; voir rubrique 4 sous « Effets indésirables graves »).
Enfants et adolescents
ACTIQ n’est pas recommandé chez les enfants et les adolescents de moins de 16 ans.
Autres médicaments et ACTIQ 200 microgrammes, comprimé avec applicateur buccal
N’utilisez pas ce médicament et informez votre médecin ou votre pharmacien :
· Si vous prenez d’autres traitements contenant du fentanyl précédemment prescrits pour soulager vos accès douloureux paroxystiques. Si vous avez encore certains de ces traitements chez vous, contactez votre pharmacien pour vérifier comment les éliminer.
· Si vous prenez des inhibiteurs de la monoamine oxydase (MAO) (médicaments pour la dépression sévère) ou si vous en avez pris au cours des 2 dernières semaines (voir rubrique 2 sous « N’utilisez jamais ACTIQ, comprimé avec applicateur buccal » et « Adressez-vous à votre médecin ou pharmacien AVANT d’utiliser ACTIQ si »).
Avant d’utiliser ACTIQ, informez votre médecin ou votre pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament. Ceci comprend les médicaments obtenus sans prescription, incluant les médicaments à base de plantes. En particulier, veuillez informer votre médecin ou votre pharmacien si vous prenez l’un des médicaments suivants :
· L’utilisation concomitante d’ACTIQ et de sédatifs, tels que des benzodiazépines ou des médicaments apparentés, augmente le risque d’étourdissements, de difficultés respiratoires (dépression respiratoire), de coma et peut menacer le pronostic vital. Compte tenu de ces risques, l’utilisation concomitante ne doit être envisagée que lorsque les autres options de traitement ne sont pas possibles.
Toutefois, si votre médecin vous prescrit ACTIQ avec des sédatifs, il devra limiter la dose et la durée du traitement concomitant.
Veuillez avertir votre médecin de tous les sédatifs que vous prenez (tels que des somnifères, des médicaments contre l’anxiété, certains médicaments pour traiter les réactions allergiques [antihistaminiques] ou des tranquilisants) et respecter scrupuleusement les recommandations de votre médecin. Il pourrait être utile de demander à vos amis et à votre famille d’être attentifs aux signes et symptômes décrits ci-dessus. Contactez votre médecin si vous présentez de tels symptômes.
· Certains décontracturants musculaires - tels que baclofène, diazépam (voir également rubrique « Avertissements et précautions »).
· Tout médicament qui pourrait avoir un effet sur la manière dont votre organisme dégrade ACTIQ - tel que le ritonavir ou d’autres traitements de l’infection au VIH, ou d’autres médicaments appelés « inhibiteurs du CYP3A4 » tels que le kétoconazole, l’itraconazole ou le fluconazole (utilisé pour les infections fongiques) et la troléandomycine, la clarithromycine ou l’érythromycine (médicaments utilisés pour les infections bactériennes) et les médicaments appelés « inducteurs du CYP3A4 » tels que la rifampicine ou la rifabutine (médicaments utilisés pour les infections bactériennes), la carbamazépine, le phénobarbital ou la phénytoïne (médicaments utilisés pour traiter les crises convulsives).
· Certains types d’antalgiques puissants, appelés agonistes/antagonistes partiels, par exemple buprénorphine, nalbuphine et pentazocine (médicaments du traitement de la douleur). Vous pouvez ressentir des symptômes du syndrome de sevrage (nausées, vomissements, diarrhée, anxiété, frissons, tremblements, et sécrétion de sueur) quand vous utilisez ces médicaments.
· Certains anti-douleurs pour traiter les douleurs neuropathiques (gabapentine et prégabaline).
· Les médicaments sérotoninergiques utilisés pour traiter la dépression sont les antidépresseurs : tels que les inhibiteurs sélectifs de la recapture de la sérotonine (ISRS), et les inhibiteurs de la recapture de la sérotonine et de la noradrénaline (IRSN) ou les neuroleptiques. L’utilisation de ces médicaments avec ACTIQ peut entraîner un syndrome sérotoninergique susceptible de mettre en jeu le pronostic vital (voir rubrique 2 sous « Adressez-vous à votre médecin ou pharmacien AVANT d’utiliser ACTIQ si » et « N’utilisez jamais ACTIQ, comprimé avec applicateur buccal »). Les symptômes du syndrome sérotoninergique peuvent inclure des altérations de votre état mental (par exemple, agitation, hallucinations, coma), et d'autres effets tels qu’une température corporelle supérieure à 38°C, une augmentation de la fréquence cardiaque, une pression artérielle instable, et une exagération des réflexes, une rigidité musculaire, un manque de coordination et/ou des symptômes gastro-intestinaux (par exemple, nausées, vomissements, diarrhée). Votre médecin vous dira si ACTIQ est adapté pour vous.
Si vous devez subir une intervention chirurgicale avec un anesthésique par voie générale, parlez-en à votre médecin ou à votre infirmier/èr(e).
ACTIQ 200 microgrammes, comprimé avec applicateur buccal avec des aliments, boissons et de l’alcool
· ACTIQ peut être utilisé avant ou après les repas. Cependant, ne pas utiliser pendant les repas.
· Vous pouvez boire un peu d’eau avant d’utiliser ACTIQ afin d’humidifier votre bouche. Cependant, ne pas boire ni manger pendant l’utilisation d’ACTIQ.
· Ne pas boire de jus de pamplemousse lorsque vous utilisez ACTIQ car ceci peut influencer la manière dont votre organisme dégrade ACTIQ.
· Ne buvez pas d’alcool lorsque vous prenez ACTIQ. L’alcool peut augmenter le risque de survenue d’effets indésirables graves, incluant le décès.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant d’utiliser ce médicament.
Grossesse
ACTIQ ne doit pas être utilisé pendant la grossesse à moins d’en avoir parlé avec votre médecin.
Si ACTIQ est utilisé de façon prolongée pendant la grossesse, il existe également un risque de survenue de symptômes de sevrage chez le nouveau-né pouvant engager le pronostic vital, s’ils ne sont pas identifiés et traités par un médecin (voir rubrique 4 sous « Autres effets indésirables - Fréquence indéterminée »).
Vous ne devez pas utiliser ACTIQ lors de l’accouchement car le fentanyl peut entraîner une dépression respiratoire chez le nouveau-né.
Allaitement
Le fentanyl peut passer dans le lait maternel et entraîner des effets indésirables chez le nourrisson allaité. N’utilisez pas ACTIQ si vous allaitez. Vous ne devriez pas commencer l’allaitement jusqu’à au moins 5 jours après la dernière dose d’ACTIQ.
Conduite de véhicules et utilisation de machines
Ce médicament peut affecter votre capacité à conduire ou à utiliser tout outil ou machine. Veuillez en parler à votre médecin afin de savoir s’il est sans danger pour vous de conduire un véhicule ou d’utiliser des outils ou machines dans les premières heures suivant l’utilisation d’ACTIQ.
Ne conduisez pas de véhicule ou n’utilisez pas d’outils ou de machines si vous présentez l’un des symptômes suivants : somnolence, sensations vertigineuses, vision trouble ou double, difficultés à se concentrer. Il est important de savoir comment vous réagissez à ACTIQ avant de conduire un véhicule ou d’utiliser des outils ou machines.
ACTIQ contient du glucose
Contient 1,89 g de glucose par dose. Ceci est à prendre en compte pour les patients atteints de diabète sucré.
Si votre médecin vous a informé(e) d’une intolérance à certains sucres, contactez-le avant de prendre ce médicament.
Peut être nocif pour les dents.
ACTIQ contient du saccharose
Si votre médecin vous a informé(e) que vous avez une intolérance à certains sucres, contactez votre médecin avant de prendre ce médicament.
Peut être nocif pour les dents.
ACTIQ contient du sodium
Ce médicament contient moins de 1 mmol (23 mg) de sodium par comprimé, c.-à-d. qu’il est essentiellement « sans sodium ».
3. COMMENT UTILISER ACTIQ 200 microgrammes, comprimé avec applicateur buccal ?
Avant de commencer le traitement et régulièrement pendant le traitement, votre médecin discutera également avec vous de ce que vous pouvez attendre de l’utilisation d’ACTIQ, quand vous devez l’utiliser et pendant combien de temps, quand vous devez contacter votre médecin et quand vous devez l’arrêter (voir également rubrique 2).
Au début du traitement, votre médecin va rechercher avec vous la dose d'ACTIQ efficace pour traiter vos accès douloureux paroxystiques. Vous devez utiliser ACTIQ exactement comme votre médecin vous l'indiquera.
· Vous ne devez pas changer les doses d’ACTIQ ou de vos autres antalgiques de vous-même. Tout changement de dose doit être prescrit et contrôlé par votre médecin.
· En cas d'incertitude concernant la dose correcte ou pour toute question concernant l’utilisation de ce médicament, n'hésitez pas à en parler à votre médecin.
Comment le médicament entre-t-il dans votre corps ?
Quand vous placez le comprimé dans votre bouche :
· Le comprimé se dissout et libère ainsi la substance active. Cela se produit environ en 15 minutes.
· La substance active est alors absorbée par la muqueuse de votre bouche, pour aller dans la circulation sanguine.
L’utilisation de ce médicament de cette façon rend l’absorption plus rapide, ce qui permet de soulager plus vite votre accès douloureux paroxystique.
Quand la dose correcte a-t-elle été trouvée ?
Vous devez vous sentir soulagé rapidement lorsque vous utilisez ACTIQ. Cependant, pendant que vous et votre médecin déterminez la dose contrôlant votre accès douloureux paroxystique, vous pouvez ne pas être suffisamment soulagé au bout de 30 minutes après avoir commencé d'utiliser une seule unité d'ACTIQ (15 minutes à partir du moment où vous finissez d’utiliser l’unité d’ACTIQ). Si cela arrive, votre médecin peut vous permettre d’utiliser une seconde unité d’ACTIQ, de même dosage, pour traiter ce même accès douloureux paroxystique. N'utilisez pas une seconde unité d'ACTIQ à moins d'y avoir été autorisé par votre médecin. N'utilisez jamais plus de deux unités d'ACTIQ pour traiter un même accès douloureux paroxystique.
Quand la dose correcte est trouvée, vous pouvez avoir besoin d’avoir plus d’un dosage d’ACTIQ à la maison.
Cependant, ne conservez chez vous que les dosages d’ACTIQ dont vous avez besoin. Ceci pour éviter toute confusion possible ou surdosage. Demandez à votre pharmacien comment éliminer les unités d’ACTIQ dont vous n’avez pas besoin.
Combien d’unités utiliser ?
Une fois la dose correcte trouvée avec votre médecin, utilisez une unité pour traiter un même accès douloureux paroxystique.
Veuillez informer votre médecin si votre dose correcte ne soulage pas votre accès douloureux paroxystique lors de plusieurs accès douloureux paroxystiques se suivant. Votre médecin décidera si votre dose a besoin d’être changée.
Vous devez signaler immédiatement à votre médecin si vous prenez ACTIQ plus de quatre fois par jour car un changement de votre schéma thérapeutique peut être nécessaire. Votre médecin pourrait modifier votre traitement pour les douleurs persistantes ; lorsque vos douleurs persistantes seront contrôlées, il sera peut-être nécessaire que votre médecin modifie la dose d’ACTIQ que vous prenez. Si votre médecin pense que vous présentez une sensibilité à la douleur due à ACTIQ (une hyperalgésie), une réduction de votre dose d’ACTIQ sera peut-être envisagée (voir rubrique 2 sous « Avertissements et précautions »). Pour bénéficier d’un soulagement efficace, parlez avec votre médecin de votre douleur et de l’efficacité d’ACTIQ, de sorte que la dose puisse être modifiée si nécessaire.
Comment utiliser le médicament ?
Ouverture de l’unité - chaque unité d’ACTIQ est scellée dans un blister individuel.
· Ouvrez ce blister au moment de l'utilisation d'ACTIQ. Ne l’ouvrez pas à l’avance.
· Prendre le blister en tenant le côté non imprimé vers vous.
· Tenir fermement la partie la plus courte du blister.
· Placez les ciseaux près de l'extrémité opposée d'ACTIQ et coupez entièrement la languette la plus longue comme indiqué sur le dessin.
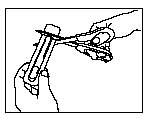
· Retirer complètement l'opercule (partie imprimée) du blister.
· Sortir l'unité d'ACTIQ du blister et placer aussitôt le comprimé d’ACTIQ dans votre bouche.
Utilisation de l’unité d’ACTIQ
· Placer le comprimé entre la joue et la gencive.
· Frottez en continu l'applicateur contre la face interne de la joue. Tournez souvent l'applicateur.
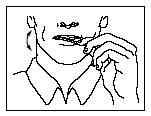
· Pour obtenir un soulagement maximum, le comprimé d'ACTIQ doit être dissout en 15 minutes. Si le comprimé d'ACTIQ se dissout trop rapidement, le médicament sera avalé avec la salive et votre accès douloureux paroxystique sera moins bien soulagé.

· Ne pas avaler en entier. Ne pas croquer ou mâcher le comprimé d’ACTIQ. Cela entrainerait une diminution de la libération du médicament dans la circulation sanguine, entraînant un soulagement de la douleur moindre que si ACTIQ est utilisé comme recommandé ci-dessus.
· Si vous ne finissez pas entièrement l'unité d'ACTIQ à chaque douleur paroxystique, quelle que soit la raison, informez-en votre médecin.
A quelle fréquence devez-vous utiliser ACTIQ ?
Une fois la dose contrôlant efficacement votre douleur trouvée, ne pas utiliser plus de quatre unités d'ACTIQ par jour. Si vous pensez que vous pourriez avoir besoin de plus de quatre unités d'ACTIQ par jour, informez-en immédiatement votre médecin.
Combien d’unités d’ACTIQ devez-vous utiliser ?
N'utilisez jamais plus de deux unités d'ACTIQ pour traiter un même accès douloureux paroxystique.
Si vous avez pris plus de ACTIQ 200 microgrammes, comprimé avec applicateur buccal que vous n’auriez dû
· Les effets indésirables les plus fréquents dus à un usage excessif sont la somnolence, les nausées ou les sensations vertigineuses. Si vous commencez à ressentir des sensations vertigineuses, des nausées ou à vous endormir avant la dissolution complète du comprimé, retirez le comprimé de votre bouche et appelez quelqu'un pour vous aider.
· Un effet indésirable grave d'ACTIQ est le ralentissement de la respiration et/ou une respiration superficielle. Cela peut arriver si votre dose d'ACTIQ est trop élevée ou si vous avez pris trop d'ACTIQ. Dans les cas sévères, la prise d’une quantité trop importante d’ACTIQ peut également conduire à un coma. Si vous ressentez une forte sensation de vertige, une grande somnolence ou si votre respiration est lente ou superficielle, contactez immédiatement un médecin.
Que faire si un enfant ou un adulte prend accidentellement ACTIQ ?
Si vous pensez que quelqu'un a pris ACTIQ accidentellement, appelez immédiatement un centre médical d’urgence. En attendant les secours, essayez de maintenir la personne éveillée (en l'appelant par son nom et en la secouant par le bras ou par l'épaule).
Si vous oubliez d’utiliser ACTIQ 200 microgrammes, comprimé avec applicateur buccal
Si vous avez encore un accès douloureux paroxystique, vous pouvez utiliser ACTIQ, tel que votre médecin vous l’a conseillé. Si l’accès douloureux paroxystique est terminé, n’utilisez pas ACTIQ avant le prochain accès douloureux paroxystique.
Si vous arrêtez d’utiliser ACTIQ 200 microgrammes, comprimé avec applicateur buccal
Vous devez arrêter la prise d’ACTIQ lorsque vous n’avez plus d’accès douloureux paroxystique. Cependant, vous devez continuer à prendre votre antidouleur habituel pour traiter votre douleur cancéreuse persistante comme vous l’a conseillé votre médecin. À l’arrêt d’ACTIQ, vous pouvez ressentir des symptômes de sevrage, comparables aux effets indésirables potentiels d’ACTIQ. Si vous ressentez des symptômes de sevrage ou si vous vous inquiétez du soulagement de votre douleur, contactez votre médecin. Votre médecin évaluera la nécessité d’un traitement pour réduire ou éliminer les symptômes de sevrage.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Effets indésirables graves
· Les effets indésirables les plus graves sont une respiration superficielle, une tension artérielle basse et un arrêt respiratoire.
Vous ou votre soignant devez retirer l’unité d’ACTIQ de la bouche du patient, contacter immédiatement votre médecin et appeler les services médicaux d’urgence si vous ressentez l’un des effets indésirables graves suivants - vous pourriez avoir besoin de soins médicaux d’urgence :
o Une somnolence importante ou une respiration lente et/ou superficielle.
o Des difficultés à respirer ou des sensations vertigineuses, un gonflement de la langue, des lèvres ou de la gorge qui pourraient être les premiers signes d’une réaction allergique grave.
A l'attention de l'entourage du patient ou des soignants :
· En cas de respiration lente ou faible d'une personne traitée avec ACTIQ, ou encore si vous avez des difficultés à la réveiller, vous devez IMMEDIATEMENT suivre les instructions suivantes :
o Retirez l'unité d'ACTIQ de la bouche du patient à l'aide de l'applicateur et maintenez-la hors de portée des enfants et des animaux domestiques avant de l'éliminer.
o APPELEZ UN CENTRE MEDICAL D'URGENCE.
o En attendant les secours, si la personne respire lentement ou faiblement, obligez-la à respirer en la stimulant toutes les 5 à 10 secondes.
Si vous ressentez des sensations vertigineuses, si vous êtes somnolent(e), si votre respiration devient lente ou faible, ou si vous vous sentez mal en utilisant une unité d'ACTIQ, retirez le médicament de votre bouche à l'aide de l'applicateur et éliminez-le, conformément aux instructions fournies dans cette notice (voir rubrique 5). Contactez ensuite votre médecin afin qu'il vous indique comment continuer votre traitement.
· Contactez votre médecin si vous ressentez plusieurs des symptômes suivants : nausées, vomissements, perte d’appétit, fatigue, faiblesse, sensations vertigineuses et tension artérielle basse. La présence conjointe de ces symptômes peut être le signe d’un trouble pouvant engager le pronostic vital, appelé insuffisance surrénalienne, qui correspond à une incapacité des glandes surrénales à produire suffisamment d’hormones.
· L’utilisation prolongée de fentanyl pendant la grossesse peut entraîner un risque de syndrome de sevrage chez le nouveau-né, pouvant engager son pronostic vital (voir rubrique 2 sous « Grossesse et allaitement »).
Autres effets indésirables
Très fréquent : pouvant affecter plus de 1 personne sur 10
· Vomissements, nausées/sensation de malaise, constipation, maux d’estomac (douleurs abdominales).
· Fatigue (faiblesse), somnolence, sensations vertigineuses, maux de tête.
· Souffle court.
Fréquent : pouvant affecter jusqu’à 1 personne sur 10
· Confusion, anxiété, voir ou entendre des choses qui n’existent pas (hallucinations), dépression, humeur changeante.
· Malaises.
· Contractions musculaires involontaires, sensation d’étourdissement, perte de conscience, sédation, fourmillements ou engourdissement, incoordination des mouvements, augmentation ou modification de la sensibilité au toucher, convulsions (crises d’épilepsie).
· Sécheresse de la bouche, inflammation de la bouche, affections de la langue (par exemple, brûlures ou ulcérations), altération du goût.
· Flatulences, ballonnements, digestion difficile, perte d’appétit, perte de poids.
· Vision trouble ou double.
· Sécrétion de sueur, rougeurs cutanées, démangeaisons.
· Difficulté à uriner.
· Blessures accidentelles (par exemple : chutes).
Peu fréquent : pouvant affecter jusqu’à 1 personne sur 100
· Caries dentaires (pouvant nécessiter une extraction dentaire), paralysie de l'intestin, ulcères de la bouche, saignement des gencives.
· Coma, troubles de l’élocution.
· Rêves anormaux, difficulté de concentration, troubles de la pensée, sensation excessive de bien-être.
· Dilatation des vaisseaux sanguins.
· Urticaire.
Fréquence indéterminée
Les effets indésirables suivants ont été rapportés au cours de l’utilisation d’ACTIQ mais leur fréquence est indéterminée :
· Rétraction gingivale, inflammation des gencives, chute de dent, problèmes respiratoires importants, bouffées de chaleur, sensation d’avoir très chaud, diarrhée, œdème des bras ou des jambes, fatigue, insomnie, fièvre, syndrome de sevrage (peut se manifester par l’apparition des effets indésirables suivants : nausées, vomissements, diarrhée, anxiété, frissons, tremblements et sécrétion de sueur).
· Manque d’hormones sexuelles (carence en androgènes).
· Pharmacodépendance (addiction) (voir rubrique 2).
· Utilisation abusive (voir rubrique 2).
· Tolérance au médicament (voir rubrique 2).
· Délire (les symptômes peuvent inclure une combinaison d’agitation, d’impatience, de désorientation, de confusion, de peur, de troubles du sommeil et de cauchemars, ou le fait d’avoir des visions ou d’entendre des choses qui ne sont pas réellement présentes).
· Difficultés à respirer pendant le sommeil.
· Saignement au site d’application.
· Difficultés à avaler.
Un traitement de longue durée par le fentanyl pendant la grossesse peut provoquer des symptômes de sevrage chez le nouveau-né pouvant engager le pronostic vital (voir rubrique 2).
Lors de l’utilisation d’ACTIQ, vous pouvez ressentir une irritation, des douleurs et des ulcères au niveau du site d’application et présenter un saignement des gencives.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER ACTIQ 200 microgrammes, comprimé avec applicateur buccal ?
Conservez ce médicament dans un endroit sûr et sécurisé, où d’autres personnes ne peuvent pas y accéder. Il peut causer des dommages graves et être fatal pour les personnes qui peuvent prendre ce médicament par accident, ou intentionnellement alors qu’il ne leur a pas été prescrit.
ACTIQ contient un médicament contre la douleur très puissant qui peut être mortel pour un enfant en cas de prise accidentelle. ACTIQ doit être conservé hors de la vue et de la portée des enfants.
· N’utilisez pas ce médicament après la date de péremption indiquée sur l’étiquette et la boîte. La date de péremption fait référence au dernier jour de ce mois.
· A conserver à une température ne dépassant pas 30°C.
· Conservez toujours ACTIQ dans son blister jusqu’à ce que vous soyez prêt à l’utiliser. Ne pas utiliser ACTIQ si le blister est abîmé ou s'il a été ouvert.
· Si vous arrêtez votre traitement ou si vous avez des unités d'ACTIQ non utilisées à votre domicile, vous devez les rapporter à votre pharmacien ou à votre médecin.
Comment éliminer ACTIQ après utilisation ?
Lorsqu'elles ne sont pas complètement utilisées, les unités d'ACTIQ peuvent contenir une quantité de produit suffisante pour être dangereuse et même mortelle pour un enfant.
Même s'il reste peu ou pas de produit sur l'applicateur, celui-ci doit être éliminé comme suit :
· Si le comprimé a été entièrement consommé, jetez l'applicateur dans un container d'élimination prévu à cet effet et maintenez-le hors de portée des enfants et des animaux domestiques.
· S'il reste du médicament sur l'applicateur, placez l'unité d'ACTIQ sous l'eau chaude jusqu'à ce que le comprimé soit complètement dissout, puis jetez l'applicateur dans un container d'élimination hors de portée des enfants et des animaux domestiques.
· Lorsque le container d’élimination qui vous a été fourni est plein, rapportez-le à votre pharmacien qui vous en fournira un nouveau.
· Si vous ne finissez pas complètement votre unité d'ACTIQ et que vous ne pouvez pas dissoudre immédiatement le résidu du comprimé, placez l'unité d'ACTIQ hors de portée des enfants et des animaux domestiques jusqu'au moment où vous pourrez l'éliminer comme décrit ci-dessus.
· Ne jetez pas les unités d'ACTIQ partiellement utilisées, les applicateurs ou les blisters dans les toilettes.
Normalement, l’unité d’ACTIQ est blanche. Elle peut cependant avoir un aspect tacheté au bout d’un certain temps de conservation. Ceci est dû à de légères altérations de l’arôme du médicament et n’affecte en rien son efficacité.
Ne jetez aucun médicament au tout-à-l'égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient ACTIQ 200 microgrammes, comprimé avec applicateur buccal
· La substance active est :
Fentanyl (sous forme de citrate)..................................................................... 200 microgrammes
Pour un comprimé.
· Les autres composants sont :
Comprimé :
Dextrates hydratés (équivalant à 1,89 grammes de glucose environ), acide citrique, phosphate disodique, arôme artificiel de baies (maltodextrine (contenant du glucose), propylène glycol, arômes artificiels, citrate de triéthyle) et stéarate de magnésium.
Colle alimentaire utilisée pour lier le comprimé à l’applicateur :
Amidon de maïs modifié (E 1450), saccharose, amidon de maïs et eau.
Encre pour le marquage des comprimés :
Eau, gomme laque décirée blanche, colorant bleu synthétique à base de goudron (E 133), hydroxyde d’ammonium (E 527) pour ajustement du pH.
ACTIQ est constitué d’un comprimé blanc à blanc cassé fixé sur un applicateur permettant l’application au niveau de la muqueuse buccale. Le comprimé peut avoir un aspect tacheté au bout d’un certain temps de conservation. Ceci est dû à de légères altérations de l’arôme du médicament et n’affecte en rien son efficacité.
Il existe six dosages différents d'ACTIQ : 200, 400, 600, 800, 1200 et 1600 microgrammes. Le dosage est inscrit sur le comprimé blanc, sur l'applicateur, sur le blister et sur la boîte, afin que vous soyez assuré de prendre le bon dosage. Chaque dosage est associé à une couleur spécifique.
Chaque blister contient une seule unité d'ACTIQ, et est conditionné en boîtes de 3, 6, 15 ou 30 unités.
Titulaire de l’autorisation de mise sur le marché
PHOENIX LABS UNLIMITED COMPANY
SUITE 12 BUNKILLA PLAZA
BRACETOWN BUSINESS PARK
CLONEE, COUNTY MEATH
IRLANDE
Exploitant de l’autorisation de mise sur le marché
CENTRE SPECIALITES PHARMACEUTIQUES
76-78 AVENUE DU MIDI
63800 COURNON D’AUVERGNE
FRANCE
LUDWIG-MERCKLE-STRAßE 3
89143 BLAUBEUREN
ALLEMAGNE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).