
ANSM - Mis à jour le : 06/11/2023
FLIXOVATE 0,005 %, pommade
Propionate de fluticasone
Veuillez lire attentivement cette notice avant d’utiliser ce médicament car elle contient des informations importantes pour vous.
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que FLIXOVATE 0,005 %, pommade et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser FLIXOVATE 0,005 %, pommade ?
3. Comment utiliser FLIXOVATE 0,005 %, pommade ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver FLIXOVATE 0,005 %, pommade ?
6. Contenu de l’emballage et autres informations.

Classe pharmacothérapeutique : corticoïde d’activité forte (groupe III)- code ATC : D07AC17
Ce médicament contient du propionate de fluticasone qui est un corticoïde local d'activité forte, il est destiné à une application cutanée.
Ce médicament est préconisé chez l'adulte et l'enfant à partir de l'âge de 1 an, dans certaines maladies de peau comme l'eczéma de contact, la dermatite atopique, le psoriasis. Ce médicament est également utilisé chez le nourrisson, à partir de l'âge de 3 mois, uniquement pour traiter la dermatite atopique.

N’utilisez jamais FLIXOVATE 0,005 %, pommade dans les cas suivants :
· si vous êtes allergique à la substance active, le propionate de fluticasone ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6,
· lésions ulcérées,
· acné,
· rosacée (affection de la peau, siégeant sur le visage, provoquant des rougeurs sur le nez, les joues, le menton, le front ou la totalité du visage, pouvant engendrer une dilatation des petits vaisseaux sanguins et l'apparition de boutons (papules) parfois remplis de pus (pustules)),
· dermatite péri-orale (éruption et rougeur autour de la bouche),
· démangeaisons autour de l’anus ou des zones génitales (pénis et vagin),
· maladies de la peau chez le nourrisson de moins de trois mois, y compris dermatite et érythème fessier,
· maladies infectieuses de la peau non traitées d'origine virale (herpès, zona, varicelle...), bactérienne (exemple impétigo...), mycosique (dues à des champignons microscopiques) ou parasitaire.
Avertissements et précautions
Adressez-vous à votre médecin ou à votre pharmacien avant d’utiliser FLIXOVATE 0,005 %, pommade.
· éviter tout contact avec les yeux et les muqueuses.
· ne pas appliquer sur les paupières en cas de traitement prolongé en raison du risque de cataracte et de glaucome.
· ne pas appliquer sur le visage en cas de traitement prolongé en raison du risque d'atrophie cutanée (amincissement de la peau) sauf en cas de prescription formelle de votre médecin.
Il est souhaitable d'éviter les applications sur une grande surface, sous un pansement ou couche imperméable en particulier chez les enfants et nourrissons en raison de la possibilité de passage d'une partie du principe actif dans le sang.
· Un risque de passage dans le sang de ce corticoïde local existe par augmentation de sa pénétration cutanée dans les situations suivantes :
o Traitement prolongé
o Application sur une zone étendue
o Application cutanée sous occlusion : par ex. au niveau des plis ou sous pansement occlusif ou chez les nourrissons où les couches peuvent avoir les mêmes conséquences qu’un pansement occlusif.
o Augmentation de l’hydratation de la peau
o Application sur des surfaces cutanées fines comme le visage
o Application sur des lésions cutanées
o Application chez l’enfant, particulièrement chez le nourrisson et l'enfant en bas âge car plus à risque d'effets indésirables généraux que l'adulte en raison d'une peau immature et d'un rapport surface corporelle / poids plus important que l’adulte. Ces effets disparaissent à l'arrêt du traitement, mais un arrêt progressif est nécessaire.
En cas d'occlusion chez le nourrisson, il existe un risque d'infection bactérienne favorisée par la chaleur et l’humidité présentes dans les plis cutanés ou sous un pansement occlusif ou sous les couches. En cas d’utilisation d’un pansement occlusif, la peau devra être nettoyée avant chaque changement du pansement.
Une utilisation dans le traitement du psoriasis nécessite une surveillance médicale attentive des rechutes, le développement d’une accoutumance, un risque de psoriasis pustuleux généralisé et une toxicité locale ou générale due à l’altération de la barrière cutanée.
Signalez toute irritation ou infection à votre médecin car un traitement antimicrobien approprié devra être utilisé chaque fois que les lésions inflammatoires traitées s’infectent. Si l’infection se propage, il faut arrêter la corticothérapie locale et traiter l'infection.
Ulcères chroniques de jambe
Les corticoïdes locaux sont parfois utilisés en traitement des lésions inflammatoires de la peau (dermatites) entourant les ulcères chroniques de jambe. Cet usage peut être associé à une augmentation des réactions allergiques locales et du risque d’infection locale.
Risque d’inflammabilité
Lors de l’utilisation de FLIXOVATE 0,005 % pommade, ne pas fumer ni s'approcher de flammes nues en raison du risque de brûlures graves. Les tissus (vêtements, literie, pansements, etc.) qui ont été en contact avec ce produit brûlent plus facilement et peuvent constituer un risque d'incendie. Le lavage des vêtements et de la literie peut réduire l'accumulation de produit, mais ne peut pas l'éliminer totalement.
Si une allergie locale apparaît, vous devez arrêter le traitement et consulter votre médecin.
· chez le nourrisson, en l'absence de données cliniques en dessous de l'âge de 3 mois, il est préférable d'éviter l'utilisation des dermocorticoïdes d'activité forte.
En raison du risque d'insuffisance corticosurrénalienne, chez le nourrisson et l’enfant de moins de 12 ans, le traitement doit être soumis à une stricte surveillance médicale, avec un traitement limité à quelques jours seulement et une réévaluation chaque semaine.
Contactez votre médecin en cas de vision floue ou d’autres troubles visuels.
Autres médicaments et FLIXOVATE 0,005 %, pommade
Informez votre médecin ou pharmacien si vous utilisez, avez récemment utilisé ou pourriez utiliser tout autre médicament.
Lors de l'utilisation concomitante de corticostéroïdes locaux et d'antidiabétiques, une diminution de la tolérance au glucose a été observée. Vous devez par conséquent renforcer votre autosurveillance glycémique et urinaire, surtout en début de traitement.
FLIXOVATE 0,005 %, pommade avec des aliments et boissons
Sans objet.
Grossesse, allaitement et fertilité
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant d'utiliser ce médicament.
Grossesse
Si nécessaire, ce médicament peut être utilisé pendant la grossesse.
Allaitement
L’administration de propionate de fluticasone pendant l’allaitement est possible.
Il faut éviter que le nourrisson soit en contact prolongé avec la zone de peau traitée de la mère.
En cas d'application de FLIXOVATE sur les seins, la peau devra être nettoyée avant chaque tétée afin d’éviter tout risque d’ingestion par le nourrisson.
Ne pas appliquer sur les seins lors de l'allaitement, en raison du risque d'ingestion du produit par le nouveau-né.
Conduite de véhicules et utilisation de machines
Sans objet.
FLIXOVATE 0,005 %, pommade contient du propylène glycol
Ce médicament contient 50 mg de propylène glycol dans chaque gramme de pommade. Le propylène glycol peut causer une irritation cutanée.

Veillez à toujours utiliser ce médicament en suivant exactement les indications de votre médecin ou pharmacien. Vérifiez auprès de votre médecin ou de votre pharmacien en cas de doute.
Posologie
Adulte et enfant à partir de l’âge de 1 an : 1 à 2 applications par jour.
Nourrisson à partir de l’âge de 3 mois uniquement dans la dermatite atopique : 1 application par jour.
Ne pas augmenter le nombre d'applications par jour.
En fonction des résultats obtenus, votre médecin pourra substituer FLIXOVATE 0,005 %, pommade par un dermocorticoïde d’activité plus forte ou moins forte sur tout ou partie des lésions.
Mode d’administration
Voie cutanée.
Afin d'utiliser à chaque application la bonne quantité de médicament pour vous-même ou votre enfant, il est conseillé d'utiliser la méthode suivante : l'unité phalangette.
Presser doucement le tube de façon à déposer, sur toute la longueur de la dernière phalange de votre index, un trait continu de produit.
Par définition, cette quantité de produit déposée sur la dernière phalange de votre index (= 1 unité phalangette) permet de traiter une surface de peau correspondant à la surface de vos deux mains.
1 unité phalangette correspond à : la surface des deux mains jointes.

Ainsi, pour mesurer la surface à traiter, vous comptez combien de mains (posées à plat avec les doigts joints) sont nécessaires pour couvrir les lésions : si cela correspond par exemple à 4 mains, alors vous devez utiliser 2 unités phalangettes ; ou si cela correspond à 1 main, vous devez utiliser 0,5 unité phalangette (c. à. d. une demi-longueur de la dernière phalange de votre index).
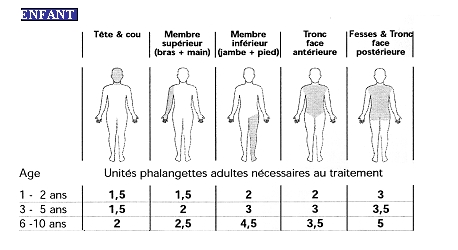
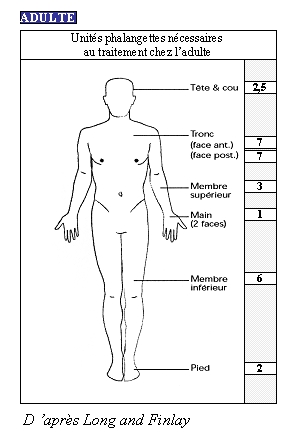
En pratique, voici le nombre d'unités phalangettes nécessaires suivant la localisation de la zone à traiter au cas où chaque zone serait à traiter en totalité.
Appliquer en fine couche sur la surface à traiter seulement et faire pénétrer par léger massage, jusqu'à ce que la pommade soit entièrement absorbée.
Lavez-vous les mains après chaque utilisation, sauf si vous devez également traiter les mains.
Si vous utilisez simultanément un produit émollient (hydratant), laissez pénétrer FLIXOVATE avant d’appliquer l’émollient.
Durée du traitement
En cas d’aggravation ou d’absence d’amélioration au bout de 2 à 4 semaines, le traitement et le diagnostic doivent être réévalués par votre médecin.
L'arrêt du traitement se fera de façon progressive en espaçant les applications et/ou en utilisant un corticoïde local moins fort ou moins dosé.
Si vous avez utilisé plus de FLIXOVATE 0,005 %, pommade que vous n’auriez dû :
Consultez immédiatement votre médecin ou votre pharmacien.
Si vous avez appliqué ou accidentellement avalé une grande quantité de FLIXOVATE 0,005 %, pommade, des effets généraux tels que des symptômes d’hypercorticisme (prise de poids, gonflement, hypertension...) peuvent apparaître.
Si vous oubliez d’utiliser FLIXOVATE 0,005 %, pommade :
Si vous avez oublié d’utiliser FLIXOVATE 0,005 %, pommade, appliquez-le dès que possible et poursuivez le traitement normalement.
N’appliquez pas davantage de FLIXOVATE 0,005 %, pommade pour compenser les applications oubliées.
Si vous arrêtez d’utiliser FLIXOVATE 0,005 %, pommade :
Si vous utilisez FLIXOVATE 0,005 %, pommade régulièrement, vous devez demander l’avis de votre médecin avant d’arrêter le traitement.

Comme tous les médicaments, ce médicament peut provoquer des effets indésirables, mais ils ne surviennent pas systématiquement chez tout le monde.
Les effets indésirables peuvent survenir avec les fréquences suivantes :
Fréquent : pouvant affecter jusqu’à 1 personne sur 10
· Démangeaisons
Peu fréquent : pouvant affecter jusqu’à 1 personne sur 100
· Brûlure cutanée locale
Très rare : pouvant affecter jusqu’à 1 personne sur 10 000
· Infections cutanées, particulièrement sous pansement occlusif ou dans les plis,
· Allergie locale,
· Fonction surrénalienne diminuée à l'arrêt brutal du traitement,
· Syndrome cushingoïde dont les symptômes incluent notamment un visage "lunaire", gonflé, une obésité, ainsi que les signes cutanés suivants : amincissement et fragilité de la peau, vergetures, dilatation de petits vaisseaux sanguins,
· Réactions cutanées allergiques au site d'application,
· Réaction cutanée inflammatoire +/- allergique, rougeur, éruption cutanée, urticaire, psoriasis pustuleux (inflammation chronique de la peau accompagnée de pustules),
· Modifications de la coloration de la peau,
· Développement de pilosité en dehors du point d'application,
· Irritation au site d’application.
Fréquence indéterminée : ne peut être estimé sur la base des données disponibles
· Vision floue
Surtout en cas d’utilisation prolongée, il y a un risque d’amincissement et de fragilité de la peau accompagnée d'une dilatation de petits vaisseaux sanguins avec des « bleus » (purpura ecchymotique).
En cas d'application sur le visage, il y a également un risque de rougeurs et d’irritations autour de la bouche.
Un retard de cicatrisation des plaies, des escarres, des ulcères de jambes est également possible.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou à votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.

Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur la boîte et le tube après {EXP}. La date de péremption fait référence au dernier jour de ce mois.
A conserver à une température inférieure à 30°C.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.

Ce que contient FLIXOVATE 0,005 %, pommade 
· La substance active est :
Propionate de fluticasone............................................................................................... 0,005 g
Pour 100 g de pommade
· Les autres composants sont :
Propylène glycol*, sesquioléate de sorbitane, cire microcristalline, paraffine liquide.
* Voir rubrique 2
Qu’est-ce que FLIXOVATE 0,005 %, pommade et contenu de l’emballage extérieur 
Ce médicament se présente sous forme de pommade. Tube de 30 g.
Titulaire de l’autorisation de mise sur le marché 
LABORATOIRE GLAXOSMITHKLINE
23 RUE FRANCOIS JACOB
92500 RUEIL-MALMAISON
Exploitant de l’autorisation de mise sur le marché 
LABORATOIRE GLAXOSMITHKLINE
23 RUE FRANCOIS JACOB
92500 RUEIL-MALMAISON
Delpharm Poznań Spółka Akcyjna
ul. Grunwaldzka 189
60-322 Poznan
Pologne
Ou
Glaxosmithkline Trading Services Limited
12 Riverwalk,
Citywest Business Campus
Dublin 24
Irlande
Noms du médicament dans les Etats membres de l'Espace Economique Européen 
Sans objet.
La dernière date à laquelle cette notice a été révisée est : 
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
|
| Plan du site | Accessibilité | Contact | Téléchargement | Declaration de confidentialité | Service-Public.fr | Legifrance | Gouvernement.fr |