Dernière mise à jour le 28/04/2026
SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule
Indications thérapeutiques
Classe pharmacothérapeutique : AGONISTE SELECTIF DES BETA-2 RECEPTEURS PAR VOIE SYSTEMIQUE BRONCHODILATATEUR - ANTIASTHMATIQUE - code ATC : R03CC02
(R : système respiratoire)
UTERORELAXANT.
(G : système génito-urinaire)
Ce médicament est un bêta-2 mimétique.
Il exerce un effet bronchodilatateur rapide (il augmente le calibre des bronches).
Il agit également au niveau de l'utérus et favorise sa relaxation lors de la grossesse.
Il peut être indiqué chez les sujets asthmatiques ou chez la femme enceinte.
SI CE MEDICAMENT VOUS A ETE PRESCRIT EN TRAITEMENT DE L'ASTHME
Il est indiqué par voie intraveineuse en perfusion chez l'adulte et l'enfant en traitement de l'asthme aigu grave.
SI CE MEDICAMENT VOUS A ETE PRESCRIT POUR VOTRE GROSSESSE
SALBUMOL FORT est utilisé chez les femmes enceintes dont le début du travail s’est déclenché de manière imprévue entre 22 et 37 semaines d’aménorrhée (travail prématuré), afin de retarder d’un court délai la délivrance du bébé. La durée de traitement par SALBUMOL FORT ne doit pas dépasser 48 heures. Ce délai permettra à votre médecin ou votre sage-femme de prendre les mesures nécessaires pour améliorer l’état de santé de votre bébé.
Ce médicament est aussi utilisé en urgence dans certaines situations particulières nécessitant de diminuer les contractions de l’utérus.
Présentations
> 5 ampoule(s) en verre de 5 ml
Code CIP : 380 923-9 ou 34009 380 923 9 4
Déclaration de commercialisation : 01/02/2011
Cette présentation est agréée aux collectivités
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 03/11/2010 | Inscription (CT) | Le service médical rendu par cette spécialité est important. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 03/11/2010 | Inscription (CT) | Cette spécialité est un complément de gamme qui n'apporte pas d'amélioration du service médical rendu (ASMR V). |
ANSM - Mis à jour le : 15/03/2024
SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Quantité correspondante en salbutamol base .............................................................................. 5,0 mg
Pour une ampoule de 5 ml.
Pour la liste complète des excipients, voir rubrique 6.1.
Solution pour perfusion intraveineuse en ampoule.
4.1. Indications thérapeutiques
Une absence d’amélioration sous salbutamol peut nécessiter une assistance médicale en urgence.
· Voie intraveineuse en perfusion continue : traitement de l'asthme aigu grave (état de mal asthmatique)
Remarque : l'asthme aigu grave nécessite une hospitalisation en unité de soins intensifs.
Une oxygénothérapie et une corticothérapie par voie systémique doivent être associées au traitement bronchodilatateur.
Utilisation en obstétrique
Traitement à court terme du travail prématuré sans complication
Pour arrêter un travail prématuré entre 22 et 37 semaines d’aménorrhée chez les patientes sans contre‑indication médicale ou obstétricale à un traitement tocolytique.
Utilisation en urgence dans des situations obstétricales particulières
4.2. Posologie et mode d'administration
Posologie
Adulte :
La dose se situe entre 0,25 et 1,5 mg/heure soit ½ à 3 ampoules en 10 heures. La dose sera adaptée toutes les 10 minutes en fonction de l'évolution clinique du patient et de la tolérance du produit.
Population pédiatrique
Enfant et nourrisson : une dose de charge de 5 microgrammes/kg sera administrée sur une durée de 5 minutes, suivie d'une dose d'entretien de 0,1 à 0,3 microgrammes/kg/min.
Mode d’administration
· Voie intraveineuse en perfusion continue à la seringue électrique et en unité de soins intensifs sous surveillance électrocardiographique.
Attention : cette spécialité n'est pas adaptée à l'administration par voie inhalée par nébuliseur.
UTILISATION EN OBSTETRIQUE
Traitement à court terme du travail prématuré sans complication et traitement d’urgence
Le traitement par SALBUMOL FORT 5 mg/5 ml doit être initié seulement par des obstétriciens/médecins expérimentés dans l’utilisation des agents tocolytiques. Il doit être mené dans des établissements pourvus d’équipements adéquats afin d’effectuer une surveillance continue de l'état de santé de la mère et du fœtus.
Il se fait chez la femme hospitalisée, au repos, placée en décubitus latéral gauche.
La durée de traitement ne doit pas excéder 48 heures car les données montrent que le principal effet du traitement tocolytique est de retarder l’accouchement jusqu’à 48 heures ; aucun effet statistiquement significatif sur la mortalité ou la morbidité périnatale n’a été observé dans les essais randomisés contrôlés.
Ce délai de courte durée peut être utilisé pour mettre en œuvre d’autres mesures connues pour améliorer la santé périnatale.
SALBUMOL FORT 5 mg/5 ml doit être administré le plus tôt possible après le diagnostic d’un travail prématuré, et après un examen de la patiente pour éliminer les contre‑indications à l’usage du sulfate de salbutamol (voir rubrique 4.3). Cela doit inclure une évaluation adéquate de l’état cardiovasculaire de la patiente avec une surveillance de la fonction cardiorespiratoire et un contrôle continu par ECG durant le traitement (voir rubrique 4.4).
L'arrêt du traitement doit être envisagé en cas d'apparition de signes d'œdème pulmonaire ou d'ischémie myocardique (voir rubriques 4.4 et 4.8).
Mises en garde spéciales pour la perfusion : la dose permettant la suppression des contractions doit être ajustée individuellement en fonction de l’augmentation de la fréquence cardiaque et des modifications de la pression artérielle, qui sont des facteurs limitants. Ces paramètres doivent être étroitement surveillés pendant le traitement. Une fréquence cardiaque maternelle maximum de 120 battements /min ne doit pas être dépassée.
Un contrôle attentif du niveau d’hydratation est essentiel pour éviter le risque d’œdème pulmonaire chez la mère (voir rubrique 4.4). Le volume de liquide dans lequel le médicament est administré doit donc être maintenu à un minimum. Un dispositif de perfusion contrôlé doit être utilisé, de préférence un pousse seringue électrique.
Dans le cas où l'administration serait réalisée au moyen d'une perfusion, la vitesse de perfusion ne devrait pas dépasser 1,5 l de volume total perfusé par 24 heures. Préparer alors une solution titrant 20μg/ml en diluant, par exemple, 2 ampoules de SALBUMOL FORT 5 mg/5 ml, soit 10 mg de salbutamol, dans 500 ml de solution isotonique salée ou glucosée.
Quel que soit le mode d'administration employé, le débit initial sera de 15 à 20 μg/min (soit 15 à 20 gouttes/min dans le cas d'une perfusion titrant 20 μg/ml).
S'il y a lieu, ce débit peut être augmenté progressivement, par paliers de 5 à 10 μg/min toutes les 10 minutes.
En règle générale, le débit d'entretien efficace est inférieur au débit initial, et compris en moyenne entre 10 et 20 μg/min.
Maintenir encore le débit pendant l'heure qui suit l'arrêt des contractions puis le diminuer à la dose minimale efficace pour maintenir ce résultat jusqu'au lendemain.
· Hypersensibilité à l’un des constituants.
UTILISATION EN OBSTETRIQUE
SALBUMOL FORT 5 mg/5 ml est contre-indiqué dans les situations suivantes :
· hypersensibilité au salbutamol ou à l’un des constituants
· toute situation avec un âge gestationnel < 22 semaines
· comme agent tocolytique chez les patientes présentant une pathologie cardiaque ischémique pré‑existante ou ayant des facteurs de risque significatifs de pathologies cardiaques ischémiques.
· menace d’avortement spontané au cours du 1er et du 2ème trimestre.
· toute situation de la mère ou du fœtus dans laquelle la prolongation de la grossesse est dangereuse, par exemple, toxémie grave, infection intra‑utérine, saignements vaginaux résultant d’un placenta praevia, éclampsie ou pré‑éclampsie grave, décollement placentaire ou compression du cordon.
· mort fœtale in‑utéro, malformation congénitale ou chromosomique létales connues.
SALBUMOL FORT 5 mg/5 ml est également contre‑indiqué dans les situations médicales déjà préexistantes avec lesquelles un bêta-2 mimétique aurait un effet inapproprié, par exemple, l’hypertension artérielle pulmonaire et des troubles cardiaques telles que la cardiomyopathie hypertrophique obstructive ou tout type d’obstruction de la voie d’éjection du ventricule gauche, par exemple une sténose aortique.
4.4. Mises en garde spéciales et précautions d'emploi
Mises en garde
L'utilisation des bêta-2 mimétiques par voie générale peut parfois démasquer une pathologie cardiaque préexistante méconnue. Dans la mesure du possible l'administration par voie inhalée doit être privilégiée car elle représente le meilleur rapport efficacité/tolérance.
Les médicaments ayant une activité sympathomimétique, dont fait partie le salbutamol, peuvent entraîner des effets cardiovasculaires. Des cas d'ischémies myocardiques associées au salbutamol ont été rapportés lors de notifications spontanées depuis la commercialisation ainsi que dans la littérature. Les patients présentant une cardiopathie sévère sous-jacente (par exemple, cardiopathie ischémique, troubles du rythme ou insuffisance cardiaque sévère) devront être informés de la nécessité de consulter leur médecin en cas de douleur thoracique ou autres symptômes évocateurs d’une aggravation de leur cardiopathie. L'origine cardiaque de symptômes respiratoires telle qu'une dyspnée doit également être évoquée.
Une anesthésie à l'halotane est déconseillée durant le traitement (voir rubrique 4.5).
Précautions d'emploi
Le salbutamol doit être utilisé avec précaution chez les patients ayant reçu des doses importantes d’autres médicaments sympathomimétiques.
L'administration par voie injectable de salbutamol doit être envisagée avec prudence en cas d'hyperthyroïdie, d'affection cardio-vasculaire notamment troubles coronariens, cardiomyopathie obstructive, trouble du rythme cardiaque, hypertension artérielle et de diabète.
Les bêta-2 mimétiques à forte dose (en particulier par voie parentérale ou par nébulisation), peuvent être à l’origine d’une hypokaliémie potentiellement grave, pouvant favoriser la survenue de troubles du rythme cardiaque. Une surveillance de la kaliémie est recommandée dans la mesure du possible, en particulier lors de l’administration simultanée de thérapeutiques hypokaliémiantes, en cas d’hypoxie ou chez les sujets chez qui le risque de survenue de torsades de pointes est majoré (QT long ou traitements susceptibles d’augmenter le QTc).
Comme d'autres agonistes des récepteurs béta adrénergiques, le salbutamol peut induire une augmentation de la glycémie. Des cas d’acidocétose ont été rapportés chez les patients diabétiques. L’administration concomitante de corticoïdes peut majorer ces effets.
Des cas d'acidose lactique ont été très rarement rapportés en association à de fortes doses de bêta-2 agonistes de courte durée d’action par voie intraveineuse ou par voie inhalée par nébulisation, principalement chez des patients traités pour une exacerbation aiguë de leur asthme (voir 4.8 Effets indésirables). Une augmentation du taux d’acide lactique peut entraîner une dyspnée et une hyperventilation compensatoire, qui peut être interprétée à tort comme un signe d’échec au traitement de l’asthme conduisant à l'augmentation inapproprié du traitement par bêta-agoniste de courte durée d’action. Par conséquent, le risque d'acidose lactique doit faire l'objet d'une surveillance attentive en particulier dans les situations sévères.
L’utilisation de préparations parentérales de salbutamol dans le traitement du bronchospasme sévère ou de l’asthme aigü grave (aussi appelé état de mal asthmatique) ne dispense pas de la nécessité d’un traitement par glucostéroïdes quand cela est approprié.
UTILISATION EN OBSTETRIQUE
Mises en garde spéciales
Tocolyse
Toute décision d’initier le traitement par SALBUMOL FORT 5 mg/5 ml doit être prise après un examen attentif des risques et des bénéfices du traitement.
Le traitement doit seulement être effectué dans des établissements adéquats équipés pour assurer une surveillance continue de l’état de santé maternel et fœtal. La tocolyse avec des béta-2 mimétiques n’est pas recommandée quand les membranes sont rompues ou si la dilatation du col est de plus de 4 cm.
SALBUMOL FORT 5 mg/5 ml doit être utilisé avec précaution dans la tocolyse et la surveillance de la fonction cardio‑respiratoire et le contrôle de l’ECG doivent être effectués tout au long du traitement.
Les mesures de surveillance suivantes doivent être constamment conduites chez la mère et, quand cela est possible/approprié, chez le fœtus :
· pression artérielle et rythme cardiaque
· ECG
· bilan électrolytique et hydrique pour surveiller les œdèmes pulmonaires
· taux de glucose et de lactate avec une attention particulière chez les patientes diabétiques
· taux de potassium – les béta-2 mimétiques sont associés à une diminution du potassium sérique ce qui augmente le risque d’arythmie (voir rubrique 4.5.)
Le traitement doit être interrompu si des signes d’ischémie myocardique (comme une douleur dans la poitrine ou des modifications de l’ECG) apparaissent.
SALBUMOL FORT 5 mg/5 ml ne doit pas être utilisé comme un agent tocolytique chez les patientes avec des facteurs de risque importants, ou une suspicion de toute pathologie cardiaque pré‑existante (c'est‑à‑dire tachycardie, insuffisance cardiaque, ou maladie cardiaque valvulaire ; voir rubrique 4.3.). Lors d’un travail prématuré chez une patiente ayant une maladie cardiaque connue ou suspectée, un médecin spécialisé en cardiologie doit évaluer la pertinence du traitement avant la perfusion intraveineuse avec SALBUMOL FORT 5 mg/5 ml.
Œdème pulmonaire
Des cas d’œdème pulmonaire maternel et d’ischémie myocardique ont été rapportés pendant ou à la suite du traitement d’une menace d’accouchement prématuré par des béta-2 mimétiques ; une attention particulière doit donc être accordée à l’équilibre hydrique et à la fonction cardio‑respiratoire. Les patientes ayant des facteurs de risque incluant grossesses multiples, surcharge liquidienne, infection maternelle et pré‑éclampsie, peuvent avoir une augmentation du risque de développement d’un œdème pulmonaire. L’administration avec un pousse seringue électrique contrairement à la perfusion IV limitera le risque de surcharge hydrique. Si des signes d’œdème pulmonaire ou d’ischémie myocardique apparaissent, l’arrêt du traitement doit être envisagé (voir rubrique 4.2 et 4.8).
Pression artérielle et rythme cardiaque
Des augmentations de la fréquence cardiaque maternelle de l'ordre de 20 à 50 battements par minute accompagnent habituellement la perfusion de bêta‑2 mimétiques. Le pouls maternel doit être surveillé et la nécessité de maîtriser ces augmentations par la réduction de la dose ou l'arrêt du traitement doit être évaluée au cas par cas. En général, le pouls de la mère ne doit pas dépasser un taux constant de 120 battements par minute. L'effet de la perfusion sur le rythme cardiaque du fœtus est moins marqué, mais des augmentations allant jusqu'à 20 battements par minute peuvent se produire.
La pression artérielle maternelle peut diminuer légèrement au cours de la perfusion, l'effet étant plus marqué sur la pression diastolique que sur la pression systolique. Les chutes de la pression diastolique sont habituellement de l'ordre de 10 à 20 mmHg.
Afin de minimiser le risque d'hypotension associée à un traitement tocolytique, une précaution particulière doit être prise pour éviter la compression cave en gardant la patiente dans les positions latérales gauche ou droite tout au long de la perfusion.
Diabète
L'administration des bêta-2 mimétiques est associée à une augmentation de la glycémie. Par conséquent, la glycémie et le taux de lactate doivent être surveillés chez les mères atteintes de diabète et le traitement du diabète doit être ajusté en conséquence pour répondre aux besoins de la mère diabétique au cours de la tocolyse (voir rubrique 4.5).
Chez les diabétiques, il est préférable, le cas échéant, d'effectuer les dilutions dans du sérum physiologique.
Hyperthyroïdie
SALBUMOL FORT 5 mg/5 ml doit seulement être administré avec prudence aux patientes souffrant de thyréotoxicose après une évaluation attentive des bénéfices et des risques du traitement.
Anesthésiques halogénés
Une anesthésie par anesthésiques halogénés est déconseillée en association avec ce traitement (voir rubrique 4.5).
Précautions d'emploi
Hypokaliémie :
Les bêta-2 mimétiques, principalement par voie parentérale, peuvent être à l'origine d'une hypokaliémie. Une surveillance de la kaliémie est nécessaire, en particulier lors de l'administration simultanée de thérapeutiques hypokaliémiantes.
Anesthésie générale ou péridurale :
Tenir compte de l'effet vasodilatateur périphérique des bêta-2 mimétiques et de l'inertie utérine.
Surveillance néonatale :
L'accélération du rythme cardiaque foetal est fréquente et parallèle à la tachycardie maternelle mais il est exceptionnel de la voir persister à la naissance. De même, les valeurs de la glycémie post-natale ne sont qu'exceptionnellement perturbées.
SPORTIFS :
L'attention des sportifs est attirée sur le fait que cette spécialité contient un principe actif pouvant induire une réaction positive des tests pratiqués lors de contrôles antidopage.
SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule contient du sodium
Ce médicament contient moins de 1 mmol (23 mg) de sodium par ampoule de 5 ml, c’est à dire qu’il est essentiellement « sans sodium ».
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
+ Béta-bloquants non sélectifs
Le salbutamol et les bêta-bloquants non sélectifs, tel que le propranolol, ne doivent généralement pas être prescrits de façon concomitante.
+ Anesthésiques halogénés (Halothane)
Lors d'une utilisation chez la femme enceinte, du fait de l'effet antihypertenseur supplémentaire, il existe une augmentation de l'inertie utérine avec un risque d'hémorragie ; de plus, de graves troubles du rythme ventriculaire dus à une augmentation de la réactivité cardiaque, ont été signalés lors d’interaction avec les anesthésiques halogénés. Le traitement doit être interrompu dans la mesure du possible au moins 6 heures avant toute anesthésie programmée avec des anesthésiques halogénés.
Associations faisant l'objet de précautions d’emploi
+ Corticostéroïdes
Les corticostéroïdes systémiques sont fréquemment donnés lors du travail prématuré pour améliorer le développement des poumons du fœtus. Des cas d'œdème pulmonaire chez les femmes auxquelles il a été administré concomitamment des bêta-2 mimétiques et des corticostéroïdes ont été rapportés.
Les corticostéroïdes sont connus pour augmenter la glycémie et peuvent épuiser le potassium sérique, par conséquent une administration concomitante doit être faite avec prudence avec une surveillance continue de la patiente en raison du risque accru d'hyperglycémie et d’une hypokaliémie (voir rubrique 4.4).
Cette surveillance est également requise lors de l'utilisation dans l'indication en pneumologie (cf rubrique 4.4.),
+ Antidiabétiques
L'administration de bêta-2 mimétiques est associée à une augmentation de la glycémie, ce qui peut être interprété comme une diminution de l'effet du traitement antidiabétique, par conséquent, il peut être nécessaire de réajuster le traitement antidiabétique (voir rubrique 4.4).
+ Agents entrainant une déplétion potassique
En raison de l'effet hypokaliémiant des bêta-2 mimétiques, l'administration concomitante d’agents entraînant une déplétion potassique connus pour aggraver le risque d'hypokaliémie, comme les diurétiques, la digoxine, les méthyl‑xanthines et les corticostéroïdes doit être effectuée avec prudence après une évaluation minutieuse des bénéfices et des risques avec une attention particulière pour l'augmentation du risque d'arythmies cardiaques résultant d'une hypokaliémie (voir rubrique 4.4).
4.6. Fertilité, grossesse et allaitement
Grossesse
En clinique, il existe un recul important, avec un nombre suffisant de grossesses documentées, pour que l’on puisse conclure à l’innocuité du salbutamol pendant la grossesse.
En conséquence, le salbutamol, par voie orale peut être administré en cas de grossesse.
Lors de l’administration pendant la grossesse :
L’accélération du rythme cardiaque fœtal est fréquente et parallèle à la tachycardie maternelle. Il est exceptionnel de la voir persister à la naissance.
De même, les valeurs de la glycémie post-natale ne sont qu’exceptionnellement perturbées.
En cas d’administration avant accouchement tenir compte de l’effet vasodilatateur périphérique des bêta-2 mimétiques et de l’inertie utérine.
Les bêta-2 mimétiques passent dans le lait maternel.
Fertilité
Il n'existe aucune information sur les effets du salbutamol sur la fertilité humaine. Il n'a pas été mis en évidence d'effet indésirable sur la fertilité chez l’animal (voir rubrique 5.3).
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
UTILISATION EN PNEUMOLOGIE
Les effets indésirables sont cités ci-dessous, listés par classe organe et par fréquence.
Les fréquences sont définies en très fréquent (≥1/10), fréquent (³1/100 à <1/10), peu fréquent (³1/1000 à <1/100), rare (≥1/10000 à <1/1000) et très rare (<1/10000) y compris les cas isolés.
Les effets très fréquents et fréquents ont généralement été décrits dans les essais cliniques. Les effets indésirables rares et très rares sont généralement issus des notifications spontanées depuis la commercialisation.
Classe organe |
Effets indésirables |
Fréquence |
|
Affections du système immunitaire |
Réactions d’hypersensibilité incluant : œdème angioneurotique, urticaire, bronchospasme, hypotension et collapsus. |
Très rare |
|
Troubles du métabolisme et de la nutrition |
Hypokaliémie. * |
Rare |
|
Acidose lactique** |
Très rare |
|
|
Affections du système nerveux |
Tremblements. |
Très fréquent |
|
Céphalées. |
Fréquent |
|
|
Affections psychiatriques |
Modification du comportement incluant agitation, nervosité. |
Très rare |
|
Affections cardiaques |
Tachycardie, palpitations. |
Très fréquent |
|
Arythmies cardiaques incluant fibrillation auriculaire, tachycardie supraventriculaire et extrasystoles. |
Rare
|
|
|
Ischémies myocardiques*** (voir rubrique 4.4) |
Indéterminée |
|
|
Affections vasculaires |
Vasodilatation périphérique. |
Rare |
|
Affections musculo-squelettiques et systémiques |
Crampes musculaires. |
Fréquent |
* Les bêta-2 mimétiques à fortes doses peuvent entraîner des hyperglycémies réversibles à l’arrêt du traitement et des hypokaliémies.
** Des cas d'acidose lactique ont été très rarement rapportés chez des patients recevant du salbutamol par voie intraveineuse ou par voie inhalée par nébulisation pour le traitement d’exacerbations aiguës d'asthme.
*** La fréquence de survenue des ischémies myocardiques ne peut être déterminée car les cas rapportés sont issus de notifications spontanées depuis la commercialisation.
Peuvent également être observés des troubles digestifs (nausées, vomissements).
UTILISATION EN OBSTETRIQUE
Les effets indésirables les plus fréquents de SALBUMOL FORT 5 mg/5 ml sont corrélés à l’activité pharmacologique béta-2 mimétique et peuvent être limités ou évités par une surveillance étroite des paramètres hémodynamiques, comme la pression artérielle et le rythme cardiaque, et un ajustement approprié de la dose. Ils disparaissent normalement à l’arrêt du traitement.
Les effets secondaires sont cités ci-dessous, listés par classe organe et par fréquence. Les fréquences sont définies en très fréquent (≥1/10), fréquent (≥1/100 et <1/10), peu fréquent (≥1/1000 et <1/100), rare (≥1/10000 et <1/1000) et très rare (<1/10000) y compris les cas isolés. Les effets très fréquents et fréquents ont généralement été décrits dans les essais cliniques.
Les effets indésirables rares et très rares sont généralement issus des notifications spontanées après commercialisation.
|
Classe organe |
Effets indésirables |
Fréquence |
|
Affections du système immunitaire |
Réactions d'hypersensibilité incluant : œdème angioneurotique, urticaire, bronchospasme, hypotension et collapsus |
Très rare
|
|
Troubles du métabolisme et de la nutrition |
Hypokaliémie * |
Fréquent |
|
Hyperglycémie |
Rare |
|
|
Affections du système nerveux |
Tremblements |
Très fréquent |
|
Céphalées |
Fréquent |
|
|
Affections psychiatriques |
Modification du comportement incluant agitation, nervosité |
Très rare |
|
Affections cardiaques |
Tachycardie |
Très fréquent |
|
Palpitations |
Fréquent |
|
|
Diminution de la pression artérielle diastolique |
Fréquent |
|
|
Arythmies cardiaques incluant fibrillation auriculaire, tachycardie supra ventriculaire et extrasystoles, ischémie myocardique (voir rubrique 4.4) |
Rare
|
|
|
Affections vasculaires |
Hypotension (voir rubrique 4.4) |
Fréquent |
|
Vasodilatation périphérique |
Rare |
|
|
Affections respiratoires, thoraciques et médiastinales |
Œdème pulmonaire*** |
Peu fréquent
|
|
Affections gastro-intestinales |
Nausées, vomissements |
Très rare |
|
Affections musculo-squelettiques et systémiques |
Crampes musculaires |
Fréquent |
|
Lésions, intoxications et complications liées aux procédures |
Légère douleur ou sensation de brûlure au point d’injection (injection non diluée par voie I.M.) |
Très rare |
*Le traitement par bêta-2 mimétique peut entraîner des hypokaliémies sévères, ainsi que des augmentations de la glycémie régressant à l'arrêt du traitement.
***Les patientes ayant des prédispositions incluant grossesses multiples, surcharge liquidienne, infection maternelle et pré-éclampsie peuvent présenter un risque accru de développer un œdème pulmonaire.
Ces réactions ont été rapportées en association avec l’utilisation d’un béta-2 mimétique de courte durée d’action dans les indications obstétricales et sont considérées comme des effets de classe (voir rubrique 4.4)
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr
UTILISATION EN PNEUMOLOGIE ET EN OBSTETRIQUE
Les signes et symptômes d’un surdosage en salbutamol correspondent à l'exacerbation des effets pharmacodynamiques des bêta2-agonistes (voir rubriques 4.4 et 4.8).
Une hypokaliémie peut survenir suite à un surdosage en salbutamol. La kaliémie doit donc être surveillée en cas de surdosage.
Des nausées, vomissements et hyperglycémie ont été rapportées, en particulier chez les enfants et lorsque le surdosage est dû à une prise de salbutamol par voie orale.
Des cas d’acidose lactique ont été rapportés avec des doses élevées de béta-2 agonistes d’action rapide. En cas de surdosage, il convient donc de surveiller les taux sériques de lactate et le risque d’acidose lactique, en particulier en cas de persistance ou aggravation de la tachypnée malgré la disparition des symptômes de bronchospasme tels que les sibilants, qui peut être lié à l'acidose métabolique.
Conduite à tenir : surveillance et traitement symptomatique.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
UTERORELAXANT (G : système génito-urinaire).
Le salbutamol est un agoniste des récepteurs bêta adrénergiques présentant une action beaucoup plus sélective sur les récepteurs bêta-2 (en particulier bronchiques, utérins et vasculaires)
5.2. Propriétés pharmacocinétiques
L'élimination, essentiellement urinaire, se fait en partie sous forme active, en partie sous forme de métabolites inactifs.
Le salbutamol passe la barrière placentaire et diffuse dans le lait.
5.3. Données de sécurité préclinique
Chlorure de sodium, acide sulfurique, eau pour préparations injectables.
Gaz d'inertage : azote.
Ne pas mélanger à d'autres spécialités dans la même seringue ou la même perfusion.
4 ansAprès ouverture : le produit doit être utilisé immédiatement.
6.4. Précautions particulières de conservation
A conserver à une température inférieure ou égale à 25°C et à l'abri de la lumière.
Après dilution, une utilisation immédiate est recommandée.
6.5. Nature et contenu de l'emballage extérieur
Ampoule de 5 ml en verre neutre incolore (type I).
Boîte de 1, 5, 6, 10 ou 12.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Le salbutamol peut être dilué dans du sérum physiologique (NaCl 9 ), une solution glucosée isotonique ou une solution mixte de chlorure de sodium et de glucose isotoniques.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
23, RUE FRANCOIS JACOB
92500 RUEIL-MALMAISON
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 320 697 2 4 : 5 ml en ampoule (verre). Boîte de 1.
· 34009 380 923 9 4 : 5 ml en ampoule (verre). Boîte de 5.
· 34009 315 235 4 4 : 5 ml en ampoule (verre). Boîte de 6.
· 34009 330 202 6 4 : 5 ml en ampoule (verre). Boîte de 10.
· 34009 553 150 6 4 : 5 ml en ampoule (verre). Boîte de 10.
· 34009 315 237 7 4 : 5 ml en ampoule (verre). Boîte de 12.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
Date de première autorisation : 31 octobre 1996
Date de dernier renouvellement : 27 février 2011
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I
ANSM - Mis à jour le : 15/03/2024
SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule
Salbutamol
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, qu'il soit mentionné ou non dans cette notice, parlez-en à votre médecin ou votre pharmacien. Voir rubrique 4.
1. Qu'est-ce que SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule ?
3. Comment utiliser SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : AGONISTE SELECTIF DES BETA-2 RECEPTEURS PAR VOIE SYSTEMIQUE BRONCHODILATATEUR - ANTIASTHMATIQUE - code ATC : R03CC02
(R : système respiratoire)
UTERORELAXANT.
(G : système génito-urinaire)
Ce médicament est un bêta-2 mimétique.
Il exerce un effet bronchodilatateur rapide (il augmente le calibre des bronches).
Il agit également au niveau de l'utérus et favorise sa relaxation lors de la grossesse.
Il peut être indiqué chez les sujets asthmatiques ou chez la femme enceinte.
SI CE MEDICAMENT VOUS A ETE PRESCRIT EN TRAITEMENT DE L'ASTHME
Il est indiqué par voie intraveineuse en perfusion chez l'adulte et l'enfant en traitement de l'asthme aigu grave.
SI CE MEDICAMENT VOUS A ETE PRESCRIT POUR VOTRE GROSSESSE
SALBUMOL FORT est utilisé chez les femmes enceintes dont le début du travail s’est déclenché de manière imprévue entre 22 et 37 semaines d’aménorrhée (travail prématuré), afin de retarder d’un court délai la délivrance du bébé. La durée de traitement par SALBUMOL FORT ne doit pas dépasser 48 heures. Ce délai permettra à votre médecin ou votre sage-femme de prendre les mesures nécessaires pour améliorer l’état de santé de votre bébé.
Ce médicament est aussi utilisé en urgence dans certaines situations particulières nécessitant de diminuer les contractions de l’utérus.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule ?
SI CE MEDICAMENT VOUS A ETE PRESCRIT EN TRAITEMENT DE L'ASTHME
N’utilisez jamais SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule :
· si vous êtes allergique à la substance active ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
EN CAS DE DOUTE, IL EST INDISPENSABLE DE DEMANDER L'AVIS DE VOTRE MEDECIN.
Avertissements et précautions
Faites attention avec SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule :
Mises en garde spéciales
Une anesthésie à l'halothane est déconseillée durant le traitement.
Précautions d'emploi
· Prévenez votre médecin :
o -si vous avez des problèmes en lien avec votre glande thyroïde,
o -si vous avez des problèmes cardio-vasculaires, notamment certains troubles du rythme cardiaque, une angine de poitrine (sensation d'oppression thoracique et douleurs violentes localisées au niveau de la poitrine et pouvant s’étendre dans le bras gauche), ou une hypertension artérielle (augmentation de la pression du sang dans les artères),
o -si vous avez un diabète
afin qu'il détermine les modalités de traitement les mieux adaptées à votre cas.
EN CAS DE DOUTE NE PAS HESITER A DEMANDER L'AVIS DE VOTRE MEDECIN.
SI CE MEDICAMENT VOUS A ETE PRESCRIT POUR VOTRE GROSSESSE
N'utilisez jamais SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule :
· si vous êtes allergique à la substance active ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
· si vous êtes enceinte de moins de 22 semaines.
· si vous souffrez ou avez connaissance d’un risque de développer une maladie cardiaque ischémique (maladie caractérisée par une diminution de l’apport sanguin vers le muscle cardiaque, provoquant des symptômes tels que des douleurs thoraciques (angine de poitrine)).
· si vous avez eu une menace de fausse couche dans les deux premiers trimestres de cette grossesse
· si vous êtes enceinte et si vous ou votre bébé présentez certaines conditions où la prolongation de la grossesse serait dangereuse (comme l’hypertension artérielle sévère, une infection de l’utérus, des saignements, le placenta qui recouvre l’orifice utérin ou se décolle, ou si votre bébé est mort in-utero).
· si vous souffrez d’une maladie cardiaque avec des palpitations (par exemple dysfonctionnement de la valve cardiaque) ou d’une maladie pulmonaire de longue date (par exemple bronchite chronique, emphysème) provoquant une augmentation de la pression artérielle dans vos poumons (hypertension pulmonaire).
EN CAS DE DOUTE, IL EST INDISPENSABLE DE DEMANDER L'AVIS DE VOTRE MEDECIN OU DE VOTRE PHARMACIEN.
Avertissements et précautions
Faites attention avec SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule :
Mises en garde spéciales
La mise en route du traitement se fera en milieu hospitalier sous surveillance médicale cardiaque et respiratoire (auscultation cardiaque, tension artérielle).
Avant de recevoir votre injection, il est important de vérifier au préalable avec votre médecin ou sage-femme si :
· vous avez eu des problèmes lors de votre grossesse.
· si pendant la grossesse, la poche des eaux s’est rompue.
· vous avez œdème pulmonaire (liquide dans les poumons provoquant un essoufflement).
· vous avez une pression artérielle élevée (hypertension).
· vous êtes diabétique. Dans ce cas, vous devez faire des analyses sanguines complémentaires quand vous avez reçu SALBUMOL FORT.
· vous avez une hyperthyroïdie (glande thyroïde hyperactive).
· vous avez un antécédent de problèmes cardiaques tels que des essoufflements, des palpitations ou une angine de poitrine (voir la rubrique « N’utilisez jamais SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule»).
Votre médecin surveillera votre cœur et celui de votre bébé. Votre médecin peut également demander des tests sanguins pour surveiller d’éventuelles modifications du bilan sanguin (voir rubrique 3).
Précautions d'emploi
Prévenez votre médecin si vous devez subir une anesthésie générale. Une anesthésie par anesthésiques halogénés (ex: halothane) est déconseillée durant le traitement.
EN CAS DE DOUTE NE PAS HESITER A DEMANDER L'AVIS DE VOTRE MEDECIN OU DE VOTRE PHARMACIEN.
Sportifs, attention cette spécialité contient un principe actif pouvant rendre positifs les tests pratiqués lors des contrôles antidopage.
Autres médicaments et SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule
Informez votre médecin, sage-femme ou pharmacien si vous prenez ou avez pris récemment tout autre médicament, y compris des médicaments obtenus sans ordonnance ou des médicaments à base de plantes.
SALBUMOL FORT peut avoir un effet sur le mode d’action de certains médicaments, et certains médicaments peuvent avoir des effets sur le mode d’action de SALBUMOL FORT.
En particulier, informez votre médecin, sage-femme ou pharmacien si vous prenez :
· des médicaments pour des battements rapides ou irréguliers du cœur (comme la digoxine).
· Des bêta‑bloquants (comme l’aténolol ou le propranolol), incluant les gouttes oculaires (comme le timolol).
· des dérivés xanthiques (comme la théophylline ou l’aminophylline).
· des corticoïdes (comme la prednisolone).
· des diurétiques (comme le furosémide).
· des anti‑diabétiques pour réduire le taux de sucre dans votre sang (comme l’insuline, la metformine, le glibenclamide).
Si vous devez subir une intervention chirurgicale avec une anesthésie générale, votre médecin stoppera l’administration de SALBUMOL FORT, 6 heures avant la chirurgie, lorsque cela est possible, pour vous protéger des effets indésirables (par exemple, rythme cardiaque irrégulier ou saignement de votre utérus).
SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule avec des aliments et boissons
Sans objet.
D'une façon générale, demandez conseil à votre médecin ou à votre pharmacien avant de prendre tout médicament.
Ce médicament dans les conditions normales d'utilisation peut être utilisé pendant la grossesse.
En cas d'allaitement, le passage de ce médicament dans le lait maternel peut exposer l'enfant à un faible risque d'augmentation du rythme cardiaque et de survenue d'hyperglycémie (augmentation du taux de sucre dans le sang). L’allaitement n’est pas recommandé lors d’un traitement avec SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule.
Conduite de véhicules et utilisation de machines
Sans objet.
SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule contient du sodium
Ce médicament contient moins de 1 mmol (23 mg) de sodium par ampoule de 5 ml, c’est à dire qu’il est essentiellement « sans sodium ».
3. COMMENT UTILISER SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule ?
SI CE MEDICAMENT VOUS A ETE PRESCRIT EN TRAITEMENT DE L'ASTHME
Mode d'administration
Ce médicament s'administre en perfusion continue intraveineuse lente à la seringue électrique.
L'administration de salbutamol par voie intraveineuse sera réalisée en milieu hospitalier, sous surveillance de l'électrocardiogramme.
Attention, ce médicament n'est pas adapté à l'administration par voie inhalée par nébuliseur.
Posologie
Par voie intraveineuse, la posologie est variable en fonction de votre état, elle varie de 1/2 à 3 ampoules en 10 heures.
DANS TOUS LES CAS SE CONFORMER STRICTEMENT A L'ORDONNANCE DE VOTRE MEDECIN.
Durée de traitement
Ce médicament est réservé au traitement de la crise d'asthme, la durée du traitement par ce médicament est fonction de votre état.
SI CE MEDICAMENT VOUS A ETE PRESCRIT POUR VOTRE GROSSESSE
Ne prenez jamais ce médicament par vous-même. Il doit toujours vous être administré par une personne habilitée après un examen minutieux des bénéfices de SALBUMOL FORT, pour vous ou votre bébé par rapport aux effets indésirables éventuels pouvant survenir lors du traitement.
Pour retarder temporairement le travail qui s'est déclenché de manière imprévue
SALBUMOL FORT sera administré par un médecin dans un lieu dont l'équipement est adapté pour pour une surveillance continue de votre état et de celui de votre bébé durant toute l’administration.
Les mesures suivantes devront être prises si nécessaire :
· surveillance de la pression artérielle et du rythme des battements du cœur. Votre médecin envisagera une diminution de la dose ou l’arrêt de SALBUMOL FORT, si votre rythme cardiaque dépasse 120 battements par minute.
· surveillance de l'électrocardiogramme (ECG, activité électrique de votre cœur). Informez immédiatement votre médecin si vous ressentez une douleur thoracique durant le traitement. S’il y a des modifications à l’ECG et si vous avez une douleur thoracique, votre médecin arrêtera l’administration de SALBUMOL FORT.
· Trouble de l'équilibre entre l’eau et les sels minéraux dans votre corps. Informez immédiatement votre médecin si vous toussez ou si vous êtes essoufflée durant le traitement. Si des signes tels que toux ou essoufflement, qui peuvent être des signes d'œdème pulmonaire (accumulation d’eau dans les poumons) apparaissent, votre médecin peut décider d'arrêter l’administration de SALBUMOL FORT.
· surveillance du taux de sucre et de lactate dans le sang (une augmentation excessive est appelée acidose lactique).
· surveillance du taux de potassium dans le sang (un taux trop faible de potassium dans le sang peut entrainer un rythme irrégulier des battements cardiaques.
Posologie
La posologie est variable et adaptée à chaque patiente.
Mode d'administration
Ce médicament s'administre en perfusion continue intraveineuse lente à la seringue électrique.
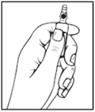
MODE D'EMPLOI POUR L'OUVERTURE DES AMPOULES
|
1. Tenir l'ampoule en orientant le point de couleur vers le haut. Si du liquide se trouve dans la partie haute de l'ampoule, tapoter pour le faire descendre dans le corps de l'ampoule. |
|
|
|
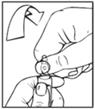
2. Puis saisir l'extrémité de l'ampoule (au-dessus du point) et exercer une pression pour casser l'embout. |
|
|
Si vous avez pris plus de SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule que vous n’auriez dû
Si vous prenez accidentellement une dose supérieure à la dose recommandée, vous pouvez présenter des effets indésirables tels que tachycardie, maux de tête, tremblements ou agitation (voir les effets indésirables éventuels).
Consultez immédiatement votre médecin et emportez avec vous cette notice ou votre médicament afin que votre médecin sache ce que vous avez pris.
Si vous oubliez de prendre SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule
Si vous arrêtez de prendre SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule
Sans objet.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
UTILISATION EN TRAITEMENT DE L'ASTHME
Peuvent être observés :
· Très fréquemment : tremblements, augmentation du rythme cardiaque, palpitations.
· Fréquemment : maux de tête, crampes musculaires.
· Rarement : diminution du taux de potassium dans le sang, bouffées de chaleur, rougeurs cutanées, irrégularités du rythme cardiaque.
· Très rarement :
o agitation ou nervosité,
o réactions allergiques pouvant se manifester par une telles que sensation d’oppression danse la poitrine, des démangeaisons, un sifflement respiratoire, un gonflement des paupières, du visage et/ou des lèvres et éruption cutanée, une baisse de la tension artérielle pouvant aller jusqu’au malaise,
o augmentation du taux d’acide lactique dans le sang (se manifestant par une respiration rapide, un essoufflement, même si vous ressentez une amélioration des sifflements respiratoires, sensation de froid, douleurs à l'estomac, nausées et vomissements).
Des augmentations de la quantité de sucre dans le sang ont également été rapportées, régressant à l'arrêt du traitement. La surveillance sanguine et urinaire doit être renforcée chez les sujets diabétiques.
Lors d'un traitement avec le salbutamol, certaines personnes peuvent parfois (fréquence de survenue non connue) ressentir une douleur dans le thorax (sensation d'oppression) qui peut être due à des problèmes cardiaques tels qu’une angine de poitrine. Prévenez rapidement votre médecin si vous ressentez de tels symptômes.
SI CE MEDICAMENT VOUS A ETE PRESCRIT POUR VOTRE GROSSESSE
Effets secondaires importants à surveiller lors d’un traitement pour un travail prématuré :
Rare (peuvent affecter moins d’une personne sur 1 000) :
Douleur thoracique (due à des problèmes cardiaques comme l’angine de poitrine). Si cela vous arrive, parlez‑en immédiatement à votre médecin ou votre sage-femme.
Les effets secondaires suivants ont été également observés avec tous les bêta-2 mimétiques comme SALBUMOL FORT quand ils sont utilisés pour retarder le travail prématuré.
Très fréquent (peuvent affecter plus d’une personne sur 10) :
· Battements cardiaques rapides, tremblements
Fréquent (peuvent affecter moins d’une personne sur 10) :
· Battements accélérés du cœur (palpitations)
· Pression sanguine basse qui peut provoquer des étourdissements ou des vertiges.
· Niveau faible de potassium dans votre sang qui peut provoquer une faiblesse musculaire, la soif ou « des fourmillements et picotements ».
· Maux de tête
· Crampes musculaires
Peu fréquent (peuvent affecter moins d’une personne sur 100) :
· Une accumulation d’eau dans les poumons (œdème pulmonaire) qui peut provoquer des difficultés pour respirer.
Rare (peuvent affecter moins d’une personne sur 1 000) :
· Battements de cœur irréguliers ou inhabituels
· Une ischémie myocardique (diminution de l'apport de sang dans le muscle cardiaque pouvant être ressentie comme une douleur thoracique).
· Un niveau élevé de sucre (glucose) effet régressant à l'arrêt du traitement- et/ou d’acide lactique dans votre sang
· Rougeurs du visage
· Bouffées de chaleur
Très rare (peuvent affecter moins d’une personne sur 10 000) :
· Agitation ou nervosité,
· Nausées, vomissements,
· Réactions allergiques à type de gonflement du visage, des lèvres, de la bouche, des paupières et de la gorge, d'urticaire, de gêne respiratoire, ou de diminution rapide de la pression artérielle.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien ou à votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur la boîte. La date de péremption fait référence au dernier jour de ce mois.
Après ouverture : le produit doit être utilisé immédiatement.
A conserver à une température inférieure ou égale à 25°C et à l'abri de la lumière.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient SALBUMOL FORT 5 mg/5 ml, solution pour perfusion intraveineuse en ampoule
· La substance active est :
Sulfate de salbutamol ............................................................................................................ 6 mg
Quantité correspondante en salbutamol base........................................................................... 5 mg
Pour une ampoule de 5 ml.
· Les autres composants sont :
Chlorure de sodium, acide sulfurique, eau pour préparations injectables.
Gaz d’inertage : azote.
Ce médicament se présente sous forme de solution pour perfusion intraveineuse. Boîte de 1, 5, 6, 10 et 12 ampoules.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
23, RUE FRANCOIS JACOB
92500 RUEIL-MALMAISON
Exploitant de l’autorisation de mise sur le marché
23, RUE FRANCOIS JACOB
92500 RUEIL-MALMAISON
GLAXOSMITHKLINE MANUFACTURING SPA
STRADA PROVINCIALE ASOLANA, 90
43056 San Polo di Torrile
PARME
Italie
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
mois AAAA
Sans objet.
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).