Dernière mise à jour le 30/03/2026
LEPTICUR 10 mg/2 ml, solution injectable
Indications thérapeutiques
Classe pharmacothérapeutique : Antiparkinsonien Anticholinergique
Code ATC : N04AA12
Ce médicament est préconisé dans les symptômes provoqués par certains médicaments (neuroleptiques).
Présentations
> 1 ampoule(s) en verre de 2 ml
Code CIP : 317 561-6 ou 34009 317 561 6 3
Déclaration de commercialisation : 19/05/1993
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 3,60 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 4,62 €
- Taux de remboursement :65%
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 20/05/2015 | Renouvellement d'inscription (CT) | Le service médical rendu par LEPTICUR injectable reste important dans la correction d’urgence des manifestations aiguës de type extrapyramidal induites par les neuroleptiques et dans le traitement des syndromes parkinsoniens induits par les neuroleptiques. |
Amélioration du service médical rendu (ASMR)
Pas d'ASMR disponible pour ce médicament (plus d'informations dans l'aide )
ANSM - Mis à jour le : 05/11/2021
LEPTICUR 10 mg/2 ml, solution injectable
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chlorhydrate de tropatépine................................................................................................... 10 mg
Pour une ampoule de 2 ml.
Pour la liste complète des excipients, voir rubrique 6.1.
4.1. Indications thérapeutiques
4.2. Posologie et mode d'administration
1 à 2 ampoules par jour selon l'intensité des troubles.
Mode d’administration
Voie I.M. ou I.V. lente.
Population pédiatrique
LEPTICUR n’est pas recommandé chez les enfants de moins de 18 ans en raison de l’absence de données de sécurité et d’efficacité
· Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
· Risque de glaucome par fermeture de l'angle.
· Cardiopathies décompensées.
· Risque de rétention urinaire liée à des troubles urétroprostatiques
4.4. Mises en garde spéciales et précautions d'emploi
Risque d'aggravation d'une détérioration intellectuelle dans les démences, en particulier chez les patients parkinsoniens.
La survenue d'un iléus paralytique pouvant être révélée par une distension et des douleurs abdominales impose une prise en charge d'urgence.
Une éventuelle pharmacodépendance à la tropatépine ne peut être exclue
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Associations faisant l'objet de précautions d’emploi
+ Alcaloïdes de l'ergot de seigle dopaminergiques (bromocriptine, cabergoline, lisuride, pergolide)
Risque d'apparition de confusion mentale. Surveillance clinique régulière, notamment en début d'association.
Associations à prendre en compte
+ Atropine et autres substances atropiniques (antidépresseurs imipraminiques, antihistaminiques H1 sédatifs, antispasmodiques atropiniques, autres antiparkinsoniens anticholinergiques, disopyramide, neuroleptiques phénothiaziniques, clozapine)
Addition des effets indésirables atropiniques à type de rétention urinaire, constipation, sécheresse de la bouche
4.6. Fertilité, grossesse et allaitement
Grossesse
Les données animales sont insuffisantes pour conclure.
Au cours du 1er trimestre de la grossesse, les données cliniques pour la tropatépine, à ce jour, bien que limitées, ne vont pas dans le sens d'une augmentation d'un risque malformatif.
Chez le nouveau-né, un traitement par la tropatépine en fin de grossesse, peut être responsable d'effets liés à ses propriétés atropiniques (tachycardie, hyperexcitabilité, rétention urinaire, retard à l'émission de méconium).
Compte tenu de ces données, il est préférable, d'éviter d'utiliser la tropatépine au cours de la grossesse quel qu'en soit le terme.
S'il s'avère indispensable de prescrire un traitement par tropatépine au cours de la grossesse, tenir compte, pour la surveillance du nouveau-né des effets précédemment décrits
En l'absence des données de passage dans le lait de la tropatépine, et en raison de possible survenu d'effets anticholinergiques chez le nouveau-né, l'allaitement est déconseillé.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Il faut toutefois remarquer que les indications de LEPTICUR concernent le plus souvent des malades pour lesquels la conduite de véhicules n'est pas recommandée.
Comme avec tous les anticholinergiques, des effets atropiniques peuvent être observés :
· Sécheresse de la bouche.
· Troubles de l'accommodation.
· Hypertonie oculaire.
· Troubles mictionnels.
· Constipation.
Ils cèdent rapidement, soit de façon spontanée, soit après une réduction de la posologie.
· De rares cas de confusion.
· De très rares cas d'iléus paralytique ont été rapportés en association avec d'autres médicaments anticholinergiques, comme les neuroleptiques (voir rubrique 4.4).
On peut parfois observer des indurations au point d'injection, notamment en cas d'administration prolongée
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.signalement-sante.gouv.fr.
Symptômes
Ceux de l'intoxication aiguë par les anticholinergiques : mydriase, agitation, confusion, hallucinations, convulsions, hyperventilation, tachycardie, hyperthermie.
Traitement
Evacuation du toxique, traitement symptomatique ; antidote proposé : néostigmine 0,5 à 2,5 mg, en injection IM ou IV lente.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : Antiparkinsonien anticholinergique, code ATC : N04AA12.
Pharmacologiquement, la tropatépine présente des propriétés anticholinergiques centrales; elle entraîne aussi des effets périphériques parasympatholytiques, mais l'expérimentation animale a montré que ceux-ci n'apparaissaient qu'à des doses plus élevées.
5.2. Propriétés pharmacocinétiques
L'élimination urinaire se fait sous forme de tropatépine inchangée, de desméthyltropatépine et, surtout, de sulfoxyde de tropatépine.
5.3. Données de sécurité préclinique
Non renseignée.
Eau pour préparations injectables.
En l’absence d’études de compatibilité, ce médicament ne doit pas être mélangé avec d’autres médicaments.
Avant ouverture : 3 ans.
Après ouverture : le produit doit être utilisé immédiatement
6.4. Précautions particulières de conservation
Pas de précautions particulières de conservation.
6.5. Nature et contenu de l'emballage extérieur
2 ml en ampoule (verre). Boîte de 1 ou 10 ampoule(s).
6.6. Précautions particulières d’élimination et de manipulation
Pas d’exigences particulières.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
49 RUE ROUELLE
75015 PARIS
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· CIP 34009 323 108 8 3 : 2 ml en ampoule (verre). Boîte de 10.
· CIP 34009 317 561 6 3 : 2 ml en ampoule (verre). Boîte de 1.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
<{JJ mois AAAA}>
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I
ANSM - Mis à jour le : 05/11/2021
LEPTICUR 10 mg/2 ml, solution injectable
Chlorhydrate de tropatépine
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que LEPTICUR 10 mg/2 ml, solution injectable et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser LEPTICUR 10 mg/2 ml, solution injectable ?
3. Comment utiliser LEPTICUR 10 mg/2 ml, solution injectable ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver LEPTICUR 10 mg/2 ml, solution injectable ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE LEPTICUR 10 mg/2 ml, solution injectable ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : Antiparkinsonien Anticholinergique
Code ATC : N04AA12
Ce médicament est préconisé dans les symptômes provoqués par certains médicaments (neuroleptiques).
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER LEPTICUR 10 mg/2 ml, solution injectable ?
N’utilisez jamais LEPTICUR 10 mg/2 ml, solution injectable dans les cas suivants :
· Si vous êtes allergique à la tropatépine ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
· Risque de glaucome (augmentation de la pression à l'intérieur de l'œil).
· Troubles de la miction (difficultés pour uriner d'origine prostatique ou autre).
· Maladie cardiaque non contrôlée par le traitement.
La sécurité et l’efficacité de LEPTICUR 10 mg/2 ml, solution injectable n’ont pas été établies chez les enfants de moins de 18 ans.
EN CAS DE DOUTE, IL EST INDISPENSABLE DE DEMANDER L'AVIS DE VOTRE MEDECIN OU DE VOTRE PHARMACIEN.
Avertissements et précautions
Adressez-vous à votre médecin ou pharmacien avant d’utiliser LEPTICUR 10 mg/2 ml, solution injectable.
NE PAS ARRETER BRUTALEMENT LE TRAITEMENT SANS AVIS MEDICAL.
Une aggravation peut être observée chez les patients parkinsoniens présentant une détérioration intellectuelle.
En cas de constipation persistante, de ballonnement important et de douleurs abdominales, consultez rapidement un médecin. Ce médicament peut, dans de très rares cas, provoquer une occlusion intestinale lorsqu'il est associé avec d'autres médicaments possédant les mêmes propriétés (par exemple les neuroleptiques).
EN CAS DE DOUTE, NE PAS HESITER A DEMANDER L'AVIS DE VOTRE MEDECIN OU DE VOTRE PHARMACIEN.
Autres médicaments et LEPTICUR 10 mg/2 ml, solution injectable
AFIN D'EVITER D'EVENTUELLES INTERACTIONS ENTRE PLUSIEURS MEDICAMENTS, notamment le lisuride, les antiparkinsoniens de la même classe, certains antidépresseurs, antihistaminiques ou neuroleptiques, IL FAUT SIGNALER SYSTEMATIQUEMENT TOUT AUTRE TRAITEMENT EN COURS A VOTRE MEDECIN OU A VOTRE PHARMACIEN.
LEPTICUR 10 mg/2 ml, solution injectable avec des aliments et des boissons
Sans objet.
Grossesse
Il est préférable de ne pas utiliser ce médicament pendant la grossesse. Si vous découvrez que vous êtes enceinte, consultez votre médecin, lui seul peut juger de la nécessité de poursuivre le traitement.
Allaitement
L'allaitement est déconseillé en cas d'utilisation de ce produit.
Demandez conseil à votre médecin ou à votre pharmacien avant de prendre tout médicament.
Conduite de véhicules et utilisation de machines
L'attention des conducteurs de véhicules et des utilisateurs de machines est attirée sur la possibilité de troubles de la vision, lors de l'utilisation de ce médicament. Dans ce cas, vous ne devez pas conduire de véhicules ou d'engins mécaniques.
3. COMMENT UTILISER LEPTICUR 10 mg/2 ml, solution injectable ?
La posologie est variable et doit être adaptée à l'intensité des troubles ainsi qu'à la susceptibilité individuelle de chaque patient.
DANS TOUS LES CAS, SE CONFORMER STRICTEMENT A L'ORDONNANCE DE VOTRE MEDECIN.
Mode et voie d'administration
Voie intramusculaire ou intraveineuse lente.
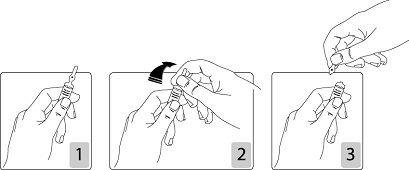
Pour ouvrir l’ampoule :
Tenir fermement l’ampoule, le point coloré face à vous (schéma 1). Saisir la tête de l’ampoule entre le pouce et l’index (le pouce sur le point coloré), puis exercer une pression vers l’arrière (schémas 2 et 3).
|
|
Fréquence d'administration
Le nombre d'injections et leur répartition sont adaptés individuellement.
Durée du traitement
Vous devez impérativement respecter la posologie et la durée du traitement prescrit, en particulier vous ne devez pas interrompre le traitement sans demander l'avis de votre médecin.
Si vous avez utilisé plus de LEPTICUR 10 mg/2 ml, solution injectable que vous n’auriez dû
Consultez immédiatement votre médecin ou votre pharmacien.
Si vous oubliez d’utiliser LEPTICUR 10 mg/2 ml, solution injectable
Si vous arrêtez d’utiliser LEPTICUR 10 mg/2 ml, solution injectable
L'interruption brutale du traitement peut provoquer la réapparition ou l'aggravation des symptômes.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
· Sécheresse de la bouche.
· Troubles de l'accommodation (vision floue).
· Hypertonie oculaire (augmentation de pression dans l'œil).
· Difficultés pour uriner.
· Constipation.
Généralement, ils cèdent rapidement, soit de façon spontanée, soit après une réduction de la dose.
Rarement :
· Confusion.
Très rarement :
· Occlusion intestinale.
Occasionnellement :
· Induration (durcissement de la peau) au point d'injection, notamment en cas d'administration prolongée.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.signalement-sante.gouv.fr.
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER LEPTICUR 10 mg/2 ml, solution injectable ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur la boîte. La date de péremption fait référence au dernier jour de ce mois.
Avant ouverture : pas de précautions particulières de conservation.
Après ouverture : le produit doit être utilisé immédiatement.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient LEPTICUR 10 mg/2 ml, solution injectable
· La substance active est :
Chlorhydrate de tropatépine................................................................................................... 10 mg
Pour une ampoule de 2 ml
· L’autre composant est :
Eau pour préparations injectables
Qu’est-ce que LEPTICUR 10 mg/2 ml, solution injectable et contenu de l’emballage extérieur
Ce médicament se présente sous forme de solution injectable.
Boîte de 1 ou 10 ampoule(s).
Titulaire de l’autorisation de mise sur le marché
49 RUE ROUELLE
75015 PARIS
Exploitant de l’autorisation de mise sur le marché
49 RUE ROUELLE
75015 PARIS
1 RUE COMTE DE SINARD,
26250 LIVRON-SUR-DROME,
FRANCE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).