 Participez à la création d’un site d'informations accessibles sur les médicaments pensé pour le grand public !
Participez à la création d’un site d'informations accessibles sur les médicaments pensé pour le grand public !Inscrivez-vous ici pour le tester en avant-première, partager vos impressions, et nous aider à l’améliorer !
 Participez à la création d’un site d'informations accessibles sur les médicaments pensé pour le grand public !
Participez à la création d’un site d'informations accessibles sur les médicaments pensé pour le grand public !ANSM - Mis à jour le : 08/02/2018
BRIMONIDINE TEVA 2 mg/ml, collyre en solution
Tartrate de brimonidine
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que BRIMONIDINE TEVA 2 mg/ml, collyre en solution et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser BRIMONIDINE TEVA 2 mg/ml, collyre en solution ?
3. Comment utiliser BRIMONIDINE TEVA 2 mg/ml, collyre en solution ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver BRIMONIDINE TEVA 2 mg/ml, collyre en solution ?
6. Contenu de l’emballage et autres informations.

Classe pharmacothérapeutique : Sympathomimétiques antiglaucomateux
Votre œil contient un liquide transparent, qui ressemble à de l’eau, et qui remplit l’intérieur de l’œil. Ce liquide est constamment drainé vers l’extérieur de l’œil, tandis que du nouveau liquide est fabriqué en remplacement. Si ce liquide n’est pas drainé assez rapidement, la pression s’accumule dans l’œil et peut affecter votre vision. La brimonidine réduit la production de liquide et augmente la quantité de liquide drainé. Ceci réduit la pression à l’intérieur de l’œil, tout en maintenant l’alimentation de l’œil.

N’utilisez jamais BRIMONIDINE TEVA 2 mg/ml, collyre en solution :
· si vous êtes allergique à la brimonidine ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
· si le patient a moins de 2 ans.
· si vous prenez des inhibiteurs de la monoamine oxydase (IMAO) ou certains autres médicaments antidépresseurs.
Avertissements et précautions
Adressez-vous à votre médecin ou pharmacien avant d’utiliser BRIMONIDINE TEVA :
· si vous avez ou si vous avez eu :
o une dépression ou d’autres troubles psychiatriques ;
o des troubles cardiaques ou des troubles de la pression artérielle ;
o des troubles circulatoires au niveau du cerveau, des jambes ou des bras ;
o des affections des reins ou du foie ;
· si vous portez des lentilles de contact. Ne mettez pas les gouttes si vous portez vos lentilles. Attendez au moins 15 minutes, après avoir mis les gouttes, avant de remettre vos lentilles de contact. Le chlorure de benzalkonium, agent conservateur présent dans ce produit, est susceptible d'entraîner une irritation oculaire et peut aussi décolorer les lentilles de contact souples.
Enfants
La brimonidine n'est pas recommandée chez les enfants de 2 à 12 ans.
Autres médicaments et BRIMONIDINE TEVA 2 mg/ml, collyre en solution
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
Indiquez à votre médecin si vous prenez l'un des médicaments suivants :
· inhibiteurs de la monoamine oxydase (IMAO) et certains autres antidépresseurs,
· antidouleurs, sédatifs, opiacés, barbituriques ou si vous consommez régulièrement de l'alcool,
· anesthésiques,
· médicament qui affecte le métabolisme tel que la chlorpromazine, le méthylphénidate et la réserpine,
· traitement pour le cœur ou pour réduire la tension artérielle,
· médicament qui agit sur les mêmes récepteurs que BRIMONIDINE TEVA 2 mg/ml, collyre en solution, par exemple : isoprénaline et prazosine.
BRIMONIDINE TEVA 2 mg/ml, collyre en solution avec des aliments et boissons
Sans objet.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
Ce médicament ne doit pas être utilisé au cours de la grossesse sauf si votre médecin le recommande.
Ce médicament ne doit pas être utilisé si vous allaitez.
Conduite de véhicules et utilisation de machines
Ce médicament est susceptible de provoquer une certaine fatigue ou somnolence, et une vision trouble chez certains patients. Ne conduisez pas et n’utilisez pas de machines tant que les symptômes n’ont pas disparu. Si vous avez des problèmes, parlez-en à votre médecin.
BRIMONIDINE TEVA 2 mg/ml, collyre en solution contient du chlorure de benzalkonium
Ce médicament contient 0,05 mg/ml de chlorure de benzalkonium. Voir rubrique « Avertissements et précautions » ci-dessus.

Voie oculaire.
Posologie
La dose recommandée est d’une goutte du médicament deux fois par jour à environ 12 heures d’intervalle. Ne modifiez par la dose et n’arrêtez pas d’utiliser le médicament sans en parler d’abord avec votre médecin.
Si vous utilisez plusieurs collyres, attendez au moins cinq minutes entre la brimonidine et les autres gouttes.
Mode d’administration
N’utilisez pas le flacon si le bouchon inviolable a été cassé avant que vous ne commenciez à l’utiliser.
Lavez-vous les mains avant d’ouvrir le flacon.
Penchez la tête vers l’arrière et regardez vers le haut.
1. Tirez doucement sur la paupière inférieure jusqu’à ce qu’il y ait une petite poche.
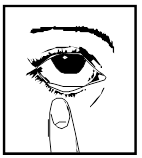
2. Retournez le flacon et appuyez dessus pour placer une goutte dans chaque œil à traiter.

3. Relachez la paupière inférieure et fermez l’oeil.

4. Gardez l’œil fermé et appuyez un doigt contre le coin de l’œil (du côté du nez) pendant une minute.

Si la goutte tombe à côté de l’œil, recommencez.
Pour prévenir les infections, ne touchez pas votre œil ou d’autres parties annexes avec l’embout du flacon. Replacez le bouchon à vis sur le flacon et refermez-le immédiatement après utilisation.
Utilisation chez les enfants
La brimonidine n’est pas recommandée chez les enfants de moins de 12 ans et ne doit pas être utilisée chez les nourrissons ni les enfants âgés de moins de 2 ans.
Si vous avez utilisé plus de BRIMONIDINE TEVA 2 mg/ml, collyre en solution que vous n’auriez dû
Adultes
Si vous avez utilisé plus de BRIMONIDINE TEVA 2 mg/ml, collyre en solution que vous n’auriez dû, cela ne devrait pas entraîner d’effets nocifs. Instillez la dose suivante à l’heure habituelle. Si vous êtes inquiet, parlez-en à votre médecin ou à votre pharmacien. En cas d’ingestion, contactez votre médecin.
Les adultes ayant accidentellement avalé BRIMONIDINE TEVA 2 mg/ml, collyre en solution ont présenté une diminution de la pression sanguine, suivie chez certains patients par une augmentation de cette pression.
Nouveau-nés
Quelques cas de surdosage ont été rapportés chez des nouveau-nés (jusqu’à 4 semaines) auxquels de la brimonidine a été administrée. Les signes de surdosage incluent : somnolence, mollesse, température basse, pâleur et difficultés respiratoires.
Si l’un de ces signes apparaît, contactez immédiatement votre médecin.
Si vous oubliez d’utiliser BRIMONIDINE TEVA 2 mg/ml, collyre en solution
Si vous oubliez d’utiliser BRIMONIDINE TEVA 2 mg/ml, collyre en solution, instillez la dose oubliée dès que vous vous en rendez compte puis reprenez le traitement comme avant. Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre.
Si vous arrêtez d’utiliser BRIMONIDINE TEVA 2 mg/ml, collyre en solution
BRIMONIDINE TEVA 2 mg/ml, collyre en solution doit être utilisé chaque jour pour agir correctement.
N’interrompez pas le traitement par BRIMONIDINE TEVA 2 mg/ml, collyre en solution, sans en avoir parlé d’abord à votre médecin.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.

Très fréquents (pouvant affecter plus de 1 personne sur 10) :
· Irritation oculaire (rougeur, brûlures, picotements, démangeaisons, sensation de corps étranger, points blancs sous la paupière), vision trouble et réaction allergique de l’œil.
· Céphalées, somnolence.
· Sécheresse de la bouche.
· Fatigue.
Fréquents (pouvant affecter jusqu’à 1 personne sur 10) :
· Irritation autour de l’œil, gonflement, rougeur et inflammation de la paupière ou sous la paupière, yeux douloureux ou collants, larmoiement, sensibilité à la lumière, petites ruptures sur la surface de la cornée, sécheresse oculaire, blanchiment sous la paupière, problèmes de vision.
· Vertige, troubles du goût.
· Symptômes ressemblant à un rhume.
· Problèmes digestifs.
· Faiblesse.
Peu fréquents (pouvant affecter jusqu’à 1 personne sur 100) :
· Réactions allergiques générales.
· Dépression.
· Palpitations, effets sur le rythme du cœur.
· Sécheresse du nez.
Rares (pouvant affecter jusqu’à 1 personne sur 1 000) :
· Essoufflement.
Très rares (pouvant affecter jusqu’à 1 personne sur 10 000) :
· Inflammation de l’œil ou diminution de la pupille.
· Somnolence.
· Evanouissements.
· Hypertension ou hypotension.
Fréquence indéterminée (ne peut être estimée sur la base des données disponibles) :
· Démangeaisons des paupières.
· Réactions cutanées incluant rougeur, gonflement du visage, démangeaisons, rash et dilatation des vaisseaux sanguins.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.ansm.sante.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.

Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’emballage et le flacon. La date de péremption fait référence au dernier jour de ce mois.
A conserver à une température ne dépassant pas 25°C.
Ne pas mettre au réfrigérateur. Ne pas congeler.
Jetez le flacon 28 jours après ouverture, même s’il reste du collyre.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.

Ce que contient BRIMONIDINE TEVA 2 mg/ml, collyre en solution 
· La substance active est le tartrate de brimonidine. 1 ml de solution contient 2,0 mg de tartrate de brimonidine, équivalant à 1,3 mg de brimonidine.
· Les autres composants sont : solution de chlorure de benzalkonium à 50 %, alcool polyvinylique, citrate de sodium, acide citrique monohydraté, chlorure de sodium, eau pour préparations injectables, hydroxyde de sodium ou acide chlorhydrique (pour ajustement du pH).
Qu’est-ce que BRIMONIDINE TEVA 2 mg/ml, collyre en solution et contenu de l’emballage extérieur 
Ce médicament se présente sous la forme d’un collyre en solution.
Solution transparente jaune-verdâtre dans un flacon en plastique de 5 ml doté d’un bouchon à vis.
Boîte de 1, 3 ou 6 flacons. Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché 
100-110, ESPLANADE DU GENERAL DE GAULLE
92931 PARIS LA DEFENSE CEDEX
FRANCE
Exploitant de l’autorisation de mise sur le marché 
TEVA SANTE
100-110, ESPLANADE DU GENERAL DE GAULLE
92931 PARIS LA DEFENSE CEDEX
FRANCE
BRAMPTON ROAD, HAMPDEN PARK, EASTBOURNE, EAST SUSSEX, BN22 9AG
ROYAUME UNI
ou
TEVA PHARMACEUTICAL EUROPE B.V.
SWENSWEG 5
2031 GA HARLEEM
PAYS BAS
Noms du médicament dans les Etats membres de l'Espace Economique Européen 
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[à compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est : 
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
|
| Plan du site | Accessibilité | Contact | Téléchargement | Declaration de confidentialité | Service-Public.fr | Legifrance | Gouvernement.fr |