
ALBEY VENIN D'ABEILLE Apis mellifera 550 microgrammes, poudre et solvant pour solution injectable - Notice patient |
 |
|
ANSM - Mis à jour le : 01/09/2023
ALBEY VENIN D'ABEILLE Apis mellifera 550 microgrammes, poudre et solvant pour solution injectable
Venin d’abeille
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, qu'il soit mentionné ou non dans cette rubrique, parlez-en à votre médecin ou votre pharmacien. Voir rubrique 4.
1. Qu'est-ce que ALBEY VENIN D’ABEILLE Apis mellifera 550 microgrammes, poudre et solvant pour solution injectable et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant qu’ALBEY VENIN D’ABEILLE Apis mellifera 550 microgrammes, poudre et solvant pour solution injectable ne vous soit administré ?
3. Comment ALBEY VENIN D’ABEILLE Apis mellifera 550 microgrammes, poudre et solvant pour solution injectable est administré?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver ALBEY VENIN D’ABEILLE Apis mellifera 550 microgrammes, poudre et solvant pour solution injectable ?
6. Contenu de l’emballage et autres informations.

Classe pharmacothérapeutique : Extraits allergéniques, Insectes - code ATC : V01AA07
Ce médicament est utilisé chez les adultes, adolescents et enfants de plus de 2 ans pour :
· le diagnostic cutané de l'allergie au venin d’abeille,
· le traitement de l’allergie aux piqûres (venin) d'abeille (immunothérapie allergénique).
L'utilisation de ALBEY VENIN D’ABEILLE 550 microgrammes doit être supervisée par un médecin expérimenté en allergologie et dans le traitement de l'allergie par immunothérapie allergénique sous surveillance stricte en milieu hospitalier. Voir rubrique 3.
· si vous êtes allergique à l’un des composants contenus dans ce médicament, en dehors du venin d’abeille, mentionnés dans la rubrique 6,
· si en plus de la réaction allergique, vous avez eu des réactions inhabituelles rénales, musculaires, cutanées, neurologiques, hématologiques et articulaires lorsque vous avez été piqué par une abeille,
· si vous avez une maladie immunitaire (maladie chronique auto-immune) telles que vascularite systémique, périartérite noueuse ou autre,
· si vous avez un asthme et que les symptômes respiratoires ne sont pas suffisamment contrôlés,
L’immunothérapie allergénique aux venins d'hyménoptères ne doit pas être débutée pendant la grossesse en raison du risque de réactions généralisée.
Ce médicament est contre-indiqué chez les enfants de moins de 2 ans.
Avertissements et précautions
Adressez-vous à votre médecin ou pharmacien avant l’administration d’ALBEY VENIN D’ABEILLE Apis mellifera 550 microgrammes, poudre et solvant pour solution injectable :
Si au cours du traitement vous ressentez l’un des symptômes suivants, contactez immédiatement un médecin :
· Symptômes allergiques affectant tout le corps (par exemple des démangeaisons intenses de la paume des mains et de la plante des pieds, urticaire, gonflement de la bouche ou de la gorge entrainant des difficultés à avaler, respirer ou modifiant la voix, nausées, vomissement) (voir rubrique 4). Le médecin réévaluera la possibilité ou non de poursuivre le traitement.
En raison du risque de réactions allergiques systémiques pouvant dans leur sévérité extrême avoir des conséquences létales, le traitement doit être réalisé en présence ou par un médecin expérimenté dans l’immunothérapie allergénique et dans des conditions permettant un traitement d’urgence si nécessaire (incluant l’adrénaline).
Informez votre médecin si :
· si vous avez eu récemment une crise d’asthme, il peut être nécessaire de reporter l’injection à une date ultérieure,
· si vous avez une maladie cardiovasculaire ou bronchopulmonaire,
· si vous avez une mastocytose ou un taux sanguin de tryptase élevé,
· si vous prenez des médicaments pour le traitement de la dépression (anti-dépresseurs tricycliques, inhibiteurs de la monoamine oxydase (IMAO),
· si vous prenez des médicaments dits « inhibiteurs de COMT» utilisés dans le traitement de la maladie de Parkinson,
· si vous prenez des médicaments dits « bêtabloquants » qui sont des médicaments utilisés pour le traitement de problèmes cardiaques, de l'hypertension artérielle, ou en collyres (goutte pour les yeux) pour le traitement du glaucome,
· si vous prenez des médicaments dits « inhibiteurs de l’enzyme de conversion » (IEC) qui sont des médicaments utilisés dans le traitement des problèmes cardiaques ou de l'hypertension artérielle,
· si vous avez un cancer ou un déficit immunitaire ou si vous prenez des médicaments qui affectent votre système immunitaire,
· si vous avez une maladie auto-immune en rémission,
· si votre état de santé s’est dégradé.
Enfants et adolescents
L'immunothérapie allergénique aux venins d'hyménoptères est contre-indiquée chez les enfants de moins de 2 ans.
La décision d'une immunothérapie allergénique aux venins d'hyménoptères chez les enfants de 2 à 5 ans doit faire l'objet d'une attention toute particulière.
En cas de doute, il est indispensable de demander l’avis de votre médecin ou de votre pharmacien.
Autres médicaments et ALBEY VENIN D’ABEILLE Apis mellifera 550 microgrammes, poudre et solvant pour solution injectable
Informez votre médecin ou pharmacien si vous utilisez, avez récemment utilisé ou pourriez utiliser tout autre médicament ou si vous avez récemment été vacciné ou si vous prévoyez une vaccination prochainement.
Avant la réalisation des tests diagnostiques de l'allergie, informez votre médecin si vous prenez ou avez pris des médicaments antiallergiques (antihistaminiques ou corticoïdes) ou d'autres médicaments.
Certains médicaments peuvent altérer les résultats des tests diagnostiques cutanés. Votre médecin peut vous demander d'interrompre certains traitements avant la réalisation de tests cutanés.
ALBEY VENIN D’ABEILLE Apis mellifera 550 microgrammes, poudre et solvant pour solution injectable avec des aliments, boissons et de l’alcool
Les repas copieux et la prise d'alcool sont déconseillés les jours où sont réalisées les injections.
Grossesse, allaitement et fertilité
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou si vous envisagez une grossesse, demandez conseil à votre médecin ou à votre pharmacien avant de commencer l’immunothérapie allergénique avec ALBEY VENIN D’ABEILLE Apis mellifera.
Grossesse
Il n’y a pas d’expérience concernant l'utilisation d’ALBEY VENIN D’ABEILLE Apis mellifera au cours de la grossesse.
La pratique des tests de diagnostic cutanés avec ALBEY VENIN D’ABEILLE Apis mellifera n’est pas recommandée pendant la grossesse.
Un traitement de l’allergie au venin d’abeille avec ALBEY VENIN D’ABEILLE Apis mellifera ne doit pas être débuté en cours de la grossesse.
Un traitement d’entretien déjà en cours et bien toléré peut être poursuivi durant la grossesse.
Si vous constatez que vous êtes enceinte en cours de traitement, demandez l'avis de votre médecin, qui déterminera avec vous si le traitement par ALBEY VENIN D’ABEILLE Apis mellifera peut être poursuivi ou non.
Allaitement
Il n’y a pas d'étude concernant l'utilisation d’ALBEY VENIN D’ABEILLE Apis mellifera au cours de l'allaitement.
Votre médecin déterminera s'il y a lieu ou pas d'interrompre le traitement pendant l'allaitement.
Fertilité
Il n’y a pas de donnée concernant l'utilisation d’ALBEY VENIN D’ABEILLE Apis mellifera sur la fertilité.
Conduite de véhicules et utilisation de machines
ALBEY VENIN D’ABEILLE Apis mellifera n’a pas d’effet ou un effet négligeable sur l’aptitude à conduire des véhicules et à utiliser des machines.
ALBEY VENIN D’ABEILLE Apis mellifera 550 microgrammes, poudre et solvant pour solution injectable contient du chlorure de sodium.
Ce médicament contient moins de 1 mmol (23 mg) de sodium par dose, c-à-d. qu’il est essentiellement « sans sodium ».

L’utilisation de ce médicament doit être supervisée par un médecin expérimenté en allergologie et dans le traitement par immunothérapie allergénique et il sera administré sous surveillance stricte en milieu hospitalier.
Préparation du médicament :
La poudre contenue dans le flacon doit être diluée avec le solvant spécifiquement destiné à cet effet. La dilution dépend de l'utilisation du médicament (cf ci-après)
Modalités d'administration :
Les modalités d'administration sont fonction de l'utilisation du médicament.
Utilisation en tests cutanés pour le diagnostic de l'allergie :
. Prick-test : la concentration de la solution utilisée est habituellement de 100 µg/ml
. Intradermoréaction : le test consiste en des injections par voie intradermique de doses progressivement croissantes jusqu'à obtention d'une réaction sur la peau.
Utilisation pour le traitement de l'allergie aux piqûres (venin) d’abeilles :La solution reconstituée est injectée par voie sous cutanée stricte sur la face externe ou postérieure du bras.
Le jour de l'injection, il est recommandé d'éviter les repas copieux, la prise d'alcool, les bains chauds, l'exercice physique.
Les modalités du traitement (dose, fréquence des injections) seront déterminées par votre médecin.
Si vous avez de la fièvre ou présentez tout autre signe d’infection le jour de l’injection ou si vous avez un eczéma qui s’est aggravé, votre médecin peut décider de reporter l’injection.
Le suivi du traitement doit être régulièrement inscrit sur un carnet que vous devez conserver et qui doit mentionner la date et la dose injectée.
Le traitement de l’allergie au venin d’abeille comporte deux étapes :
· La phase initiale consiste en des injections permettant une augmentation progressive de la dose administrée pour atteindre la dose d’entretien. Il existe différents schémas d'administration plus ou moins rapides pour cette phase. Votre médecin décidera du schéma le mieux adapté pour vous. Quel que soit le protocole choisi, l'initiation du traitement doit être réalisée sous surveillance médicale stricte en milieu hospitalier.
· La deuxième phase consiste en des injections de cette dose d’entretien, en principe toutes les 4 semaines au cours de la première année, toutes les 6 semaines au cours de la deuxième année et toutes les 8 semaines les années suivantes. Votre médecin déterminera le rythme des injections selon votre cas.
Le traitement de l’allergie au venin d’abeille peut être poursuivi au minimum pendant 3 à 5 ans, ou plus longtemps dans certains cas.
Il est impératif que vous restiez sous surveillance médicale pendant au moins 30 minutes après chaque injection.
Dans les heures qui suivent l'administration de ce produit, contactez immédiatement un médecin en cas de survenue de symptômes tels que :
· une sensation d'étouffement, de gêne respiratoire, de difficulté à avaler ou une modification de la voix.
En cas de survenue d’effets secondaires généralisés ou d’une importante réaction locale après une injection du traitement, votre médecin peut être amené à vous prescrire des médicaments antiallergiques comme des antihistaminiques en prévention pour les prochaines injections.
Si vous interrompez votre traitement ou avez dépassé les délais recommandés entre 2 injections (sans lien avec des effets secondaires) :
· Le traitement de l’allergie au venin d’abeille nécessite le strict respect du protocole. Il est important de respecter le schéma d’injections défini par le médecin et le délai entre deux injections sauf si le traitement est interrompu à la suite d’un effet secondaire.
· En cas d’interruption du traitement, il n’est pas défini de protocole précis pour la reprise du traitement.
Votre médecin prescripteur adaptera avec vous les modalités de reprise des injections en fonction de votre cas et de la durée écoulée depuis la dernière injection. Une phase de reprise progressive peut être nécessaire pour revenir à la dose d'entretien. Une surveillance stricte en milieu hospitalier est requise lors de la reprise du traitement.
Utilisation chez les enfants et les adolescents
Les schémas de traitement préconisés sont identiques chez les adultes, les adolescents et les enfants.
Si vous avez utilisé plus de ALBEY VENIN D’ABEILLE Apis mellifera 550 microgrammes, poudre et solvant pour solution injectable que vous n’auriez dû
En cas de surdosage le risque d’effets indésirables, en particulier de manifestations généralisées ou locales telles que décrites dans la rubrique 4, est augmenté ; vous devez rester sous surveillance médicale.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.
Si vous oubliez d’utiliser ALBEY VENIN D’ABEILLE Apis mellifera 550 microgrammes, poudre et solvant pour solution injectable
Si vous arrêtez d’utiliser ALBEY VENIN D’ABEILLE Apis mellifera 550 microgrammes, poudre et solvant pour solution injectable
Sans objet.

Lors d’un traitement par ALBEY VENIN D’ABEILLE Apis mellifera, vous êtes exposé au venin d’abeille pouvant provoquer des réactions allergiques se manifestant au niveau de l’injection et/ou dans tout votre corps.
Un choc anaphylactique provoquant un malaise général brutal avec chute de la pression artérielle et nécessitant un traitement d’urgence peut survenir. Un choc anaphylactique est une réaction allergique sévère avec apparition brutale de symptômes qui affectent l’ensemble de l’organisme tels que des démangeaisons intenses ou une éruption cutanée, des difficultés respiratoires, des douleurs abdominales, ou des symptômes liés à une chute de tension comme des vertiges ou des malaises. Contactez immédiatement votre médecin si vous ressentez l’un de ces effets.
Si cela vous arrivait, votre médecin aura à disposition une trousse d’urgence comprenant une seringue d’adrénaline prête à l’emploi. C’est la raison pour laquelle vous devez rester sous surveillance médicale pendant au moins 30 minutes après avoir reçu une injection de ce médicament.
La tolérance d’une dose est susceptible de varier dans le temps en fonction de votre réactivité et de votre environnement.
Les effets indésirables suivants ont été observés :
· réactions locales au site d’injection pouvant s’accompagner de gonflement, douleurs, démangeaisons, rougeurs, induration
· rythme cardiaque rapide
· étourdissements
· hypotension (pression artérielle basse)
· manifestations généralisées (réactions de tout le corps): choc anaphylactique, hypersensibilité, gêne thoracique, douleur thoracique, sensation de chaleur
· gonflement généralisé ou local, malaise, sensation de fatigue extrême
· troubles respiratoires : crises d’asthme, difficultés à respirer, toux, nez bouché, gonflement dans la gorge, irritations de la gorge, sensation de gorge serrée, respiration sifflante
· arthralgie (douleur des articulations)
· diarrhée, douleurs abdominales, douleurs gastriques et nausée
· gonflement du visage, urticaire, démangeaisons, rougeurs
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou à votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.

Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur le conditionnement extérieur. La date de péremption fait référence au dernier jour de ce mois.
Le produit, avant et après reconstitution, ainsi que les dilutions doivent être conservés au réfrigérateur (entre + 2°C et + 8°C).
Les durées maximales de conservation varient selon la concentration des solutions.
Pour une concentration de 100 µg/ml, la durée maximale de conservation de la solution est de 28 jours entre +2 et +8°C.
Pour une concentration inférieure à 100 µg/ml, la solution est à préparer le jour même.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.

Ce que contient ALBEY VENIN D’ABEILLE Apis mellifera 550 microgrammes, poudre et solvant pour solution injectable 
· La substance active est :
Venin d’abeille quantité correspondant en protéines à 550 microgrammes pour un flacon de poudre.
· Les autres composants sont :
Flacon de poudre : mannitol, chlorure de sodium
Solvant : albumine humaine, chlorure de sodium, phénol, eau pour préparations injectables.
Qu’est-ce que ALBEY VENIN D’ABEILLE Apis mellifera 550 microgrammes, poudre et solvant pour solution injectable et contenu de l’emballage extérieur 
Ce médicament se présente sous forme de poudre et solvant pour solution injectable.
Coffret multidose : 1 flacon de poudre + 1 flacon de solvant de 6 ml+ 5 flacons de solvant de 1,8 ml.
1 flacon de poudre.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché 
6 Rue ALEXIS DE TOCQUEVILLE
92160 ANTONY
FRANCE
Exploitant de l’autorisation de mise sur le marché 
STALLERGENES
6 Rue ALEXIS DE TOCQUEVILLE
92160 ANTONY
FRANCE
6 Rue ALEXIS DE TOCQUEVILLE
92160 ANTONY
FRANCE
Noms du médicament dans les Etats membres de l'Espace Economique Européen 
Sans objet.
La dernière date à laquelle cette notice a été révisée est : 
[à compléter ultérieurement par le titulaire]
< {MM/AAAA}>< {mois AAAA}.>
Les informations suivantes sont destinées exclusivement aux professionnels de santé :
Reconstitution et dilutions
La solution est reconstituée en ajoutant 5,5 ml de solvant au contenu d'un flacon de poudre.
Mélanger doucement jusqu’à dissolution complète en retournant le flacon plusieurs fois. Ne pas agiter pour éviter la formation de mousse.
La concentration ainsi obtenue est de 100 µg/ml.
Pour obtenir une concentration 10 fois plus faible (10 µg/ml), prélever un volume de 0,2 ml de solution reconstituée et l’injecter dans le flacon contenant 1,8 ml de solvant. Cette opération sera renouvelée pour obtenir des dilutions successives au 1/10. Des flacons supplémentaires de solvant sont fournis si besoin séparément en fonction des dilutions utilisées.
Avant de prélever la dose à injecter, veillez à retourner le flacon plusieurs fois pour mélanger soigneusement son contenu sans agiter pour éviter la formation de mousse.
Exemple de schéma de dilutions
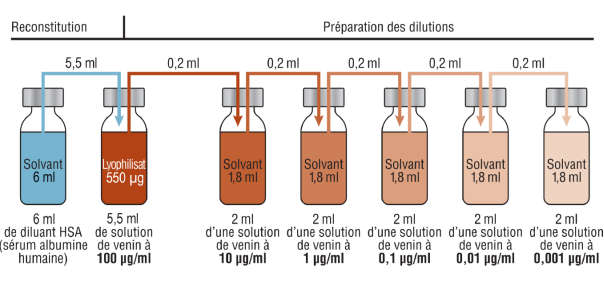
Utilisation pour le test diagnostique
. Prick-test : la concentration usuelle utilisée est de 100 µg/ml.
. Test par intradermoréaction : le test sera réalisé en injectant 0,02 à 0,03 ml d’une solution de venin diluée à 0,001 µg/ml par voie intradermique. En cas de réponse négative, répéter l’injection en utilisant une concentration 10 fois plus élevée et ceci jusqu’à obtention d’une réaction cutanée positive, sans dépasser une concentration maximale de 1 µg/ml. Dans certains cas, notamment pour des patients particulièrement sensibilisés au venin d’abeille, il est prudent de démarrer les tests à la concentration de 0,0001 µg/ml.
Il existe une période réfractaire d’au moins deux semaines suivant une réaction allergique systémique à une piqure d’hyménoptère au cours de laquelle il est possible d’observer un résultat faussement négatif d’un test cutané. Cette période peut néanmoins être prolongée. Aussi, il peut être préférable de réaliser le test 4 à 6 semaines après la réaction allergique à la piqure afin d’éviter la possibilité d’un faux-négatif.
Utilisation pour immunothérapie allergénique aux venins d'hyménoptères
Voie sous-cutanée stricte.
Ne PAS injecter par voie intraveineuse.
Le produit sera injecté lentement par voie sous-cutanée sur la face externe du bras ou dans la région deltoïdienne, en prenant soin de ne pas faire une injection intra-veineuse (procéder à cet effet à une légère aspiration préalable qui peut être renouvelée tous les 0,2 ml au cours de l'injection lente).
Avant chaque injection, vérifier soigneusement la nature de l’allergène utilisé, le dosage, le volume et la date de l'injection précédente (intervalle entre chaque injection).
Le patient doit être gardé sous surveillance médicale pendant au minimum 30 minutes après chaque injection.
Le patient doit être averti des facteurs qui pourraient déclencher des réactions allergiques le jour de l'injection : la pratique d'un sport intense, les bains chauds, les repas copieux et la consommation d'alcool sont déconseillés le jour de l’injection.
En cas d’épisode fébrile, de signes d'infection ou de maladie inflammatoire, il est recommandé de suspendre les injections jusqu’à résolution de l’affection.
En cas de dermatite atopique sévère, il est recommandé de traiter l’affection avant d’initier une immunothérapie allergénique. Les injections devront être suspendues en cas d’exacerbations aigües.
Chez les patients asthmatiques, l’injection devra être reportée en cas d’exacerbation aigüe jusqu’à 24 à 48 heures après résolutions des symptômes respiratoires.
L’initiation du traitement (quel que soit le protocole utilisé) doit être réalisée sous surveillance stricte en milieu hospitalier.
Le protocole utilisé pour atteindre la dose d'entretien doit être adapté par un médecin expérimenté en allergologie et en immunothérapie allergénique, en fonction de l'état clinique et de la tolérance du patient.
Les délais pour atteindre la dose d’entretien sont fonction de la méthode utilisée :
· en quelques heures (Ultrarush) ou quelques jours (Rush),
· en quelques semaines: schéma dit «cluster » ou méthode conventionnelle.
La dose d’entretien préconisée est de 100 µg d’extrait de venin. Elle peut être augmentée à 200 μg notamment pour des apiculteurs ou pour des patients insuffisamment protégés par 100 µg.
Carnet de suivi :
La conduite de l’immunothérapie allergénique aux venins d'hyménoptères doit être régulièrement inscrite sur le carnet de suivi que doit conserver le patient.
|
| Plan du site | Accessibilité | Contact | Téléchargement | Declaration de confidentialité | Service-Public.fr | Legifrance | Gouvernement.fr |