Dernière mise à jour le 28/04/2026
DICYNONE 250 mg/2 ml, solution injectable
Indications thérapeutiques
AUTRE HEMOSTATIQUE SYSTEMIQUE - code ATC : B02BX01
Ce médicament est un antihémorragique et un vasculoprotecteur.
Il est proposé:
· dans le traitement des saignements par fragilité des petits vaisseaux sanguins et dans les saignements gynécologiques,
· en cas d'intervention chirurgicale pour diminuer les pertes sanguines.
Présentations
> 6 ampoule(s) en verre de 2 ml
Code CIP : 303 088-1 ou 34009 303 088 1 3
Déclaration de commercialisation : 19/01/1965
Cette présentation n'est pas agréée aux collectivités
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Insuffisant | Avis du 08/06/2005 | Réévaluation SMR | Le service médical rendu de ces spécialités est insuffisant dans l'ensemble de leurs indications. |
Amélioration du service médical rendu (ASMR)
Pas d'ASMR disponible pour ce médicament (plus d'informations dans l'aide )
ANSM - Mis à jour le : 29/01/2025
DICYNONE 250 mg/2 ml, solution injectable
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Etamsylate..................................................................................................................... 250,00 mg
Pour une ampoule.
Excipient(s) à effet notoire : sulfites
Pour la liste complète des excipients, voir rubrique 6.1.
4.1. Indications thérapeutiques
En médecine dans le traitement des:
· saignements par fragilité capillaire,
· ménorragies sans cause organique décelable,
Et en chirurgie générale ou spécialisée (O.R.L, ophtalmologie, gynécologie) pour:
Diminuer les pertes sanguines au cours des interventions chirurgicales, en particulier hémorragies en nappe, malades sous anti-coagulants.
4.2. Posologie et mode d'administration
Adultes:
· en urgence: 2 à 3 ampoules, trois fois par jour, en I.V. ou I.M.
· en pré-opératoire: 1 heure avant l'intervention, 2 ampoules I.V. ou I.M.
· en per-opératoire: à la demande
· en post-opératoire: 1 ampoule I.V. ou I.M., 2 fois par jour.
Population pédiatrique (nourrissons et enfants)
même schéma thérapeutique que chez l'adulte en réduisant la posologie de moitié.
N.B.: la solution injectable peut être utilisée:
· par voie orale: diluée dans un demi-verre d'eau,
· localement: en tamponnements
4.4. Mises en garde spéciales et précautions d'emploi
Plusieurs cas de fièvre isolée et réapparaissant en cas de reprise du traitement ont été rapportés avec l’étamsylate. En cas d'apparition d'une fièvre, le traitement doit être arrêté et ne doit pas être repris.
En l’absence d’information sur l’innocuité de l’étamsylate chez les patients atteints de prophyrie aiguë, ce médicament est déconseillé chez ces patients.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Les données disponibles à ce jour ne laissent pas supposer l’existence d’interactions cliniquement significatives.
Interactions avec les examens paracliniques
La prise d’étamsylate à doses thérapeutiques peut fausser le dosage enzymatique de la créatinine en donnant des valeurs plus basses.
Pendant le traitement avec l’étamsylate, le prélèvement d’échantillon (par exemple une prise de sang) requis pour les tests de laboratoire doit être fait avant la première administration quotidienne du médicament afin de minimiser toute interaction potentielle d’étamsylate avec les tests de laboratoire
4.6. Fertilité, grossesse et allaitement
Grossesse
Les données sur l’utilisation d’étamsylate chez les femmes enceintes sont limitées.
Les études menées chez l’animal n’ont mis en évidence aucun effet nocif direct ou indirect en ce qui concerne la toxicité sur la reproduction.
Par mesure de précaution, il est préférable d’éviter l’utilisation d’étamsylate pendant la grossesse
En l'absence de données sur le passage dans le lait maternel, l'allaitement est déconseillé pendant la durée du traitement.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Sans objet.
Les effets indésirables sont classés par fréquence et par classe de système d'organe. La fréquence est définie de la manière suivante:
· Très fréquente (≥ 1/10),
· Fréquent (≥ 1/100 à< 1/10),
· Peu fréquent (≥ 1/1 000 à <1/100),
· Rare (≥ 1/10 000 à < 1/1 000),
· Très rare (< 1/10 000),
· Fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
Troubles gastro intestinaux
Fréquence indéterminée : nausées, diarrhées, vomissements
Troubles cutanés et sous-cutanés :
Fréquence indéterminée : éruption cutanée
Troubles généraux et réactions au point d’injections
Fréquence indéterminée : fièvre
Troubles du système nerveux
Fréquence indéterminée : céphalées
Troubles sanguins et du système lymphatique :
Fréquence indéterminée : agranulocytose, neutropénie
Troubles du système immunitaire
Fréquence indéterminée : réaction d’hypersensibilité principalement à type d’urticaire, imposant l’arrêt du traitement.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
A ce jour aucun cas de surdosage n’a été rapporté. Dans le cas d’un surdosage, le traitement sera symptomatique.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : AUTRE HEMOSTATIQUE SYSTEMIQUE, code ATC : B02BX01.
Effets pharmacodynamiques
Amélioration de l'adhésivité plaquettaire et restauration de la résistance capillaire.
5.2. Propriétés pharmacocinétiques
Voie injectable: 1 heure après injection (I.V. ou I.M.) de 500 mg d'étamsylate, on obtient une concentration plasmatique de 30 µg/ml. Les demi-vies plasmatiques sont respectivement de 1,9 heure (I.V.) et 2,1 heures (I.M).
Le taux de liaison aux protéines plasmatiques est élevé: il est de l'ordre de 95 %. L'étamsylate est éliminé essentiellement par voie urinaire, sous forme inchangée (> 80 %).
5.3. Données de sécurité préclinique
Solution diluée de sulfite monosodique, bicarbonate de sodium, eau pour préparations injectables.
Après ouverture: le produit doit être utilisé immédiatement.
6.4. Précautions particulières de conservation
Pas de précautions particulières de conservation.
6.5. Nature et contenu de l'emballage extérieur
2 ml en ampoule (verre). Boîte de 6 ou 50.
6.6. Précautions particulières d’élimination et de manipulation
Pas d’exigences particulières pour l’élimination.
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
Avenida António Augusto de Aguiar nº 19 – 4º
1050-012 Lisboa
Portugal
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 303 088 1 3 : 2 ml en ampoule (verre). Boîte de 6.
· 34009 551 331 3 1 : 2 ml en ampoule (verre). Boîte de 50
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Médicament non soumis à prescription médicale.
ANSM - Mis à jour le : 29/01/2025
DICYNONE 250 mg/2 ml, solution injectable
étamsylate
Vous devez toujours prendre ce médicament en suivant scrupuleusement les informations fournies dans cette notice ou par votre médecin ou votre pharmacien.
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Adressez-vous à votre pharmacien pour tout conseil ou information.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
· Vous devez vous adresser à votre médecin si vous ne ressentez aucune amélioration ou si vous vous sentez moins bien.
Ne laissez pas ce médicament à la portée des enfants.
1. Qu'est-ce que DICYNONE 250 mg/2 ml, solution injectable et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d’utiliser DICYNONE 250 mg/2 ml, solution injectable ?
3. Comment utiliser DICYNONE 250 mg/2 ml, solution injectable ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver DICYNONE 250 mg/2 ml, solution injectable ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE DICYNONE 250 mg/2 ml, solution injectable ET DANS QUELS CAS EST-IL UTILISE ?
AUTRE HEMOSTATIQUE SYSTEMIQUE - code ATC : B02BX01
Ce médicament est un antihémorragique et un vasculoprotecteur.
Il est proposé:
· dans le traitement des saignements par fragilité des petits vaisseaux sanguins et dans les saignements gynécologiques,
· en cas d'intervention chirurgicale pour diminuer les pertes sanguines.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER DICYNONE 250 mg/2 ml, solution injectable ?
N’utilisez jamais DICYNONE 250 mg/2 ml, solution injectable :
· Si vous êtes allergique (hypersensible) à la substance active (l'étamsylate) ou à l'un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
Avertissements et précautions
· Ce médicament contient du « sulfite » et peut provoquer des réactions allergiques sévères et une gêne respiratoire.
· Si vous avez de la fièvre ou une réaction au niveau de la peau, arrêtez de prendre ce médicament et consultez immédiatement votre médecin.
· Ce médicament est généralement déconseillé en cas de maladie du sang touchant l’hémoglobine (porphyrie aigüe).
· Analyses de sang : Prévenez votre médecin si vous prenez Dicynone et que vous devez faire un test sanguin car ce médicament peut fausser les résultats de votre taux de créatinine dans le sang en donnant des valeurs plus basses.
· Veuillez informer votre médecin ou votre pharmacien si vous allez subir des examens médicaux : pendant le traitement avec l’étamsylate, le prélèvement d’échantillon (par exemple une prise de sang) requis pour les tests de laboratoire doit être fait avant la première administration quotidienne du médicament afin de minimiser toute interaction potentielle d’étamsylate avec les tests de laboratoire.
Autres médicaments et DICYNONE 250 mg/2 ml, solution injectable
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
DICYNONE 250 mg/2 ml, solution injectable avec des aliments et boissons
Sans objet.
Les données sur l’utilisation de Dicynone chez les femmes enceintes sont limitées. Par mesure de précaution, il est préférable d’éviter l’utilisation de Dicynone pendant la grossesse.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
L'allaitement est déconseillé pendant la durée du traitement.
Sportifs
Sans objet.
Conduite de véhicules et utilisation de machines
Sans objet.
DICYNONE 250 mg/2 ml, solution injectable contient : sulfite de sodium.
3. COMMENT UTILISER DICYNONE 250 mg/2 ml, solution injectable ?
Adultes:
· en urgence: 2 à 3 ampoules, trois fois par jour, en I.V. ou I.M.
· en pré-opératoire: 1 heure avant l'intervention, 2 ampoules I.V. ou I.M.
· en per-opératoire: à la demande.
· en post-opératoire: 1 ampoule I.V. ou I.M, 2 fois par jour.
Utilisation chez les enfants
Nourrissons et enfants: même schéma thérapeutique que chez l'adulte en réduisant la posologie de moitié.
N.B.: la solution injectable peut être utilisée:
· par voie orale: diluée dans un demi-verre d'eau,
· localement: en tamponnements.
Mode d'administration
Voie injectable.
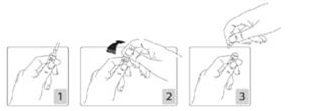
Pour ouvrir l'ampoule: Tenir fermement l'ampoule, le point coloré face à vous (schéma 1). Saisir la tête de l'ampoule entre le pouce et l'index (le pouce sur le point coloré), puis exercer une pression vers l'arrière (schémas 2 et 3).
Si vous avez pris plus de DICYNONE 250 mg/2 ml, solution injectable que vous n’auriez dû :
Sans objet.
Si vous oubliez de prendre DICYNONE 250 mg/2 ml, solution injectable :
Si vous arrêtez de prendre DICYNONE 250 mg/2 ml, solution injectable :
Sans objet.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
· nausées, vomissements, diarrhée,
· éruptions de boutons et/ou plaques sur la peau,
· fièvre,
· maux de tête,
· diminution sévère du nombre de globules blancs (agranulocytose)
· diminution du nombre de globules blancs (neutropénie)
· réactions allergiques, allant de l'éruption de boutons et/ou plaques sur la peau jusqu’à une réaction plus grave (choc anaphylactique) avec malaise et baisse importante de la pression artérielle et/ou gêne respiratoire (bronchospasme).
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: https://signalement.social-sante.gouv.fr/
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER DICYNONE 250 mg/2 ml, solution injectable ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’emballage. La date de péremption fait référence au dernier jour de ce mois.
Après ouverture: le produit doit être utilisé immédiatement.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient DICYNONE 250 mg/2 ml, solution injectable
· La substance active est :
Etamsylate..................................................................................................................... 250 mg
Pour une ampoule.
· Les autres composants excipients sont :
Solution diluée de sulfite monosodique, bicarbonate de sodium, eau pour préparations injectables.
Qu’est-ce que DICYNONE 250 mg/2 ml solution injectable et contenu de l’emballage extérieur
Ce médicament se présente sous forme d'une solution injectable en ampoule.
Boîte de 6 ou 50 ampoules.
Titulaire de l’autorisation de mise sur le marché
Avenida António Augusto de Aguiar nº 19 – 4º
1050-012 Lisboa
Portugal
Exploitant de l’autorisation de mise sur le marché
FOSUN PHARMA SAS
ZONE D’ACTIVITE LA BALME
2 RUE DES PYRENEES
31450 BELBERAUD
FRANCE
6, BOULEVARD DE L'EUROPE
21800 QUETIGNY
FRANCE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
à compléter ultérieurement par le titulaire
Sans objet.