Dernière mise à jour le 28/04/2026
JOSACINE 125 mg/5 ml, granulés pour suspension buvable
Ce médicament n'est ou ne sera bientôt plus disponible sur le marché.
Si vous prenez actuellement ce médicament, il vous est recommandé d'en parler avec votre médecin
ou avec votre pharmacien qui pourra vous orienter vers un autre traitement.
Indications thérapeutiques
Classe pharmacothérapeutique : ANTIBACTERIENS A USAGE SYSTEMIQUE - code ATC : J01FA07.
Ce médicament est un antibiotique antibactérien de la famille des macrolides.
Ce médicament est utilisé pour traiter ou prévenir certaines infections dues à des bactéries et sur lesquelles la substance active (la josamycine) a un effet.
JOSACINE existe en plusieurs formes et dosages. La forme "granulés pour suspension buvable" est spécialement adaptée pour l'enfant et existe en 3 dosages : 125 mg/5 ml, 250 mg/5 ml et 500 mg/5 ml.
Le dosage à utiliser dépend du poids de votre enfant :
Le dosage "JOSACINE 125 mg/5 ml" est réservé au nourrisson pesant entre 2 et 5 kg.
Le dosage "JOSACINE 250 mg/5 ml" est réservé à l'enfant pesant entre 5 et 10 kg.
Le dosage "JOSACINE 500 mg/5 ml" est réservé à l'enfant pesant entre 10 et 40 kg.
Documents de bon usage du médicament
- Choix et durée de l'antibiothérapie : Rhinopharyngite aiguë enfant
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Juillet 2024
- Choix et durée de l'antibiothérapie : Rhinopharyngite aiguë l’adulte
Auteur : Haute autorité de santé
Type : Fiche mémo
Date de mise à jour :Juillet 2024
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 22/02/2017 | Renouvellement d'inscription (CT) | Le service médical rendu par JOSACINE reste important dans ces indications : • angines documentées à streptocoque A bêta-hémolytique, en alternative au traitement par bêta lactamines, particulièrement lorsque celui-ci ne peut être utilisé • exacerbations des bronchites chroniques • pneumonies communautaires • infections cutanées bénignes • infections stomatologiques • infections génitales non gonococciques • chimioprophylaxie des rechutes du RAA en cas d'allergie aux bêta-lactamines. |
| Insuffisant | Avis du 22/02/2017 | Renouvellement d'inscription (CT) | Le service médical rendu par JOSACINE reste insuffisant dans l’indication « sinusites aiguës ». Les recommandations actuelles précisent clairement que l’abstention de toute prescription d’antibiotique doit être la règle dans la prise en charge thérapeutique des bronchites aiguës, y compris chez les sujets à risque. |
Amélioration du service médical rendu (ASMR)
Pas d'ASMR disponible pour ce médicament (plus d'informations dans l'aide )
ANSM - Mis à jour le : 14/05/2024
JOSACINE 125 mg/5 ml, granulés pour suspension buvable
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Josamycine base................................................................................................................. 125 mg
(Sous forme de propionate de josamycine)
Pour 5 ml de suspension reconstituée.
Excipients à effet notoire par 5 ml de suspension buvable : saccharose (842,33 mg), parahydroxybenzoate de méthyle (E218 ; 6,625 mg), parahydroxybenzoate de propyle (E216 ; 0,875 mg), sodium (moins de 2,3 mg) et alcool benzylique (0,001 mg) (présent dans l’arôme fraise).
Pour la liste complète des excipients, voir rubrique 6.1.
Granulés pour suspension buvable.
Fins granulés blancs avec une odeur de fraise.
4.1. Indications thérapeutiques
Elles sont limitées aux infections dues aux germes définis comme sensibles :
· angines documentées à streptocoque A bêta-hémolytique, en alternative au traitement par bêta-lactamines, particulièrement lorsque celui-ci ne peut être utilisé.
· sinusites aiguës. Compte-tenu du profil microbiologique de ces infections, les macrolides sont indiqués lorsqu'un traitement par une bêta-lactamine est impossible.
· surinfections des bronchites aiguës.
· exacerbations des bronchites chroniques.
· pneumopathies communautaires chez des sujets :
o sans facteurs de risque,
o sans signes de gravité clinique,
o en l'absence d'éléments cliniques évocateurs d'une étiologie pneumococcique.
En cas de suspicion de pneumopathie atypique, les macrolides sont indiqués quels que soient la gravité et le terrain.
· infections cutanées bénignes : impétigo, impétiginisation des dermatoses, ecthyma, dermo-hypodermite infectieuse (en particulier, érysipèle), érythrasma.
· infections stomatologiques.
· infections génitales non gonococciques.
· chimioprophylaxie des rechutes du RAA en cas d'allergie aux bêta-lactamines.
Il convient de tenir compte des recommandations officielles concernant l'utilisation appropriée des antibactériens.
4.2. Posologie et mode d'administration
Cette présentation est réservée au nourrisson de 2 à 5 kg.
La posologie est de 50 mg/kg de poids et par jour, à répartir en deux prises par jour.
Soit en pratique : 1 prise (25 mg/kg) le matin et 1 prise (25 mg/kg) le soir.
La dose par prise, est indiquée en fonction du poids de l'enfant sur le piston de la seringue pour administration orale graduée en kilo. Elle se lit directement sur les graduations de la seringue. Ainsi le poids indiqué correspond à la dose pour une prise.
La seringue pour administration orale est graduée de 2 à 5 kg, chaque graduation successive de 0,5 kg correspond à 12,5 mg de josamycine.
Attention, cette seringue pour administration orale ne doit pas être utilisée pour un autre médicament, la graduation étant spécifique à ce produit.
Deux prises par jour sont nécessaires.
Par exemple, pour un enfant de 4 kg, la dose à administrer par prise correspond à la seringue pour administration orale remplie jusqu'à la graduation 4.
Cas particuliers :
Angines : 50 mg/kg/jour à répartir en 2 prises journalières.
Soit en pratique : 1 prise (25 mg/kg) le matin et 1 prise (25 mg/kg) le soir.
La durée du traitement des angines est de 5 jours.
Mode d’administration
VOIE ORALE.
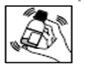 Préparation de la suspension
Préparation de la suspension
1) Agiter le flacon
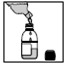
2) Puis ajouter de l’eau jusqu’au trait
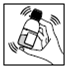
3) Agiter de nouveau et laisser reposer

4) Compléter avec de l’eau jusqu’au trait du flacon
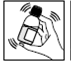
5) Agiter de nouveau
Administration du médicament
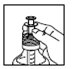 1) Plonger la seringue graduée dans le flacon
1) Plonger la seringue graduée dans le flacon
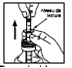 2) Tirer sur le piston pour aspirer la suspension jusqu’au trait correspondant au poids de l’enfant
2) Tirer sur le piston pour aspirer la suspension jusqu’au trait correspondant au poids de l’enfant
 3) Après utilisation, rincer la seringue avec de l’eau
3) Après utilisation, rincer la seringue avec de l’eau
 4) Coller le support sur le côté du flacon
4) Coller le support sur le côté du flacon
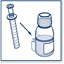 5) Replacer la seringue dans son support
5) Replacer la seringue dans son support
Attention, cette seringue pour administration orale ne doit pas être utilisée pour un autre médicament, la graduation étant spécifique à ce produit.
Utiliser uniquement la seringue graduée fournie (correspondant à ce dosage).
Ce médicament NE DOIT PAS ETRE UTILISÉ dans les cas suivants :
· hypersensibilité à la substance active ou à l'un des excipients mentionnés à la rubrique 6.1,
· en association avec :
o l'ergotamine et la dihydroergotamine,
o le pimozide,
o l’ivabradine,
o la colchicine,
(voir rubrique 4.5).
4.4. Mises en garde spéciales et précautions d'emploi
Des effets indésirables cutanés sévères à type de nécrolyse épidermique toxique et de syndrome de Stevens-Johnson ont été rapportés chez certains patients sous josamycine. En cas de survenue d'effets indésirables cutanés sévères, la josamycine doit être arrêtée et un traitement et/ou des mesures adapté(e)s doivent être instauré(e)s.
En cas d'insuffisance hépatique, l'administration de josamycine n'est pas recommandée. Si elle est nécessaire, elle justifie alors une surveillance régulière des tests hépatiques et éventuellement une réduction de posologie.
Des cas de colite pseudomembraneuse ont été rapportés avec la josamycine (voir rubrique 4.8) ; il est donc important d'évoquer ce diagnostic chez les patients présentant une diarrhée sévère pendant ou après un traitement par josamycine. Dans cette situation, des mesures thérapeutiques adéquates doivent être initiées immédiatement. Les médicaments inhibant le péristaltisme sont contre-indiqués dans cette situation.
Ce médicament est généralement déconseillé en association avec :
· les alcaloïdes de l'ergot de seigle dopaminergiques (bromocriptine, cabergoline, lisuride, pergolide),
· l'halofantrine,
· le tacrolimus.
(voir rubrique 4.5).
L’administration de josamycine doit se faire avec prudence chez les patients présentant une hypersensibilité connue à l’érythromycine ou à d’autres antibiotiques de la famille des macrolides.
Une résistance croisée avec d’autres antibiotiques de la famille des macrolides peut être observée.
Des cas d’arythmie ont été rapportés chez des patients prenant des macrolides, dont la josamycine (voir rubrique 4.8). La josamycine doit être administrée avec prudence chez les patients à haut risque suivants :
· Patients ayant une cardiopathie préexistante ou concomitante, en particulier chez les patients très jeunes (nouveau-né, nourrisson) et âgés.
· Patients ayant d’autres affections (non cardiaques) potentiellement arythmogènes (par ex., troubles/détresse respiratoire(s), déséquilibre électrolytique).
· Patients sous traitement concomitant potentiellement arythmogène (par ex., digoxine).
Ce médicament contient du saccharose. Les patients présentant une intolérance au fructose, un syndrome de malabsorption du glucose et du galactose ou un déficit en sucrase/isomaltase (maladies héréditaires rares) ne doivent pas prendre ce médicament.
Ce médicament contient du parahydroxybenzoate de méthyle et de propyle et peut provoquer des réactions allergiques (éventuellement retardées).
Ce médicament contient moins de 1 mmol (23 mg) de sodium pour 5 ml de suspension buvable, c’est-à-dire qu’il est essentiellement « sans sodium ».
Ce médicament contient également de l’alcool benzylique présent dans l’arôme fraise.
Ce médicament contient 0,001 mg pour 5 ml de suspension buvable. L’alcool benzylique peut provoquer des réactions allergiques.
L’alcool benzylique est associé à un risque d’effets indésirables graves y compris des problèmes respiratoires (appelés « syndrome de suffocation ») chez les jeunes enfants. Ne pas utiliser chez le nouveau-né (jusqu’à 4 semaines) sauf en cas de nécessité uniquement.
Du fait du risque accru en raison de l’accumulation chez les jeunes enfants, ne pas utiliser pendant plus d’une semaine chez les jeunes enfants (moins de 3 ans) sauf en cas de nécessité uniquement.
Les volumes élevés doivent être utilisés avec prudence et en cas de nécessité uniquement, en particulier chez les personnes atteintes d’insuffisance hépatique ou rénale en raison du risque d’accumulation et de toxicité (acidose métabolique).
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
De nombreux cas d'augmentation de l'activité des antivitamines K ont été rapportés chez des patients recevant des antibiotiques. Le contexte infectieux ou inflammatoire marqué, l'âge et l'état général du patient apparaissent comme des facteurs de risque. Dans ces circonstances, il apparaît difficile de faire la part entre la pathologie infectieuse et son traitement dans la survenue du déséquilibre de l'INR. Cependant, certaines classes d'antibiotiques sont davantage impliquées : il s'agit notamment des fluoroquinolones, des macrolides, des cyclines, du cotrimoxazole et de certaines céphalosporines, qui imposent, dans ces conditions, de renforcer la surveillance de l’INR.
Associations contre-indiquées
+ Dihydroergotamine
Ergotisme avec possibilité de nécrose des extrémités (inhibition de l'élimination hépatique de l’alcaloïde de l'ergot de seigle).
+ Ergotamine
Ergotisme avec possibilité de nécrose des extrémités (diminution de l'élimination hépatique de l’ergotamine).
+ Pimozide
Risque majoré de troubles du rythme ventriculaire, notamment de torsades de pointes.
+ Ivabradine
Augmentation des concentrations plasmatiques de l’ivabradine et par conséquent de ses effets indésirables (inhibition de son métabolisme hépatique par la josamycine).
+ Colchicine
Augmentation des effets indésirables de la colchicine aux conséquences potentiellement fatales.
+ Alcaloïdes de l'ergot de seigle dopaminergiques (bromocriptine, cabergoline, lisuride, pergolide)
Augmentation des concentrations plasmatiques du dopaminergique avec accroissement possible de son activité ou apparition de signes de surdosage.
+ Halofantrine
Risque majoré de troubles du rythme ventriculaire, notamment de torsades de pointes.
Si cela est possible, interrompre le macrolide. Si l'association ne peut être évitée, contrôle préalable du QT et surveillance ECG monitorée.
+ Tacrolimus
Augmentation des concentrations sanguines de tacrolimus et de la créatininémie, par inhibition du métabolisme hépatique du tacrolimus par la josamycine.
Associations faisant l'objet de précautions d’emploi
+ Carbamazépine
Augmentation des concentrations plasmatiques de carbamazépine avec signes de surdosage, par diminution de son métabolisme hépatique.
Surveillance clinique et, si besoin, dosage plasmatique et réduction éventuelle de la posologie de la carbamazépine.
+ Ciclosporine
Risque d'augmentation des concentrations sanguines de ciclosporine et de la créatininémie. Dosage des concentrations sanguines de la ciclosporine, contrôle de la fonction rénale et adaptation de la posologie pendant l'association et après l'arrêt du macrolide.
+ Disopyramide
Risque de majoration des effets indésirables du disopyramide : hypoglycémies sévères, allongement de l'intervalle QT et troubles du rythme ventriculaire graves, notamment à type de torsade de pointes.
Surveillance clinique, biologique et électrocardiographique régulière.
+ Antivitamines K
Augmentation de l'effet de l'antivitamine K et du risque hémorragique.
Contrôle plus fréquent de l'INR. Adaptation éventuelle de la posologie de l'antivitamine K pendant le traitement par le macrolide et après son arrêt.
+ Sildénafil
Augmentation des concentrations plasmatiques de sildénafil, avec risque d’hypotension. Débuter le traitement par sildénafil à la dose minimale en cas d’association avec la josamycine.
Associations à prendre en compte
+ Théophylline (et, par extrapolation, aminophylline)
Risque d'augmentation de la théophyllinémie, particulièrement chez l'enfant.
+ Digoxine
Augmentation de la digoxinémie par majoration de son absorption.
Surveillance clinique et éventuellement de la digoxinémie pendant le traitement par josamycine et après son arrêt.
4.6. Fertilité, grossesse et allaitement
Bien que cette présentation soit réservée au nourrisson, les données portant sur la grossesse et l’allaitement sont les suivantes :
Grossesse
Les données cliniques chez la femme enceinte sont limitées. Les études effectuées chez l’animal ont mis en évidence une toxicité sur la reproduction à doses élevées. Il est préférable, par mesure de précaution, d’éviter l’utilisation de la josamycine au cours de la grossesse, sauf si nécessaire.
Le passage de la plupart des macrolides dans le lait maternel est documenté, avec des concentrations dans le lait égales ou supérieures aux concentrations plasmatiques. Cependant, les quantités ingérées par le nouveau-né restent faibles au regard des posologies pédiatriques. Le risque majeur consiste en une modification de la flore intestinale de l’enfant. En conséquence, l’allaitement est possible. En cas de survenue de troubles digestifs chez le nourrisson (candidose intestinale, diarrhée), il est nécessaire d’interrompre l’allaitement (ou le médicament).
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Affections cardiaques
Arythmie (voir rubrique 4.4)
Affections gastro-intestinales
Nausées, vomissements, gastralgies, diarrhée, douleurs abdominales, colite pseudomembraneuse, stomatite (fréquence indéterminée).
Affections de la peau et du tissu sous-cutané
Eruption érythémateuse ou maculopapuleuse, érythème multiforme, dermatose bulleuse, syndrome de Stevens-Johnson, syndrome de Lyell (nécrolyse épidermique toxique).
Affections du système immunitaire
· Réactions d'hypersensibilité à type de prurit, urticaire, œdème de la face, œdème de Quincke (angiœdème), gêne respiratoire, réaction et choc anaphylactique;
· Maladie sérique.
Affections hépatobiliaires
Augmentation des transaminases et phosphatases alcalines, ictère, hépatite cholestatique ou hépatite cytolytique.
Affections vasculaires
Purpura, vascularite cutanée.
Troubles du métabolisme et de la nutrition
Diminution de l’appétit (fréquence indéterminée).
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
Un surdosage avec la josamycine peut entraîner des troubles gastro-intestinaux tels que nausées et diarrhées, et doivent être traités en conséquence.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : ANTIBACTERIENS A USAGE SYSTEMIQUE, code ATC : J01FA07.
Antibiotique antibactérien de la famille des macrolides.
SPECTRE D'ACTIVITE ANTIBACTERIENNE
Les concentrations critiques séparent les souches sensibles des souches de sensibilité intermédiaire et ces dernières, des résistantes :
S ≤ 1 mg/l et R > 4 mg/l
La prévalence de la résistance acquise peut varier en fonction de la géographie et du temps pour certaines espèces. Il est donc utile de disposer d'informations sur la prévalence de la résistance locale, surtout pour le traitement d'infections sévères. Ces données ne peuvent apporter qu'une orientation sur les probabilités de la sensibilité d'une souche bactérienne à cet antibiotique.
Lorsque la variabilité de la prévalence de la résistance en France est connue pour une espèce bactérienne, elle est indiquée dans le tableau ci-dessous :
|
Catégories |
Fréquence de résistance acquise en France (> 10%) (valeurs extrêmes) |
|
ESPÈCES SENSIBLES |
|
|
Aérobies à Gram positif |
|
|
Bacillus cereus |
|
|
Corynebacterium diphtheriae |
|
|
Entérocoques |
50 - 70 % |
|
Rhodococcus equi |
|
|
Staphylococcus méti-S |
|
|
Staphylococcus méti-R * |
70 - 80 % |
|
Streptococcus B |
|
|
Streptococcus non groupable |
30 - 40 % |
|
Streptococcus pneumoniae |
35 - 70 % |
|
Streptococcus pyogenes |
16 – 31 % |
|
|
|
|
Aérobies à Gram négatif |
|
|
Bordetella pertussis |
|
|
Branhamella catarrhalis |
|
|
Campylobacter |
|
|
Legionella |
|
|
Moraxella |
|
|
|
|
|
Anaérobies |
|
|
Actinomyces |
|
|
Bacteroides |
30 - 60 % |
|
Eubacterium |
|
|
Mobiluncus |
|
|
Peptostreptococcus |
30 - 40 % |
|
Porphyromonas |
|
|
Prevotella |
|
|
Propionibacterium acnes |
|
|
|
|
|
Autres |
|
|
Borrelia burgdorferi |
|
|
Chlamydia |
|
|
Coxiella |
|
|
Leptospires |
|
|
Mycoplasma pneumoniae |
|
|
Treponema pallidum |
|
|
|
|
|
ESPÈCES MODÉRÉMENT SENSIBLES |
|
|
(in vitro de sensibilité intermédiaire) |
|
|
|
|
|
Aérobies à Gram négatif |
|
|
Neisseria gonorrhoeae |
|
|
Anaérobies |
|
|
Clostridium perfringens |
|
|
Autres |
|
|
Ureaplasma urealyticum |
|
|
|
|
|
ESPÈCES RÉSISTANTES |
|
|
|
|
|
Aérobies à Gram positif |
|
|
Corynebacterium jeikeium |
|
|
Nocardia asteroïdes |
|
|
Aérobies à Gram négatif |
|
|
Acinetobacter |
|
|
Entérobactéries |
|
|
Haemophilus |
|
|
Pseudomonas |
|
|
Anaérobies |
|
|
Fusobacterium |
|
|
Autres |
|
|
Mycoplasma hominis |
|
La josamycine possède une activité in vitro et in vivo sur Toxoplasma gondii.
* La fréquence de résistance à la méticilline est environ de 30 à 50 % de l'ensemble des staphylocoques et se rencontre surtout en milieu hospitalier.
5.2. Propriétés pharmacocinétiques
Prise par voie orale, la josamycine est absorbée rapidement au niveau de la partie initiale de l'intestin grêle.
Distribution
Le pic sérique est obtenu entre 1 et 4 heures après la prise orale. La concentration plasmatique maximale atteint 0,2 à 0,3 mg/l après absorption de 1 g de josamycine base et 0,3 à 0,4 mg/l après absorption de 1 g de propionate de josamycine.
La pharmacocinétique de la josamycine après dose unique comme à l'équilibre, montre une grande variabilité inter et intra individuelle. Ainsi, sa Cmax peut varier dans un rapport de 1 à 7 pour le propionate et de 1 à 10 pour la forme base. Le degré de variation est du même ordre pour l'AUC.
La josamycine présente une très forte affinité tissulaire qui se traduit par une diffusion rapide vers les parenchymes notamment dans les poumons et les végétations adénoïdes. Les concentrations tissulaires sont élevées : après administration de 1 g de josamycine en doses multiples, les valeurs médianes atteignent 1,4 microgrammes/gramme pour une moyenne de 3,4 microgrammes/gramme dans le parenchyme pulmonaire, et de 0,7 microgrammes/gramme pour les valeurs médianes et moyennes comparables dans les végétations adénoïdes.
Il faut noter une pénétration de la josamycine dans la plupart des tissus et milieux biologiques tels que les sinus, la prostate, les amygdales, les sécrétions bronchiques, le pus de l'oreille, la salive, la sueur et les larmes.
Les macrolides pénètrent et s'accumulent dans les phagocytes (polynucléaires neutrophiles, monocytes, macrophages péritonéaux et alvéolaires).
Les concentrations intra-phagocytaires sont élevées chez l'homme. Ces propriétés expliquent l'activité de la josamycine sur les bactéries intracellulaires.
Le passage transplacentaire de la josamycine est faible. La josamycine diffuse très bien dans le lait maternel avec un rapport lait maternel/plasma de 100 %. La josamycine ne diffuse pas dans le liquide céphalo-rachidien.
La liaison aux protéines plasmatiques est de l'ordre de 15 %.
Biotransformation
La biotransformation s'effectue au niveau du foie et ne concerne que 40 à 50 % de la josamycine absorbée.
Les 2 principaux métabolites, qui sont des métabolites hydroxylés, conservent la même activité bactériologique sur le plan qualitatif.
Élimination
L'élimination est principalement digestive : bile et fèces pour 90 % environ.
L'élimination urinaire est très faible (< 10 %).
La demi-vie d'élimination est de l'ordre de 2 heures.
5.3. Données de sécurité préclinique
Dans des études chez des souris et des rates portant sur l’administration de propionate de josamycine au cours de l’organogénèse, un ralentissement de la prise de poids et une splénomégalie ont été rapportés à des doses élevées (2,0 g/kg/jour) chez la souris femelle gravide.
5 ans.
Après reconstitution, la durée de conservation de la suspension est de 7 jours.
6.4. Précautions particulières de conservation
Flacon non-ouvert : pas de précautions particulières de conservation.
Pour les conditions de conservation du médicament après reconstitution, voir rubrique 6.3.
6.5. Nature et contenu de l'emballage extérieur
15 g en flacon (verre) correspondant à 60 ml de suspension reconstituée avec une seringue pour administration orale.
20 g en flacon (verre) correspondant à 80 ml de suspension reconstituée avec une seringue pour administration orale.
25 g en flacon (verre) correspondant à 100 ml de suspension reconstituée avec une seringue pour administration orale.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Pas d’exigences particulières.
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
9 PLACE MARIE-JEANNE BASSOT
92300 LEVALLOIS-PERRET
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 323 062 8 2 : 15 g en flacon (verre) correspondant à 60 ml de suspension reconstituée + seringue pour administration orale.
· 34009 323 063 4 3 : 20 g en flacon (verre) correspondant à 80 ml de suspension reconstituée + seringue pour administration orale.
· 34009 323 064 0 4 : 25 g en flacon (verre) correspondant à 100 ml de suspension reconstituée + seringue pour administration orale.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I.
Ce médicament n'est ou ne sera bientôt plus disponible sur le marché.
Si vous prenez actuellement ce médicament, il vous est recommandé d'en parler avec votre médecin
ou avec votre pharmacien qui pourra vous orienter vers un autre traitement.
ANSM - Mis à jour le : 14/05/2024
JOSACINE 125 mg/5 ml, 250 mg/5 ml, 500 mg/5 ml
Granulés pour suspension buvable
Josamycine
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que JOSACINE, granulés pour suspension buvable et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant de prendre JOSACINE, granulés pour suspension buvable ?
3. Comment prendre JOSACINE, granulés pour suspension buvable ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver JOSACINE, granulés pour suspension buvable ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE JOSACINE, granulés pour suspension buvable ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : ANTIBACTERIENS A USAGE SYSTEMIQUE - code ATC : J01FA07.
Ce médicament est un antibiotique antibactérien de la famille des macrolides.
Ce médicament est utilisé pour traiter ou prévenir certaines infections dues à des bactéries et sur lesquelles la substance active (la josamycine) a un effet.
JOSACINE existe en plusieurs formes et dosages. La forme "granulés pour suspension buvable" est spécialement adaptée pour l'enfant et existe en 3 dosages : 125 mg/5 ml, 250 mg/5 ml et 500 mg/5 ml.
Le dosage à utiliser dépend du poids de votre enfant :
Le dosage "JOSACINE 125 mg/5 ml" est réservé au nourrisson pesant entre 2 et 5 kg.
Le dosage "JOSACINE 250 mg/5 ml" est réservé à l'enfant pesant entre 5 et 10 kg.
Le dosage "JOSACINE 500 mg/5 ml" est réservé à l'enfant pesant entre 10 et 40 kg.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT DE PRENDRE JOSACINE, granulés pour suspension buvable ?
Ne prenez jamais JOSACINE, granulés pour suspension buvable :
· si vous êtes allergique à la substance active (la josamycine) ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
· En association avec :
o l'ergotamine et la dihydroergotamine (utilisés pour traiter la migraine),
o le pimozide (utilisé pour traiter certains troubles psychiatriques),
o l’ivabradine (médicament utilisé dans l’angor),
o la colchicine (médicament utilisé pour le traitement de la crise de goutte).
(voir rubrique « Prise d’autres médicaments »).
Avertissements et précautions
Faites attention avec JOSACINE, granulés pour suspension buvable :
· Avant le traitement, vous devez informer votre médecin si vous avez une maladie du foie.
· Si vous êtes allergique à l’érythromycine ou à d’autres antibiotiques de la famille des macrolides.
· Des troubles du rythme cardiaque ont été rapportés avec la josamycine. Avant de prendre la josamycine, avertissez votre médecin ou votre pharmacien si vous avez des problèmes cardiaques (par ex. maladie cardiaque, trouble du rythme cardiaque), avez une affection susceptible de causer des troubles du rythme cardiaque (par ex., maladie respiratoire, taux de potassium anormal, faible taux de magnésium), prenez un médicament susceptible de causer des troubles du rythme cardiaque (par ex., digoxine), ou si vous ou le patient êtes âgés de moins d’1 an ou de plus de 65 ans et avez des problèmes cardiaques.
· Ce médicament contient moins de 1 mmol (23 mg) de sodium pour 5 ml de suspension buvable, c’est-à-dire qu’il est essentiellement « sans sodium ».
· Les patients présentant une intolérance au fructose, un syndrome de malabsorption du glucose et du galactose ou un déficit en sucrase/isomaltase (maladies héréditaires rares) ne doivent pas prendre ce médicament.
· Si votre médecin vous a informé(e) que vous avez une intolérance à certains sucres, contactez votre médecin avant de prendre ce médicament.
· Ce médicament contient du parahydroxybenzoate de méthyle et de propyle et peut provoquer des réactions allergiques (éventuellement retardées).
Pendant ou après le traitement, vous devez contacter immédiatement votre médecin :
· Si vous avez des diarrhées sévères, persistantes et/ou sanglantes (colites pseudo-membraneuses), vous devez contacter immédiatement votre médecin. Il sera peut-être nécessaire d'arrêter ce médicament et de prendre un traitement spécifique prescrit par votre médecin.
· Si vous présentez des symptômes de réaction allergique ou cutanée lors de la prise de Josacine, vous devez contacter immédiatement votre médecin.
Adressez-vous à votre médecin ou pharmacien avant de prendre JOSACINE, granulés pour suspension buvable.
Enfants et adolescents
Sans objet.
Autres médicaments et JOSACINE, granulés pour suspension buvable
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
Josacine peut possiblement majorer le risque d’effets indésirables de certains autres médicaments en augmentant la quantité de ces médicaments dans le sang. N’oubliez pas d’indiquer à votre médecin tous les médicaments que vous prenez (obtenus sur et sans ordonnance).
Ce médicament NE DOIT GENERALEMENT PAS ETRE UTILISÉ, sauf avis contraire de votre médecin, en même temps que :
· le pergolide (médicament utilisé dans la maladie de Parkinson),
· la bromocriptine, la cabergoline et le lisuride (médicaments utilisés dans la maladie de Parkinson ou en cas d'augmentation dans le sang de l'hormone prolactine régulant notamment la sécrétion de lait),
· l'halofantrine (médicament utilisé dans le traitement du paludisme),
· le tacrolimus (médicament immunosuppresseur utilisé par voie générale lors d’une greffe d’organe).
Ce médicament DOIT ETRE UTILISÉ AVEC PRUDENCE, lorsqu’il est pris en même temps que :
· le disopyramide (médicament utilisé dans la prévention de certains troubles du rythme cardiaque),
· la digoxine (médicament utilisé dans le traitement de certains troubles cardiaques incluant l’insuffisance cardiaque ou les battements irréguliers du cœur).
JOSACINE, granulés pour suspension buvable avec des aliments et boissons
Sans objet.
Bien que cette présentation soit réservée à l’enfant, les données portant sur la grossesse et l’allaitement sont les suivantes :
Grossesse
Si vous êtes enceinte ou si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament. Par mesure de précaution, il est préférable d’éviter l’utilisation de la josamycine au cours de la grossesse, sauf si nécessaire.
Allaitement
L’allaitement est possible en cas de traitement par ce médicament. Toutefois, si des troubles digestifs (diarrhée, candidose) apparaissent chez votre enfant, stoppez l’allaitement maternel consultez rapidement votre médecin.
Demandez conseil à votre médecin ou à votre pharmacien avant de prendre tout médicament.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
Conduite de véhicules et utilisation de machines
Sans objet.
JOSACINE, granulés pour suspension buvable contient du parahydroxybenzoate de méthyle (E218) et du parahydroxybenzoate de propyle (E216) et peut provoquer des réactions allergiques.
JOSACINE, granulés pour suspension buvable contient du sodium.
Ce médicament contient moins de 1 mmol (23 mg) de sodium pour 5 ml de suspension buvable, c’est-à-dire qu’il est essentiellement « sans sodium ».
JOSACINE, granulés pour suspension buvable contient une faible quantité d’alcool benzylique.
Ce médicament contient 0,001 mg (125 mg – 250 mg) ou 0,0013 mg (500 mg) pour 5 ml de suspension buvable. L’alcool benzylique peut provoquer des réactions allergiques.
L’alcool benzylique est associé à un risque d’effets secondaires graves y compris des problèmes respiratoires (appelés « syndrome de suffocation ») chez les jeunes enfants. Ne pas utiliser chez le nouveau-né (jusqu’à 4 semaines) sauf recommandation contraire de votre médecin.
Ne pas utiliser pendant plus d’une semaine chez les jeunes enfants (moins de 3 ans), sauf avis contraire de votre médecin ou de votre pharmacien.
Demandez conseil à votre médecin ou à votre pharmacien si vous souffrez d’une maladie du foie ou du rein. De grandes quantités d’alcool benzylique peuvent s’accumuler dans votre corps et entraîner des effets secondaires (appelés « acidose métabolique »).
3. COMMENT PRENDRE JOSACINE, granulés pour suspension buvable ?
La seringue graduée fournie est spécifique à ce médicament et adaptée au poids du patient. N’utilisez pas un dispositif d’administration autre que la seringue graduée fournie correspondant à votre dosage (seringue, cuillère ou pipette d’un autre médicament) (uniquement pour les formes suspension buvable).
Posologie
Respectez toujours la dose indiquée par votre médecin. En cas de doute, consultez votre médecin ou votre pharmacien.
A titre d'information :
· La dose recommandée est de 50 mg par kg de poids et par jour, à répartir en 2 prises par jour, sans dépasser 1 g le matin et 1 g le soir. Soit en pratique : 1 prise (25 mg/kg) le matin et 1 prise (25 mg/kg) le soir.
· Dans le cas particulier du traitement de certaines angines, vous devrez prendre ce traitement durant 5 jours à 50 mg/kg/jour à répartir en 2 prises par jour. Soit en pratique : 1 prise (25 mg/kg) le matin et 1 prise (25 mg/kg) le soir.
Si vous avez l'impression que l'effet de JOSACINE, granulés pour suspension buvable est trop fort ou trop faible, consultez votre médecin ou votre pharmacien.
Mode d’administration
Ce médicament est utilisé par voie orale.
Avant de prendre ce médicament, vous devez ajouter de l'eau dans le flacon jusqu'au trait circulaire gravé dans le verre du flacon.
Ce médicament s'administre avec une seringue à utiliser oralement. La seringue est graduée en kg de poids corporel (les graduations figurent sur le piston de la seringue).
Préparation de la suspension
1) Agitez le flacon pour homogénéiser la poudre.
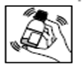
2) Ajoutez de l’eau jusqu’au trait circulaire gravé dans le verre du flacon.
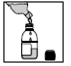
3) Agitez jusqu’à obtention d’un liquide homogène.
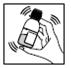
4) Laissez reposer pendant quelques minutes pour bien visualiser le niveau du liquide.
5) Complétez avec de l’eau de manière à amener le niveau du liquide à présent visible jusqu’au trait circulaire gravé dans le verre du flacon. La mousse qui s’est formée doit alors se trouver au-dessus de ce trait.
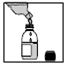
6) Agitez de nouveau, la suspension est prête à l’emploi.
Après ouverture du flacon et reconstitution de la suspension, la durée de conservation de la suspension est de 7 jours.
Administration du médicament
1) Plongez la seringue dans le flacon en ayant vérifié que le piston est bien enfoncé.
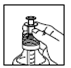
2) Tirez sur le piston pour aspirer la suspension, jusqu’au trait correspondant au poids de l’enfant.
Si le poids de l’enfant dépasse celui indiqué sur les graduations de la seringue, complétez en prélevant la quantité manquante.
JOSACINE 500 mg/5 ml, granulés pour suspension buvable : Pour un enfant pesant 30 kg, prélevez une première fois jusqu’à la graduation 20 kg puis prélevez une seconde fois jusqu’à la graduation 10 kg.
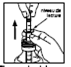
3) Après utilisation, refermez le flacon et rincez la seringue avec de l’eau.

4) Enlevez la pellicule de protection du support de la seringue et coller le support sur le côté du flacon.

5) Replacez la seringue dans son support fixé sur le flacon.
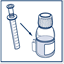
Attention, cette seringue pour administration orale ne doit pas être utilisée pour un autre médicament, la graduation étant spécifique à ce produit.
Durée du traitement
Pour être efficace, cet antibiotique doit être utilisé régulièrement aux doses prescrites et aussi longtemps que votre médecin vous l'aura conseillé.
La disparition de la fièvre ou de tout autre symptôme, ne signifie pas que votre enfant est complètement guéri.
L'éventuelle impression de fatigue n'est pas due au traitement antibiotique mais à l'infection elle-même. Le fait de réduire ou de suspendre votre traitement serait sans effet sur cette impression et retarderait la guérison.
Si vous avez pris plus de JOSACINE, granulés pour suspension buvable que vous n’auriez dû :
Cela peut entraîner des effets gastro-intestinaux comme des nausées ou des diarrhées qui doivent être traités.
Consultez immédiatement votre médecin ou votre pharmacien.
Si vous oubliez de prendre JOSACINE, granulés pour suspension buvable
Ne prenez pas de dose double pour compenser la dose que vous avez oubliée de prendre.
Si vous arrêtez de prendre JOSACINE, granulés pour suspension buvable
Sans objet.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
· Effets digestifs : nausées, vomissements, maux d'estomac, diarrhée, douleur au ventre, colite pseudo-membraneuse (diarrhée sévère, persistante et/ou sanglante), inflammation de la muqueuse de la bouche (stomatite).
· Effets sur la peau : éruptions, rougeurs, lésions sur la peau avec des bulles, décollement de la peau pouvant rapidement s'étendre de façon très grave à tout le corps (syndromes de Lyell et de Stevens-Johnson appelés également nécrolyse épidermique toxique).
· Effets généraux (manifestations allergiques) : réactions allergiques telles que des démangeaisons, un urticaire, un gonflement du visage, un brusque gonflement du visage et du cou (œdème de Quincke), des difficultés pour respirer, une réaction ou un choc d'origine allergique généralisé avec chute de la tension artérielle, une maladie sérique (maladie due à une réaction allergique avec fièvre et douleurs articulaires).
· Effets sur le foie : perturbation des résultats d'analyse évaluant le fonctionnement du foie (élévation de certaines enzymes du foie : transaminases ASAT-ALAT, phosphatases alcalines), jaunisse (reconnaissable par des taches sur la peau et un fond de l'œil jaune), une inflammation du foie (hépatite).
· Effets sur les vaisseaux sanguins : purpura (« bleus » ou petites taches rouges sur la peau), vascularite (inflammation des vaisseaux).
· Effets sur le métabolisme et la nutrition : diminution de l’appétit.
· Effets sur le cœur : arythmie (battements irréguliers du cœur).
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: https://signalement.social-sante.gouv.fr/.
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER JOSACINE, granulés pour suspension buvable ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’emballage après {EXP}. La date de péremption fait référence au dernier jour de ce mois.
Après ouverture du flacon et reconstitution de la suspension, la durée de conservation de la suspension est de 7 jours.
Ne pas conserver le flacon après la fin de traitement pour lequel il a été prescrit.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient JOSACINE, granulés pour suspension buvable
· La substance active est :
JOSACINE 125 mg/5 ml, granulés pour suspension buvable
Josamycine base................................................................................................................. 125 mg
(Sous forme de propionate de josamycine). Pour 5 ml de suspension reconstituée.
JOSACINE 250 mg/5 ml, granulés pour suspension buvable
Josamycine base................................................................................................................. 250 mg
(Sous forme de propionate de josamycine). Pour 5 ml de suspension reconstituée.
JOSACINE 500 mg/5 ml, granulés pour suspension buvable
Josamycine base................................................................................................................. 500 mg
(Sous forme de propionate de josamycine). Pour 5 ml de suspension reconstituée.
· Les autres composants sont :
Mannitol, citrate trisodique, hydroxypropylcellulose, cellulose microcristalline/carmellose (AVICEL RC), parahydroxybenzoate de méthyle (E218), parahydroxybenzoate de propyle (E216), arôme fraise en poudre (citrate de triéthyle; alcool benzylique; propylène glycol; butyrate d'éthyle; 3-hexenol; acide propionique; cinnamate de méthyle; acide acétique; maltol; vanilline; acide méthylbutyrique; caproate d'éthyle; décalactone; maltodextrine), siméticone, sucre glace amylacé à 3%, canthaxanthine à 10% hydrosoluble (pour JOSACINE 250 mg/5 ml, granulés pour suspension buvable) et bêta-carotène à 10% hydrosoluble (pour JOSACINE 500 mg/5 ml, granulés pour suspension buvable). Voir rubrique 2 pour plus d’informations.
Qu’est-ce que JOSACINE, granulés pour suspension buvable et contenu de l’emballage extérieur
Ce médicament se présente sous forme de granulés pour suspension buvable. Boîte de 1 flacon et 1 seringue pour administration orale.
Josacine 125 mg/5 ml, granulés pour suspension buvable
Fins granulés blancs avec une odeur de fraise.
- 15 g dans un flacon en verre, correspondant à 60 ml de suspension reconstituée, avec une seringue pour administration orale.
- 20 g dans un flacon en verre, correspondant à 80 ml de suspension reconstituée, avec une seringue pour administration orale.
- 25 g dans un flacon en verre, correspondant à 100 ml de suspension reconstituée, avec une seringue pour administration orale.
Josacine 250 mg/5 ml, granulés pour suspension buvable
Fins granulés roses avec une odeur de fraise.
- 15 g dans un flacon en verre, correspondant à 60 ml de suspension reconstituée, avec une seringue pour administration orale.
- 20 g dans un flacon en verre, correspondant à 80 ml de suspension reconstituée, avec une seringue pour administration orale.
- 25 g dans un flacon en verre, correspondant à 100 ml de suspension reconstituée, avec une seringue pour administration orale.
Josacine 500 mg/5 ml, granulés pour suspension buvable
Fins granulés jaunes avec une odeur de fraise.
- 20 g dans un flacon en verre, correspondant à 60 ml de suspension reconstituée, avec une seringue pour administration orale.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
9 PLACE MARIE-JEANNE BASSOT
92300 LEVALLOIS-PERRET
Exploitant de l’autorisation de mise sur le marché
ASTELLAS PHARMA
9 PLACE MARIE-JEANNE BASSOT
92300 LEVALLOIS-PERRET
29, AVENUE CHARLES DE GAULLE
69230 SAINT GENIS LAVAL
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
CONSEIL D’EDUCATION SANITAIRE :
QUE SAVOIR SUR LES ANTIBIOTIQUES ?
Les antibiotiques sont efficaces pour combattre les infections dues aux bactéries. Ils ne sont pas efficaces contre les infections dues aux virus.
Aussi, votre médecin a choisi de vous prescrire cet antibiotique parce qu’il convient précisément à votre cas et à votre maladie actuelle.
Les bactéries ont la capacité de survivre ou de se reproduire malgré l’action d’un antibiotique. Ce phénomène est appelé résistance : il rend certains traitements antibiotiques inactifs.
La résistance s’accroît par l’usage abusif ou inapproprié des antibiotiques.
Vous risquez de favoriser l’apparition de bactéries résistantes et donc de retarder votre guérison ou même de rendre inactif ce médicament, si vous ne respectez pas :
· la dose à prendre,
· les moments de prise,
· et la durée de traitement.
En conséquence, pour préserver l’efficacité de ce médicament :
1. N’utilisez un antibiotique que lorsque votre médecin vous l’a prescrit.
2. Respectez strictement votre ordonnance.
3. Ne réutilisez pas un antibiotique sans prescription médicale même si vous pensez combattre une maladie apparemment semblable.
4. Ne donnez jamais votre antibiotique à une autre personne, il n’est peut-être pas adapté à sa maladie.
5. Une fois votre traitement terminé, rapportez à votre pharmacien toutes les boîtes entamées pour une destruction correcte et appropriée de ce médicament.