Dernière mise à jour le 30/03/2026
FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé
Indications thérapeutiques
Formoair est un médicament à inhaler qui délivre son principe actif directement dans les poumons, là où il est nécessaire. Formoair est indiqué dans le traitement des symptômes que sont la respiration sifflante et l'essoufflement chez les patients souffrant d'asthme modéré à sévère. Son principe actif, le fumarate de formotérol, appartient à un groupe de médicaments appelés bronchodilatateurs: ils facilitent la respiration en s'opposant à la contraction excessive des bronches. Formoair pris de façon régulière avec des corticoïdes (oraux ou inhalés), aide à prévenir la survenue des troubles respiratoires sur le long terme.
Formoair peut également être utilisé pour soulager les symptômes tels que la toux, les sifflements et l'essoufflement des patients souffrant de bronchopneumopathie chronique obstructive (BPCO) nécessitant un traitement de longue durée par bronchodilatateurs.
Présentations
> flacon(s) pressurisé(s) aluminium de 100 doses avec valve(s) doseuse(s)
Code CIP : 369 512-6 ou 34009 369 512 6 6
Déclaration de commercialisation : 04/09/2006
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 28,03 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 29,05 €
- Taux de remboursement :65%
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 09/11/2016 | Renouvellement d'inscription (CT) | Le service médical rendu par FORMOAIR reste important dans les indications de l’AMM. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 06/02/2008 | Extension d'indication | FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé n'apporte pas d'amélioration du service médical rendu (ASMR V) par rapport aux autres bronchodilatateurs de longue durée d'action disponibles dans cette indication. |
| V (Inexistant) | Avis du 15/02/2006 | Inscription (CT) | FORMOAIR 12 µg/dose, solution pour inhalation en flacon pressurisé, n’apporte pas d’amélioration du service médical rendu (niveau V) par rapport à FORADIL 12 µg, poudre pour inhalation. |
ANSM - Mis à jour le : 16/01/2025
FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Fumarate de formotérol dihydraté.......................................................................... 12 microgrammes
Pour une dose mesurée.
La dose délivrée à l'embout buccal est de 10,1 microgrammes.
Excipient à effet notoire : éthanol anhydre.
FORMOAIR 12 microgrammes/dose contient une faible quantité d’alcool (éthanol), 8.9 mg par inhalation ce qui équivaut à 0.25 mg/kg pour la dose de deux inhalations par jour chez l’adulte et équivaut à 0,44 mg/kg pour la dose de deux inhalations par jour chez l’adolescent.
Pour la liste complète des excipients, voir rubrique 6.1.
Solution pour inhalation en flacon pressurisé.
4.1. Indications thérapeutiques
La corticothérapie associée devra être maintenue en prises régulières.
Traitement symptomatique de l'obstruction bronchique au cours de la bronchopneumopathie chronique obstructive.
4.2. Posologie et mode d'administration
La posologie est fonction de la sévérité de la maladie.
Le médicament ne devra pas être utilisé plus de 3 mois après la date de dispensation au patient par le pharmacien (voir rubrique 6.4).
Bien que Formoair agisse rapidement, c'est un bronchodilatateur inhalé de longue durée d'action et il doit, par conséquent, être réservé au traitement régulier continu.
ASTHME
Adultes (y compris les sujets âgés) et adolescents âgés de 12 ans et plus
Dose usuelle: une bouffée matin et soir (soit 24 microgrammes de fumarate de formotérol dihydraté par jour).
Dans les cas sévères: jusqu'à deux bouffées matin et soir au maximum (soit 48 microgrammes de fumarate de formotérol dihydraté par jour).
La dose journalière maximale est de 4 bouffées (48 microgrammes de fumarate de formotérol dihydraté).
Enfants âgés de moins de 12 ans
L’efficacité et la tolérance de Formoair chez les enfants âgés de moins de 12 ans n’a pas encore été établie, par conséquent Formoair ne doit pas être utilisé chez ces enfants.
Formoair ne constitue pas le traitement de la crise d'asthme aiguë.
Pour le traitement des crises aiguës d'asthme, il est recommandé d'avoir recours à un bronchodilatateur β2 mimétique par voie inhalée de courte durée d'action.
Les patients devront être avertis de ne pas arrêter ou modifier leur corticothérapie lors de l'instauration du traitement par Formoair.
La persistance ou l'augmentation des symptômes ou leur contrôle insuffisant avec les doses recommandées de Formoair témoignent d'une instabilité de la maladie sous-jacente.
BRONCHOPNEUMOPATHIE CHRONIQUE OBSTRUCTIVE (BPCO)
Adultes (âgés de 18 ans et plus)
La dose usuelle est de 1 inhalation 2 fois par jour (1 inhalation le matin et 1 inhalation le soir, soit 24 microgrammes de fumarate de formotérol par jour).
En traitement continu, la dose journalière ne doit pas dépasser 2 inhalations.
Si besoin, des inhalations supplémentaires peuvent néanmoins être prises occasionnellement pour soulager les symptômes, sans toutefois dépasser une dose totale maximum de 4 inhalations par jour (traitement continu et inhalations supplémentaires comprises). Ne pas dépasser plus de 2 inhalations à chaque prise.
Insuffisance hépatique et rénale
Il n'a pas été réalisée d'étude clinique dans ces populations, néanmoins, les données existantes ne suggèrent pas la nécessité d'un ajustement de la posologie en cas d'insuffisance rénale ou hépatique.
Mode d’administration
Afin de limiter le risque d'erreur de manipulation du dispositif par le patient, il est utile que le médecin ou un professionnel de santé s'assure que celui-ci utilise correctement l'inhalateur.
Avant la première utilisation de l'inhalateur et après trois jours ou plus de non utilisation, une bouffée sera libérée dans l'air pour assurer le bon fonctionnement du dispositif.
Dans la mesure du possible, les patients doivent être en position verticale, debout ou assis, quand ils actionnent l'inhalateur.
1. Retirer le capuchon protecteur de l'embout buccal.
2. Expirer hors du dispositif aussi profondément que possible.
3. Tenir la cartouche verticalement, en dirigeant le fond vers le haut, et introduire l'embout buccal entre les lèvres bien serrées.
4. Inspirer profondément par la bouche tout en appuyant sur le fond de la cartouche (en haut) afin de libérer une bouffée.
5. Retenir son souffle aussi longtemps que possible sans effort et, pour terminer, retirer l'inhalateur de la bouche.
Si une autre bouffée doit être inhalée, maintenir l'inhalateur en position verticale pendant environ 30 secondes puis répéter les étapes 2 à 5.
Toujours refermer après emploi à l'aide du capuchon protecteur.
IMPORTANT: les étapes 2 à 4 ne doivent pas être effectuées trop rapidement.
Si une partie du gaz s'échappe de la partie supérieure de l'inhalateur ou du côté de l'embout buccal, recommencez à partir de l'étape 2.
Chez les patients dont la capacité de préhension est défaillante, l'inhalateur sera tenu avec les deux mains. Dans ce cas, la partie supérieure de l'inhalateur sera maintenue entre les deux index et la partie inférieure entre les deux pouces.
En cas de difficulté pour le patient de synchroniser l'inspiration avec le déclenchement de l'appareil, une chambre d'inhalation devra être utilisée. Néanmoins, aucune donnée clinique n'est disponible concernant l'emploi de Formoair avec une chambre d'inhalation.
Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1.
4.4. Mises en garde spéciales et précautions d'emploi
Formoair ne devra pas être utilisé (et n’est pas suffisant) en traitement de première intention dans l’asthme.
Les patients asthmatiques nécessitant un traitement par ß2-agonistes à longue durée d’action doivent également recevoir un traitement anti-inflammatoire d’entretien optimal par corticoïdes. Par conséquent, il doit être conseillé aux patients de continuer de prendre leur traitement anti-inflammatoire après l’introduction du traitement par formotérol même si les symptômes régressent. La persistance des symptômes ou la nécessité d’augmenter le traitement par ß2-agonistes indique une aggravation de la pathologie sous-jacente et doit motiver une réévaluation du traitement d’entretien. Bien que Formoair puisse être introduit comme traitement additionnel lorsque les corticostéroïdes inhalés ne permettent pas un contrôle adéquat des symptômes de l’asthme, un traitement par Formoair ne doit pas être initié au cours d’une exacerbation sévère aigue d’asthme, ou lors d’une aggravation significative ou d’une détérioration aigue de l’asthme.
Des effets indésirables graves liés à l’asthme et des exacerbations peuvent intervenir durant le traitement par Formoair. Les patients devront être informés de la nécessité de continuer leur traitement mais de demander un avis médical si les symptômes de l’asthme demeurent incontrôlés ou empirent après initiation du traitement par Formoair.
Les posologies recommandées devront être respectées (voir rubrique 4.2). Lorsque les symptômes de l’asthme sont contrôlés, une réduction régulière de la dose de Formoair pourra être envisagée. Il est important de revoir régulièrement les patients dont le traitement a été diminué. La dose minimale efficace de Formoair devra être utilisée.
La dose journalière maximale ne doit pas être dépassée.
Un avis médical urgent est requis en cas d'aggravation rapide ou brutale de l'asthme car le pronostic vital peut être engagé à court terme.
L'utilisation de doses unitaires ou quotidiennes significativement plus élevées que celles préconisées devra être évitée en raison de la possibilité d'un retentissement délétère au niveau cardiaque (arythmies, augmentation de la pression artérielle) et de l'apparition de troubles électrolytiques.
Pathologies associées:
La prudence s’impose lors du traitement des patients présentant un bloc auriculo-ventriculaire du troisième degré, un diabète réfractaire, une thyrotoxicose, un phéochromocytome, une cardiomyopathie hypertrophique obstructive, un rétrécissement aortique sous-valvulaire idiopathique, une hypertension sévère, un anévrisme ou toute autre pathologie cardiovasculaire sévère, telle qu’une cardiopathie ischémique, une tachyarythmie ou une insuffisance cardiaque sévère et des vasculopathies occlusives, notamment une artériosclérose.
Le formotérol peut induire un allongement de l’intervalle QTc. Il convient d’être prudent lors du traitement des patients présentant un allongement de l’intervalle QTc, qu’il soit congénital ou induit par un médicament (QTc > 0,44 secondes) et chez les patients traités par des médicaments affectant l’intervalle QTc (voir rubrique 4.5).
En raison des effets hyperglycémiques des ß2-agonistes, une surveillance supplémentaire de la glycémie est recommandée initialement chez les patients diabétiques.
Formoair ne devra pas être administré dans les 12 heures minimum précédent une anesthésie aux anesthésiques halogénés.
Bronchospasme paradoxal
Comme pour tout traitement inhalé, le risque de bronchospasme paradoxal doit être pris en considération. Si un bronchospasme paradoxal se produit, le traitement doit être arrêté immédiatement et un autre traitement doit être instauré (voir rubrique 4.8).
Hypokaliémie
Le traitement par ß2-agoniste peut induire une hypokaliémie potentiellement grave. Il est recommandé d’être particulièrement prudent en cas d’asthme sévère aigu car le risque associé peut être augmenté par l’hypoxie. L’effet hypokaliémant peut être potentialisé par un traitement concomitant par dérivés de xanthine, corticoïdes ou diurétiques. Le taux sanguin de potassium doit donc être surveillé.
Chez les sujets présentant des taux plasmatiques de potassium initialement faibles ou des facteurs de risques associés, la kaliémie sera dosée régulièrement. Cette recommandation vaut même en l'absence d'antécédent d'hypokaliémie lors de traitements antérieurs. Une supplémentation en potassium devra être envisagée si besoin.
Le retentissement des digitaliques est accentué par la baisse de la kaliémie.
La quantité pour la dose de deux inhalations de ce médicament équivaut à moins de 1 ml de bière ou de vin.
La faible quantité d'alcool contenue dans ce médicament n'est pas susceptible d'entraîner d'effet notable
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Aucune étude d’interaction spécifique n’a été réalisée avec le formotérol.
En cas d’administration concomitante d’autres médicaments connus pour allonger l’intervalle QTc, il existe un risque théorique d’interaction pharmacodynamique avec le formotérol et d’augmentation du risque d’arythmie ventriculaire. Ces médicaments incluent, par exemple, certains antihistaminiques (terfénadine, astémizole, mizolastine), certains antiarythmiques (quinidine, disopyramide, procaïnamide), l’érythromycine et les antidépresseurs tricycliques.
L'administration concomitante d'autres substances sympathomimétiques telles que d’autres β2-agonistes ou l’éphédrine peut potentialiser les effets indésirables de Formoair et peut nécessiter une adaptation de la dose.
L'administration concomitante de formotérol et de théophylline potentialise le risque de survenue d'effets indésirables tels que les troubles du rythme. Les substances ayant une activité sympathomimétique intrinsèque, comme la L-dopa, la L-thyroxine, l'ocytocine ou l'alcool, peuvent également interférer sur le système de régulation autonome lorsqu'elles sont administrées en même temps que le formotérol.
La prudence est requise en cas d'association simultanée de Formoair avec les inhibiteurs de la monoamine oxydase ou les antidépresseurs tricycliques, en raison du risque de potentialisation des effets β2 -adrénergiques sur le système cardio-vasculaire.
L'administration concomitante des dérivés de la xanthine, des corticoïdes ou des diurétiques comme des diurétiques thiazidiques et des diurétiques de l’anse peut potentialiser l'effet indésirable hypokaliémiant rare des béta2-agonistes. L'hypokaliémie est susceptible d’augmenter le risque d’arythmies chez les patients recevant des glycosides digitaliques.
Le risque d’arythmie est plus élevé chez les patients recevant une anesthésie concomitante par hydrocarbures halogénés.
Les effets bronchodilatateurs du formotérol peuvent être augmentés par les médicaments anticholinergiques.
Les bêta-bloquants peuvent affaiblir ou inhiber les effets béta-stimulants de Formoair et ne devront donc pas, sauf nécessité absolue, être administrés en même temps (y compris sous forme de collyre).
4.6. Fertilité, grossesse et allaitement
Grossesse
Il n’existe pas de données ou il existe des données limitées sur l'utilisation du formotérol chez la femme enceinte. Dans les études effectuées chez l’animal, le formotérol a provoqué des pertes implantatoires ainsi qu’une diminution de la survie postnatale précoce et du poids de naissance. Les effets sont apparus à des concentrations systémiques considérablement plus importantes que celles atteintes pendant l’utilisation clinique du formotérol. Le traitement par formotérol peut être envisagé à tous les stades de la grossesse s’il est indispensable pour contrôler l’asthme et si les bénéfices attendus pour la mère sont supérieurs aux risques possibles pour le fœtus. Le risque potentiel chez l’humain est inconnu.
On ne sait pas si le formotérol est excrété dans le lait maternel. Chez le rat, de faibles quantités de formotérol ont été détectées dans le lait maternel. L’administration de formotérol chez des femmes qui allaitent ne doit être envisagée que si les bénéfices attendus pour la mère sont supérieurs aux risques possibles pour l’enfant.
Le risque pour les nouveau-nés/nourrissons ne peut être exclu.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Formoair n’a aucun effet sur l’aptitude à conduire des véhicules et à utiliser des machines.
Les événements indésirables les plus fréquents observés sous traitement par β2-agoniste, comme les tremblements et les palpitations, ont tendance à être légers et à disparaître quelques jours après le début du traitement.
Les réactions indésirables associées au formotérol sont présentées ci-dessous par classe de systèmes d’organes et fréquence. La fréquence est définie selon la convention suivante : Très fréquent (≥ 1/10), fréquent (≥1/100, <1/10), peu fréquent (≥1/1000, <1/100), rare (≥1/10 000, <1/1000), très rare (<1/10 000).
|
Classe de systèmes d’organes |
Réaction indésirable |
Fréquence |
|
Affections hématologiques et du système lymphatique |
Thrombopénie |
Très rare |
|
Affections du système immunitaire |
Réaction d’hypersensibilité, par exemple angio-œdème, bronchospasme, exanthème, urticaire, prurit. |
Rare |
|
Troubles du métabolisme et de la nutrition |
Hypokaliémie, hyperglycémie |
Peu fréquent |
|
Affections psychiatriques |
Agitation, impatiences, troubles du sommeil |
Peu fréquent |
|
Comportement anormal, hallucination |
Très rare |
|
|
Affections du système nerveux |
Tremblements, céphalées |
Fréquent |
|
Sensations vertigineuses, troubles du goût |
Peu fréquent |
|
|
Stimulation du système nerveux central |
Très rare |
|
|
Affections cardiaques
|
Palpitations |
Fréquent |
|
Tachycardie |
Peu fréquent |
|
|
Arythmies cardiaques, par exemple, fibrillation auriculaire, tachycardie supraventriculaire, extrasystoles, angor |
Rare |
|
|
Allongement de l’intervalle QTc |
Très rare |
|
|
Affections vasculaires |
Variation de la pression artérielle |
Rare |
|
Affections respiratoires, thoraciques et médiastinales |
Toux |
Fréquent |
|
Irritation de la gorge |
Peu fréquent |
|
|
Bronchospasme paradoxal (voir rubrique 4.4) |
Rare |
|
|
Dyspnée, exacerbation de l’asthme |
Très rare |
|
|
Affections gastro-intestinales |
Nausées |
Peu fréquent |
|
Affections de la peau et du tissu sous-cutané |
Hyperhidrose |
Peu fréquent |
|
Affections musculo-squelettiques et du tissu conjonctif |
Crampes musculaires, myalgies |
Peu fréquent |
|
Affections du rein et des voies urinaires |
Néphrite |
Rare |
|
Troubles généraux et anomalies au site d'administration |
Œdèmes périphériques |
Très rare |
Nausées, dysgueusie, irritation de la gorge, hyperhidrose, agitation, maux de tête, sensations vertigineuses et crampes musculaires peuvent disparaître spontanément au bout de 1 à 2 semaines de traitement.
Une stimulation du système nerveux central, se manifestant par une hyperexcitabilité, a été rapportée sporadiquement après inhalation de ß2-sympathomimétiques. Cet effet a essentiellement été observé chez les enfants jusqu’à l’âge de 12 ans.
Le traitement par ß2-agonistes peut provoquer une augmentation des taux sanguins d’insuline, d’acides gras libres, de glycérol et de corps cétoniques.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/
Traitement du surdosage
Surveillance et traitement symptomatique. L'hospitalisation sera envisagée dans les cas graves.
L'emploi de bêta-bloquants cardiosélectifs est envisageable mais avec une extrême prudence du fait du risque de bronchoconstriction qu'ils induisent. Une surveillance de la kaliémie est recommandée.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Mécanisme d’action et effets pharmacodynamiques
Le formotérol est un bêta2-stimulant sélectif. Il exerce un effet bronchodilatateur chez les patients présentant un syndrome respiratoire obstructif réversible. Après inhalation d'une dose unique, l'effet bronchodilatateur apparaît dans un délai de 1 à 3 minutes. Un effet marqué sur la bronchodilatation persiste encore dans les 12 heures suivant l'inhalation. Chez l'Homme, le formotérol a montré son efficacité dans la prévention du bronchospasme induit par la métacholine.
5.2. Propriétés pharmacocinétiques
Comme avec les autres substances administrées par voie inhalée, 90 % de la dose de formotérol administrée sont déglutis et absorbés au niveau du tractus gastro-intestinal. Les caractéristiques pharmacocinétiques de l'administration par voie orale peuvent ainsi être étendues à l'administration par voie inhalée.
L'absorption est rapide et complète: après l'inhalation d'une dose thérapeutique (12 microgrammes) de solution pour inhalation en flacon pressurisé de Formoair chez des asthmatiques, la concentration plasmatique maximale (Cmax) en formotérol est atteinte au bout d'environ 15 minutes, c'est-à-dire plus rapidement qu'avec une poudre pour inhalation de formotérol. D'une manière générale, il conviendra de prendre en compte le taux d'absorption lors du remplacement d'une formulation de formotérol par une autre.
L'absorption du formotérol est linéaire après l'inhalation de 12 à 96 μg de fumarate de formotérol dihydraté.
Les doses orales allant jusqu'à 300 microgrammes de formotérol sont rapidement absorbées au niveau du tractus gastro-intestinal. La concentration plasmatique maximale de la molécule inchangée est atteinte au bout de 30 minutes à 1 heure. Plus de 65 % d'une dose orale de 80 microgrammes sont absorbés. La linéarité dose-concentration plasmatique est établie dans l'intervalle de doses administrées par voie orale allant de 20 à 300 μg. Du fait d'une demi-vie brève, il n'existe pas d'accumulation après administration quotidienne répétée de doses allant de 40-160 microgrammes. Il n'a pas été mis en évidence de différence significative en fonction du sexe.
Distribution
La liaison aux protéines plasmatiques est de 61 à 64 % (albumine: 34 %); il n'a pas été mis en évidence de saturation des sites de fixation aux doses thérapeutiques.
Biotransformation
Le formotérol est essentiellement métabolisé par glucuronisation directe et est entièrement éliminé. Une autre voie de métabolisation consiste en une O-déméthylation suivie d'une glucuronisation puis élimination complète. Les iso-enzymes du CYP 450: 2D6, 2C19, 2C9 et 2A6, sont impliqués dans le métabolisme du formotérol, et le risque d'interaction médicamenteuse cinétique reste faible. La cinétique du formotérol n'est pas modifiée après administration unique et répétée, éliminant l'éventualité d'un phénomène d'auto-induction ou inhibition du métabolisme.
Elimination
L'élimination du formotérol apparaît comme un processus en plusieurs phases interférant sur la demi-vie retrouvée en fonction du temps. Au vu des concentrations plasmatiques ou sanguines mesurées 6, 8 ou 12 heures après administration orale, la demi-vie d'élimination est estimée à 2 à 3 heures.
La demi-vie calculée sur la base de l'excrétion rénale entre 3 et 16 heures après l'inhalation est de 5 heures.
La substance active et ses métabolites sont entièrement éliminés, les deux tiers d'une dose orale étant éliminés dans les urines et un tiers dans les selles. Après l'inhalation de formotérol, 6 à 9 % de la dose (en moyenne) sont éliminés sous forme inchangée dans les urines. La clairance rénale du formotérol est de 150 ml/min.
5.3. Données de sécurité préclinique
Chez le rat et le chien, les effets du formotérol ont été observés essentiellement au niveau du système cardio-vasculaire et consistaient en une accentuation des effets pharmacologiques connus avec les doses fortes d'agoniste β2.
Une légère réduction de la fertilité a été retrouvée chez les rats mâles exposés aux plus fortes doses.
Les études menées in vitro et in vivo n'ont pas montré d'effets génotoxiques du formotérol. Chez la rate et la souris femelle, on a constaté une légère augmentation de l'incidence des léiomyomes utérins bénins. Cet effet est considéré comme un effet de classe chez les rongeurs, après une exposition prolongée à de fortes doses d'agonistes β2.
Norflurane, éthanol anhydre, acide chlorhydrique.
18 mois.
6.4. Précautions particulières de conservation
A conserver au réfrigérateur (entre 2°C et 8°C) pendant 15 mois au maximum.
Après la remise au patient:
A conserver à une température ne dépassant pas 30°C (pendant 3 mois au maximum).
6.5. Nature et contenu de l'emballage extérieur
50, 100 ou 120 doses en flacon pressurisé (Aluminium) avec valve doseuse, système d'activation et capuchon protecteur.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Pour les pharmacies:
Inscrire sur la boîte la date de remise au patient.
S'assurer qu'il y a bien au moins trois mois entre la date de remise au patient et la date de péremption imprimée sur la boîte.
Tout produit non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
26/A Via Palermo
43122 PARMA
ITALIE
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 374 166 5 8: 50 doses en flacon pressurisé (Aluminium).
· 34009 369 512 6 6: 100 doses en flacon pressurisé (Aluminium).
· 34009 369 513 2 7: 120 doses en flacon pressurisé (Aluminium).
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I
ANSM - Mis à jour le : 16/01/2025
FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé
Fumarate de formotérol dihydraté
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant de prendre FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé ?
3. Comment prendre FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé ET DANS QUELS CAS EST-IL UTILISE ?
Formoair est un médicament à inhaler qui délivre son principe actif directement dans les poumons, là où il est nécessaire. Formoair est indiqué dans le traitement des symptômes que sont la respiration sifflante et l'essoufflement chez les patients souffrant d'asthme modéré à sévère. Son principe actif, le fumarate de formotérol, appartient à un groupe de médicaments appelés bronchodilatateurs: ils facilitent la respiration en s'opposant à la contraction excessive des bronches. Formoair pris de façon régulière avec des corticoïdes (oraux ou inhalés), aide à prévenir la survenue des troubles respiratoires sur le long terme.
Formoair peut également être utilisé pour soulager les symptômes tels que la toux, les sifflements et l'essoufflement des patients souffrant de bronchopneumopathie chronique obstructive (BPCO) nécessitant un traitement de longue durée par bronchodilatateurs.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT DE PRENDRE FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé ?
Ne prenez jamais FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé
· si vous êtes allergique à la substance active ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
Avertissements et précautions
Adressez-vous à votre médecin ou pharmacien avant de prendre FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé:
· si vous souffrez d'une maladie cardiaque sévère, particulièrement si vous avez eu récemment un infarctus du myocarde, une maladie des artères coronaires du cœur (coronaropathie) ou une défaillance sévère du muscle cardiaque (insuffisance cardiaque congestive),
· si vous souffrez de troubles du rythme cardiaque tels qu'une accélération du rythme des battements du cœur (tachycardie), d'une anomalie d'une valve cardiaque ou de certaines anomalies de l'électrocardiogramme ou de toute autre maladie cardiaque,
· si vous avez un rétrécissement de vaisseaux sanguins (vasculopathie occlusive), particulièrement des artères (athérosclérose), ou un élargissement anormal de la paroi d'un vaisseau (anévrisme),
· si votre pression artérielle est élevée (hypertension),
· si le taux de sucre dans votre sang (glycémie) est élevé (diabète),
· si la concentration du potassium dans votre sang est basse (hypokaliémie),
· si votre glande thyroïde est trop active (hyperthyroïdie),
· si vous avez une tumeur de la glande surrénale produisant de l'adrénaline et de la noradrénaline en excès (phéochromocytome),
· si vous avez subi une intervention chirurgicale quelconque ou avez reçu un anesthésique halogéné.
Autres médicaments et FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament même s’il s’agit d’un médicament obtenu sans ordonnance.
Certains médicaments peuvent interférer avec l'action du Formoair, dont notamment:
· les médicaments qui contrôlent les anomalies du rythme cardiaque (anti-arythmiques) tels que la quinidine, le disopyramide, et le procaïnamide,
· les médicaments destinés au traitement des maladies du cœur (digitaliques),
· les médicaments destinés au traitement de la congestion nasale, par exemple éphédrine,
· les médicaments appelés bêta-bloquants utilisés pour le traitement d'affections cardiaques ou du glaucome (augmentation de la pression dans l'œil), sous forme de comprimés ou de collyre,
· les médicaments contenant de l’érythromycine (utilisé pour traiter les infections),
· les médicaments destinés au traitement des troubles dépressifs: inhibiteurs de la monoamine-oxydase (par exemple phénelzine et isocarboxazide) ou antidépresseurs tricycliques (par exemple amitriptyline et imipramine),
· les médicaments destinés au traitement de troubles mentaux sévères (par exemple chlorpromazine et trifluopérazine),
· les médicaments destinés au traitement de réactions allergiques tels que les anti-histaminiques, comme la terfenadine, l’astemizole, la mizolastine,
· les médicaments destinés au traitement de l'asthme tels que la théophylline ou l'aminophylline et les corticoïdes,
· les médicaments destinés à augmenter la production d'urine (diurétiques),
· les médicaments destinés au traitement de la maladie de Parkinson (tels que la lévodopa),
· les médicaments contenant de l'ocytocine, qui induit des contractions de l'utérus,
· les médicaments destinés à traiter une insuffisance d'activité de la glande thyroïde (thyroxine).
L’ajout d’anticholinergiques (comme le bromure de tiotropium ou d’ipratropium) au traitement par Formoair peut aider à ouvrir encore plus vos voies respiratoires.
· Votre médecin vous a également prescrit un médicament à base de corticoïdes pour vos troubles respiratoires. Il est très important de continuer à le prendre régulièrement. N'ARRETEZ PAS de le prendre et ne modifiez pas sa dose quand vous commencez à prendre Formoair.
Sans objet.
Grossesse et allaitement
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
La prise du Formoair au cours d'une grossesse, n'est indiquée que si elle est strictement nécessaire.
Si vous allaitez, parlez-en à votre médecin avant d’utiliser Formoair.
Conduite de véhicules et utilisation de machines
Il est peu probable que Formoair puisse avoir un effet quelconque sur l'aptitude à conduire des véhicules et à utiliser des machines.
FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé contient de l’éthanol anhydre.
.
Formoair contient une faible quantité d’alcool (éthanol), 8.9 mg par inhalation ce qui équivaut à 0.25 mg/kg pour la dose de deux inhalations par jour chez l’adulte et équivaut à 0,44 mg/kg pour la dose de deux inhalations par jour chez l’adolescent.
La quantité pour la dose de deux inhalations de ce médicament équivaut à moins de 1 ml de bière ou de vin.
La faible quantité d'alcool contenue dans ce médicament n'est pas susceptible d'entraîner d'effet notable.
3. COMMENT UTILISER FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé ?
ASTHME
La dose de Formoair que vous devez inhaler dépend du type et de la sévérité de votre asthme.
Votre médecin doit décider de la dose adéquate, et il est important que vous preniez régulièrement uniquement la dose prescrite.
La dose habituelle chez l'adolescent à partir de 12 ans et l'adulte, y compris âgé, est de 12 microgrammes (une bouffée) matin et soir. Vous devez donc inhaler au total 24 microgrammes de formotérol par jour.
Si votre asthme est plus sévère, votre médecin a pu vous prescrire 48 microgrammes de formotérol par jour (quatre bouffées au total, deux le matin et deux le soir).
La dose maximale quotidienne est de 48 microgrammes (4 bouffées) de formotérol, et il est important de ne pas dépasser la dose quotidienne totale prescrite par votre médecin.
Formoair ne convient pas aux enfants de moins de 12 ans.
Formoair n'est pas le traitement d'un essoufflement survenant brutalement. Pour traiter ces crises, vous utiliserez votre traitement de « secours » par inhalation que votre médecin vous aura prescrit à cet effet et le conserverez toujours avec vous.
BRONCHOPNEUMOPATHIE chronique obstructive (BPCO)
Chez les sujets de plus de 18 ans:
La dose usuelle chez l'adulte (de 18 ans et plus) est d'une bouffée le matin et une bouffée le soir. Cela signifie que vous ne devez pas dépasser un total de 2 bouffées par jour (24 microgrammes de Formoair par jour).
Si besoin, des inhalations supplémentaires peuvent néanmoins être prises occasionnellement pour soulager les symptômes, sans toutefois dépasser une dose totale maximum de 4 inhalations par jour (traitement continu et inhalations supplémentaires comprises). Ne pas dépasser plus de 2 inhalations à chaque prise.
Mode d’administration
Il est important que vous sachiez utiliser correctement votre inhalateur. Votre médecin, infirmière ou pharmacien vous montrera comment utiliser correctement votre inhalateur. Vous devez suivre attentivement ses instructions afin de savoir COMMENT et QUAND prendre Formoair et COMBIEN de bouffées inhaler. Cette notice vous donne les instructions à suivre. Si vous avez des doutes sur ce que vous devez faire ou avez des difficultés à inhaler, demander conseil à votre médecin, infirmière ou pharmacien.
Si votre inhalateur est neuf ou n'a pas été utilisé pendant trois jours ou plus, une bouffée doit être libérée dans l'air avant utilisation, afin de s'assurer qu'il fonctionne. Vous devez être en position debout ou assise le buste vertical quand vous utilisez l'inhalateur.
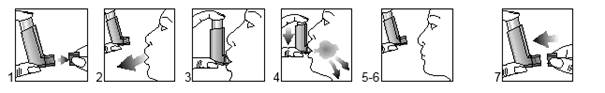
1. Enlevez le capuchon de l'embout buccal de l'inhalateur et tenez l'inhalateur entre le pouce et l'index comme sur l'illustration.
2. Soufflez afin de vider vos poumons au maximum sans ressentir de gêne.
3. Tenez l'inhalateur verticalement, comme sur l'illustration, en plaçant votre pouce sous la base au-dessous de l'embout buccal; placez l'embout dans votre bouche entre vos dents et refermez étroitement vos lèvres tout autour.
4. Inspirez profondément par la bouche et appuyez en même temps sur le haut de l'inhalateur afin de délivrer une bouffée.
5. Retenez votre respiration aussi longtemps que vous n'en éprouvez pas de gêne, puis retirez l'embout de votre bouche.
6. Si vous devez prendre une seconde bouffée, tenez l'inhalateur verticalement et attendez environ 30 secondes avant de refaire les étapes 2 à 5.
7. Après utilisation, remettez toujours le capuchon de l'embout en place afin de protéger ce dernier de la poussière et des particules. Remettez-le en place et appuyez fermement jusqu'au déclic.
|
|
IMPORTANT Effectuez les étapes 2, 3, 4 et 5 sans précipitation.
Il est important que vous commenciez à inspirer aussi lentement que possible immédiatement avant d'appuyer sur l'inhalateur.
Si vous voyez de la «vapeur » sortir du haut de l'inhalateur ou des côtés de votre bouche, vous devez recommencer à partir de l'étape 2.
Si vos mains sont faibles, il peut être plus facile de tenir l'inhalateur avec vos deux mains, en plaçant les deux index sur le sommet de l'inhalateur et les deux pouces sur le fond au-dessous de l'embout.
Si vous éprouvez des difficultés quelconques, parlez-en à votre médecin, infirmière ou pharmacien.
Nettoyage:
Il est important de nettoyer régulièrement votre inhalateur, au moins une ou deux fois par semaine, afin d'assurer son fonctionnement correct.
· Sortez la cartouche en métal du corps en plastique de l'inhalateur et retirez le capuchon de l'embout buccal.
· Rincez le corps en plastique et le capuchon de l'embout à l'eau chaude.
· Ne mettez pas la cartouche en métal dans l'eau.
· Laissez totalement sécher dans un endroit chaud. Evitez toute chaleur excessive.
· Remettez en place la cartouche et le capuchon de l'embout buccal.
Si vous avez pris plus de FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé que vous n’auriez dû
Vous pouvez noter que votre cœur bat plus vite que d'habitude et vous sentir agité. Vous pouvez également avoir des maux de tête, des tremblements, vous sentir ou être nauséeux (nausées et vomissements) ou avoir des somnolences. Appelez votre médecin dès que possible pour avis.
Si vous oubliez de prendre FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé
Prenez-la dès que vous vous apercevez de votre oubli. Prenez la dose suivante au moment habituel. Si c'est presque le moment de la dose suivante, ne prenez pas la dose que vous avez oubliée, prenez juste la dose suivante au moment prévu.
Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre.
Si vous arrêtez de prendre FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé
N'arrêtez pas de prendre Formoair et ne réduisez pas sa dose, et n'arrêtez pas les autres médicaments pour vos troubles respiratoires uniquement parce que vous vous sentez mieux. Consultez votre médecin auparavant. Il est très important de prendre régulièrement ces médicaments.
N'augmentez pas votre dose de Formoair sans consulter votre médecin auparavant.
Si vous vous sentez essoufflés ou que votre respiration devient sifflante durant l’utilisation de Formoair, vous devez continuer à utiliser Formoair mais aller voir votre médecin aussi vite que possible, vous avez peut-être besoin d’un traitement additionnel. Une fois votre asthme contrôlé, votre médecin décidera peut-être de réduire régulièrement la dose de Formoair.
Si vous avez d'autres questions sur l'utilisation de ce médicament, demandez plus d’informations à votre médecin ou votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Les effets indésirables possibles sont mentionnés ci-dessous en fonction de leur fréquence.
Fréquents (survenant chez plus d'un patient sur 100 mais chez moins d'un sur 10)
· battements cardiaques inhabituellement rapides et palpitations, toux, tremblements, maux de tête.
Peu fréquents (survenant chez plus d'un patient sur 1000 mais chez moins d'un sur 100)
· crampes musculaires, douleurs musculaires (myalgies), nausées, agitation, impatiences, troubles du sommeil, étourdissement, anomalie ou altération du goût (dysgueusie), irritation de la gorge, battements cardiaques anormalement rapides (tachycardie), troubles du rythme cardiaque avec accélération des battements cardiaques (tachyarythmie), concentration anormalement basse du potassium dans le sang (hypokaliémie), augmentation du taux de sucre dans le sang (hyperglycémie), augmentation de la concentration sanguine de l'insuline, des acides gras libres, du glycérol et des cétones, sueurs excessives (hyperhidrose).
Rares (survenant chez plus d'un patient sur 10 000 mais chez moins d'un sur 1000)
· Battements cardiaques manquants en raison de la contraction trop précoce des ventricules cardiaques (extrasystoles ventriculaires), sensation de serrement dans la poitrine (angor ou angine de poitrine), augmentation ou diminution de la pression artérielle, respiration sifflante immédiatement après utilisation de l'inhalateur (bronchospasme paradoxal), diminution sévère de la pression artérielle, inflammation des reins (néphrite) , réaction allergique telle que démangeaison, éruption, bronchospasme, urticaire, gonflement de la peau et des muqueuses persistant pendant plusieurs jours (œdème de Quincke), urticaire.
Très rares (survenant chez moins d'un patient sur 10 000)
· Aggravation de l'asthme, difficultés à respirer (dyspnée), gonflement des mains et/ou des pieds (œdème périphérique), battements irréguliers du cœur (fibrillation auriculaire), diminution du nombre des plaquettes sanguines (thrombopénie), hyperexcitabilité, troubles du comportement et hallucinations.
Certains effets indésirables tels que tremblements, nausées, anomalie ou altération du goût, irritation de la gorge, transpiration excessive, agitation, maux de tête, étourdissements et crampes musculaires peuvent disparaître progressivement en une ou deux semaines d'utilisation continue de votre médicament de l'asthme.
Si vous ressentez une aggravation de votre essoufflement ou de votre respiration sifflante, arrêtez le traitement par Formoair et avertissez votre médecin dès que possible. Ces troubles sont dus à un rétrécissement des bronches (bronchospasme), mais surviennent très rarement.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: https://signalement.social-sante.gouv.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’étiquette. La date de péremption fait référence au dernier jour de ce mois.
Pour le pharmacien:
A conserver au réfrigérateur (entre 2°C et 8°C) pendant 15 mois au maximum.
Après la remise au patient:
Le médicament devra être conservé à une température ne dépassant pas 30°C (pendant 3 mois au maximum).
Ce médicament devra être utilisé dans les 3 mois maximum qui suivent la délivrance par le pharmacien en veillant à ne pas dépasser la date de péremption imprimée sur le carton.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient FORMOAIR 12 microgrammes/dose, solution pour inhalation en flacon pressurisé
· La substance active est :
Fumarate de formotérol dihydraté......................................................................... 12 microgrammes.
Pour une dose mesurée.
La dose délivrée à l'embout buccal est de 184 microgrammes de budésonide.
· Les autres composants sont :
Norflurane, éthanol anhydre, acide chlorhydrique. (Chaque bouffée contient 9 mg d’éthanol).
Ce médicament contient des gaz à effet de serre fluorés.
Chaque inhalateur de 50 doses contient 5,842 g de Norflurane (HFC-134A) correspondant à 0.008 tonne équivalent CO2 (potentiel de réchauffement global PRG=1430).Chaque inhalateur de 100 doses contient 9,087 g de Norflurane (HFC-134A) correspondant à 0.013 tonne équivalent CO2 (potentiel de réchauffement global PRG=1430).
Chaque inhalateur de 120 doses contient 10,384 g de Norflurane (HFC-134A) correspondant à 0.015 tonne équivalent CO2 (potentiel de réchauffement global PRG=1430).
Ce médicament appartient à la classe des bronchodilatateurs..
Titulaire de l’autorisation de mise sur le marché
26/A via Palermo
43122 PARMA
ITALIE
Exploitant de l’autorisation de mise sur le marché
CHIESI SAS
17 avenue de l’Europe
92270 BOIS COLOMBES
VIA S. Leonardo 96
43122 PARMA
ITALIE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants :
[à compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).