Dernière mise à jour le 28/04/2026
PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW 40 mg/0,04 mg par 4 ml, solution injectable
Indications thérapeutiques
Classe pharmacothérapeutique : antispasmodique musculotrope - code ATC : A03AX12.
PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW appartient à une classe de médicaments appelés antispasmodiques. Il agit contre les spasmes (contractions).
Ce médicament est indiqué dans le traitement des douleurs spasmodiques de l’intestin, des voies biliaires, de la vessie et de l’utérus.
Présentations
> 10 ampoule(s) en verre de 4 ml
Code CIP : 418 453-4 ou 34009 418 453 4 5
Déclaration de commercialisation : 05/12/2011
Cette présentation est agréée aux collectivités
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Faible | Avis du 21/09/2011 | Inscription (CT) | Le service médical rendu par cette spécialité est faible dans le traitement symptomatique des douleurs aiguës liées aux troubles fonctionnels du tube digestif, dans le traitement des manifestations spasmodiques et douloureuses aiguës des voies urinaires (coliques néphrétiques), dans le traitement symptomatique des manifestations douloureuses aiguës en gynécologie. |
| Insuffisant | Avis du 21/09/2011 | Inscription (CT) | Le service médical rendu par cette spécialité est insuffisant dans le traitement symptomatique des douleurs aiguës liées aux troubles fonctionnels des voies biliaires. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 21/09/2011 | Inscription (CT) | Absence d'amélioration du service médical rendu (ASMR V) par rapport à SPASFON solution injectable en ampoule. |
ANSM - Mis à jour le : 04/01/2023
PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW 40 mg/0,04 mg par 4 ml, solution injectable
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Phloroglucinol dihydraté.................................................................................................... 40,00 mg
Quantité correspondant à phloroglucinol anhydre................................................................ 31,12 mg
Triméthylphloroglucinol........................................................................................................ 0,04 mg
Pour une ampoule de 4 ml.
Ce médicament contient moins de 1 mmol (23 mg) de sodium par ampoule, c.-à-d. qu’il est essentiellement « sans sodium ».
Pour la liste complète des excipients, voir rubrique 6.1.
4.1. Indications thérapeutiques
· Traitement des manifestations spasmodiques et douloureuses aiguës des voies urinaires : coliques néphrétiques.
· Traitement symptomatique des manifestations douloureuses aiguës en gynécologie.
4.2. Posologie et mode d'administration
Posologie
Chez l’adulte
Traitement d’attaque
La posologie usuelle est d’1 ampoule, administrée au moment de la crise, renouvelée en cas de spasmes importants, sans dépasser 3 ampoules par 24 heures.
Traitement d’entretien
Les comprimés ou les suppositoires prendront le relais du traitement d’attaque selon une posologie de 6 comprimés ou 3 suppositoires par 24 heures.
Pour plus de précisions, se référer à la posologie et au mode d’administration des formes comprimé ou suppositoires.
Population pédiatrique
Aucune donnée n’est disponible.
Mode d’administration
Voie injectable.
L’administration peut se faire par voie intraveineuse directe ou intramusculaire.
En l’absence d’études de compatibilité, ce médicament ne doit pas être mélangé avec d’autres médicaments.
Schéma d’ouverture de l’ampoule :
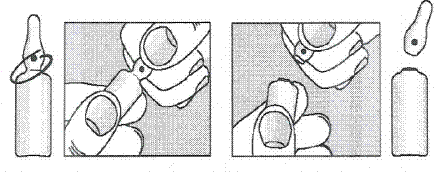
Hypersensibilité aux substances actives ou à l’un des excipients mentionnés à la rubrique 6.1.
4.4. Mises en garde spéciales et précautions d'emploi
L’association de phloroglucinol avec des antalgiques majeurs tels que la morphine ou ses dérivés doit être évitée en raison de leur effet spasmogène.
Ce médicament contient moins de 1 mmol (23 mg) de sodium par ampoule, c.-à-d. qu’il est essentiellement « sans sodium ».
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
4.6. Fertilité, grossesse et allaitement
Grossesse
Les études réalisées chez l’animal n’ont pas mis en évidence d’effet tératogène du phloroglucinol. En l’absence d’effet tératogène chez l’animal, un effet malformatif dans l’espèce humaine n’est pas attendu. En effet, à ce jour, les substances responsables de malformations dans l’espèce humaine se sont révélées tératogènes chez l’animal au cours d’études bien conduites sur deux espèces.
En clinique, l’utilisation relativement répandue du phloroglucinol n’a apparemment révélé aucun risque malformatif à ce jour. Toutefois, des études épidémiologiques sont nécessaires pour vérifier l’absence de risque.
En conséquence, l’utilisation de phloroglucinol ne doit être envisagée au cours de la grossesse que si nécessaire.
En l’absence de données, il est conseillé d’éviter l’utilisation de ce médicament pendant l’allaitement.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Manifestations cutanéo-muqueuses et allergiques : éruption, rarement urticaire, prurit, exceptionnellement œdème de Quincke, choc anaphylactique (hypotension artérielle).
|
Classe de systèmes d’organes |
Effet indésirable |
Fréquence |
|
Affections de la peau et du tissu sous-cutané |
Pustulose exanthématique aiguë généralisée |
Fréquence indéterminée |
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.signalement-sante.gouv.fr
Des cas de surdosage ont été rapportés sans symptomatologie spécifique.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : ANTISPASMODIQUE MUSCULOTROPE, code ATC : A03AX12
Mécanisme d’action
Le phloroglucinol et le triméthylphloroglucinol possèdent une activité spasmolytique sur les muscles lisses et un effet anti-nociceptif viscéral, en particulier au décours d’épisodes de douleur aiguë.
5.2. Propriétés pharmacocinétiques
Distribution
La distribution tissulaire du phloroglucinol est rapide et importante.
Biotransformation
Le phloroglucinol est métabolisé au niveau du foie par glucuroconjugaison.
Elimination
L’élimination s’effectue par voie urinaire sous forme glucuroconjuguée et par voie biliaire sous forme libre et conjuguée. La demi-vie d’élimination est de l’ordre de 1h40.
5.3. Données de sécurité préclinique
Les données non cliniques issues des études conventionnelles de toxicologie en administration répétée, génotoxicité et des fonctions de reproduction, n'ont pas révélé de risque particulier pour l'homme.
En l’absence d’études de compatibilité, ce médicament ne doit pas être mélangé avec d’autres médicaments.
2 ans.
6.4. Précautions particulières de conservation
A conserver dans l’emballage extérieur d’origine, à l’abri de la lumière.
6.5. Nature et contenu de l'emballage extérieur
4 ml en ampoule (verre type I).
Boîte de 6, 10 ou 20 ampoules.
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
Pas d’exigences particulières.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
VAULT 14, LEVEL 2,
VALLETTA WATERFRONT,
FLORIANA, FRN 1914,
MALTE
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 418 452 8 4 : 4 ml en ampoule (verre type I) ; boîte de 6.
· 34009 418 453 4 5 : 4 ml en ampoule (verre type I) ; boîte de 10.
· 34009 418 454 0 6 : 4 ml en ampoule (verre type I) ; boîte de 20.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I.
ANSM - Mis à jour le : 04/01/2023
PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW 40 mg/0,04 mg par 4 ml, solution injectable
Phloroglucinol dihydraté/Triméthyphloroglucinol
Veuillez lire attentivement cette notice avant d’utiliser ce médicament car elle contient des informations importantes pour vous.
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin, votre pharmacien ou votre infirmier/ère.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW 40 mg/0,04 mg par 4 ml, solution injectable et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW 40 mg/0,04 mg par 4 ml, solution injectable ?
3. Comment utiliser PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW 40 mg/0,04 mg par 4 ml, solution injectable ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW 40 mg/0,04 mg par 4 ml, solution injectable ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW 40 mg/0,04 mg par 4 ml, solution injectable ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : antispasmodique musculotrope - code ATC : A03AX12.
PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW appartient à une classe de médicaments appelés antispasmodiques. Il agit contre les spasmes (contractions).
Ce médicament est indiqué dans le traitement des douleurs spasmodiques de l’intestin, des voies biliaires, de la vessie et de l’utérus.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW 40 mg/0,04 mg par 4 ml, solution injectable ?
· si vous êtes allergique au phloroglucinol, au triméthylphloroglucinol ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6.
Avertissements et précautions
Adressez-vous à votre médecin, pharmacien ou votre infirmier/ère avant d’utiliser PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW 40 mg/0,04 mg par 4 ml, solution injectable.
Autres médicaments et PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW 40 mg/0,04 mg par 4 ml, solution injectable
Il est contre-indiqué de mélanger dans la même seringue la solution injectable de phloroglucinol avec de la noramidopyrine en raison d’une incompatibilité physico-chimique (risque de phlébo-thrombose).
Ce médicament ne doit pas être mélangé avec d’autres médicaments.
Informez votre médecin si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW 40 mg/0,04 mg par 4 ml, solution injectable avec des aliments et des boissons
Sans objet.
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
Grossesse
L'utilisation de ce médicament ne doit être envisagée au cours de la grossesse que si nécessaire.
Allaitement
L'administration de ce médicament est déconseillée chez la femme qui allaite.
Demandez conseil à votre médecin ou à votre pharmacien avant de prendre tout médicament.
Conduite de véhicules et utilisation de machines
PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW n’a aucun effet ou un effet négligeable sur l’aptitude à conduire des véhicules et à utiliser des machines.
PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW 40 mg/0,04 mg par 4 ml, solution injectable contient du sodium.
Ce médicament contient moins de 1 mmol (23 mg) de sodium par ampoule, c.-à-d. qu’il est essentiellement « sans sodium ».
3. COMMENT UTILISER PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW 40 mg/0,04 mg par 4 ml, solution injectable ?
Posologie
PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW est un traitement symptomatique. La durée du traitement est variable en fonction de l’indication. Si les symptômes persistent, consultez votre médecin.
Chez l’adulte
Traitement d’attaque
1 ampoule sera administrée au moment de la crise, renouvelée en cas de spasmes importants, sans dépasser 3 ampoules par 24 heures.
Traitement d’entretien
Les comprimés ou les suppositoires prendront le relais du traitement d’attaque selon une posologie de 6 comprimés ou 3 suppositoires par jour.
Pour plus de précisions, se référer à la posologie et au mode d’administration des formes comprimé ou suppositoire.
Utilisation chez les enfants
Aucune donnée n’est disponible.
Mode d’administration
Voie injectable.
L’administration peut se faire par voie intraveineuse directe ou intramusculaire.
Ce médicament ne doit pas être mélangé avec d’autres médicaments.
Schéma d’ouverture de l’ampoule :
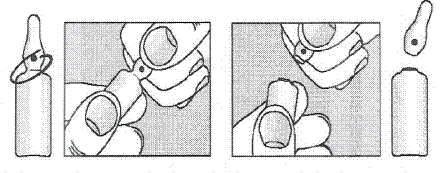
Si vous avez utilisé plus de PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW 40 mg/0,04 mg par 4 ml, solution injectable que vous n’auriez dû
Consultez immédiatement votre médecin ou votre pharmacien.
Si vous oubliez d’utiliser PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW 40 mg/0,04 mg par 4 ml, solution injectable
Ne prenez pas de dose double pour compenser la dose que vous avez oublié de prendre.
Si vous arrêtez d’utiliser PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW 40 mg/0,04 mg par 4 ml, solution injectable
Sans objet.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin, à votre pharmacien ou à votre infirmier/ère.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Fréquence indéterminée : une éruption étendue squameuse rouge avec des masses sous la peau et des cloques accompagnée de fièvre à l’instauration du traitement (pustulose exanthématique aiguë généralisée).
Si vous développez ces symptômes, arrêtez d’utiliser ce médicament et contactez votre généraliste ou consultez immédiatement un médecin.
Dans certains cas une allergie peut survenir.
Vous reconnaitrez les signes d’une allergie :
· par des boutons et/ou des rougeurs sur la peau, démangeaisons,
· par un brusque gonflement du visage et du cou (œdème de Quincke),
· ou par un malaise brutal dû à une chute de la pression artérielle (choc anaphylactique).
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou à votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.signalement-sante.gouv.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER PHLOROGLUCINOL/TRIMETHYLPHLOROGLUCINOL ARROW 40 mg/0,04 mg par 4 ml, solution injectable ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’emballage. La date de péremption fait référence au dernier jour de ce mois.
A conserver dans l'emballage extérieur d'origine, à l'abri de la lumière.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
· Les substances actives sont :
Phloroglucinol dihydraté.............................................................................................. 40,00 mg
Quantité correspondant à phloroglucinol anhydre.......................................................... 31,12 mg
Triméthylphloroglucinol.................................................................................................. 0,04 mg
Pour une ampoule de 4 ml.
· Les autres composants sont : chlorure de sodium, acide chlorhydrique concentré (pour ajustement du pH), eau pour préparations injectables.
Ce médicament se présente sous forme de solution injectable en ampoule (verre type I) de 4 ml.
Boîtes de 6, 10 ou 20 ampoules.
Titulaire de l’autorisation de mise sur le marché
EUGIA PHARMA (MALTA) LTD
VAULT 14, LEVEL 2,
VALLETTA WATERFRONT,
FLORIANA, FRN 1914,
MALTE
Exploitant de l’autorisation de mise sur le marché
ARROW GENERIQUES
26 AVENUE TONY GARNIER
69007 LYON
RUE PAUL LANGEVIN
BP 90241
37172 CHAMBRAY LES TOURS CEDEX
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Sans objet.
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).