Dernière mise à jour le 08/01/2026
APROKAM 50 mg, poudre pour solution injectable
Indications thérapeutiques
Classe pharmacothérapeutique Organes sensoriels – Médicaments ophtalmologiques – Anti-infectieux – Antibiotiques, - code ATC : S01AA27
· APROKAM 50 mg, poudre pour solution injectable contient une substance active, la céfuroxime (sous forme de céfuroxime sodique) qui appartient au groupe d’antibiotiques appelé céphalosporines. Les antibiotiques sont utilisés pour tuer les bactéries ou « germes » causant les infections.
· Ce médicament sera utilisé si vous allez subir une intervention chirurgicale de l’œil pour cataracte (opacification du cristallin).
· Votre chirurgien ophtalmologiste vous administrera ce médicament par injection dans l’œil à la fin de l’intervention chirurgicale de la cataracte, afin de prévenir une infection de l’œil
Présentations
> 10 flacons en verre de 50 mg avec 10 aiguilles filtres de 5 microns stériles
Code CIP : 34009 550 285 1 2
Déclaration de commercialisation : 05/07/2017
Cette présentation est agréée aux collectivités
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 08/03/2017 | Inscription (CT) | Le service médical rendu par APROKAM est important dans l’indication de l’AMM. |
| Important | Avis du 02/04/2014 | Inscription (CT) | Le service médical rendu par APROKAM 50 mg est important dans l’indication de l’AMM. Toutefois, la prescription en ville d’APROKAM n’est pas justifiée car la chirurgie de la cataracte ne peut se faire que dans des établissements santé que ce soit à l’hôpital ou hors hôpital. Par conséquent, la Commission donne un avis défavorable à l'inscription sur la liste des spécialités remboursables aux assurés sociaux dans l’indication « Traitement de première intention dans la prévention des endophtalmies post-opératoires après chirurgie de la cataracte » et aux posologies de l’AMM |
| Important | Avis du 20/03/2013 | Inscription (CT) | Le service médical rendu par APROKAM 50 mg, poudre pour solution injectable, est important dans l’indication de l’AMM. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 08/03/2017 | Inscription (CT) | Cette spécialité est un complément de gamme qui n’apporte pas d’amélioration du service médical rendu (ASMR V) par rapport aux présentations déjà inscrites. |
| IV (Mineur) | Avis du 20/03/2013 | Inscription (CT) | APROKAM 50 mg, poudre pour solution injectable, apporte une amélioration du service médical rendu mineure (ASMR IV) par rapport à la stratégie habituelle de prévention des endophtalmies post-opératoires liées à la chirurgie de la cataracte. |
Autres informations
- Titulaire de l'autorisation : Laboratoires THEA
- Conditions de prescription et de délivrance :
- liste I
- prescription réservée aux spécialistes et services OPHTALMOLOGIE
- Statut de l'autorisation : Valide
- Type de procédure : Procédure décentralisée
- Code CIS : 6 037 816 8
ANSM - Mis à jour le : 19/03/2024
APROKAM 50 mg, poudre pour solution injectable
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chaque flacon contient 50 mg de céfuroxime (sous forme de 52,6 mg de céfuroxime sodique).
Après reconstitution avec 5 ml de solvant (voir rubrique 6.6), 0,1 ml de solution contient 1 mg de céfuroxime.
Pour la liste complète des excipients, voir rubrique 6.1.
Poudre pour solution injectable.
Poudre blanche à presque blanche.
4.1. Indications thérapeutiques
Antibioprophylaxie des endophtalmies post-opératoires après une chirurgie de la cataracte (voir rubrique 5.1).
Il convient de tenir compte des recommandations officielles concernant l'utilisation appropriée des antibactériens, incluant celles sur l’antibioprophylaxie en chirurgie oculaire.
4.2. Posologie et mode d'administration
Voie intra-camérulaire. Un flacon pour un usage unique seulement.
Posologie
Adultes :
La posologie recommandée est de 0,1 ml de solution reconstituée (voir rubrique 6.6), c'est-à-dire de 1 mg de céfuroxime.
NE PAS INJECTER UNE DOSE SUPERIEURE A CELLE RECOMMANDEE (voir rubrique 4.9).
Population pédiatrique
La posologie optimale et la sécurité d’emploi d’APROKAM n’ont pas été établies dans la population pédiatrique.
Sujets âgés :
L’adaptation posologique n’est pas nécessaire.
Insuffisants rénaux et hépatiques :
Considérant la faible dose et le passage systémique négligeable de céfuroxime attendu après utilisation d’APROKAM, aucun ajustement posologique n’est nécessaire
Mode d’administration
APROKAM doit être administré après reconstitution, par injection intra-oculaire dans la chambre antérieure de l’œil (voie intra-camérulaire), par un chirurgien ophtalmologiste, dans les conditions d’asepsie recommandées pour la chirurgie de la cataracte. Seule une solution pour injection de chlorure de sodium 9 mg/ml (0,9 %) doit être utilisée lors de la reconstitution de APROKAM (voir rubrique 6.6).
Après reconstitution, APROKAM doit être contrôlé visuellement afin de rechercher la présence de particules ou d’une coloration anormale avant administration.
Injecter lentement 0,1 ml de solution reconstituée dans la chambre antérieure de l’œil en fin de chirurgie de la cataracte.
Pour les instructions concernant la reconstitution d’APROKAM avant l’administration, voir rubrique 6.6.
Hypersensibilité à la céfuroxime ou aux antibiotiques du groupe des céphalosporines.
4.4. Mises en garde spéciales et précautions d'emploi
APROKAM doit être utilisé uniquement par voie intra-camérulaire.
En raison d'un possible risque de réaction allergique croisée, une précaution particulière doit être prise chez les patients ayant des antécédents de réactions allergiques aux pénicillines ou aux autres bêta-lactamines.
Chez les patients à risque d’infections dues à des souches résistantes, par exemple les patients ayant eu une infection ou une colonisation avec un SARM (Staphylococcus aureus résistant à la méticilline), un autre traitement antibiotique prophylactique doit être envisagé.
En l’absence de données chez des groupes de patients particuliers (patients à haut risque d’infection, patients avec des cataractes compliquées, patients devant subir des interventions combinées à la chirurgie de la cataracte, patients ayant une maladie sévère de la thyroïde, patients ayant moins de 2000 cellules endothéliales cornéennes), APROKAM doit être uniquement utilisé qu’après une évaluation attentive du rapport bénéfice/risque.
L’utilisation de la céfuroxime ne doit pas être considérée comme une mesure isolée car d’autres précautions sont tout aussi importantes, comme le traitement prophylactique antiseptique.
Aucune toxicité endothéliale cornéenne n’a été rapportée à la concentration recommandée de céfuroxime ; néanmoins, ce risque ne peut être exclu et durant la surveillance post-opératoire, les médecins doivent garder à l’esprit ce risque potentiel.
Ce médicament contient moins de 1 mmol (23 mg) de sodium par dose, c-à-d. qu’il est essentiellement « sans sodium ».
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
L’exposition systémique attendue étant négligeable, les interactions systémiques sont peu probables.
Aucune incompatibilité avec les produits les plus fréquemment utilisés dans la chirurgie de la cataracte, n’a été rapportée dans la littérature.
4.6. Fertilité, grossesse et allaitement
Grossesse
Il existe des données limitées sur l’utilisation de la céfuroxime chez la femme enceinte. Les études chez l’animal n’ont montré aucun effet délétère sur le développement embryonnaire ou fœtale. La céfuroxime atteint l’embryon ou le fœtus au travers du placenta. Aucun effet pendant la grossesse n’est à prévoir, étant donné que l’exposition systémique à la céfuroxime suite à l’utilisation d’APROKAM est négligeable. APROKAM peut être utilisé pendant la grossesse.
Allaitement
La céfuroxime peut être excrétée dans le lait maternel en très faible quantité. Des effets indésirables aux doses thérapeutiques ne sont pas attendus après l’utilisation d’APROKAM. La céfuroxime peut être utilisée pendant l’allaitement.
Fertilité
Il n’y a pas de données sur les effets de la céfuroxime sodique sur la fertilité chez l’Homme. Des études sur la reproduction chez l’animal n’ont montré aucun effet sur la fertilité.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Sans objet.
Aucun effet indésirable particulier n’a été rapporté dans la littérature quand la céfuroxime est administrée par injection intra-oculaire, sauf les suivants :
Affections oculaires
Fréquence indéterminée (ne peut être estimée sur la base des données disponibles) : Œdème maculaire
Affections du système immunitaire
Très rare (<1/10 000) : réaction anaphylactique.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : www.signalement-sante.gouv.fr.
Les cas de surdosage rapportés sont ceux décrits dans la littérature après dilution incorrecte et utilisation non autorisée de céfuroxime destinée à un usage systémique.
Une dose excessive de céfuroxime (3 fois la dose recommandée) a été administrée par inadvertance par voie intra-camérulaire chez 6 patients suite à une erreur de dilution d’une préparation magistrale de céfuroxime. Ces injections n’ont provoqués aucun effet indésirable détectable, chez tous les patients, même au niveau des tissus oculaires.
Des données de toxicité sont disponibles suite à l’injection intra-camérulaire, pendant la chirurgie de la cataracte de doses 40 à 50 fois supérieures à celle recommandée en céfuroxime, chez 6 patients, après des erreurs de dilution. L’acuité visuelle moyenne initiale était de 20/200. Une inflammation sévère du segment antérieur était présente, et la tomographie en cohérence optique de la rétine a montré un important œdème maculaire. Six semaines après la chirurgie, l’acuité visuelle moyenne atteignait 20/25. Le profil maculaire en tomographie en cohérence optique revint à la normale. Une diminution de 30% de l’électrorétinographie scotopique a cependant été observée chez tous les patients.
L’administration de céfuroxime incorrectement diluée (10-100 mg par œil) chez 16 patients a entraîné une toxicité oculaire avec un œdème cornéen qui s’est résorbé en quelques semaines, une augmentation transitoire de la pression oculaire, une perte de cellules endothéliales cornéennes et des modifications à l’électrorétinographie. Un certain nombre de ces patients ont eu une perte de vision sévère et permanente.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : Organes sensoriels – Médicaments ophtalmologiques – Anti-infectieux – Antibiotiques, code ATC : S01AA27.
Mécanisme d’action
La céfuroxime inhibe la synthèse de la paroi bactérienne en se fixant aux protéines de liaison aux pénicillines (PLP). Ceci conduit à un arrêt de la biosynthèse de la paroi cellulaire (peptidoglycanes) entrainant une lyse cellulaire et la mort de la bactérie.
Relations pharmacodynamiques/pharmacocinétiques
Pour les céphalosporines, il a été montré que l’index pharmacocinétique/pharmacodynamique le plus prédictif de l’efficacité in vivo était le pourcentage de temps (T%) pendant lequel la concentration de la forme libre en céfuroxime se situe au-dessus la concentration minimale inhibitrice (CMI) pour des bactéries cibles (c'est-à-dire T%>CMI).
Après injection intra-camérulaire de 1 mg de céfuroxime, les taux en céfuroxime dans l’humeur aqueuse étaient supérieurs aux CMI de plusieurs espèces concernées jusqu’à 4 à 5 heures après la chirurgie.
Mécanismes de résistance
La résistance bactérienne à la céfuroxime peut être due à un ou plusieurs des mécanismes suivants :
· Hydrolyse par des bêta-lactamases. La céfuroxime peut être hydrolysée efficacement par certaines bêta-lactamases à spectre étendu (BLSE) et par des bêta-lactamases chromosomiques (AmpC) qui peuvent être induites ou déréprimées de façon stable chez certaines espèces de bactéries aérobies à Gram négatif.
· Diminution de l’affinité des protéines de liaison aux pénicillines pour la Céfuroxime.
· Imperméabilité de la paroi externe, qui restreint l’accès de la céfuroxime aux protéines de liaison aux pénicillines chez des bactéries Gram négatif.
· Pompes à efflux bactériennes.
Les Staphylococcus résistants à la méticilline (SARM) sont résistants aux bêta-lactamines actuellement disponibles, dont la céfuroxime.
Les Streptococcus pneumoniae résistants à la pénicilline ont une résistance croisée aux céphalosporines comme la céfuroxime, par une altération des protéines de liaison aux pénicillines.
Des souches d’H. influenzae résistantes à l’ampicilline sans production de bêta-lactamase (BLNAR) devraient être considérées résistantes à la céfuroxime malgré une apparente sensibilité in vitro.
Concentrations critiques
La liste des micro-organismes présentés ci-après a tenu compte de l’indication (voir rubrique 4.1).
APROKAM doit être utilisé uniquement par voie intra-camérulaire et ne doit pas être utilisé pour traiter des infections systémiques (voir rubrique 5.2); les concentrations critiques cliniques ne sont pas transposables à cette voie d’administration. Les valeurs des seuils épidémiologiques (ECOFF), distinguant la population des souches sauvages des souches isolées avec des résistances acquises sont les suivantes :
|
|
ECOFF (mg/L) |
|
Staphylococcus aureus |
≤ 4 |
|
Streptococcus pneumoniae |
≤ 0,125 |
|
E. coli |
≤ 8 |
|
Proteus mirabilis |
≤ 4 |
|
H. influenzae |
≤ 2 |
La sensibilité des staphylococcus à la céfuroxime est déduite de la sensibilité à la méticilline.
La sensibilité des streptococcus de groupes A, B, C et G peut être déduite de leur sensibilité à la benzylpénicilline.
Informations issues des essais cliniques
Une étude prospective randomisée, dont l’aveugle n’a été que partiel, multicentrique, menée dans la chirurgie de la cataracte, a été réalisée sur 16 603 patients. Vingt-neuf patients (24 dans le groupe « sans céfuroxime » et 5 dans le groupe « céfuroxime par injection intra-camérulaire ») ont présentés une endophtalmie dont 20 (17 dans le groupe « sans céfuroxime » et 3 dans le groupe « céfuroxime par injection intra-camérulaire » furent considérés comme ayant une endophtalmie infectieuse prouvée. Parmi ces 20 endophtalmies prouvées : 10 patients sont dans le groupe « collyre de placebo et sans céfuroxime", 7 patients dans le groupe « levofloxacine collyre et sans céfuroxime », 2 patients dans le groupe « collyre de placebo et céfuroxime intra-camérulaire » et 1 patient dans le groupe « levofloxacine collyre et céfuroxime intra-camérulaire ». L’administration prophylactique d’une solution à 1 mg de céfuroxime par 0,1 ml de chlorure de sodium 9 mg/ml (0,9%) par voie intra-camérulaire a permis de diminuer le risque d’endophtalmies post-opératoires d’un facteur égal à 4.92.
Deux études prospectives (Wedje 2005 et Lundström 2007) et 5 études rétrospectives sont en support de l’étude pivotale ESCRS permettant d’étayer d’avantage l’efficacité de la céfuroxime administrée en intra-camérulaire dans la prévention des endophtalmies post-opératoires.
5.2. Propriétés pharmacocinétiques
L’exposition systémique suite à une injection intra-camérulaire n’a pas été étudiée, mais devrait être négligeable.
Après injection unique intra-camérulaire, de la dose recommandée de 0,1 ml d’une solution à 10 mg/ml de céfuroxime chez des patients atteints de cataracte, la concentration moyenne intra-camérulaire était de 2614 ± 209 mg/l (10 patients) à 30 secondes et de 1027 ± 43 mg/l (9 patients) à 60 minutes après administration de la solution.
5.3. Données de sécurité préclinique
Lors d’études précliniques, des effets ont été observés chez l’animal uniquement à des expositions largement supérieures à l’exposition maximale observée chez l’Homme, et ont eu peu de traduction clinique.
Trente minutes suivant l’injection intra-vitréenne de 1 mg de céfuroxime chez des lapins albinos, des taux de 19-35 mg/l et de 600-780 mg/l ont été retrouvés respectivement dans l’humeur aqueuse et dans le vitré. Ces taux après 6 heures diminuent à 1,9-7,3 mg/l et 190-260 mg/l respectivement dans ces deux structures. Il n’y a pas d’augmentation de la pression intra-oculaire pendant les 3 premiers jours. L’histopathologie n’a montré aucune modification dégénérative en comparaison avec la solution saline.
Electrorétinogramme (ERG) : les ondes a-, b- et c- diminuent jusqu’au 14ème jour aussi bien dans le groupe « témoin » que dans le groupe « œil avec injection d’antibiotique ».
Le retour à la normale est observé mais il peut être plus lent que dans le groupe « témoin ». L’ERG n’a montré aucun changement définitif suggérant une toxicité rétinienne jusqu’à 55 jours après l’administration intra-vitréenne.
Sans objet.
Ce médicament ne doit pas être mélangé avec d’autres médicaments à l’exception de ceux mentionnés dans la rubrique 6.6.
18 mois.
Après reconstitution : le produit doit être utilisé immédiatement après reconstitution et ne doit pas être réutilisé.
6.4. Précautions particulières de conservation
A conserver à une température ne dépassant pas 25°C.
Conserver le flacon dans l’emballage extérieur à l’abri de la lumière
Pour les conditions de conservation du médicament reconstitué, voir rubrique 6.3.
6.5. Nature et contenu de l'emballage extérieur
Flacon verre de type I de 8 ml, fermé par un bouchon en bromobutyle et une capsule aluminium flip-off.
Boite de 1, 10 ou 20 flacons de 50 mg.
Boîte de 10 flacons de 50 mg avec 10 aiguilles-filtre de 5 microns stériles
Toutes les présentations peuvent ne pas être commercialisées.
6.6. Précautions particulières d’élimination et de manipulation
APROKAM doit être administré par injection intra-camérulaire, par un chirurgien ophtalmologiste dans les conditions d’asepsie recommandées de la chirurgie de la cataracte.
FLACON POUR USAGE UNIQUE SEULEMENT.
UTILISER UN FLACON POUR UN PATIENT. Coller l’étiquette drapeau du flacon dans le dossier patient.
Pour préparer le produit pour l’administration intra-camérulaire, veuillez suivre de façon stricte les instructions suivantes :
1. Retirer la capsule flip-off.
2. Avant d’insérer l’aiguille stérile, désinfecter la partie extérieure du bouchon en caoutchouc du flacon.
3. Enfoncer l'aiguille verticalement au centre du bouchon, en maintenant le flacon en position verticale. Ensuite, injecter dans le flacon 5 ml de solution pour injection de chlorure de sodium 9 mg/ml (0,9%) en suivant les règles d’asepsie.
4. Secouer doucement le flacon jusqu’à que la solution soit sans particule visible.
5. Fixer une aiguille-filtre de 5 microns stérile (18G x 1½, 1,2 mm x 40 mm, filtre de 5 microns en copolymère acrylique sur nylon non-tissé) sur une seringue stérile de 1 ml. Enfoncer l’aiguille verticalement au centre du bouchon, en maintenant le flacon en position verticale.
6. Aspirer de façon aseptique au moins 0,1 ml de solution.
7. Déconnecter l’aiguille-filtre de 5 microns stérile de la seringue et assembler la seringue sur une canule appropriée pour la chambre antérieure.
8. Expulser doucement l’air de la seringue et ajuster la dose à la marque 0,1 ml de la seringue. La seringue est prête pour l’injection.
La solution reconstituée doit être inspectée visuellement et doit être utilisée uniquement si elle est incolore à jaunâtre et sans particule visible. Elle a un pH et une osmolalité proche des valeurs physiologiques (pH environ de 7,3 et osmolalité environ de 335 mosmol/kg).
Après utilisation, jeter la solution reconstituée restante. Ne pas la garder pour une utilisation ultérieure.
Tout produit non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
Jeter les aiguilles usagées dans un conteneur pour objets piquants.
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
LABORATOIRES THEA
12 RUE LOUIS BLERIOT
63017 CLERMONT-FERRAND CEDEX 2
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 224 104 4 9 : poudre en flacon (verre) ; boîte de 1
· 34009 582 956 5 2 : poudre en flacon (verre) ; boîte de 10
· 34009 582 957 1 3 : poudre en flacon (verre) ; boîte de 20
· 34009 550 285 1 2 : poudre en flacon (verre) ; boîte de 10 avec 10 aiguilles-filtre de 5 microns stériles
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
Date de première autorisation:{JJ mois AAAA}
Date de dernier renouvellement:{JJ mois AAAA}
10. DATE DE MISE A JOUR DU TEXTE
{JJ mois AAAA}
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Sans objet.
Liste I
Prescription réservée aux spécialistes en ophtalmologie.
ANSM - Mis à jour le : 19/03/2024
APROKAM 50 mg, poudre pour solution injectable
Céfuroxime
Veuillez lire attentivement cette notice avant d’utiliser ce médicament car elle contient des informations importantes pour vous.
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien ou votre infirmier/ère.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que APROKAM 50 mg, poudre pour solution injectable et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser APROKAM 50 mg, poudre pour solution injectable ?
3. Comment utiliser APROKAM 50 mg, poudre pour solution injectable?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver APROKAM 50 mg, poudre pour solution injectable ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE APROKAM 50 mg, poudre pour solution injectable ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique Organes sensoriels – Médicaments ophtalmologiques – Anti-infectieux – Antibiotiques, - code ATC : S01AA27
· APROKAM 50 mg, poudre pour solution injectable contient une substance active, la céfuroxime (sous forme de céfuroxime sodique) qui appartient au groupe d’antibiotiques appelé céphalosporines. Les antibiotiques sont utilisés pour tuer les bactéries ou « germes » causant les infections.
· Ce médicament sera utilisé si vous allez subir une intervention chirurgicale de l’œil pour cataracte (opacification du cristallin).
· Votre chirurgien ophtalmologiste vous administrera ce médicament par injection dans l’œil à la fin de l’intervention chirurgicale de la cataracte, afin de prévenir une infection de l’œil
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER APROKAM 50 mg, poudre pour solution injectable ?
N’utilisez jamais APROKAM 50 mg, poudre pour solution injectable:
· si vous êtes allergique (hypersensible) à la céfuroxime ou à tout autre antibiotiques du groupe des céphalosporines.
Avertissements et précautions
Faites attention avec APROKAM :
Adressez-vous à votre médecin ou, pharmacien avant d’utiliser APROKAM 50 mg, poudre pour solution injectable:
· si vous êtes allergique à d’autres antibiotiques comme la pénicilline,
· si vous présentez un risque d’infection due à une bactérie appelée Staphylococcus aureus résistant à la méticilline,
· si vous présentez un risque d’avoir une infection qui peut être sévère,
· s’il vous a été diagnostiqué une cataracte compliquée,
· si une autre chirurgie de l’œil est planifiée en même temps que celle pour votre cataracte,
· si vous avez une grave maladie de la thyroïde.
APROKAM est uniquement administré par injection dans l’œil (injection intra-camérulaire).
APROKAM doit être administré dans les conditions aseptiques recommandées pour la chirurgie de la cataracte (cela veut dire dans un environnement propre et sans germe).
Un flacon d’APROKAM doit être utilisé pour un seul patient.
Enfants et adolescents
Sans objet.
Autres médicaments et APROKAM 50 mg, poudre pour solution injectable
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
APROKAM 50 mg, poudre pour solution injectable avec des aliments et boissons
Sans objet.
Grossesse et allaitement
· Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez de l’être, demandez conseil à votre médecin ou pharmacien avant de prendre ce médicament.
· APROKAM vous sera administré uniquement si les bénéfices sont supérieurs aux risques potentiels
Conduite de véhicules et utilisation de machines
Sans objet.
APROKAM 50 mg, poudre pour solution injectable contient du sodium
Ce médicament contient moins de 1 mmol (23 mg) de sodium par dose, c-à-d. qu’il est essentiellement « sans sodium ».
3. COMMENT UTILISER APROKAM 50 mg, poudre pour solution injectable ?
· Les injections d’APROKAM seront réalisées par un chirurgien ophtalmologiste à la fin de la chirurgie de la cataracte.
· APROKAM est une poudre stérile qui doit être dissoute dans une solution saline pour injection avant d’être administrée.
Si vous avez utilisé plus de APROKAM 50 mg, poudre pour solution injectable que vous n’auriez dû :
D’une façon générale, ce traitement sera administré par un professionnel de santé. Si vous pensez avoir reçu trop de produit, parlez-en à votre médecin ou à votre infirmier/ère.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin, à votre pharmacien ou à votre infirmier/ère.
Si vous oubliez d’utiliser APROKAM 50 mg, poudre pour solution injectable :
D’une façon générale, ce traitement sera administré par un professionnel de santé. Si vous pensez que la dose a été oubliée, parlez-en à votre médecin ou à votre infirmier/ère.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin, à votre pharmacien ou à votre infirmier/ère.
Si vous arrêtez d’utiliser APROKAM 50 mg, poudre pour solution injectable
Sans objet.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Comme tous les médicaments, ce médicament peut provoquer des effets indésirables, mais ils ne surviennent pas systématiquement chez tout le monde.
L’effet indésirable suivant est très rare (affectant moins de 1 patient sur 10 000) :
· Réaction allergique sévère pouvant occasionner des difficultés à respirer ou provoquer des vertiges.
L’effet indésirable suivant est rapporté avec une fréquence « indéterminée » (ne peut être estimée sur la base des données disponibles)
· Œdème maculaire (vision floue ou ondulée près du centre de votre champ de vision ou au centre de celui-ci)
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien ou à votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: www.signalement-sante.gouv.fr
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER APROKAM 50 mg, poudre pour solution injectable ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur la boîte et l’étiquette du flacon après EXP. La date de péremption fait référence au dernier jour de ce mois.
A conserver à une température ne dépassant pas 25°C. Conserver le flacon dans l’emballage extérieur à l’abri de la lumière.
Pour usage uniquement seulement.
Après reconstitution : le produit doit être utilisé immédiatement.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient APROKAM 50 mg, poudre pour solution injectable
· La substance active est : la céfuroxime (sous forme de céfuroxime sodique)
Chaque flacon contient 50 mg de céfuroxime.
Après reconstitution, 0,1 ml de solution contient 1 mg de céfuroxime.
· Les autres composants sont : Il n’y a pas d’autres composants
Qu’est-ce que APROKAM 50 mg, poudre pour solution injectable et contenu de l’emballage extérieur
APROKAM est une poudre pour solution injectable, la poudre est blanche à presque blanche et est fournie dans un flacon en verre.
Chaque boite contient un ou dix ou vingt flacons ou 10 flacons avec 10 aiguilles-filtre stériles. Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
LABORATOIRES THEA
12 RUE LOUIS BLERIOT
63017 CLERMONT-FERRAND CEDEX 2
Exploitant de l’autorisation de mise sur le marché
THEA PHARMA
37 RUE GEORGES BESSE
63100 CLERMONT-FERRAND
BIOPHARMA S.R.L.
VIA DELLE GERBERE 22/30 (loc. S. PALOMBA)
00134 ROMA (RM)
ITALIE
ou
LABORATOIRES THEA
12 RUE LOUIS BLERIOT
63017 CLERMONT-FERRAND CEDEX 2
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
{MM/AAAA}
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
Les informations suivantes sont destinées exclusivement aux professionnels de santé:
Incompatibilité
Aucune incompatibilité avec les produits utilisés le plus couramment dans la chirurgie de la cataracte n’a été rapportée dans la littérature.
Ce médicament ne doit pas être mélangé avec d’autres médicaments à l’exception de ceux mentionnés ci-dessous [solution pour injection de chlorure de sodium 9 mg/ml (0,9%)].
Comment préparer et administrer APROKAM
Flacon à usage unique seulement pour administration par voie intra-camérulaire.
APROKAM doit être administré, après reconstitution, par injection intra-oculaire dans la chambre antérieure de l’œil (injection intra-camérulaire), par un chirurgien ophtalmologiste dans les conditions d’asepsie recommandées pour la chirurgie de la cataracte.
La solution reconstituée doit être inspectée visuellement et doit être utilisée uniquement si elle est incolore à jaunâtre et sans particule visible.
Le produit doit être utilisé immédiatement après reconstitution et ne doit pas être ré-utilisé.
La dose recommandée de céfuroxime est de 1 mg dans 0,1 ml de solution pour injection de chlorure de sodium 9 mg/ml (0,9%).
NE PAS INJECTER UNE DOSE SUPERIEURE A CELLE RECOMMANDEE
Flacon pour usage unique seulement
Utiliser un flacon pour un patient seulement. Coller l’étiquette drapeau du flacon dans le dossier patient.
|
Pour préparer le produit pour l’administration intra-camérulaire, veuillez suivre de façon stricte les instructions suivantes : |
|
|
Doit être désinfecté |
1. Vérifier l’intégrité de la capsule flip-off avant de la retirer. |
|
|
2. Désinfecter la partie extérieure du bouchon en caoutchouc du flacon avant de passer à l’étape 3.
|
|
|
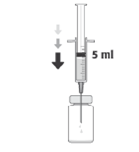
3. Enfoncer l'aiguille stérile verticalement au centre du bouchon, en maintenant le flacon en position verticale. Injecter de façon aseptique dans le flacon, 5 ml de solution pour injection de chlorure de sodium 9 mg/ml (0,9%), en utilisant une aiguille stérile.
|
|
|
4. Secouer doucement le flacon jusqu’à que la solution soit sans particule visible. |
|
|
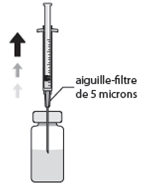
5. Fixer une aiguille-filtre de 5 microns stérile (18G x 1½, 1,2 mm x 40 mm, filtre de 5 microns en copolymère acrylique sur nylon non-tissé) sur une seringue stérile de 1 ml (l’aiguille-filtre de 5 microns stérile peut être fournie dans la boîte). Enfoncer l’aiguille verticalement au centre du bouchon, en maintenant le flacon en position verticale.
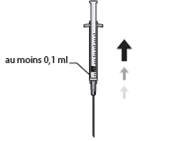
6. Aspirer de façon aseptique au moins 0,1 ml de solution
|
|
|
7. Déconnecter l’aiguille de la seringue et assembler la seringue sur une canule appropriée pour la chambre antérieure.
8. Expulser doucement l’air de la seringue et ajuster la dose à la marque 0,1 ml de la seringue. La seringue est prête pour l’injection.
|
|
|
|
|
Après utilisation, jeter la solution reconstituée restante. Ne pas la garder pour une utilisation ultérieure. |
|
Tout produit non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
Jeter les aiguilles usagées dans un conteneur pour objets piquants.