Dernière mise à jour le 28/04/2026
NEBIDO 1000 mg/4 ml, solution injectable
Indications thérapeutiques
Classe pharmacothérapeutique : Androgènes - code ATC : G03B A03
NEBIDO contient de la testostérone, une hormone masculine, comme substance active.
NEBIDO est injecté dans un muscle du corps où il peut être stocké et libéré progressivement sur une certaine période de temps.
NEBIDO est utilisé chez l'homme adulte pour remplacer la testostérone afin de traiter divers problèmes de santé dus au manque de testostérone (hypogonadisme masculin). Ce diagnostic doit être confirmé par deux dosages séparés de la testostérone dans le sang, ainsi que par la présence de symptômes tels que :
· impuissance,
· infertilité,
· diminution de la libido,
· fatigue,
· humeur dépressive,
· perte osseuse due aux faibles taux d'hormones.
Présentations
> 1 flacon(s) en verre jaune(brun) de 4 ml
Code CIP : 277 134-5 ou 34009 277 134 5 3
Déclaration de commercialisation : 21/05/2015
Cette présentation n'est pas agréée aux collectivités
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 29/11/2006 | Inscription (CT) | Le service médical rendu par cette spécialité est important dans l’indication de l’AMM. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 29/11/2006 | Inscription (CT) | L'étude versée au dossier est de méthodologie insuffisante et ne permet pas de caractériser la quantité d'effet de NEBIDO comparé à ANDROTARDYL. Par conséquent, NEBIDO n'apporte pas d'amélioration du service médical rendu (ASMR V) par rapport à ANDROTARDYL mais constitue un moyen thérapeutique supplémentaire utile dans la prise en charge de l'hypogonadisme caractérisé de l'adulte. |
Autres informations
- Titulaire de l'autorisation : LABORATOIRES GRUNENTHAL
- Conditions de prescription et de délivrance :
- liste I
- prescription initiale réservée à certains spécialistes
- prescription réservée aux médecins compétents en NUTRITION
- prescription réservée aux spécialistes en MEDECINE ET BIOLOGIE DE LA REPRODUCTION - ANDROLOGIE
- prescription réservée aux spécialistes et services DIABETOLOGIE
- prescription réservée aux spécialistes et services ENDOCRINOLOGIE
- prescription réservée aux spécialistes et services GYNECOLOGIE
- prescription réservée aux spécialistes et services UROLOGIE
- Statut de l'autorisation : Valide
- Type de procédure : Procédure de reconnaissance mutuelle
- Code CIS : 6 903 375 7
ANSM - Mis à jour le : 29/01/2026
NEBIDO 1000 mg/4 ml, solution injectable
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Chaque ml de solution injectable contient 250 mg d’undécanoate de testostérone (correspondant à 157,9 mg de testostérone).
Chaque ampoule/flacon contient 4 ml de solution injectable soit 1000 mg d’undécanoate de testostérone (correspondant à 631,5 mg de testostérone).
Excipient à effet notoire : benzoate de benzyle (2000 mg par ampoule/flacon).
Pour la liste complète des excipients, voir rubrique 6.1.
Solution huileuse limpide incolore à brun-jaunâtre.
4.1. Indications thérapeutiques
4.2. Posologie et mode d'administration
Injecter une ampoule/un flacon de NEBIDO (correspondant à 1000 mg d’undécanoate de testostérone) toutes les 10 à 14 semaines. Des injections à cette fréquence permettent de maintenir des taux de testostérone suffisants et n’entraînent pas d’accumulation.
Début du traitement
Le taux de testostérone sérique doit être mesuré avant le début du traitement et au cours de la phase d’instauration. En fonction du taux de testostérone sérique et des symptômes cliniques, l’intervalle après la première injection peut être réduit à un minimum de six semaines au lieu de l’intervalle recommandé de 10 à 14 semaines pour le traitement d’entretien. Cette dose de charge permettra d’atteindre plus rapidement les concentrations sériques de testostérone suffisantes.
Suivi et individualisation du traitement
L’intervalle recommandé entre les injections est de 10 à 14 semaines. Un suivi attentif des taux de testostérone sérique est nécessaire au cours du traitement d’entretien. Il est conseillé de mesurer régulièrement le taux de testostérone sérique. Ces mesures doivent être réalisées à la fin de l’intervalle entre deux injections et en tenant compte des signes cliniques. Ces taux sériques doivent se situer dans le tiers inférieur des valeurs normales. Des taux sériques inférieurs à la normale indiquent la nécessité de réduire l’intervalle entre 2 injections. En cas de taux élevés, on peut envisager d’augmenter l’intervalle entre 2 injections.
Populations particulières
Population pédiatrique
NEBIDO n'est pas indiqué chez l'enfant ni l’adolescent et n'a pas fait l'objet d'études cliniques chez les garçons de moins de 18 ans (voir rubrique 4.4).
Patients âgés
Des données limitées ne suggèrent pas la nécessité d’adapter les doses chez les patients âgés (voir rubrique 4.4).
Insuffisance hépatique
Aucune étude formelle n’a été conduite chez des patients présentant une insuffisance hépatique. L’utilisation de NEBIDO est contre-indiquée chez l'homme en cas de tumeur hépatique ou d’antécédents de tumeur hépatique (voir rubrique 4.3).
Insuffisance rénale
Aucune étude formelle n’a été conduite chez des patients présentant une insuffisance rénale.
Mode d’administration
Voie intramusculaire.
Les injections doivent être administrées très lentement (pendant plus de 2 minutes). NEBIDO doit uniquement être injecté par voie intramusculaire. Il faut prêter attention à injecter NEBIDO profondément dans le muscle fessier en suivant les précautions d'usage pour les injections intramusculaires. Des précautions particulières doivent être prises afin d'éviter une injection intravasculaire (voir le paragraphe « Administration » en rubrique 4.4). Le contenu de l'ampoule/du flacon doit être administré par voie intramusculaire immédiatement après ouverture (pour l'ampoule, voir en rubrique 4.6 les instructions pour une ouverture sécurisée de l'ampoule).
NEBIDO est contre-indiqué chez l'homme en cas de :
· cancer androgéno-dépendant de la prostate ou des glandes mammaires chez l'homme,
· présence ou antécédents de tumeurs hépatiques,
· hypersensibilité connue à la substance active ou à l’un des excipients (mentionnés à la rubrique 6.1).
L'utilisation de NEBIDO est contre-indiquée chez les femmes.
4.4. Mises en garde spéciales et précautions d'emploi
L’utilisation de NEBIDO n’est pas recommandée chez les enfants et les adolescents.
Le traitement par NEBIDO ne doit être débuté que si un hypogonadisme (hypo ou hypergonadotrophique) a été confirmé et si les autres étiologies pouvant être à l'origine de la symptomatologie ont été exclues. L'insuffisance en testostérone doit être clairement démontrée par des signes cliniques (régression des caractères sexuels secondaires, modification de la composition corporelle, asthénie, diminution de la libido, dysfonction érectile...) et confirmée par 2 dosages séparés de testostéronémie.
Patients âgés
L’expérience disponible concernant la sécurité et l’efficacité de NEBIDO utilisé chez les patients âgés de plus de 65 ans est limitée. Actuellement, il n'existe pas de consensus quant aux valeurs de référence de la testostéronémie en fonction de l'âge. Cependant, la diminution des valeurs physiologiques de la testostéronémie avec l'âge doit être prise en compte.
Examen médical et examens biologiques
Examen médical
Avant d'instaurer un traitement par la testostérone, les patients doivent subir impérativement un examen approfondi afin d'écarter tout risque de cancer de la prostate préexistant. Une surveillance attentive et régulière de la prostate et des seins devra être effectuée selon les méthodes usuelles recommandées (toucher rectal et dosage du PSA - antigène spécifique de la prostate), au moins une fois par an chez tout patient suivant un traitement par la testostérone et deux fois par an chez les sujets âgés et les patients à risque (facteurs cliniques ou familiaux). Les recommandations en vigueur pour le suivi de la tolérance d'un traitement substitutif en testostérone doivent être prises en considération.
Examens biologiques
Les taux de testostérone doivent être contrôlés avant le début du traitement, puis à intervalles réguliers pendant le traitement. La posologie doit être adaptée à chaque patient, afin de s’assurer que les taux de testostérone sont maintenus à un niveau eugonadique.
Chez les patients recevant un traitement androgénique au long cours, les paramètres biologiques suivants doivent être contrôlés régulièrement : taux d’hémoglobine, hématocrite, fonction hépatique et bilan lipidique (voir rubrique 4.8).
En raison de la variabilité des résultats d’analyse entre les différents laboratoires, tous les dosages de testostérone doivent être effectués par le même laboratoire pour un sujet donné.
Tumeurs
Les androgènes pourraient accélérer l'évolution d'un cancer de la prostate infraclinique ou d'une hyperplasie bénigne de la prostate.
NEBIDO doit être utilisé avec prudence chez les patients ayant un cancer avec un risque d'hypercalcémie et d'hypercalciurie lié à des métastases osseuses. Il est recommandé d'assurer un suivi régulier de la calcémie chez ces patients.
Des cas de tumeurs hépatiques bénignes et malignes ont été rapportés chez des patients recevant un traitement hormonal comme les androgènes. En cas de douleurs abdominales sévères, d’augmentation de volume du foie, ou de signes d’hémorragie intra-abdominale chez les hommes traités par NEBIDO, une tumeur hépatique doit être considérée dans le diagnostic différentiel.
Insuffisance cardiaque, hépatique et rénale
Chez les patients atteints d'insuffisance cardiaque, hépatique ou rénale sévère ou de pathologies cardiaques ischémiques, le traitement par la testostérone pourrait entraîner des complications sévères caractérisées par un œdème, avec ou sans insuffisance cardiaque congestive. Dans ce cas, le traitement doit être interrompu immédiatement.
Insuffisance hépatique et rénale
Aucune étude n’a été réalisée pour démontrer l’efficacité et la tolérance de NEBIDO chez les patients souffrant d’insuffisance rénale ou hépatique. Par conséquent, NEBIDO doit être utilisé avec prudence chez ces patients.
Insuffisance cardiaque
NEBIDO doit être utilisé avec prudence chez les patients prédisposés aux œdèmes, par exemple en cas d’insuffisance cardiaque, hépatique ou rénale sévère ou de pathologies cardiaques ischémiques, car le traitement par des androgènes peut entrainer une rétention hydrosodée. En cas de complications sévères caractérisées par un œdème avec ou sans insuffisance cardiaque congestive, le traitement doit être interrompu immédiatement (voir rubrique 4.8).
La testostérone peut entraîner une augmentation de la pression artérielle. Par conséquent, NEBIDO doit être utilisé avec précaution chez les hommes présentant une hypertension.
Troubles de la coagulation
En règle générale, les restrictions à l’utilisation d’injections intramusculaires chez les patients ayant des troubles acquis ou héréditaires de la coagulation sanguine doivent être observées.
La testostérone et ses dérivés peuvent majorer l’activité des anticoagulants oraux dérivés de la coumarine (voir également la rubrique 4.5).
La testostérone doit être utilisée avec prudence chez les patients souffrant de thrombophilie ou présentant des facteurs de risque de thromboembolie veineuse (TEV) car des cas d’événements thromboemboliques ont été rapportés chez ces patients sous traitement par testostérone lors d’études et de suivis post-commercialisation (par exemple : thrombose veineuse profonde, embolie pulmonaire, thrombose oculaire). Chez les patients atteints de thrombophilie, des cas de TEV ont été rapportés même sous traitement anticoagulant. Par conséquent, la poursuite du traitement par la testostérone après un premier événement thrombotique doit être évaluée attentivement. En cas de poursuite du traitement, d'autres mesures doivent être prises afin de réduire au maximum le risque de TEV.
Autres
NEBIDO doit être utilisé avec prudence chez les patients souffrant d'épilepsie et de migraine, leur état pouvant s’aggraver sous traitement.
Une amélioration de la sensibilité à l'insuline peut être observée chez les patients traités par androgène et ayant des taux plasmatiques de testostérone normaux sous traitement. Par conséquent, il peut être nécessaire de réduire la dose des agents hypoglycémiants.
Certains signes cliniques de type irritabilité, nervosité, prise de poids, érections prolongées ou fréquentes peuvent témoigner de concentrations sériques d’androgènes trop importantes et nécessiter une adaptation posologique.
Une apnée du sommeil préexistante peut s’aggraver sous traitement.
Les athlètes recevant un traitement de substitution à la testostérone pour hypogonadisme masculin primaire ou secondaire doivent être informés que ce médicament contient une substance active susceptible d’entraîner une réaction positive lors de tests antidopage.
Les androgènes ne sont pas recommandés pour développer la masse musculaire des sujets en bonne santé, ni pour augmenter les capacités physiques.
NEBIDO doit être arrêté définitivement si des symptômes liés à des concentrations sériques d’androgènes trop importantes persistent ou réapparaissent en cours de traitement avec le schéma d’administration recommandé.
Abus médicamenteux et dépendance
La testostérone a fait l’objet d’utilisations abusives, généralement à des doses supérieures à celles recommandées dans l’indication approuvée et en association avec d’autres stéroïdes androgènes anabolisants. L’utilisation abusive de testostérone et d’autres stéroïdes androgènes anabolisants peut provoquer des effets indésirables graves incluant : des événements cardiovasculaires (avec issue fatale dans certains cas), hépatiques et/ou psychiatriques. L’utilisation abusive de testostérone peut entraîner une dépendance et des symptômes de sevrage en cas de réduction significative de la dose ou d’interruption brutale de l’utilisation. L’utilisation abusive de testostérone et d’autres stéroïdes androgènes anabolisants présente de graves risques pour la santé et doit être déconseillée.
Administration
Comme avec toutes les solutions huileuses, NEBIDO doit uniquement être injecté par voie intramusculaire et très lentement (pendant plus de 2 minutes). Une micro-embolie pulmonaire due aux solutions huileuses peut, dans de rares cas, entraîner des signes et symptômes tels que toux, dyspnée, malaise, hyperhidrose, douleurs thoraciques, étourdissements, paresthésies ou syncope. Ces réactions peuvent se produire pendant ou immédiatement après l'injection et elles sont réversibles. Le patient doit donc faire l'objet d'une surveillance régulière pendant et immédiatement après chaque injection de NEBIDO afin de pouvoir reconnaître au plus vite les possibles signes et symptômes d'une micro-embolie pulmonaire due aux solutions huileuses. Le traitement est généralement symptomatique, par exemple par l'administration d'une oxygénothérapie.
Des cas suspectés de réactions anaphylactiques après l’injection de NEBIDO ont été rapportés.
Informations sur les excipients
Ce médicament contient 2000 mg de benzoate de benzyle dans chaque ampoule/flacon de 4 ml, ce qui équivaut à 500 mg/ml.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
La testostérone et ses dérivés peuvent majorer l’activité des anticoagulants oraux dérivés de la coumarine. Les patients sous anticoagulants oraux nécessitent un suivi attentif, tout particulièrement au début et à l’arrêt du traitement par les androgènes. Un contrôle plus fréquent du taux de prothrombine et de l'INR est recommandé.
Insuline et autres médicaments anti-diabétiques
Les androgènes peuvent améliorer la tolérance au glucose et réduire les besoins en insuline ou autres médicaments anti-diabétiques chez les patients diabétiques (voir rubrique 4.4). Les patients atteints de diabète doivent donc faire l’objet d’une surveillance, en particulier au début ou à la fin du traitement et à intervalles réguliers pendant le traitement par Nebido.
L’utilisation concomitante d’un traitement de substitution à base de testostérone et d’inhibiteurs du co-transporteur de sodium-glucose de type 2 (SGLT2) a été associée à une augmentation du risque d’érythrocytose. Les deux substances pouvant chacune provoquer indépendamment une augmentation du taux d’hématocrite, un effet cumulatif est possible (voir également rubrique 4.4). Une surveillance des taux d’hématocrite et d’hémoglobine est recommandée chez les patients recevant ces deux traitements.
Autres interactions
L'administration concomitante de testostérone et d'ACTH ou de corticoïdes peut majorer le risque de survenue d'œdèmes. Par conséquent, ces médicaments doivent être administrés avec prudence, en particulier chez les patients présentant une pathologie cardiaque ou hépatique ou des facteurs de risques d’œdèmes.
Interactions avec des analyses de laboratoire : les androgènes peuvent diminuer les taux de thyroxin-binding globulin, entraînant une réduction des taux sériques de T4 totale et une augmentation du captage sur résine de la T3 et de la T4. Néanmoins, les taux d'hormones thyroïdiennes libres restent inchangés, sans manifestation clinique de dysfonctionnement thyroïdien.
4.6. Fertilité, grossesse et allaitement
Grossesse et allaitement
NEBIDO n’est pas indiqué chez la femme et ne doit pas être utilisé chez les femmes enceintes ou qui allaitent (voir rubrique 4.3).
Fertilité
Un traitement de substitution à la testostérone peut réduire la spermatogénèse de manière réversible (voir rubriques 4.8 et 5.3).
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
NEBIDO n’a aucun effet sur l’aptitude à conduire des véhicules et à utiliser des machines.
Résumé du profil de tolérance
Concernant les effets indésirables associés à l’utilisation d’androgènes, voir aussi la rubrique 4.4.
Les effets indésirables les plus fréquemment rapportés pendant un traitement par NEBIDO sont l’acné et les douleurs au site d’injection.
Une micro-embolie pulmonaire due aux solutions huileuses peut, dans de rares cas, entraîner des signes et symptômes tels que toux, dyspnée, malaise, hyperhidrose, douleurs thoraciques, étourdissements, paresthésies ou syncope. Ces réactions peuvent se produire pendant ou immédiatement après l'injection et sont réversibles. Des cas suspectés de micro-embolie graisseuse pulmonaire ont été rapportés rarement dans les études cliniques (entre ≥ 1 cas / 10 000 injections et < 1 cas / 1000 injections) ainsi que dans l’expérience post-marketing (voir rubrique 4.4).
Des cas suspectés de réactions anaphylactiques après l’injection de NEBIDO ont été rapportés.
Les androgènes pourraient accélérer l'évolution d'un cancer de la prostate infraclinique ou d'une hyperplasie bénigne de la prostate.
Le tableau 1 ci-dessous reporte les effets indésirables rapportés avec NEBIDO selon la classification par classes de systèmes d'organes MedDRA. Les fréquences sont basées sur des données d’essais cliniques et sont définies comme fréquentes (≥ 1/100 à < 1/10), peu fréquentes (≥ 1/1000 à < 1/100) et rares (≥ 1/10000 à < 1/1000). Les effets indésirables ont été enregistrés dans 6 études cliniques (N=422) et un lien de causalité avec NEBIDO est suspecté.
Tableau des effets indésirables
Tableau 1 : effets indésirables chez l'homme classés par fréquence relative, selon la classification MedDRA SOC, sur la base de données poolées issues de 6 essais cliniques, N=422 (100,0 %), soit N=302 hommes hypogonadiques traités avec des injections IM de 4 ml et N=120 avec 3 ml d'undécanoate de testostérone 250 mg/ml.
|
Classe de systèmes d’organes |
Fréquent (≥ 1/100 à < 1/10) |
Peu fréquent (≥ 1/1000 à < 1/100) |
Rare (≥ 1/10000 à < 1/1000) |
|
Affections hématologiques et du système lymphatique |
Polycythémie Augmentation de l’hématocrite* Augmentation de la numération des globules rouges* Augmentation du taux d’hémoglobine* |
|
|
|
Affections du système immunitaire |
|
Hypersensibilité |
|
|
Troubles du métabolisme et de la nutrition |
Prise de poids |
Augmentation de l’appétit Hémoglobine glyquée augmentée Hypercholestérolémie Triglycérides sanguins augmentés Cholestérol sanguin augmenté |
|
|
Affections psychiatriques |
|
Dépression Troubles émotionnels Insomnie Agitation Agressivité Irritabilité |
|
|
Affections du système nerveux |
|
Céphalées Migraine Tremblements |
|
|
Affections vasculaires |
Bouffées de chaleur |
Troubles cardiovasculaires Hypertension Vertiges |
|
|
Affections respiratoires, thoraciques et médiastinales |
|
Bronchite Sinusite Toux Dyspnée Ronflement Dysphonie |
Micro-embolie pulmonaire due aux solutions huileuses** |
|
Affections gastro-intestinales |
|
Diarrhée Nausées |
|
|
Affections hépatobiliaires |
|
Tests de la fonction hépatique anormaux Aspartate aminotransférase augmentée |
|
|
Affections de la peau et du tissu sous-cutané |
Acné |
Alopécie Erythème Rash1 Prurit Sécheresse de la peau |
|
|
Affections musculo-squelettiques et systémiques |
|
Arthralgie Douleur des extrémités Trouble musculaire2 Raideur musculo-squelettique Créatine phosphokinase sanguine augmentée |
|
|
Affections du rein et des voies urinaires |
|
Débit urinaire diminué Rétention urinaire Troubles des voies urinaires Nycturie Dysurie |
|
|
Affections des organes de reproduction et du sein |
Antigène prostatique spécifique augmenté Examen de la prostate anormal Hypertrophie bénigne de la prostate |
Dysplasie prostatique Induration de la prostate Prostatite Trouble prostatique Troubles de la libido Douleurs testiculaires Induration mammaire Douleur mammaire Gynécomastie Estradiol augmenté Testostérone sanguine augmentée |
|
|
Troubles généraux et anomalies au site d’administration |
Divers types de réactions au site d’injection3 |
Fatigue Asthénie Hyperhidrose4 |
|
|
|
|
|
|
* Cette fréquence a été reliée à l’utilisation de médicaments contenant de la testostérone.
** La fréquence dépend du nombre d’injections.
Le terme MedDRA le plus approprié pour décrire une certaine réaction indésirable est listé. Les synonymes ou maladies associées ne sont pas listés, mais doivent aussi être pris en compte.
1 Rash incluant rash papuleux.
2 Trouble musculaire : spasmes musculaires, tension musculaire et myalgie.
3 Divers types de réactions au site d’injection : douleurs, gêne, prurit, érythème, hématome, irritation, réaction.
4 Hyperhidrose : hyperhidrose et sueurs nocturnes.
Description de certains effets indésirables
La 4 de peut, dans de rares cas, entraîner des signes et symptômes tels que toux, dyspnée, malaise, hyperhidrose, douleur thoracique, sensations vertigineuses,, paresthésies ou syncope. Ces réactions peuvent survenir pendant ou immédiatement après l'injection et sont réversibles. Des cas suspectés de micro-embolie graisseuse pulmonaire ont été rapportés rarement dans les études cliniques (entre ≥ 1 cas / 10 000 injections et < 1 cas / 1000 injections) ainsi que dans l’expérience post-marketing (voir rubrique 4.4).
En plus des réactions indésirables mentionnées ci-dessus, nervosité, hostilité, apnée du sommeil, diverses réactions cutanées incluant séborrhée, augmentation de la pilosité, fréquence augmentée des érections et dans de très rares cas jaunisse ont été rapportés sous traitement avec des préparations contenant de la testostérone.
Le traitement avec des doses élevées de testostérone interrompt ou réduit de façon fréquente et réversible la spermatogénèse, réduisant ainsi la taille des testicules; le traitement de substitution à la testostérone de l’hypogonadisme peut dans de rares cas provoquer des érections persistantes et douloureuses (priapisme). L’administration à forte dose ou à long terme de testostérone augmente de façon occasionnelle les cas de rétention d’eau et d’œdème.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
Aucune mesure thérapeutique autre que l’arrêt du traitement ou une réduction de la dose n’est nécessaire après un surdosage.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : Androgènes, code ATC : G03BA03.
Ce médicament est un dérivé du 3-oxoandrostène (4).
L’undécanoate de testostérone est un ester d’un androgène naturel, la testostérone. La forme active, la testostérone, est formée par clivage de la chaîne latérale.
La testostérone est le principal androgène chez l’homme. Elle est principalement synthétisée au niveau des testicules et, en faibles quantités, au niveau du cortex surrénalien.
La testostérone est responsable de l’expression des caractères sexuels masculins au cours du développement fœtal, de la petite enfance et de la puberté et du maintien ultérieur du phénotype masculin et des fonctions androgéno-dépendantes (par exemple la spermatogenèse, les glandes sexuelles accessoires). Elle remplit également d’autres fonctions, par exemple au niveau de la peau, des muscles, du squelette, des reins, du foie, de la moelle osseuse et du système nerveux central.
En fonction de l’organe cible, le spectre d’activité de la testostérone est principalement androgénique (par exemple prostate, vésicules séminales, épididyme) ou anabolisant protidique (muscles, os, hématopoïèse, reins, foie).
Les effets de la testostérone sur certains organes cibles ne se manifestent qu'après conversion au niveau périphérique de la testostérone en œstradiol, qui se lie alors aux récepteurs nucléaires des estrogènes des cellules cibles, par exemple, dans l'hypophyse, le tissu adipeux, le cerveau, l'os et les cellules de Leydig des testicules.
5.2. Propriétés pharmacocinétiques
NEBIDO est une préparation retard d’undécanoate de testostérone administrée par voie intramusculaire et ainsi ne subit pas l’effet de premier passage hépatique. Après injection intramusculaire d’undécanoate de testostérone sous forme de solution huileuse, le composant est progressivement libéré et est presque entièrement clivé par les estérases sériques en testostérone et en acide undécanoïque. Une augmentation des taux sériques de testostérone au-delà des valeurs basales peut s’observer dès le lendemain de l’administration.
Etat d’équilibre
Après la première injection intramusculaire de 1000 mg d’undécanoate de testostérone chez des hommes souffrant d’hypogonadisme, des valeurs moyennes de Cmax de 38 nmol/l (11 ng/ml) ont été obtenues après 7 jours. La seconde dose a été administrée six semaines après la première injection et des concentrations maximales en testostérone de l’ordre de 50 nmol/l (15 ng/ml) étaient atteintes. Un intervalle d’administration constant de dix semaines a été maintenu pour les trois injections suivantes et l’état d’équilibre a été atteint entre la 3ème et la 5ème injection. Les valeurs moyennes de Cmax et de Cmin à l’équilibre ont été d’environ 37 nmol/l (11 ng/ml) et 16 nmol/l (5 ng/ml) respectivement.
La variabilité intra et inter-individuelle médiane (coefficient de variation, %) des valeurs de Cmin a été respectivement de 22 % (9-28 %) et de 34 % (25-48 %).
Distribution
Chez l’homme, environ 98 % de la testostérone circulante dans le sérum se trouve sous forme liée à la SHBG (Sex Hormone Binding Globulin) et à l’albumine. Seule la fraction libre de la testostérone est considérée comme biologiquement active. Après perfusion intraveineuse de testostérone à des hommes âgés, la demi-vie d’élimination de la testostérone était d’environ une heure, avec un volume de distribution apparent de l’ordre de 1,0 l/kg.
Biotransformation
La testostérone, obtenue par clivage de la liaison ester de l’undécanoate de testostérone est métabolisée et excrétée de la même manière que la testostérone endogène. L’acide undécanoïque est métabolisé par β-oxydation de la même manière que les autres acides carboxyliques aliphatiques. Les principaux métabolites actifs de la testostérone sont l’œstradiol et la dihydrotestostérone.
Élimination
La testostérone subit un métabolisme hépatique et extra-hépatique important. Après administration de testostérone marquée, environ 90 % de la radioactivité se retrouvent dans les urines sous forme de conjugués d’acide sulfurique et glucuronique et 6 % dans les selles après circulation entérohépatique. Les métabolites urinaires de ce médicament sont notamment l’androstérone et l’étiocholanolone. Après administration intramusculaire de cette formulation retard, la vitesse de libération se caractérise par une demi-vie de 90 ± 40 jours.
5.3. Données de sécurité préclinique
La testostérone s'est révélée non mutagène in vitro selon le modèle des mutations réverses (test d'Ames) ou des cellules ovariennes de hamster. Lors d’études chez l’animal, un lien entre le traitement par les androgènes et certains cancers a été observé. Des données expérimentales chez les rats ont montré une augmentation de l'incidence du cancer de la prostate après traitement par la testostérone.
Les hormones sexuelles sont connues pour faciliter le développement de certaines tumeurs induites par des agents carcinogènes connus. La signification clinique de cette dernière observation n’est pas connue.
Les études de fertilité chez les rongeurs et les primates ont montré que le traitement par la testostérone est susceptible de diminuer la fertilité par suppression de la spermatogenèse proportionnellement à la dose.
Benzoate de benzyle, huile de ricin raffinée.
5 ans.
Le médicament doit être utilisé immédiatement après 1ère ouverture.
6.4. Précautions particulières de conservation
Pas de précautions particulières de conservation.
6.5. Nature et contenu de l'emballage extérieur
Ampoule
Ampoule en verre brun (de type I) de 5 ml contenant 4 ml de solution ; boîte de 1.
Flacon
Flacon en verre brun (de type I) de 6 ml contenant 4 ml de solution, muni d’un bouchon gris en bromobutyle (recouvert d’un film d’ETFE) scellé par une capsule ; boîte de 1.
6.6. Précautions particulières d’élimination et de manipulation
En cas de stockage à basse température, les propriétés de cette solution à base d’huile peuvent changer temporairement (par ex. viscosité plus élevée, aspect trouble de la solution). En cas de stockage à basse température, le produit doit être ramené à température ambiante ou corporelle avant utilisation.
Inspecter visuellement la solution pour injection intramusculaire avant utilisation et ne l’utiliser que si la solution est limpide et exempte de particules.
Ce médicament est strictement à usage unique et tout reste de solution non utilisé doit être éliminé conformément à la réglementation locale.
Ampoule
Remarques concernant l'ouverture de l'ampoule OPC (One-Point-Cut)
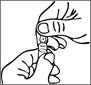
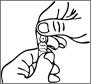
L'ampoule dispose d'une gravure au niveau du point coloré qui permet de casser l'ampoule sans devoir limer le col. Avant d'ouvrir l'ampoule, assurez-vous qu'il ne reste plus de solution dans la partie supérieure de l'ampoule. Utilisez les deux mains pour l'ouverture; tenez la partie inférieure de l'ampoule dans une main et utilisez l'autre main pour casser la partie supérieure dans la direction opposée au point coloré.
|
|
Flacon
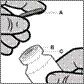
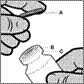
Le flacon est strictement à usage unique. Le contenu d'un flacon doit être injecté par voie intramusculaire immédiatement après son prélèvement dans la seringue. Après avoir retiré le capuchon en plastique (A), ne pas retirer la bague métallique (B) ni la capsule de sertissage (C).
|
|
7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE
TOUR PACIFIC
11-13 COURS VALMY
92800 PUTEAUX
8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE
· 34009 367 582 7 8 : 1 ampoule en verre brun (de type I) de 5 ml contenant 4 ml de solution ; boîte de 1.
· 34009 277 134 5 3 : 1 flacon en verre brun (de type I) de 6 ml contenant 4 ml de solution, muni d’un bouchon gris en bromobutyle (recouvert d’un film d’ETFE) scellé par une capsule ; boîte de 1.
9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION
[à compléter ultérieurement par le titulaire]
10. DATE DE MISE A JOUR DU TEXTE
[à compléter ultérieurement par le titulaire]
Sans objet.
12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES
Liste I.
Prescription initiale réservée aux spécialistes en endocrinologie – diabétologie – nutrition, en urologie, en gynécologie ou en médecine et biologie de la reproduction – andrologie.
ANSM - Mis à jour le : 29/01/2026
NEBIDO 1000 mg/4 ml, solution injectable
Undécanoate de testostérone
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin, votre pharmacien ou votre infirmier/ère.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que NEBIDO 1000 mg/4 ml, solution injectable et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant d'utiliser NEBIDO 1000 mg/4 ml, solution injectable ?
3. Comment utiliser NEBIDO 1000 mg/4 ml, solution injectable ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver NEBIDO 1000 mg/4 ml, solution injectable ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE NEBIDO 1000 mg/4 ml, solution injectable ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : Androgènes - code ATC : G03B A03
NEBIDO contient de la testostérone, une hormone masculine, comme substance active.
NEBIDO est injecté dans un muscle du corps où il peut être stocké et libéré progressivement sur une certaine période de temps.
NEBIDO est utilisé chez l'homme adulte pour remplacer la testostérone afin de traiter divers problèmes de santé dus au manque de testostérone (hypogonadisme masculin). Ce diagnostic doit être confirmé par deux dosages séparés de la testostérone dans le sang, ainsi que par la présence de symptômes tels que :
· impuissance,
· infertilité,
· diminution de la libido,
· fatigue,
· humeur dépressive,
· perte osseuse due aux faibles taux d'hormones.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT D’UTILISER NEBIDO 1000 mg/4 ml, solution injectable ?
N’utilisez jamais NEBIDO 1000 mg/4 ml, solution injectable :
· si vous êtes allergique à la testostérone (undécanoate) ou à l'un des autres composants contenus dans ce médicament mentionnés dans la rubrique 6,
· si vous avez un cancer androgéno-dépendant ou un cancer suspecté de la prostate ou des seins,
· si vous avez ou avez eu une tumeur du foie.
NEBIDO ne doit pas être utilisé chez la femme.
Avertissements et précautions
Prévenez votre médecin ou votre pharmacien avant d’utiliser NEBIDO si vous avez (ou avez déjà eu) :
· une épilepsie,
· des problèmes cardiaques, rénaux ou hépatiques,
· des migraines,
· des interruptions temporaires de la respiration au cours du sommeil (apnée) car celles-ci pourraient s'aggraver,
· un cancer car le taux de calcium dans votre sang peut devoir être dosé régulièrement,
· une pression artérielle élevée (hypertension) ou si vous êtes traité pour une hypertension car la testostérone peut entraîner une augmentation de la pression artérielle,
· des troubles de la coagulation du sang
o des problèmes de saignements (par exemple, l’hémophilie),
o une thrombophilie (une anomalie de la coagulation sanguine qui augmente le risque de thrombose - formation de caillots sanguins dans les vaisseaux sanguins),
o des facteurs qui augmentent le risque de formation de caillots sanguins dans une veine : antécédents de caillots sanguins dans une veine, tabagisme, obésité, cancer, immobilisation, si un membre de votre famille proche a eu un caillot sanguin dans une jambe, un poumon ou un autre organe à un âge jeune (par exemple, avant environ 50 ans), ou à mesure que votre âge augmente.
Comment reconnaître un caillot sanguin : gonflement douloureux d'une jambe ou changement soudain de la couleur de la peau qui par exemple devient pâle, rouge ou bleue, essoufflement soudain, toux soudaine et inexpliquée pouvant faire cracher du sang ou douleur soudaine dans la poitrine, sensation d’étourdissement importante ou vertige, douleur intense à l’estomac, perte de vision brutale. Consultez immédiatement un médecin si vous présentez l'un de ces symptômes.
Si vous souffrez d'une maladie grave du cœur, du foie ou des reins, le traitement par NEBIDO peut entraîner des complications sévères se manifestant par une rétention d'eau dans le corps, parfois accompagnée d'une insuffisance cardiaque (congestive).
Les analyses sanguines suivantes devront être effectuées par votre médecin avant et pendant le traitement : taux de testostérone dans le sang, analyse complète des cellules du sang (numération-formule sanguine).
Si votre foie ne fonctionne pas
Aucune étude formelle n'a été réalisée chez des patients présentant une insuffisance hépatique. NEBIDO ne vous sera pas prescrit si vous avez déjà eu une tumeur du foie (voir le paragraphe "N'utilisez jamais NEBIDO").
Enfants et adolescents
NEBIDO ne doit pas être utilisé chez l'enfant et l'adolescent. Il n’y a pas de données disponibles sur l’utilisation de NEBIDO chez les garçons de moins de 18 ans.
Patients âgés (65 ans et plus)
Le médecin n'a pas besoin d'ajuster la dose si vous avez plus de 65 ans (voir le paragraphe "Examen médical/suivi").
Développement musculaire et contrôles antidopage
NEBIDO n’est pas indiqué pour développer les muscles chez les individus en bonne santé ou pour augmenter la force physique.
NEBIDO peut induire une réaction positive des tests pratiqués lors des contrôles antidopage.
Abus médicamenteux et dépendance
Utilisez toujours ce médicament en suivant exactement les indications de votre médecin ou votre pharmacien.
L’abus de testostérone, en particulier si vous utilisez trop ce médicament seul ou en association avec d’autres stéroïdes androgènes anabolisants, peut provoquer de graves problèmes de santé affectant votre cœur et vos vaisseaux sanguins (qui peuvent entraîner le décès), votre santé mentale et/ou votre foie.
Les personnes ayant abusé de la testostérone peuvent devenir dépendantes et ressentir des symptômes de manque lorsque la posologie est modifiée significativement ou lorsque l’utilisation est interrompue brutalement. Vous ne devez pas utiliser ce médicament de manière abusive, seul ou en association avec d’autres stéroïdes androgènes anabolisants car cela peut entraîner de graves risques pour la santé (voir la rubrique 4. « QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ? »).
Examen médical/suivi
Les hormones masculines peuvent accélérer l’évolution d'un cancer de la prostate ou d’une augmentation du volume de la prostate (hypertrophie bénigne de la prostate). Avant l'injection de NEBIDO, votre médecin vous examinera afin de vérifier que vous ne souffrez pas d'un cancer de la prostate.
Votre médecin réalisera des examens réguliers de la prostate et des seins, en particulier si vous êtes âgé. Il effectuera aussi des prises de sang régulières.
Après l'utilisation de substances hormonales telles que les androgènes, des cas de tumeurs du foie bénignes (non cancéreuses) et malignes (cancéreuses) ont été observés.
Autres médicaments et NEBIDO 1000 mg/4 ml, solution injectable
Si vous prenez, avez pris récemment ou pourriez prendre un autre médicament, y compris un médicament obtenu sans ordonnance, parlez-en à votre médecin ou à votre pharmacien. Le médecin devra peut-être ajuster la dose si vous utilisez l'un des produits suivants :
· l'hormone ACTH ou des corticoïdes (utilisés pour traiter diverses affections telles que les rhumatismes, l'arthrite, les maladies allergiques et l'asthme) : NEBIDO peut accroître le risque de rétention d'eau, notamment si votre cœur et votre foie ne fonctionnent pas correctement,
· des médicaments qui fluidifient le sang (des anticoagulants oraux dérivés de la coumarine) car cela peut augmenter le risque de saignement. Votre médecin vérifiera la dose.
· des médicaments utilisés pour traiter le diabète. Il peut être nécessaire d'ajuster la dose du médicament qui fait baisser votre taux de sucre dans le sang. Comme d'autres substances androgènes, la testostérone peut augmenter l'effet de l'insuline. La prise d’inhibiteurs du SGLT2 (par exemple, empagliflozine, dapagliflozine ou canagliflozine) en association avec la testostérone pourrait entrainer une augmentation du nombre de vos globules rouges dans le sang. Votre médecin pourrait être amené à surveiller votre sang plus régulièrement.
Assurez-vous d'informer votre médecin si vous êtes atteint d'un trouble de la coagulation du sang, car il est important pour votre médecin de le savoir avant qu’il ne décide de vous injecter NEBIDO.
NEBIDO peut également modifier les résultats de certains examens biologiques (par exemple les examens de la glande thyroïde). Veuillez indiquer à votre médecin ou au laboratoire que vous utilisez NEBIDO.
Grossesse, allaitement et fertilité
Grossesse et allaitement
NEBIDO n'est pas indiqué chez la femme et ne doit pas être utilisé chez les femmes enceintes ou qui allaitent.
Fertilité
Un traitement par de fortes doses de testostérone peut fréquemment arrêter ou réduire la production de spermatozoïdes de manière réversible (voir également la rubrique « QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ? ».
Conduite de véhicules et utilisation de machines
Aucun effet sur l'aptitude à conduire des véhicules ou à utiliser des machines n’a été observé avec NEBIDO.
NEBIDO 1000 mg/4 ml, solution injectable contient du benzoate de benzyle
Ce médicament contient 2000 mg de benzoate de benzyle dans chaque ampoule/flacon de 4ml, ce qui équivaut à 500 mg/ml.
3. COMMENT UTILISER NEBIDO 1000 mg/4 ml, solution injectable ?
Posologie/Mode d'administration
Votre médecin injectera NEBIDO (1 ampoule/flacon) très lentement dans un muscle. Il vous administrera les injections toutes les 10 à 14 semaines.
Cela suffit pour maintenir des taux de testostérone suffisants sans entraîner d'accumulation de testostérone dans le sang.
NEBIDO doit être uniquement injecté par voie intramusculaire. Il faut prêter particulièrement attention à ne pas faire d'injection dans un vaisseau sanguin (voir le paragraphe « Administration »).
Début du traitement
Votre médecin mesurera les taux sanguins de testostérone avant le début du traitement et pendant les premiers temps du traitement. Votre médecin peut réduire l'intervalle entre les deux premières injections à un minimum de 6 semaines afin d'atteindre rapidement le taux nécessaire de testostérone. Cela dépendra de vos symptômes et de votre taux de testostérone.
Maintien des taux de NEBIDO au cours du traitement
L'intervalle recommandé entre deux injections est toujours de 10 à 14 semaines.
Votre médecin mesurera régulièrement les taux sanguins de testostérone à la fin de l'intervalle entre deux injections pour s’assurer que celui-ci est correct. Si le taux est trop faible, votre médecin peut décider de vous faire des injections plus souvent. Si votre taux de testostérone est trop élevé, votre médecin peut décider de vous faire des injections moins souvent. Ne manquez pas les visites prévues pour les injections sinon votre taux optimal de testostérone ne sera pas maintenu.
Si vous pensez que les effets de NEBIDO sont trop importants ou pas assez importants, parlez-en à votre médecin.
Si vous avez utilisé plus de NEBIDO 1000 mg/4 ml, solution injectable que vous n’auriez dû :
Les symptômes associés à l'utilisation d'une trop grande quantité de NEBIDO sont les suivants :
· irritabilité,
· nervosité,
· prise de poids,
· érections fréquentes ou prolongées.
Si vous présentez l'un de ces symptômes, signalez-le à votre médecin. Celui-ci fera des injections moins fréquentes ou arrêtera le traitement.
Si vous oubliez d’utiliser NEBIDO 1000 mg/4 ml, solution injectable :
Sans objet.
Si vous arrêtez d’utiliser NEBIDO 1000 mg/4 ml, solution injectable :
Sans objet.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Les effets indésirables les plus fréquents sont l'acné et les douleurs au site d'injection.
Effets indésirables fréquents (peuvent toucher jusqu’à 1 patient sur 10) :
· nombre anormalement élevé de globules rouges,
· prise de poids,
· bouffées de chaleur,
· acné,
· augmentation du volume de la prostate et problèmes associés,
· diverses réactions au site d'injection (douleur, ecchymoses, ou irritation).
Effets indésirables peu fréquents (peuvent toucher jusqu’à 1 patient sur 100) :
· réaction allergique,
· augmentation de l'appétit, modifications des résultats des tests sanguins (c’est-à-dire sucres ou graisses du sang augmentés),
· dépression, trouble émotionnel, insomnie, agitation, agressivité ou irritabilité,
· maux de tête, migraine, ou tremblement,
· affection cardiovasculaire, hypertension artérielle, ou étourdissements,
· bronchite, sinusite, toux, essoufflement, ronflements, ou problèmes de voix,
· diarrhée ou nausées,
· changements des résultats des tests hépatiques,
· perte de cheveux, ou diverses réactions cutanées (c’est-à-dire démangeaisons, rougeur, ou sécheresse de la peau),
· douleurs articulaires, douleurs dans les membres, problèmes musculaires (spasme, douleur ou raideur), ou augmentation de la créatine phosphokinase dans le sang,
· troubles urinaires (c’est-à-dire diminution du débit d'urine, rétention urinaire, besoin soudain et urgent d’uriner survenant la nuit (impériosité mictionnelle nocturne)),
· troubles de la prostate (c’est-à-dire dysplasie prostatique, ou durcissement ou inflammation de la prostate), modification du désir sexuel (libido), douleurs testiculaires, douleur, durcissement ou hypertrophie des seins, ou taux augmentés des hormones masculines et féminines,
· fatigue, sensation générale de faiblesse, transpiration accrue, ou sueurs nocturnes.
Effets indésirables rares (peuvent toucher jusqu’à 1 patient sur 1000) :
· La solution huileuse de NEBIDO pourrait atteindre les poumons (micro-embolie pulmonaire due aux solutions huileuses), ce qui peut conduire dans de rares cas à des signes et symptômes tels que toux, difficultés à respirer, sensation générale de malaise, transpiration accrue, douleur dans la poitrine, étourdissements, fourmillements, ouévanouissement. Ces réactions peuvent se produire pendant ou immédiatement après l'injection et sont réversibles. Le patient devra donc être surveillé pendant et immédiatement après chaque injection afin que les éventuels signes et symptômes d’une micro-embolie pulmonaire due aux solutions huileuses puissent être détectés rapidement.
Des cas suspectés de réactions anaphylactiques après l’injection de NEBIDO ont été rapportés.
En plus des effets indésirables mentionnés ci-dessus, les effets suivants ont été rapportés avec des préparations contenant de la testostérone : nervosité, hostilité, interruptions brèves de la respiration pendant le sommeil, diverses réactions cutanées dont pellicules et peau grasse, augmentation de la pilosité, érections plus fréquentes et de très rares cas de jaunissement de la peau et des yeux (jaunisse).
Un traitement à doses élevées de testostérone interrompt ou réduit fréquemment et de manière réversible la spermatogénèse.
Le traitement de substitution par la testostérone en cas d'insuffisance de fonctionnement des testicules (hypogonadisme) peut, dans de rares cas, provoquer des érections persistantes et douloureuses (priapisme). L'administration de doses élevées ou à long terme de testostérone augmente occasionnellement les cas de rétention d'eau et d'œdème (gonflement dû à la rétention d'eau).
Un risque fréquent d’augmentation du nombre de globules rouges, de l'hématocrite (pourcentage de globules rouges dans le sang) et du taux d’hémoglobine (la partie des globules rouges qui transporte l’oxygène), révélée par les prises de sang régulières, a été observé pour les médicaments à base de testostérone.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin, votre pharmacien ou à votre infirmier/ère. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet: https://signalement.social-sante.gouv.fr/.
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER NEBIDO 1000 mg/4 ml, solution injectable ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur la boîte et l'étiquette après « EXP ». La date de péremption fait référence au dernier jour de ce mois.
Pas de précautions particulières de conservation.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient NEBIDO 1000 mg/4 ml, solution injectable
· La substance active est : l’undécanoate de testostérone : 250 mg/ml (correspondant à 157,9 mg de testostérone).
Chaque ampoule/flacon contient 1000 mg d’undécanoate de testostérone (correspondant à 631,5 mg de testostérone).
· Les autres composants (excipients) sont : le benzoate de benzyle et l’huile de ricin raffinée.
Qu’est-ce que NEBIDO 1000 mg/4 ml, solution injectable et contenu de l’emballage extérieur
NEBIDO est une solution huileuse limpide incolore à brun-jaunâtre.
Le contenu de l'emballage extérieur est :
1 ampoule/flacon en verre brun contenant 4 ml de solution injectable.
Titulaire de l’autorisation de mise sur le marché
TOUR PACIFIC
11-13 COURS VALMY
92800 PUTEAUX
Exploitant de l’autorisation de mise sur le marché
TOUR PACIFIC
11-13 COURS VALMY
92800 PUTEAUX
MÜLLERSTRASSE 178
13353 BERLIN
ALLEMAGNE
EVER PHARMA JENA GMBH
BRÜSSELER STRASSE 18
07747 JENA
ALLEMAGNE
OU
GRÜNENTHAL GMBH
ZIEGLERSTRASSE 6
52078 AACHEN
ALLEMAGNE
OU
GRÜNENTHAL PHARMACEUTICALS GMBH & CO. KG
PHILIPP-OTT-STRASSE 3
51373 LEVERKUSEN
ALLEMAGNE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
< {MM/AAAA}>< {mois AAAA}.>
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).
Les informations suivantes sont destinées exclusivement aux professionnels de santé :
En cas de stockage à basse température, les propriétés de cette solution à base d’huile peuvent changer temporairement (par ex. viscosité plus élevée, aspect trouble de la solution). En cas de stockage à basse température, le produit doit être ramené à température ambiante ou corporelle avant utilisation. La solution pour injection intramusculaire doit être inspectée visuellement avant utilisation et seules les solutions claires exemptes de particules doivent être utilisées.
Le contenu d'une ampoule/d’un flacon doit être injecté par voie intramusculaire immédiatement après l'ouverture de l'ampoule/du flacon.
Le médicament est à usage unique et toute solution inutilisée doit être éliminée.
Administration
Il faut prêter particulièrement attention à ne pas faire d'injection intravasculaire.
Comme avec toutes les solutions huileuses, NEBIDO doit être injecté par voie intramusculaire stricte et très lentement. Une micro-embolie pulmonaire de solution huileuse peut, dans de rares cas, entraîner des signes et symptômes tels que toux, dyspnée, malaise, hyperhidrose, douleurs thoraciques, étourdissements, paresthésies ou syncope. Ces réactions peuvent se produire pendant ou immédiatement après l'injection et sont réversibles. Le traitement est généralement symptomatique, par exemple par l'administration d'une oxygénothérapie.
Des cas suspectés de réactions anaphylactiques après l’injection de NEBIDO ont été rapportés.
Mises en garde
Une surveillance attentive et régulière de la prostate et des glandes mammaires doit être réalisée selon les méthodes recommandées (toucher rectal et dosage du PSA) chez les patients traités par la testostérone une fois par an au moins et deux fois par an chez les sujets âgés et les patients à risque (ceux avec des facteurs cliniques ou familiaux).
En plus des examens biologiques des taux de testostérone chez les patients recevant un traitement androgénique au long cours, les paramètres biologiques suivants doivent être contrôlés régulièrement : taux d’hémoglobine, hématocrite, fonction hépatique et bilan lipidique.
Chez les patients atteints d'insuffisance cardiaque, hépatique ou rénale sévère ou de pathologies cardiaques ischémiques, le traitement par la testostérone pourrait entraîner des complications sévères caractérisées par un œdème, avec ou sans insuffisance cardiaque congestive. Dans ce cas, le traitement doit être interrompu immédiatement.
Remarques concernant l'ouverture de l'ampoule OPC (One-Point-Cut)
L'ampoule dispose d'une gravure au niveau du point coloré qui permet de casser l'ampoule sans devoir limer le col. Avant d'ouvrir l'ampoule, assurez-vous qu'il ne reste plus de solution dans la partie supérieure de l'ampoule. Utilisez les deux mains pour l'ouverture ; tenez la partie inférieure de l'ampoule dans une main et utilisez l'autre main pour casser la partie supérieure dans la direction opposée au point coloré.
|
|
Remarques concernant l'ouverture du flacon
Le flacon est strictement à usage unique. Le contenu d'un flacon doit être injecté par voie intramusculaire immédiatement après son prélèvement dans la seringue. Après avoir retiré le capuchon en plastique (A), ne pas retirer la bague métallique (B) ni la capsule de sertissage (C).
|
|