Dernière mise à jour le 28/04/2026
CRESTOR 5 mg, comprimé pelliculé
Indications thérapeutiques
Classe pharmacothérapeutique : Inhibiteur de l’HMG-CoA réductase - code ATC : C10A A07
CRESTOR appartient au groupe des médicaments appelés statines.
CRESTOR vous a été prescrit parce que :
· Vous avez un taux élevé de cholestérol ce qui signifie que vous présentez un risque de faire une attaque cardiaque ou un accident vasculaire cérébral. CRESTOR est utilisé chez les adultes, les adolescents et les enfants âgés de 6 ans et plus pour traiter un taux de cholestérol élevé.
· Il vous est recommandé de prendre des statines, car parfois un régime alimentaire adapté et une activité physique ne suffisent pas à corriger votre taux de cholestérol. Vous devez poursuivre le régime hypocholestérolémiant et l’activité physique en même temps que la prise de CRESTOR.
Ou
· Vous avez d’autres facteurs qui augmentent votre risque d’avoir une attaque cardiaque, un accident vasculaire cérébral ou des problèmes de santé liés à ces facteurs.
Une attaque cardiaque, un accident vasculaire cérébral ou des problèmes de santé liés à ces facteurs peuvent être causés par une maladie appelée l’athérosclérose. L’athérosclérose est due à une accumulation de dépôts de graisse dans vos artères.
Pourquoi il est important de continuer de prendre CRESTOR :
CRESTOR est utilisé pour corriger le taux de substances graisseuses dans le sang appelées lipides, le plus fréquent étant le cholestérol.
Il y a différents types de cholestérol trouvé dans le sang : le « mauvais cholestérol » (LDL-C) et le « bon cholestérol » (HDL-C).
· CRESTOR peut réduire le « mauvais cholestérol » et augmenter le « bon cholestérol ».
· Il agit en aidant à bloquer la production de « mauvais cholestérol » par votre organisme. Il améliore également l’aptitude de votre corps à l’éliminer de votre sang.
Pour la plupart des personnes, un taux de cholestérol élevé n’a pas de conséquence sur la façon dont elles se sentent parce que cela n’entraîne aucun symptôme. Cependant, sans traitement, des dépôts graisseux peuvent s’accumuler sur la paroi des vaisseaux sanguins et réduire leur diamètre.
Parfois, ce rétrécissement des vaisseaux peut empêcher le passage du sang jusqu’au cœur ou au cerveau conduisant à une attaque cardiaque ou un accident vasculaire cérébral.
En diminuant votre taux de cholestérol, vous pouvez réduire le risque d’avoir une attaque cardiaque, un accident vasculaire cérébral ou des problèmes de santé qui y sont liés.
Il est très important de continuer à prendre CRESTOR, même si votre taux de cholestérol revient à la normale, parce qu’il prévient la remontée de votre taux de cholestérol et donc l’accumulation de dépôts de graisse. Cependant, vous devez arrêter votre traitement si votre médecin vous le dit, ou si vous découvrez que vous êtes enceinte.
Présentations
> plaquette(s) aluminium de 30 comprimé(s)
Code CIP : 369 853-8 ou 34009 369 853 8 4
Déclaration de commercialisation : 23/09/2009
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 6,34 €
- Honoraire de dispensation : 1,02 €
- Prix honoraire compris : 7,36 €
- Taux de remboursement :65%
> plaquette(s) aluminium de 90 comprimé(s)
Code CIP : 391 690-0 ou 34009 391 690 0 2
Déclaration de commercialisation : 29/09/2009
Cette présentation est agréée aux collectivités
- Prix hors honoraire de dispensation : 18,90 €
- Honoraire de dispensation : 2,76 €
- Prix honoraire compris : 21,66 €
- Taux de remboursement :65%
Service médical rendu (SMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprès de la HAS (plus d'informations dans l'aide). Les avis et synthèses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur du SMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| Important | Avis du 20/02/2019 | Extension d'indication | Le service médical rendu par CRESTOR est important dans : • le traitement des enfants âgés de 6 à 9 ans atteints d’hypercholestérolémie familiale hétérozygote, en complément d’un régime lorsque la réponse au régime et aux autres traitements non pharmacologiques n’est pas suffisante, • le traitement des enfants et adolescents âgés de 6 à 17 ans avec hypercholestérolémie familiale homozygote, en complément d’un régime et d’autres traitements hypolipidémiants (notamment l’aphérèse des LDL) ou lorsque ces traitements ne sont pas appropriés. |
| Insuffisant | Avis du 20/02/2019 | Extension d'indication | Le service médical rendu par CRESTOR est insuffisant pour justifier d’une prise en charge par la solidarité nationale dans le traitement des enfants âgés de 6 à 9 ans atteints d’hypercholestérolémies pures non familiales ou de dyslipidémies mixtes, en complément d’un régime lorsque la réponse au régime et aux autres traitements non pharmacologiques n’est pas suffisante. |
| Important | Avis du 20/02/2019 | Renouvellement d'inscription (CT) | Le service médical rendu par CRESTOR reste important dans : • le traitement des adultes avec : - hypercholestérolémies pures (type IIa incluant les hypercholestérolémies familiales hétérozygotes) ou dyslipidémies mixtes (type IIb), en complément d’un régime lorsque la réponse au régime et aux autres traitements non pharmacologiques (exercice, perte de poids) n’est pas suffisante, - hypercholestérolémies familiales homozygotes, en complément d’un régime et d’autres traitements hypolipidémiants (notamment l’aphérèse des LDL) ou lorsque ces traitements ne sont pas appropriés. • le traitement des enfants et adolescents âgés de 10 ans ou plus avec hypercholestérolémies familiales hétérozygotes, en complément d’un régime lorsque la réponse au régime et aux autres traitements non pharmacologiques (exercice, perte de poids) n’est pas suffisante, • la prévention des événements cardiovasculaires majeurs chez les patients estimés à haut risque de faire un premier événement cardiovasculaire, en complément de la correction des autres facteurs de risque. |
| Insuffisant | Avis du 20/02/2019 | Renouvellement d'inscription (CT) | Le service médical rendu par CRESTOR est insuffisant pour justifier d’une prise en charge par la solidarité nationale dans le traitement des enfants et adolescents âgés de 10 ans ou plus avec hypercholestérolémies non familiales ou dyslipidémies mixtes, en complément d’un régime lorsque la réponse au régime et aux autres traitements non pharmacologiques (exercice, perte de poids) n’est pas suffisante. |
Amélioration du service médical rendu (ASMR)
Les libellés affichés ci-dessous ne sont que des résumés ou extraits issus des avis rendus par la Commission de la Transparence. Seul l'avis complet de la Commission de la Transparence fait référence.
Cet avis est consultable à partir du lien `Avis du jj/mm/aaaa` ou encore sur demande auprés de la HAS (plus d'informations dans l'aide). Les avis et synthéses d'avis contiennent un paragraphe sur la place du médicament dans la stratégie thérapeutique.
| Valeur de l'ASMR | Avis | Motif de l'évaluation | Résumé de l'avis |
|---|---|---|---|
| V (Inexistant) | Avis du 20/02/2019 | Extension d'indication | CRESTOR n’apporte pas d’amélioration du service médical rendu (ASMR V) dans la stratégie thérapeutique actuelle de prise en charge de l’hypercholestérolémie familiale hétérozygote chez les enfants âgés de 6 à 9 ans. La stratégie thérapeutique comprend les comparateurs mentionnés dans le Chapitre 06 de cet avis. CRESTOR n’apporte pas d’amélioration du service médical rendu (ASMR V) dans la stratégie thérapeutique actuelle de prise en charge de l’hypercholestérolémie familiale homozygote chez les enfants et adolescents âgés de 6 à 17 ans. La stratégie thérapeutique comprend les comparateurs mentionnés dans le Chapitre 06 de cet avis. |
| V (Inexistant) | Avis du 23/07/2014 | Inscription (CT) | Les spécialités CRESTOR 5, 10 et 20 mg en boîte de 60 comprimés sont des compléments de gamme qui n’apportent pas d’amélioration du service médical rendu (ASMR V, inexistante) par rapport aux présentations déjà inscrites (CRESTOR 5 mg, 10 mg et 20 mg en comprimés pelliculés en boites de 30, 50 et 90). |
| V (Inexistant) | Avis du 06/10/2010 | Extension d'indication | Chez les enfants et adolescents de 10 à 17 ans avec hypercholestérolémie familiale hétérozygote, l'efficacité de CRESTOR repose sur les résultats de l'étude PLUTO. Compte tenu de la méthodologie de cette étude (faible effectif, courte durée de suivi, inclusion de patients en majorité pubères, exclusion des patients intolérants aux statines) et de l'absence de données relatives à l'impact potentiel du traitement sur la croissance et la maturité sexuelle des patients, CRESTOR n'apporte pas d'amélioration du service médical rendu (ASMR V) par rapport à la pravastatine. |
| V (Inexistant) | Avis du 06/10/2010 | Extension d'indication | La Commission de la Transparence considère que CRESTOR n'apporte pas d'amélioration su service médical rendu (ASMR V) dans la prise en charge des patients à haut risque de faire un premier événement cardiovasculaire. |
| Commentaires sans chiffrage de l'ASMR | Avis du 01/04/2009 | Renouvellement d'inscription (CT) | Dans les hypercholestérolémies familiales homozygotes, en l'absence de nouvelles données disponibles, CRESTOR conserve l'ASMR attribuée dans son avis du 12 et 26 novembre 2003. |
| V (Inexistant) | Avis du 01/04/2009 | Renouvellement d'inscription (CT) | Dans les hypercholestérolémies pures ou les dyslipidémies mixtes, CRESTOR n'apporte pas d'amélioration du service médical rendu (ASMR V) par rapport aux autres statines. |
| V (Inexistant) | Avis du 01/04/2009 | Inscription (CT) | Complément de gamme, absence d'amélioration du service médical rendu (ASMR V). |
ANSM - Mis à jour le : 22/10/2025
CRESTOR 5 mg, comprimé pelliculé
2. COMPOSITION QUALITATIVE ET QUANTITATIVE
Sous forme de rosuvastatine calcique
Pour un comprimé pelliculé
Chaque comprimé contient 94,88 mg de lactose monohydraté.
Pour la liste complète des excipients, voir rubrique 6.1.
Comprimé de couleur jaune, rond, gravé « ZD4522 » et « 5 » sur une face et lisse sur l’autre face.
4.1. Indications thérapeutiques
Traitement des hypercholestérolémies
Adultes, adolescents et enfants âgés de 6 ans ou plus avec hypercholestérolémies pures (type IIa incluant les hypercholestérolémies familiales hétérozygotes) ou dyslipidémies mixtes (type IIb) en complément d’un régime lorsque la réponse au régime et aux autres traitements non pharmacologiques (exercice, perte de poids) n’est pas suffisante.
Adultes, adolescents et enfants âgés de 6 ans ou plus avec hypercholestérolémie familiale homozygote, en complément d’un régime et d’autres traitements hypolipidémiants (notamment l’aphérèse des LDL) ou lorsque ces traitements ne sont pas appropriés.
Prévention des événements cardiovasculaires
Prévention des événements cardiovasculaires majeurs chez les patients estimés à haut risque de faire un premier événement cardiovasculaire (voir rubrique 5.1), en complément de la correction des autres facteurs de risque.
4.2. Posologie et mode d'administration
Avant de débuter le traitement, le patient doit suivre un régime hypocholestérolémiant adapté qu’il devra continuer pendant toute la durée du traitement.
La posologie sera adaptée selon l’objectif thérapeutique et la réponse du patient, en fonction des recommandations en vigueur.
CRESTOR peut être administré à tout moment de la journée, indépendamment des repas.
Traitement des hypercholestérolémies
La dose initiale recommandée est de 5 ou 10 mg une fois/jour par voie orale aussi bien chez les patients naïfs que chez les patients précédemment traités par un autre inhibiteur de l’HMG-CoA Réductase. Pour un patient donné, le choix de la dose initiale devra tenir compte du taux de LDL-C, du risque cardiovasculaire potentiel ainsi que du risque de survenue d’effets indésirables.
Une augmentation de la posologie à la dose supérieure peut se faire après 4 semaines si besoin est (voir rubrique 5.1).
Compte-tenu de l’augmentation du nombre d’effets indésirables observés à la dose de 40 mg par rapport aux doses plus faibles (voir rubrique 4.8), une dose maximale de 40 mg (2 fois 20 mg) ne sera envisagée que chez des patients présentant une hypercholestérolémie sévère avec un risque cardiovasculaire élevé (en particulier ceux présentant une hypercholestérolémie familiale) n’ayant pas atteint l’objectif thérapeutique fixé à une dose de 20 mg/jour et qui feront l’objet d’un suivi régulier (voir rubrique 4.4). Il est recommandé que l’avis d’un spécialiste soit pris lors de l’initiation d’une dose à 40 mg.
Prévention des événements cardiovasculaires
Dans l’étude de réduction du risque des événements cardiovasculaires, la dose utilisée était de 20 mg une fois par jour (voir rubrique 5.1).
Population pédiatrique
L’utilisation en pédiatrie doit être exclusivement réservée aux spécialistes.
Enfants et adolescents de 6 à 17 ans (stades II-V sur l’échelle de Tanner).
Hypercholestérolémie familiale hétérozygote
Chez les enfants et les adolescents ayant une hypercholestérolémie familiale hétérozygote, la dose d’initiation usuelle est de 5 mg par jour.
· Chez les enfants âgés de 6 à 9 ans présentant une hypercholestérolémie familiale hétérozygote, la dose usuelle varie entre 5 et 10 mg une fois par jour par voie orale. La sécurité d’emploi et l’efficacité des doses supérieures à 10 mg n’ont pas été étudiées dans cette population.
· Chez les enfants âgés de 10 à 17 ans présentant une hypercholestérolémie familiale hétérozygote, la dose usuelle moyenne varie entre 5 et 20 mg une fois par jour par voie orale. La sécurité d’emploi et l’efficacité des doses supérieures à 20 mg n’ont pas été étudiées dans cette population.
Les ajustements posologiques doivent être réalisés en fonction de la réponse individuelle et de la tolérance au traitement de la population pédiatrique, en tenant compte des recommandations sur les traitements pédiatriques (voir rubrique 4.4). Les enfants et adolescents doivent suivre un régime hypocholestérolémiant standard avant l’initiation du traitement par rosuvastatine, le régime devant être poursuivi pendant la période de traitement.
Hypercholestérolémie familiale homozygote
Chez les enfants âgés de 6 à 17 ans présentant une hypercholestérolémie familiale homozygote, la dose maximale recommandée est de 20 mg une fois par jour.
Une dose initiale de 5 à 10 mg administrée une fois par jour est recommandée en fonction de l’âge, du poids et de l’utilisation précédente d’une statine. Les ajustements posologiques jusqu’à une dose maximale de 20 mg une fois par jour doivent être réalisés en fonction de la réponse individuelle et de la tolérance au traitement de la population pédiatrique en tenant compte des recommandations sur les traitements pédiatriques (voir rubrique 4.4). Les enfants et adolescents doivent suivre un régime hypocholestérolémiant standard avant l’initiation du traitement par rosuvastatine, le régime devant être poursuivi pendant la période de traitement.
L’expérience est limitée pour des doses autres que 20 mg dans cette population.
La dose de 40 mg ne doit pas être utilisée dans la population pédiatrique.
Enfants de moins de 6 ans
La sécurité d’emploi et l’efficacité de l’utilisation chez les enfants de moins de 6 ans n’ont pas été étudiées. Pour cette raison, CRESTOR n’est pas recommandé chez les enfants âgés de moins de 6 ans.
Utilisation chez le sujet âgé :
Une dose initiale de 5 mg est recommandée chez les patients > 70 ans (voir rubrique 4.4).
Aucun autre ajustement thérapeutique lié à l’âge n’est nécessaire.
Posologie chez l’insuffisant rénal :
En cas d’insuffisance rénale légère à modérée, aucun ajustement posologique n’est nécessaire.
Une dose initiale de 5 mg est recommandée chez les patients avec une insuffisance rénale modérée (clairance de la créatinine < 60ml/min),
La dose de 40 mg est également contre-indiquée chez les patients avec une insuffisance rénale modérée.
En cas d’insuffisance rénale sévère, tous les dosages de CRESTOR sont contre-indiqués (voir rubriques 4.3 et 5.2).
Posologie chez l’insuffisant hépatique :
Chez les patients avec un score de Child-Pugh ≤ 7, aucune augmentation de l’exposition systémique à la rosuvastatine n’a été observée.
Chez les patients avec un score de Child-Pugh de 8 ou 9 : une augmentation de l’exposition systémique à la rosuvastatine a été observée (voir rubrique 5.2). Chez ces patients une évaluation de la fonction rénale sera réalisée (voir rubrique 4.4).
Chez les patients avec un score de Child-Pugh > 9 : aucune donnée n’est disponible.
CRESTOR est contre-indiqué chez les patients présentant une affection hépatique évolutive (voir rubrique 4.3).
Particularités ethniques
Une augmentation de l’exposition systémique a été observée chez les sujets asiatiques (voir rubriques 4.3, 4.4 et 5.2). Une dose initiale de 5 mg est recommandée chez les patients ayant des origines asiatiques. La dose de 40 mg est contre-indiquée chez ces patients.
Polymorphismes génétiques :
Il a été montré que les génotypes SLCO1B1 (OATP1B1) c.521CC et ABCG2 (BCRP) c.421AA sont associés à une augmentation de l’exposition à la rosuvastatine.
Pour les patients connus pour avoir le génotype c.521CC ou c.421AA, la moitié de la dose habituellement recommandée et une dose maximum de 20 mg par jour sont recommandées (voir rubriques 4.4, 4.5 et 5.2).
Posologie chez les patients présentant des facteurs prédisposant de myopathie :
La dose initiale recommandée est de 5 mg chez les patients présentant des facteurs prédisposant de myopathie (voir rubrique 4.4).
La dose de 40 mg est contre-indiquée chez ces patients (voir rubrique 4.3).
Traitements concomitants
La rosuvastatine est un substrat de divers transporteurs protéiques (par exemple OATP1B1 et BCRP). Le risque de myopathie (y compris de rhabdomyolyse) est augmenté lorsque CRESTOR est administré de façon concomitante avec certains médicaments qui peuvent augmenter la concentration plasmatique de rosuvastatine en raison de leurs interactions avec ces transporteurs protéiques (par exemple la ciclosporine, ticagrélor et certains inhibiteurs de protéases, y compris des associations de ritonavir avec l’atazanavir, le lopinavir et/ou le tipranavir ; voir rubriques 4.4 et 4.5). Si possible, des alternatives thérapeutiques doivent être considérées et, si nécessaire, un arrêt temporaire du traitement par CRESTOR doit être envisagé. Dans les situations où la co-administration de ces médicaments avec CRESTOR est inévitable, le bénéfice et le risque du traitement associé et les ajustements posologiques de CRESTOR doivent être attentivement pris en considération (voir rubrique 4.5).
· Hypersensibilité à la substance active ou à l’un des excipients mentionnés à la rubrique 6.1
· Affection hépatique évolutive y compris élévations inexpliquées et prolongées des transaminases sériques et toute augmentation des transaminases sériques au-delà de 3 fois la limite supérieure de la normale ;
· Insuffisance rénale sévère (clairance de la créatinine < 30 ml/min) ;
· Myopathie ;
· Traitement concomitant par sofosbuvir/velpatasvir/voxilaprévir (voir rubrique 4.5) ;
· Traitement concomitant par la ciclosporine ;
· Grossesse, allaitement et chez les femmes en âge de procréer n’utilisant pas de moyens contraceptifs appropriés.
La dose de 40 mg est contre-indiquée chez les patients présentant des facteurs prédisposant de myopathie/rhabdomyolyse. Ces facteurs incluent :
· Insuffisance rénale modérée (clairance de la créatinine < 60 ml/min) ;
· Hypothyroïdie ;
· Antécédents personnels ou familiaux de maladies musculaires génétiques ;
· Antécédents personnels d’atteinte musculaire avec un autre inhibiteur de l’HMG-CoA réductase ou un fibrate ;
· Consommation excessive d’alcool ;
· Situations favorisant une élévation des taux plasmatiques de rosuvastatine ;
· Patients asiatiques;
· Association aux fibrates ; (voir rubriques 4.4, 4.5 et 5.2).
4.4. Mises en garde spéciales et précautions d'emploi
Une protéinurie, détectée par bandelette urinaire et principalement d’origine tubulaire, a été observée chez les patients traités par de fortes doses de CRESTOR, en particulier à la dose de 40 mg.
Elle est, dans la plupart des cas, transitoire ou intermittente. Cette protéinurie n’apparaît pas être un facteur prédictif d’une affection rénale aiguë ou évolutive (voir rubrique 4.8).
Le taux de notification d’évènements rénaux sérieux depuis la mise sur le marché est plus élevé à la dose de 40 mg.
Des tests fonctionnels rénaux devront être envisagés régulièrement au cours du suivi des patients traités par une dose de 40 mg.
Effets musculaires :
Des effets musculaires tels que des myalgies, des myopathies et rarement des rhabdomyolyses ont été observés chez des patients traités par CRESTOR à toutes les doses, en particulier aux doses > 20 mg.
De très rares cas de rhabdomyolyses ont été rapportés lors de l’utilisation d’ézétimibe en association avec les inhibiteurs de l’HMG-CoA réductase. Une interaction pharmacodynamique ne peut pas être exclue (voir rubrique 4.5) et toute précaution doit être prise lors d’une utilisation associée. Comme avec les autres inhibiteurs de l’HMG-CoA réductase, le taux de notification de rhabdomyolyses associé à CRESTOR depuis la mise sur le marché est plus élevé à la dose de 40 mg.
Dosage de la créatine phosphokinase (CPK) :
Le dosage des CPK ne doit pas être pratiqué après un effort musculaire intense ou en présence d’une autre cause possible d’élévation des CPK qui pourrait fausser l’interprétation des résultats. Si le taux de CPK initial est significativement élevé (supérieur à 5 fois la normale), le taux devra être recontrôlé dans les 5 à 7 jours suivants. Si le taux initial de CPK > 5 fois la normale est confirmé, le traitement ne devra pas être débuté.
Avant le traitement :
CRESTOR, comme les autres inhibiteurs de l’HMG-CoA réductase, sera prescrit avec précaution chez les patients présentant des facteurs prédisposant de myopathie/rhabdomyolyse.
Ces facteurs incluent :
· insuffisance rénale,
· hypothyroïdie,
· antécédents personnels ou familiaux de maladie musculaire génétique,
· antécédents personnels d’atteinte musculaire avec un autre inhibiteur de l’HMG-CoA réductase ou avec un fibrate,
· consommation excessive d’alcool,
· âge > 70 ans,
· situations favorisant une élévation des taux plasmatiques de rosuvastatine (voir rubriques 4.2, 4.5 5.2).
· association aux fibrates
Dans ces situations, il est nécessaire de bien évaluer l’intérêt du traitement et de surveiller le patient au plan clinique. Si le taux initial de CPK est significativement élevé (supérieur à 5 fois la normale), le traitement ne doit pas être débuté.
Pendant le traitement :
Il convient de demander au patient de signaler immédiatement toute douleur musculaire inexpliqué, fatigue musculaire ou crampes, particulièrement si elles sont associées à des malaises ou de la fièvre. Un dosage des CPK doit être pratiqué chez ces patients. Le traitement sera interrompu en cas d’élévation importante des CPK (supérieure à 5 fois la normale) ou en cas de symptomatologie musculaire importante avec gêne fonctionnelle quotidienne (même si les CPK sont inférieures à 5 fois la normale). Si les symptômes disparaissent et que le taux de CPK revient à la normale, la réintroduction de CRESTOR ou d’un autre inhibiteur de l’HMG-CoA réductase, à la dose la plus faible pourra être envisagée sous surveillance clinique attentive. En l’absence de signes cliniques, la surveillance systématique des CPK n’est pas nécessaire.
De très rares cas de myopathies nécrosantes à médiation auto-immune ont été signalés pendant ou après le traitement par les statines, y compris la rosuvastatine. La myopathie nécrosante à médiation auto-immune est caractérisée cliniquement par une faiblesse musculaire proximale et une élévation de la créatine kinase sérique, qui persiste malgré l’arrêt du traitement par la statine.
Dans quelques cas, il a été rapporté que les statines induisaient de novo ou aggravaient une myasthénie préexistante ou une myasthénie oculaire (voir rubrique 4.8). CRESTOR doit être arrêté en cas d’aggravation des symptômes. Des récurrences ont été rapportées lorsque la même statine ou une statine différente a été (ré)administrée.
Durant les études cliniques, il n’a pas été mis en évidence d’augmentation des effets musculaires chez quelques patients traités par CRESTOR en association à d’autres traitements.
Cependant, une augmentation de l’incidence des cas de myosites et de myopathies a été observée chez des patients traités par des inhibiteurs de l’HMG-CoA réductase en association avec des fibrates dont le gemfibrozil, la ciclosporine, l’acide nicotinique, les antifongiques azolés, les inhibiteurs de la protéase et les macrolides.
Le gemfibrozil augmente le risque de myopathie quand il est associé à certains inhibiteurs de l’HMG-CoA réductase. L’association de CRESTOR et du gemfibrozil n’est donc pas recommandée. Le bénéfice obtenu de l’association de CRESTOR avec les fibrates ou la niacine sur les paramètres lipidiques sera évalué en fonction du risque potentiel de telles associations. La dose de 40 mg est contre-indiquée en cas d’association aux fibrates (voir rubriques 4.5 et 4.8).
CRESTOR ne doit pas être co-administré avec des formulations systémiques d’acide fusidique ou dans les 7 jours suivant l’arrêt d’un traitement par l’acide fusidique. Chez les patients pour lesquels l’utilisation de l’acide fusidique par voie systémique est considérée comme essentiel, le traitement par statine doit être arrêté pendant toute la durée du traitement par l’acide fusidique. Des cas de rhabdomyolyses ont été rapportés (dont certains fatals) chez des patients recevant de l’acide fusidique et des statines en association (voir rubrique 4.5). Il est conseillé aux patients de solliciter immédiatement un avis médical s’ils rencontrent des symptômes de faiblesse, douleur ou sensibilité musculaire. Le traitement par statines peut être réintroduit 7 jours après la dernière prise d’acide fusidique. Dans des circonstances exceptionnelles où la prolongation du traitement par l’acide fusidique par voie systémique est nécessaire, comme par exemple pour le traitement d’infections sévères, la nécessité d’une co-administration de CRESTOR et de l’acide fusidique doit être envisagée uniquement au cas par cas et sous surveillance médicale étroite.
CRESTOR ne doit pas être utilisé en cas de survenue de symptômes graves, aigus suggérant une myopathie ou prédisposant à l’apparition d’une insuffisance rénale secondaire à une rhabdomyolyse (ex. infection aiguë sévère, hypotension, intervention chirurgicale majeure, traumatisme, troubles métaboliques, électrolytiques ou endocriniens sévères ou épilepsie non contrôlée).
Effets indésirables cutanés graves
Des effets indésirables cutanés sévères, y compris un syndrome de Stevens-Johnson (SJS) et un syndrome d’hypersensibilité médicamenteuse avec éosinophilie et symptômes systémiques (DRESS), pouvant engager le pronostic vital ou être fatals, ont été rapportés avec la rosuvastatine (voir rubrique 4.8). Au moment de la prescription, les patients doivent être informés des signes et symptômes de réactions cutanées sévères puis être étroitement surveillés. En cas d’apparition de signes et symptômes évocateurs d’une telle réaction, le traitement par CRESTOR doit être interrompu immédiatement et un traitement alternatif doit être envisagé.
Si le patient a développé une réaction grave telle qu’un SSJ ou un DRESS lors de l'utilisation de CRESTOR, le traitement par CRESTOR ne doit en aucun cas être réinstauré chez ce patient.
Effets hépatiques :
Comme les autres inhibiteurs de l’HMG-CoA réductase, CRESTOR doit être utilisé avec précaution chez les patients consommant d’importantes quantités d’alcool et/ou présentant des antécédents de maladie hépatique.
Il est recommandé de pratiquer des tests fonctionnels hépatiques avant le début du traitement et 3 mois après. Une élévation des transaminases supérieure à 3 fois la limite supérieure de la normale doit conduire à l’arrêt du traitement ou à une diminution de la dose.
Le taux de notification d’évènements hépatiques sérieux (consistant principalement en une augmentation des transaminases hépatiques) depuis la mise sur le marché est plus élevé à la dose de 40 mg.
Chez les patients avec une hypercholestérolémie secondaire à une hypothyroïdie ou à un syndrome néphrotique, la pathologie sous-jacente devra être traitée avant tout démarrage d’un traitement par CRESTOR.
Particularités ethniques
Les études de pharmacocinétique montrent une augmentation de l’exposition chez des sujets asiatiques comparativement aux caucasiens (voir rubriques 4.2, 4.3 et 5.2).
Inhibiteurs de protéases :
Une augmentation de l’exposition systémique à la rosuvastatine a été observée chez les sujets recevant de façon concomitante de la rosuvastatine avec divers inhibiteurs de protéases en association avec le ritonavir. Il doit être pris en considération à la fois le bénéfice hypolipémiant de l’utilisation de CRESTOR chez les patients atteints du VIH recevant des inhibiteurs de protéases et l’augmentation potentielle des concentrations plasmatiques de la rosuvastatine, à l’initiation du traitement et par la suite, lors de l’augmentation de la dose de CRESTOR chez les patients traités avec des inhibiteurs de protéases. L’utilisation concomitante avec certains inhibiteurs de protéases n’est pas recommandée à moins que la posologie de CRESTOR soit ajustée (voir rubriques 4.2 et 4.5).
Intolérance au lactose :
Ce médicament contient du lactose. Son utilisation est déconseillée chez les patients présentant une intolérance au galactose, un déficit total en lactase ou un syndrome de malabsorption du glucose ou du galactose (maladies héréditaires rares).
Pneumopathie interstitielle
Des cas exceptionnels de pneumopathie interstitielle ont été rapportés avec certaines statines, en particulier en cas de traitement à long terme (voir rubrique 4.8). Les symptômes peuvent comprendre une dyspnée, une toux non productive et une altération de l’état de santé général (fatigue, perte de poids et fièvre). En cas de suspicion de pneumopathie interstitielle chez un patient, le traitement par statine doit être interrompu.
Diabète
Certaines données suggèrent que la classe pharmacologique des statines, augmenterait la glycémie et que chez certains patients à risque élevé de survenue d'un diabète, les statines pourraient entraîner une hyperglycémie nécessitant l'instauration d'un traitement anti-diabétique. Ce risque est néanmoins compensé par la réduction du risque vasculaire sous statines et par conséquent il ne doit pas être un motif d'arrêt des statines. Les patients à risque (glycémie à jeun comprise entre 5,6 et 6,9 mmol/l, IMC > 30 kg/m2, triglycérides élevés, hypertension) devront faire l'objet d'une surveillance clinique et biologique conformément aux recommandations nationales.
Dans l'étude JUPITER, l'incidence des cas de diabète était de 2,8% dans le groupe rosuvastatine et de 2,3% dans le groupe placebo. La majorité des patients présentaient une glycémie à jeun comprise entre 5,6 et 6,9 mmol/l.
Population pédiatrique
L’évaluation de la croissance (taille), du poids, de l’IMC (indice de masse corporelle), et des caractéristiques secondaires de maturation sexuelle en fonction des stades de Tanner chez les patients pédiatriques de 6 à 17 ans traités par de la rosuvastatine sont limitées à une période de deux ans. Après deux ans de traitement, aucun effet sur la croissance, le poids et l’IMC ou la maturation sexuelle n’a été détecté (voir rubrique 5.1).
Dans une étude clinique réalisée chez des adolescents et des enfants recevant de la rosuvastatine pendant 52 semaines, les élévations de CPK > 10x LSN et les symptômes musculaires suivant un exercice ou une augmentation de l’activité physique ont été observés plus fréquemment que dans les essais cliniques conduits chez l’adulte (voir rubrique 4.8).
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Effet de l'administration concomitante de médicaments sur la rosuvastatine
Inhibiteurs des transporteurs protéiques : la rosuvastatine est un substrat pour certains transporteurs protéiques, dont le transporteur hépatocytaire d'influx OATP1B1 et le transporteur d'efflux BCRP. L'administration concomitante de CRESTOR avec des médicaments inhibiteurs de ces transporteurs protéiques peut entraîner une augmentation des concentrations plasmatiques de rosuvastatine et un risque accru de myopathie (voir rubriques 4.2, 4.4 et 4.5 Tableau 1).
Ciclosporine : lors de l’administration concomitante de CRESTOR et de ciclosporine, les valeurs de l’ASC de la rosuvastatine sont en moyenne 7 fois plus élevées que celles observées chez le volontaire sain (voir Tableau 1). CRESTOR est contre-indiqué chez les patients recevant de la ciclosporine de façon concomitante (voir rubrique 4.3). L’administration concomitante de ciclosporine et de CRESTOR ne modifie pas les concentrations plasmatiques de ciclosporine.
Inhibiteurs de protéases : bien que le mécanisme exact d’interaction n’ait pas été élucidé, une utilisation concomitante d’inhibiteurs de protéases peut augmenter fortement l’exposition à la rosuvastatine (voir Tableau 1). Par exemple, au cours d’une étude de pharmacocinétique conduite chez des volontaires sains, l’administration concomitante de la rosuvastatine 10 mg avec une association de deux inhibiteurs de protéases (300 mg d’atazanavir / 100 mg de ritonavir) a entraîné, une augmentation de l’ASC et de la Cmax de la rosuvastatine, d’environ 3 et 7 fois respectivement. L'utilisation concomitante de CRESTOR et de certaines associations d'inhibiteurs de protéases peut être envisagée après un examen attentif des ajustements de la posologie de CRESTOR basés sur l'augmentation attendue de l'exposition à la rosuvastatine (voir rubriques 4.2, 4.4 et 4.5 Tableau 1).
Ticagrélor : Ticagrélor inhibe le transporteur BCRP, provoquant une augmentation de 2,6 fois de l’ASC de la rosuvastatine, ce qui peut entraîner un risque accru de myopathie. Il convient de prendre en compte les avantages de la prévention des événements indésirables cardiovasculaires majeurs par l'utilisation de la rosuvastatine et les risques liés à l'augmentation des concentrations plasmatiques de rosuvastatine.
gemfibrozil et autres hypolipémiants : l’association de CRESTOR et du gemfibrozil augmente la concentration maximale (Cmax) et l’ASC (multipliées par deux) de la rosuvastatine (voir rubrique 4.4).
Sur la base de données d’études d’interactions spécifiques, aucune interaction pharmacocinétique significative avec le fénofibrate n’est attendue ; cependant, une interaction pharmacodynamique peut survenir. Le gemfibrozil, le fénofibrate, les autres fibrates et la niacine (acide nicotinique) à des doses hypolipémiantes (doses ³ à 1g/jour), administrés en association avec certains inhibiteurs de l’HMG-CoA réductase, augmentent le risque de myopathie, probablement parce qu’ils sont eux-mêmes à l’origine de myopathie lorsqu’ils sont administrés seuls. La dose de 40 mg est contre-indiquée lors de l’association aux fibrates (voir rubriques 4.3 et 4.4). Ces patients doivent aussi débuter leur traitement avec la dose de 5 mg.
Ezétimibe : l’utilisation concomitante de CRESTOR 10 mg et de 10 mg d’ézétimibe entraîne une augmentation de l’ASC de la rosuvastatine de 1,2 fois sa valeur chez les patients présentant une hypercholestérolémie (voir Tableau 1). Une interaction pharmacodynamique au regard des effets indésirables, entre CRESTOR et l’ézétimibe ne peut pas être exclue (voir rubrique 4.4).
Antiacides : la prise concomitante de CRESTOR et d’un antiacide contenant un hydroxyde d’aluminium et de magnésium entraîne une diminution de la concentration plasmatique de rosuvastatine d’environ 50%. Cet effet diminue si l’antiacide est administré 2 heures après CRESTOR. La signification clinique de cette interaction n’a pas été étudiée.
Érythromycine : l’utilisation concomitante de CRESTOR et d’érythromycine entraîne une diminution de 20% de l’ASC et une diminution de 30% de la concentration maximale (Cmax) de rosuvastatine. Cette interaction peut être due à une augmentation de la motilité intestinale induite par l’érythromycine.
Cytochrome P450 : les résultats des études in vitro et in vivo montrent que la rosuvastatine n’est ni un inhibiteur ni un inducteur des isoenzymes du cytochrome P450. De plus, la rosuvastatine est un substrat mineur pour ces isoenzymes. Par conséquent, aucune interaction résultant du métabolisme via le cytochrome P450 n’est attendue.
Aucune interaction cliniquement significative n’a été observée entre la rosuvastatine et le fluconazole (inhibiteur du CYP2C9 et CYP3A4) ou le kétoconazole (inhibiteur du CYP2A6 et CYP3A4).
Interactions nécessitant des ajustements de la posologie de rosuvastatine (voir Tableau 1)
Lorsqu’il est nécessaire de co-administrer CRESTOR avec d’autres médicaments connus pour augmenter l’exposition à la rosuvastatine, la posologie de CRESTOR doit être ajustée.
Commencer avec une dose de CRESTOR 5 mg une fois par jour si l’augmentation attendue de l’exposition (ASC) est d’approximativement 2 fois sa valeur ou plus. La dose maximale journalière de CRESTOR doit être ajustée afin que l’exposition attendue à la rosuvastatine ne soit pas supérieure à celle d’une dose journalière de 40 mg de CRESTOR sans interaction médicamenteuse, comme par exemple une dose de CRESTOR 20 mg avec du gemfibrozil (augmentation de l’exposition de 1,9 fois), et une dose de CRESTOR 10 mg avec l’association ritonavir/ atazanavir (augmentation de l’exposition de 3,1 fois).
S’il est observé que le médicament augmente l’ASC de la rosuvastatine de moins de 2 fois, il n’est pas nécessaire de diminuer la dose initiale mais il faut être prudent si la dose de CRESTOR est augmentée au-delà de 20 mg.
Tableau 1. Effet de l’administration concomitante de médicaments sur l’exposition à la rosuvastatine (ASC ; par ordre décroissant de surface) à partir des essais cliniques publiés
|
Multiplication par deux ou plus de l’ASC de la rosuvastatine |
||
|
Schéma posologique du médicament administré en association |
Schéma posologique de la rosuvastatine |
Modification de l’ASC de la rosuvastatine* |
|
Sofosbuvir/velpatasvir/voxilaprévir (400 mg - 100 mg - 100 mg) + Voxilaprévir (100 mg) 1 fois par jour, 15 jours |
10 mg, dose unique |
↑ 7,4 fois |
|
Ciclosporine 75 mg 2 fois/jour jusqu’à 200 mg 2 fois/jour, 6 mois |
10 mg 1 fois/jour, 10 jours |
↑ 7,1 fois |
|
Darolutamide 600 mg 2 fois/jour, 5 jours |
5 mg, dose unique |
↑ 5,2 fois |
|
Régorafénib 160 mg, 1 fois par jour, 14 jours |
5 mg, dose unique |
↑ 3,8 fois |
|
Atazanavir 300 mg / Ritonavir 100 mg 1 fois/jour, 8 jours |
10 mg, dose unique |
↑ 3,1 fois |
|
Roxadustat 200 mg, 1 jour sur 2 |
10 mg, dose unique |
↑ 2,9 fois |
|
Velpatasvir 100 mg 1 fois par jour |
10 mg, dose unique |
↑ 2,7 fois |
|
Momelotinib 200 mg 1 fois/jour, 6 jours |
10 mg, dose unique |
↑ 2,7 fois |
|
Ticagrélor 90 mg 2 fois/jour, 2 jours |
10 mg, dose unique |
↑ 2,6 fois |
|
Ombitasvir 25 mg/paritaprévir 150 mg/ Ritonavir 100 mg 1 fois par jour / dasabuvir 400 mg 2 fois par jour, 14 jours |
5 mg, dose unique |
↑ 2,6 fois |
|
Teriflunomide, Leflunomide |
Non disponible |
↑ 2,5 fois |
|
Vadadustat 600 mg 1 fois/jour, 8 jours |
20 mg, dose unique |
↑ 2,5 fois |
|
Grazoprévir 200 mg/elbasvir 50mg 1 fois par jour, 11 jours |
10 mg, dose unique |
↑ 2,3 fois |
|
Glécaprévir 400 mg/pibrentasvir 120 mg 1 fois par jour, 7 jours |
5 mg, 1 fois par jour, 7 jours |
↑ 2,2 fois |
|
Lopinavir 400 mg / Ritonavir 100 mg 2 fois/jour, 17 jours |
20 mg 1 fois/jour, 7 jours |
↑ 2,1 fois |
|
Capmatinib 400 mg 1 fois par jour |
10 mg, dose unique |
↑ 2,1 fois |
|
Clopidogrel 300 mg dose de charge, suivi par 75 mg à 24h |
20 mg, dose unique |
↑ 2 fois |
|
Fostamatinib 100 mg 2 fois par jour |
20 mg, dose unique |
↑ 2,0 fois |
|
Febuxostat 120 mg 1 fois par jour |
10 mg, dose unique |
↑ 1,9 fois |
|
Tafamidis 61 mg, 2 fois/jour pendant 2 jours puis 1 fois/jour pendant 7 jours |
10 mg, dose unique |
↑ 2,0 fois |
|
Gemfibrozil 600 mg 2 fois/jour, 7 jours |
80 mg, dose unique |
↑ 1,9 fois |
|
Augmentation de moins de 2 fois de l’ASC de la rosuvastatine |
||
|
Schéma posologique du médicament administré en association |
Schéma posologique de la rosuvastatine |
Modification de l’ASC de la rosuvastatine* |
|
Eltrombopag 75 mg 1 fois/jour, 5 jours |
10 mg, dose unique |
↑ 1,6 fois |
|
Darunavir 600 mg / Ritonavir 100 mg 2 fois/jour, 7 jours |
10 mg 1 fois/jour, 7 jours |
↑ 1,5 fois |
|
Tipranavir 500 mg / Ritonavir 200 mg 2 fois/jour, 11 jours |
10 mg, dose unique |
↑ 1,4 fois |
|
Dronédarone 400 mg 2 fois/jour |
Non disponible |
↑ 1,4 fois |
|
Itraconazole 200 mg 1 fois/jour, 5 jours |
10 mg, dose unique |
↑ 1,4 fois** |
|
Ezétimibe 10 mg 1 fois/jour, 14 jours |
10 mg 1 fois/jour, 14 jours |
↑ 1,2 fois** |
|
Diminution de l’ASC de la rosuvastatine |
||
|
Schéma posologique du médicament administré en association |
Schéma posologique de la rosuvastatine |
Modification de l’ASC de la rosuvastatine* |
|
Erythromycine 500 mg 4 fois/jour, 7 jours |
80 mg, dose unique |
↓ 20% |
|
Baicaline 50 mg 3 fois/jour, 14 jours |
20 mg, dose unique |
↓ 47% |
|
*Les résultats présentés en multiples de (ou x-fois) représentent le rapport entre l'administration concomitante des deux produits et la rosuvastatine seule. Les résultats présentés en % représentent la différence relative en % par rapport à la rosuvastatine seule. Une augmentation est indiquée par « ↑ », une diminution par « ↓ ». **Plusieurs études d’interaction ont été effectuées à différentes doses de CRESTOR, le tableau met en évidence le rapport le plus significatif. ASC = aire sous la courbe |
||
Les médicaments/combinaisons suivants n’ont pas eu d’effet cliniquement significatif sur le ratio de l’ASC de la rosuvastatine lors de la co-administration :
Aleglitazar 0,3 mg, 7 jours ; Fénofibrate 67 mg 3 fois/jour, 7 jours ; Fluconazole 200 mg 1 fois/jour, dose unique, 11 jours ; Fosamprénavir 700 mg / Ritonavir 100 mg 2 fois/jour, 8 jours ; Kétoconazole 200 mg 2 fois/jour, 7 jours ; Rifampicine 450 mg 1 fois/jour, dose unique, 7 jours ; Silymarine 140 mg 3 fois/jour, 5 jours
Effet de la rosuvastatine sur les médicaments co-administrés
AntiVitamine K : comme avec les autres inhibiteurs de l’HMG-CoA réductase, l’initiation du traitement ou l’augmentation de la posologie de CRESTOR chez les patients traités par AVK (par exemple la warfarine ou un autre anticoagulant coumarinique) peut entraîner une augmentation de l’INR.
L’arrêt de CRESTOR ou la baisse de sa posologie peut entraîner une diminution de l’INR. Dans ces conditions, une surveillance de l’INR est recommandée.
Contraception orale / traitement hormonal substitutif (THS) : l’utilisation concomitante de CRESTOR et d’une contraception orale entraîne une augmentation de l’ASC de l’éthinylestradiol et du norgestrel (respectivement de 26% et 34%). Ces augmentations de taux plasmatiques doivent être prises en compte lors du choix de la dose du contraceptif oral. Il n’existe pas de données pharmacocinétiques disponibles pour des sujets traités simultanément par CRESTOR et un THS, par conséquent, un effet similaire ne peut être exclu. Cette association a été cependant largement utilisée chez des femmes au cours des essais cliniques et a été bien tolérée.
Autres médicaments
Digoxine : sur la base de données d’études d’interactions spécifiques, aucune interaction cliniquement significative avec la digoxine n’est attendue.
Acide fusidique : les études d’interactions entre la rosuvastatine et l’acide fusidique n’ont pas été conduites. Le risque de myopathie incluant une rhabdomyolyse peut être augmenté par l’administration concomitante d’acide fusidique par voie systémique avec les statines. Le mécanisme de cette interaction (qu’il soit pharmacodynamique ou pharmacocinétique, ou les deux) est encore inconnu. Des cas de rhabdomyolyse ont été rapportés (dont certains fatals) chez les patients recevant cette association.
Si le traitement par l’acide fusidique par voie systémique est nécessaire, celui par CRESTOR doit être arrêté pendant toute la durée du traitement par l’acide fusidique (voir également rubrique 4.4).
Population pédiatrique
Les études d’interaction ont été uniquement réalisées chez l’adulte. L’étendue des interactions dans la population pédiatrique n’est pas connue.
4.6. Fertilité, grossesse et allaitement
CRESTOR est contre-indiqué pendant la grossesse et l’allaitement.
Les femmes en âge de procréer doivent prendre des mesures de contraception adéquates.
Grossesse
Le cholestérol et ses dérivés étant essentiels au développement du fœtus, le risque potentiel de l’inhibition de l’HMG-CoA réductase prime sur le bénéfice attendu d’un traitement par statine lors d’une grossesse. Les études sur l’animal mettent en évidence une toxicité limitée sur la reproduction (voir rubrique 5.3).
En cas de découverte d’une grossesse pendant le traitement, celui-ci doit être interrompu immédiatement.
Il n’y a pas d’effets connus sur la fertilité après l’utilisation de la rosuvastatine.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Les effets indésirables observés avec CRESTOR sont généralement légers et transitoires.
Dans les essais cliniques contrôlés, moins de 4% des patients traités par CRESTOR ont dû arrêter le traitement en raison d’effets indésirables.
Tableau des effets indésirables
Le tableau ci-dessous présente les effets indésirables de la rosuvastatine, identifiés au cours des essais cliniques et après commercialisation. Les effets indésirables listés ci-dessous sont classés en fonction de leur fréquence et de leur classe de système d’organes.
Les fréquences des effets indésirables sont classées selon la convention suivante :
Fréquents (≥ 1/100 - < 1/10) ; peu fréquents (≥ 1/1 000 - < 1/100) ; rares (≥ 1/1 0000 - < 1/1 000) ; très rares (< 1/10 000) ; inconnus (fréquence ne pouvant pas être estimée avec les données disponibles).
Tableau 2. Effets indésirables identifiés au cours des essais cliniques et après commercialisation
|
Classe de Système d’organes |
Fréquent |
Peu fréquent |
Rare |
Très rare |
Inconnu |
|
Affections hématologiques et du système lymphatique |
|
|
Thrombocytopénie |
|
|
|
Affections du système immunitaire |
|
|
Réactions d’hypersensibilité y compris angio-œdème |
|
Réaction anaphylactique |
|
Affections endocriniennes |
Diabète de type II1 |
|
|
|
|
|
Affections psychiatriques |
|
|
|
|
Dépression |
|
Affections du système nerveux |
Céphalées Sensations vertigineuses |
|
|
Polyneuropathie Perte de mémoire |
Neuropathie périphérique Troubles du sommeil (y compris insomnies et cauchemars) Myasthénie |
|
Affections oculaires |
|
|
|
|
Myasthénie oculaire |
|
Affections respiratoires, thoraciques et médiastinales |
|
|
|
|
Toux Dyspnée |
|
Affections gastro-intestinales |
Constipation Nausée Douleur abdominale |
|
Pancréatite |
|
Diarrhée |
|
Affections hépatobiliaires |
|
|
Augmentation des transaminases |
Ictère Hépatite |
|
|
Affections de la peau et du tissus sous-cutané |
|
Prurit Rash Urticaire |
|
|
Syndrome de Stevens-Johnson Syndrome d’hypersensibilité médicamenteuse avec éosinophilie et symptômes systémiques (DRESS) |
|
Affections musculo-squelettiques et systémiques |
Myalgie |
|
Myopathie (y compris myosite) Rhabdomyolyse Syndrome lupique Déchirure musculaire |
Arthralgie |
Tendinopathies, quelquefois compliquées par une rupture du tendon Myopathie nécrosante à médiation auto-immune |
|
Affections du rein et des voies urinaires |
|
|
|
Hématurie |
|
|
Affections des organes de reproduction et du sein |
|
|
|
Gynécomastie |
|
|
Troubles généraux et anomalies au site d'administration |
Asthénie |
|
|
|
Œdème |
1 : la fréquence dépend de la présence ou non de facteurs de risque (glycémie à jeun ≥ 5,6 mmol /L, IMC> 30 kg/m², augmentation des triglycérides, antécédents d'hypertension).
Comme avec les autres inhibiteurs de l’HMG-CoA réductase, l’incidence des événements indésirables semble être dose-dépendante.
Effets rénaux :
Une protéinurie, détectée par bandelette urinaire et principalement d’origine tubulaire, a été observée chez des patients traités par CRESTOR. Les modifications des protéines urinaires d’absence ou traces à ++ ou plus ont été observées chez moins de 1% des patients traités par 10 mg et 20 mg, et chez approximativement 3% des patients traités par 40 mg. Une augmentation mineure des modifications d’absence ou traces à + a été observée avec la dose de 20 mg.
Dans la plupart des cas, la protéinurie diminue ou disparaît spontanément alors que le traitement est poursuivi. La revue des données issues des essais cliniques et de l’expérience depuis la mise sur le marché n’a pas identifié de lien de causalité entre la protéinurie et une affection rénale aiguë ou évolutive.
Une hématurie a été observée chez des patients traités par CRESTOR et les données des essais cliniques montrent que le taux de survenue est faible.
Effets musculaires :
Des effets musculaires tels des myalgies, des myopathies (y compris myosites) et rarement des rhabdomyolyses avec ou sans insuffisance rénale aiguë ont été observés chez des patients traités par CRESTOR, à toutes les doses et en particulier aux doses > 20 mg.
Une augmentation dose-dépendante des CPK a été observée chez des patients prenant de la rosuvastatine ; la majorité des cas étaient bénins, asymptomatiques et transitoires.
Si les taux de CPK sont élevés (supérieurs à 5 fois la normale), le traitement doit être interrompu (voir rubrique 4.4).
Effets hépatiques :
Comme avec les autres inhibiteurs de l’HMG-CoA réductase, une augmentation dose-dépendante des transaminases a été rapportée chez un faible nombre de patients traités par rosuvastatine. La majorité des cas rapportés était bénins, asymptomatiques et transitoires.
Les effets indésirables suivants ont été rapportés avec quelques statines :
Troubles sexuels
Des cas exceptionnels de pneumopathie interstitielle, en particulier lors d’un traitement à long terme (voir rubrique 4.4)
Le taux de notification de rhabdomyolyses, d’évènements rénaux sérieux et d’évènements hépatiques sérieux (consistant principalement en une augmentation des transaminases hépatiques) depuis la mise sur le marché est plus élevé à la dose de 40 mg.
Population pédiatrique
Des élévations de la créatine kinase > 10 fois la LSN (limite supérieure de la normale) ainsi que des symptômes musculaires après une activité physique augmentée ont été observés plus fréquemment dans une étude clinique de 52 semaines chez des enfants, des adolescents comparativement à des adultes (voir rubrique 4.4).
Pour les autres aspects, le profil de tolérance de la rosuvastatine était similaire chez les enfants et adolescents comparativement à celui des adultes.
Déclaration des effets indésirables suspectés
La déclaration des effets indésirables suspectés après autorisation du médicament est importante. Elle permet une surveillance continue du rapport bénéfice/risque du médicament. Les professionnels de santé déclarent tout effet indésirable suspecté via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
La fonction hépatique et le taux de CPK doivent être surveillés. L’hémodialyse n’est probablement pas utile.
5. PROPRIETES PHARMACOLOGIQUES
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : Inhibiteur de l’HMG-CoA réductase, Code ATC : C10A A07
Mécanisme d’action
La rosuvastatine est un inhibiteur sélectif et compétitif de l’HMG-CoA réductase, enzyme responsable du contrôle de la transformation de la 3-hydroxy-3 méthylglutaryl coenzyme A en mévalonate, précurseur du cholestérol. Le principal site d’action de la rosuvastatine est le foie, organe cible pour la baisse du cholestérol.
La rosuvastatine augmente le nombre des récepteurs des LDL à la surface des hépatocytes, augmentant la captation du LDL cholestérol, et renforçant son catabolisme et inhibant la synthèse hépatique des VLDL, réduisant ainsi le nombre de particules de VLDL et de LDL.
Effets pharmacodynamiques
CRESTOR réduit les taux élevés de LDL-cholestérol, de cholestérol total et de triglycérides et augmente le taux de HDL-cholestérol.
Il réduit également les taux des ApoB, du non HDL-C, du VLDL-C, du VLDL-TG et augmente le taux d’ApoA-I (voir Tableau 3).
CRESTOR réduit également les ratios LDL-C / HDL-C, cholestérol total / HDL-C, non HDL-C / HDL- C et ApoB/ApoA-I.
Tableau 3 : Résultats sur les paramètres lipidiques en fonction de la dose chez les patients avec hypercholestérolémie primaire (type IIa et IIb) (variation moyenne ajustée en pourcentage par rapport à la valeur initiale)
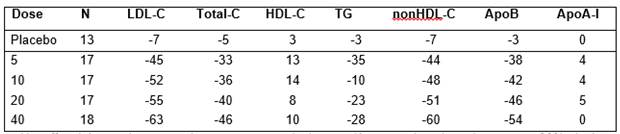
Un effet thérapeutique est obtenu au cours de la première semaine de traitement et 90% de la réponse maximale sont observés au bout de 2 semaines. La réponse maximale est habituellement atteinte en 4 semaines et se maintient ensuite.
Efficacité et sécurité clinique
CRESTOR est efficace chez les patients adultes présentant une hypercholestérolémie avec ou sans hypertriglycéridémie, quels que soient la particularité ethnique, le sexe ou l'âge, et chez des populations spécifiques telles que les diabétiques et les patients avec une hypercholestérolémie familiale.
Dans les études poolées de phase III, il a été démontré que l’efficacité de CRESTOR a permis à la majorité des patients présentant une hypercholestérolémie type IIa ou IIb (valeur moyenne initiale du LDL-C : environ 4,8 mmol/L) d’atteindre les objectifs des recommandations de la Société Européenne sur l’Athérosclérose (EAS ; 1998) ; environ 80 % des patients traités par rosuvastatine 10 mg ont atteint la valeur cible (< 3 mmol/L) de LDL-C.
Dans une grande étude, 435 sujets atteints d'hypercholestérolémie familiale hétérozygote ont reçu 20 mg à 80 mg de CRESTOR suivant un schéma de titration forcée. Toutes les doses testées ont montré un bénéfice sur les paramètres lipidiques et ont permis d’atteindre les objectifs thérapeutiques. Après une titration jusqu’à la dose quotidienne de 40 mg (12 semaines de traitement), le LDL-C a été réduit de 53%. Trente-trois pourcent (33%) des patients ont atteint la valeur cible des recommandations de l’EAS pour le LDL-C (< 3 mmol/L).
Dans un essai en ouvert en titration forcée, 42 patients (incluant 8 patients pédiatriques) atteints d'une hypercholestérolémie familiale homozygote ont été traités avec des doses de 20 à 40 mg de CRESTOR. La réduction moyenne du taux de LDL-C sur l’ensemble des patients a été de 22%.
Durant des essais cliniques, sur un nombre limité de patients, une efficacité supplémentaire de CRESTOR a été démontrée sur la baisse des triglycérides en association avec le fénofibrate et sur l’augmentation du taux de HDL-C en association avec la niacine (voir rubrique 4.4).
Dans une étude clinique multicentrique, en double aveugle, contrôlée versus placebo (METEOR), 984 patients âgés de 45 à 70 ans présentant un faible risque coronaire (risque < 10 % à 10 ans selon le score de Framingham), avec des taux moyens de LDL-C de 4,0 mmol/l (154,5 mg/dl), mais une athérosclérose infraclinique (déterminée par mesure de l'épaisseur intima-média carotidienne), ont été randomisés pour recevoir soit 40 mg de rosuvastatine une fois par jour soit un placebo, sur une durée de 2 ans. La rosuvastatine a réduit significativement l'évolution de l'épaisseur maximale intima-media carotidienne de – 0,0145 mm/an pour les 12 sites carotidiens en comparaison avec le placebo [intervalle de confiance : 95% -0,0196, -0,0093 ; p < 0,0001].
La diminution de l'épaisseur intima-media, par rapport à la valeur de base, a été de – 0,0014 mm/an (- 0,12% par an (non significatif)) sous rosuvastatine contre une progression de +0,0131 mm/an (1,12% par an (p < 0,0001)) avec le placebo. Aucune corrélation directe entre la diminution de l'épaisseur intima-media carotidienne et la réduction du risque d'événements cardiovasculaires n'a encore été démontrée.
La population étudiée dans METEOR a un faible risque coronaire et ne représente pas la population cible de CRESTOR 40 mg. La dose de 40 mg ne doit être prescrite qu'aux patients avec une hypercholestérolémie très sévère avec un risque cardiovasculaire élevé (voir rubrique 4.2).
Dans l’étude sur la « justification de l’utilisation d’une statine en prévention primaire : étude interventionnelle évaluant la rosuvastatine » (JUPITER), l’effet de la rosuvastatine sur la fréquence des événements majeurs de la maladie cardiovasculaire athérosclérotique a été évaluée chez 17 802 patients hommes (≥ 50 ans) et femmes (≥ 60 ans).
Les sujets participant à cette étude étaient randomisés soit dans le groupe placebo (n= 8901) soit dans le groupe rosuvastatine 20 mg une fois par jour (n=8901) et ont été suivis pendant une durée moyenne de 2 ans.
Le taux de LDL-cholestérol a été réduit de 45% (p< 0,001) dans le groupe rosuvastatine comparé au groupe placebo.
Dans une analyse réalisée a posteriori dans un sous-groupe de patients à haut risque présentant à l’inclusion un risque > 20% selon l’échelle de Framingham (1558 patients), une réduction significative (p<0,03) du critère combiné : décès d’origine cardiovasculaire, accident vasculaire cérébral et infarctus du myocarde (p= 0,028) dans le groupe rosuvastatine versus placebo a été observée.
La réduction du risque absolu du taux d’événements pour 1000 patient-années a été de 8,8.
La mortalité totale était inchangée dans ce groupe de patients à haut risque (p= 0,193).
Dans une analyse réalisée a posteriori portant sur un sous-groupe de patients à haut risque (total de 9302 patients) présentant à l’inclusion un risque ≥ 5% selon l’échelle de SCORE (extrapolé pour inclure les patients de plus de 65 ans), une réduction significative (p=0,0003) du critère combiné : décès d’origine cardiovasculaire, accident vasculaire cérébral et infarctus du myocarde pour le bras rosuvastatine versus placebo a été observée. La réduction du risque absolu du taux d’événements pour 1000 patient-années était de 5,1. La mortalité totale était inchangée dans ce groupe de patients à haut risque (p= 0,076).
Dans l’étude JUPITER l’arrêt de traitement en raison d’événements indésirables a été de 6,6% pour les sujets traités par rosuvastatine et de 6,2% pour ceux recevant le placebo. Les événements indésirables les plus fréquents entrainant le plus fréquemment l’arrêt de l’étude étaient : les myalgies (rosuvastatine 0,3%, placebo 0,2%), douleur abdominale (rosuvastatine 0,03%, placebo 0,02%), et éruption cutanée (rosuvastatine 0,02%, placebo 0,03%).
Les événements indésirables les plus fréquents, avec une fréquence supérieure ou égale au placebo étaient : les infections du tractus urinaires (rosuvastatine 8,7%, placebo 8,6%), rhinopharyngite (rosuvastatine 7,6%, placebo 7,2%), douleur lombaire (rosuvastatine 7,6%, placebo 6,9%), et myalgie (rosuvastatine 7,6%, placebo 6,6%).
Population pédiatrique
Dans une étude randomisée, en double aveugle, multicentrique, contrôlée versus placebo de 12 semaines (n= 176, 97 garçons et 79 filles), suivie d’une période de titration de la dose de rosuvastatine en ouvert pendant 40 semaines (n= 173, 96 garçons et 77 filles), les patients âgés de 10 à 17 ans (stade II-V sur l’échelle de Tanner, filles 1 an au moins après l’apparition des règles) avec une hypercholestérolémie familiale hétérozygote ont reçu soit de la rosuvastatine 5 mg, 10 mg ou 20 mg soit un placebo une fois par jour pendant 12 semaines puis ils ont tous reçu de la rosuvastatine une fois par jour pendant 40 semaines.
A l’entrée dans l’étude, approximativement 30% des patients étaient âgés de 10 à 13 ans et approximativement 17%, 18%, 40% et 25% étaient respectivement au stade II, III, IV et V sur l’échelle de Tanner.
Le LDL-C a été réduit dans le groupe rosuvastatine 5 mg, 10 mg et 20 mg de 38,3%, 44,6% et 50% respectivement comparé à 0,7% dans le groupe placebo.
A la fin de la période de 40 semaines de l’étude en ouvert d’ajustement de la dose vers la dose cible avec un dosage maximum de 20 mg une fois par jour, 70 patients sur 173 (40,5%) ont atteint l’objectif de LDL-C de moins de 2,8 mmol/l.
Après 52 semaines de traitement, aucun effet sur la croissance, le poids, l’IMC ou la maturation sexuelle n’a été détecté (voir rubrique 4.4).
Cette étude (n= 176) n’était pas conçue pour la comparaison d’effets indésirables rares.
La rosuvastatine a aussi fait l’objet d’une étude de recherche de doses cibles en ouvert pendant 2 ans sur 198 enfants présentant une hypercholestérolémie familiale hétérozygote et âgés de 6 à 17 ans (88 garçons et 110 filles, stade Les patients âgés de 6 à 9 ans (n= 64) pouvaient recevoir jusqu’à 10 mg maximum une fois par jour et les patients âgés de 10 à 17 ans (n= 134) pouvaient recevoir jusqu’à 20 mg maximum une fois par jour. Après 24 mois de traitement avec la rosuvastatine, la réduction en pourcentage de la valeur de référence du LDL-C, calculée par la méthode des moindres carrés, était de 43% (valeur de référence : 236 mg/dL, à 24 mois : 133 mg/dL). Pour chaque tranche d’âge, les réductions des valeurs de références du taux de LDL-C, calculées par la méthode des moindres carrés, étaient respectivement de 43% (valeur de référence : 234 mg/dL, à 24 mois : 124 mg/dL), 45% (valeur de référence : 234 mg/dL, à 24 mois : 124 mg/dL), et 35% (valeur de référence : 241 mg/dL, à 24 mois : 153 mg/dL) dans les groupes 6 à <10 ans, 10 à <14 ans, et 14 à <18 ans. La rosuvastatine aux doses de 5 mg, 10 mg et 20 mg a également entraîné des variations statistiquement significatives des valeurs de référence pour les variables lipidiques et lipoprotéiniques secondaires suivantes : HDL-C, CT (Cholestérol Total), non-HDL-C, LDL-C/HDL-C, CT/HDL-C,TG/HDL-C, non HDL-C/HDL-C, ApoB, ApoB/ApoA-1. Ces variations ont toutes conduit à l’amélioration de la réponse lipidique et ont été maintenues pendant 2 ans. Après 24 mois de traitement, aucun effet sur la croissance, le poids, l’IMC ou la maturation sexuelle n’a été détecté (voir rubrique 4.4) La rosuvastatine a été étudiée dans une étude multicentrique randomisée, en double aveugle, croisée avec 20 mg une fois par jour versus placebo chez 14 enfants et adolescents (âgés de 6 à 17 ans) présentant une hypercholestérolémie familiale homozygote. L’étude comprenait une phase d’introduction active de 4 semaines de régime pendant laquelle les patients étaient traités par la rosuvastatine 10 mg, une phase croisée de 6 semaines de traitement par la rosuvastatine 20 mg précédée ou suivie par une période de traitement de 6 semaines par placebo, et une phase d’entretien de 12 semaines pendant laquelle tous les patients étaient traités par la rosuvastatine 20 mg. Les patients ayant débuté l’étude sous ezétimibe ou aphérèse ont continué le traitement durant toute l’étude. Une réduction statistiquement significative (p=0.005) du LDL-C (22,3 %, 85,4 mg/dL ou 2,2 mmol/L) a été observée après 6 semaines de traitement par la rosuvastatine 20 mg versus placebo. Des réductions statistiquement significatives du CT (20,1 %, p=0.003), du non HDL-C (22,9 %, p=0.003), et de l’ApoB (17,1 %, p=0.024) ont été observées. Des réductions des TG, LDL-C /HDL-C, CT/HDL-C, non HDL-C/HDL-C, et ApoB/ApoA-1 ont également été observées après 6 semaines de traitement par la rosuvastatine 20 mg versus placebo. La réduction du LDL-C après 6 semaines de traitement par la rosuvastatine 20 mg et suivant 6 semaines de traitement par placebo a été maintenue après 12 semaines de thérapie continue. Un patient a présenté une réduction supplémentaire du LDL-C (8,0 %), du cholestérol total (6,7 %) et du non HDL-C (7,4 %) suite à 6 semaines de traitement à 40 mg après titration de la dose. Au cours d’un traitement prolongé en ouvert pour 9 de ces patients sous 20 mg de rosuvastatine sur une durée pouvant aller jusqu’à 90 semaines, la réduction du LDL-C a été maintenue entre -12,1 % et - 21,3 %. Parmi les 7 patients enfants et adolescents évaluables (âgés de 8 à 17 ans) issus de l’étude ouverte de titration présentant une hypercholestérolémie familiale homozygote (voir ci-dessus), le pourcentage de réduction du LDL-C (21,0 %), du CT (19,2 %), et du non-HDL-C (21,0 %) depuis leur valeur de départ après 6 semaines de traitement par la rosuvastatine 20 mg était cohérent avec les observations de l’étude susmentionnée chez les enfants et adolescents présentant une hypercholestérolémie familiale homozygote. L’Agence Européenne des Médicaments a différé l’obligation de soumettre les résultats des études réalisées avec la rosuvastatine dans tous les sous-ensembles de la population pédiatrique dans le traitement de l’hypercholestérolémie familiale homozygote, de la dyslipidémie (mixte) primaire combinée, et dans la prévention des évènements cardiovasculaires (voir rubrique 4.2 pour les informations concernant l’utilisation pédiatrique). 5.2. Propriétés pharmacocinétiques Après administration orale, les concentrations plasmatiques maximales de rosuvastatine sont atteintes en 5 heures environ. La biodisponibilité absolue est approximativement de 20 %. Distribution La rosuvastatine est majoritairement captée par le foie, qui est l'organe principal de la synthèse du cholestérol et de la clairance de LDL-C. Le volume de distribution est d’environ 134 litres. Approximativement 90% de rosuvastatine sont liés aux protéines plasmatiques et principalement à l'albumine. Biotransformation La rosuvastatine subit un métabolisme limité (approximativement 10 %). Les études de métabolisme in vitro utilisant des hépatocytes humains montrent que la rosuvastatine est un substrat mineur des cytochromes P450. Le CYP2C9 est le principal isoenzyme impliqué avec, dans une moindre mesure, le 2C19, le 3A4 et le 2D6. Les principaux métabolites identifiés sont les métabolites N-desméthyl et lactone. Le métabolite N-desméthyl est approximativement 50 % moins actif que la rosuvastatine alors que la lactone est considérée comme cliniquement inactive. La rosuvastatine est responsable de plus de 90 % de l'activité inhibitrice de l’HMG-CoA réductase circulante. Élimination Environ 90 % de la dose de rosuvastatine sont excrétés sous forme inchangée dans les selles (fraction absorbée et non absorbée de la substance active), le reste étant excrété dans les urines. Approximativement 5% sont excrétés sous forme inchangée dans les urines. La ½ vie d'élimination plasmatique est d’environ 19 heures et n'augmente pas avec les fortes doses. La moyenne géométrique de la clairance plasmatique est approximativement de 50 L/heure (coefficient de variation de 21.7%). Comme avec les autres inhibiteurs de l’HMG-CoA réductase, le passage hépatique implique le transporteur membranaire OATP-C. Ce transporteur joue un rôle important dans l’élimination hépatique de la rosuvastatine. Linéarité/non-linéarité L’exposition systémique à la rosuvastatine augmente en fonction de la dose. Il n’y a pas de changement des paramètres pharmacocinétiques après une administration quotidienne répétée. Populations particulières Âge et sexe : il n’y a pas d'effet clinique significatif de l’âge ou du sexe sur la pharmacocinétique de la rosuvastatine chez les adultes. L’exposition à la rosuvastatine chez les enfants et les adolescents ayant une hypercholestérolémie familiale hétérozygote semble être similaire ou inférieure à celle des adultes ayant une dyslipidémie (voir population pédiatrique ci-dessous). Particularités ethniques : les études de pharmacocinétique montrent une multiplication par 2 environ de l’ASC médiane et de la Cmax chez les asiatiques (Japonais, Chinois, Philippins, Vietnamiens et Coréens) comparativement aux caucasiens. Une augmentation de 1,3 de l’ASC médiane et de la Cmax a été montrée chez les Indiens. Une analyse de pharmacocinétique de population n’a démontré aucune différence cliniquement significative entre les populations caucasiennes et noires. Insuffisance rénale : dans une étude incluant des patients avec différents degrés d’insuffisance rénale, une altération légère à modérée de la fonction rénale n’a pas eu d’effet sur les concentrations plasmatiques de rosuvastatine ou de N-desméthyl. Cependant une insuffisance rénale sévère (clairance de la créatinine < 30 ml/min) a entraîné une multiplication par 3 des concentrations plasmatiques et une multiplication par 9 de la concentration du métabolite N-desméthyl comparées à celles des volontaires sains. Les concentrations plasmatiques à l’état d’équilibre de la rosuvastatine chez les sujets hémodialysés étaient approximativement 50% plus élevées que chez les volontaires sains. Insuffisance hépatique : dans une étude avec des patients présentant différents degrés d’insuffisance hépatique, il n’a pas été démontré d’augmentation des concentrations de rosuvastatine chez les sujets présentant un score de Child-Pugh de 7 ou inférieur. Cependant, chez deux sujets présentant des scores de Child-Pugh de 8 et 9, une augmentation de l’exposition systémique au moins double de celle des sujets avec des scores de Child-Pugh inférieurs a été observée. Il n’existe pas de données chez les sujets ayant un score de Child-Pugh supérieur à 9. Polymorphisme génétique : la configuration des inhibiteurs de l'HMG-CoA réductase, dont la rosuvastatine, implique les transporteurs protéiques OATP1B1 et BCRP codés par les gènes SLCO1B1 (OATP1B1) et ABCG2 (BCRP). Certains variants de ces gènes, comme SLCO1B1 c.521CC et ABCG2 c.421AA sont associés à une exposition à la rosuvastatine environ 1.6 fois plus élevée (ASC) ou 2.4 fois plus élevée, respectivement, par rapport aux génotypes SLCO1B1 c.521TT ou ABCG2 c.421CC. Pour les patients dont on sait qu'ils présentent ces génotypes (SLCO1B1 c.521CC ou ABCG2 c.421AA), une dose quotidienne plus faible de CRESTOR est recommandée. Population pédiatrique : Deux études pharmacocinétiques avec la rosuvastatine (prise sous forme de comprimés) conduites chez des patients pédiatriques, présentant une hypercholestérolémie familiale hétérozygote, âgés de 10 à 17 ou de 6 à 17 ans (214 patients au total), ont montré que l’exposition des patients pédiatriques apparaît comparable ou inférieure à celle des patients adultes. L’exposition à la rosuvastatine était prévisible en ce qui concerne la dose et le temps tout au long des 2 ans. 5.3. Données de sécurité préclinique Les effets indésirables non observés dans les études cliniques, mais vus chez les animaux à des niveaux d’exposition similaires aux expositions cliniques sont les suivants : dans les études de toxicité à doses répétées, des changements histopathologiques au niveau hépatique probablement dus à l’action pharmacologique de la rosuvastatine ont été observés chez la souris, le rat et dans une moindre mesure avec des effets sur la vésicule biliaire chez le chien, mais pas chez le singe. En outre, une toxicité testiculaire a été observée chez le singe, chez le chien à des doses plus élevées. Une toxicité de reproduction a été évidente chez le rat, avec une diminution de la taille et du poids de la portée ainsi que du nombre de jeunes survivants à des doses materno-toxiques lorsque l’exposition systémique était plusieurs fois supérieures aux doses thérapeutiques. Pelliculage : lactose monohydraté, hypromellose, triacétine, dioxyde de titane (E171), oxyde de fer jaune (E172). 6.4. Précautions particulières de conservation A conserver à une température ne dépassant pas 30°C. A conserver dans l’emballage d’origine, à l’abri de l’humidité. Flacons (PEHD) : A conserver à une température ne dépassant pas 30°C. Conserver le flacon soigneusement fermé, à l'abri de l'humidité. 6.5. Nature et contenu de l'emballage extérieur 7, 14, 15, 20, 28, 30, 42, 50, 56, 60, 84, 90, 98 et 100 comprimés pelliculés sous plaquettes (Aluminium/Aluminium). 30 et 100 comprimés pelliculés en flacon (PEHD). Toutes les présentations peuvent ne pas être commercialisées. 6.6. Précautions particulières d’élimination et de manipulation Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur. 7. TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE TOUR PACIFIC 11-13 COURS VALMY 92800 PUTEAUX 8. NUMERO(S) D’AUTORISATION DE MISE SUR LE MARCHE · 34009 369 852 1 6 : 28 comprimés sous plaquettes (Aluminium/Aluminium) · 34009 369 853 8 4 : 30 comprimés sous plaquettes (Aluminium/Aluminium) · 34009 369 854 4 5 : 50 comprimés sous plaquettes (Aluminium/Aluminium) · 34009 276 104 5 5 : 60 comprimés sous plaquettes (Aluminium/Aluminium). · 34009 369 855 0 6 : 84 comprimés sous plaquettes (Aluminium/Aluminium) · 34009 391 690 0 2 : 90 comprimés sous plaquettes (Aluminium/Aluminium) 9. DATE DE PREMIERE AUTORISATION/DE RENOUVELLEMENT DE L’AUTORISATION [À compléter ultérieurement par le titulaire] 10. DATE DE MISE A JOUR DU TEXTE [À compléter ultérieurement par le titulaire] Sans objet. 12. INSTRUCTIONS POUR LA PREPARATION DES RADIOPHARMACEUTIQUES Liste I
ANSM - Mis à jour le : 22/10/2025
CRESTOR 5 mg, comprimé pelliculé
Rosuvastatine
· Gardez cette notice. Vous pourriez avoir besoin de la relire.
· Si vous avez d’autres questions, interrogez votre médecin ou votre pharmacien.
· Ce médicament vous a été personnellement prescrit. Ne le donnez pas à d’autres personnes. Il pourrait leur être nocif, même si les signes de leur maladie sont identiques aux vôtres.
· Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Voir rubrique 4.
1. Qu'est-ce que CRESTOR 5 mg, comprimé pelliculé et dans quels cas est-il utilisé ?
2. Quelles sont les informations à connaître avant de prendre CRESTOR 5 mg, comprimé pelliculé ?
3. Comment prendre CRESTOR 5 mg, comprimé pelliculé ?
4. Quels sont les effets indésirables éventuels ?
5. Comment conserver CRESTOR 5 mg, comprimé pelliculé ?
6. Contenu de l’emballage et autres informations.
1. QU’EST-CE QUE CRESTOR 5 mg, comprimé pelliculé ET DANS QUELS CAS EST-IL UTILISE ?
Classe pharmacothérapeutique : Inhibiteur de l’HMG-CoA réductase - code ATC : C10A A07
CRESTOR appartient au groupe des médicaments appelés statines.
CRESTOR vous a été prescrit parce que :
· Vous avez un taux élevé de cholestérol ce qui signifie que vous présentez un risque de faire une attaque cardiaque ou un accident vasculaire cérébral. CRESTOR est utilisé chez les adultes, les adolescents et les enfants âgés de 6 ans et plus pour traiter un taux de cholestérol élevé.
· Il vous est recommandé de prendre des statines, car parfois un régime alimentaire adapté et une activité physique ne suffisent pas à corriger votre taux de cholestérol. Vous devez poursuivre le régime hypocholestérolémiant et l’activité physique en même temps que la prise de CRESTOR.
Ou
· Vous avez d’autres facteurs qui augmentent votre risque d’avoir une attaque cardiaque, un accident vasculaire cérébral ou des problèmes de santé liés à ces facteurs.
Une attaque cardiaque, un accident vasculaire cérébral ou des problèmes de santé liés à ces facteurs peuvent être causés par une maladie appelée l’athérosclérose. L’athérosclérose est due à une accumulation de dépôts de graisse dans vos artères.
Pourquoi il est important de continuer de prendre CRESTOR :
CRESTOR est utilisé pour corriger le taux de substances graisseuses dans le sang appelées lipides, le plus fréquent étant le cholestérol.
Il y a différents types de cholestérol trouvé dans le sang : le « mauvais cholestérol » (LDL-C) et le « bon cholestérol » (HDL-C).
· CRESTOR peut réduire le « mauvais cholestérol » et augmenter le « bon cholestérol ».
· Il agit en aidant à bloquer la production de « mauvais cholestérol » par votre organisme. Il améliore également l’aptitude de votre corps à l’éliminer de votre sang.
Pour la plupart des personnes, un taux de cholestérol élevé n’a pas de conséquence sur la façon dont elles se sentent parce que cela n’entraîne aucun symptôme. Cependant, sans traitement, des dépôts graisseux peuvent s’accumuler sur la paroi des vaisseaux sanguins et réduire leur diamètre.
Parfois, ce rétrécissement des vaisseaux peut empêcher le passage du sang jusqu’au cœur ou au cerveau conduisant à une attaque cardiaque ou un accident vasculaire cérébral.
En diminuant votre taux de cholestérol, vous pouvez réduire le risque d’avoir une attaque cardiaque, un accident vasculaire cérébral ou des problèmes de santé qui y sont liés.
Il est très important de continuer à prendre CRESTOR, même si votre taux de cholestérol revient à la normale, parce qu’il prévient la remontée de votre taux de cholestérol et donc l’accumulation de dépôts de graisse. Cependant, vous devez arrêter votre traitement si votre médecin vous le dit, ou si vous découvrez que vous êtes enceinte.
2. QUELLES SONT LES INFORMATIONS A CONNAITRE AVANT DE PRENDRE CRESTOR 5 mg, comprimé pelliculé ?
Ne prenez jamais CRESTOR 5 mg, comprimé pelliculé :
· Si vous êtes allergique à la rosuvastatine ou à l’un des autres composants contenus dans ce médicament, mentionnés dans la rubrique 6 ;
· Si vous êtes enceinte, si vous allaitez, arrêtez immédiatement le traitement et prévenez votre médecin ; il convient de prendre un contraceptif approprié pour éviter d’être enceinte pendant le traitement par CRESTOR ;
· Si vous avez actuellement des problèmes hépatiques ;
· Si vous avez des problèmes rénaux graves (si vous avez un doute, demandez à votre médecin) ;
· Si vous avez des troubles musculaires appelés myopathie (douleurs musculaires répétées ou inexpliquées) ;
· Si vous prenez l’association sofosbuvir/velpatasvir/voxilaprévir (utilisée dans le cas d’une infection virale du foie nommée hépatite C) ;
· Si vous prenez de la ciclosporine (utilisée par exemple lors de greffes d’organes).
Si vous êtes concernés par l’une de ces situations (ou si vous avez un doute), parlez-en à votre médecin.
De plus, vous ne devez pas prendre 40 mg de CRESTOR (dosage le plus élevé) si :
· Vous avez une insuffisance rénale modérée (en cas de doute, demandez à votre médecin) ;
· Vous avez des troubles de la thyroïde ;
· Vous avez des douleurs musculaires répétées ou inexpliquées, des antécédents personnels ou familiaux de problèmes musculaires ou si vous avez déjà présenté des douleurs musculaires avec un autre médicament abaissant les taux de cholestérol ;
· Vous consommez régulièrement des quantités importantes d’alcool ;
· Vous êtes d’origine asiatique (japonais, chinois, philippin, vietnamien, coréen et indien) ;
· Vous êtes déjà traité par un autre médicament abaissant les taux de cholestérol appelé fibrate.
Si vous êtes concernés par l’une de ces situations (ou si vous avez un doute), parlez-en à votre médecin.
Avertissements et précautions
Adressez-vous à votre médecin ou pharmacien avant de prendre CRESTOR.
· Si vous avez des problèmes hépatiques ;
· Si vous avez des problèmes rénaux ;
· Si vous avez des douleurs musculaires répétées ou inexpliquées, des antécédents personnels ou familiaux de problèmes musculaires ou si vous avez déjà présenté des douleurs musculaires avec un autre médicament abaissant les taux de cholestérol ; contacter immédiatement votre médecin si vous avez des douleurs musculaires inexpliquées particulièrement si vous ne vous sentez pas bien ou si vous avez de la fièvre ; informer également votre médecin ou votre pharmacien si vous avez une faiblesse musculaire qui est constante.
· Si vous avez ou avez eu une myasthénie (maladie accompagnée d'une faiblesse musculaire générale, pouvant parfois toucher les muscles utilisés pour respirer) ou une myasthénie oculaire (maladie provoquant une faiblesse musculaire au niveau des yeux), car les statines peuvent parfois aggraver ces affections ou entraîner leur apparition (voir rubrique 4).
· Si vous avez déjà développé une éruption cutanée sévère ou une desquamation de la peau, des cloques et/ou des plaies buccales après avoir pris CRESTOR ou d'autres médicaments apparentés ;
· Si vous consommez régulièrement des quantités importantes d’alcool ;
· Si vous avez des troubles de la thyroïde ;
· Si vous êtes déjà traité par un autre médicament abaissant le taux de cholestérol appelé fibrate ; veuillez consulter les informations contenues dans la notice ; et ce, même si vous avez déjà pris dans le passé un médicament qui abaisse le taux de cholestérol
· Si vous prenez un médicament pour traiter l’infection au VIH, par exemple du ritonavir avec lopinavir et/ou atazanavir, reportez-vous à la rubrique « Autres médicaments et CRESTOR ».
· Si vous prenez ou avez pris durant les 7 derniers jours un médicament appelé acide fusidique (un médicament contre les infections bactériennes), par voie orale ou par injection. L’association d’acide fusidique et de CRESTOR peut causer de graves problèmes musculaires (rhabdomyolyse). Reportez-vous à la rubrique « Autres médicaments et CRESTOR ».
· Si vous avez plus de 70 ans (votre médecin a besoin de choisir la dose initiale de CRESTOR adaptée pour vous) ;
· Si vous avez une insuffisance respiratoire grave ;
· Si vous êtes d’origine asiatique (japonais, chinois, philippin, vietnamien, coréen et indien) (votre médecin a besoin de choisir la dose initiale de CRESTOR adaptée pour vous).
Si vous êtes concernés par l’une de ces situations (ou si vous avez un doute) :
Vous ne devez pas prendre 40 mg de CRESTOR (le dosage le plus élevé) ; vous devez vérifier avec votre médecin ou pharmacien la dose de CRESTOR avant de débuter le traitement.Des réactions cutanées graves, y compris un syndrome de Stevens-Johnson et un syndrome d’hypersensibilité médicamenteuses avec éosinophilie et symptômes systémiques (DRESS), ont été rapportées en association avec le traitement par CRESTOR. Arrêtez de prendre CRESTOR et consultez immédiatement un médecin si vous remarquez l'un des symptômes décrits dans la rubrique 4.
Chez un petit nombre de sujets, les statines peuvent avoir un effet sur le foie, ceci est identifié par un simple test de recherche d’augmentation des enzymes du foie dans le sang. Pour cette raison, votre médecin pratiquera habituellement un test sanguin (bilan hépatique) avant traitement et au cours du traitement.
Au cours de votre traitement avec ce médicament, si vous êtes diabétique ou si vous présentez un risque de survenue d’un diabète, vous serez suivi attentivement par votre médecin. Vous pouvez débuter un diabète si vous avez un taux de sucre (glycémie) et de graisses élevés dans le sang, si vous êtes en surpoids et si vous avez une pression artérielle (tension) élevée.
Enfants et adolescents
· Si le patient est un enfant âgé de moins de 6 ans : CRESTOR ne doit pas être donné aux enfants de moins de 6 ans ;
· Si le patient est âgé de moins de 18 ans : la dose de 40 mg ne doit pas être utilisée chez les enfants et adolescents de moins de 18 ans ;
Autres médicaments et CRESTOR 5 mg, comprimé pelliculé
Informez votre médecin ou pharmacien si vous prenez, avez récemment pris ou pourriez prendre tout autre médicament.
Dîtes à votre médecin si vous prenez l’un des médicaments suivants :
· ciclosporine (utilisée par exemple après une greffe d’organe),
· warfarine, clopidogrel ou ticagrélor (ou tout autre médicament pour fluidifier le sang),
· fibrates (comme le gemfibrozil, le fénofibrate), ou tout autre médicament qui abaisse le cholestérol sanguin (comme l’ézétimibe),
· un antiacide (utilisé pour neutraliser l’acidité de votre estomac),
· érythromycine (antibiotique), acide fusidique (un antibiotique – voir ci-dessous et rubrique « Avertissements et précautions »),
· un contraceptif oral (pilule),
· régorafénib (utilisé pour traiter le cancer),
· darolutamide (utilisé pour traiter le cancer),
· capmatinib (utilisé pour traiter le cancer),
· un traitement hormonal substitutif (THS) de la ménopause,
· fostamatinib (utilisé pour traiter une numération plaquettaire basse),
· febuxostat (utilisé pour traiter et prévenir un taux sanguin élevé d’acide urique) ,
· teriflunomide (utilisé pour traiter la sclérose en plaques),
· léflunomide (utilisé pour traiter la polyarthrite rhumatoïde),
· n’importe lequel des médicaments suivants utilisés pour traiter des infections virales, incluant l’infection par le VIH et l’hépatite C, seul ou en association (voir Avertissements et précautions d’emploi) : ritonavir, lopinavir, atazanavir, sofosbuvir, voxilaprévir, ombitasvir, paritaprévir, dasabuvir, velpatasvir, grazoprévir, elbasvir, glécaprévir, pibrentasvir,
· tafamidis (utilisé pour traiter l’amylose à transthyrétine),
· momelotinib (utilisé pour traiter la myélofibrose chez les adultes souffrant d’une anémie).
Les effets de ces médicaments pourraient être modifiés par CRESTOR ou pourraient modifier l’effet de CRESTOR.
Si vous avez besoin de prendre de l’acide fusidique par voie orale pour traiter une infection bactérienne, vous aurez besoin d’arrêter temporairement ce médicament. Votre docteur vous indiquera le moment le plus sûr pour reprendre CRESTOR. Prendre CRESTOR en association avec de l’acide fusidique peut, dans de rares cas, mener à des faiblesses musculaires, une sensibilité ou des douleurs musculaires (rhabdomyolyse). Plus d’informations sur la rhabdomyolyse sont disponibles à la rubrique 4.
CRESTOR 5 mg, comprimé pelliculé avec des aliments et boissons
Vous pouvez prendre CRESTOR avec ou sans aliments
Grossesse et allaitement
Vous ne devez pas prendre CRESTOR si vous êtes enceinte ou si vous allaitez. Si vous découvrez que vous êtes enceinte pendant le traitement, arrêtez le traitement immédiatement et consultez votre médecin. Les femmes doivent éviter une grossesse pendant un traitement par CRESTOR en utilisant un contraceptif adapté.
Demandez conseil à votre médecin ou à votre pharmacien avant de prendre tout médicament.
Conduite de véhicules et utilisation de machines
La plupart des personnes peuvent conduire une voiture ou utiliser une machine lorsqu’ils prennent CRESTOR, leur aptitude n’est pas affectée. Cependant, quelques personnes ont des vertiges lors du traitement par CRESTOR. Si vous éprouvez des vertiges, consultez votre médecin avant de conduire ou d’utiliser une machine.
CRESTOR 5 mg, comprimé pelliculé contient du lactose
Ce médicament contient du lactose.
L’utilisation de ce médicament est déconseillée chez les patients présentant une intolérance au galactose, un déficit total en lactase ou un syndrome de malabsorption du glucose ou du galactose (maladies héréditaires rares).
Voir la rubrique « Contenu de l’emballage et autres informations » si vous souhaitez la liste complète des composants.
3. COMMENT PRENDRE CRESTOR 5 mg, comprimé pelliculé ?
Doses usuelles chez les adultes :
Si vous prenez CRESTOR pour un taux de cholestérol élevé :
Dose initiale
Votre traitement avec CRESTOR doit débuter avec une dose de 5 ou 10 mg, même si vous preniez une dose plus élevée d’une autre statine avant.
Le choix de la dose initiale dépendra de :
· Votre taux de cholestérol,
· Vos risques d’avoir une attaque cardiaque ou un accident vasculaire cérébral
· Facteurs pouvant vous rendre plus sensible à certains effets indésirables.
Veuillez vérifier auprès de votre médecin ou pharmacien la dose initiale qui vous est le mieux adaptée.
Une dose initiale de 5 mg par jour est recommandée chez les patients :
· D’origine asiatique (japonais, chinois, philippin, vietnamien, coréen et indien),
· Agés de plus de 70 ans,
· Présentant une insuffisance rénale modérée,
· Présentant des facteurs prédisposant à une myopathie (atteinte musculaire).
Augmentation de la dose et dose maximale quotidienne
Votre médecin peut décider d’augmenter les doses jusqu’à ce que la posologie soit appropriée pour vous. Si vous débutez à 5 mg, votre médecin peut décider de doubler la dose jusqu’à 10 mg puis 20 mg puis 40 mg si nécessaire.
Si vous commencez avec 10 mg, votre médecin peut décider de doubler la dose jusqu’à 20 mg puis 40 mg si nécessaire. Une période de 4 semaines est nécessaire entre chaque adaptation de dose.
La dose maximale quotidienne est de 40 mg. Cette dose concerne les patients ayant un taux de cholestérol élevé et un risque élevé d’avoir une attaque cardiaque ou un accident cérébral vasculaire pour lesquels le taux de cholestérol n’a pas été suffisamment baissé avec 20 mg.
Si vous prenez CRESTOR pour réduire le risque d’avoir une attaque cardiaque, un accident vasculaire cérébral ou des problèmes de santé qui y sont liés :
La dose recommandée est de 20 mg une fois par jour. Cependant votre médecin pourra décider d’utiliser une dose plus faible si vous avez l’un des facteurs mentionnés ci-dessus.
Utilisation chez les enfants et adolescents âgés de 6 à 17 ans :
La dose moyenne chez les enfants et adolescents âgés de 6 à 17 ans est de 5 à 20 mg une fois par jour. La dose initiale usuelle est de 5 mg par jour et votre docteur pourra augmenter progressivement votre dose afin de trouver la dose adaptée de CRESTOR. La dose journalière maximale de CRESTOR est 10 ou 20 mg pour les enfants âgés de 6 à 17 ans en fonction de votre pathologie sous-jacente traitée. Prenez cette dose une fois par jour. La dose de 40 mg de CRESTOR ne doit pas être utilisée chez les enfants.
Prise de vos comprimés
Avalez chaque comprimé en entier avec de l’eau.
CRESTOR doit être pris une fois par jour. Vous pouvez prendre le comprimé à tout moment de la journée avec ou sans nourriture.
Il est recommandé de prendre votre comprimé chaque jour à la même heure, ceci vous évitera d’oublier de le prendre.
Contrôle régulier de votre cholestérol
Il est important que vous retourniez voir votre médecin pour des contrôles réguliers de votre cholestérol afin d’être sûr que ce dernier est bien contrôlé. Votre médecin peut décider d’augmenter la dose de CRESTOR jusqu’à ce qu’elle soit appropriée pour vous.
Si vous avez pris plus de CRESTOR 5 mg, comprimé pelliculé que vous n’auriez dû :
Consultez immédiatement votre médecin ou votre pharmacien ou l’hôpital le plus proche pour avis.
Si vous allez à l’hôpital ou recevez un traitement pour une autre cause, prévenez l’équipe médicale que vous prenez CRESTOR.
Si vous oubliez de prendre CRESTOR 5 mg, comprimé pelliculé :
Si vous arrêtez de prendre CRESTOR 5 mg, comprimé pelliculé :
Informez votre médecin si vous souhaitez arrêter CRESTOR car votre taux de cholestérol devrait encore augmenter.
Si vous avez d’autres questions sur l’utilisation de ce médicament, demandez plus d’informations à votre médecin ou à votre pharmacien.
4. QUELS SONT LES EFFETS INDESIRABLES EVENTUELS ?
Il est important que vous soyez informés des effets indésirables possibles. Ils sont habituellement légers et de courte durée.
Arrêtez de prendre CRESTOR et consulter immédiatement un médecin si vous avez les réactions allergiques suivantes :
· Difficulté à respirer avec ou sans gonflement du visage, des lèvres, de la langue et/ou de la gorge
· Gonflement du visage, des lèvres, de la langue et/ou de la gorge qui peut causer des difficultés pour avaler
· Démangeaison sévère de la peau (avec des cloques)
· Tâches rougeâtres, sans relief, en forme de cible ou circulaires sur le buste, souvent accompagnées de cloques en leur centre, d’un décollement de la peau, d’ulcérations de la bouche, de la gorge, du nez, des organes génitaux et des yeux. Ces éruptions cutanées graves peuvent être précédées de fièvre et de symptômes pseudo-grippaux (syndrome de Stevens-Johnson).
· Eruption cutanée étendue, température corporelle élevée et gonflement des ganglions lymphatiques (syndrome DRESS ou syndrome d’hypersensibilité médicamenteuse).
Consultez votre médecin immédiatement :
· Si vous ressentez des douleurs musculaires inhabituelles qui durent anormalement longtemps. Les symptômes musculaires sont plus fréquents chez les enfants et adolescents que chez les adultes. Comme avec les autres statines, un très petit nombre de personnes ont eu des problèmes musculaires qui ont rarement entraîné un danger pour la vie de ces personnes (rhabdomyolyses).
· Si vous présentez une déchirure musculaire.
· Si vous souffrez d’un syndrome lupique (y compris une éruption cutanée, des troubles articulaires et des effets sur les cellules sanguines).
Effets indésirables fréquents (entre 1 cas sur 10 et 1 cas sur 100 patients)
· Maux de tête, douleurs d’estomac, constipation, sensation de malaise, douleurs musculaires, sentiment général de faiblesse, sensations vertigineuses.
· Augmentation des protéines dans les urines à la dose de 40 mg – ceci revient généralement à la normale sans avoir à arrêter le traitement.
· Diabète : vous pouvez débuter un diabète si vous avez un taux de sucre (glycémie) et de graisses élevées dans le sang, si vous êtes en surpoids et si vous avez une pression artérielle (tension) élevée. Vous serez suivi attentivement par votre médecin au cours de votre traitement avec ce médicament.
Effets indésirables peu fréquents (entre 1 cas sur 100 et 1 cas sur 1000 patients)
· Eruption cutanée, démangeaisons, autres réactions cutanées,
· Augmentation des protéines dans les urines – ceci revient généralement à la normale sans avoir à arrêter le traitement de CRESTOR.
Effets indésirables rares (entre 1 cas sur 1000 et 1 cas sur 10 000 patients)
· Réactions allergiques graves ; elles peuvent se manifester par un gonflement du visage, des lèvres, de la langue et/ou de la gorge avec difficultés à avaler et respirer, une démangeaison sévère de la peau (avec des cloques). Si vous ressentez ces signes, vous devez arrêter de prendre CRESTOR et consulter immédiatement un médecin.
· Atteintes des muscles chez l’adulte. Par mesure de précaution, si vous ressentez des douleurs musculaires inhabituelles qui durent anormalement longtemps, arrêtez de prendre CRESTOR et consultez votre médecin immédiatement,
· Douleur sévère au niveau de l’estomac (inflammation du pancréas),
· Augmentation des enzymes du foie dans le sang.
· Saignement ou apparition d’hématomes plus facilement qu’habituellement dus au faible taux de plaquettes.
· Syndrome lupique (y compris une éruption cutanée, des troubles articulaires et des effets sur les cellules sanguines).
Effets indésirables très rares (moins de 1 cas sur 10 000 patients)
· Jaunisse (jaunissement de la peau et des yeux), hépatites (inflammation du foie), traces de sang dans les urines, atteinte des nerfs de vos bras et de vos jambes (tels que des engourdissements), douleur au niveau des articulations, perte de mémoire et augmentation de la taille de la poitrine chez l’homme et la femme (gynécomastie).
Effets indésirables de fréquence inconnue
· Diarrhée, toux, essoufflement, œdème (gonflement), troubles du sommeil, y compris insomnie et cauchemars, difficultés sexuelles, dépression, problèmes respiratoires, y compris toux persistante et/ou essoufflement ou fièvre, atteinte des tendons et faiblesse musculaire qui est constante, myasthénie (maladie provoquant une faiblesse musculaire générale, pouvant parfois toucher les muscles utilisés pour respirer), myasthénie oculaire (maladie provoquant une faiblesse des muscles oculaires).
Adressez-vous à votre médecin si vous présentez une faiblesse dans vos bras ou vos jambes qui s’aggrave après des périodes d’activité, une vision double ou des paupières tombantes, des difficultés à avaler ou un essoufflement.
Déclaration des effets secondaires
Si vous ressentez un quelconque effet indésirable, parlez-en à votre médecin ou votre pharmacien. Ceci s’applique aussi à tout effet indésirable qui ne serait pas mentionné dans cette notice. Vous pouvez également déclarer les effets indésirables directement via le système national de déclaration : Agence nationale de sécurité du médicament et des produits de santé (ANSM) et réseau des Centres Régionaux de Pharmacovigilance - Site internet : https://signalement.social-sante.gouv.fr/.
En signalant les effets indésirables, vous contribuez à fournir davantage d’informations sur la sécurité du médicament.
5. COMMENT CONSERVER CRESTOR 5 mg, comprimé pelliculé ?
Tenir ce médicament hors de la vue et de la portée des enfants.
N’utilisez pas ce médicament après la date de péremption indiquée sur l’emballage après EXP. La date de péremption fait référence au dernier jour de ce mois.
Plaquettes :
A conserver à une température ne dépassant pas 30°C.
A conserver dans l’emballage d’origine, à l’abri de l’humidité.
Flacons (PEHD) :
A conserver à une température ne dépassant pas 30°C.
Conserver le flacon soigneusement fermé, à l’abri de l’humidité.
Ne jetez aucun médicament au tout-à-l’égout ou avec les ordures ménagères. Demandez à votre pharmacien d’éliminer les médicaments que vous n’utilisez plus. Ces mesures contribueront à protéger l’environnement.
6. CONTENU DE L’EMBALLAGE ET AUTRES INFORMATIONS
Ce que contient CRESTOR 5 mg, comprimé pelliculé
Rosuvastatine.............................................................................................................. 5,00 mg
Sous forme de rosuvastatine calcique
Pour un comprimé pelliculé
· Les autres composants sont :
Noyau du comprimé : lactose monohydraté, cellulose microcristalline, phosphate tricalcique, crospovidone, stéarate de magnésium.
Pelliculage : lactose monohydraté, hypromellose, triacétine, dioxyde de titane (E171), oxyde de fer jaune (E172).
Qu’est-ce que CRESTOR 5 mg, comprimé pelliculé et contenu de l’emballage extérieur
Ce médicament se présente sous forme de comprimés pelliculés, de couleur jaune, ronds ; gravés « ZD4522 » et « 5 » sur une face et lisse sur l’autre face.
Boîte de 7-14-15-20-28-30-42-50-56-60-84-90-98 ou 100 comprimés pelliculés sous plaquettes ou flacon de 30 ou 100 comprimés pelliculés.
Toutes les présentations peuvent ne pas être commercialisées.
Titulaire de l’autorisation de mise sur le marché
TOUR PACIFIC
11-13 COURS VALMY
92800 PUTEAUX
Exploitant de l’autorisation de mise sur le marché
TOUR PACIFIC
11-13 COURS VALMY
92800 PUTEAUX
S-152 57 Södertälje
SUEDE
OU
GRUNENTHAL GMBH
ZIEGLERSTRAßE 6
52078 AACHEN
ALLEMAGNE
OU
FARMACEUTICI FORMENTI S.P.A
VIA DI VITTORIO 2
21040 ORIGGIO (VA)
ITALIE
Noms du médicament dans les Etats membres de l'Espace Economique Européen
Ce médicament est autorisé dans les Etats membres de l'Espace Economique Européen sous les noms suivants : Conformément à la réglementation en vigueur.
[À compléter ultérieurement par le titulaire]
La dernière date à laquelle cette notice a été révisée est :
[à compléter ultérieurement par le titulaire]
< {MM/AAAA}>< {mois AAAA}.>
Des informations détaillées sur ce médicament sont disponibles sur le site Internet de l’ANSM (France).